122 BAB V
KESIMPULAN DAN SARAN A. KESIMPULAN
Berdasarkan analisis data dan pembahasan secara deskriptif dan statistik dapat disimpulkan sebagai berikut:
1. Penerapan pendekatan Discovery Learning efektif pada materi pokok larutan penyangga SMA Negeri 5 Kupang tahun ajaran 2014/2015. Secara terperinci dapat disimpulkan sebagai berikut:
a. Guru mampu mengelola pembelajaran dengan menerapkan pendekatan discovery learning pada materi pokok larutan penyangga dengan rata-rata kemampuan guru dalam mengelola kegiatan pembelajaran sebesar 3,88 termasuk dalam kategori baik.
b. Ketuntasan indikator tercapai dengan menerapkan pendekatan
discovery learning pada materi pokok larutan penyangga siswa kelas XIMIA 4 SMA Negeri 5 Kupang tahun ajaran 2014/2015. Secara terperinci ketuntasan indikator hasil belajar meliputi: 1) Ketuntasan indikator hasil belajar aspek sikap spiritual (KI 1)
yang diperoleh melalui observasi sebesar 0,97 dan angket sebesar 0,89 dinyatakan tuntas.
2) Ketuntasan indikator hasil belajar aspek sikap sosial (KI 2) yang diperoleh melalui observasi sebesar 0,872 dan angket sebesar 0,833 dinyatakan tuntas.
123
3) Ketuntasan indikator aspek pengetahuan (KI 3) yang diperoleh dari indikator THB soal essay sebesar 0,801 dinyatakan tuntas.
4) Ketuntasan indikator aspek keterampilan (KI 4) yang diperoleh dari indikator keterampilan sebesar 0,88 dinyatakan tuntas.
c. Hasil belajar tuntas dengan menerapkan pendekatan discovery learning pada materi pokok larutan penyangga siswa kelas XI MIA 4 SMA Negeri 5 Kupang tahun ajaran 2014/2015. Secara terperinci ketuntasan hasil belajar meliputi:
1) Ketuntasan hasil belajar aspek sikap spiritual (KI 1) yang diperoleh melalui observasi dan angket dengan rata-rata sebesar 93,9 dinyatakan tuntas.
2) Ketuntasan hasil belajar aspek sikap sosial (KI 2) yang diperoleh melalui observasi dan angket dengan rata- rata sebesar 85,12 dinyatakan tuntas.
3) Ketuntasan hasil belajar aspek pengetahuan (KI 3) yang diperoleh melalui kuis, tugas dan ulangan dengan rata-rata sebesar 81,9 dinyatakan tuntas.
4) Ketuntasan hasil belajar aspek keterampilan (KI-4) yang diperoleh melalui psikomotor, presentasi dan portofolio dengan rata-rata sebesar 93,93 dinyatakan tuntas.
124
2. Kecerdasan emosional siswa kelas XI MIA 4 SMA Negeri 5 Kupang tahun ajaran 2014/2015 dengan presentase rata-rata yang diperoleh sebesar 76,5% dengan kategori tinggi.
3. Lingkungan keluarga siswa kelas XIMIA SMA Negeri 5 Kupang tahun ajaran 2014/2015 dengan presentase rata-rata yang diperoleh sebesar 77,63% dengan kategori baik.
4. a. Ada hubungan yang signifikan antara kecerdasan emosional siswa dengan hasil belajar siswa pada pembelajaran yang menerapkan pendekatan discovery learning pada materi pokok larutan penyangga siswa kelas XI MIA SMA Negeri 5 Kupang tahun ajaran 2014/2015 dengan nilai korelasi product moment yang diperoleh sebesar 0,413 yang termasuk dalam kategori cukup kuat .
b. Ada hubungan yang signifikan antara lingkungana keluarga siswa dengan hasil belajar siswa pada pembelajaran yang menerapkan pendekatan discovery learning pada materi pokok larutan penyangga siswa kelas XI MIA SMA Negeri 5 Kupang tahun ajaran 2014/2015 dengan nilai korelasi product moment yang diperoleh sebesar 0,431 yang termasuk dalam kategori cukup kuat.
c. Ada hubungan yang signifikan antara kecerdasan emosional dan lingkungan keluarga siswa dengan hasil belajar siswa pada pembelajaran yang menerapkan pendekatan discovery learning pada materi pokok larutan penyangga siswa kelas XI MIA SMA Negeri 5
125
Kupang tahun ajaran 2014/2015 dengan nilai korelasi ganda yang diperoleh sebesar 0,527 yang termasuk dalam kategori cukup kuat. 5. a. Ada pengaruh yang signifikan antara kecerdasan emosional siswa
terhadap hasil belajar siswa pada pembelajaran yang menerapkan pendekatan discovery learning pada materi pokok larutan penyangga siswa kelas XI MIA SMA Negeri 5 Kupang tahun ajaran 2014/2015 yang ditunjukan dengan persamaan regresi . b. Ada pengaruh yang signifikan antara lingkungan keluarga siswa
terhadap hasil belajar siswa pada pembelajaran yang menerapkan pendekatan discovery learning pada materi pokok larutan penyangga siswa kelas XI MIA SMA Negeri 5 Kupang tahun ajaran 2014/2015 yang ditunjukan dengan persamaan .
c. Ada pengaruh yang signifikan antara kecerdasan emosional dan lingkungan keluarga siswa terhadap hasil belajar siswa pada pembelajaran yang menerapkan pendekatan discovery learning pada materi pokok larutan penyanga siswa kelas XI MIA SMA Negeri 5 Kupang tahun ajaran 2014/2015 yang ditunjukan dengan persamaan regresi ganda .
126 B. SARAN
Berdasarkan hasil penelitian yang diperoleh, maka dapat dikemukakan beberapa saran sebagai berikut:
1. Bagi siswa
Diharapkan dapat menunjukkan dan meningkatkan kecerdasan emosional yang dimiliki sehingga dapat meningkatkan hasil belajar. . 2. Bagi Guru
a. Pendekatan discovery learning sangat baik dan efektif dalam pembelajaran kimia, oleh karena itu disarankan agar guru mata pelajaran kimia dapat menerapkannya dalam pembelajaran, pada materi pokok lain yang sesuai.
b. Bagi guru perlu memperhatikan dan meningkatkan kecerdasan emoisonal siswa agar siswa lebih aktif dalam kegiataan pembelajaran di kelas.
3. Bagi Orang tua
Disarankan dapat memberikan perhatian secara intens kepada anak baik itu perhatian secara material maupun non material sehingga dapat meningkatkan hasil belajarnya.
4. Bagi Peneliti Selanjutnya
Yang ingin melakukan penelitian dengan menggunakan pendekatan
discovery learning agar benar-benar melaksanakan langkah-langkah pembelajaran agar siswa dapat aktif mengikuti proses pembelajaran dengan baik sehingga dapat meningkatkan hasil belajarnya.
127
DAFTAR PUSTAKA
Ali, Muhamad dan Muhamad, Asori. 2009. Psikologi Remaja. Jakarta: Bumi Aksara
Book, E. Haward dan Stein, J. Steven. 2014. Ledakan EQ 15 Prinsip Dasar Kecerdasan Emosional Meraih Sukses. Bandung: Mizan Pustaka Chang, Raymond. 2005. Kimia Dasar Edisi ke Tiga Konsep-konsep Inti. Jakarta:
Erlangga
Goleman, Daniel. 2002. Emotional Intellengence. Jakarta: Gramedia.
Iskandar. 2012. Psikologi Pendidikan (Sebuah Orientasi Baru). Jakarta: Referensi Jihad, Asep., Abdul Haris. 2012. Evaluasi Pembelajaran. Jakarta: Multipressindo Kementrian Pendidikan dan Kebudayaan. 2013. Materi Pelatihan Guru
Implementasi Kurikulum 2013
Kementrian Pendidikan dan Kebudayaan. 2014. Materi Pelatihan Guru Implementasi Kurikulum 2013
Lestari, Sri. 2012. Psikologi Keluarga. Jakarta: Kencana
Petrucci, H. Ralph, dkk. 2008. Kimia Dasar Prinsip-prinsip dan Aplikasi Modern. Jakarta: Erlangga
Riduwan., Akdon.2013. Rumus dan Data dalam Analisis Statistika. Bandung: Alfabeta
Sadulloh, Uyo. 2011. Pedagogik (Ilmu Mendidik). Bandung: Alvabet
Sani, Riduwan Abdullah. 2014. Pembelajaran Scientific untuk Implementasi Kurikulum 2013. Jakarta: Bumi Aksara
Slameto. 2003. Belajar dan Faktor-faktor yang Mempengaruhi. Jakarta:Rineka Cipta
Sudarmo, Unggul. Kimia untuk SMA/MA/ Kelas XI Kelompok Peminatan Matematika dan Ilmu Alam. Jakarta: Erlangga
128
Syah, Muhibin. 2013. Psikologi Pendidikan dengan Pedekatan Baru. Bandung: Rosdakarya
Trianto. 2007. Model-model Pembelajaran inovatif Berorientasi Konstruktifistik. Jakarta: Prestasi Pustaka Publisher
Uno, B. Hamzah. 2012. Orientasi dalam Psikologi Pembelajaran. Jakarta: Sinar Grafika Offset.
Uno, B. Hamzah., Masri Umar. 2010. Mengelola Kecerdaasan dalam Pembelajaran.Jakarta: Bumi Aksara
Walgito, Bimo. 2004. Pengantar Psikologi Umum. Yogyakarta: Andi
Yusuf, Syamsu. 2007. Psikologi Perkembangan Anak dan Remaja. Bandung: Remaja Rosdakarya
0
L
A
M
P
I
R
A
N
179
Lampiran 01
SILABUS MATA PELAJARAN KIMIA (Peminatan Bidang MIPA)
Satuan Pendidikan : SMA
Kelas : XI
Kompetensi Inti
KI 1 : Menghayati dan mengamalkan ajaran agama yang dianutnya
KI 2 : Menghayati dan mengamalkan perilaku jujur, disiplin, tanggung jawab, peduli (gotong royong, kerjasama, toleran, damai), santun, responsif dan proaktif, dan menunjukan sikap sebagai bagian dari solusi atas berbagai permasalahan dalam berinteraksi secara efektif dengan lingkungan sosial dan alam serta dalam menempatkan diri sebagai cerminan bangsa dalam pergaulan dunia
KI 3 : Memahami, menerapkan, dan menganalisis pengetahuan faktual, konseptual, prosedural, dan metakognitif berdasarkan rasa ingin tahunya tentang ilmu pengetahuan, teknologi, seni, budaya, dan humaniora dengan wawasan kemanusiaan, kebangsaan, kenegaraan, dan peradaban terkait penyebab fenomena dan kejadian, serta menerapkan pengetahuan prosedural pada bidang kajian yang spesifik sesuai dengan bakat dan minatnya untuk memecahkan masalah
KI 4 : Mengolah, menalar, dan menyaji dalam ranah konkret dan ranah abstrak terkait dengan pengembangan dari yang dipelajarinya di sekolah secara mandiri, bertindak secara efektif dan kreatif, serta mampu menggunakan metoda sesuai kaidah keilmuan
Kompetnsi Dasar Materi Pokok
Pembelajaran Penilaian Alokasi Waktu
Sumber Belajar 1.1 Menyadari adanya keteraturan
dari sifat hidrokarbon, termokimia, laju reaksi, kesetimbangan kimia, larutan dan koloid sebagai wujud kebesaran Tuhan YME dan pengetahuan tentang adanya keteraturan tersebut sebagai hasil pemikiran kreatif
Sifat larutan penyangga pH larutan penyangga Peranan larutan penyangga dalam tubuh makhluk Mengamati (Observing)
Mencari informasi dari berbagai sumber tentang larutan penyangga, sifat dan pH larutan penyangga serta peranan larutan penyangga dalam tubuh makhluk hidup
Mencari informasi tentang darah yang berhubungan
Tugas Merancang percobaan larutan penyangga Observasi Sikap ilmiah dalam 3 mgg x 4 jp - Buku kimia kelas XI - Lembar kerja - Berbagai sumber lainnya
180 manusia yang kebenarannya
bersifat tentatif.
hidup dengan kemampuannya dalam mempertahankan pH terhadap penambahan asam atau basa dan pengenceran Menanya (Questioning)
Mengajukan pertanyaan bagaimana terbentuknya larutan penyangga
Mengapa larutan penyangga pHnya relatif tidak berubah dengan penambahan sedikit asam atau basa
Apa manfaat larutan penyangga dalam tubuh makhluk hidup Mengumpulkan data (Eksperimenting) Mendeskripsikan terbentuknya larutan penyangga Mendeskripsikan sifat larutan penyangga
Merancang percobaan untuk mengetahui larutan yang bersifat penyangga atau
melakukan percobaan dan presentasi, misalnya: cara menggunaka n kertas lakmus, indikator universal atau pH meter; melihat skala volume dan suhu, cara menggunaka n pipet, cara menim-bang, keaktifan, kerja sama, komunikatif, dan peduli lingkungan, dsb) 2.1 Menunjukkan perilaku ilmiah
(memiliki rasa ingin tahu, disiplin, jujur, objektif, terbuka, mampu membedakan fakta dan opini, ulet, teliti, bertanggung jawab, kritis, kreatif, inovatif, demokratis, komunikatif) dalam merancang dan melakukan percobaan serta berdiskusi yang diwujudkan dalam sikap sehari-hari. 2.2 Menunjukkanperilaku
kerjasama, santun, toleran, cintadamai dan peduli
lingkungan serta hemat dalam memanfaatkan sumber daya alam.
2.3 Menunjukkan perilaku responsifdan pro-aktif serta bijaksana sebagai wujud kemampuan memecahkan masalah dan membuat keputusan
181 3.13 Mendeskripsikan sifat larutan
penyangga dan peranan larutan penyangga dalam tubuh
makhluk hidup.
larutan yang bukan penyangga dengan menggunakan indikator universal atau pH meter serta mempresentasikan hasil racangan untuk menyamakan persepsi
Merancang percobaan untuk mengetahui sifat larutan penyangga atau larutan yang bukan penyangga dengan penambahan sedikit asam atau basa atau bila
diencerkan serta mem-presentasikan hasil rancangan untuk menyamakan persepsi
Melakukan percobaan
Mengamati dan mencatat data hasil pengamatan Mengasosiasi (Associating)
Mengolah dan menganalisis data untuk menyimpulkan larutan yang bersifat penyangga Menentukan pH larutan penyangga melalui Portofolio Laporan percobaan Tes tertulis uraian Menganalisi s data untuk menyimpulk an larutan yang bersifat penyangga Menghitung pH larutan penyangga Menganalisi s grafik hubungan perubahan harga pH pada titrasi asam basa untuk menjelaskan sifat larutan penyangga 4.13 Merancang, melakukan, dan
menyimpulkan serta
menyajikan hasil percobaan untuk menentukan sifat larutan penyangga.
182 perhitungan
Menentukan grafik
hubungan perubahan harga pH pada titrasi asam basa untuk menjelaskan sifat larutan penyangga Mengkomunikasikan (Communicating)
Membuat laporan percobaan identifikasi garam dan mempresentasikannya dengan mengguna-kan tata bahasa yang benar
Mengkomunikasikan sifat larutan penyangga dan manfaat larutan penyangga dalam tubuh makhluk hidup.
183
Lampiran 02 a
RENCANA PELAKSANAAN PEMBELAJARAN 01 (RPP 1)
A. IDENTITAS
Sekolah : SMA Negeri 5 Kupang Mata pelajaran : Kimia
Kelas/ semester : XI/II (Genap) Materi Pokok : Larutan Penyangga Alokasi waktu : 2 x 45 menit B. KOMPETENSI INTI
KI 1 : Menghayati dan mengamalkan ajaran agama yang dianutnya.
KI 2 : Menghayati dan mengamalkan perilaku jujur, disiplin, tanggung jawab, peduli (gotong royong, kerjasama, toleran, damai), santun, responsif dan proaktif, dan menunjukkan sikap sebagai bagian dari solusi atas berbagai permasalahan dalam berinteraksi secara efektif dengan lingkungan sosial dan alam serta dalam menempatkan diri sebagai cerminan bangsa dalam pergaulan dunia.
KI 3 : Memahami, menerapkan, dan menganalisis pengetahuan faktual, konseptual, prosedural, dan metakognitif berdasarkan rasa ingin tahunya tentang ilmu pengetahuan, teknologi, seni, budaya, dan humaniora dengan wawasan kemanusiaan, kebangsaan, kenegaraan, dan peradaban terkait penyebab fenomena dan kejadian, serta menerapkan pengetahuan prosedural pada bidang kajian yang spesifik sesuai dengan bakat dan minatnya untuk memecahkan masalah.
KI 4 : Mengolah, menalar, dan menyaji dalam ranah konkret dan ranah abstrak terkait dengan pengembangan dari yang dipelajarinya di sekolah secara mandiri, bertindak secara efektif dan kreatif, serta mampu menggunakan metode sesuai kaidah keilmuan.
184
C. KOMPETENSI DASAR (KD) DAN INDIKATOR
KOMPETENSI DASAR INDIKATOR PENCAPAIAN
KOMPETENSI 1.3 Menyadari adanya keteraturan
dari sifat hidrokarbon, termokimia, laju reaksi, kesetimbangan kimia, larutan dan koloid sebagai wujud kebesaran Tuhan Yang Maha Esa dan pengetahuan tentang adanya keteraturan tersebut sebagai hasil pemikiran kreatif manusia yang kebenarannya bersifat tentatif.
1.1.1 Berdoa sebelum dan sesudah pembelajaran sesuai dengan ajaran agama yang dianutnya.
1.1.2 Bersyukur adanya keteraturan sifat larutan penyangga sebagai wujud kebesaran Tuhan yang Maha Esa. 1.1.3 Menyadari bahwa adanya keteraturan
sifat larutan penyangga sebagai wujud kebesaran Tuhan yang Maha Esa.
1.1.4 Menyadari bahwa pengetahuan tentang larutan penyangga yang diperoleh bersifat tentatif. 2.1 Menunjukkan perilaku ilmiah
(memiliki rasa ingin tahu, disiplin, jujur, obyektif, terbuka, mampu mebedakan fakta dan opini, ulet, teliti, bertanggung jawab, kritis, kreativ, inovatif, demokratis dan komunikatif) dalam melakukan percobaan serta berdiskusi yang
diwujudkan dalam sikap sehari-hari.
2.2 Menunjukkan perilaku kerja sama, santun, toleran, cinta damai, dan peduli lingkungan serta hemat dalam
memanfaatkan sumber daya alam.
2.3 Menunjukkan perilaku responsif dan pro-aktif serta bijaksana sebagai wujud kemampuan memecahkan masalah dan membuat keputusan
2.1.1 Menunjukkan perilaku jujur dalam mengerjakan kuis, soal diskusi, melakukan percobaan dan mengerjakan tugas laporan
menentukan sifat larutan penyangga. 2.1.2 Menunjukkan perilaku bertanggung
jawab dalam menjaga keselamatan alat-alat percobaan, mengerjakan laporan percobaan, dalam diskusi kelompok dan dalam
mempresentasikan hasil diskusi kelompok.
2.2.1 Menunjukkan perilaku kerja sama dalam mengerjakan soal diskusi dan melakukan percobaan menentukan sifat larutan penyangga dan sebagai wujud kemampuan memecahkan masalah dan membuat keputusan. 2.3.1 Menunjukkan perilaku pro-aktif
sebagai wujud kemampuan
memecahkan masalah dan membuat keputusan dalam mengerjakan soal diskusi dan melakukan percobaan menentukan sifat larutan penyangga
185 3.13Mendeskripsikan sifat larutan
penyangga dan peranan larutan penyangga dalam tubuh
makhluk hidup.
3.13.1 Menjelaskan pengertian larutan penyangga.
3.13.2 Mendeskripsikan sifat larutan penyangga berdasarkan percobaan. 4.13 Merancang, melakukan dan
menyimpulk an serta menyajikan hasil praktikum untuk menentukan sifat larutan penyangga.
4.13.1 Melakukan percobaan tentang menentukan sifat larutan penyangga.
4.13.2 Menyimpulkan data hasil percobaan tentang menentukan sifat larutan penyangga.
4.13.3 Menyajikan/Mempresentasikan hasil percobaan menentukan sifat larutan penyangga.
D. Tujuan Pembelajaran
Setelah mempelajari materi ini, siswa diharapkan mampu:
1. Mengagungkan kebesaran Tuhan yang Maha Esa dengan cara berdoa sebelum dan sesudah pembelajaran sebagai wujud syukur kepada Tuhan sesuai dengan agama yang dianutnya.
2. Menyadari bahwa adanya keteraturan sifat larutan penyangga sebagai wujud kebesaran Tuhan yang Maha Esa.
3. Menunjukkan perilaku jujur dalam melakukan praktikum dan mengerjakan tugas laporan menentukan sifat larutan penyangga.
4. Menunjukkan perilaku bertanggung jawab dalam menjaga keselamatan alat-alat praktikum, mengerjakan laporan praktikum, dalam diskusi kelompok dan mempresentasikan hasil diskusi kelompok.
5. Menunjukkan perilaku kerja sama dalam melakukan praktikum menentukan sifat larutan penyangga dan mengerjakan soal diskusi sebagai wujud kemampuan memecahkan masalah dan membuat keputusan.
6. Menunjukkan perilaku pro-aktif sebagai wujud kemampuan memecahkan masalah dan membuat keputusan dalam melakukan praktikum menentukan sifat larutan penyangga dan mengerjakan soal diskusi. 7. Menjelaskan pengertian larutan penyangga.
8. Melakukan percobaan penentuan sifat larutan penyangga.
9. Menjelaskan pengaruh penambahan sedikit asam terhadap larutan penyangga.
10. Menjelaskan pengaruh penambahan sedikit basa terhadap larutan penyangga.
11. Menjelaskan pengaruh pengenceran terhadap larutan penyangga.
186
13. Menyajikan/mempresentasikan hasil percobaan penentuan sifat larutan penyangga.
E. Materi Pembelajaran
1. pengertian Larutan Penyangga. 2. Sifat Larutan Penyangga.
F. Pendekatan dan Metode Pembelajaran Pendekatan : Discovery Learning terbimbing.
Metode : Diskusi, kuis, eksperimen dan penugasan. G. Media dan Sumber Pembelajaran
1. Media
Lembar Kerja Siswa, alat dan bahan percobaan, laptop dan LCD. 2. Sumber Belajar
Sudarmo, Unggul. 2014. Kimia untuk SMA/ MA kelas XI kelompok peminatan matematika dan ilmu alam. Penerbit Erlangga.
Nana, Sutresna. 2014. Kimia untuk kelas XI SMA Kelompok Peminatan Matematika dan Ilmu-Ilmu Alam. Penerbit Grafindo.
Tim Masmedia Buana. Kimia Untuk SMA/MA Kelas XI.
Harnanto, Ari. 2009. Kimia untuk SMA/MA Kelas XI. Pusat Perbukuan Dapartemen Pendidikan Nasional.
187 H. Tahap-tahap Pembelajaran
Kegiatan Tahap-tahap DL Kegiatan Guru Alokasi
Waktu Pendahuluan Menciptakan
Situasi (stimulus)
Memberikan salam pembuka Meminta salah satu siswa untuk
memimpin doa sebagai wujud syukur kepada Tuhan Yang Maha Esa sesuai dengan ajaran agamanya masing-masing.
Mengecek kehadiran siswa.
Menyampaikan topik, sub topik dan tujuan pembelajaran.
Menyampaikan penilaian otentik yang akan diambil saat
pembelajaran.
Memotivasi siswa dengan cara mendemokan kepada siswa mengenai sifat larutan penyangga yaitu menyiapkan dua buah gelas kimia, 10 mL CH3COOH 0,1 M, 10 mL CH3COONa 0,1 M dan HCl 0,1 M. Pada kedua gelas kimia tersebut dimasukkan 5 mL CH3COOH 0,1 M dan 5 mL CH3COONa 0,1 M. Pada gelas kimia pertama ditambahkan beberapa tetes HCl 0,1 M.
Kemudian membandingkan pH masing-masing larutan tersebut menggunakan kertas lakmus universal.
Memberikan pertanyaan kepada siswa “Bagaimanakah perubahan pH setelah penambahan HCl pada larutan tersebut?”
Mengarahkan siswa kekegiatan pembelajaran selanjutnya.
15 menit
Kegiatan Inti Problem Statemen (pertanyaan/ide ntifikasi
masalah)
Meminta siswa untuk
mengumpulkan beberapa masalah atau pertanyaan sifat larutan
penyangga berdasakan pengamatan demonstrasi “Mengapa penambahan HCl pada larutan CH3COOH dan CH3COONa tidak menyebabkan perubahan pH yang besar?”
60 menit
188 Pengumpulan data
Pengolahan data dan analisis data Verifikasi
Generalisasi
Meminta siswa untuk
mengumpulkan informasi sebanyak-banyaknya dari literatur yang ada sesuai dengan materi pembelajaran. Membagi siswa ke dalam kelompok
percobaan secara heterogen. Membagikan LKS penentuan sifat
larutan penyangga dan bahan ajar kemasing-masing kelompok. Membimbing siswa dalam
melakukan percobaan penentuan sifat larutan penyangga.
Membimbing siswa menuliskan data hasil pengamatan.
Membimbing siswa dalam
menganalisis data hasil percobaan. Membimbing siswa memeriksa
secara cermat untuk membuktikan benar atau tidaknya pengolahan data dan analisis data pengamatan berdasarkan dari literatur yang tersedia.
Membimbing mempresentasikan hasil percobaan dan diskusi di depan kelas sebagai cerminan perilaku bertanggung jawab. Meminta kelompok lain
menanggapi hasil presentasi. Membimbing siswa menyimpulkan
hasil percobaan dan diskusi
penentuan sifat larutan penyangga.
Penutup Mereview materi pembelajaran.
Memberikan penghargaan kepada kelompok yang kinerjanya baik. Guru memberikan kuis mengenai
sifat larutan pemyangga.
Memberikan tugas rumah berupa membuat laporan praktikum secara individual.
Meminta salah satu siswa untuk memimpin doa.
15 menit
189 I. Penilaian
1. Jenis / teknik penilaian
No Aspek Teknik Bentuk instrumen 1 Sikap Observasi, angket. a. Lembar observasi
sikap spiritual (KI 1).
b. Lembar angket penilaian diri sikap spiritual (KI 1). c. Lembar observasi
sikap sosial (KI 2). d. Lembar angket
penilaian diri sikap sosial (KI 2). 2 Pengetahuan Test tertulis. a. Lembar Diskusi
siswa.
b. Soal uraian (kuis). c. Tugas rumah. 3 Ketrampilan Observasi. a. Lembar observasi
aspek keterampilan (KI 4). b. Lembar penilaian keterampilan. c. Lembar penilaian presentasi.
190
Soal Kuis 1. Sebut dan jelaskan sifat larutan penyangga!
Jawaban 1. Sifat larutan penyangga:
a. pH larutan buffer praktis tidak berubah pada penambahan sedikit asam kuat atau sedikit basa kuat atau pengenceran. b. pH larutan buffer berubah pada penambahan asam kuat atau
basa kuat yang relatif banyak, yaitu apabila asam kuat atau basa kuat yang ditambahkan menghabiskan komponen larutan buffer
itu, maka pH larutan akan berubah drastis.
c. Terbentuk dari asam lemah dengan basa konjugasinya, atau basa lemah dengan asam konjugasinya
Tugas kelompok (membuat laporan hasil percobaan tentang sifat-sifat larutan penyangga).
191
Lampiran 02b
LEMBAR KERJA SISWA 01 (LKS 01)
A. Tujuan: Menentukan sifat larutan penyangga. B. Dasar Teori:
Konsep Larutan Penyangga
Larutan penyangga atau larutan buffer adalah: larutan yang dapat mempertahankan pH pada kisarannya. Larutan penyangga dibedakan menjadi larutan penyangga asam dan larutan penyangga basa. Meskipun terjadi penambahan sedikit asam, sedikit basa ataupun pengencaran, larutan penyangga dapat mempertahankan pH pada kisarannya.
C. Alat dan Bahan: a. Alat:
Gelas kimia 4 buah
Kertas lakmus universal 5 buah
Spatula 1 buah
Gelas ukur 1 buah b. Bahan: Larutan CH3COOH 0,1 M 90 mL Larutan CH3COONa 0,1 M 30 mL Larutan HCl 0,1 M 5 mL Larutan NaOH 0,1 M 5 mL Akuades 50 mL
192 D. Prosedur kerja
a. Menyiapkan Larutan Penyangga 1. Masukkan 30 mL CH3COOH 0,1 M
dalam gelas kimia!
2. Tambahkan 30 mL CH3COONa 0,1 M! 3. Aduk sampai bercampur sempurna dan
ukur pH-nya! Gunakan sebagai larutan penyangga CH3COOH/CH3COO-! b. Menyiapkan Larutan Non-penyangga
1. Masukkan 60 mL CH3COOH dalam gelas kimia!
2. Ukur pH-nya. Gunakan sebagai larutan non-penyangga!
c. Mengetahui Pengaruh Penambahan Sedikit Asam Kuat Terhadap pH Larutan Penyangga
1. Masukkan 20 mL larutan penyangga dalam gelas kimia!
2. Tambahkan 20 mL larutan
non-penyangga dalam gelas kimia lainnya! 3. Siapkan 10 mL HCl 0,1 M!
4. Tambahkan HCl ke masing-masing larutan secara bertahap sesuai dengan tabel di bawah ini!
193 HCl V ditambahkan (mL) Vtotal (mL) 0 0 1 1 1 2 1 3 1 4 1 5
5. Aduk sampai bercampur sempurna, kemudian ukur pH-nya!
d. Mengetahui Pengaruh Penambahan Sedikit Basa Kuat Terhadap pH
larutan penyangga
Lakukan cara kerja seperti cara mengetahui pengaruh penambahan sedikit asam kuat tetapi HCl diganti dengan NaOH 0,1 M! Perhatikan tabel penambahan NaOH di bawah ini!
NaOH V ditambahkan (mL) V total (mL) 0 0 1 1 1 2 1 3 1 4 1 5
194
Tambahkan akuades seperti cara kerja pada kegiatan c dan d! Perhatikan tabel penambahan akuades di bawah ini!
Akuades V ditambahkan (mL) V total (mL) 0 0 10 10 10 20 10 30 10 40 10 50 E. Hasil Pengamatan
Buat dan lengkapi tabel berikut pada buku kerja kalian!
a. Mengetahui Pengaruh Penambahan Sedikit Asam Kuat HCl pH Larutan penyangga (CH3COOH/CH3C OO-) pH larutan non penyangga (CH3COO H) V ditambahk an (mL) V tota l (mL ) 0 0 .... .... 1 1 .... .... 1 2 .... .... 1 3 .... .... 1 4 .... .... 1 5 .... ....
195
NaOH pH Larutan penyangga (CH3COOH/CH3COO-) pH Larutan non penyangga (CH3COOH) V ditambahkan (mL) V total (mL) 0 0 .... .... 1 1 .... .... 1 2 .... .... 1 3 .... .... 1 4 .... .... 1 5 .... ....
b. Mengetahui pengaruh pengenceran
Akuades pH Larutan penyangga (CH3COOH/CH3COO-) pH Larutan non penyangga (CH3COOH) V ditambahkan (mL) V total (mL) 0 0 .... .... 10 10 .... .... 10 20 .... .... 10 30 .... .... 10 40 .... .... 10 50 .... ....
196 Kerjakan di buku kerja kalian!
1. Apa yang terjadi ketika CH3COOH direaksikan dengan CH3COONa? Apakah terjadi reaksi? Jika ya, maka tuliskan persamaan reaksinya! 2. Apakah terjadi perubahan harga pH ketika larutan ditambahkan asam
kuat (HCl), basa kuat (NaOH)? Jelaskan!
3. Bagaimanakah pengaruh pengenceran terhadap pH larutan penyangga dan non penyangga?
4. Buatlah kesimpulan dari kegiatan ini dan diskusikan dengan teman kalian!
Lampiran 02 c
198 (RPP 02)
A. IDENTITAS
Sekolah : SMA Negeri 5 Kupang Mata pelajaran : Kimia
Kelas/ semester : XI/II (Genap) Materi Pokok : Larutan Penyangga Alokasi waktu : 2 x 45 menit B. KOMPETENSI INTI
KI 1 : Menghayati dan mengamalkan ajaran agama yang dianutnya.
KI 2 : Menghayati dan mengamalkan perilaku jujur, disiplin, tanggung jawab, peduli (gotong royong, kerjasama, toleran, damai), santun, responsif dan proaktif, dan menunjukkan sikap sebagai bagian dari solusi atas berbagai permasalahan dalam berinteraksi secara efektif dengan lingkungan sosial dan alam serta dalam menempatkan diri sebagai cerminan bangsa dalam pergaulan dunia.
KI 3 : Memahami, menerapkan, dan menganalisis pengetahuan faktual, konseptual, prosedural, dan metakognitif berdasarkan rasa ingin tahunya tentang ilmu pengetahuan, teknologi, seni, budaya, dan humaniora dengan wawasan kemanusiaan, kebangsaan, kenegaraan, dan peradaban terkait penyebab fenomena dan kejadian, serta menerapkan pengetahuan prosedural pada bidang kajian yang spesifik sesuai dengan bakat dan minatnya untuk memecahkan masalah.
KI 4 : Mengolah, menalar, dan menyaji dalam ranah konkret dan ranah abstrak terkait dengan pengembangan dari yang dipelajarinya di sekolah secara mandiri, bertindak secara efektif dan kreatif, serta mampu menggunakan metode sesuai kaidah keilmuan.
C. KOMPETENSI DASAR (KD) DAN INDIKATOR
199
KOMPETENSI 1.1 Menyadari adanya keteraturan
dari sifat hidrokarbon, termokimia, laju reaksi, kesetimbangan kimia, larutan dan koloid sebagai wujud kebesaran Tuhan Yang Maha Esa dan pengetahuan tentang adanya keteraturan tersebut sebagai hasil pemikiran kreatif manusia yang kebenarannya bersifat tentatif.
1.1.1 Berdoa sebelum dan sesudah pembelajaran sesuai dengan ajaran agama yang dianutnya.
1.1.2 Bersyukur adanya keteraturan sifat larutan penyangga sebagai wujud kebesaran Tuhan yang Maha Esa. 1.1.3 Menyadari bahwa adanya keteraturan
sifat larutan penyangga sebagai wujud kebesaran Tuhan yang Maha Esa.
1.1.4 Menyadari bahwa pengetahuan tentang larutan penyangga yang diperoleh bersifat tentatif. 2.1 Menunjukkan perilaku ilmiah
(memiliki rasa ingin tahu, disiplin, jujur, obyektif, terbuka, mampu mebedakan fakta dan opini, ulet, teliti, bertanggung jawab, kritis, kreativ, inovatif, demokratis dan komunikatif) dalam melakukan percobaan serta berdiskusi yang
diwujudkan dalam sikap sehari-hari.
2.2 Menunjukkan perilaku kerja sama, santun, toleran, cinta damai, dan peduli lingkungan serta hemat dalam
memanfaatkan sumber daya alam.
2.3 Menunjukkan perilaku responsif dan pro-aktif serta bijaksana sebagai wujud kemampuan memecahkan masalah dan membuat keputusan
2.1.1 Menunjukkan perilaku jujur dalam mengerjakan kuis, soal diskusi, melakukan percobaan dan mengerjakan tugas laporan
menentukan sifat larutan penyangga. 2.1.2 Menunjukkan perilaku bertanggung
jawab dalam menjaga keselamatan alat-alat percobaan, mengerjakan laporan percobaan, dalam diskusi kelompok dan dalam
mempresentasikan hasil diskusi kelompok.
2.2.1 Menunjukkan perilaku kerja sama dalam mengerjakan soal diskusi dan melakukan percobaan menentukan sifat larutan penyangga dan sebagai wujud kemampuan memecahkan masalah dan membuat keputusan. 2.3.1 Menunjukkan perilaku pro-aktif
sebagai wujud kemampuan
memecahkan masalah dan membuat keputusan dalam mengerjakan soal diskusi dan melakukan percobaan menentukan sifat larutan penyangga
200 3.13Mendeskripsikan sifat larutan
penyangga dan peranan larutan penyangga dalam tubuh
makhluk hidup.
3.13.3 Menjelaskan macam-macam larutan penyangga
3.13.4 Menentukan pH larutan penyangga 4.13 Merancang, melakukan dan
menyimpulk an serta menyajikan hasil praktikum untuk menentukan sifat larutan penyangga.
4.13.1 Melakukan diskusi kelompok untuk soal-soal yang ada dalam LDS 4.13.2 Menyimpulkan hasil diskusi
kelompok.
4.13.3 Menyajikan/Mempresentasikan hasil diskusi kelompok.
D. Tujuan Pembelajaran
Setelah mempelajari materi ini, siswa diharapkan mampu:
1. Mengagungkan kebesaran Tuhan yang Maha Esa dengan cara berdoa sebelum dan sesudah pembelajaran sebagai wujud syukur kepada Tuhan sesuai dengan agama yang dianutnya.
2. Menyadari bahwa adanya keteraturan sifat larutan penyangga sebagai wujud kebesaran Tuhan yang Maha Esa.
3. Menunjukkan perilaku jujur dalam mengerjakan soal diskusi dan mempresentasikan hasil diskusi.
4. Menunjukkan perilaku kerja sama sebagai wujud kemampuan memecahkan masalah dan membuat keputusan.
5. Menunjukkan perilaku bertanggung jawab dalam diskusi dan mempresentasikan hasil diskusi kelompok.
6. Menunjukkan perilaku pro-aktif sebagai wujud kemampuan memecahkan masalah dan membuat keputusan.
7. Menjelaskan campuran penyangga dari campuran asam lemah dan basa konjugasinya.
8. Menjelaskan campuran penyangga dari campuran basa lemah dan asam konjugasinya.
9. Menentukan pH larutan penyangga asam lemah dan basa konjugasinya. 10. Menentukan pH larutan penyangga basa lemah dan asam konjugasinya. 11. Menentukan pH larutan penyangga ketika ditambahkan sedikit asam. 12. Menentukan pH larutan penyangga ketika ditambahkan sedikit basa. 13. Menentukan pH larutan penyangga ketika diencerkan.
14. Melakukan diskusi kelompok untuk soal-soal yang ada dalam LDS. 15. Menyimpulkan hasil diskusi kelompok.
201 E. Materi Pembelajaran
pH Larutan Penyangga.
F. Pendekatan dan Metode Pembelajaran Pendekatan : Discovery Learning terbimbing.
Metode : Diskusi, kuis, eksperimen dan penugasan. G. Media dan Sumber Pembelajaran
1. Media
Lembar Diskusi Siswa, alat dan bahan percobaan, laptop dan LCD. 2. Sumber Belajar
Sudarmo, Unggul. 2014. Kimia untuk SMA/ MA kelas XI kelompok peminatan matematika dan ilmu alam. Penerbit Erlangga.
Nana, Sutresna. 2014. Kimia untuk kelas XI SMA Kelompok Peminatan Matematika dan Ilmu-Ilmu Alam. Penerbit Grafindo.
Tim Masmedia Buana. Kimia Untuk SMA/MA Kelas XI.
Harnanto, Ari. 2009. Kimia untuk SMA/MA Kelas XI. Pusat Perbukuan Dapartemen Pendidikan Nasional.
H. Tahap-tahap Pembelajaran
Kegiatan Tahap-tahap DL Kegiatan Guru Alokasi
Waktu Pendahuluan Menciptakan
Situasi (stimulus)
Memberikan salam pembuka. Meminta salah satu siswa untuk
memimpin doa sebagai wujud syukur kepada Tuhan Yang Maha Esa sesuai dengan ajaran agamanya masing-masing.
Mengecek kehadiran siswa.
Menyampaikan topik, sub topik dan tujuan pembelajaran.
Menyampaikan penilaian otentik yang akan diambil saat pembelajaran. Memotivasi siswa dengan cara
menggali pengetahuan awal siswa dengan bertanya kepada siswa “Bagaimana pengaruh penambahan sedikit asam ke dalam larutan penyangga?”
Memberikan pertanyaan kepada siswa 15 menit
202
“Bagaimanakah perubahan pH setelah penambahan HCl pada larutan
penyangga?”
Meminta siswa untuk menanggapi pertanyaan tersebut. Jawaban yang diharapkan adalah “Penambahan sedikit asam ke dalam larutan penyangga tidak menyebabkan perubahan pH yang besar. Mengarahkan siswa kekegiatan
pembelajaran selanjutnya. Kegiatan Inti Problem
Statemen (pertanyaan/iden tifikasi masalah) Pengumpulan data Pengolahan data dan analisis data
Verifikasi
Generalisasi
Mengarahkan siswa dengan bertanya kesiswa “Bagaimana cara menghitung pH larutan penyangga?”
Meminta siswa untuk mengumpulkan informasi sebanyak-banyaknya dari literatur yang ada sesuai dengan materi pembelajaran.
Membagi siswa ke dalam kelompok diskusi secara heterogen.
Membagikan LDS penentuan pH larutan penyangga dan bahan ajar kemasing-masing kelompok.
Membimbing siswa dalam melakukan diskusi penentuan pH larutan
penyangga.
Membimbing siswa mengola dan menganalisis butir soal yang ada di LDS.
Membimbing siswa memeriksa secara cermat untuk membuktikan benar atau tidaknya pengolahan data dan analisis butir soal yang ada di LDS berdasarkan literatur yang tersedia.
Membimbing siswa dalam
mempresentasikan hasil pekerjaan kelompok di depan kelas sebagai cerminan perilaku bertanggung jawab.
60 menit
203
Meminta kelompok lain menanggapi hasil presentasi.
Membimbing siswa menyimpulkan secara umum hasil pekerjaan kelompok.
Penutup Mereview materi pembelajaran.
Memberikan penghargaan kepada kelompok yang kinerjanya baik. Memberikan kuis mengenai pH larutan
penyangga.
Memberikan tugas rumah untuk dikerjakan secara mandiri. Meminta salah satu siswa untuk
memimpin doa.
15 menit
I. Penilaian
1. Jenis / teknik penilaian
No Aspek Teknik Bentuk instrumen 1 Sikap Observasi, angket. a. Lembar observasi
sikap spiritual (KI 1).
b. Lembar angket penilaian diri sikap spiritual (KI 1). c. Lembar observasi
sikap sosial (KI 2). d. Lembar angket
penilaian diri sikap sosial (KI 2).
2 Pengetahuan Test tertulis. a. Lembar Diskusi siswa.
204
b. Soal uraian (kuis). c. Tugas rumah. 3 Ketrampilan Observasi. a. Lembar penilaian
presentasi.
Lembar Diskusi Siswa (LDS)
205
1. Suatu larutan penyangga mengandung CH3COONa 0,4 mol dan CH3COOH 0,25 mol. Jika Ka = 1,8 x 10-5, maka tentukan pH larutan
penyangga!
2. Tentukan pH suatu larutan penyangga yang mengandung NH4Cl 0,2 mol dan NH3 0,15 mol jika pKbNH3 = 4,74!
3. Sebanyak 1 L larutan penyangga mengandung CH3COOH 0,1 M dan CH3COONa 0,1 M. Jika Ka CH3COOH = 1,8 x 10-5, maka tentukan
a. pH larutan penyangga
b. pH larutan penyangga jika ditambahkan 10 mL HCl 0,1 M c. pH larutan penyangga jika ditambah 10 mL NaOH 0,1 M
Jawaban 1. Diketahui:
206 = 0,25 mol =1,8 x 10-5 Ditanya: pH...? Jawab:
Jumlah mol basa konjugasi (CH3COO-) diperoleh dari garam CH3COONa
Awal 0,4 mol - - Reaksi 0,4 mol 0,4 mol 0,4 mol Akhir 0 0,4 mol 0,4 mol
pH larutan penyangga dapat dihitung sebagai berikut.
Jadi, pH larutan penyangga sebesar 4,94. 2. Diketahui: Ditanya: pH...? Jawaban:
Jumlah mol asam konjugasi (NH4+) diperoleh dari ionisasi NH4Cl
Awal 0,2 mol - - Reaksi 0,2 mol 0,2 mol 0,2 mol
207
Akhir 0 0,2 mol 0,2 mol
pOH larutan penyangga dapat ditentukan sebagai berikut.
Jadi, larutan penyangga basa NH3/NH4+ sebesar 9,14 3. Diketahui: Ditanya: a. pH larutan penyangga...?
b. pH larutan penyangga ditambah 10 mL HCl 0,1 M...?
c. pH larutan penyangga jika ditambahkan 10 mL NaOH 0,1 M...? Jawab:
a. Jumlah mol basa konjugasi (CH3COO-) diperoleh dari garam CH3COONa
Awal 0,1 mol - - Reaksi 0,1 mol 0,1 mol 0,1 mol Akhir - 0,1 mol 0,1 mol
Jadi, pH larutan penyangga adalah 4,74
b. Jumlah mol masing-masing zat dapat ditentukan dengan cara sebagai berikut.
208 = 0,1 mol
Jumlah mol CH3COONa = 1 L x 0,1 mol L-1 = 0,1 mol
Jumlah mol HCl = 0,01 L x 0,1 mol L-1 = 0,001 mol
Pada larutan penyangga, CH3COONa akan menetralisir HCl dan membentuk CH3COOH
Awal 0,1 mol 0,001 mol 0,1 mol - Reaksi 0,001 mol 0,001 mol 0,001 mol 0,001 mol
akhir 0,099 mol 0 0,101 mol 0,001 mol
Dari reaksi diperoleh
[CH3COO-] = [CH3COONa] = 0,099 [CH3COOH] = 0,101
pH larutan penyangga setelah ditambah asam kuat HCl dapat dihitung sebagai berikut.
Jadi, pH larutan penyangga jika ditambah 10 mL HCl 0,1 M adalah 4,73
c. Pada larutan penyangga, CH3COOH akan menetralisir basa kuat NaOH yang ditambahkan. Jumlah mol NaOH yang ditambahkan dapat dihitung dengan cara sebagai berikut.
Jumlah mol NaOH = 0,01 L x 0,1 mol L-1 = 0,001 mol Persamaan reaksi yang terjadi
209
Reaksi 0,001 mol 0,001 mol 0,001 mol 0,001 mol
Akhir 0,099 mol 0 0,101 mol 0,01mol Dari reaksi diperoleh
[CH3COO-] = 0,101 [CH3COOH] = 0,099
pH larutan penyangga setelah penambahan basa kuat dapat dihitung sebagai berikut.
Jadi, pH larutan penyangga jika ditambahkan 10 mL NaOH 0,1 M adalah 4,75.
Kuis
1. Jelaskan pembentukan larutan penyangga dari campuran asam lemah dan basa konjugasinya !
Jawaban
1. Reaksi antara asam lemah dan basa kuat dapat menghasilkan garam yang anionnya berasal dari asam lemah pembentuknya. Untuk dapat menghasilkan larutan penyangga, jumlah mol asam lemah harus bersisa sehingga setelah reaksi terjadi akan diperoleh campuran asam lemah (sisa) dan garamnya.
210
1. Jika 1 L larutan NH4OH 0,1 M (Kb NH4OH = 1,8 x 10-5) dicampur dengan 1 L larutan NH4Cl 0,1 M, tentukan:
a. pH larutan penyangga tersebut
b. pH larutan penyangga jika pada campuran tesebut ditambahkan 10 mL HCl 0,1 M.
Jawaban 1. a. pH larutan penyangga
Jumlah mol NH4OH = jumlah mol b = V x M = 1 L x 0,1 M = 0,1 mol
Jumlah mol NH4Cl = jumlah mol g = V x M = 1 L x 0,1 M = 0,1 mol [OH-] = x = 1,8 x 10 -5 x = 5 – log 1,8 = 4,745
pOH = - log [OH-] = 1,8 x 10-5= 5 – log 1,8 = 4,745 pH = 14 - pOH = 14 – 4,745 = 9,255
b. pH larutan penyangga jika pada campuran tesebut ditambahkan 10 mL HCl 0,1 M.
Pada campuran NH4OH dan NH4Cl ditambah HCl sehingga NH4OH akan bereaksi dengan HCl membentuk NH4Cl.
Jumlah mmol NH4OH semula = 0,1 mol = 100 mmol Jumlah mmol NH4Cl semula = 0,1 mol = 100 mmol Jumlah mmol HCl = V x M = 10 mL x 0,1 M = 1 mmol NH4OH + HCl NH4Cl + H2O
Mula-mula : 100 mmol 1 mmol 100 mmol - Reaksi : 1 mmol 1 mmol 1 mmol 1 mmol Sisa : 99 mmol - 99 mmol 1 mmol
211
= 1,8 x 10-5 x = 1,7644 x 10-5 pOH = - log [OH-] = 5- log 1,7644 = 4,753 pH = 14 – pOH = 14 – 4,753 = 9,247
211
Lampiran 02 d
RENCANA PELAKSANAAN PEMBELAJARAN 03 (RPP 03)
A. IDENTITAS
Sekolah : SMA Negeri 5 Kupang Mata pelajaran : Kimia
Kelas/ semester : XI/II (Genap) Materi Pokok : Larutan Penyangga Alokasi waktu : 2 x 45 menit B. KOMPETENSI INTI
KI 1 : Menghayati dan mengamalkan ajaran agama yang dianutnya.
KI 2 : Menghayati dan mengamalkan perilaku jujur, disiplin, tanggung jawab, peduli (gotong royong, kerjasama, toleran, damai), santun, responsif dan proaktif, dan menunjukkan sikap sebagai bagian dari solusi atas berbagai permasalahan dalam berinteraksi secara efektif dengan lingkungan sosial dan alam serta dalam menempatkan diri sebagai cerminan bangsa dalam pergaulan dunia.
KI 3 : Memahami, menerapkan, dan menganalisis pengetahuan faktual, konseptual, prosedural, dan metakognitif berdasarkan rasa ingin tahunya tentang ilmu pengetahuan, teknologi, seni, budaya, dan humaniora dengan wawasan kemanusiaan, kebangsaan, kenegaraan, dan peradaban terkait penyebab fenomena dan kejadian, serta menerapkan pengetahuan prosedural pada bidang kajian yang spesifik sesuai dengan bakat dan minatnya untuk memecahkan masalah.
KI 4 : Mengolah, menalar, dan menyaji dalam ranah konkret dan ranah abstrak terkait dengan pengembangan dari yang dipelajarinya di sekolah secara mandiri, bertindak secara efektif dan kreatif, serta mampu menggunakan metode sesuai kaidah keilmuan.
212
C. KOMPETENSI DASAR (KD) DAN INDIKATOR
KOMPETENSI DASAR INDIKATOR PENCAPAIAN
KOMPETENSI 1.1 Menyadari adanya keteraturan
dari sifat hidrokarbon, termokimia, laju reaksi, kesetimbangan kimia, larutan dan koloid sebagai wujud kebesaran Tuhan Yang Maha Esa dan pengetahuan tentang adanya keteraturan tersebut sebagai hasil pemikiran kreatif manusia yang kebenarannya bersifat tentatif.
1.1.1 Berdoa sebelum dan sesudah pembelajaran sesuai dengan ajaran agama yang dianutnya.
1.1.2 Bersyukur adanya keteraturan sifat larutan penyangga sebagai wujud kebesaran Tuhan yang Maha Esa. 1.1.3 Menyadari bahwa adanya keteraturan
sifat larutan penyangga sebagai wujud kebesaran Tuhan yang Maha Esa.
1.1.4 Menyadari bahwa pengetahuan tentang larutan penyangga yang diperoleh bersifat tentatif. 2.1 Menunjukkan perilaku ilmiah
(memiliki rasa ingin tahu, disiplin, jujur, obyektif, terbuka, mampu mebedakan fakta dan opini, ulet, teliti, bertanggung jawab, kritis, kreativ, inovatif, demokratis dan komunikatif) dalam melakukan percobaan serta berdiskusi yang
diwujudkan dalam sikap sehari-hari.
2.2 Menunjukkan perilaku kerja sama, santun, toleran, cinta damai, dan peduli lingkungan serta hemat dalam
memanfaatkan sumber daya alam.
2.3 Menunjukkan perilaku responsif dan pro-aktif serta bijaksana sebagai wujud kemampuan memecahkan masalah dan membuat keputusan
2.1.1 Menunjukkan perilaku jujur dalam mengerjakan kuis, soal diskusi, melakukan percobaan dan mengerjakan tugas laporan
menentukan sifat larutan penyangga. 2.1.2 Menunjukkan perilaku bertanggung
jawab dalam menjaga keselamatan alat-alat percobaan, mengerjakan laporan percobaan, dalam diskusi kelompok dan dalam
mempresentasikan hasil diskusi kelompok.
2.2.1 Menunjukkan perilaku kerja sama dalam mengerjakan soal diskusi dan melakukan percobaan menentukan sifat larutan penyangga dan sebagai wujud kemampuan memecahkan masalah dan membuat keputusan. 2.3.1 Menunjukkan perilaku pro-aktif
sebagai wujud kemampuan
memecahkan masalah dan membuat keputusan dalam mengerjakan soal diskusi dan melakukan percobaan menentukan sifat larutan penyangga
213 3.13Mendeskripsikan sifat larutan
penyangga dan peranan larutan penyangga dalam tubuh
makhluk hidup.
3.13.5 Mendeskripsikan contoh-contoh larutan penyangga dalam
kehidupan sehari-hari.
3.13.6 Mendeskripsikan fungsi/peranan larutan penyangga dalam
kehidupan sehari-hari. 4.13 Merancang, melakukan dan
menyimpulk an serta menyajikan hasil praktikum untuk menentukan sifat larutan penyangga.
4.13.1 Melakukan diskusi kelompok untuk soal-soal yang ada dalam LDS 4.13.2 Menyimpulkan hasil diskusi
kelompok.
4.13.3 Menyajikan/Mempresentasikan hasil diskusi kelompok.
D. Tujuan Pembelajaran
Setelah mempelajari materi ini, siswa diharapkan mampu:
1. Mengagungkan kebesaran Tuhan yang Maha Esa dengan cara berdoa sebelum dan sesudah pembelajaran sebagai wujud syukur kepada Tuhan sesuai dengan agama yang dianutnya.
2. Menyadari bahwa adanya keteraturan sifat larutan penyangga sebagai wujud kebesaran Tuhan yang Maha Esa.
3. Menunjukkan perilaku jujur dalam mengerjakan soal diskusi dan mempresentasikan hasil diskusi.
4. Menunjukkan perilaku kerja sama sebagai wujud kemampuan memecahkan masalah dan membuat keputusan.
5. Menunjukkan perilaku bertanggung jawab dalam diskusi dan mempresentasikan hasil diskusi kelompok.
6. Menunjukkan perilaku pro-aktif sebagai wujud kemampuan memecahkan masalah dan membuat keputusan.
7. Menjelaskan bagaimana pengaruh larutan penyangga dalam darah. 8. Menjelaskan bagaimana pengaruh larutan penyangga dalam air ludah. 9. Menjelaskan bagaimana pengaruh larutan penyangga dalam industri. 10. Menjelakan fungsi/peranan larutan penyangga dalam darah.
11. Menjelakan fungsi/peranan larutan penyangga dalam air ludah. 12. Menjelakan fungsi/peranan larutan penyangga dalam industri. 13. Melakukan diskusi kelompok untuk soal-soal yang ada dalam LDS 14. Menyimpulkan hasil diskusi kelompok.
214 E. Materi Pembelajaran
Contoh Larutan Penyangga dalam Kehidupan Sehari-hari. F. Pendekatan dan Metode Pembelajaran
Pendekatan : Discovery Learning terbimbing.
Metode : Diskusi, kuis, eksperimen dan penugasan. G. Media dan Sumber Pembelajaran
1. Media
Lembar Diskusi Siswa, alat dan bahan percobaan, laptop dan LCD. 2. Sumber Belajar
Sudarmo, Unggul. 2014. Kimia untuk SMA/ MA kelas XI kelompok peminatan matematika dan ilmu alam. Penerbit Erlangga.
Nana, Sutresna. 2014. Kimia untuk kelas XI SMA Kelompok Peminatan Matematika dan Ilmu-Ilmu Alam. Penerbit Grafindo.
Tim Masmedia Buana. Kimia Untuk SMA/MA Kelas XI.
Harnanto, Ari. 2009. Kimia untuk SMA/MA Kelas XI. Pusat Perbukuan Dapartemen Pendidikan Nasional.
H. Tahap-tahap Pembelajaran
Kegiatan Tahap-tahap DL Kegiatan Guru Alokasi
Waktu Pendahuluan Menciptakan
Situasi (stimulus)
Memberikan salam pembuka. Meminta salah satu siswa untuk
memimpin doa sebagai wujud syukur kepada Tuhan Yang Maha Esa sesuai dengan ajaran agamanya masing-masing.
Mengecek kehadiran siswa.
Menyampaikan topik, sub topik dan tujuan pembelajaran.
Menyampaikan penilaian otentik yang akan diambil saat
pembelajaran.
Memotivasi siswa dengan cara menunjukkan beberapa jenis minuman atau buah-buahan di supermarket sambil bertanya kepada siswa “Mengapa buah atau
minuman dalam kemasan tersebut tidak mudah rusak?”
15 menit
215
Meminta siswa untuk menanggapi pertanyaan tersebut. Jawaban yang diharapkan adalah “Karena
minuman dan buah-buahan tersebut telah diberi campuran asam sitrat dan natrium sitrat sebagai larutan penyangga untuk mengontrol pH sehingga buah dan minuman tersebut tidak mudah rusak oleh bakteri”.
Mengarahkan siswa kekegiatan pembelajaran selanjutnya. Kegiatan Inti Problem
Statemen (pertanyaan/ide ntifikasi masalah) Pengumpulan data Pengolahan data dan analisis data Verifikasi
Generalisasi
Mengarahkan siswa dengan bertanya ke siswa “Bagaimanakah peranan larutan penyangga dalam tubuh makhluk hidup?”
Meminta siswa untuk
mengumpulkan informasi sebanyak-banyaknya dari literatur yang ada sesuai dengan materi pembelajaran. Membagi siswa ke dalam kelompok
diskusi secara heterogen. Membagikan LDS larutan
penyangga dalam kehidupan sehari-hari dan bahan ajar kemasing-masing kelompok.
Membimbing siswa dalam melakukan diskusi.
Membimbing siswa mengola dalam menganalisis butir soal yang ada di LDS.
Membimbing siswa memeriksa secara cermat untuk membuktikan benar atau tidaknya pengolahan data dan analisis butir soal yang ada di LDS berdasarkan dari literatur yang tersedia.
Membimbing siswa dalam
60 menit
216
mempresentasikan hasil pekerjaan kelompok sebagai cerminan perilaku bertanggung jawab. Meminta kelompok lain
menanggapi hasil presentasi. Membimbing siswa menyimpulkan
secara umum hasil pekerjaan kelompok.
Penutup Mereview materi pembelajaran.
Memberikan penghargaan kepada kelompok yang kinerjanya baik. Guru memberikan kuis mengenai
peranan larutan penyangga dalam tubuh makhluk hidup.
Memberikan tugas rumah untuk dikerjakan secara mandiri. Meminta salah satu siswa untuk
memimpin doa.
15 menit
I. Penilaian
1. Jenis / teknik penilaian
No Aspek Teknik Bentuk instrumen 1 Sikap Observasi, angket. a. Lembar observasi
sikap spiritual (KI 1).
b. Lembar angket penilaian diri sikap spiritual (KI 1). c. Lembar observasi
sikap sosial (KI 2). d. Lembar angket
penilaian diri sikap sosial (KI 2).
217
2 Pengetahuan Test tertulis. a. Lembar Diskusi siswa.
b. Soal uraian (kuis). c. Tugas rumah. 3 Ketrampilan Observasi. a. Lembar penilaian
presentasi.
218 (LDS)
1. Mengapa seorang pendaki gunung dapat terkena alkalosis?
2. Berikan contoh peran larutan penyangga pada obat-obatan! Jelaskan! Jawaban
1. Kadar oksigen yang sedikit di gunung dapat membuat para pendaki bernapas lebih cepat sehingga gas CO2 dilepaskan terlalu banyak, padahal CO2 dapat larut dalam air menghasilkan H2CO3. Hal ini mengakibatkan pH darah akan naik sehingga menyebabkan terjadinya alkalosis.
2. Contohnya asam asetilsalisilat merupakan komponen utama dari tablet aspirin, merupakan obat penghilang rasa nyeri. Adanya asam pada aspirin dapat menyebabkan perubahan pH pada perut. Perubahan pH ini dapat mengakibatkan pembentukan hormon yang dapat merangsang penghambatan penggumppalan darah sehingga pendarahan tidak dapat dihindarkan. Oleh karena itu, pada aspirin ditambahkan MgO yang dapat mentransfer kelebihan asam.
Kuis
1. Uraikan fungsi air ludah sebagai larutan penyangga! Jawaban
1. Gigi dapat larut jika dimasukkan pada larutan asam yang kuat. Email gigi yang rusak dapat menyebabkan kuman masuk kedalam gigi. Air ludah dapat mempertahankan pH pada mulut sekitar 6,8. Air liur mengandung larutan penyangga fosfat yang dapat menetralisir asam yang terbentuk dari fermentasi sisa-sisa makanan.
219
1. Berikan salah satu contoh fungsi larutan penyangga dalam bidang kesehatan!
Jawaban
1. Contohnya untuk obat suntik atau obat tetes mata, pH obat-obatan tersebut harus disesuaikan dengan pH cairan tubuh. Obat tetes mata harus memiliki pH yang sesuai dengan pH air mata agar tidak menimbulkan iritasi yang menyebabkan rasa perih pada mata. Begitu juga obat suntik harus disesuaikan dengan pH darah agar tidak menimbulkan alkalosis atau asidosis pada darah.
220
Lampiran 03 a
BAHAN AJAR SISWA (BAS)
RPP 1
Konsep Larutan Penyangga
Larutan penyangga atau larutan buffer adalah
larutan yang dapat mempertahankan pH pada kisarannya.
Larutan penyangga dibedakan menjadi larutan penyangga asam dan larutan penyangga basa. Meskipun terjadi penambahan sedikit asam, sedikit basa ataupun
pengenceran, larutan penyangga dapat mempertahankan pH pada kisarannya. Biasanya, sistem penyangga terdiri dari dua zat terlarut, yang satu berperan sebagai asam Brønsted lemah dan yang satunya lagi sebagai basa Brønsted lemah. Dua zat terlarut ini merupakan
pasangan asam-basa konjugat. Jika yang menjadi asam adalah molekul, maka yang menjadi basa konjugatnya adalah garam terlarut dari asam tersebut. Ada pula larutan penyangga yang terdiri dari pasangan basa lemah dengan asam konjugatnya. Jadi, dapat dikatakan bahwa
penyangga merupakan pasangan asam lemah atau basa lemah dengan garamnya.
1. Larutan Penyangga Asam
Larutan ini dapat mempertahankan pH pada daerah asam (pH ˂ 7). Larutan penyangga asam terdiri dari asam lemah (HA) dan basa konjugasinya (A-). Larutan ini dapat dibuat dengan mencampurkan larutan asam lemah dengan garamnya. Misalnya, larutan penyangga dari campuran asam asetat dengan natrium asetat.
A
Penyangga asam:
campuran asam lemah (HA) dan basa
konjugatnya (A -)
221
10 mL larutan 10 mL larutan Larutan bufer CH3COOH 0,2 M CH3COONa 0,2 M asam
Gambar 1.1
Pembuatan larutan penyangga asam
Berikut ini persamaan reaksinya.
Larutan ini juga dapat dibuat dari campuran asam lemah dengan basa kuat, tetapi basa kuat harus habis bereaksi sehingga pada akhir reaksi hanya terdapat asam lemah dan garamnya (basa konjugasinya).
Asam lemah Basa Konjugasi
2. Larutan Penyangga Basa
Larutan ini dapat mempertahankan pH pada daerah basa (pH > 7). Larutan penyangga basa terdiri
atas basa lemah (B) dan asam konjugasinya (BH+).
Larutan ini dapat dibuat dengan mencampurkan larutan basa lemah dengan garamnya, misalnya larutan penyangga dari campuran amonia dengan amonium klorida. Penyangga basa: campuran basa lemah (B) dan asam konjugatnya (BH+).
222
15 mL larutan 15 mL larutan Larutan bufer NH3 0,2 M NH4Cl
0,2 M basa Gambar 1.2
Pembuatan larutan penyangga basa
Persamaan reaskinya sebagai berikut.
Larutan ini juga dapat dibuat dari campuran basa lemah dengan asam kuat, dengan catatan asam kuat harus habis bereaski sehingga pada akhir reaksi hanya terdapat basa lemah dan garamnya (asam
konjugasinya). Persamaan reaskinya adalah sebagai berikut.
Reaksi kesetimbangan pada larutan penyangga adalah sebagai berikut.
Sifat Larutan Penyangga
Pengaruh penambahan sedikit asam, sedikit basa, atau pengenceran terhadap pH larutan penyangga dan bukan larutan penyangga dapat dilihat pada tabel 1.1 dan tabel 1.2 berikut.
223
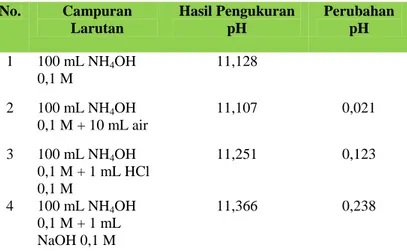
Tabel 1.1 Data Hasil Pengukuran pH NH4OH 0,1 M Setelah Penambahan Air, Sedikit Asa, dan Sedikit Basa. No. Campuran Larutan Hasil Pengukuran pH Perubahan pH 1 100 mL NH4OH 0,1 M 11,128 2 100 mL NH4OH 0,1 M + 10 mL air 11,107 0,021 3 100 mL NH4OH 0,1 M + 1 mL HCl 0,1 M 11,251 0,123 4 100 mL NH4OH 0,1 M + 1 mL NaOH 0,1 M 11,366 0,238
Tabel 1.2 Data Hasil Pengukuran pH Larutan Penyangga A (Campuran 50 mL CH3COOH 0,1 M dan 50 mL CH3COONa 0,1 M) dan Perubahan pH Setelah Penambahan Air, Sedikit Asam, dan Sedikkit Basa. No. Campuran Larutan Hasil
Pengukuran pH Perubahan pH 1 100 mL larutan penyangga A 4,745 2 100 mL larutan penyangga A + 10 mL air 4,745 0 3 100 mL larutan penyangga A + 1 mL HCl 0,1 M 4,736 0,009 4 100 mL larutan penyangga A + 1 mL NaOH 0,1 M 5,753 0,008
Berdasarkan data-data tersebut, penambahan air ke dalam larutan NH4OH (basa lemah) menyebabkan perubahan nilai pH. Adapun penambahan air ke dalam larutan penyangga A praktis tidak mengubah nilai pH campuran.
224
Kemudian penambahan sedikit asam atau sedikit basa sebanyak 1 mL asam atau basa ke dalam larutan NH4OH (basa lemah/bukan larutan penyangga), dan larutan penyangga A menyebabkan perubahan nilai pH. Perbedaannya, perubahan pH pada larutan penyangga A kecil sekali (dapat diabaikan), sedangkan perubahan pH pada NH4OH (bukan larutan penyangga) cukup besar, yaitu 0,123.
Berdasarkan hal tersebut, dapat disimpulkan bahwa larutan penyangga adalah larutan yang dapat mempertahankan nilai pH sehingga tidak mengalami perubahan akibat penambahan air (pengenceran), sedikit asam, ataupun sedikit basa.
Prinsip Kerja Larutan Penyangga
Sebenarnya penambahan sedikit asam, basa, atau pengenceran pada larutan penyangga menimbulkan sedikit perubahan pH (tetapi perubahan pH sangat kecil) sehingga pH larutan dianggap tidak bertambah atau pH tetap pada kisarannya. Prinsip kerja larutan penyangga yang dapat mempertahankan harga pH pada kisarannya adalah sebagai berikut.
1. Larutan Penyangga Asam HA/A
-a. Jika ditambahkan sedikit asam kuat (H+)
Ion H+ dari asam kuat akan menaikkan konsentrasi H+ dalam larutan sehingga reaski kesetimbangan larutan terganggu, reaksi akan bergeser ke kiri. Akann tetapi, basa konjugasi (A-) akan menetralisasi H+ dan membentuk HA.
Akibatnya, pada kesetimbangan yang baru tidak terdapat perubahan konsentrasi H+ yang berarti, dan besarnya pH dapat dipertahankan pada kisarannya.
225
b. Jika ditambahkan sedikit basa kuat (OH-)
Gambar 1.3
Penambahan sedikit basa kuat ke dalam larutan penyangga
Ion OH- dari basa kuat akan bereaksi dengan H+ dalam larutan sehingga konsentrasi H+ menurun dan kesetimbangan larutan terganggu. Oleh karena itu, HA dalam larutan akan terionisasi membentuk H+ dan A-, reaksi kesetimbangan bergeser ke kanan.
Dengan demikian, pada kesetimbangan yang baru tidak terdapat perubahan konsentrasi H+ yang nyata, pH larutan dapat dipertahankan pada kisarannya. Asam lemah dapat menetralisasi penambahan sedikit basa (OH-).
c. Jika larutan penyangga diencerkan
Pengenceran larutan penyangga merupakan penambahan air (H2O) pada larutan. Air (H2O) akan mengalami reaski kesetimbangan menjadi H+ dan OH-. Akan tetapi, H2O yang terurai sangat sedikit sehingga penambahan konsentrasi H+ dan OH- sangat kecil dan dapat diabaikan.
226 2. Larutan Penyangga Basa B/BH
a. Penambahan sedikit asam kuat (H+)
Ion H+ dari asam kuat dapat bereaksi dengan OH- pada larutan sehingga konsentrasi OH- menurun dan reaksi kesetimbangan akan bergeser ke kiri. Di sisi lain, basa lemah (B) dalam larutan akan bereaksi dengan H2O membentuk asam konjugasinya dan ion OH-.
Pada kesetimbangan yang baru tidak terdapat perubahan pH yang nyata, besarnya pH dapat dipertahankan. Basa lemah dapat menetralkan penambahan sedikit asam (H+).
b. Penambahan sedikit basa kuat (OH-)
Adanya basa kuat (OH-) dapat meningkatkan konsentrasi OH -dalam larutan sehingga reaksi kesetimbangan akan bergeser ke kiri. Namun demikian, adanya asam konjugasi (BH+) dapat menetralkan kehadiran OH- dan membentuk B dan H2O. Oleh karena itu, pada kesetimbangan tidak terdapat perubahan konsentrasi OH- yang nyata dan pH larutan dapat dipertahankan.
c. Penambahan air (pengenceran)
Penambahan H2O dalam larutan akan langsung terionisasi menjadi H+ dan OH-, tetapi konsentrasi H+ dan OH- hasil ionisasi sangat kecil sehingga dapat diabaikan.
221
Lampiran 03 b
BAHAN AJAR SISWA (BAS) RPP 02
1. Larutan Penyangga Asam (HA/A-)
pH larutan penyangga asam bergantung pada tetapan ionisasi asam lemah (Ka) dan perbandingan konsentrasi asam dengan konsentrasi basa
konjugasinya. Contoh larutan penyangga asam adalah campuran dari larutan asam asetat (CH3COOH) dan larutan natrium asetat (CH3COONa), asam asetat akan terionisasi sebagian, sedangkan natrium asetat akan terionisasi sempurna. Jika terdapat a mol asam asetat dan g mol natrium asetat, maka susunan reaksinya sebagai berikut : Mula-mula a - - mol Reaksi -α +α +α mol Seimbang a – α α α mol Mula-mula g - - mol Reaksi -g g +g mol Seimbang - g g mol
Reaksi kesetimbangan asam asetat mempunyai harga tetapan ionisasi (Ka), yaitu:
228 Keterangan:
Ka = tetapan ionisasi asam
a = jumlah mol asam penyangga
g = jumlah mol basa konjugasi (garam) 2. Larutan Penyangga Basa (B/BH+) pH larutan penyangga basa sangat bergantung pada tetapan ionisasi basa (Kb), dan perbandingan konsentrasi basa (lemah), dengan konsentrasi asam konjugasinya. Contoh larutan penyangga basa adalah campuran dari gas amonia (NH3) dan larutan amonium klorida (NH4Cl). Amonia merupakan basa lemah sehingga hanya terionisasi sebagian, sedangkan amonium klorida akan terionisasi sempurna. Jika terdapat b mol amonia dan g mol amonium klorida, maka susunan reaksinya dapat ditulis sebagai berikut :
Mula-mula b - - mol Reaksi -α +α +α mol Seimbang (b-α) α α mol
229
Mula-mula g - - mol Reaksi -g +g +g mol
Akhir - g g mol Pada reaksi kesetimbangan amonia, harga tetapan ionisasi basa adalah sebagai berikut.
pOH =
230
Lampiran 03 c
BAHAN AJAR SISWA (BAS) RPP 03
E. Fungsi Larutan Penyangga
Bidang – bidang analisis kimia, biokimia, bakteriologi, fotografi dan industri kulit terkait erat dengan konsep larutan penyangga adalah :
1. Darah sebagai larutan penyangga
pH darah manusia berkisar antara 7,39 – 7,45. Organ yang berperan dalam mengatur pH darah adalah paru-paru dan ginjal. Keadaan ketika pH darah kurang dari normal disebut asidosis. Sebaliknya keadaan ketika pH darah lebih dari normal disebut alkilosis. Agar pH darah selalu dalam kisaran normal, di dalam tubuh terdapat penyangga alami sebagai berikut :
a. Penyangga karbonat
Penyangga karbonat berasal dari campuran asam karbonaat (H2CO3) dengan basa kojugasi bikarbonat (HCO3). Larutan penyangga pada tanaman Larutan penyangga pada tanaman berfungsi untuk melindungi tanaman dari perubahan pH yang mungkin terjadi akibat penambahan pupuk, dll.
231
Kadar oksigen yang sedikit di gunung dapat membuat para pendaki bernapas lebih cepat sehingga gas CO2 dilepas terlalu banyak. Padahal CO2 dapat laruta dalam air menghasilkan H2CO3. Hal ini dapat
mengakibatkan pH darah akan naik sehingga mengakibatkan terjadinya alkalosis.
Gbr. Penyangga karbonat dalam tubuh.
b. Penyangga Hemoglobin
Oksigen masuk ke tubuh melalui proses
pernapasan. Di dalam tubuh oksigen diikat oleh hemoglobin di dalam darah. Oksigen bersifat peka terhadap perubahan pH. Reaksi kesetimbangan larutan penyangga oksi hemoglobin dapat dituliskan sebagai berikut :
HHb O2 H + HBO2
Hasil dari pernapasan adalah CO2 yang di dalam tubuh dapat membentuk senyawa H2CO3.
Berdasarkan reaksi penyangga karbonat di atas, H2CO3 ini akan terurai menjadi H + dan HCO3-. Masuknya H+ dalam darah ini tentu saja akan meningkatkan PH darah. Akan tetapi hemoglobin yang telah melepaskan O2 dapat mengikat H+ ini menjadi asam hemoglobin (HHb+) sehingga pH darah tetap dalam kisaran normal.