14 IV. HASIL DAN PEMBAHASAN
4.1. Optimasi Larutan Starter
Pembuatan minuman stevia pada penelitian ini dilakukan dengan proses
fermentasi menggunakan starter madu. Untuk mengetahui pertumbuhan mikroba
yang paling efektif, dilakukan optimasi terlebih dahulu, dengan berbagai
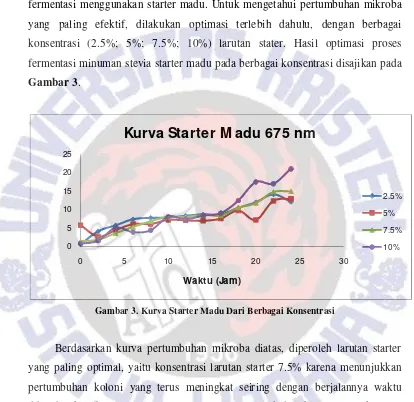
konsentrasi (2.5%; 5%; 7.5%; 10%) larutan stater. Hasil optimasi proses
fermentasi minuman stevia starter madu pada berbagai konsentrasi disajikan pada
Gambar 3.
Gambar 3. Kurva Starter Madu Dari Berbagai Konsentrasi
Berdasarkan kurva pertumbuhan mikroba diatas, diperoleh larutan starter
yang paling optimal, yaitu konsentrasi larutan starter 7.5% karena menunjukkan
pertumbuhan koloni yang terus meningkat seiring dengan berjalannya waktu
dibandingkan dengan larutan starter lain yang pertumbuhan koloninya naik turun.
Berdasarkan kurva yang telah diperhalus, konsentrasi larutan starter madu 7,5%
dapat dilihat pada Gambar 4.
Kurva Starter M adu 675 nm
2.5% 5%
15
Gambar 4. Kurva Stater Madu 7.5%
Pertumbuhan mikroorganisme dapat ditinjau dari dua sudut, yaitu
pertumbuhan individu dan pertumbuhan koloni atau pertumbuhan populasi.
Pertumbuhan individu diartikan sebagai bertambahnya ukuran tubuh, sedangkan
pertumbuhan populasi diartikan sebagai bertambahnya kuantitas individu dalam
suatu populasi (Purnomo, 2004).
Pertumbuhan mikroorganisme dimulai dari awal pertumbuhan sampai
dengan berakhirnya aktivitas, merupakan proses bertahap yang dapat digambarkan
sebagai kurva pertumbuhan. Kurva pertumbuhan terbagi menjadi 4 fase, yaitu fase
lag, fase eksponensial, fase stasioner, dan fase kematian.
Pada Gambar 4, fase lag ditunjukkan pada waktu 0-4 jam. Sedangkan pada waktu 4-10 jam merupakan fase eksponensial dimana selama waktu tersebut
menunjukkan penambahan jumlah koloni yang terus meningkat. Pada waktu
10-22 jam merupakan fase stasioner yang menunjukkan keseimbangan antara koloni
yang hidup dan mati. Sedangkan pada waktu diatas 22 jam merupakan fase
stasioner dilanjutkan fase kematian dimana pertumbuhan koloni mulai menurun
dan akhirnya akan menurun dengan drastis. Larutan starter 7.5% ini memiliki
masa inkubasi sampai dimulainya fase eksponensial adalah 4 jam. Larutan starter
16 4.2. Penetapan Kadar Steviosida Secara HPLC
Kadar steviosida dapat ditentukan dengan metode high performance liquid
chromatography (HPLC) fase terbalik dengan sistem elusi isokratik (Martono
dkk., 2009). Berdasarkan pemilihan minuman stevia dari berbagai massa dan
waktu fermentasi yang dianalisis secara HPLC, diperoleh minuman stevia yang
memiliki kadar steviosida paling besar yaitu minuman stevia dengan massa 50
gram dan waktu fermentasi selama 4 hari. Hal ini disebabkan perbandingan massa
dan volume ekstraksi paling besar (1:40) sehingga senyawa yang terekstrak juga
menjadi lebih banyak. Kadar steviosida untuk tiap perlakuan dapat dilihat pada
Tabel 1 dan Lampiran 2.
Tabel 1. Hasil Pengukuran Kadar Steviosida
No Massa (Gram) Waktu Fermentasi (Hari) Kadar Steviosida (%)
1 50 0 0,45
2 50 4 0,99*
3 100 2 0,51
4 200 4 0,26
5 300 6 0,23
Keterangan : * kadar steviosida paling tinggi
Hasil pengukuran kadar steviosida secara HPLC, diperoleh bahwa minuman
stevia dengan massa 50 gram dan waktu fermentasi 4 hari (H-4; 50gram) memiliki
kadar steviosida yang paling besar yaitu 0,99%. Minuman stevia inilah yang
nantinya akan digunakan dalam uji in vivo. Minuman stevia optimal yang akan
digunakan untuk uji in vivo memiliki kadar steviosida sebesar 4,51%. Perbedaan
kadar steviosida ini muncul karena minuman stevia optimal diekstraksi secara
berulang-ulang menggunakan air panas sehingga steviosida yang terlarut menjadi
lebih banyak. Profil kromatogram standar steviosida serta minuman stevia awal
17 [a] [b]
[c]
Gambar 5. Profil Kromatogram Kadar Steviosida [a] Standar Steviosida (puncak no.1 dengan tR = 14,317 menit) [b] Minuman Stevia Awal (puncak no.4 dengan tR = 12,800
menit) [c] Minuman Stevia Optimal (puncak no.6 dengan tR = 13,650 menit)
4.3. Uji Aktivitas Hipoglikemik
Hasil uji aktivitas hipoglikemik pada penelitian ini disajikan pada Tabel 2. Data kadar glukosa darah dibuat kurva hubungan kadar glukosa darah (mg/dL) vs
waktu (menit). Profil kurva kadar glukosa darah mencit setelah perlakuan dengan
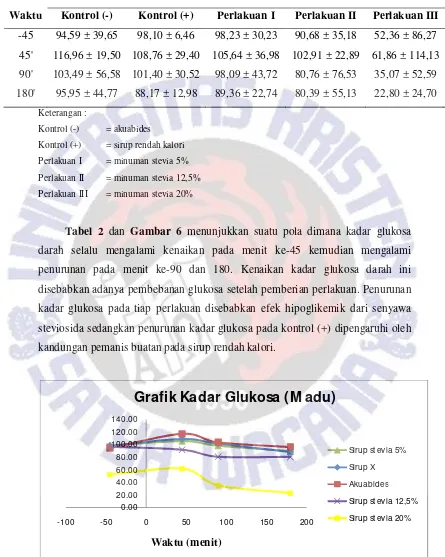
18 Tabel 2. Purata Kadar Glukosa Darah (mg/dL) Terhadap Waktu (Menit)
Waktu
Kadar Glukosa Darah Rata-rata ± SE
Kontrol (-) Kontrol (+) Perlakuan I Perlakuan II Perlakuan III -45 94,59 ± 39,65 98,10 ± 6,46 98,23 ± 30,23 90,68 ± 35,18 52,36 ± 86,27 Perlakuan II = minuman stevia 12,5% Perlakuan III = minuman stevia 20%
Tabel 2 dan Gambar 6 menunjukkan suatu pola dimana kadar glukosa darah selalu mengalami kenaikan pada menit ke-45 kemudian mengalami
penurunan pada menit ke-90 dan 180. Kenaikan kadar glukosa darah ini
disebabkan adanya pembebanan glukosa setelah pemberian perlakuan. Penurunan
kadar glukosa pada tiap perlakuan disebabkan efek hipoglikemik dari senyawa
steviosida sedangkan penurunan kadar glukosa pada kontrol (+) dipengaruhi oleh
kandungan pemanis buatan pada sirup rendah kalori.
19 Hasil purata kadar glukosa darah kemudian dilanjutkan dengan perhitungan
area under curve (AUC-45-180) dan penurunan kadar gula darah (PKGD). Nilai
AUC dan PKGD dari berbagai perlakuan dapat dilihat pada Tabel 3 dan Lampiran 3.
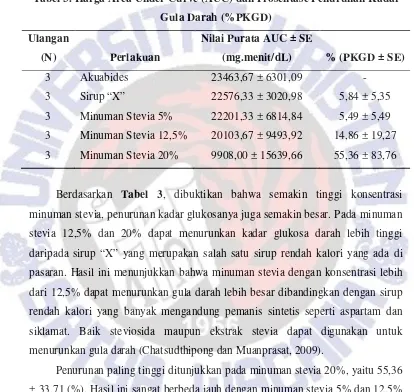
Tabel 3. Harga Area Under Curve (AUC) dan Prosentase Penurunan Kadar Gula Darah (%PKGD)
Berdasarkan Tabel 3, dibuktikan bahwa semakin tinggi konsentrasi minuman stevia, penurunan kadar glukosanya juga semakin besar. Pada minuman
stevia 12,5% dan 20% dapat menurunkan kadar glukosa darah lebih tinggi
daripada sirup “X” yang merupakan salah satu sirup rendah kalori yang ada di
pasaran. Hasil ini menunjukkan bahwa minuman stevia dengan konsentrasi lebih
dari 12,5% dapat menurunkan gula darah lebih besar dibandingkan dengan sirup
rendah kalori yang banyak mengandung pemanis sintetis seperti aspartam dan
siklamat. Baik steviosida maupun ekstrak stevia dapat digunakan untuk
menurunkan gula darah (Chatsudthipong dan Muanprasat, 2009).
Penurunan paling tinggi ditunjukkan pada minuman stevia 20%, yaitu 55,36
± 33,71 (%). Hasil ini sangat berbeda jauh dengan minuman stevia 5% dan 12,5%
yang hanya dapat menurunkan gula darah tidak lebih dari 15%. Dari hasil
penelitian lain yang mirip dengan penelitian ini, minuman stevia yang
menggunakan starter gula 20% hanya memiliki penurunan kadar gula darah
sebesar 25,70%. Perbedaan yang cukup jauh ini terjadi karena adanya interaksi
antara senyawa pada madu, yang digunakan sebagai starter, dengan senyawa aktif
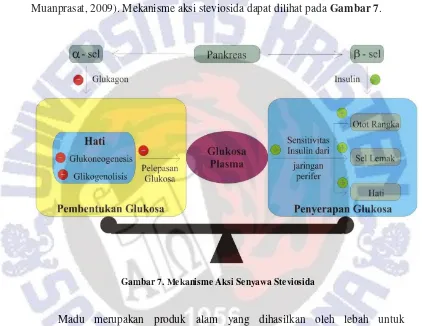
20 Mekanisme aksi senyawa steviosida dalam menurunkan kadar gula dalam
darah adalah meningkatkan sekresi dan sensitivitas insulin sehingga mengurangi
jumlah gula dalam darah. Selain itu, steviosida juga dapat menghambat
penyerapan glukosa di usus dan pembentukan glukosa di liver dengan cara
mengubah aktivitas enzim kunci yang terlibat dalam sintesis glukosa, sehingga
dapat mengurangi penumpukan glukosa pada plasma darah (Chatsudthipong dan
Muanprasat, 2009). Mekanisme aksi steviosida dapat dilihat pada Gambar 7.
Gambar 7. Mekanisme Aksi Senyawa Steviosida
Madu merupakan produk alam yang dihasilkan oleh lebah untuk
dikonsumsi, karena mengandung bahan gizi yang sangat essensial. Madu bukan
hanya merupakan bahan pemanis, atau penyedap makanan, tetapi sering pula
digunakan sebagai obat-obatan (Murtidjo, 1991; Purbaya, 2002). Standar mutu
madu salah satunya didasarkan pada kandungan gula pereduksi (glukosa dan
fruktosa) total yaitu minimal 60%. Sedangkan jenis gula pereduksi yang erdapat
pada madu tidak hanya glukosa dan fruktosa, tetapi juga terdapat maltosa dan
dekstrin (Jarvis, 1995; Purbaya, 2002).
Fruktosa yang merupakan konstituen utama pada madu ternyata memiliki
21 adalah dengan mengaktifkan glukokinase yang merupakan enzim kunci dalam
metabolisme glukosa intraselular. Kemudian glukosa diubah menjadi
glukosa-6-fosfat sehingga mengurangi kadar glukosa dalam darah (Watford, 2002). Sebuah
studi sebelumnya juga melaporkan bahwa sekresi insulin dirangsang fruktosa dari
pankreas (Grodsky dkk., 1963). Selain itu, madu juga mengandung unsur-unsur
seperti seng, selenium, tembaga, kalsium, kalium, kromium, mangan, dll
(Bogdanov dkk., 2008). Beberapa mineral dilaporkan berperan penting dalam
pemeliharaan glukosa dan sekresi insulin (Anderson dkk., 1997 dan Kar dkk.,
1999). Ion lain seperti tembaga dan seng diketahui terlibat dalam pemeliharaan

![Gambar 5. Profil Kromatogram Kadar Steviosida [a] Standar Steviosida (puncak no.1](https://thumb-ap.123doks.com/thumbv2/123dok/716962.570910/4.612.104.518.80.514/gambar-profil-kromatogram-kadar-steviosida-standar-steviosida-puncak.webp)