BAB II
TINJAUAN PUSTAKA
2.1 Uraian Landak Laut
Landak laut merupakan organisme yang tergolong sederhana yang tidak memiliki banyak organ yang ditemukan pada hewan yang lebih tinggi, mereka tidak memiliki sistem saluran pernafasan dan sistem peredaran darah yang khusus seperti hati, pembuluh darah dan tidak ada molekul yang mengikat oksigen didalam cairan tubuh mereka. Sistem anatomi tubuh landak laut terdiri mulut, usus (saluran pencernaan), gonad dan sistem saraf yang dikelilingi oleh cangkang keras, bagian luarnya terdiri dari duri-duri. Landak laut mampu bertahan dalam waktu yang lama dengan sedikit atau tidak ada makanan karena mereka memiliki kemampuan untuk menurunkan metabolisme tubuh mereka dan fungsi biologi yang sesuai dengan kondisi lingkungan (James, 2015).
2.1.1 Habitat
2.1.2 Morfologi dan anatomi
Tubuh landak laut terdiri dari duri-duri panjang menutup tubuh. Tubuh terbungkus oleh cangkang yang terdiri dari lempengan-lempengan yang menyatu. Mulut landak laut terletak dibawah dan ditengah-tengah bagian mulut atau gigi merapat jadi satu yang dilekatkan oleh sederetan bagian untuk membentuk struktur yang dinamakan lentera aristotle. Lentera aristotle ini adalah himpunan gigi yang terdapat pada banyak jenis landak laut, kaki tabung bersama dengan duri digunakan untuk berjalan dan landak laut memiliki kelamin yang terpisah (Romimohtarto, 2009).
Landak laut biasanya berukuran dari 6 sampai 12 cm, ukuran terbesarnya bisa mencapai 36 cm. Semua organ dari landak laut ini terletak di dalam cangkang. Permukaan cangkangnya terdapat tonjolan-tonjolan bulat dan pendek tempat menempelnya duri, pangkal duri berlekuk ke dalam yang sesuai dengan tonjolan pada cangkang, dengan adanya otot penghubung maka duri dapat digerakkan kesegala arah. Sistem anatomi landak laut terdiri dari sistem respirasi, sistem saraf, sistem pencernaan dan sistem reproduksi. Kelas Echinoidea termasuk organisme yang pertumbuhannya lambat. Umur, warna, ukuran dan pertumbuhan tergantung pada jenis dan lokasi tempat tinggal (Sugiarti, 2005).
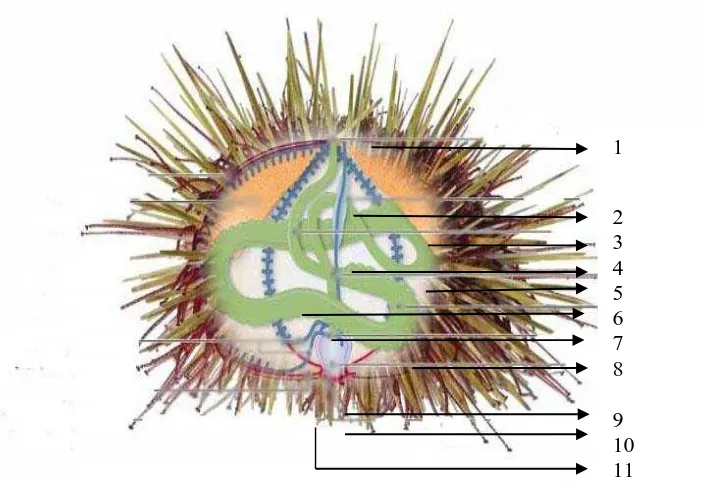
Gambar 2.1 Struktur anatomi landak laut (James, 2015).
Keterangan: 1. duri, 2.anus, 3.cangkang, 4.organ axial, 5. gonad, 6. usus, 7. esofagus, 8. perut, 9. lentera aristotel, 10. mulut, 11. saraf.
2.1.3 Klasifikasi landak laut
Klasifikasi hewan landak laut menurut LIPI (2015) adalah sebagai berikut: Filum : Echinodermata
Kelas : Echinoidea Bangsa : Diadematoida Suku : Diadematidae Marga : Diadema
Jenis : Diadema setosum (Leske ,1778).
2.2 Kandungan Golongan Senyawa Kimia
2.2.1 Alkaloid
Alkaloida merupakan golongan senyawa sekunder yang terbesar. Alkaloida mencakup senyawa bersifat basa yang mengandung satu atau lebih atom nitrogen,
1
2 3 4 5 6 7 8
biasanya sebagai bagian dari sistem siklik. Alkaloida mempunyai aktivitas fisiologi yang menonjol, sehingga banyak diantaranya digunakan dalam bidang pengobatan (Harborne, 1987).
Alkaloid selama ini diketahui adalah senyawa metabolit sekunder yang hanya terdapat dalam tumbuhan, namun setelah diidentifikasi senyawa alkaloid juga terdapat pada biota laut, Arthropoda dan katak neotropis (katak bewarna cerah). Alkaloid pada hewan berfungsi sebagai zat pertahanan seperti 2-metil-6-nonil piperidin yang diperoleh dari semut solenopsis yang memiliki khasiat sebagai hemolitik, insektisida dan antibiotik (Wiryowidagdo, 2008).
2.2.2 Glikosida
Glikosida adalah suatu golongan senyawa bila dihidrolisis akan terurai
menjadi gula (glikon) dan senyawa lain (aglikon atau genin). Gula yang ditemukan di dalam glikosida biasanya adalah monosakarida seperti glukosa, rhamnosa dan fruktosa. Glikosida terbentuk secara alami dimana setiap unsurnya mengandung gugus gula, bagian aglikon dari senyawa glikosida memiliki sifat fisika kimia yang bervariasi dan dan efek farmakologi yang dihasilkan juga berbeda (Evans, 2009).
Menurut Sirait (2007), berdasarkan ikatan antara glikon dan aglikon, glikosida dapat dibedakan menjadi:
a. Tipe O-glikosida, ikatan antara bagian glikon dengan aglikon melalui jembatan O. Mayoritas glikosida termasuk ke dalam kelompok ini.
c. Tipe C-glikosida, ikatan antara bagian glikon dengan aglikon melalui jembatan C, yakni gula melekat pada aglikon melalui ikatan karbon-karbon.
d. Tipe N-glikosida, ikatan antara bagian dari glikon dengan aglikon melalui jembatan N. Contoh: nikleosidin, kronotosidin.
2.2.3 Saponin
Saponin tersebar luas diantara tanaman tingkat tinggi. Saponin merupakan senyawa yang memiliki berat molekul yang besar dan sifat kepolarannya juga tinggi. Saponin adalah senyawa aktif permukaan yang kuat dan menimbulkan busa jika dikocok dalam air dan pada konsentrasi yang rendah menyebabkan hemolisis sel darah merah. Saponin mula-mula diberi nama demikian karena sifatnya yang menyerupai sabun (bahasa latin sapo berarti sabun) (Robinson, 1995).
Molekul saponin terdiri dari dua bagian yaitu, aglikon dan glikon. Berdasarkan aglikonnya, Hostettman (1995) membagi saponin menjadi 3 kelas utama yaitu:
1. Saponin triterpenoid 2. Saponin steroid
3. Saponin steroid alkaloid
2.2.4 Steroid/triterpenoid
Steroid adalah triterpena yang kerangka dasarnya sistem cincin
siklopentana perhidropenantren. Triterpenoid adalah senyawa yang kerangka karbonnya berasal dari enam satuan isoprena dan secara biosintesis masuk jalur asam mevalonat yang diturunkan dari hidrokarbon C30 asiklik, yaitu skualena (Harbone, 1987).
Uji yang banyak digunakan ialah reaksi Liebermannn-Burchard yang dengan kebanyakan triterpen memberikan warna merah-ungu dan steroid warna hijau-biru (Fansworth, 1996). Steroid pada umumnya berupa alkohol dengan gugus hidroksil pada C3 sehingga steroid sering juga disebut sterol (Robinson, 1995). Senyawa ini tersebar luas di alam dan memiliki fungsi biologi yang sangat penting, misalnya untuk kontrasepsi dan antiinflamasi. Gambar struktur dasar dapat dilihat pada Gambar 2.2.
Gambar 2.2 Struktur dasar steroid
2.3 Ekstraksi
dengan menggunakan pelarut menurut Depkes, RI (2000) yaitu: A. Cara dingin
1. Maserasi
Maserasi adalah proses ekstraksi simplisia menggunakan pelarut dengan beberapa kali pengocokan atau pengadukan pada temperatur kamar. Maserasi kinetik berarti dilakukan pengadukan yang kontinu (terus menerus). Remaserasi berarti dilakukan penyaringan berulang dan seterusnya.
2. Perkolasi
Perkolasi adalah proses ekstraksi simplisia dengan pelarut yang selalu baru sampai sempurna yang umumnya dilakukan pada temperatur ruangan. Proses perkolasi terdiri dari tahap pengembangan bahan, tahap maserasi antara, tahap perkolasi sebenarnya (penetesan/penampungan ekstrak), terus menerus sampai diperoleh ekstrak (perkolat) yang jumlahnya 1–5 kali bahan.
B. Cara panas 1. Refluks
Refluks adalah ekstraksi dengan menggunakan pelarut pada temperatur titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya pendingin balik.
2. Sokletasi
Sokletasi adalah proses ekstraksi dengan menggunakan alat Soklet dengan pelarut yang selalu baru, sehingga terjadi ekstraksi kontinu dengan jumlah pelarut yang relatif konstan dengan adanya pendingin balik.
3. Infundasi
4. Dekoktasi
Dekoktasi adalah proses ekstraksi dengan pelarut air pada temperatur penangas air (bejana infus tercelup dalam penangas mendidih, temperatur terukur 96–98oC), bedanya dengan infundasi adalah waktu yang digunakan lebih lama (≥ 30 menit).
2.4 Kromatografi
Kromatografi adalah suatu metode pemisahan berdasarkan perbedaan perpindahan dari komponen-komponen senyawa di antara dua fase yaitu fase diam (dapat berupa zat cair atau zat padat) dan fase gerak (dapat berupa gas atau zat cair). Kromatografi serapan dikenal jika fase diam berupa zat, jika zat cair dikenal sebagai kromatografi partisi (Sastrohamidjojo, 1985). Pemisahan dan pemurnian kandungan tumbuhan dilakukan dengan menggunakan salah satu atau gabungan dari beberapa teknik tersebut dan dapat digunakan pada skala mikro maupun makro (Harborne, 1987).
2.4.1 Kromatografi lapis tipis
Kromatografi lapis tipis merupakan analisis cepat yang memerlukan bahan sangat sedikit, baik penjerap maupun cuplikan. KLT dapat digunakan untuk memisahkan senyawa-senyawa yang sifatnya hidrofilik seperti lipid-lipid dan hidrokarbon yang sukar dikerjakan dengan kromatografi kertas. Bahan lapis tipis seperti silika gel adalah senyawa yang tidak bereaksi dengan pereaksi-pereaksi yang lebih reaktif seperti asam sulfat (Fessenden, 2003).
Pendeteksian bercak hasil pemisahan dapat dilakukan dengan beberapa cara. Pengamatan dengan sinar ultraviolet adalah cara sederhana yang dilakukan untuk senyawa tak berwarna. Beberapa senyawa organik bersinar atau berfluorosensi jika disinari dengan sinar ultraviolet gelombang pendek (254 nm) atau gelombang panjang (366 nm), jika dengan cara itu senyawa tidak dapat dideteksi maka harus dicoba dengan penyemprotan pereaksi yang membuat bercak tersebut tampak yaitu pertama tanpa pemanasan, kemudian bila perlu dengan pemanasan (Rohman, 2007).
2.4.2 Kromatografi preparatif
plat kromatografi lapis tipis preparatif dilakukan dalam bejana kaca yang dapat menampung beberapa plat. Bejana dijaga tetap jenuh dengan pelarut pengembang dengan bantuan kertas saring yang diletakkan berdiri disekeliling permukaan bagian dalam bejana (Hostettmann, 1995).
2.5 Spektrofotometri
2.5.1 Spektrofotometri sinar ultraviolet (UV)
Sinar ultraviolet mempunyai panjang gelombang antara 200-400 nm. Serapan cahaya oleh molekul dalam daerah spektrum ultraviolet tergantung pada struktur elektronik dari molekul yang bersangkutan (Sastrohamidjojo, 1985). Sistem ikatan rangkap yang diperpanjang dikenal sebagai kromofor. Kromofor paling umum ditemukan di dalam molekul obat adalah cincin benzena, jika terdapat lebih banyak ikatan rangkap pada struktur dalam konjugasi (yaitu dua ikatan rangkap atau lebih dalam suatu seri yang dipisahkan oleh ikatan tunggal), serapan terjadi pada panjang gelombang yang lebih panjang dan dengan intensitas yang lebih besar (Watson, 2010).
2.5.2.Spektrofotometri sinar inframerah(IR)
Pengukuran pada spektrum inframerah dilakukan pada daerah cahaya inframerah tengah (mid-infrared) yaitu pada panjang gelombang 2.5–50 �m atau bilangan gelombang 4000–200 cm-1. Energi yang dihasilkan oleh radiasi ini akan menyebabkan vibrasi atau getaran pada molekul. Pita absorpsi sinar inframerah
sangat khas dan spesifik untuk setiap tipe ikatan kimia atau gugus fungsi. Beberapa sinyal sangat mudah digunakan untuk mengidentifikasi jenis ikatan
variabel bending molekul menyerap pada daerah ini. Daerah ini disebut dengan daerah sidik jari (Dachriyanus, 2004).
Menurut pavia (1988), langkah-langkah umum untuk memeriksa pita-pita serapan yang penting yang umum untuk memeriksa gugus yang penting pada spektrum inframerah sebagai berikut :
1. Apakah terdapat gugus karbonil
Gugus C=O memberikan puncak pada daerah 1660-1820 cm-1. Puncak ini biasanya merupakan yang terkuat dengan lebar medium pada spektrum.
2. Jika gugus C=O ada, periksalah gugus-gugus berikut dan jika C=O tidak ada langsung ke nomor 3.
a. Asam: yaitu pada serapan melebar 2500-3000 cm -1 (biasanya tumpang tindih dengan C-H).
b. Amida: yaitu pada serapan medium di dekat 3500 cm-1, kadang-kadang dengan puncak rangkap.
c. Ester : yaitu pada serapan dengan intensitas medium di daerah 1000–1300 cm-1.
d. Anhidrida : mempunyai dua serapan C=O di daerah 1810 dan 1760 cm-1. e. Aldehida : yaitu dua serapan lemah di dekat 2850-2750 cm-1 disebelah
kanan serapan C-H
f. Keton : jika kelima kemungkinan diatas tidak ada. 3. Jika gugus C=O tidak ada
c. Eter : periksalah gugus C-O (dan tidak adanya –OH), yaitu serapan medium di daerah 1000–1300 cm-1.
4. Ikatan rangkap dua atau cincin aromatik yaitu adanya :
a. C=C yang mempunyai serapan lemah di daerah 1650 cm-1.
b. Serapan medium sampai kuat pada daerah 1450-1650 cm-1 sering menunjukkan adanya cincin aromatik.
5. Ikatan rangkap tiga yaitu adanya;
a. C≡N yang mempunyai serapan medium dan tajam di daerah 2250 cm-1 b. C≡C mempunyai serapan lemah tapi tajam di daerah 2150 cm-1 periksa juga
CH asetilenik di dekat 3300 cm-1. 6. Hidrokarbon