SISTEM ZAT CAIR TIGA KOMPONEN I. Tujuan
Membuat kurva kelarutan suatu cairan yang terdapat dalam dua cairan tertentu.
II. Dasar Teori
Sistem adalah suatu zat yang dapat diisolasikan dari zat – zat lain dalam suatu bejana inert, yang menjadi pusat perhatian dalam mengamati pengaruh perubahan temperature, tekanan serta konsentrasi zat tersebut. Sedangkan komponen adalah yang ada dalam sistem, seperti zat terlarut dan pelarut dalam senyawa biner. Banyaknya komponen dalam sistem C adalah jumlah minimum spesies bebas yang diperlukan untuk menentukan komposisi semua fase yang ada dalam sistem. Definisi ini mudah diberlakukan jika spesies yang ada dalam sistem tidak bereaksi sehingga kita dapat menghitung banyaknya.
Fasa merupakan keadaan materi yang seragam di seluruh bagiannya, tidak hanya dalam komposisi kimianya tetapi juga dalam keadaan fisiknya. Contohnya: dalam sistem terdapat fasa padat, fasa cair dan fasa gas. Banyaknya fasa dalam sistem diberi notasi P. Gas atau campuran gas adalah fasa tunggal ; Kristal adalah fasa tunggal dan dua cairan yang dapat bercampur secara total membentuk fasa tunggal. Campuran dua logam adalah sistem dua fasa (P=2), jika logam – logam itu tidak dapat bercampur, tetapi merupakan sistem satu fasa (P=1), jika logam-logamnya dapat dicampur.
Pada perhitungan dalam keseluruhan termodinamika kimia, J.W Gibbs menarik kesimpulan tentang aturan fasa yang dikenal dengan Hukum Fasa Gibbs, jumlah terkecil perubahan bebas yang diperlukan untuk menyatakan keadaan suatu sistem dengan tepat pada kesetimbangan diungkapkan sebagai:
F = C – P + 2 ...(1) dimana,
F = jumlah derajat kebebasan C = jumlah komponen
P = jumlah fasa
Kesetimbangan dipengaruhi oleh suhu, tekanan, dan komposisi sistem. Jumlah derajat kebebasan untuk sistem tiga komponen pada suhu dan tekanan tetap dapat dinyatakan sebagai :
Jika dalam sistem hanya terdapat satu fasa maka V = 2 berarti untuk menyatakan suatu sistem dengan tepat perlu ditentukan konsentrasi dari dua komponennya. Sedangkan bila dalam sistem terdapat dua fasa dalam kesetimbangan, V = 1; berarti hanya satu komponen yang harus ditentukan konsentrasinya dan konsentrasi komponen yang lain sudah tertentu berdasarkan diagram fasa untuk diagram fasa untuk sistem tersebut. Oleh karena itu sistem tiga komponen pada suhu dan tekanan tetap punya derajat kebebasan maksimum = 2 (jumlah fasa minimum = 1), maka diagram fasa sistem ini dapat digambarkan dalam satu bidang datar berupa suatu segitiga samasisi yang menggambarkan suatu komponen murni disebut diagram terner.
Cara terbaik untuk menggambarkan sistem tiga komponen adalah dengan mendapatkan suatu kertas grafik segitiga. Konsentrasi dapat dinyatakan dengan istilah persen berat atau fraksi mol. Fraksi mol tiga komponen dari sistem terner (C = 3) sesuai dengan: XA + XB + XC = 1. Diagram fasa yang digambarkan segitiga sama sisi, menjamin dipenuhinya sifat ini secara otomatis, sebab jumlah jarak ke sebuah titik di dalam segitiga sama sisi yang diukur sejajar denga sisi-sisinya sama dengan panjang sisi segitiga itu, yang dapat diambil sebagai satuan panjang. Puncak – puncak dihubungi ke titik tengah dari sisi yang berlawanan yaitu : Aa, Bb, Cc. Titik nol mulai dari titik a,b,c dan A,B,C menyatakan komposisi adalah 100% atau 1, jadi garis Aa, Bb, Cc merupakan konsentrasi A,B,C merupakan konsentrasi A,B,C.
Jumlah fasa dalam sistem zat cair tiga komponen bergantung pada daya saing larut antara zat cair tersebut dan suhu praktikum. Apabila pada suhu dan tekanan yang tetap digunakan kurva bimodal untuk menentukan kelarutan C dalam berbagai komposisi A dan B. Pada daerah di dalam kurva merupakan daerah dua fasa, sedangkan yang di luarnya adalah daerah satu fasa. Untuk menentukan kurva bimodal yaitu dengan menambahkan zat B ke dalam campuran A dan C. Penambahan zat C kedalam campuran A dan B akan memperbesar atau memperkecil daya saling larut A dan B.
Pada praktikum ini hanya akan ditinjau sistem yang memperbesar daya saling larut A dan B. Dalam hal ini A dan C serta B dan C saling larut sempurna. Kelarutan cairan C dalam berbagai komposisi campuran A dan B pada suhu tetap dapat digambarkan pada suatu diagram terner. Prinsip menggambarkan komposisi dalam diagram terner dapat dilihat pada gambar (1) dan (2) di bawah ini:
x
z
Titik A, B dan C menyatakan kompoenen murni. Titik-titik pada sisi Ab, BC dan Ac menyatakan fraksi dari dua komponen, sedangkan titik didalam segitiga menyatakan fraksi dari tiga komponen. Titik P menyatakan suatu campuran dengan fraksi dari A, B dan C masing-masing sebanyak x, y dan z.
Titik X menyatakan suatu campuran dengan fraksi A = 25%, B = 25%, dan C = 50%. Titik-titik pada garis BP dan BQ menyatakan campuran dengan perbandingan dengan jumlah A dan C yang tetap, tetapi dengan jumlah B yang berubah. Hal yang sama berlaku bagi garis-garis yang ditarik dari salah satu sudut segitiga kesisi yang ada dihadapannya. Daerah didalam lengkungan merupakan daerah dua fasa. Salah satu cara untuk menentukan garis binoidal atau kurva kelarutan ini ialah dengan cara menambah zat B ke dalam berbagai komposisi campuran A dan C. Titik-titik pada lengkungan menggambarkan komposisi sistem pada saat terjadi perubahan
dari jernih menjadi keruh. Kekeruhan timbul karena larutan tiga komponen yang homogen pecah menjadi dua larutan konjugat terner.
III. Alat dan Bahan
1. Labu tertutup 100 ml 5 buah 2. Erlenmeyer 250 ml 3 buah 3. Buret 50 ml 3 buah
4. Neraca 5. Thermometer 6. Kloroform
7. Asam asetat glasial 8. Aquades
IV. Cara Kerja
1. Dalam labu erlenmeyer yang bersih, kering dan tertutup, buatlah 9 macam campuran cairan A dan C yang saling larut sempurna dengan komposisi sebagai berikut :
Labu 1 2 3 4 5 6 7 8 9
mL A 1 2 3 4 5 6 7 8 9
mL C 9 8 7 6 5 4 3 2 1
Semua pengukuran volume dilakukan dengan buret
2. Titrasi tiap campuran dalam labu 1 s/d 9 dengan zat B sampai tepat timbul kekeruhan, dan catat jumlah volume zat B yang digunakan. Lakukan titrasi dengan perlahan-lahan
3. Tentukan rapat massa masing-masing cairan murni A, B dan C 4. Catat suhu kamar sebelum dan sesudah praktikum
V. Hasil Pengamatan dan Pembahasan
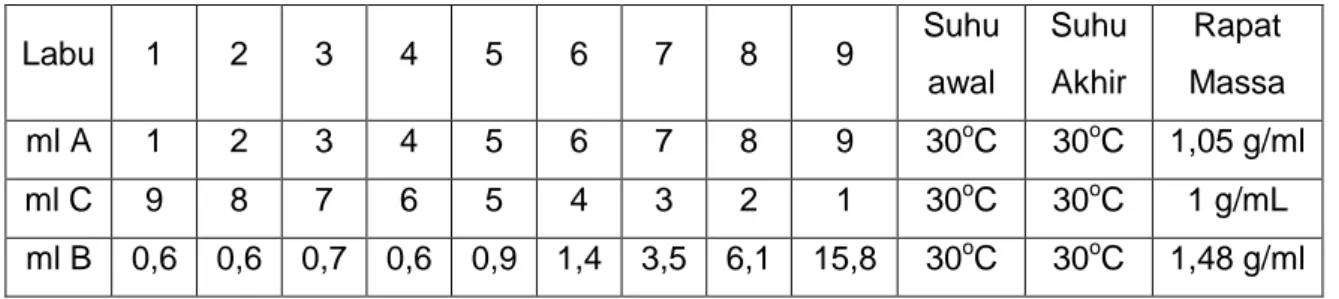
Labu 1 2 3 4 5 6 7 8 9 Suhu awal Suhu Akhir Rapat Massa ml A 1 2 3 4 5 6 7 8 9 30oC 30oC 1,05 g/ml ml C 9 8 7 6 5 4 3 2 1 30oC 30oC 1 g/mL ml B 0,6 0,6 0,7 0,6 0,9 1,4 3,5 6,1 15,8 30oC 30oC 1,48 g/ml
Pada praktikum ini dilakukan percobaan mengenai sistem zat cair tiga komponen. Praktikum ini bertujuan untuk membuat kurva kelarutan suatu cairan yang terdapat dalam campuran dua zat cair tertentu. Prinsip dasar dari praktikum ini adalah pemisahan suatu campuran dengan ekstraksi yang terdiri dari dua komponen cair yang saling larut dengan sempurna. Pemisahan dapat dilakukan dengan menggunakan pelarut yang tidak larut dengan sempurna terhadap campuran, tetapi dapat melarutkan salah satu komponen (solute) dalam campuran tersebut. Cairan yang digunakan dalam praktikum ini adalah air, kloroform dan asam asetat. Dalam system tiga komponen digunakan tiga jenis larutan yang mempunyai sifat yang berbeda-beda, air (polar), kloroform (nonpolar), dan asam asetat yang bersifat semipolar. Penggunaan ketiga zat ini karena hanya akan bercampur sebagian (menurut teori) sehingga digunakan bahan ini untuk membuktikan teori tersebut. Asam asetat sebagai zat A, air sebagai zat C, sedangkan kloroform digunakan sebagai titran (zat B).Penambahan air dilakukan dengan menggunakan buret agar dapat dilakukan dengan teliti. Setelah larutan dicampur terbentuk dua lapisan yaitu asam asetat yang sifatnya semipolar pada bagian atas karena memiliki massa jenis yang lebih rendah (1,05 g/mL) sedangkan kloroform yang bersifat nonpolar berada pada bagian bawah karena massa jenisnya lebih besar dari air yaitu 1,48 g/mL. Campuran ini kemudian dititrasi dengan air agar larutan ini menjadi satu fasa, karena air bersifat polar sehingga dapat mencampurkan dua jenis larutan yang berbeda sifat menjadi satu fasa. Titrasi dihentikan saat larutan telah menjadi keruh.
Volume yang digunakan untuk membuat larutan menjadi keruh itulah
banyaknya
larutan kloroform yang dapat larut dalam air dan asam asetat. Untuk titrasi ini
dilakukan dengan
sembilan buah labu erlenmeyer dimana masing masing labu dimasukkan
air dan asam asetat
dengan fraksi mol yang berbeda,
fraksi mol asam asetat meningkat
dengan naiknya nomor labu
erlenmeyer, sedangkan fraksi mol air turun dengan naiknya
nomor labu erlenmeyer. Dari
percobaan didapat bahwa untuk mengeruhkan larutan asam
asetat diperlukan kloform makin
banyak dengan naiknya nomor labu erlenmeyer.
Metode titrasi ini dapat digunakan untuk memisahkan campuran yang terdiri dari dua cairan yang saling melarut sempurna yaitu air dan asam asetat dititrasi dengan zat yang tidak larut dengan campuran tersebut yaitu kloroform.Dari percobaan yang dilakukan proses percampuran tiga komponen terjadi pada
suhu konstan, suhu awal dan suhu akhir pada kedua tahap percobaan tidak mengalami
perubahandan tetap pada suhu 30
oC ini membuktikan bahwa sistem tiga komponen terjadi
padatemperatur dan tekanan tetap. Dari perhitungan dapat disimpulkan bahwa kloroform lebih
banyak larut dalam asam asetat,karena banyaknya kloroform yang dibutuhkan untuk mengeruhkan
larutan titer sebanding dengan banyaknya asam asetat yang terdapat dalamlarutan titer sehingga
berdasarkan data yang diperoleh dapat diketahui bahwa
harga fraksi mol rata-rata untuk zat A (asam asetat) adalah sebesar 26,8; zat B (kloroform) sebesar 8,462; zat C (air) sebesar 64,72 sehingga dapat dibuat diagram fasa sistem untuk masing – masing praktikum yang digambarkan dalam satu bidang datar berupa suatu segitiga sama sisi yang disebut diagram terner. Tiap sudut segitiga itu menggambarkan suatu komponen murni. Titik menyatakan campuran terner dengan komposisi x% mol A, y% mol B dan z% mol C. Jumlah fasa dalam sistem zat cair tiga komponen bergantung pada daya saling larut antar zat cair tersebut.Berdasarkan praktikum yang telah dilakukan terlihat bahwa semakin banyak volume asam asetat dan air yang digunakan semakin banyak maka kloroform yang digunakan semakin sedikit. Larutan yang mengandung dua komponen yang saling larut sempurna akan membentuk daerah berfase tunggal, sedangkan untuk komponen yang tidak saling larut sempurna akan membentuk daerah fase dua. Semakin kecil perbandingan volume asam asetat maka konsentrasinya makin kecil.
Chemistry.2010.Kesetimbangan Fasa dan Diagram Fasa.http://chem-is-try.com
(diakses pada tanggal 27 November 2012 06:23 pm)
Dogra.2008.Kimia Fisik Dan Soal-Soal.Erlangga.Bandung.
Konneth.1993.Prinsip-Prisip Kesetimbangan Kimia Edisi Keempat.UI-press Jakarta.
Mulyani,Sri.2004.Kimia Fisik I.UPI.Jakarta
Sukardjo.1997.Kimia Fisika.Bineka Cipta.Jogyakarta
LAMPIRAN
Tabel Hasil Pengamatan
Perhitungan Labu 1 Labu 1 2 3 4 5 6 7 8 9 Suhu awal Suhu Akhir Rapat Massa ml A 1 2 3 4 5 6 7 8 9 30oC 30oC 1,05 g/ml ml C 9 8 7 6 5 4 3 2 1 30oC 30oC 1 g/mL ml B 0,6 0,6 0,7 0,6 0,9 1,4 3,5 6,1 15,8 30oC 30oC 1,48 g/ml
Labu 2 Labu 3
Labu 4 Labu 5
Labu 6 Labu 7
Labu 8 Labu 9 ̅̅̅
̅̅̅̅ ̅̅̅̅