UIN SYARIF HIDAYATULLAH JAKARTA
HUBUNGAN KUANTITATIF STRUKTUR
AKTIVITAS (HKSA) TURUNAN ASAM SINAMAT
TERHADAP SEL P388
SKRIPSI
AHMAD ARSYADUL MUSHLIHIN
1111102000020
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
PROGRAM STUDI FARMASI
JAKARTA
JUNI 2015
UIN SYARIF HIDAYATULLAH JAKARTA
HUBUNGAN KUANTITATIF STRUKTUR
AKTIVITAS (HKSA) TURUNAN ASAM SINAMAT
TERHADAP SEL P388
SKRIPSI
Diajukan sebagai salah satu syarat memperoleh gelar Sarjana Farmasi
AHMAD ARSYADUL MUSHLIHIN
1111102000020
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
PROGRAM STUDI FARMASI
JAKARTA
JUNI 2015
ABSTRAK
Judul : HUBUNGAN KUANTITATIF STRUKTUR AKTIFITAS
(HKSA) TURUNAN ASAM SINAMAT TERHADAP SEL P388
Telah dilakukan analisis hubungan kuantitatif struktur dan aktivitas (HKSA) turunan asam sinamat terhadap sel p388 dengan menggunakan deskriptor parameter hidrofobik berupa log P dan log D, parameter sterik berupa indeks Harary, indeks Randic, dan indeks Wiener, dan parameter elektronik berupa PPSA1 dan PNSA1. Tujuan dari penelitian ini adalah untukpmendapatkan model persamaan HKSA yang baik dan dapat digunakan untuk memprediksi aktivitas antikanker senyawa turunan asam sinamat lain.Data aktivitas biologis yang digunakan ialah data aktivitas antikanker terhadap sel p388 yang didapat dari berbagai literatur. Data set yang didapat kemudian dibagi menjadi training set 75% dan tes set 25%.Model persamaan HKSA dibentuk dengan menggunakan Multilinear Regression (MLR) dengan metode enter sehingga didapatkan model persamaan seagai berikut :
Log1/IC50= -4,793 + (-0,983 logP) + (-0,00898 PPSA) + (-0,00138 PNSA) + 0,378 harary + 0,191 randic + (-0,008705 WPATH) + (-0,3247 WPOL)
Dari 6 senyawa turunan asam sinamat lain yang diprediksi aktivitasnya senyawa 2-(3-Phenyl-acryloyloxy)-benzoic acidmemiliki aktivitas antikanker paling baik dengan IC50 4,29 µM
ABSTRACT
Title : QUANTITATIVE STRUCTURE ACTIVITY RELATIONSHIP (QSAR)CINNAMIC ACID DERIVATIVES OF THE P388CELLS
An analysis towards the quantitative structure activity relationship (QSAR) cinnamic acid derivatives of the P388 cells using a hydrophobic parameter descriptors such as of log P and log D, steric parameters such as index Harary, Randic index, and the Wiener index, and electronic parameters such as PPSAI and PNSAI has been done recently. The objectives of this research were to obtain good QSAR equation model and to predict the anticancer activity of other cinnamic acid derivatives. Biological activity data being used was the anticancer activity data of the P388 cells that were obtained from various literatures. The data set then was divided into training set 75% and test set 25%. QSAR equation model was formed by used Multilinear Regression (MLR) with enter method and it was obtained the equation model as below:
Log1/IC50= -4,793 + (-0,983 logP) + (-0,00898 PPSA) + (-0,00138 PNSA) + 0,378 harary + 0,191 randic + (-0,008705 WPATH) + (-0,3247 WPOL)
From the six other cinnamic acid derivative compounds wichactivityare being predicted,2-(3-Phenyl-acryloyloxy)-benzoic acidshowed the best anticancer activity with IC50 4.29 µM.
KATA
PENGANTAR
Puji dan syukur senantiasa kami panjatkan kehadirat Tuhan Yang Maha Esa Allah SWT yang telah melimpahkan berbagai macam nikmat, karunia serta kasih sayang-Nya sehingga penulis dapat menyelesaikan penelitian dan penyusunan skripsi ini. Shalawat serta salam tak lupa pula kami haturkan kepada pemimpin seluruh umat dan rahmat bagi semesta alam baginda Nabi Besar Muhammad SAW, beserta keluarga, sahabat dan para pengikutnya hingga hari akhir nanti, semoga kita senantiasa mendapatkan syafaat dari beliau.
Skripsi dengan judul “Hubungan Kuantitatif Struktur Aktivitas (HKSA) Turunan Asam Sinamat Terhadap Sel P388” ini disusun untuk memenuhi salah satu syarat menempuh ujian akhir guna mendapatkan gelar Sarjana Farmasi pada Program Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri Syarif Hidayatullah Jakarta.
Dalam proses penelitian dan penyusunan skripsi ini, penulis menyadari adanya beberapa pihak yang memberikan kontribusi kepada penulis. Oleh karena itu penulis mengucapkan rasa terima kasih yang sebesar-besarnya, khususnya kepada :
1. Supandi M. Si., Apt. sebagai Pembimbing I dan Andrianopsyah Mas Jaya Putra, M. Sc. sebagai Pembimbing II yang telah meluangkan waktu, pikiran dan tenaganya serta memberikan ilmu terbaik yang dimiliki sehingga menutupi banyak keterbatasan penulis.
2. Dr. H. Arif Sumantri, SKM., M. Kes. selaku Dekan Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta.
3. Yardi, M. Sc., P.hD., Apt. selaku Ketua Program Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta.
4. Ibu/Bapak Dosen dan Staff Akademika Program Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri Syarif Hidayatullah Jakarta yang telah memberikan ilmunya kepada penulis.
5. Sahabat-sahabat GR (Bisrie, Sam’ul, Fikri, Habibie) yang selalu menghibur dan menyemangati penulis.
6. Ayahanda Mohammad Yahya pemimpin dalam keluarga dunia yang selalu menjadi panutan penulis dalam meraih cita-cita dan Ibunda Balkis tercinta, bidadari dalam hidup ini yang selalu memberikan kasih sayang, semangat, dukungan, do’a dan nasihat tak terhingga yang tak akan pernah mampu penulis membalas semua itu. Saudara penulis Ade Musyrifah Zahroh, Aliya Luthfiyyah Khumairo yang selalu memberikan semangat dan dorongan untuk kesuksesan penulis. Beribu cinta untuk kalian semua. 7. Kakak-kakak Farmasi, Arif, Agung, Dimas, Fikri dan semua kakak 2009
serta 2010 lain yang selalu ikhlas membantu dan memberikan bimbingan selama penulis berada di lingkungan kampus hingga saat penulis selesai mengerjakan penelitian ini.
8. Sahabat-sahabat D8 (Akas, Deni, Rifki, Mufidah, Monic, Nanda, Puspita) yang selalu mengingatkan penulis untuk terus bersemangat menyelesaikan skripsi ini
9. Teman-teman SODA (Agus, Shinta, Bona, Hari, Kak Rima, Nasar, Jamal), PETANG, Keluarga Universitas Kehidupan, Keluarga Tantra yang menemani pendakian penulis ketika penulis sedang membutuhkan inspirasi dalam menulis skripsi.
10. Teman-teman Docking Team (Eko, Mazaya, Wahidin, Wahyu, Haidar) yang selalu membantu penulis dalam melakukan penelitian ini.
11. Teman-teman farmasi angkatan 2011, Semut (sebelas imut) yang telah berjuang bersama selama penelitian ini.
Penulis sadar bahwa dalam penulisan skripsi ini masih banyak kelemahan dan kekurangan, kritik dan saran pembaca diharapkan penulis untuk memperbaiki kemampuan penulis.
Jakarta, Juli 2015
DAFTAR ISI
Halaman
HALAMAN JUDUL ... ii
LEMBAR ORIGINALITAS ... iii
LEMBAR PERSETUJUAN SKRIPSI ... iv
LEMBAR PENGESAHAN SKRIPSI ... v
ABSTRAK ... vi
ABSTRACT ... vii
KATA PENGANTAR ... viii
HALAMAN PERSETUJUAN PUBLIKASI KARYA ILMIAH ... x
DAFTAR ISI ... xi
DAFTAR GAMBAR ... xiii
DAFTAR TABEL ... xiv
DAFTAR LAMPIRAN ... xv BAB 1 PENDAHULUAN 1.1. Latar Belakang ... 1 1.2. Rumusan Masalah ... 3 1.3. Hipotesis ... 3 1.4. Tujuan Penelitian... 3 1.5. Manfaat Penelitian... 4
BAB 2 TINJAUAN PUSTAKA 2.1. Kanker ... 5
2.1.1. Perbedaan Sel Kanker dan Sel Normal ... 7
2.1.2. Leukemia (Kanker Darah) ... 9
2.2. Asam Sinamat ... 10
2.3. Hubungan Kuantitatif Struktur Aktivitas (HKSA) ... 12
2.4. Metode Hansch ... 14
2.4.1. Parameter Sifat Kimia Fisika dalam HKSA Model Hansch . 15 2.5. Deskriptor ... 19
2.8. LigandScout………. 21
2.9. Open Babel……… 21
2.10.CDK descriptor ……….. 22
2.11PubChem ………. 22
BAB 3 METODE PENELITIAN 3.1. Waktu Penelitian dan Lokasi ... 23
3.2. Alat ... 23
3.2.1. Perangkat Keras... 23
3.2.2. Perangkat Lunak ... 23
3.3. Bahan ... 23
3.4. Prosedur Kerja ... 23
BAB 4 HASIL DAN PEMBAHASAN 4.1. Pengumpulan Data Set ... 26
4.2. Pemilihan Deskriptor... 38
4.3. Penghilangan Outlier... 45
4.4. Pembagian Data Set ... 46
4.5. Model Persamaan HKSA ... 47
4.6. Hasil Validasi Model Persamaan HKSA ... 49
4.7. PengujianAktivitas Sampel Set ... 51
BAB 5 KESIMPULAN DAN SARAN 5.1. Kesimpulan... 54
5.2. Saran ... 54
DAFTAR PUSTAKA ... 55
DAFTAR GAMBAR
Gambar 2.1. Struktur Asam Sinamat ... 11
Gambar 2.2. Naga dalam Mitologi Babylon Istar ... 20
Gambar 4.1. Pembuatan Struktur Asam Sinamat ... 26
Gambar 4.2. Struktur Senyawa dengan Kode S1 dan S7 ... 40
Gambar 4.3. Struktur Senyawa dengan Kode S14 dan S20 ... 42
Gambar 4.4. Kurva Hubungan Indeks Harary Terhadap Kenaikan Aktivitas ... 44
Gambar 4.5. Pensejajaran Data Set Terhadap Asam Sinamat ... 45
DAFTAR TABEL
Tabel 4.1. Struktur dan Aktivitas Data Set 27
Tabel 4.2. Data Aktivitas, log P, dan log D 38
Tabel 4.3. Data Deskriptor Sterik 42
Tabel 4.4. Korelasi Deskriptor terhadap Aktivitas 44
Tabel 4.5.Data Set Berdasarkan Aktivitas 46
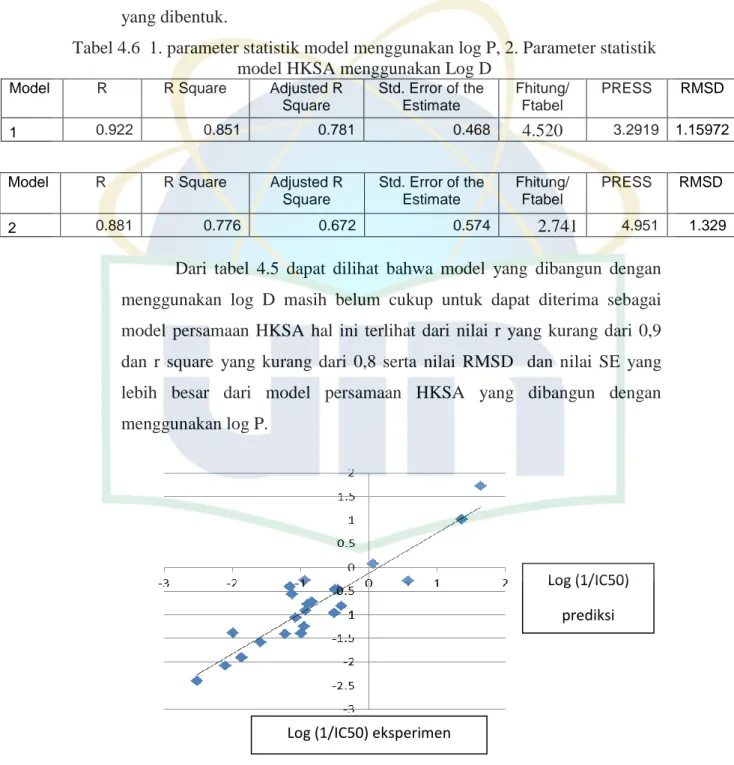
Tabel 4.6.Parameter Statistik Dua Model Persamaan HKSA 50
DAFTAR LAMPIRAN
Lampiran 1. Alur Penelitian ... 59
Lampiran 2. Tabel Korelasi Deskriptor Terhadap Aktivitas Menggunakan log D ... 60
Lampiran 3. Tabel Korelasi Deskriptor Terhadap Aktivitas Menggunakan Log P ... 60
Lampiran 4. Validasi Persamaan HKSA menggunakan log D ... 61
Lampiran 5. Validasi Persamaan HKSA menggunakan log P ... 62
Lampiran 6. Rekap Perhitungan Deskriptor ... 63
BAB I
PENDAHULUAN
1.1 Latar Belakang
Kanker adalah istilah penyakit yang dapat mempengaruhi bagian dari tubuh manusia, istilah lain yang digunakan untuk kanker adalah tumor dan neoplasma. Salah satu tanda umum yang terjadi pada kanker adalah pertumbuhan sel-sel yang lebih cepat dari pertumbuhan sel normal, kemudian sel kanker akan menyerang tubuh kemudian akan menyebar kebagian lain. Kanker merupakan penyebab kematian terbesar didunia yang dihitung dari 8,2 juta kematian pada tahun 2012. Kasus kanker yang paling banyak menyebabkan kematian berturut-turut adalah: kanker paru-paru (1,59 juta kematian), kanker hati (745.000 kematian), kanker perut (723.000 kematian), kanker kolon (694.000 kematian), kanker payudara (521.000 kematian), kanker esophagus (400.000 kematian) (WHO 2014). Kanker atau malignant neoplasm merupakan penyakit dengan karakteristik pertumbuhan sel yang tidak terkendali. Kanker umumnya disebabkan oleh pemakaian tembakau (merokok), konsumsi makanan yang tidak sehat, infeksi tertentu, paparan radiasi, kurangnya aktivitas fisik, obesitas, dan polutan lingkungan. Faktor-faktor ini dapat secara langsung merusak gen atau menyebabkan kesalahan kode genetik sehingga memicu mutasi sel kanker (Anand dkk, 2008).
Dibandingkan dengan penyakit kanker lain seperti kanker paru dan kanker payudara, leukemia (kanker darah) termasuk kanker yang jarang terjadi. Meskipun demikian, leukemia merupakan jenis kanker yang paling banyak ditemukan pada anak dibawah 15 tahun. Dari seluruh kejadian kanker terdapat 32% yang terjadi pada usia dibawah 15 tahun. Sekitar 74% dari kelompok umur yang sama adalah kanker darah atau leukemia (Belson dkk., 2007). Murine Leukimia P388 merupakan salah satu sel jenis sel kanker leukemia yang sering digunakan dalam uji sitotoksisitas untuk mengetahui aktivitas suatu senyawa dalam menghambat pertumbuhan sel
kanker. Sel kanker ini dikembang biakkan dari sel tikus yang dikenai agen leukemia (Marwati, 2012).
Terdapat 3 pengobatan yang dapat dilakukan pada pasien yang terkena kanker yaitu: pembedahan, radioterapi, dan kemoterapi. Akan tetapi kemoterapi biasanya digunakan bersamaan dengan radioterapi maupun pembedahan. Pengobatan menggunakan kemoterapi mempunyai beberapa mekanisme yang berbeda, salah satu dari mekanismenya yaitu dengan menghambat pensinyalan pada sel kanker (Patric, 2009). Pengobatan dengan menggunakan obat-obat antikanker klasik tidak mampu membedakan antara sel normal dan sel kanker, memiliki efek samping yang berbahaya, sehingga membatasi penggunaannya dalam jangka panjang. Kekurangan-kekurangan inilah yang menyebabkan peneliti mencari obat yang selektif, dan lebih tidak toksik (El-Deeb, dkk., 2009)
Asam Sinamat dan turunannya merupakan senyawa aromatis yang terdapat di alam. Isolasi asam sinamat dan turunannya dapat dilakukan dari propolis lebah, kayu manis, dan banyak tumbuhan, terutama rempah-rempah, seperti: jahe, kencur, lengkuas dan bahkan buah-buahan (Shirat, dkk., 2011). Asam sinamat dan turunannya memiliki aktivitas yang beragam diantaranya: anti inflamasi, anti hipertensi, anti mikroba, anti diabetik serta antikanker (Ramesh, 2012). Turunan asam sinamat dari propolis lebah dilaporkan memiliki aktivitas anti tumor yang dapat membunuh sel tumor (Mishima, dkk., 2005). Asam sinamat secara kimia memiliki tiga gugus fungsi yang berpotensi sebagai sisi aktif, yakni subtitusi pada cincin fenil, α,β unsaturated (ikatan rangkap), dan reaksi pada gugus karboksilat.
Kemajuan teknologi informasi pada saat ini dapat dijadikan alternatif untuk pencarian obat baru. Kimia komputasi dan bioinformatika berpotensi tinggi dalam ilmu kimia medisinal, tidak hanya mempercepat proses penemuan obat tetapi juga mengubah cara penemuan dan perancangan obat. Rational Drug Design (RDD) memfasilitasi dan mempercepat proses rancangan obat, yang melibatkan berbagai metode
untuk mengidentifikasi senyawa baru (Koko, 2011). Salah satu aplikasi kimia komputasi yang paling sering digunakan dalam desain senyawa obat antaralain adalah kajian Hubungan Kuantitatif Struktur-Aktivitas (HKSA). Kajian HKSA bertujuan untuk mencari hubungan yang konsisten secara empiris antara sifat-sifat molekular dan aktivitas biologis suatu senyawa (Saputra, 2014).
Berdasarkan pada parameter yang digunakan, analisa HKSA digolongkan dalam 3 metode, yaitu metode Hansch, metode Free-Wilson dan metode 3 dimensi (Comparative Molecular Field Analysis (CoMFA)). Metode Hansch berkembang dari pemikiran bahwa interaksi senyawa dengan reseptor terjadi karena adanya efek gaya-gaya intermolekular seperti interaksi hidrofobik, interaksi polar, interaksi elektrostatik dan efek sterik senyawa. Analisis HKSA-3D dikembangkan sebagai antisipasi permasalahan yang terdapat pada metode Hansh, yaitu senyawa-senyawa enantiomer yang memiliki kuantitas sifat fisikokimia yang sama, tetapi memiliki aktivitas biologis berbeda (Ridhatul, 2013).
Pada penelitian ini akan dilakukan pengujian Hubungan Kuantutatif Struktur Aktivitas (HKSA) senyawa turunan asam sinamat dengan metode Hansch. Hal ini dilakukan karena kemajuan teknologi dalam bidang kimia komputasi yang memungkinkan untuk mempercepat dan menghemat biaya dalam melakukan pencarian kandidat obat baru. 1.2 Rumusan Masalah
Apakah senyawa-senyawa turunan asam sinamat memiliki hubungan kuantitatif struktur dan aktivitas yang baik terhadap sel P388?
1.3 Hipotesis
Senyawa-senyawa turunan asam sinnamat memiliki hubungan kuantitatif struktur dan aktivitas yang baik terhadap sel P388
1.4 Tujuan Penelitian
1) Membentuk model persamaan hubungan kuantitatif struktur aktivitas (HKSA) turunan asam sinamat terhadap sel P388.
1.5 Manfaat Penelitian
1) Membantu memberikan informasi untuk menemukan obat antikanker yang baru
BAB 2
TINJAUAN PUSTAKA 2.1. Kanker
Kanker adalah istilah penyakit yang dapat mempengaruhi bagian dari tubuh manusia, istilah lain yang digunakan untuk kanker adalah tumor dan neoplasma. Salah satu tanda umum yang terjadi pada kanker adalah pertumbuhan sel-sel yang lebih cepat dari pertumbuhan sel normal, kemudian sel kanker akan menyerang tubuh kemudian akan menyebar kebagian lain. Kanker merupakan penyebab kematian terbesar didunia yang dihitung dari 8,2 juta kematian pada tahun 2012. Kasus kanker yang paling banyak menyebabkan kematian berturut-turut adalah: kanker paru-paru (1,59 juta kematian), kanker hati (745.000 kematian), kanker perut (723.000 kematian), kanker kolon (694.000 kematian), kanker payudara (521.000 kematian), kanker esophagus (400.000 kematian). (WHO 2014).
Kanker atau malignant neoplasm merupakan penyakit dengan karakteristik pertumbuhan sel yang tidak terkendali. Kanker umumnya disebabkan oleh pemakaian tembakau, konsumsi makanan yang tidak sehat, infeksi tertentu, paparan radiasi, kurangnya aktivitas fisik, obesitas, dan polutan lingkungan. Faktor-faktor ini dapat secara langsung merusak gen atau menyebabkan kesalahan kode genetik sehingga memicu mutasi sel kanker (Anand dkk, 2008). Penyebab lain yang juga dapat menyebabkan kanker adalah virus, contohnya yaitu Human Papilloma Virus (HPV) yang dapat menyebabkan kanker Rahim (Katzung ed 9).
Umumnya kanker berbentuk tumor, walaupun tidak semua tumor adalah kanker. Tumor adalah pertumbuhan spontan jaringan baru yang tidak mempunyai fungsi fisiologis, justru dapat menimbulkan gangguan bahkan bersifat patologis. Tumor dapat bersifat benign (beninga), artinya tidak berkembang menjadi kanker, misalnya kutil yang tidak menyebar. Akan tetapi tumor juga dapat bersifat malignant (maligna), yang artinya dapat menyebar seperti kanker paru yang dapat menyebar ke jaringan atau organ-organ sekitarnya (Silalahi, 2006 )
Kanker berawal dari kerusakan materi genetic DNA (Deoxyribo Nucleic Acid) sel. Satu sel saja yang mengalami kerusakan genetic sudah mampu menghasilkan sel kanker atau neoplasma, sehigga kanker disebut juga penyakit seluler. Kerusakan atau mutasi genetika yang dapat menyebabkan kanker dapat terjadi karena factor dalam (endogen), yaitu melalui kesalahan replikasi pada saat sel-sel digantikan oleh sel baru, atau kesalahan genetic yang disebabkan oleh keturunan (orang tua) kanker yang disebabkan factor endogen terjadi sebanyak 10-15%. Kanker juga dapat disebabkan oleh factor luar atau eksogen (85-90%) melalui perubahan struktur DNA akibat virus, infeksi berkelanjutan, polusi udara, radiasi, dan bahan-bahan kimia (Silalahi, 2006 ).
Sel kanker mengganggu sel induk karena menyebabkan desakan akibat pertumbuhan tumor, penghancuran jaringan tempat tumor berkembang atau bermetastasis, dan gangguan sistemik lain sebagai akibat sekunder dari pertumbuhan sel kanker (Nafrialdi dan Gan, 2007). Agen penyebab kanker disebut karsinogen. Penyebab tunggal untuk terjadinya kanker hingga saat ini belum diketahui. Namun demikian, berdasarkan laporan berbagai penelitian dapat diketahui bahwa karsinogen digolongkan ke dalam 4 golongan yaitu :
a. Bahan kimia, karsinogen bahan kimia melalui metabolisme membentuk gugus elektrofilik yang kurang muatan elektron, sebagai hasil antara, yang kemudian dapat berikatan dengan pusat-pusat nukleofilik pada protein, RNA dan DNA.
b. Virus, contohnya adalah pada golongan virus DNA seperti virus hepatitis B yang menyebabkan kanker hati.
c. Radiasi, terutama radiasi ultraviolet dengan panjang gelombang 290-370 nm berkaitan dengan terjadinya kanker kulit.
d. Agen biologis, antara lain hormon estrogen yang membantu pembentukan kanker payudara dan kanker rahim. Serangkaian proses berkembangnya kanker disebut karsinogenesis.
Karsinogenesis adalah suatu proses terjadinya kanker melalui mekanisme multitahap yang menunjukkan perubahan genetik dan
menyebabkan transformasi progresif sel normal menjadi sel malignan (ganas) (Hanahan dan Weinberg, 2000). Perubahan basa DNA (mutasi) merupakan perubahan selular mendasar yang menyebabkan terjadinya kanker. Kanker tidak berasal dari mutasi tunggal, namun dibutuhkan akumulasi dari beberapa mutasi (3 sampai 20 mutasi) dalam karsinogenesis (Lodish dkk., 2004).
Karsinogenesis melibatkan inisiasi, promosi, progresi, dan metastasis. Inisiasi merupakan perubahan spesifik pada DNA sel target yang menuntun pada proliferasi abnormal sebuah sel. Sel yang mengalami inisiasi atau prakanker dapat kembali ke tingkat normal secara spontan, tetapi pada tingkat lebih lanjut menjadi ganas. Promosi merupakan tingkat lanjutan dari tahap inisiasi. Sel-sel akan memperoleh beberapa keuntungan selektif untuk tumbuh sehingga pertumbuhannya menjadi cepat dan berubah menjadi bentuk tumor jinak. Tahap promosi berlangsung lama, bisa lebih dari sepuluh tahun. Pada tahap perkembangan (progression), terjadi instabilitas genetik yang menyebabkan perubahan-perubahan mutagenik dan epigenetik. Proses ini akan menghasilkan klon baru sel-sel tumor yang memiliki aktivitas proliferasi, bersifat invasif (menyerang) dan potensi metastatiknya meningkat. Metastasis melibatkan beberapa tahap yang berbeda, termasuk memisahnya sel kanker dari tumor primer, masuk ke dalam sirkulasi dan limfatik, serta perlekatan pada permukaan jaring baru (Silalahi, 2006).
Untuk menghambat metastase sel kanker, kita harus mengetahui cara kanker tersebut menyebar. Ada dua cara sel kanker ber-metastase, yaitu melalui angiogenesis (pembentukan pembuluh darah yang baru) dan penghancuran kolagen yang merupakan kerangka sel normal. Dengan demikian, metastase akan dapat dihambat bila angiogenesis dapat dicegah, sementara kolagen yang rusak bisa diperbaiki oleh tubuh sendiri dengan memanfaatkan makanan tertentu
2.1.1. Perbedaan Sel Kanker dan Sel Normal
Sel kanker memiliki perbedaan yang sangat signifikan dengan sel normal dalam tubuh. Sifat umum dari kanker ialah sebagai berikut :
1. Sel kanker tidak mengenal program kematian sel yang dikenal dengan nama apoptosis. Protein p53 mampu mencegah replikasi dari DNA yang rusak pada sel normal dan mendorong penghancuran sendiri dari sel yang mengandung DNA yang tidak normal. Peristiwa ini disebut apoptosis. Apoptosis sangat dibutuhkan untuk mengatur berapa jumlah sel yang dibutuhkan dalam tubuh, yang mana semuanya fungsional dan menempati tempat yang tepat dengan umur tertentu. Bila telah melewati masa hidupnya, sel-sel normal (nonkanker) akan mati dengan sendirinya tanpa ada efek peradangan (inflamasi), namun sel kanker berbeda dengan karakteristik tersebut. Dia akan terus hidup meski seharusnya mati (immortal). Mutasi dari gen p53 menyebabkan proliferasi dan transformasi sel menjadi kehilangan kendali (Sofyan, 2000).
2. Sel kanker tidak mengenal komunikasi ekstraseluler atau asosial. Komunikasi ekstraseluler diperlukan untuk menjalin koordinasi antar sel sehingga mereka dapat saling menunjang fungsi masing-masing. Dengan sifatnya yang asosial, sel kanker bertindak semaunya sendiri tanpa peduli apa yang dibutuhkan oleh lingkungannya. Sel kanker dapat memproduksi growth factor sendiri sehingga tidak bergantung pada rangsangan sinyal pertumbuhan dari luar untuk melakukan proliferasi. Dengan demikian sel kanker dapat tumbuh menjadi tak terkendali (Hanahan and Weinberg, 2000).
3. Sel kanker mampu menyerang jaringan lain (invasif), merusak jaringan tersebut dan tumbuh subur di atas jaringan lain membentuk anak sebar (metastasis). Semakin besar jangkauan metastasis tumor, kanker semakin sulit disembuhkan. Kanker pada stadium metastasis inilah yang merupakan penyebab 90% kematian penderita kanker (Hanahan dan Weinberg, 2000).
4. Untuk mencukupi kebutuhan pangan dirinya sendiri, sel kanker mampu membentuk pembuluh darah baru (neoangiogenesis) yang
dapat mengganggu kestabilan jaringan tempat ia tumbuh (Hanahan dan Weinberg, 2000).
5. Sel kanker memiliki kemampuan yang tak terbatas dalam memperbanyak dirinya sendiri (proliferasi), meski seharusnya ia sudah tak dibutuhkan dan jumlahnya sudah melebihi kebutuhan yang seharusnya. Dengan kemampuan untuk memenuhi kebutuhan sinyal pertumbuhan dan kemampuan menghindar dari mekanisme apoptosis, sel kanker memiliki kemampuan tak terbatas untuk bereplikasi (Hanahan dan Weinberg, 2000).
2.1.3. Leukemia (Kanker Darah)
Leukemia adalah keganasan yang ditandai dengan proliferasi sel imatur (sel leukemik) di sumsum tulang, darah tepi dengan infiltrasi organ hati, limpa, dan kelenjar limfe. Proliferasi sel imatur mengakibatkan penumpukan sel leukemik di dalam sumsum tulang dengan akibat fungsi hematopoesis dan trombopoesis tertekan. Proliferasi sel imatur biasanya disertai dengan penurunan apoptosis (Riawan, 2012).
Klasifikasi leukemia berdasarkan lama waktu terjadinya penyakit, terdiri atas leukemia akut, yaitu leukemia yang terjadi dengan waktu yang singkat (dalam hitungan hari sampai bulan), dan leukemia kronik dengan waktu yang lama (dalam hitungan bulan sampai tahun). Klasifikasi leukemia berdasarkan jenis sel darah putih matang terbanyak yaitu: leukemia granulositik (mielositik) dan leukemia limfositik (Anies. 2009).
Menurut Jan Tambayong 2000 faktor penyebab leukemia dapat dibagi menjadi tiga kelompok yaitu:
1. Faktor genetik terlihat pada kembar identik yang akan beresiko tinggi bila kembaran yang lain mengalami leukemia. Saudara sekandung dari individu yang leukemia dan individu dengan sindrom Down juga beresiko terhadap terjadinya leukemia.
2. Penyakit yang didapat dengan resiko terkena leukemia mencakup mielofibrosis, polisitemia vera, dan anemia refraktori sideroblastik, myeloma multiple dan penyakit Hodgkin.
3. Agen kimia dan fisik yang merupakan risiko signifikan terhadap leukemia mencakup radiasi dan pemajanan jangka lama terhadap benzene. Agen kemoterapi kloramfenikol dan agen pengkelat juga berisiko.
Manifestasi klinis paling fatal adalah infeksi adalah infeksi, yang ditandai dengan demam, menggigil, radang, dan lemah. Sering timbul perdarahan (kulit, gingiva atau visera) karena trombositopenia. Nafsu makan berkurang, berat badan menurun, keletihan, dan pucat (anemia). Karena meninges terkena, maka timbul sakit kepala, gangguan penglihatan, mual, dan muntah. Terdapat hepatosplenomegali, nyeri tekan pada abdomen, anoreksia. Limfadenopati (Tambayong, 2000).
Dibandingkan dengan penyakit kanker lain seperti kanker paru dan kanker payudara, leukemia (kanker darah) termasuk kanker yang jarang terjadi. Meskipun demikian, leukemia merupakan jenis kanker yang paling banyak ditemukan pada anak dibawah 15 tahun. Dari seluruh kejadian kanker terdapat 32% yang terjadi pada usia dibawah 15 tahun. Sekitar 74% dari kelompok umur yang sama adalah kanker darah atau leukemia (Belson dkk., 2007).
Murine Leukimia P388 merupakan salah satu sel jenis sel kanker leukemia yang sering digunakan dalam uji sitotoksisitas untuk mengetahui aktivitas suatu senyawa dalam menghambat pertumbuhan sel kanker. Sel kanker ini dikembang biakkan dari sel tikus yang dikenai agen leukemia (Marwati, 2012).
2.2. Asam Sinamat
Senyawa fenolik memiliki aktivitas biologis penting pada tumbuhan dan hewan seperti perannya pembawa electron pada fotosintesis dan dalam aktivitas enzim tertentu, menghambat dan mempercepat pertumbuhan, bersifat racun terhadap herbivore, sehingga dimanfaatkan sebagai herbisida dan lainnya. Selain dimanfaatkan sebagai antioksidan, senyawa fenolik bermanfaat sebagai antimikroba, antikanker dan lain-lain. Sinnamat dan turunannya merupakan salah satu senyawa fenolik yang
banyak dimanfaatkan pada industry kosmetik dan makanan serta bermanfaat dalam pengobatan kanker.
Asam sinnamat merupakan asam organic dengan bentuk Kristal yang berwarna putih dan sedikit larut dalam air, merupakan senyawa alam karena ditemukan dalam berbagai jenis tanaman, termasuk buah-buahan (Marwati, 2012).
Asam Sinamat sinamat dan turunannya merupakan senyawa aromatis yang terdapat di alam. Isolasi asam sinamat dan turunannya telah dilakukan dari propolis lebah, kayu manis, dan banyak tumbuhan, terutama rempah-rempah, seperti: jahe, kencur, lengkuas dan bahkan buah-buahan (Shirat dkk, 2011). Penelitian tentang asam sinamat dan turunannya sudah banyak dilakukan terutama untuk meningkatkan penggunaannya sebagai bahan baku obat dengan meningkatkan aktivitas biologisnya.
Asam sinamat dan turunannya memiliki aktivitas yang beragam diantaranya: anti inflamasi, anti hipertensi, anti mikroba, anti diabetik (Ramesh, 2012) serta antikanker. Turunan asam sinamat dari propolis lebah dilaporkan memiliki aktivitas anti tumor yang dapat membunuh sel tumor (Mishima dkk, 2005). Asam sinamat secara kimia memiliki tiga gugus fungsi yang berpotensi sebagai sisi aktif, yakni subtitusi pada cincin fenil, α,β unsaturated (ikatan rangkap), dan reaksi pada gugus karboksilat.
Salah satu turunan asam sinamat adalah etil para metoksisinamat (EPMS), EPMS merupakan minyak esensial terbesar yang dihasilkan dari rimpang kencur (Kaempferia galanga L) dan dilaporkan memiliki aktifitas Gambar 2.1 Struktur Asam Sinnamat dibuat menggunakan Marvin Sketch
sitotoksik pada Artemia salina dengan uji brine shrimp lethality test (Tewtrakul, 2005; Ekowati 2010). Liu dkk., 2010. Juga mengatakan bahwa EPMS menghambat proliferasi kanker human hepatocellular liver (HEP G2) dengan dosis yang belum diketahui. EPMS juga dapat menghambat kanker gastric dengan menghambat angiogenesis sehingga pembelahan sel kanker gastric terhambat (Liu dan Wei, 2005: Subchan, Bilal , 2011) 2.3. Hubungan Kuantitatif Struktur Aktivitas (HKSA)
Hubungan kuantititif struktur aktivitas (HKSA) merupakan hasil akhir dari suatu proses yang dimuai dengan mendeskripsikan suatu struktur molekul dan diakhiri dengan kesimpulan, hipotesis, dan prediksi dari sifat fisiko kimia dan biologis molekul tersebut. Hubungan kuantitatif struktur aktivitas (HKSA) didasarkan pada asumsi bahwa struktur suatu molekul (secara geometri, elektronik, sterik) bertanggung jawab terhadap terhadap sifat fisika, kimia, dan respon biologisnya yang digambarkan dalam beberapa deskriptor. Dengan menggunakan model HKSA aktivitas suatu bahan kimia yang memiliki kemiripan dan merupakan senyawa baru yang akan dirancang dan belum diuji dapat diketahui aktivitasnya (Todeschini, 2009).
Menurut Jean Piere dan Annick Panaye hipotesis yang mendasari dilakukannya pengujian HKSA yaitu karena setiap molekul memiliki fitur-fitur (geometric dan elektronik) yang berpengaruh terhadap sifat fisiko kimia dan efek biologis molekul tersebut. Dengan demikian diasumsikan dari suatu rangkaian molekul yang memiliki efek biologis yang sama serta cara kerja yang sama maka kerja dari molekul tersebut dapat diwakili oleh deskriptor dari molekul tersebut.
Tujuan akhir dari HKSA adalah membuat persamaan model HKSA yang menggambarkan sifat dari serangkaian senyawa. Untuk mendapatan model tersebut diperlukan pemilihan data set dari beberapa molekul. Pada zaman dahulu HKSA hanya dikembangkan pada senyawa konginerik akan tetapi seiring perkembangan zaman HKSA mulai digunakan untuk berbagai jenis senyawa untuk mempercepat pengetahuan tentang suatu molekul baru. Hasil dari peramalan suatu model sangat bergantung pada
tersedianya data penelitian yang telah dilakukan. Data eksperimen suatu senyawa bisa didapatkan dengan cara melakukan eksperimen dan dengan mencari dari literature (Todeschini, 2009).
Dalam pengumpulan data ini perlu berhati-hati karena model dari HKSA memiliki keterbatasan akurasi pada eksperimen dengan kualitas yang sangat tinggi. Untuk menghindari ketidak akuratan model HKSA jika data set diperoleh dari literature maka sebaiknya data diambil hanya dari satu literature saja atau dari beberapa sumber yang hamper sama proses dan perlakuannya saat eksperimen (Todeschini, 2009).
Tahapan lain dalam penentuan model HKSA adalah penentuan deskriptor yang tepat, akan tetapi pada kebanyakan kasus tidak ada yang menyatakan deskriptor manakah yang terbaik untuk digunakan. Sehingga pada beberapa peneliti cenderung untuk menggunakan deskriptor dengan jumlah yang banyak. Model HKSA dinyatakan dalam persamaan regresi yang dinyatakan sebagai berikut:
P= f (x1, x2, x3, ……, xp) P = aktivitas suatu molekul
f = fungsi yang mewakili hubungan antara respond an deskriptor
x1, x2, ……, xp = molecular deskriptor
Ordinary Least Square regression (OLS), atau biasa disebut Multiple Linear Regression (MLR) merupakan tekhnik regresi yang paling banyak digunakan dalam memperkirakan hubungan kuantitatif struktur aktivitas (HKSA) antara molecular deskriptor dan aktivitas suatu molekul. Regresi Partial Least Squares (PLS) merupakan persamaan yang biasa digunakan terutama ketika molecular deskriptor untuk pengujian suatu senyawa digunakan dalam jumlah yang banyak (Todeschini 2009).
Tahapan paling penting dalam pengembangan HKSA adalah validasi model. Terdapat beberapa teknik validasi untuk mengevaluasi kemampuan memprediksi suatu model. Validasi merupakan persyaratan paling penting untuk diterimanya suatu model HKSA. Kemampuan memprediksi suatu model dihitung berdasarkan dua data, yaitu: training
set (data yang menghasilkan suatu model), dan test set (data yang digunakan untuk mengevaluasi kemampuan suatu model untuk mempresiksi) (Todeschini, 2009).
Ketika suatu model telah divalidasi dan memberikan hasil yang baik, maka model tersebut dapat digunakan untuk memperkirakan sifat dari molekul baru, mekanisme kerja suatu turunan senyawa, dan struktur mana dari suatu molekul yang memberikan aktivitas biologis dari suatu molekul. Pada mulanya perhatian hanya untuk mendapatkan model dengan kemampuan memprediksi yang baik tanpa memperhatikan kemampuan model tersebut untuk diinterpretasikan. Tentu saja model seperti ini digunakan ketika tujuan penelitian untuk mendapatkan data kimia suatu molekul, hal yang paling penting adalah model yang didapatkan harus dapat dipercaya, dan tidak memperhatikan mengapa suatu deskriptor dipilih dalam untuk membuat suatu model (Todeschini,2009).
Akan tetapi walaupun kemampuan mempresiksi model yang tinggi untuk memprediksi suatu molekul harus berhati-hati karena jika molekul memiliki chemical space yang jauh dari model maka hasil ekstrapolasi yang didapatkan merupakan prediksi yang tidak dapat dipercaya. Untuk mengatasi masalah ini maka dilakukan pengeluaran molekul yang tidak relevan (Todeschini, 2009).
Sehingga dapat disimpulkan bahwa dalam pengembangan model HKSA memerlukan 3 hal penting yaitu:
1. Penyiapan sekumpulan data set yang telah diketahui aktifitas biologisnya dengan struktur kimia dan aktivitas yang mirip.
2. Pemilihan molecular deskriptor yang paling tepat yang mampu menggambarkan informasi tentang struktur yang akan diteliti. 3. Metode matematika untuk menentukan hubungan antara aktivitas
suatu molekul dengan strukturnya. 2.4. Metode Hansch
Hansch (1963), mengemukakan suatu konsep bahwa hubungan struktur kimia dengan aktifitas biologis (log 1/C )suatu turunan senyawa dapat dinyatakan secara kuantitatif melalui parameter-parameter sifat
fisika kimia dari subsituen yaitu parameter hidrofobik (π), elektronik (σ), dan sterik (Es) yang terdapat pada molekul, yang dapat dinyatakan secara matematis sebagai persamaan berikut:
Log A = aΣπ + bΣ σ + cΣ Es + d
Model pendekatan ini disebut juga model energy bebas linier (linier free energy relationship = LFER) atau pendekatan ekstratermodinamik. (Siswandono, 2008)
2.4.1 Parameter Sifat Kimia Fisika dalam HKSA Model Hansch
Parameter sifat kimia fisika yang sering digunakan dalam HKSA model Hansch adalah parameter hidrofobik, elektronik dan sterik. Pada proses distribusi atau pengangkutan obat, penembusan membrane biologis sangat dipengaruhi oleh kelarutan obat dalam lemak/air, suasana pH dan derajat ionisasi (pKa) sehingga dalam hubungan kuantitatif struktur dan aktifitas, parameter kimia fisika yang sering dilibatkan adalah parameter hidrofobik dan elektronik. Pada proses distribusi obat pengaruh sifat hidrofobik pada umumnya lebih besar dibanding sifat elektronik.
1. Parameter hidofobik
Parameter hidrofobik (lipofilik) yang sering digunakan dalam HKSA antara lain adalah logaritma koefisien partisi (log P), logaritma koefisien distribusi (log D), tetapan π Hansch, tetapan fragmentasi f Rekker-Manhold dan tetapan kromatogram Rm.
a. Log P (koefisien partisi)
Koefisien partisi oktanol/air yang dinyatakan dalam log P merupakan standar kuantitas untuk menentukan sifat hidrofobik/hidrofilik suatu molekul. Parameter hidrofobik/hidrofilik adalah sifat yang sangat penting dalam aplikasi biomedis. Sebagai contoh aplikasinya adalah untuk memperkirakan distribusi obat dalam tubuh. Obat-obat yang bersifat hidrofobik dengan koefisien partisi tinggi akan terdistribusi pada kompartemen yang bersifat hidrofobik pula, misalnya lapisan lemak, sedangkan obat-obat yang bersifat hidrofilik dengan koefisien partisi rendah akan terdistribusi pada kompartemen hidrofilik, misalnya serum darah (Fitri, 2008)
Nilai log P dalam oktanol/air merupakan rasio logaritma konsentrasi zat terlarut dalam oktanol dengan konsentrasi zat terlarut dalam air. Secara matematis dituliskan dalam persamaan dibawah
b. Log D (koefisien distribusi)
Dalam ilmu fisika koefisien partisi (P) dan koefisien distribusi (D) adalah perbandingan konsentrasi suatu senyawa dalam dua fase yang tidak dapat saling bersatu dalam kesetimbangan. Koefisien disini tidak sama dengan kelarutan suatu senyawa dalam dua fase tersebut (Leo, dkk. 1971). Biasanya salah satu fasenya merupakan air dan fase yang lainnya bersifat hidrofobik yaitu oktanol (Sangster, 1997).
Koefisien distribusi adalah rasio seluruh bentuk konsentrasi suatu senyawa (terion dan tak terion) pada dua fase (oktanol dan air). Untuk menghitung koefisien distribusi suatu senyawa fase air dari pelarut diberikan buffer agar dapat ditentukan nilai koefisien distribusi suatu senyawa pada pH tertentu. Logaritma dari koefisien distribusi disebut juga dengan Log D
2. Parameter elektronik
Ada tiga jenis sifat elektronik yang digunakan dalam HKSA model Hansch, yaitu:
1. Pengaruh berbagai substituent terhadap reaktifitas bagian molekul yang tidak mengalami perubahan.
2. Sifat elektronik yang berkaitan dengan tetapan ionisasi (pKa) dan berhubungan dengan bentuk terionkan dan tak terionkan dari suatu senyawa pada pH tertentu.
3. Sifat oksidasi-reduksi atau reaktifitas senyawa.
sejak tahun 1990 sebagai percobaan untuk menggambarkan informasi struktur dari suatu molekul yang membantu menjelaskan interaksi polar intermolekul. Perhitungan CPSA mempertimbangkan muatan dari setiap atom dan juga interaksi tiap atom pada pelarut. Konsep dari perhitungan ini adalah bahwa interaksi polar terjadi karena adanya perbedaan muatan antar molekul, dan interaksi ini akan dipengaruhi oleh atom-atom lain yang berikatan dengan molekul tersebut. Apabila suatu set deskriptor mampu menjelaskan jenis interaksi dari suatu molekul maka akurasi dari prediksi suatu model HKSA dapat meningkat. 25 deskriptor telah di perkenalkan dan menjelaskan muatan dan permukaan pada suatu molekul dengan berbagai cara (Staton, dkk. 2002).
Semenjak diperkenalkan CPSA telah banyak dipergunakan dalam berbagai pemodelan HKSA dalam berbagai aktivitas biologi. Kemampuan dari deskriptor inilah yang membuatnya menjadi sangat menarik. Ketika deskriptor lain hanya mampu mengambarkan interaksi polar CPSA juga mampu menggambarkan interaksi hidrofobik yang penting dengan baik pada suatu molekul (Staton, dkk. 2002).
a. PPSA
Merupakan total dari seluruh muatan positif pada permukaan atom yang berinteraksi dengan pelarut
b. PNSA
Merupakan total dari seluruh muatan negative pada permukaan atom yang berinteraksi dengan pelarut
3. Parameter sterik
Tetapan sterik substituent dapat diukur berdasarkan sifat meruah gugus-gugus dan efek gugus pada kontak obat dengan sisi reseptor yang berdekatan. (Siswandono, 2008). Parameter strerik yang digunakan pada penelitian ini adalah indeks topologi
Pada hampir setiap kasus, para kimiawan lebih memilih untuk menggunakan indeks topologi sebagai deskriptor molekular untuk melakukan evaluasi terhadap toksisitas dan untuk memprediksi aktivitas biologi. Hal ini karena indeks topologi menawarkan cara yang mudah dalam pengukuran cabang molekul, bentuk, ukuran, siklisitas, simetri, sentrisitas, dan kompleksitas (Devillers, 1997)
Indeks topologi menjelaskan bahwa suatu struktur kimia, disebut sebagai grafik kimia, yaitu suatu model kimia yang digunakan untuk menjelaskan sifat interaksi antara obyek-obyek kimia (atom, ikatan, gugusan atom, molekul, pasangan molekul, dan sebagainya) (Fitri, 2008).
Suatu grafik G = G(V,E), oleh Ivanciuc dan Balaban (1998) dijelaskan sebagai pasangan terurut yang terdiri dari dua buah himpunan V = V(G) dan E = E(G). Unsur-unsur pada himpunan V(G) disebut vertices (puncak) dan unsur-unsur pada himpunan E(G), termasuk hubungan biner antara puncak-puncak disebut edges (tepi). Jumlah puncak N menggambarkan jumlah unsur-unsur pada V(G), N = |V(G)| dan jumlah tepi M menggambarkan jumlah unsur-unsur pada E(G), M = |E(G)|. Puncak-puncak suatu grafik diberi nama dari 1 sampai N, E(G) = (ν1, ν2, ..., νN), dan tepi yang menghubungkan puncak-puncak νi dan νj disebut eij. Dua buah puncak νi dan νj pada grafik G disebut berdekatan atau berbatasan bila terdapat tepi eij yang menyertainya.
a. Indeks Harary
Indeks Harary yang dinyatakan dengan H diturunkan dari hubungan timbal balik (resiprokal) matriks jarak dan memiliki sejumlah sifat-sifat yang menarik. Indeks ini berdasarkan pada dugaan para kimiawan bahwa situs-situs yang terletak berjauhan dalam suatu struktur seharusnya memiliki pengaruh yang lebih kecil antara satu dengan lainnya daripada situs-situs yang letaknya berdekatan.
Indeks Harary H = H(G) pada grafik molekular G dengan puncak N didefinisikan sebagai setengah dari jumlah diagonal unsur-unsur pada matriks jarak resiprokal Dr = Dr(G) yang dituliskan pada persamaan dibawah
Matriks jarak resiprokal Dr diperoleh dengan mengganti semua diagonal unsur-unsur [D
ij] menjadi bentuk kebalikannya ditunjukkan pada persamaan dibawah
sehingga untuk diagonal (D
r
)
ii bernilai nol (Lucic dkk., 2002) b. Indeks Randic
Indeks Randic atau indeks konektivitas molekular Randic sangat mirip dengan indeks Zagreb, namun lebih dapat diterima dan digunakan secara luas. Secara matematis dituliskan pada persamaan dibawah
Sesuai dengan definisi yang diberikan, maka semakin rapat grafik, maka akan semakin rendah harga χ (Ivanciuc dan Balaban, 1998)
c. Indeks Wiener
Indeks Wiener atau Wiener number adalah indeks topologi suatu molekul yang dihitung berdasarkan total jarak terpendek dari suatu molekul yang mewakili atom selain hydrogen (Rouvray, 2002). Indeks Wiener merupakan indeks topologi tertua yang digunakan dalam memperhitungan percabangan suatu molekul (Todeschini, 2009). Berdasarkan kesuksesan dari indeks Wiener ini dalam grafik kimia maka dikembangkanlah indek- indeks topologi baru (Rouvray, 2002).
2.5.Deskriptor
Molekuler deskriptor adalah hasil dari logika dan matematika yang mengubah informasi yang dikodekan dalam suatu molekul kemudian direpresentasikan kedalam angka-angka yang berguna bagi penelitian berikutnya, baik sebagai pengetahuan tentang molekul tersebut maupun
sebagai model untuk mempresiksi molekul lain. Molekuler deskriptor diumpamakan sebagai naga dalam mitologi Babylon Istar yang sebenarnya merupakan pencampuran beberapa hewan, masing-masing memiliki peran sebagai bagian dari tubuh naga. Demikian halnya dengan molekuler deskriptor memiliki beberapa arti yang berbeda tergantung pada titik pandangnya (Todeschini, 2009).
2.6.Marvin Sketch
Marvin Sketch adalah sebuah aplikasi kimia untuk menggambar struktur kimia, dan reaksi kimia serta menyimpannya dalam berbagai format (MRV, CDX, SKC, SDF, RDF (V2000/V3000), RXN, MOL, MOL2, SMILES, SMARTS, InChi, CML, FASTA, dll.). Marvin Sketch mampu mengoreksi struktur kimia yang digambar baik secara 3D maupun 2D. Marvin Sketch merupakan aplikasi buatan ChemAxon dan dikembangkan dengan java sehingga memerlukan Java Runtime Environment (JRE) untuk berjalan. (ChemAxon 2015)
2.7. SPSS (Statistikal Package and Service Solution)
SPSS merupakan software statistik yang pertama kali dibuat pada tahun 1968 oleh tiga mahasiswa Stanford University, yakni Norman H. Nie, C. Hadlai Hull, dan Dale H. Bent. Saat itu software dioperasikan pada computer mainframe. Setelah penerbit terkenal menerbitkan user manual SPSS, program tersebut menjadi popular. Pada tahun 1984 SPSS pertama kali muncul dengan versi PC (bisa dipakai untuk komputer desktop)
Gambar 2.2 Naga dalam mitologi Babylon Istar diambil dari Molecular Deskriptors for Chemoinformatics
dengan nama SPSS/PC+, dan sejalan dengan mulai populernya sistem operasi Windows, pada tahun 1992 SPSS mengeluarkan versi Windows. Pada mulanya SPSS ditujukan untuk penggunaan pengolahan data statistik untuk ilmu social (SPSS adalah singkatan dari Statistikal Package for the Social Science) namun seiring berkembangnya kerjasama dengan berbagai software house maka kini SPSS memperluas pelayanannya untuk berbagai jenis pengguna, seperti untuk proses produksi di pabrik, riset ilmu-ilmu sains dan lainnya. Kini kepanjangan dari SPSS adalah Statistikal Product and Service Solutions (Santoso, 2008)
2.8. Ligand Scout
Ligand Scout adalah perangkat lunak yang memungkinkan penggunanya untuk melakukan pemodelan farmakofor secara 3D dari kompleks ligand dan protein, atau dari training set dan test set dari senyawa organic. Ligand Scout mampu menjelaskan fitur-fitur pada struktur kimia 3D (seperti pendonor dan aseptor ikatan hidrogen, daerah yang bersifat lipofil, serta grup yang memiliki sifat positif dan negative) yang menggambarkan interaksi ligand dan situs tambat disekelilingnya (makromolekul) (Wolber 2005). Ligand Scout juga mampu mensejajarkan farmakofor dari ligan tersebut pada senyawa yang memiliki gugus kromofor yang mirip (Wolber 2005). Pada tiap senyawa yang disejajarkan dapat disisipkan gugus kromofor tambahan yang mampu memberi andil pada interaksi antara ligand dan protein (makromolekul). Software ini telah sukses digunakan dalam memprediksi senyawa penuntun dalam desain obat contohnya ialah prediksi aktivitas biologi senyawa baru terhadap inhibitor HIV reverse transcriptase. (Barecca 2007).
2.9.Open Babel
Open Babel adalah perangkat lunak untuk mengubah beberapa format berkas kimia. Selain itu, perangkat ini menyediakan berbagai fungsi berguna yaitu pencarian konformer dan penggambaran 2D, penapisan, konversi batch, dan pencarian substruktur dan kemiripan. Open Babel mendukung 111 format berkas kimia, yang dapat membaca 82
format dan menulis 85 format. Perangkat ini tersedia secara gratis dari http://openbabel.org (O’Boyle, dkk., 2011).
2.10. CDK Deskriptor
CDK adalah perpustakaan Java yang mendukung berbagai informasi kimia mulai dari membaca berbagai macam format file molekul hingga pembacaan molecular deskriptor. CDK mampu menghitung molecular deskriptor secara topologi, geometri, Charge, dan secara konstitusional. Keunggulan dari CDK adalah mampu secara otomatis mengklasifikasikan deskriptor, pengguna dapat memilih deskriptor mana yang akan digunakan, output dari aplikasi ini dapat berupa .xls sehingga memudahkan dalam pengolahan data (Guha, 2014)
2.11. PubChem
PubChem (http://PubChem.ncbi.nlm.nih.gov) adalah gudang informasi molekuler untuk umum, sebuah karya ilmiah dari Institut Kesehatan Nasional Amerika (US National Institutes of Health / NIH). Basis data PubChem memiliki lebih dari 27 juta catatan struktur kimia khusus dari senyawa yang berasal dari hampir 70 juta senyawa endapan, dan berisi lebih dari 449.000 catatan bioassay dengan lebih dari ribuan biokimia in vitro dan skrining berbasis sel, dengan menargetkan lebih dari 7000 protein dan gen yang terhubung dengan lebih dari 1,8 juta senyawa (Xie, 2010). Pada situs PubChem ini dapat diunduh struktur kimia dari suatu senyawa yang telah dilakukan pengujian bioassay secara gratis.
BAB III
METODOLOGI PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian dilaksanakan di Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri Syarif Hidayatullah dan di Lembaga Ilmu Pengetahuan Indonesia (LIPI) Serpong selama bulan Mei hingga Juli 2015
3.2 Alat
3.2.1 Perangkat Keras
Notebook Samsung (300E4C) dengan spesifikasi Intel ® Celeron ® CPU B820 @1,7 GHz, RAM (Random Access Memory) 4 gigabyte, dan Graphic Card (NVIDIA Optimus Ge Force 610M).
3.2.2 Perangkat Lunak
Windows 7 Ultimate 32 bit, Marvin sketch, CDK Deskriptor Calculator 1.3.4, Marvin Sketch, SPSS 16, Open Babel GUI 2.3.2, Sigma Plot 12.0, Microsoft Office Excel 2010, Java ™, Protein Data Bank (www.pdb.org), PubChem (http://PubChem.ncbi.nlm.nih.gov), Ligand
Scout 3.1.2 trial. www.libgen.org. PubMed
(http://www.ncbi.nlm.nih.gov/pubmed)
3.3 Bahan
Senyawa-senyawa turunan asam sinamat dalam format 3D (.mol) (Terlampir)
3.4 Prosedur Kerja
3.4.1 Pengumpulan Data
Dilakukan dengan mencari senyawa-senyawa turunan asam sinamat yang telah diujikan secara invitro terhadap sel p388 dan sudah
diketahui IC50 dari senyawa tersebut. Pencarian dilakukan melalui PubChem Bioassay (http://PubChem.ncbi.nlm.nih.gov)
3.4.2 Pemilihan Deskriptor dan Perhitungan Deskriptor
Deskriptor yang dipilih adalah CPSA (PPSA1 dan PNSA1) untuk parameter elektronik, dan log D dan log P untuk mewakili parameter hidrofobik, serta indeks topologi (indeks Randic, indeks harari dan indeks Wiener) untuk parameter sterik.
Perhitungan deskriptor berupa CPSA, indeks Wiener dan log P dilakukan menggunakan aplikasi CDK deskriptor dan input yang digunakan adalah .mol serta outputnya berupa .xls. sedengkan untuk indeks Harary dan indeks Randic akan di hitung menggunakan marvin sketch kemudian nilai deskriptor yang telah didapat disatukan dalam Microsoft office excel.
3.4.4 Pembagian Data dan Penghilangan Outlier
Data yang telah didapatkan kemudian dibagi menjadi dua kelompok data yaitu training set, dan test set. Training set yang digunakan sebanyak 23 Senyawa dan test set yang digunakan sebanyak 8 Senyawa.
Penghilangan outlier dilakukan dengan menggunakan Ligand Scout trial dengan membandingkan gugus kromofor yang terdapat pada senyawa-senyawa yang didapatkan. Dari data yang didapat hanya 31 yang digunakan sebagai model persamaan HKSA karena terdapat beberapa senyawa outlier
3.4.6 Pembuatan Model Persamaan Hubungan Kuantitatif Struktur Aktivitas Model persamaan dibuat menggunakan SPSS 16 dengan varieabel dependent adalah Log 1/IC50 (aktivitas) dan variable independent berupa log D, log P, PPSA1, PNSA1, indeks Harary, indeks randiks, dan indeks Wiener.
3.4.7 Validasi Model HKSA
Validasi dilakukan dengan beberapa parameter statistik yaitu koefisien korelasi (r), koefisien determinasi (r2), Adjusted r2, standard of error (SE), Fhitung/Ftabel, prediction residual error sum of square (PRESS), dan root mean square deviation (RMSD). Untuk menentukan nilai PRESS (Prediction Error Sum Of Square) dilakukan dengan mengurangi hasil Log 1/IC50 dari persamaan dengan Log 1/IC50 dari penelitian yang telah dikakukan kemudian menjumlah seluruh simpangannya, dan RMSD (Root Mean Square Deviation) dengan mengurangi hasil Log 1/IC50 dari persamaan dengan Log 1/IC50 dari penelitian yang telah dikakukan, kemudian merata-ratakan (menjumlah seluruhnya dan membagi pada jumlah test set yang digunakan) kemudian dilakukan pengakar kuadratan terhadap rata-rata yang telah didapatkan.
3.4.6 Pengujian Aktivitas senyawa turunan asam sinamat lain
Senyawa turunan asam sinamat digambar menggunakan Marvin Sketch kemudian disimpan dalam format .mol dan dihitung deskriptornya. Untuk deskriptor indeks Harary dan indeks Randic serta log D dihitung menggunakan Marvin Sketch sedangkan CPSA, indeks Wiener, dan log P dihitung menggunakan CDK deskriptor. Kemudian deskriptor yang didapatkan dimasukkan ke dalam model persamaan yang telah didapatkan.
BAB 4
HASIL DAN PEMBAHASAN 4.1. Pengumpulan Data Set
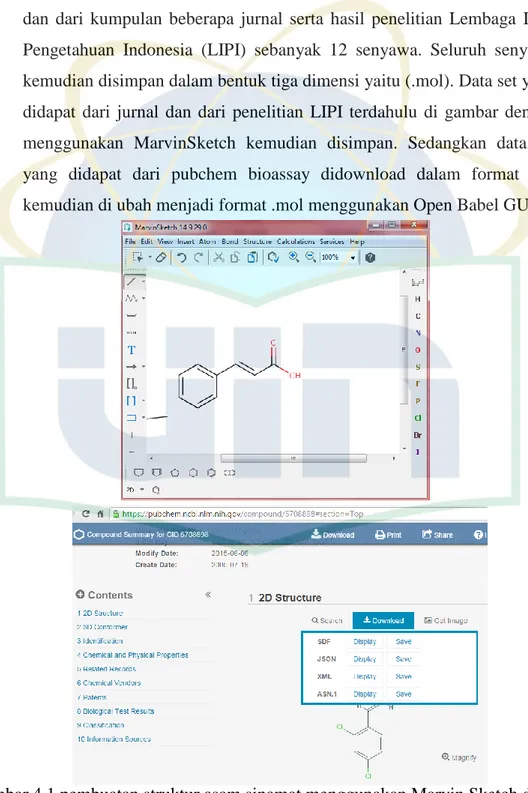
Data set senyawa turunan asam sinamat dikumpulkan dari 2 sumber yang berbeda yaitu: dari pubchem bioassay sebanyak 22 senyawa dan dari kumpulan beberapa jurnal serta hasil penelitian Lembaga Ilmu Pengetahuan Indonesia (LIPI) sebanyak 12 senyawa. Seluruh senyawa kemudian disimpan dalam bentuk tiga dimensi yaitu (.mol). Data set yang didapat dari jurnal dan dari penelitian LIPI terdahulu di gambar dengan menggunakan MarvinSketch kemudian disimpan. Sedangkan data set yang didapat dari pubchem bioassay didownload dalam format .sdf kemudian di ubah menjadi format .mol menggunakan Open Babel GUI.
Gambar 4.1 pembuatan struktur asam sinamat menggunakan Marvin Sketch dan download data set dari pubchem bioassay
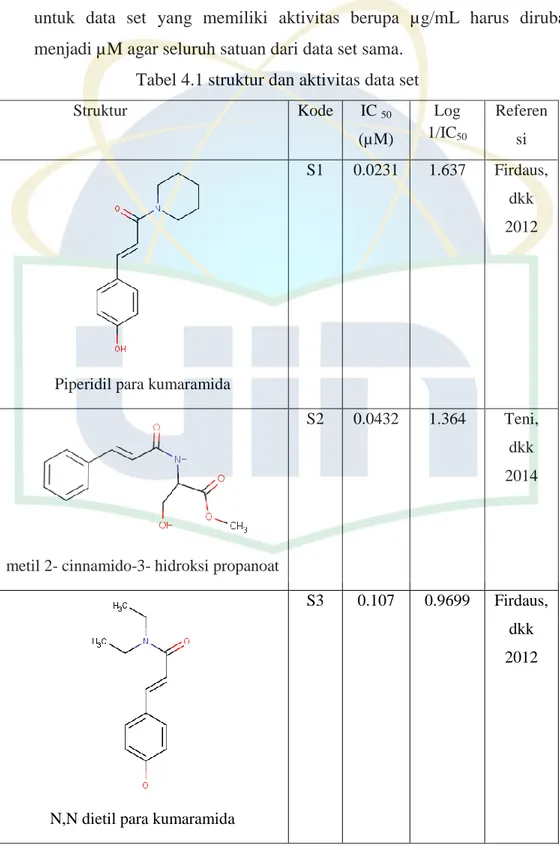
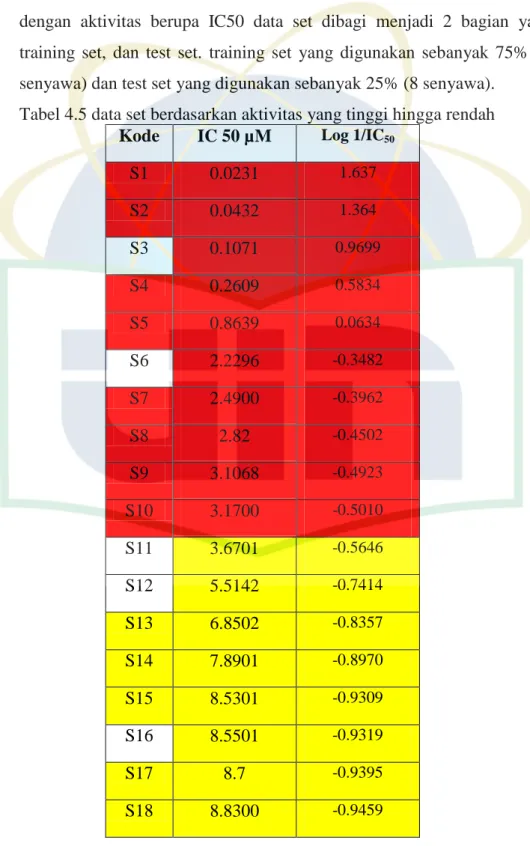
Dasar dari pemilihan data set ialah senyawa-senyawa turunan asam sinamat yang digunakan harus memiliki kesamaan baik metode pada pengujian in vitronya yaitu terhadap sel p388, begitu juga dengan kontrol positifnya. Selain itu data set yang digunakan harus memiliki nilai aktivitas berupa IC50 baik dalam satuan µM maupun dalam satuan µg/mL. untuk data set yang memiliki aktivitas berupa µg/mL harus dirubah menjadi µM agar seluruh satuan dari data set sama.
Tabel 4.1 struktur dan aktivitas data set
Struktur Kode IC 50 (µM) Log 1/IC50 Referen si
Piperidil para kumaramida
S1 0.0231 1.637 Firdaus, dkk 2012
metil 2- cinnamido-3- hidroksi propanoat
S2 0.0432 1.364 Teni, dkk 2014
N,N dietil para kumaramida
S3 0.107 0.9699 Firdaus, dkk 2012
N propil para kumaramida S4 0.2609 0.5834 Firdaus, dkk 2012 (E)-3-(2,5-difluorophenyl)-1-(4 hydroxyphenyl)prop-2-en-1-one S5 0.8639 0.0634 Dimmo ck, dkk 1998
phenyl (2E)‐3‐phenylprop‐2‐enoate
(2E)‐1‐(4‐hydroxyphenyl)‐3‐[4‐ (trifluoromethyl)phenyl]prop‐2‐en‐1‐one S7 2.490 -0.3962 Dimmo ck, dkk 1998 E)-3-(3-chlorophenyl)-1-(4-hydroxyphenyl)prop-2-en-1-one S8 2.82 -0.4502 Dimmo ck, dkk 1998 (E)-1-(4-hydroxyphenyl)-3-phenylprop 2 en-1-one S9 3.107 -0.4923 Dimmo ck, dkk 1998
(E)-3-(2,6-dichlorophenyl)-1-(4 hydroxyphenyl)prop-2-en-1-one S10 3.170 -0.5010 Dimmo ck, dkk 1998 (E)-3-(4-chlorophenyl)-1-(4-hydroxyphenyl)prop-2-en-1-one S11 3.6701 -0.5646 Dimmo ck, dkk 1998 (E)-3-(4-bromophenyl)-1-(4-hydroxyphenyl)prop-2-en-1-one S12 5.514 -0.7414 Dimmo ck, dkk 1998
(E)-3-(2-chlorophenyl)-1-(4-hydroxyphenyl)prop-2-en-1-one S13 6.8502 -0.8357 Dimmo ck, dkk 1998 (E)-3-(2,4-dichlorophenyl)-1-(4-hydroxyphenyl)prop-2-en-1-one S14 7.8901 -0.8970 Dimmo ck, dkk 1998 (E)-1-(3,4-dichlorophenyl)-3-(4-hydroxyphenyl)prop-2-en-1-one S15 8.5301 -0.9309 Dimmo ck, dkk 1998
(E)-3-(4-fluorophenyl)-1-(4-hydroxyphenyl)prop-2-en-1-one S16 8.55 -0.9319 Dimmo ck, dkk 1998 (E)-1-(4-hydroxyphenyl)-3-(4-methoxyphenyl)prop-2-en-1-one S17 8.7 -0.9395 Dimmo ck, dkk 1998 (2E,4E)-1-(4-hydroxyphenyl)-5-phenylpenta-2,4-dien-1-one S18 8.830 -0.9459 Dimmo ck, dkk 1998
(E)-1,3-diphenylprop-2-en-1-one S19 9.6302 -0.9836 Dimmo ck, dkk 1998 (E)-3-(3,4-dichlorophenyl)-1-(4-hydroxyphenyl)prop-2-en-1-one S20 11.700 -1.0681 Dimmo ck, dkk 1998 (E)-1-(4-bromophenyl)-3-(4-hydroxyphenyl)prop-2-en-1-one S21 12.9 -1.110 Dimmo ck, dkk 1998
(E)-1-(4-hydroxyphenyl)-3-(4-nitrophenyl)prop-2-en-1-one S22 13.140 1 -1.1185 Dimmo ck, dkk 1998 (E)-3-(4-hydroxyphenyl)-1-phenylprop-2-en-1-one S23 14.300 2 -1.1553 Dimmo ck, dkk 1998 (E)-3-(4-bromophenyl)-1-(4-hydroxyphenyl)prop-2-en-1-one S24 16.649 -1.2214 Dimmo ck, dkk 1998
methyl
(2E)‐3‐(4‐nitrophenyl)prop‐2‐enoate
S25 38.517 -1.5856 LIPI
Cinnamaldehid
S26 44.779 -1.6510 LIPI
2‐methylpropyl (2E)‐3‐phenylprop‐2‐enoate
Butil sinamat S28 96.494 -1.9845 LIPI Metil sinamat S29 125.47 7 -2.0985 LIPI methyl
(2E)‐3‐(2‐nitrophenyl)prop‐2‐enoate
S30 134.08 6 -2.1273 LIPI Asam sinamat S31 329.73 3 -2.5181 LIPI
4‐[(2E)‐3‐(4‐methoxyphenyl)prop‐2‐enoy l]phenyl (2E)‐3‐phenylprop‐2‐enoate
S32 10.207 -1.0088 Dimmo ck, dkk
1998
4‐[(2E)‐3‐(4‐chlorophenyl)prop‐2‐enoyl] phenyl (2E)‐3‐ phenylprop‐2‐enoate
S33 3.827 -0.5828 Dimmo ck, dkk
Catatan: Untuk mempermudah input data, nama senyawa selanjutnya akan digantikan oleh kode senyawa
4.2. Pemilihan Deskriptor
Penelitian ini menggunakan tiga buah deskriptor yang terdiri dari deskriptor hidrofobik, sterik, dan elektronik. Deskriptor hidrofobik berupa log P, dan log D, deskriptor sterik terdiri dari indeks Harary, indeks Randic, dan Indeks Wiener, serta deskriptor elektronik yaitu PPSA1 dan PNSA1 sehingga total deskriptor yang digunakan adalah 8 buah.
4.2.1. Deskriptor Hidrofobik 1. Log P
Tabel 4.2 Data aktivitas, log p dan log D dari 23 senyawa turunan asam sinamat
Kode Log 1/IC 50 Log D Log P
S1 1.636 2.32 -0.4698 S2 1.364 0.7 0.3395 S4 0.5834 2.12 0.1459 S5 0.0634 3.75 1.7694 S7 -0.3962 4.34 2.8523 S8 -0.4502 4.07 2.3185
4‐[(2E)‐3‐phenylprop‐2‐enoyl]phenyl (2E)‐3‐ phenylprop‐2‐enoate
S34 4.624 -0.6649 Dimmo ck, dkk
S9 -0.4923 3.46 1.9498 S10 -0.5010 4.67 2.6872 S13 -0.8357 4.07 2.3185 S14 -0.8970 4.67 2.6872 S15 -0.9309 4.79 2.6872 S17 -0.9395 3.3 1.4512 S18 -0.9459 3.99 2.4176 S19 -0.9836 3.89 2.5129 S20 -1.0681 4.67 2.6872 S22 -1.1185 3.4 2.1631 S23 -1.1553 3.58 1.9498 S24 -1.2214 4.23 2.4025 S25 -1.5856 2.46 1.7934 S27 -1.8633 3.76 2.0623 S28 -1.9845 3.84 0.9647 S29 -2.0985 2.52 1.5801 S31 -2.5181 -0.67 1.3291
Nilai log P dari 23 senyawa turunan asam sinamat berkisar antara -0,469 sampai dengan 2,825. Nilai log P berkaitan dengan distribusi obat dalam tubuh. Semakin positif nilai log P senyawa akan cenderung berada pada fase non polar daripada fase polar, sedangkan semakin negatif nilai log P senyawa akan cenderung berada pada fase polar daripada fase non polar, yang berarti senyawa tersebut hanya larut dalam cairan tubuh saja dan sulit untuk menembus membran biologis sehingga tidak dapat berikatan dengan reseptor.
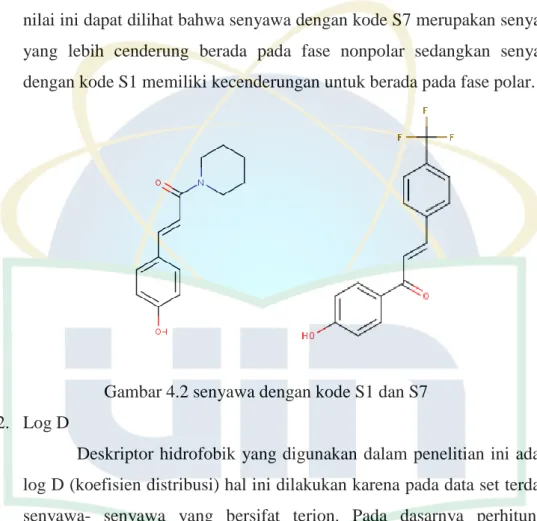
halogen yaitu fluor (F) yang bersifat nonpolar, selain itu pada senyawa ini terdapat gugus benzene yang juga bersifat nonpolar sehingga nilai dari log P senyawa ini lebih tinggi dibandingkan dengan senyawa lainnya. Senyawa dengan nilai log P paling kecil adalah senyawa dengan kode S1 (-0,469) kemungkinan hal ini terjadi karena adanya gugus amida. Dari nilai ini dapat dilihat bahwa senyawa dengan kode S7 merupakan senyawa yang lebih cenderung berada pada fase nonpolar sedangkan senyawa dengan kode S1 memiliki kecenderungan untuk berada pada fase polar.
Gambar 4.2 senyawa dengan kode S1 dan S7 2. Log D
Deskriptor hidrofobik yang digunakan dalam penelitian ini adalah log D (koefisien distribusi) hal ini dilakukan karena pada data set terdapat senyawa- senyawa yang bersifat terion. Pada dasarnya perhitungan koefisien partisi dibagi menjadi beberapa cara diantaranya adalah:
1. Berdasarkan atomik
Perhitungan berdasarkan atomic cukup baik dan banyak digunakan karena perhitungannya didasarkan pada elemen-elemen umum yang digunakan dalam pembuatan obat (oksigen, nitrogen, hydrogen, carbon, sulfur, dan halogen) (Cheng dkk. 2007)
2. Berdasarkan fragmen
Perhitungan berdasarkan fragmen mampu memberikan hasil prediksi yang lebih baik dibandingkan dengan berdasarkan atomic
akan tetapi tidak dapat digunakan untuk molekul dengan gugus fungsi yang tidak umum (Leo, 1995)
Dalam HKSA log P mampu memberikan hasil prediksi yang baik tetapi pada lingkungan yang terion dan senyawa-senyawa yang terion penggunaan logD (koefisien distribusi) akan lebih akurat.
4.2.2. Deskriptor Elektronik
Dalam penelitian ini deskriptor yang digunakan pada parameter elektronik adalah CPSA (Charge Partial Surface Area) dari 29 deskriptor CPSA yang mampu dihitung menggunakan CDK deskriptor kalkulator hanya PPSA1 dan PNSA1 saja yang digunakan dalam penelitian ini. Pemilihan deskriptor ini dilakukan karena kedua deskriptor tersebut telah terbukti memiliki korelasi yang baik berdasarkan penelitian yang telah dilakukan oleh Staton, dkk. 2002. CPSA juga mampu membedakan antara agonis dan antagonis pada senyawa yang berikatan dengan reseptor estrogen. Dalam hal interaksi nonkovalen CPSA juga mampu untuk menggantikan energy LUMO (Lowest Occupied Molecular Orbitals) untuk menggambarkan sifat elektrofilitas local dan global suatu senyawa. (Staton dkk. 2002)
Secara statistik PPSA1 dan PNSA1 memiliki korelasi yang kurang baik terhadap aktivitas antikanker sehingga, akan tetapi deskriptor ini memiliki kepekaan yang lebih baik dibandingkan dengan deskriptor indeks topologi hal ini terlihat pada senyawa dengan kode S20 dan S14 dengan struktur yang tersusun oleh atom-atom yang sama PPSA1 dan PNSA1 mampu memberikan hasil yang berbeda tidak seperti hasil yang didapat pada indeks topologi khususnya indeks Randic.
Gambar 4.3 Struktur senyawa dengan kode S14 dan S20
4.2.3. Deskriptor Sterik
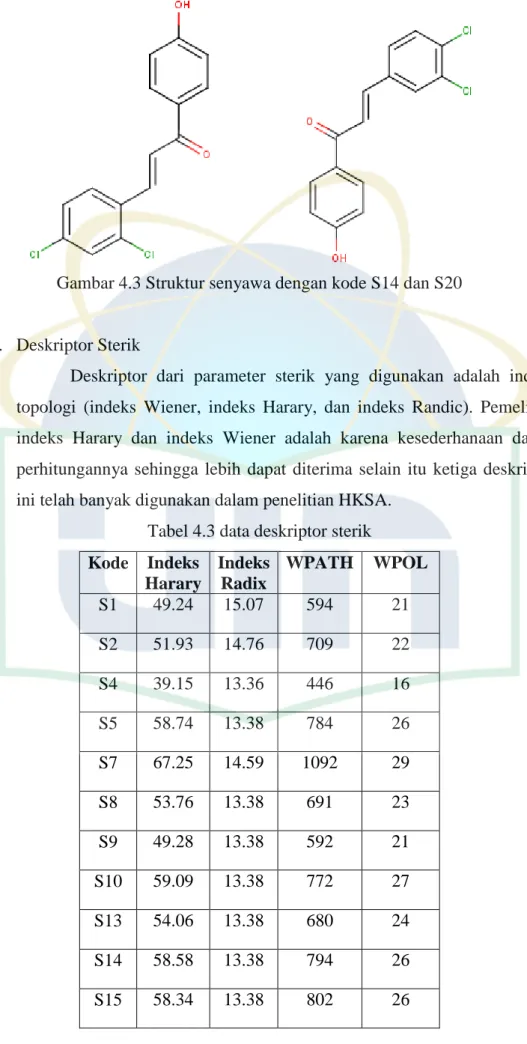
Deskriptor dari parameter sterik yang digunakan adalah indeks topologi (indeks Wiener, indeks Harary, dan indeks Randic). Pemelihan indeks Harary dan indeks Wiener adalah karena kesederhanaan dalam perhitungannya sehingga lebih dapat diterima selain itu ketiga deskriptor ini telah banyak digunakan dalam penelitian HKSA.
Tabel 4.3 data deskriptor sterik Kode Indeks Harary Indeks Radix WPATH WPOL S1 49.24 15.07 594 21 S2 51.93 14.76 709 22 S4 39.15 13.36 446 16 S5 58.74 13.38 784 26 S7 67.25 14.59 1092 29 S8 53.76 13.38 691 23 S9 49.28 13.38 592 21 S10 59.09 13.38 772 27 S13 54.06 13.38 680 24 S14 58.58 13.38 794 26 S15 58.34 13.38 802 26
S17 57.62 15.06 830 25 S18 56.34 15.2 874 23 S19 45.05 12.84 496 19 S20 58.37 13.38 804 26 S22 62.18 14.29 960 27 S23 49.24 13.38 594 21 S24 53.55 13.38 702 23 S25 40 10.79 428 18 S27 39.04 13.63 446 15 S28 38.57 13.63 458 15 S29 28.46 9.88 226 12 S31 25.1 8.73 174 10
Dari tabel 4.2 dapat terlihat bahwa senyawa yang memiliki struktur yang besar akan memberikan nilai indeks Harary, indeks Randic dan indeks Wiener yang besar pula hal ini terjadi karena molekul dengan keruahan yang besar akan memberikan nilai indeks topologi yang juga besar, selain itu perhitungan indeks topologi didasarkan pada perhitungan bahwa atom dipandang sebagai puncak (atom) dan sebagai tepian (ikatan). Berdasarkan hal tersebut maka dapat diasumsikan bahwa semakin banyak atom penyusun dari suatu molekul maka nilai dari indeks topologi molekul tersebut akan semakin besar juga.
Terdapat beberapa senyawa yang memiliki nilai indeks topologi yang sama, hal ini menunjukan bahwa deskriptor indeks topologi kurang peka terhadap adanya perubahan posisi ikatan dari suatu atom. Semakin banyak yang sama nilai dari deskriptor tersebut menunjukan bahwa deskriptor tersebut semakin kurang peka. Dilihat dari banyaknya kesamaan nilai deskriptor yang dihasilkan maka indeks randiks merupakan
indeks yang paling kurang peka dibandingkan dengan indeks topologi yang lain.
Tabel 4.4 korelasi setiap deskriptor terhadap aktivitas
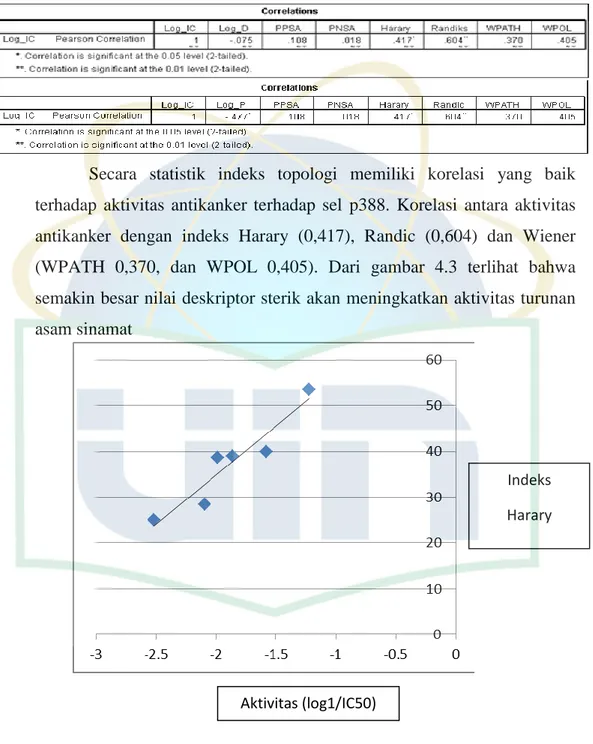
Secara statistik indeks topologi memiliki korelasi yang baik terhadap aktivitas antikanker terhadap sel p388. Korelasi antara aktivitas antikanker dengan indeks Harary (0,417), Randic (0,604) dan Wiener (WPATH 0,370, dan WPOL 0,405). Dari gambar 4.3 terlihat bahwa semakin besar nilai deskriptor sterik akan meningkatkan aktivitas turunan asam sinamat
Gambar 4.4 kurva hubungan indeks Harary terhadap kenaikan aktivitas turunan asam sinamat
Aktivitas (log1/IC50)
Indeks Harary
4.3. Penghilangan Outlier
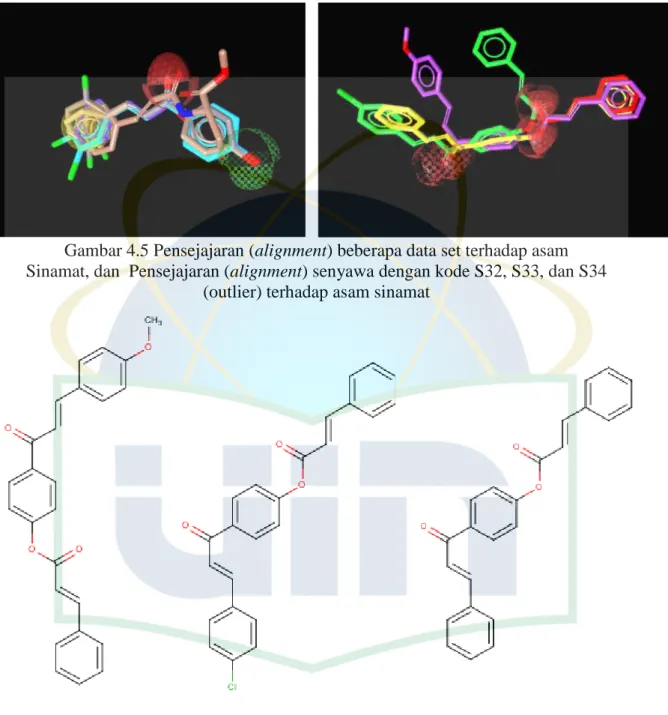
Gambar 4.5 Pensejajaran (alignment) beberapa data set terhadap asam Sinamat, dan Pensejajaran (alignment) senyawa dengan kode S32, S33, dan S34
(outlier) terhadap asam sinamat
Gambar 4.6 Senyawa dengan kode S33, S32, dan S34 berturut-turut dari kiri kekanan
Dari gambar 4.4 Dapat dilihat bahwa senyawa dengan kode S32, S33, dan S34 memiliki konformasi yang berbeda jauh dari asam sinamat sebagai senyawa penuntun. Selain itu juga terlihat bahwa senyawa dengan kode S32, S33, dan S34 memiliki gugus kromofor yang berbeda dengan asam sinamat hal ini menunjukan bahwa ketiga senyawa tersebut dapat dikatakan bukan merupakan turunan dari asam sinamat atau outlier.