UJI STABILITAS FISIK DAN PENGARUH VITAMIN C TERHADAP
AKTIVITAS DAN DAYA PENETRASI EKSTRAK ETANOL KULIT
MANGGIS (Garcinia mangostana L.) PADA SERUM ANTIKERUT
Exaudi Ebennezer, Joshita Djajadisastra, Raditya IswandanaFakultas Farmasi, Universitas Indonesia E-mail: [email protected]
ABSTRAK
Kulit Manggis (Garcinia mangostana L.) terbukti kaya akan kandungan xanton yang memiliki potensi aktivitas antioksidan yang sangat tinggi. Pada penelitian ini digunakan metode peredaman DPPH (2,2-Difenil-1-pikrilhidrazil) untuk mengetahui IC50 dari ektrak etanol kulit buah manggis dan sediaan serum. Penelitian ini merupakan aplikasi dari ekstrak kulit buah manggis dalam sediaan likuid dengan sedikit pelarut dan banyak komponen bioaktif, yang dalam istilah kosmetik disebut sebagai serum. Penelitian ini bertujuan untuk menguji stabilitas fisik dan pengaruh dari vitamin C terhadap aktivitas, stabilitas dan daya penetrasi ekstrak etanol kulit buah manggis pada serum antikerut. Selanjutnya ekstrak diformulasikan ke dalam tiga jenis sediaan yang terdapat variasi vitamin C sebagai peningkat penetrasi dan satu sediaan tanpa ekstrak dan vitamin C. Ketiga sediaan diuji daya penetrasinya secara in vitro dengan sel difusi Franz menggunakan membran abdomen tikus betina galur Sprague-Dawley. Nilai IC50 ekstrak etanol kulit manggis adalah 15,27 ppm, sedangkan sediaan formula 1, 2, 3 dan 4 berturut-turut adalah 109.347,45; 13.275,86; 2014,18 dan 126,52 ppm. Jumlah kumulatif xanton total yang terpenetrasi dari sediaan formula 2, 3 dan 4 berturut-turut adalah 15,79±0,18; 26,85±1,03 dan 61,05±2,53%. Fluks dari sediaan formula 2, 3 dan 4 berturut-turut adalah 0,15±0,003; 0,37±0,01 dan 0,92±0,03 µg/cm2.jam. Berdasarkan hasil tersebut dapat disimpulkan bahwa dengan adanya vitamin C akan meningkatkan daya penetrasi sediaan serum. Seluruh sediaan menunjukkan kestabilan secara fisik.
Kata Kunci : manggis (Garcinia mangostana L.); penetrasi, sel difusi Franz; serum; xanton
ABSTRACT
Mangosteen pericarp (Garcinia mangostana L.) has been proved to have plenty of xanthone with high antioxidant. This study was done using DPPH (2,2-diphenyl-1-picrylhydrazyl) to determine the IC50 of ethanolic extract of mangosteen pericarp and serum preparations
containing extract. This study is an application of mangosteen pericarp extract in liquid preparations with a little solvent and many bioactive components, which in terms of cosmetics called serum. The aims of this study are to test the physical stability and the effect of vitamin C on the activity, stability and penetration ability of ethanolic extract of mangosteen pericarp on antiaging serum. Furthermore, ethanolic extract formulated into three variations in preparation of vitamin C as a penetration enhancer and one preparations without extract and vitamin C. The three preparations were examined their penetration ability by in vitro Franz diffusion cell using rat abdominal skin as diffusion membrane. IC50 values of ethanolic extract
of mangosteen pericarp were obtained at 15,27 ppm, whilst the preparations formula 1, 2, 3 and 4 were 109.347,45; 13.275,86; 2014,18 and 126,52 ppm, respectively. Total cumulative
penetration of total xanthone from formula 2, 3 and 4 were 15,79±0,18; 26,85±1,03 and 61,05±2,53%, respectively. Flux of total xanthone from formula 2, 3 dan 4 were 0,15±0,003; 0,37±0,01 and 0,92±0,03 µg/cm2.hour, respectively. Based on these results, it can be concluded that the presence of vitamin C will increase the penetration ability of serum preparation. All preparations showed physical stability.
Keywords : Franz diffusion cell; mangosteen (Garcinia mangostana L.); penetration; serum; xanthone
PENDAHULUAN
Kulit merupakan organ tubuh terluar yang menutupi permukaan tubuh dan membentuk perbatasan antara organisme dan lingkungan yang dapat diamati tanda-tanda penuaan pada manusia dengan mudah berupa kerutan (Rieger & Martin, 2000). Kerutan terjadi karena penurunan kadar air lapisan tanduk kulit, serta perubahan pada jumlah dan kualitas kolagen serta serabut elastin dermis sehingga terjadi penurunan elastisitas kulit (Mitsui, 1996). Penuaan pada kulit terdiri dari dua proses yaitu proses penuaan karena faktor umur dan
photoaging oleh radiasi sinar UV dari pancaran sinar matahari (Rieger & Martin, 2000).
Faktor-faktor lain yang menyebabkan terjadinya penuaan dini antara lain faktor genetik, gaya hidup, lingkungan, mutasi gen, rusaknya sistem kekebalan dan radikal bebas. Dari semua faktor penyebab tersebut, teori radikal bebas merupakan teori yang paling sering diungkapkan. Radikal bebas adalah sekelompok bahan kimia baik berupa atom maupun molekul yang memiliki elektron tidak berpasangan pada lapisan terluarnya. Radikal bebas dengan jumlah yang berlebih akan merusak kolagen pada membran sel kulit, sehingga kulit kehilangan elastisitasnya dan akan menyebabkan terjadinya keriput. Oleh karena itu tubuh memerlukan antioksidan yang dapat membantu melindungi tubuh dari serangan radikal bebas (Kosasih et al., 2006).
Garcinia mangostana L. atau buah manggis merupakan salah satu primadona
buah-buahan tropis. Kulit buah manggis mengandung berbagai senyawa kimia yaitu derivat xanton yang memiliki aktivitas antioksidan, antimikroba, antijamur dan antikanker (Hyun-Ah et al., 2006). Derivat xanton utama yang diisolasi dari kulit buah manggis yaitu α-mangostin dan γ-mangostin (Chaverri et al., 2008).
Perkembangan dunia kosmetik saat ini telah menawarkan berbagai solusi untuk mencegah penuaan dan kerut. Target utama dari bahan anti penuaan adalah kerusakan oksidatif dan metabolisme kolagen. Paparan sinar UV terutama UV-B menyebabkan
terbentuknya radikal bebas atau ROS (Radical Oxygen Species) yang merupakan molekul tidak stabil yang dapat terbentuk pada seluruh lapisan epidermis dan jaringan yang lebih dalam (Hanson & Clegg, 2002). Derivat xanton yang terdapat pada ekstrak kulit buah manggis memiliki kemampuan sebagai antioksidan yang dapat memodulasi efek kerusakan karena UV yang diinduksi oleh ROS. ROS akan berikatan dengan komponen sel untuk menjadi stabil, sehingga akan merusak komponen sel seperti lemak, protein, dan asam nukleat (Moore, 1982).
Vitamin C selain bertindak sebagai antioksidan dan berfungsi untuk sintesis kolagen dan elastin (Ronchetti et al., 1996) juga berperan untuk meningkatkan penetrasi pada kulit dengan meningkatkan kelarutan zat aktif dalam pembawa sehingga menghasilkan gradien konsentrasi yang tinggi untuk melintasi kulit. Selain itu, pada konsentrasi rendah vitamin C akan berinteraksi dengan keratin pada kulit dan pada konsentrasi tinggi vitamin C akan berinteraksi dengan protein dan lipid pada stratum corneum sehingga mempengaruhi sifatnya sebagai barrier (Das & Ahmed, 2008).
Penelitian yang dilakukan merupakan aplikasi dari ekstrak kulit buah manggis dalam sediaan likuid dengan sedikit pelarut dan banyak komponen bioaktif, yang dalam istilah kosmetik disebut sebagai serum (Draelos, 2010). Konsep pembuatan serum adalah teknologi gel dengan viskositas yang lebih rendah dan kurang jernih (semi-transparan), dan mengandung komponen bioaktif yang lebih banyak dari sediaan kosmetik pada umumnya sehingga tercipta suatu bentuk konsentrat serta penggunaan dari vitamin C yang akan meningkatkan efektivitas serum antikerut dari ekstrak kulit manggis karena dapat berperan sebagai peningkat penetrasi dan juga aktivitasnya sebagai antioksidan (Das & Ahmed, 2008).
Penelitian ini bertujuan untuk menguji stabilitas fisik dan pengaruh dari vitamin C terhadap aktivitas, stabilitas dan daya penetrasi ekstrak etanol kulit buah manggis (Garcinia
mangostana L.) pada serum antikerut.
TINJAUAN TEORITIS
Kulit merupakan sawar karena mengandung lapisan lipid, tanduk, dan malpighi. Bagian terluar dari kulit, stratum korneum merupakan penghalang yang tangguh yang mampu menghambat penetrasi perkutan bagi kebanyakan zat aktif. Hal ini juga menjadi mekanisme perlindungan penting terhadap kemungkinan masuknya molekul eksogen yang berbahaya (Fox et al., 2011).
Peningkat penetrasi adalah suatu bahan yang berinteraksi dengan konstituen stratum korneum untuk meningkatkan penetrasi suatu zat ke kulit. Mekanisme aksi peningkat penetrasi dapat melalui berbagai cara (Williams & Barry, 2007), seperti:
a. Memodifikasi lipid intersel untuk menurunkan resistensi barrier lipid bilayer.
b. Mengubah sifat pelarut stratum korneum sehingga dapat memodifikasi partisi obat atau kosolven ke jaringan
c. Bekerja terhadap keratin intrasel stratum korneum, mendenaturasi atau memodifikasi sehingga menyebabkan peningkatan hidrasi stratum korneum. Peningkatan hidrasi dapat meningkatkan kelembaban, yang dapat mengembangkan stratum korneum sehingga dapat terbentuk anyaman serabut keratin yang stabil pada daerah polar yang kaya air dan daerah non polar yang kaya lipid. Sifat ini menyebabkan stratum korneum mempunyai afinitas yang sama terhadap senyawa larut air maupun larut lemak.
Masyarakat di Asia Tenggara menggunakan kulit buah manggis (G. mangostana L.) secara tradisional untuk pengobatan sakit perut, diare, disentri, luka terinfeksi, nanah dan ulkus kronis. Beberapa penelitian ilmiah membuktikan bahwa ekstrak kulit manggis memiliki manfaat sebagai antioksidan, antitumor, antialergi, antiinflamasi, antibakteri, antifungi dan antivirus. Kandungan kimia kulit manggis salah satunya adalah derivat xanton. Derivat xanton telah diisolasi dari kulit manggis yaitu α-mangostin, β-mangostin, dan γ-mangostin, garsinon E, 8-deoksigartanin dan gartanin (Chaverri et al., 2008).
a b c
Keterangan: a. α–mangostin d. γ–mangostin
b. β–mangostin e. Garsinon-E
c. Gartanin f. 8-deoksigartanin
[Sumber : Chaverri et al., 2008]
Gambar 2. Kandungan Xanton Kulit Manggis METODE PENELITIAN
Bahan
α-mangostin (Chengdu Sichuan, China), ekstrak etanol kulit manggis Garcinia mangostana L. (Balitro, Indonesia), asam askorbat (Indonesia), NaOH (Indonesia), gliserin (Indonesia), karbopol (Indonesia), natrium bikarbonat (Indonesia), natrium metabisulfit (Indonesia), etanol (Indonesia), metanol (Indonesia), metil paraben (Indonesia), DPPH (Wako, Jepang), kalium dihidrogen fosfat (Merck, Jerman) dan kulit tikus betina Sprague dawley usia 8-10 bulan dengan berat ± 150 gram (Institut Pertanian Bogor, Indonesia).
Metode
Uji Aktivitas Antioksidan Ekstrak Kulit Manggis Terhadap DPPH (2,2-Difenil-1-pikrilhidrazil)
Panjang gelombang DPPH ditentukan dengan cara membuat larutan DPPH 100 ppm dalam metanol dan ditentukan spektrum serapannya pada panjang gelombang 400 nm hingga 800 nm kemudian ditentukan panjang gelombang maksimumnya (Zarena et al., 2009). Ekstrak kulit manggis dilarutkan dalam metanol dan dibuat konsentrasi 2, 4, 10, 12, 16 dan 20 ppm. Blanko positif digunakan vitamin C kemudian dibuat larutan dengan konsentrasi 1, 2, 3, 4, 5 dan 6 ppm dalam metanol. Larutan uji dibuat dengan cara 2 mL dari masing-masing konsentrasi larutan ditambahkan 1 mL DPPH 100 ppm dan 1 ml metanol. Campuran dikocok selama 20 detik kemudian larutan uji dan blanko diinkubasi pada suhu 37oC selama 30 menit. Uji antioksidan dilakukan dengan metode DPPH dan pengukuran serapan menggunakan spektrofotometer UV-Vis. Serapan atau absorbansi larutan uji diukur pada panjang gelombang maksimum. Dari data absorbansi yang didapat kemudian dihitung persentase inhibisi ekstrak terhadap radikal bebas DPPH.
Penetapan Kadar Xanton Total pada Ekstrak Etanol Kulit Manggis dengan Spektrofotometer UV-Vis (Aisha et al., 2013)
Larutan standar α–mangostin dibuat dengan konsentrasi 4, 5, 6, 8, 10 dan 12 ppm dalam metanol. Kemudian ditentukan panjang gelombang maksimumnya dengan spektrofotometer UV-Vis pada larutan dengan konsentrasi 10 ppm pada panjang gelompang antara 200 – 500 nm. Larutan standar α-mangostin masing-masing diukur serapannya dengan menggunakan spektrofotometer UV-Vis pada panjang gelombang maksimum, kemudian dihitung persamaan regresi liniernya.
Larutan sampel ekstrak dibuat dengan menimbang ekstrak kental sebanyak 50,0 mg dan dilarutkan dengan metanol dalam labu tentukur 100 mL sehingga diperoleh konsentrasi 500 ppm. Kemudian diambil 2,0 mL dan diencerkan dengan metanol dalam labu tentukur 50 mL sehingga diperoleh konsentrasi 20 ppm. Selanjutnya larutan tersebut diukur serapannya pada panjang gelombang maksimum dengan menggunakan Spektrofotometer UV-Vis. Percobaan dilakukan sebanyak 3 kali.
Formulasi Serum Antikerut
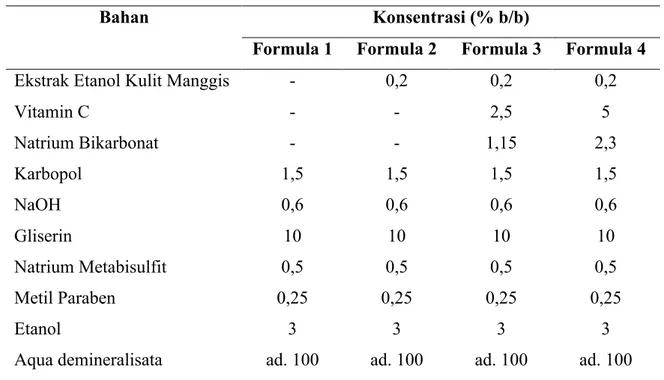
Tabel 1. Formulasi Serum Antikerut
Bahan Konsentrasi (% b/b)
Formula 1 Formula 2 Formula 3 Formula 4
Ekstrak Etanol Kulit Manggis - 0,2 0,2 0,2
Vitamin C - - 2,5 5 Natrium Bikarbonat - - 1,15 2,3 Karbopol 1,5 1,5 1,5 1,5 NaOH 0,6 0,6 0,6 0,6 Gliserin 10 10 10 10 Natrium Metabisulfit 0,5 0,5 0,5 0,5 Metil Paraben 0,25 0,25 0,25 0,25 Etanol 3 3 3 3
Aqua demineralisata ad. 100 ad. 100 ad. 100 ad. 100
Pembuatan serum ekstrak kulit manggis didasarkan pada pembuatan gel, hanya saja diharapkan viskositasnya lebih rendah. Mula-mula, karbopol didispersikan di dalam sejumlah air dengan homogenizer kecepatan 1200 rpm. Ekstrak kental kulit manggis dan metil paraben dilarukan dalam etanol, kemudian dicampurkan dengan gliserin. Natrium metabisulfit dan
NaOH dilarutkan masing-masing dalam aqua demineralisata. Vitamin C dilarutkan dalam aqua demineralisata dan kemudian ditambahkan Natrium Bikarbonat. Kemudian seluruhnya dimasukkan ke dalam dispersi karbopol kemudian larutan NaOH ditambahkan terakhir. Selanjutnya dilakukan homogenisasi dengan homogenizer kecepatan sekitar 1200 rpm dan ditingkatkan hingga 1500 rpm.
Evaluasi Serum Ekstrak Kulit Manggis Pengamatan Organoleptis
Sediaan diamati bau, warna, serta tekstur secara kualitatif.
Pengukuran Derajat Keasaman (pH)
Uji pH dilakukan menggunakan pH meter. Mula-mula elektroda dikalibrasi dengan dapar standar pH 4 dan pH 7. Kemudian elektroda dicelupkan ke dalam sediaan. Nilai pH yang muncul di layar dicatat. Pengukuran dilakukan pada suhu ruang.
Pemeriksaan konsistensi
Sediaan yang akan diperiksa dimasukkan ke dalam wadah khusus dan diletakkan pada meja penetrometer. Peralatan diatur hingga ujung kerucut menyentuh bayang permukaan serum yang diperjelas dengan menghidupkan lampu. Batang pendorong dilepas dengan mendorong tombol start. Angka penetrasi dibaca lima detik setelah kerucut menembus sediaan. Pemeriksaan konsistensi dilakukan pada minggu ke-0 dan minggu ke-12 dengan penyimpanan pada suhu ruang.
Pengukuran viskositas dan sifat alir
Pengukuran viskositas sediaan dilakukan dengan menggunakan viskometer Brookfield pada suhu ruang. Sediaan dimasukkan ke dalam beaker glass, kemudian batang pemutar diturunkan hingga batas batang pemutar tercelup dalam sediaan. Selanjutnya, alat dinyalakan dengan menekan tombol on. Kecepatan batang pemutar diatur berturut-turut 0.5; 2; 4; 10; 20 dan 50 rpm kemudian dibalik 50; 20; 10; 4; 2 dan 0.5 rpm. Dari masing-masing pengukuran dengan perbedaan rpm, skala dibaca ketika jarum merah yang bergerak telah stabil. Viskositas (η) dalam centipoise (cps) diperoleh dari hasil perkalian dial reading (dr) dengan faktor koreksi (f) khusus untuk masing-masing kecepatan batang pemutar. Sifat aliran diperoleh dengan membuat kurva antara tekanan geser (F/A) terhadap kecepatan geser (dv/dr).
Uji Stabilitas Fisik Metode cycling test
Sampel serum disimpan pada suhu 4oC selama 24 jam, lalu dipindahkan ke dalam oven yang bersuhu 40±2oC selama 24 jam (satu siklus). Uji dilakukan sebanyak 6 siklus kemudian dilakukan pengamatan organoleptis (perubahan warna, bau, dan sineresis) dan kristalisasi.
Uji stabilitas pada suhu rendah
Sampel serum disimpan pada suhu rendah (4±20C) selama 12 minggu, kemudian dilakukan pengamatan organoleptis (perubahan warna, bau, dan sineresis), pengukuran pH, dengan pengamatan setiap 2 minggu sekali.
Uji stabilitas pada suhu ruang
Sampel serum disimpan pada suhu kamar (27-300C) selama 12 minggu, kemudian dilakukan pengamatan organoleptis (perubahan warna, bau, dan sineresis), pengukuran pH, dengan pengamatan setiap 2 minggu sekali. Pengukuran viskositas dilakukan pada minggu ke-0 dan ke-12. Viskositas ditentukan dengan batang pemutar dan kecepatan yang sama.
Uji stabilitas pada suhu tinggi
Sampel serum disimpan pada suhu tinggi (40±20C) selama 12 minggu, kemudian dilakukan pengamatan organoleptis (perubahan warna, bau, dan sineresis), pengukuran pH, dengan pengamatan setiap 2 minggu sekali.
Uji Aktivitas Antioksidan dari Sediaan Serum Terhadap DPPH (2,2-Difenil-1-pikrilhidrazil) Sampel sediaan dari formula 1, 2, 3 dan 4 diekstraksi dengan penambahan mentanol, dikocok dengan cepat dan disonikasi selama 20 menit. Kemudian disaring dan ditampung filtratnya. Larutan sampel dari masing-masing formulasi dibuat beberapa konsentrasi dari 2.000 ppm sampai 120.000 ppm. Selanjutnya 1,0 mL dari masing-masing larutan sampel ditambahkan 1,0 mL DPPH dan 2,0 mL metanol kemudian dihomegenkan. Larutan uji diinkubasi pada suhu 37ºC selama 30 menit. Serapan atau absorbansi larutan uji diukur pada panjang gelombang maksimum dan dihitung persentase inhibisi dari sediaan serum.
Uji Penetrasi Sediaan Serum dengan Sel Difusi Franz
Larutan standar α–mangostin dibuat dengan konsentrasi 4, 5, 6, 8, 10 dan 12 ppm dalam campuran pelarut dapar fosfat pH 7,4 dan metanol (80:20). Kemudian ditentukan panjang gelombang maksimumnya dengan spektrofotometer UV-Vis pada larutan dengan
konsentrasi 8 ppm pada panjang gelompang antara 200 – 500 nm. Larutan standar α– mangostin masing-masing diukur serapannya dengan menggunakan spektrofotometer UV-Vis pada panjang gelombang maksimum, kemudian dihitung persamaan regresi liniernya.
Uji perolehan kembali dilakukan terhadap sediaan formula 2, 3 dan 4. Sediaan ditimbang secara seksama sebanyak ± 1,0 g, kemudian dilarutkan dengan campuran pelarut dapar fosfat dan metanol (80:20) dalam labu tentukur 100,0 mL. Larutan sampel disonikasi selama 20 menit dan dilanjutkan dengan proses penyaringan secara kuantitatif. Sampel diukur serapannya dengan menggunakan spektrofotometer UV-Vis pada panjang gelombang maksimum. Percobaan dilakukan tiga kali pada masing-masing formula 2, 3 dan 4.
Membran yang digunakan adalah kulit abdomen tikus betina galur Sprague Dawley usia 8-10 bulan dengan berat ± 150 gram. Pertama-tama tikus dikorbankan dengan eter hingga mati kemudian bulu tikus dicukur dengan hati-hati. Setelah itu kulit tikus disayat pada bagian perut dengan ketebalan 0,6 ± 0,1 mm. Kemudian kulit tikus direndam dalam medium yang akan digunakan selama 30 menit setelah itu disimpan dalam suhu 4ºC. Kulit dapat digunakan pada rentang waktu 24 jam. Uji penetrasi dilakukan menggunakan sel difusi Franz dengan luas area difusi 2,011 cm2 dan volume kompartemen 13 mL. Kompartemen reseptor diisi dengan campuran larutan dapar fosfat pH 7,4 dan metanol (80:20) dan dijaga suhunya sekitar 37 ± 0,5ºC serta diaduk dengan pengaduk magnetik kecepatan 300 rpm. Kulit abdomen tikus kemudian diletakkan di antara kompartemen donor dengan kompartemen reseptor dengan posisi stratum korneum menghadap ke atas. Sampel 1 gram diaplikasikan pada permukaan kulit. Kemudian pada menit ke-10, 30, 60, 90, 120, 180, 240, 300, 360, 420 dan 480 diambil sampel sebanyak 0,5 mL dari kompartemen reseptor menggunakan syringe dan segera digantikan dengan larutan medium sejumlah volume yang sama. Setelah itu, sampel dimasukkan ke dalam labu tentukur 5,0 ml kemudian dicukupkan volumenya dengan campuran pelarut dapar fosfat dan metanol (80:20). Sampel diukur serapannya pada panjang gelombang maksimum dengan spektrofotometer UV-Vis. Percobaan dilakukan sebanyak tiga kali.
Jumlah kumulatif xanton total yang terpenetrasi per luas area difusi (µg/cm2) dihitung dengan rumus:
Keterangan:
Q = Jumlah kumulatif xanton total yang terpenetrasi per luas area difusi (µg/cm2)
Cn = Konsentrasi xanton total (µg/µL) pada sampling menit ke-n V = Volume sel difusi Franz (13,0 mL)
= Jumlah konsentrasi xanton total (µg/µl) pada sampling pertama (menit ke-10) hingga sebelum menit ke-n
S = Volume sampling (0,5 mL) A = Luas area membran (2,011 cm2)
Kemudian dilakukan perhitungan fluks berdasarkan hukum Fick I:
Keterangan:
J = Fluks (µg/cm2 jam1)
M = Jumlah kumulatif xanton total yang melalui membran (µg) S = Luas area difusi (cm2)
t = Waktu (jam)
Selanjutnya dibuat grafik jumlah kumulatif xanton total yang terpenetrasi (µg) per luas area difusi (cm2) terhadap waktu (jam) dan grafik fluks (µg/cm2 jam1) terhadap waktu (jam).
HASIL PENELITIAN
Uji Aktivitas Antioksidan Ekstrak Kulit Manggis Terhadap DPPH (2,2-Difenil-1-pikrilhidrazil)
Hasil uji aktivitas antioksidan esktrak etanol kulit manggis (G.mangostana L.) dengan metode peredaman DPPH, diperoleh nilai IC50 sebesar 15,27 ppm yang dibandingkan dengan blanko positif yaitu vitamin C sebesar 5,15 ppm.
Penetapan Kadar Xanton Total pada Ekstrak Etanol Kulit Manggis dengan Spektrofotometer UV-Vis
Persen xanton total dinyatakan sebagai rasio antara hasil konsentrasi yang diperoleh dengan konsentrasi sebenarnya. Kadar xanton total yang terdapat pada ekstrak etanol manggis sebesar 56,5326±0,19%.
Evaluasi Serum Ekstrak Kulit Manggis
Dari hasil pengamatan sediaan formula 1 tidak memiliki warna, berbau lemah alkohol dan tampak homogen. Sediaan formula 2, 3 dan 4 memiliki karakteristik warna kuning muda, berbau lemah alkohol dan tampak homogen.
Gambar 3. Pengamatan organoleptis (a) formula 1, (b) formula 2, (c) formula 3,
(d) formula 4
pH sediaan dari formula 1, 2, 3 dan 4 secara berturut-turut adalah 6,43; 5,68; 5,87 dan 6,18. Keempat sediaan tersebut masih berada dalam rentang pH kulit, yaitu 4,5 dan 6,5.
Dari hasil pemeriksaan konsistensi didapatkan bahwa kedalaman penetrasi kerucut dari sediaan formula 1, 2, 3 dan 4 berturut-turut adalah 359; 363; 367 dan 378 (1/10 mm). Dari kedalaman penetrasi kerucut tersebut dapat diperoleh yield value untuk sediaan formula 1, 2, 3 dan 4 berturut-turut adalah 2.863,31; 2.801,53; 2.740,79 dan 2.583,59 dyne/cm2.
Untuk mengukur viskositas sediaan digunakan viskometer Brookfield. Pengukuran viskositas dilakukan pada spindel 6 dengan kecepatan putaran 20 rpm. Dari pengukuran dihasilkan nilai viskositas sediaan formula 1, 2, 3 dan 4 berturut-turut adalah 24.000; 20.250; 13.250 dan 8250 cps. Berdasarkan rheogram yang diperoleh semua sediaan memiliki aliran pseudoplastis tiksotropik.
Uji Stabilitas Fisik
Penyimpanan pada Suhu Rendah, Kamar dan Tinggi
Pada penyimpanan suhu rendah, kamar dan tinggi terjadi perubahan warna menjadi semakin gelap sesuai dengan lamanya penyimpanan. Bau dari seluruh sediaan selama 12 minggu penyimpanan adalah bau lemah alkohol. Seluruh sediaan menunjukkan karakteristik organoleptis yang stabil dan homogen
Pengukuran pH yang dilakukan selama 12 minggu pada tiga suhu yang berbeda diperoleh hasil bahwa terjadi perubahan pH pada keempat sediaan. pH keempat sediaan berkisar antara 4,44-6,43.
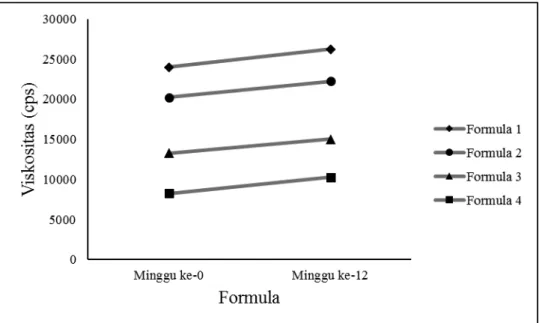
Masing-masing sediaan yang telah disimpan selama 12 minggu pada suhu kamar kemudian diukur viskositasnya. Hasil evaluasi viskositas menunjukkan bahwa terjadi perubahan viskositas masing-masing sediaan. Dari Gambar 4. sediaan formula 1, 2, 3 dan 4 mengalami kenaikan viskositas pada minggu ke-12 berturut-turut adalah 26.250; 22.250; 15.000 dan 10.250 cps. Sifat aliran keempat sediaan yang telah disimpan selama 12 minggu pada suhu kamar menunjukan tidak terjadi perubahan sifat alir dimana tetap memiliki sifat alir pseudoplastis tiksotropik.
Gambar 4. Grafik perubahan viskositas sediaan pada minggu ke-12
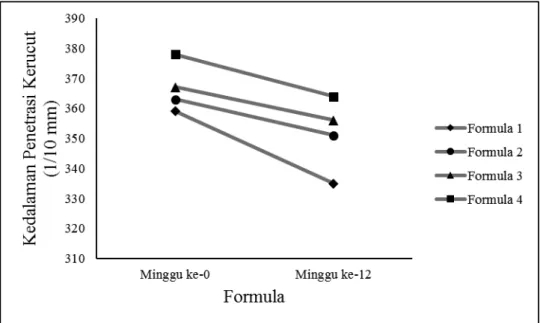
Kedalaman penetrasi kerucut dari sediaan formula 1, 2, 3 dan 4 pada minggu ke-12 berturut-turut adalah 335 1/10 mm, 351 1/10 mm, 356 1/10 mm dan 364 1/10 mm. Gambar 5. menunjukkan bahwa terjadi penurunan nilai kedalaman penetrasi kerucut atau terjadi peningkatan konsistensi dari masing-masing sediaan.
Gambar 5. Grafik perubahan konsistensi sediaan pada minggu ke-0 dan minggu ke-12
Pemeriksaan stabilitas dengan metode cycling test, diperoleh hasil bahwa keempat sediaan stabil dan tidak mengalami perubahan warna, kristalisasi, ataupun sineresis
Uji Aktivitas Antioksidan dari Sediaan Serum Terhadap DPPH (2,2-Difenil-1-pikrilhidrazil) Pengukuran aktivitas antioksidan dilakukan pada keempat sediaan. IC50 dari formula 1, 2, 3 dan 4 berturut-turut adalah 109.347,45; 13.275,86; 2070,51 dan 125,45 ppm.
Uji Penetrasi Sediaan Serum dengan Sel Difusi Franz
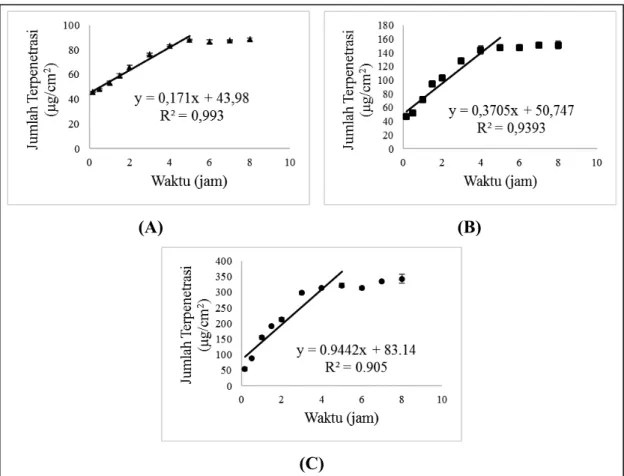
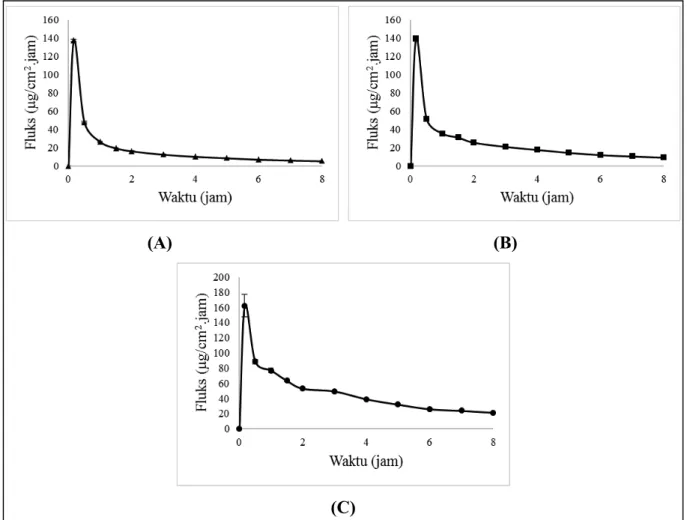
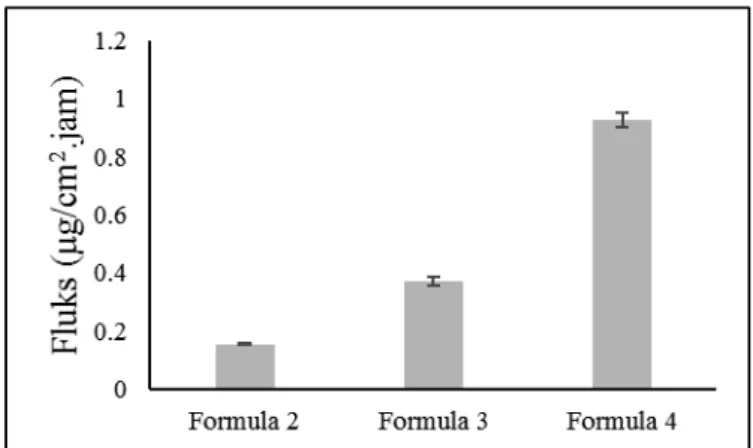
Kadar perolehan kembali xanton total untuk sediaan formula 2, 3 dan 4 berturut-turut adalah 103,54 ± 2,00; 99,52 ± 2,60 dan 95,47 ± 2,34%. Hasil pengujian penetrasi melalui membran kulit tikus dari sediaan formula 2, 3 dan 4 secara berturut-turut adalah 88,84±1,02; 151,03±5,80 dan 343,31±14,28 µg/cm2. Berdasarkan jumlah xanton total yang terpenetrasi dapat dihitung persentasi jumlah xanton total yang terpenetrasi dari dosis yang diaplikasikan. Persen xanton total yang terpenetrasi dari sediaan formula 2, 3 dan 4 secara berturut-turut yaitu 15,85±0,18; 26,95±1,03 dan 61,26±2,53%. ). Adapaun fluks dari ketiga sediaan formula 2, 3 dan 4 secara berturut-turut adalah 0,15±0,003; 0,37±0,01 dan 0,93±0,03 µg/cm2.jam.
(A) (B)
(C)
Gambar 6. Jumlah kumulatif xanton total yang terpenetrasi per satuan luas membran:
(A) (B)
(C)
Gambar 7. Fluks xanton total tiap waktu pengambilan: (A) formula 2; (B) formula 3;
(C) formula 4
Gambar 9. Fluks xanton total dari sediaan serum PEMBAHASAN
Pada pembuatan serum didasarkan pada pembuatan gel dimana digunakan karbomer sebagai pembentuk gel yang merupakan polimer asam akrilat yang bersifat hidrofilik dan stabil. Basis ini dipilih karena memiliki kompatibilitas dengan seluruh bahan dalam formula dan sangat baik digunakan untuk sediaan kosmetik karena tidak meninggalkan bekas dan kerak saat digunakan, sehingga meningkatkan kenyamaan.
Vitamin C merupakan suatu zat yang tidak stabil dan mudah teroksidasi. Oleh karena itu, diperlukan suatu antioksidan tambahan yang mampu mengalami oksidasi terlebih dahulu dibandingkan vitramin C. Natrium metabisulfit merupakan bahan yang kompatibel dengan bahan lain dalam formula dan mampu menjaga derivat xanton dan vitamin C tetap stabil pada sediaan. Selain itu, natrium metabisulfit juga berperan sebagai antibrowning agent (Rowe et al., 2009).
Karbomer akan berubah menjadi kental pada rentang pH 4,5 - 10 sehingga pH sediaan dibuat pada rentang pH tersebut dan tetap memperhatikan pH kulit yaitu 4,5 – 6,5. Larutan vitamin C bersifat asam sehingga dengan penambahan natrium bikarbonat akan merubah asam askorbat menjadi natrium askorbat sehingga dihasilkan pH netral. Pada tahap akhir pencampuran bahan, ditambahkan NaOH untuk menetralkan pH basis gel. Pengadukan menggunakan homogenizer dengan kecepatan 1200 rpm.
Seluruh sediaan menunjukkan kestabilan secara fisik. Selama penyimpanan 12 minggu, pemeriksaan pH keempat sediaan tidak menunjukkan pH yang tetap. pH seluruh sediaan lebih rendah dibandingkan pH semula. Hal ini diduga akibat terjadinya pelepasan ion hidrogen (H+) yang dimiliki vitamin C akibat adanya proses oksidasi lambat yang tergantung pada kondisi penyimpanan masing-masing sediaan. Terjadi peningkatan viskositas pada
seluruh formula menunjukkan bahwa pada minggu ke-0 setelah sediaan baru saja dibuat struktur molekul gel masih acak akibat putaran dengan kecepatan tinggi saat proses pembuatan, namun setelah disimpan selama 12 minggu struktur molekul gel kembali pada susunan semua. Pemberian tekanan geser ketika pengukuran viskositas pada minggu ke-12 tidak membuat perubahan yang besar pada susunan molekul karbomer sehingga dengan susunan molekul yang lebih rapat dibandingkan minggu ke-0 menghasilkan nilai viskositas yang lebih tinggi. Hal ini berbanding lurus dengan hasil pengukuran konsistensi sediaan yang semakin tinggi. Semakin tinggi viskositas sediaan maka semakin sukar kerucut untuk menembus sediaan sehingga jarak tempuh semakin kecil.
Pada penelitian ini dilakukan uji penetrasi secara in vitro menggunakan sel difusi Franz. Membran yang digunakan pada penelitian ini adalah membran dari kulit abdomen tikus putih betina galur Spraque Dawley yang berumur 2-3 bulan dengan berat 150-200 gram dengan ketebalan membran 0,6 ± 0,1 mm dan luas membran 2,011 cm2. Alasan penggunaan kulit tikus sebagai membran karena cukup mudah didapat dan telah dilaporkan bahwa permeabilitas kulit tikus yang telah dicukur bulunya mirip dengan permeabilitas kulit manusia. Kulit manusia memiliki koefisien permeabilitas sebesar 92,27 cm/jam x 105, sedangkan kulit tikus yang sudah dicukur bulunya memiliki koefisien permeabilitas sebesar 103,08 cm/jam x 105 (Wester & Maibach, 1990).
Medium reseptor yang digunakan untuk uji penetrasi xanton pada penelitian ini adalah campuran antara dapar fosfat pH 7,4 dan metanol dengan perbandingan 80:20. Dapar fosfat pH 7,4 dipilih sebagai medium reseptor digunakan sebagai simulasi cairan biologis tubuh. Namun, karena ekstrak etanol kulit manggis tidak larut air, pada medium reseptor ditambahkan metanol sebagai bahan pensolubilisasi. Pengadukan pada kompartemen reseptor berfungsi untuk homogenisasi dan mempertahankan sink condition. Pengadukan dilakukan dengan menggunakan pengaduk magnetik dengan kecepatan konstan. Suhu dijaga dengan menggunakan water jacket pada 37°±0,5°C dengan menggunakan air yang dialirkan dari termostat. Suhu 37°±0,5°C ini menggambarkan suhu tubuh manusia. Suhu harus tetap dijaga karena suhu juga berpengaruh pada banyaknya zat aktif yang dapat terpenetrasi ke dalam kulit. Semakin tinggi suhu, maka akan semakin banyak zat aktif yang larut dalam kompartemen reseptor sehingga nilai serapan yang diukur akan semakin besar (Ansel, 1989).
Dari Gambar 6. dapat terlihat bahwa proses absorbsi xanton melalui kulit terjadi dengan cepat dan tidak terlihat lag time di menit-menit awal. Bahan tambahan yang terdapat dalam formula seperti gliserin dan etanol juga merupakan bahan peningkat penetrasi perkutan dengan menghidrasi kulit (Barry, 2001). Etanol bekerja sebagai peningkat penetrasi perkutan
dengan cara mengubah sifat melarutkan stratum korneum sehingga zat aktif lebih banyak terlarut ke dalam stratum korneum dan membuat penetrasinya meningkat (Williams & Barry, 2007).
Fluks diperoleh pada keadaan steady state dengan mengikuti kaidah hukum Fick I. Gambar 7. menunjukkan bahwa fluks xanton dari sediaan yang awalnya menaik lalu menurun dan kemudian mendatar. Hal ini disebabkan pada menit-menit awal terdapat perbedaan konsentrasi yang cukup besar antara kompartemen reseptor dan donor. Keadaan tersebut merupakan keadaan nonsteady-state. Setelah mencapai jam ke-3 fluks menjadi lurus yang menggambarkan bahwa keadaan sudah mencapai steady state (Martin et al., 1983).
Berdasarkan hasil tersebut dapat dilihat bahwa sediaan formula 4 dengan konsentrasi vitamin C sebagai peningkat penetrasi yang paling tinggi memiliki kecepatan penetasi yang paling tinggi pula jika dibandingkan dengan sediaan formula 2 tanpa vitamin C. Meningkatnya konsentrasi vitamin C akan meningkatkan jumlah kumulatif dari zat aktif yang terpenetrasi. Jumlah kumulatif dari xanton toal yang terpenetrasi dan fluks ketiga sediaan dapat dilihat masing-masing pada Gambar 8. dan 9. Vitamin C berperan untuk meningkatkan penetrasi dengan meningkatkan kelarutan zat aktif dalam pembawa sehingga menghasilkan gradien konsentrasi yang tinggi untuk melintasi kulit. Selain itu, pada konsentrasi rendah vitamin C akan berinteraksi dengan keratin pada kulit dan pada konsentrasi tinggi vitamin C akan berinteraksi dengan protein dan lipid pada stratum korneum sehingga mempengaruhi sifatnya sebagai barrier (Das & Ahmed, 2008).
KESIMPULAN
Pengukuran aktivitas antioksidan sediaan serum menggunakan metode peredaman DPPH menunjukkan semua sediaan memiliki aktivitas antioksidan. Nilai IC50 dari sediaan formula 1, 2, 3 dan 4 berturut-turut adalah 109.347,45; 13.275,86; 2014,18 dan 126,52 ppm. Vitamin C juga berfungsi sebagai antioksidan sehingga sediaan formula 3 dan 4 yang mengandung vitamin C memiliki aktivitas antioksidan yang lebih tinggi.
Berdasarkan hasil uji penetrasi xanton total secara in vitro dapat disimpulkan bahwa sediaan formula 4 yang mengandung ekstrak etanol kulit manggis dan vitamin C dengan konsentrasi tertinggi memberikan hasil penetrasi yang paling tinggi. Meningkatnya konsentrasi vitamin C akan meningkatkan penetrasi dari xanton total pada ekstrak etanol kulit manggis. Hasil ini diperoleh dengan membandingkan jumlah kumulatif xanton total terpenetrasi dan fluks selama 8 jam menggunakan sel difusi Franz dengan kulit abdomen tikus
putih betina galur Sprague-Dawley sebagai membran. Jumlah kumulatif xanton total yang terpenetrasi dari sediaan formula 2, 3 dan 4 berturut-turut adalah 15,79±0,18; 26,85±1,03 dan 61,05±2,53%. Fluks dari sediaan formula 2, 3 dan 4 berturut-turut adalah 0,15±0,003; 0,37±0,01 dan 0,92±0,03 µg/cm2.jam.
Keempat sediaan yang disimpan pada suhu rendah (4±2oC), suhu kamar (28±2oC), dan suhu tinggi (40±2oC) selama 8 minggu dapat dinyatakan stabil secara fisik dengan parameter organoleptis, homogenitas, viskositas dan konsistensi.
SARAN
1. Perlu digunakan alat kromatografi cair kinerja tinggi (KCKT) dalam analisa sampel sehingga didapatkan hasil yang lebih spesifik terhadap α-mangostin dan lebih sensitif. 2. Perlu dilakukan uji stabilitas kimia dan stabilitas mikrobiologi karena parameter
kestabilan fisik saja tidak cukup untuk mengetahui kestabilan suatu sediaan.
3. Perlu dilakukan uji penetrasi sediaan menggunakan membran dari kulit kadaver manusia.
KEPUSTAKAAN
Aisha, A.F.A., Abu-Salah, K.M., Ismail, Z., & Majid, A.M.S.A. (2013). Determination of total xanthones in Garcinia mangostana fruit rind extracts by ultraviolet (UV) spectrofotometry. Journal of Medicinal Plants, 7, 29-35.
Das, M., & Ahmed, A. (2008). Skin permeation enhancement effects of ascorbic acid and triethyl citrate on rofecoxib. Malaysian Journal of Pharmaceutical Sciences, 6, 69-86. Draelos, Z.D. (2010). Cosmetic dermatology products and procedures. West Sussex:
Wiley-Blackwell, 504.
Hanson, K., Clegg, R. (2002). Obervation and quantification of ultraviolet-induced reactive oxygen species in ex vivo human skin. Photochemistry and photobiology, 76, 57-63. Hyun-Ah Jung, Bao-Ning Su, W.J. Keller, R.G. Mehta, A.D. Kinghorn. (2006). Antioxidant
xanthones from the pericarp of garcinia mangostana (mangosteen). J. Agri. Food
Chem., 54, 2077-2082.
Kosasih, E.N., Tony S., Hendro H. (2006). Peran antioksidan pada lanjut usia. Pusat Kajian Nasional Masalah Lanjut Usia. Jakarta, 48-49, 56-59.
Lund, W. (1994). The pharmaceutical codex (12th ed). London: The Pharmaceutical Press, 135-142.
Martin, A., Swarbick, J., & Cammarata, A. (1983). Farmasi Fisik Jilid II edisi ketiga terj. dari Physical Pharmacy oleh Joshita. Jakarta: UI Press, 1143-1183.
Mitsui, Takeo. (Ed.). (1996). New cosmetic science. Amsterdam : Elsevier, 3, 13-14.
Pedraza-Chaverri, J., N.Cardenas-Rodriguez, M. Orozco-Ibarra J.M. Perez-Rojas. (2008). Medicinal properties of mangosteen (Garcinia mangostana L.). Food Chem. Toxic., 46, 3227–3239.
Rieger, Martin M. (2000). Harry’s cosmeticology (8th ed.). New York: Chemical Publishing Co, Inc, 3, 895.
Ronchetti, I.P., Quaglino, D Jr., Bergamini, G. (1996). Ascorbic acid and connective tissue.
Biochemistry and biomedical cell biology. New York (NY): Plenum Press, 41.
Rowe, R.C., Sheskey, P.J., Quinn, M.E. (2009). Handbook of pharmaceutical excipients (6th ed.). Grayslake: Pharmaceutical Press and American Pharmacists Association, 110, 283, 441, 629, 654.
Wester, R. C., & Maibach, H. I. (1990) In vitro testing of topical pharmaceutical formulations. Topical drug delivery formulations. New York: Marcel Dekker Inc, 653-659.
Williams, Adrian C. & Barry, Brian W. (2007). Enhancement in drug delivery. USA: CRC Press, 233-248.
Zarena, A.S., & K.U. Sankar. (2009). A study of antioxidant properties from Garcinia