LAJU KOROSI BAJA TERELEKTROPLATING
DI
LINGKUNGAN AIR LAUT
TUGAS AKHIR
Diajukan Untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Teknik
Jurusan Teknik Mesin
Disusun Oleh:
KRISTOFHORUS KURO UMANG
NIM : 045214065
PROGRAM STUDI TEKNIK MESIN
FAKULTAS SAINS DAN TEKNOLOGI
UNIVERSITAS SANATA DHARMA
YOGYAKARTA
i
LAJU KOROSI BAJA TERELEKTROPLATING
DI
LINGKUNGAN AIR LAUT
TUGAS AKHIR
Diajukan Untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Teknik
Jurusan Teknik Mesin
Disusun Oleh:
KRISTOFHORUS KURO UMANG
NIM : 045214065
PROGRAM STUDI TEKNIK MESIN
FAKULTAS SAINS DAN TEKNOLOGI
UNIVERSITAS SANATA DHARMA
YOGYAKARTA
ii
CORROSION RATE OF STEEL ELECTROPLATING
IN
SEA WATER ENVIRONMENT
FINAL PROJECT
Presented as Partial fulfillment of the Requirements To Obtain the Sarjana Teknik Degree
In Mechanical Engineering
By :
KRISTOFHORUS KURO UMANG
Student Number : 045214065
MECHANICAL ENGINEERING STUDY PROGRAM
MECHANICAL ENGINEERING DEPARTMENT
SCIENCE AND TECHNOLOGY FACULTY
SANATA DHARMA UNIVERSITY
vii
INTISARI
LAJU KOROSI BAJA TERELEKTROPLATING
DI LINGKUNGAN AIR LAUT
Tujuan penelitian adalah untuk mengetahui pengaruh lingkungan air laut terhadap sifat fisis dan mekanis baja karbon rendah terelektroplating seng dengan pengujian: kekuatan tarik baja karbon rendah terelektoplating seng, pengamatan struktur makro baja karbon rendah terelektroplating seng, pengamatan struktur mikro baja karbon rendah terelektroplating seng, dan penurunan berat baja karbon rendah terelektroplating seng.
Penelitian dilakukan di Universitas Sanata Dharma, Yogyakarta. Obyek penelitian sebanyak 27 benda uji, terdiri dari: 3 benda uji awal, 12 benda uji baja karbon rendah terelektroplating seng, dan 12 benda uji baja karbon rendah tanpa terelektroplating. 24 benda uji tersebut direndam air laut. Total waktu perendaman benda uji adalah 40 hari, setiap 10 hari dilakukan pengambilan data.
viii
KATA PENGANTAR
Puji syukur penulis haturkan kepada Allah, Bapa, Putra dan Roh kudus
yang telah melimpahkan rahmat-Nya kepada penulis sehingga dapat
menyelesaikan tugas akhir ini.
Tugas akhir ini merupakan salah satu syarat yang harus dipenuhi bagi
mahasiswa Teknik Mesin sebelum dinyatakan lulus sebagai Sarjana Teknik.
Pelaksanaan dan penulisan tugas akhir ini tidak lepas dari bantuan berbagai pihak,
baik berupa materi, bimbingan, kerja sama serta dukungan moril. Dalam
kesempatan ini penulis mengucapkan terimakasih sebanyak-banyaknya kepada :
1. Yosef Agung Cahyanta, S.T., M.T., Dekan Fakultas Sains dan Teknologi
Universitas Sanata Dharma Yogyakarta.
2. Ir. Petrus Kanisius Purwadi, M.T., Ketua Program Studi Teknik Mesin
Universitas Sanata Dharma.
3. Wibowo Kusbandono, S.T., M.T., Dosen pembimbing akademik..
4. Budi Setyahandana, S.T., M.T., Dosen Pembimbing Tugas Akhir.
5. Seluruh dosen dan karyawan Fakultas Sains dan Teknologi Universitas
Sanata Dharma
6. Martono Dwiyaning Nugroho, Ag. Ronny Widaryawan, Intan Widanarko,
ix
7. Kepada Papa, Mama, adik, kakak saya yang tercinta, terimakasih atas
dukungan moral, finansial, doa dan motivasi yang tiada henti hingga tugas
akhir ini dapat selesai.
8. Saudara, saudari anggota organisasi ”TEKSAPALA”, teman-teman di
Universitas Sanata Dharma, khususnya Ronal Yawand, teman-teman satu
kos, Andi Suwung, Agus beserta istri, Suroso beserta istri, Bambang,
Maria, Anang, Lia, Andri, Aten Lakapu, Jek, Bapak kos, Ibu kos, dll.
9. Rekan-rekan dan semua pihak yang membantu dalam penulisan tugas
akhir ini.
Yogyakarta, Oktober 2011
x
DAFTAR ISI
LEMBAR JUDUL ... i
LEMBAR JUDUL BAHASA INGGRIS ... ii
LEMBAR PERSETUJUAN DOSEN PEMBIMBING ... iii
LEMBAR PENGESAHAN DOSEN PENGUJI DAN DEKAN ... iv
LEMBAR PERNYATAAN KEASLIAN KARYA ... v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS ... vi
INTISARI ... vii
KATA PENGANTAR ... viii
DAFTAR ISI ... x
DAFTAR GAMBAR ... xiii
DAFTAR TABEL ... xv
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang Penelitian ... 1
1.2 Tujuan Penelitian ... 2
1.3 Batasan Penelitian ... 2
BAB II DASAR TEORI ... 4
2.1 Baja Karbon ... 5
2.2 Produksi Bijih Besi ... 6
2.2.1 Proses Pemurnian Bijih Besi...7
xi
2.2.3 Proses Pengolahan Baja ... 9
2.3 Elektroplating ... 14
2.3.1 Prinsip kerja Elektroplating ... 16
2.3.2 Efisiensi Plating ... 18
2.3.3 Faktor-faktor Yang Berpengaruh Pada Plating ... 19
2.4 Pelapisan Seng ... 26
2.4.1 Kegunaan Dan Sifat-sifat Seng ... 26
2.4.2 Peralatan Pelapisan Seng ... 29
2.4.3 Komposisi Dan Kondisi Operasi ... 29
2.4.4 Fungsi Komponen Utama ... 32
2.4.5 Permasalahan Dan Pemecahannya ... 33
2.5 Korosi ... 36
2.5.1 Macam-macam Korosi Yang Disebabkan Oleh Air Laut ... 37
2.5.2 Laju Korosi ... 37
BAB III METODE PENELITIAN ……… 39
3.1 Skema Penelitian ……….. 39
3.2 Bahan Dan Peralatan ... 40
3.3 Pembuatan Benda Uji ... 41
3.3.1 Uji Tarik ... 41
3.3.2 Pengamatan Struktur Mikro ... 42
3.3.3 Pengamatan Struktur Makro ... 43
xii
3.4.1 Uji Tarik ... 43
3.4.2 Pengamatan Struktur Mikro ... 44
3.4.3 Pengamatan Makro ... 45
3.4.4 Uji Berat ... 45
BAB IV HASIL PENELITIAN DAN PEMBAHASAN ... 46
4.1 Hasil Uji Komposisi ... 46
4.2 Pengujian Tarik ... 46
4.3 Pengujian Struktur Mikro ... 53
4.4 Uji Berat ... 54
4.5 Pengamatan Struktur Makro ... 56
BAB V PENUTUP ... 58
5.1 Kesimpulan ... 58
5.2 Saran ... 59
DAFTAR PUSTAKA ... 60 LAMPIRAN
Lampiran : Hasil Uji Komposisi kimia
Lampiran : Gambar Mesin Uji dan Alat
Lampiran : Gambar Pengamatan Struktur Mikro
xiii
DAFTAR GAMBAR
Gambar 2.1 Proses Bijih Besi Sebelum Dimasukkan Kedalam
Dapur/Konverter ... 8
Gambar 2.2 Konstruksi Dapur Tinggi ... 10
Gambar 2.3 Diagram Alir Proses Dapur Tinggi ... 11
Gambar 2.4 Dapur Tinggi ... 12
Gambar 2.5 Diagram Alir Pembuatan Baja Dengan Menggunakan Konverter ... 12
Gambar 2.6 Proses Pembuatan Baja Setelah Melalui konverter ... 13
Gambar 2.7 Proses Elektroplating ... 16
Gambar 3.1 Benda Uji Tarik ( spesimen ) ... 41
gambar 3.2 Standarisasi Dimensi Plat ASTM A370 ... 42
Gambar 4.1 Grafik Kekuatan Tarik Rata–rata Benda Uji Terelektroplating Seng ... 48
Gambar 4.2 Grafik Regangan Rata–rata Benda Uji Terelektroplating Seng ………. 48
Gambar 4.3 Grafik Kekuatan Tarik Rata–rata Benda Uji Tanpa Terelektroplating ………. 50
Gambar 4.4 Grafik Regangan Rata – rata Benda Uji Tanpa Terelektroplating ……….. 50
Gambar 4.5 Grafik Kekuatan Tarik Rata–rata Benda Uji ………... 51
xiv
Gambar 4.7 Benda Uji 3 ( kontak air laut 30 hari ) Tanpa Perlakuan
Elektroplating ... 53
Gambar 4.8 Benda Uji (kontak air laut 10 hari) Tanpa Perlakuan
Elektroplating ... 56
Gambar 4.9 Benda Uji (kontak air laut 10 hari) Dengan Perlakuan
xv
DAFTAR TABEL
Tabel 2.1 Perbandingan Kekuatan ... 6
Tabel 2.2 Komposisi Dan Kondisi Operasi Plating Seng Sianida Tinggi ... 30
Tabel 2.3 Komposisi Dan Kondisi Operasi Plating Seng (lanjut) ... 31
Tabel 4.1 Benda Uji Hasil Fabrikasi (tanpa elekroplating) ... 47
Tabel 4.2 Benda Uji Kontak Air Laut Selama 10 s/d 40 Hari Terelektroplating Seng ... 47
Tabel 4.3 Benda Uji Kontak Air Laut Selama 10 s/d 40 Hari Tanpa Elektroplating ... 49
Tabel 4.4 Kedalaman Korosi ………... 53
Tabel 4.5 Berat Benda Uji Tanpa Perlakuan Elektroplating ... 54
Tabel 4.6 Berat Benda Uji Dengan Perlakuan Elektroplating seng ... 55
1 BAB I PENDAHULUAN
1.1. Latar Belakang Penelitian
Menurut data, sebagian besar permukaan bumi merupakan perairan
khususnya laut. Berbagai macam bentuk penelitian menjadi semakin luas
tidak hanya di dataran, tetapi juga berkembang di perairan (laut) bahkan
ditempatkan jauh dari daratan yang mempunyai fungsi beragam (Trethewey
K.R, 1991).
Adapun beberapa fungsi kemajuan teknologi yang diletakkan di
perairan (khususnya laut) diantaranya adalah: alat pendeteksi gempa, kilang
minyak, bahkan yang tidak ketinggalan dan dikembangkan saat ini adalah
alat penghasil energi alternatif. Kesemuanya itu tentu harus didukung
dengan berbagai macam aspek penelitian, salah satunya adalah pengetahuan
bahan yang dapat dipahami sebagai cara mendisain dan merekayasa struktur
material secara optimal melalui proses yang sesuai untuk menghasilkan
sifat-sifat optimal yang diperlukan untuk aplikasi tertentu khususnya kontak
dengan air laut.
Pengetahuan bahan juga dapat dipahami sebagai pengetahuan yang
diperlukan untuk memilih dan memanfaatkan bahan secara optimal untuk
menghasilkan disain struktur atau komponen yang aman dan efisien dengan
biaya yang rendah. Atas dasar dari pengetian pengetahuan bahan tersebut,
elektroplating. Seperti kita tahu sifat-sifat baja karbon rendah selain mudah
didisain (dibentuk), harga murah, juga banyak diproduksi sehingga untuk
mencari baja tersebut tidak mengalami kesulitan. Untuk mengurangi laju
korosi akibat kontak dengan air laut (karena korosi tetap akan terjadi,
sehingga kita hanya dapat mengurangi laju korosi), penulis memilih
perlakuan elektroplating dengan bahan pelapis seng, ini juga tidak terlepas
dari minimnya biaya yang penulis keluarkan untuk mendukung penelitian
(Tata Surdia dan Saito Shinroku, 1999).
1.2. Tujuan Penelitian
Penelitian ini bertujuan mengetahui pengaruh laju korosi yang
ditimbulkan oleh air laut terhadap sifat fisis dan mekanis pada baja yang
dilapisi seng dengan cara elektroplating, yaitu uji:
a) Kekuatan tarik
b) Pengamatan Struktur Mikro
c) Pengamatan Struktur Makro
d) Uji Berat
1.3. Batasan Penelitian
Dalam penelitian ini diberikan batasan-batasan masalah agar dapat
terarah dan lebih sistematis. Berikut daftar spesifikasi batasan masalah:
a) Bahan yang digunakan adalah baja karbon rendah
c) Benda uji terelektroplating berjumlah 12
d) Benda uji tanpa elektroplating berjumlah 12
e) Korosi dilakukan dalam air laut
f) Pengambilan data pertama 10 hari
g) Pengambilan data kedua 20 hari
h) Pengambilan data ketiga 30 hari
4 BAB II DASAR TEORI
Baja dan besi sampai saat ini menduduki peringkat pertama logam yang
paling banyak penggunaanya. Besi dan baja mempunyai kandungan unsur utama
yang sama yaitu Fe. Penggunaan besi dan baja dewasa ini sangat luas mulai dari
perlatan yang sepele seperti jarum, peniti sampai dengan alat – alat dan mesin
berat.
Berikut merupakan sejarah baja:
Besi ditemukan digunakan pertama kali pada sekitar 1500 SM
Tahun 1100 SM, Bangsa hittites yang merahasiakan pembuatan tersebut
selama 400 tahun dikuasai oleh bangsa asia barat, pada tahun tersebut
proses peleburan besi mulai diketahui secara luas.
Tahun 1000 SM, bangsa yunani, mesir, jews, roma, carhaginians dan
asiria juga mempelajari peleburan dan menggunakan besi dalam
kehidupannya.
Tahun 800 SM, India berhasil membuat besi setelah di invansi oleh
bangsa arya.
Tahun 700 – 600 SM, Cina belajar membuat besi.
Tahun 400 – 500 SM, baja sudah ditemukan penggunaannya di eropa.
Tahun 1000 M, baja dengan campuran unsur lain ditemukan pertama
kali pada 1000 M pada kekaisaran fatim yang disebut dengan baja
damascus.
1300 M, rahasia pembuatan baja damaskus hilang.
1700 M, baja kembali diteliti penggunaan dan pembuatannya di eropa.
(www.oke.or.id, Ahmad Hasnan S)
2.1. Baja Karbon
Unsur pada baja cor dan baja tempa hampir sama, kecuali unsur Si dan Mn
yang berfungsi mengikat O2. Baja cor dihasilkan dari penambahan karbon sekitar
0,05% sampai 1,7% pada besi murni (ferrit). Baja ini dibedakan atas:
Baja karbon rendah (unsur C < 0,3%)
Baja karbon sedang (unsur C 0,3% - 0,5%)
Baja karbon tinggi (unsur C > 0,5%)
Baja karbon rendah
Baja karbon rendah merupakan perpaduan unsur logam atau ferrous (Fe)
dengan unsur karbon (C) dengan kurang dari 0,3%. Bahan jenis ini biasanya
banyak digunakan untuk alat perkakas dan bahan bangunan atau konstruksi.
Baja karbon rendah mempunyai sifat mekanis, yaitu:
1. Liat atau ulet (memiliki kekuatan tarik tinggi)
2. Cukup tangguh dan kuat (tidak mudah retak)
3. Mudah dibentuk
5. Kekuatan baik
Baja karbon rendah juga memiliki sifat yang tidak menguntungkan
dibandingkan dengan logam lainnya, seperti:
1. Kekuatan baik, tetapi massa besar.
2. Tidak tahan temperatur rendah.
3. Tidak tahan korosi, dll.
(Tata Surdia dan Saito Shinroku, 1999)
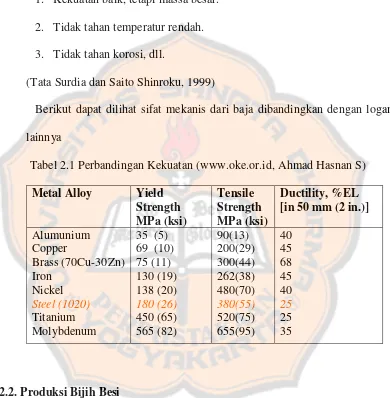
Berikut dapat dilihat sifat mekanis dari baja dibandingkan dengan logam
lainnya
Tabel 2.1 Perbandingan Kekuatan (www.oke.or.id, Ahmad Hasnan S)
Metal Alloy Yield
2.2. Produksi Bijih Besi
Bahan baku pembuatan baja adalah bijih besi. Bijih besi adalah bahan
tambang dengan sumber yang tak habis-habisnya dan bisa ditemukan hampir
diseluruh dunia. Tempat-tempat yang paling penting dimana bijih besi
2.2.1. Proses Pemurnian Bijih Besi
Bijih besi antara lain : Hematite (Fe2O3 - 70 % iron), Magnetite
(Fe3O4 - 72 % iron), Limonite (Fe2O3 + H2O - 50 % to 66 % iron) dan
Siderite(FeCO3- 48 % iron).
Proses pemurnian besi memiliki prinsip dasar yaitu menghilangkan
kandungan oksigen dalam bijih besi. Untuk memurnikan bijih besi kita
dapat melakukannya dengan cara dua cara, yaitu: cara tradisional
(blomery) dan dengan proses yang lebih moderen.
Cara tradisional : blomery, pada proses ini bijih besi dibakar
dengan charcoal, dimana banyak mengandung carbon sehingga terjadi
pengikatan oksigen, pembakaran tersebut menghasilkan karbondiokasida
dan karbon monoksida yang terlepas ke udara, sehingga besi murni
didapat dan dikeluarkan dari dapur, kekurangnya tidak semua besi dapat
melebur sehingga terbentuk spoge (spoge berisi besi dan silica).
Proses lebih modern adalah dengan blast furnace. Blast furnace
diisi oleh bijih besi, charcoal atau coke (coke adalah charcoal yang
terbuat dari coal) dan limestone (CaCO3). Angin secara kencang dan
kontinu ditiupkan dari bawah dapur. Hasil peleburan besi akan berada di
bawah. Cairan besi yang keluar ditampung dan disebut denganpig iron.
Bahan baku pembuatan baja adalah bijih besi, dan diperlukan
bahan bakar, bahan tambah, dan juga oksigen. Bahan-bahan tersebut
diperlukan untuk proses pembuatan baja baik menggunakan dapur
maupun konverter.
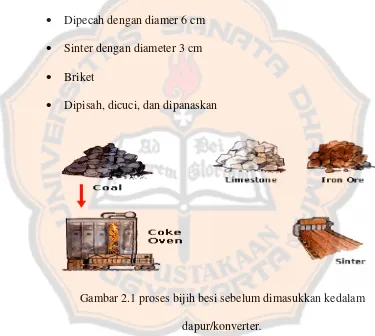
Sebelum bijih besi dimasukkan kedalam dupur atau konverter, maka
pertama kali bijih besi dibentuk dengan cara:
Dipecah dengan diamer 6 cm
Sinter dengan diameter 3 cm
Briket
Dipisah, dicuci, dan dipanaskan
Gambar 2.1 proses bijih besi sebelum dimasukkan kedalam
dapur/konverter.
Kemudian bahan bakar bisa berupa: kokas (mengandung P dan S,
nilai kalor tinggi), atau Arang kayu (tidak mengandung P dan S, nilai
kalor rendah) setelah itu udara (oksigen).
Pada persiapan berikutnnya untuk memproses pembuatan baja
dolomit. Fungsi dari bahan tambah adalah untuk mengikat kotoran (P
dan S) sekaligus untuk menurunkan titik lebur bijih besi.
Bahan terakhir yang dibutuhkan dalam proses pembuatan baja
adalah oksigen, dimana berfungsi untuk menaikkan suhu yang
dipergunakan untuk meleburkan bijih besi dengan cara menaikkan
tekanan pada dapur maupun konverter.
2.2.3 Proses Pengolahan Baja
Seperti yang ditulis diatas, pengolahan baja dapat menggunakan
dapur maupun konverter. Masing-masing penggunaan baik itu dapur
atau konverter untuk mengolah bijih besi menjadi baja mempunyai
keunggulan serta hasil yang berbeda-beda.
Dapur sendiri bermacam-macam begitupula dengan konverter.
Jenis dapur yang sering digunakan untuk mengolah bijih besi menjadi
baja diantaranya: dapur Tinggi, dapur Siemen martin, dapur induksi,
dapur duplex dan lain-lain. Begitu juga dengan konverter, terdapat:
konverter Thomas, konverter Bessemer dan lain-lain. Disini penulis
hanya menjelaskan sedikit mengenai dapur tinggi dan konverter Thomas.
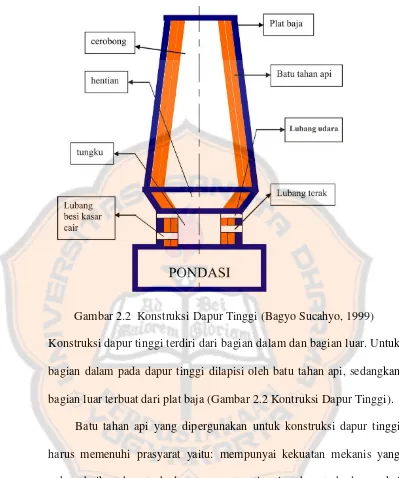
Pada dapur tinggi dapat dilihat bentuk konstruksinya pada gambar
Gambar 2.2 Konstruksi Dapur Tinggi (Bagyo Sucahyo, 1999)
Konstruksi dapur tinggi terdiri dari bagian dalam dan bagian luar. Untuk
bagian dalam pada dapur tinggi dilapisi oleh batu tahan api, sedangkan
bagian luar terbuat dari plat baja (Gambar 2.2 Kontruksi Dapur Tinggi).
Batu tahan api yang dipergunakan untuk konstruksi dapur tinggi
harus memenuhi prasyarat yaitu: mempunyai kekuatan mekanis yang
cukup baik, tahan terhadap temperatur tinggi, tahan terhadap reaksi
kimia yang terjadi pada dapur tinggi, mempunyai angka pemuaian yang
rendah, dan porous (berpori).
Proses pengolahan baja pada dapur tinggi dapat dilihat pada
Gambar 2.3 Diagram Alir Proses Dapur Tinggi (Bagyo Sucahyo, 2003)
Proses pengolahan bijih besi menjadi baja akan menghasilkan
terak, besi kasar kelabu, besi tuang dan gas buang. Terak biasa juga
digunakan untuk bahan pembuat semen dan juga pupuk. Besi kasar cair
(mengandung 1,7 – 2,3% C) yang dihasilkan oleh dapur tinggi berupa
besi kasar putih (kadar Si tinggi) dapat dituang dan besi kasar kelabu
(kadar Si rendah) mempunyai kekuatan tarik rendah. Gas buang
dialirkan ke pemanas udara untuk disaring (Gambar 2.3 Diagram Alir
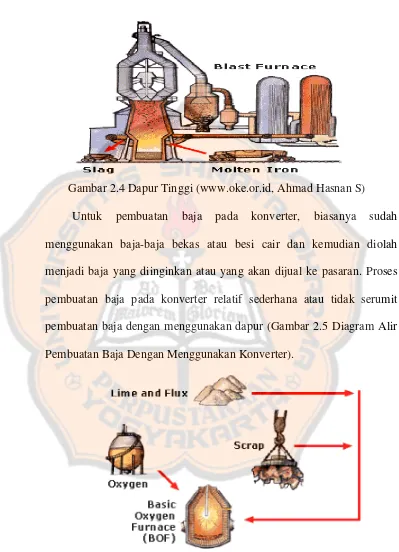
Gambar 2.4 Dapur Tinggi (www.oke.or.id, Ahmad Hasnan S)
Untuk pembuatan baja pada konverter, biasanya sudah
menggunakan baja-baja bekas atau besi cair dan kemudian diolah
menjadi baja yang diinginkan atau yang akan dijual ke pasaran. Proses
pembuatan baja pada konverter relatif sederhana atau tidak serumit
pembuatan baja dengan menggunakan dapur (Gambar 2.5 Diagram Alir
Pembuatan Baja Dengan Menggunakan Konverter).
Gambar 2.5 Diagram Alir Pembuatan Baja Dengan Menggunakan
Gambar 2.6 Proses Pembuatan Baja Setelah Melalui Konverter
Adapun tujuan dari proses pembuatan baja dengan konverter
adalah mencairkan kembali besi bekas dan mengubah besi cair kasar
menjadi baja. Sehingga dalam praktek pembuatan baja menggunakan
konverter dilapangan sangat jarang atau bahkan tidak pernah sama sekali
mencairkan biji besi menjadi baja. Akan tetapi proses setelah melalui
dapur tinggi untuk menjadi baja dalam bentuk cairan besi kasar
seringkali diproses didalam konverter.
Untuk konverter Thomas, bentuk dan cara kerja sama dengan
konverter siemen Bessemer menggunakan batu tahan api yang bersifat
basa (dolomit). Tidak untuk mengolah besi kasar yang mengandung Si
(0,3% - 0,8%) karena akan bereaksi dengan batu tahan api. Sebagai
pengganti Si, dengan unsur P (1,7% – 2%) dan Mn (1% – 2 %).
Proses pada konverter Thomas dimulai dari memasukkan bahan
tambah, besi kasar putih kemudian dihembuskan udara. Pada saat
naik dan terbentuk terak basa. Unsur phospor belum terpisah dengan Fe.
Proses selanjutnya pembakaran karbon, suhu turun. Setelah suhu turun
terjadi oksidasi Phospor terhadap Fe, saat terjadi oksidasi suhu kembali
naik. Hasilnya berupa baja dengan kadar 0,005 – 0,5% C, untuk baja
profil dan baja tuang (Bagyo Sucahyo, 1999).
2.3. Elektroplating
Elektroplating didefinisikan sebagai perpindahan ion logam dengan
bantuan arus listrik melalui elektrolit sehingga ion logam mengendap pada
benda padat konduktif membentuk lapisan logam. Ion logam dapat diperoleh
dari elektrolit maupun berasal dari pelarutan anoda logam ke dalam
elektrolit. Pengendapan terjadi pada benda kerja yang berlaku sebagai
katoda. Lapisan logam yang mengendap disebut juga sebagai deposit. Dalam
pembahasan selanjutnya digunakan istilah plating atau lapis listrik atau
pelapisan logam yang maksudnya adalah elektroplating.
Ion merupakan atom atau molekul bermuatan listrik positif atau
negatif. Atom atau molekul bermuatan positif bila mempunyai proton lebih
besar daripada electron. Suatu ion logam atau molekul bermuatan positif bila
melepas electron disebut kation. Muatan negatif diperoleh bila suatu atom
atau molekul menerima electron disebut anion.
Atom merupakan bagian terkecil suatu unsur, terdiri dari inti berupa
proton dan neutron yang dikelilingi oleh electron. Bila jumlah proton sama
Elektron adalah bagian dari suatu atom yang mempunyai massa
sangat kecil dan bermuatan negatif. Proton merupakan partikel atom yang
menentukan massa atom dan bermuatan positif. Sedangkan neutron
merupakan partikel bermassa tetapi tidak bermuatan.
Arus listrik pada dasarnya adalah aliran elektron, yang dapat
mengalir dari satu atom ke atom yang lainnya. Bila arah arus selalu sama
setiap saat disebut sebagai arus searah (DC: direct current), dan bila terjadi
arah balik terhadap arah dasarnya disebut sebagai arus bolak-balik (AC:
alternating current). Arus yang dipakai pada electroplating adalah arus
searah. Sumber arus DC dapat diperoleh dari accumulator, batu baterai atau
dengan mengubah arus AC menjadi DC dengan menggunakan adaptor atau
rectifier.
Elektrolit merupakan larutan yang mengandung ion-ion sehingga
dapat menghantarkan arus listrik. Sebagai contoh elektrolit untuk plating
tembaga mengandung senyawa tembaga sulfat (CuSO4) yang terurai dalam
larutan yang membentuk ion positif Cu2+ dan ion negatif SO42. Untuk
memperbesar hantaran arus listrik ditambahkan asam sulfat (H2SO4) yang
terurai menjadi ion positif H3O+ (berasal dari H2O + H+ = H3O+) dan ion
negatif SO42-.
Apabila buah benda padat disambungkan dengan arus listrik dan
dicelupkan kedalam elektrolit, bagian yang tersambung dengan kotub positif
disebut anoda dan yang tersambung dengan kutub negatif disebut katoda.
Mn+
M0 Penghantar arus
Anoda
Bak plating
Larutan elektrolit Sumber arus
searah, DC
(+)
(-) Katoda larutan seperti anoda tembaga (Cu), nikel (Ni) dan anoda inaktif yang tidak
akan terionisasi seperti karbon (C).
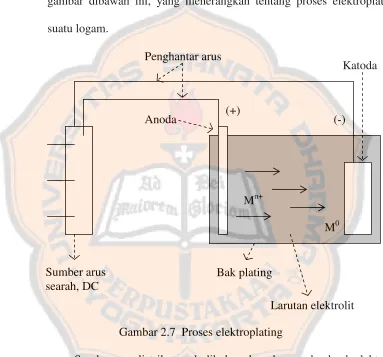
2.3.1. Prinsip Kerja Elektroplating
Prisip utama terjadinya proses elektroplating ditunjukkan pada
gambar dibawah ini, yang menerangkan tentang proses elektroplating
suatu logam.
Gambar 2.7 Proses elektroplating
Sumber arus listrik searah dihubungkan dengan dua buah elektroda
yaitu elektroda yang dihubungkan dengan kutub negatif disebut sebagai
katoda dan elektroda positif disebut anoda. Benda yang akan dilapisi
harus bersifat konduktif atau menghantarkan arus listrik dan berfungsi
anoda aktif digunakan anoda logam yang mempunyai kemurnian tinggi.
Arus mengalir dari anoda menuju katoda melalui elektrolit.
Proses pelapisan pada benda kerja dilakukan pada suatu elektrolit
yang mengandung senyawa logam. Untuk meningkatkan hantaran arus
dapat ditambahkan asam atau basa. Ion logam (Mn+) dalam elektrolit yang bermuata positif menuju benda kerja sebagai katoda yang
bermuatan negatif sehingga ion logam Mn+ akan tereduksi menjadi logam M dan mengendap di katoda membentuk lapisan logam (deposit),
menurut reaksi:
Mn++ ne Mo
Ion logam dalam elektrolit yang telah tereduksi dan menempel
dikatoda, posisinya akan diganti oleh anoda logam yang teroksidasi dan
larut dalam elektrolit atau dari penambahan larutan senyawa logam. Pada
anoda terjadi oksidasi menurut reaksi:
Mo Mn+ +ne
Apabila proses electroplating berjalan seimbang maka konsentrasi
akan tetap, anoda makin lama berkurang dan terjadi pengendapan logam
yang melapisi katoda sebagai benda kerja. Reaksi oksidasi-reduksi
secara keseluruhan dapat dituliskan sebagai berikut:
Anoda : Mo Mn++ ne Katoda : Mn++ ne Mo
Apabila plating menggunakan anoda inaktif maka logam yang
menempel pada katoda hanya berasal dari larutan, sehingga konsentrasi
larutan makin berkurang dan diperlukan kontrol yang ketat terhadap
konsentrasi larutan elektroplating untuk menjaga efisiensi proses dan
kualitas lapisan (gambar 2.7 proses elektroplating).
2.3.2. Efisiensi Plating
Efisiensi plating pada umumnya dinyatakan sebagai efisiensi arus
anoda maupun katoda. Efisiensi katoda yaitu arus yang digunakan untuk
pengendapan logam pada katoda dibandingkan dengan total arus masuk.
Arus yang tidak dipakai untuk pengendapan digunakan untuk penguraian
air membentuk gas hydrogen, hilang menjadi panas atau pengendapan
logam-logam lain sebagai impuritas yang tak diinginkan. Efisiensi anoda
yaitu perbandingan antara jumlah logam yang terlarut dalam elektrolit
disbanding dengan jumlah teoritis yang dapat larut menurut hokum
Faraday.
Kondisi plating yang baik bila diperoleh efisiensi katoda sama
dengan efisiensi anoda, sehingga konsentrasi larutan bila menggunakan
anoda aktif akan selalu tetap.
Efesiensi arus katoda sering dipakai sebagai pedoman menilai
apakah semua arus yang masuk digunakan untuk mengendapkan ion
logam pada katoda sehingga didapat efisiensi plating sebesar 100%
homogen dan elektrolis air merupakan beberapa penyebab rendahnya
efisiensi.
2.3.3. Fakto-Faktor Yang Berpengaruh Pada Plating
Kualitas hasil elektroplating maupun efisiensi arus sangat
dipengaruhi oleh variable proses sebagai berikut:
Konsentrasi elektrolit,
Larutan elektrolit terdiri dari komponen utama berupa senyawa
logam dalam bentuk garam terlarut dan asam atau basa. Senyawa
logam merupakan sumber logam yang menempel pada benda kerja.
Larutan asam atau basa dalam elektrolit berfungsi untuk
meningkatkan konduktifitas atau daya hantar listrik.
Konsentrasi elektrolit selama proses plating berlangsung akan
mengalami perubahan terutama penguapan dan berpindahnya ion
logam dari lrutan yang mengendap di katoda. Pada umumnya
kelebihan kadar logam menyebabkan menurunnya kekilapan dan
kerapatan lapisan, dan juga mengakibatkan terjadinya pemborosan
bahan. Apabila kadar logam rendah terjadi penurunan konduktifitas
sehingga proses plating menjadi lambat. Oleh karena itu konsentrasi
elektrolit perlu dijaga konstan dengan melakukan analisis larutan
secara teratur.
Sirkulasi elektrolit
Distribusi ion-ion didalam elektrolit seringkali tidak merata
terjadinya perpindahan ion logam positif yang mengendap,
sedangkan disekitar anoda seringkali terjadi kelebihan ion positif
yang berasal dari oksidasi logam.
Sirkulasi elektrolit bertujuan agar distribusi ion-ion baik positif
ataupun negatif didalam elektrolit menjadi merata sehingga dapat
dihindari terjadinya polarisasi. Polarisasi terjadi bila dua daerah
dalam elektrolit sangat positif dan yang lainnya sangat negatif
sehingga diperlukan tegangan yang lebih tinggi agar arus dapat
mengalir melalui elektrolit dari anoda ke katoda. Sirkulasi elektrolit
dapat dilakukan dengan bantuan pompa ataupun dengan hembusan
udara dari blower melalui pipa-pipa yang dipasang didasar tangki.
Rapat arus
Berdasarkan hukum Faraday, banyaknya endapan sebanding
dengan kuat arus. Akan tetapi dalam praktek, besaran yang
diperlukan untuk plating adalah rapat arus yaitu arus persatuan luas,
biasanya dinyatakan dalam Amper/dm2 (A/dm2) atau Amper/ft2 (A/ft2). Rapat arus antara anoda dan katoda besarnya berbeda dan rapat aruus katoda merupakan besaran yang perlu diperhatikan agar
kualitas endapan pada katoda berkualitas baik dan tidak sampai
terbakar.
Semakin besar rapat arus maka laju plating makin cepat dan
waktu yang diperlukan untuk memperoleh endapan dengan ketebalan
plating berjumlah banyak atau luasan benda besar maka diperlukan
arus yang besar dan kemudian diturunkan bila jumlah benda sedikit
atau luasan benda kecil. Rapat arus yang terlalu tinggi menyebabkan
terjadinya panas sehingga benda kerja yang diplating dapat terbakr
dengan ditandai warna yang menghitam.
Tegangan
Tegangan yang diperlukan untuk proses electroplating
tergantung dari jenis, komposisi dan kondisi elektrolit. Rapat arus
dapat dinaikkan dengan menaikan tegangan, akan tetapi hal ini dapat
menyebabkan terjadinya polarisasi dan tercapainya tegangan batas.
Pada keadaan tegangan batas, tidak terjadi aliran arus melalui
elektrolit, dan bila tegangan dinaikkan akan terjadi elektrolisis air
yang menghasilkan gas hydrogen dan oksigen. Tegangan batas dapat
dinaikkan dengan cara sirkulasi elektrolit, mempertinggi temperature
larutan dan memperbaiki konsentrasi elektrolit.
Jarak anoda-katoda
Jarak anoda-katoda menentukan hantaran arus listrik dan sangat
berpengaruh terhadap keseragaman tebal lapisan. Besarnya hantaran
berbanding terbalik dengan jarak. Apbila jarak anoda-katoda kecil,
hambatan menjadi kecil dan konduktivitas besar sehingga untuk
mendapatkan arus yang besar diperlukan tegangan yang lebih
Rasio dan bentuk anoda-katoda
Perbandingan permukaan anoda-katoda sangat penting untuk
menjaga agar ion-ion di dalam elektroplating selalu seimbang.
Standard rasio anoda-katoda tergantung dari jenis plating. Untuk
menjaga agar konsentrasi elektrolit selalu seimbang, misalnya saja
konsentrasi tembaga sulfat terhadap asam sulfat maka pada plating
tembaga harus dijaga agar perbandingan anoda tembaga terhadap
benda kerja selalu mendekati standard. Bila anoda lebih sedikit
dibanding katoda akan terjadi kekurangan ion tembaga di dalam
larutan dan endapan yang terbentuk menjadi lambat dan tidak
normal.
Distribusi arus
Lintasan arus dari anoda ke katoda tidak semuanya lurus tetapi
cenderung melengkung terutama yang berasal dari ujung anoda ke
ujung katoda. Keadaan ini menyebabkan rapat arus ke ujung-ujung
katoda menjadi lebih besar sehingga endapan yang terbentuk pada
bagian ujung cenderung lebih tebal. Itulah sebabnya apabila
melakukan plating batangan besi dengan tembaga ataupun silinder
dengan tembaga dan krom sering dihasilkan ujung-ujung silinder
cenderung lebih tebal dibandingkan pada bagian tengah.
Pada plating benda-benda yang rumit seringkali dihasilkan
pelapisan yang tak merata terutama pada daerah arus rendah (low
keadaan tersebut biasanya dipasang anoda sekunder sehingga dapat
diperoleh rapat arus yang seragam dan daerah yang sulit atau berarus
rendah dapat diperkuat dengan adanya anoda bantuan tersebut.
Sedangkan pada daerah dengan arus yang tinggi dapat dipasang
pemecah arus yang biasanya berupa plastik berbentuk sikat gigi.
Temperatur
Temperatur berpengaruh terhadap konduktivitas. Temperatur
semakin tinggi menyebabkan konduktivitas larutan makin besar
sehingga mempercepat hantaran arus listrik. Pada temperatur tinggi
dapat diperoleh rapat arus yang besar dan juga mempertinggi
tegangan batas polarisasi. Namun demikian setiap semua jenis
plating mempunyai rentang temperatur operasi optimum yang
berkaitan dengan sifat endapan logam pada benda kerja maupun sifat
dari aditif. Temperatur yang terlalu tinggi dapat menyebabkan
endapan terdapakar dan terjadi kerusakan aditif.
Daya tembus
Daya tembus didefinisikan sebagai kemampuan proses
elektroplating untuk menutup katoda dengan lapisan seseragam
mungkin, ditentukan oleh pengaturan geometri tanki dan berbagai
parameter proses termasuk juga jenis elektrolit. Letak geometri
katoda-anoda menentukan distribusi arus primer seperti yang telah
dibahas pada distribusi arus diatas. Daya tembus terutama sangat
Rapat arus yang besar cenderung membuat lapisan pada
ujung-ujung benda kerja menjadi lebih tebal karena mendapat rapat arus
yang lebih besar. Keadaan ini dapat diatasi dengan pemasangan
pemecah arus dari bahan-bahan isolator seperti plastic berbentuk
gerigi yang dipasang antara anoda dengan ujung benda kerja.
Edealnya pemasangan anoda-katoda tepat berhadap-hadapan pada
jarak yang sama, namun dalam praktek hal ini jarang dapat dilakukan
dan menyebabkan daya tembus tidak sama. Pengaruh lanjut dari daya
tembus adalah distribusi arus sekunder sebagai hasil antara distribusi
arus primer dan polarisasi.
Epitaxy dan leveling
Pengertian epitaxy adalah lapisan mengikuti bentuk dan
struktur benda kerja sebagai katoda, sehingga benda kerja yang kasar
menghasilkan lapisan kasar. Contoh dapat diamati bila benda yang
akan dilapis dengan krom permukaannya kasar dan berserat maka
hasil akhir pelapisan krom juga kasar dan berserat.
Leveling dimaksudkan bahwa lapisan meratakan bagian-bagian
benda kerja yang cekung, sehingga plating mempunyai
kecendrungan menutupi permukaan-permukaan benda yang cekung
menjadi rata. Epitaxy dapat dicegah dengan persiapan permukaan
benda kerja yang halus. Pembentukan leveling yang baik dapat
dilakukan dengan penambahan aditif pada plating tembaga akan
Aditif
Aditif merupakan zat tambahan dengan jumlah kecil
dimaksudkan untuk mengatur pertumbuhan kristal sehingga
diperoleh hasil plating dengan kualitas yang baik meliputi kecerahan
atau kekilapan (bright) dan kekerasan (hard). Pemberian aditif dapat
juga memperbaiki leveling. Aditif umumnya berupa senyawa organik
yang bekerja pada rentang temperatur tertentu dan dapat rusak
selama proses berlangsung. Oleh karena itu kontrol dan tambahan
aditif diperlukan bila terjadi penurunan kualitas hasil plating,
misalnya endapan tidak lagi cemerlang dan rapuh.
Kontaminan
Adanya padatang yang melayang-layang, tersuspensi maupun
terlarut dalam elektrolit dapat menyebabkan kontaminasi bagi
elektrolit yang berpengaruh pada kualitas hasil plating. Padatang
yang melayang-layang dapat pula ikut mengendap dikatoda sehingga
hasil plating pada benda kerja menjadi kasar. Adanya ion logam
yang tak dikehendaki dapat menyebabkan terjadinya noda-noda atau
bintik-bintik pada permukaan plating.
Elektrolit seringkali juga menjadi rusak karena adanya
kontaminan sehingga pengendapan pada katoda tidak dapat
berlangsung dengan sempurna. Kontaminan berupa padatan
tersuspensi juga akan mengganggu endapan logam pada benda kerja.
elektrolit, dan dapat pula berasal dari alat-alat untuk kerja maupun
benda kerja yang tidak dilakukan pembersihan dengan baik.
Kontaminan berupa partikel-partikel yang melayang maupun
tersuspensi dapat dihilangkan dengan cara filtrasi pada aliran
sirkulasi cairan yang dipasang sebelum pompa. Bila kontaminan
berupa ion-ion terlarut dalam air dilakukan pengolahan air sehingga
kandungan ion-ion logam menjadi sangat rendah. Penggunaan air
desrilasi atau air demineralisasi yang kandungan ion-ion sangat kecil
mencegah kontaminasi. Kontaminan bahan organik yang terjadi pada
saat proses dihilangkan secara oksidasi denga hidrogen peroksida
maupun secara filtrasi dan penukar ion. Sedangkan kontaminan
bahan organik dihilangkan denga melakukan dummy, yaitu
elektroplating menggunakan arus yang sangat rendah sehingga
ion-ion logam pengotor akan menempel pada katoda yang berbentuk plat
bergelombang.
2.4. Pelapisan Seng
2.4.1 Kegunaan dan Sifat-Sifat Seng
Banyak sekali bahan-bahan dari besi atau baja yang dilapisi dengan
dengan logam seng dengan berbagai tujuan, diantaranya adalah untuk:
Melindungi bahan dari koroasi
Memberikan penampilan yang lebih bagus dan menarik dari benda
dasarnya
Pelapisan seng dapat dilakukan dengan dua cara, yaitu:
1. Proses pencelupan panas atau lebih dikenal galvanizing.
Pada proses ini benda kerja dicelupkan dalam lelehan logam seng
(hot dipping), sehingga lapisan seng menempel padanya.
Barang-barang seperti atap rumah, ember logam, tangki, pagar jalan
tol, pagar trails, tiang listrik dilapisi seng melalui proses ini.
2. proses pencelupan dingin atau dikenal dengan elektrogalvanizing
atau zinc plating
benda kerja dimasukkan dalam larutan elektrolit yang
mengandung ion-ion seng dan alkali atau asam. Dengan bantuan arus
searah ion-ion seng tersebut direduksi menjadi logam seng dan
menempel pada benda kerja yang bertindak sebagai katoda. Logam
seng sebagai anoda melarut memberikan ion-ion seng ke dalam
larutan.
Cara ini lebih cocok untuk barang-barang teknik yang
memerlukan ketelitian dimensional misalnya ketebalan yang
seragam, dan lekuk-lekuk atau bagian-bagian kecil dari benda kerja
yang tidak boleh mengalami perubahan bentuk. Barang-barang yang
dibuat melalui proses plating misalnya mur baut, paku, komponen
sepeda dan motor, peralatan pertanian, klem-klem untuk jaringan
Hasil pelapisan seng berwarna putih kebiru-biruan, dan dapat
dijadikan warna lain seperti pelangi, hitam, kuning melalui proses
pewarnaan lanjut.
Sifat-sifat fisika seng:
logam yang berwarna putih kebiru-biruan
dapat ditempa dan di bengkokkan
penghantar listrik yang baik
berat atom = 65,38
densiti = 7,14 gr/cm3, (density air = 1 gr/cm3)
titik leleh = 419 ºC
titik didih = 909 ºC
konduktivitas listrik pada 0ºC = 0,1816 s/cm
sifat-sifat kimia seng:
seng mudah teroksidasi oleh oksigen dari udara dan terbentuk
lapisan tipis dari seng karbonat basa yang dapat melindungi seng
dari proses korosi lebih lanjut.
Zn + O2+ CO2+ H2O (ZnOH)2CO3
seng bersifat atmosfir, dapat bereaksi denga asam maupun basa,
membebaskan gas hidrogen.
Zn + H2SO4 ZnSO4+ H2
Zn + 2 NaOH NaZnO2+ H2
Seng dapat bereaksi langsung dengan belerang dan halogen
Zn + Cl2 ZnCl2
2.4.2 Peralatan Pelapisan Seng
Peralatan plating seng terdiri dari rectifier, bak plating, anoda seng
penghantar,dan dengan atau tanpa barrel, pompa serta filter.
Anoda berbentuk batangan atau lempengan dengan kemurnian
tinggi. Untuk menjaga kontaminasi larutan dari anoda, maka perlu
dibungkus denagan kain sehingga selama elektroplating kotoran dari
anoda tertahan pada kain tersebut.
Benda kerja yang kecil-kecil dimasukkan didalam tabung yang
berputar dengan kecepatan tertentu yang dimasukkan kedalam bak
plating sehingga lapisan merata. Perputaran tersebut sekaligus berfungsi
mengaduk-aduk larutan elektrolit sehingga lebih homogen.
Pompa serta filter hanya dipakai untuk plating seng menggunakan
elektrolit asam.
2.4.3. Komposisi Dan Kondisi Operasi
Larutan elektrolit yang digunakan untuk pelapisan seng ada tiga
macam yaitu larutan sianida, larutan basa dan larutan asam. Larutan
yang piling banyak digunakan industri yaitu larutan sianida dengan
komponen utamanya seng oksida (zinc oxcide), soda api (caustic soda)
dan sodium sianida (sodium cyanide).
Anoda seng (Zn) terlarut kedalam elektrolit, menggantikan ion
pelarutan logam Zn dari anoda dan pengendapan pada katoda melewati
elektrolit sebagai berikut:
Reaksi pelarutan anoda seng adalah:
Zn Zn2+ + 2e
Sedangkan pada katoda terjadi reaksi pengendapan sebagai:
Zn2++ 2e Znº
dan membentuk lapisan tipis pada benda kerja sebagai katoda.
Larutan elektroplating yang dipergunakan ada beberapa tipe, yaitu:
Laruatan sianida tinggi
Larutan sianida rendah
Larutan tanpa sianida
Larutan asam
Tabel 2.2. Komposisi dan kindisi operasi plating seng sianida tinggi
Komponen dan kondisi operasi
Larutan Sianida Tinggi
Seng oksida 35 g/L
Sodium sianida total 90 g/L
Sodium hidroksida total 50 g/L
pH >13
Temperatur ruangan
Rapat arus katoda 1-6 A/dm2
Rapat arus normal 1,5-2 A/dm2
Komponen dan kondisi operasi
Larutan Sianida Rendah
Seng oksida 7,5 g/L
Sodium sianida total 7,5 g/L Sodium hidroksida total 7,5 g/L
pH >13
Temperatur ruangan
Rapat arus katoda 1-6 A/dm2 Rapat arus normal 1,5-2 A/dm2
Efisiensi katoda 65-80%
Tabel 2.3. komposisi dan kondisi operasi plating seng (lanjut)
Komponen dan kondisi operasi Larutan Tanpa Sianida Tinggi Seng oksida 11 g/L
Sodium hidroksida total 120 g/L
pH >13
Temperatur ruangan
Rapat arus katoda 1-6 A/ft2
Komponen dan kondisi operasi Larutan Sianida Tinggi
Seng klorida 45 g/L
Ammonium klorida 225 g/L
Asam borat 45 g/L
pH 3-4
Temperatur ruangan
Rapat arus katoda 1-15 A/ft2 Rapat arus normal 1,5-2 A/ft2 Efisiensi katoda 95-100%
2.4.4. Fungsi Komponen Utama 1. Seng Oksida, zinc oxide (ZnO)
Fungsinya sebagai sumber utama ion seng yang akan membentuk
kompleks seng sebagai pengganti seng yang terlapis. Bila plating
berjalan dengan baik artinya jumlah seng yang melapisi katoda sama
dengan seng yang terlarut dari anoda maka tidak perlu dilakukan
penambahan senyawa seng oksida.
2. Sodium sianida, sodium cyanide (NaCN)
Sodium sianida membantu laju pelarutan anoda seng sehingga
konsentrasi larutan seng akan selalu terjaga konstan. Sodium sianida
dapat diganti dengan potasium sianida (potassium cynide, KCN).
Sodium hidroksida atau soda api dimaksudkan untuk meningkatkan
daya hantar listrik dan juga membantu laju pelarutan anoda seng.
4. Seng klorida, zinc chloride (ZnCl2)
Sebagai sumber ion seng yang akan melapisi katoda dalam larutan
seng asam.
5. Potasium atau amonium klorida, potassium chloride (KCL) /
ammonium chloride (NH4Cl)
Berfungsi untuk menaikkan daya hantar listrik dan membantu laju
pelarutan anoda dalam larutan seng asam.
6. Asam borat (Boric acid)
Berfungsi untuk mempertahankan keasaman larutan dan membantu
peningkatan daya hantar listrik.
2.4.5. Permasalahan dan Pemecahannya
Hasil akhir dari proses plating seng adalah kualitas lapisan yang
menempel pada benda kerja. Kualitas yang diharapkan meliputi
pelapisan dan ketebalan yang merata dan seragam, warna mengkilap dan
tidak terbentuk noda-noda pada benda kerja yang dilapis.permasalahan
operasi sering juga muncul dikarenakan kondisi larutan yang sudah tidak
memenuhi syarat, adanya kontaminan, dan bisa juga disebabkan oleh
sambungan-sambungan listrik yang kurang baik.
Penyimpangan-penyimpangan dari komposisi larutan, kondisi operasi yang tidak sesuai
menyebabkan adanya permasalahan operasi (trouble) yang berakibat
Pelapisan tidak merata
Pelapisan tidak merata terutama pada daerah pada daerah yang berlekuk
atau daerah dengan rapat arus rendah disebabkan daya tembus yang
kurang baik karena perbandingan antara seng oksida dan sodium sianida
tidak sesuai. Cek komposisi dan koreksi komposisi larutan sesuai
formula dengan menambahkan komponen penyusun elektrolit atau
pengenceran elektrolit.
Waktu pelapisan lama
Konsentrasi seng rendah menakibatkan pelapisan lambat. Demikian juga
konsentrasi sodium sianida maupun soda api rendah menyebabkan daya
hantar listrik kecil sehingga arus yang dihantarkan ke anoda rendah
menyebabkan waktu pelapisan lama. Tambahkan sianida dan soda api
sesuai dengan formula.
Deposit kasar
Larutan kotor dengan padatan yang melayang-layang biasanya ikut
mengendap dikatoda sehingga menyebabkan lapisan (deposit) menjadi
kasar. Saring larutan sehingga padatan yang melayang-layang dapat
dihilangkan dari larutan.
Ujung-ujung benda kerja terbakar
Daerah yang memperoleh rapat arus besar terutama pada ujung-ujung
benda kerja terbakar karena konsentrasi seng terlalu tinggi. Cek
komposisi larutan dan lakukan koreksi ke komposisi standard sesuai
steinless steel atau titanium. Kerapatan arus yang terlalu besar
mengakibatkan suplai arus yang berlebihan pada ujung-ujung benda,
sehingga menjadi terbakar.
Deposit kurang mengkilap
Kenampakan hasil pelapisan kurang mengkilap kerena kekurangan zat
aditif berupa brightener. Tambahan brightener sesuai dengan petunjuk
penggunaan. Penambahan yang berlebihan akan menyebabkan
kontaminasi larutan.
Noda-noda hitam pada deposit
Kontaminasi yang terdapat pada larutan elektrolit akan mengakibatkan
pengendapan pada katoda sehingga membentuk noda-noda pada benda
kerja. Kandungan besi dapat dicegah dengan menggunakan air distilat.
Apabila senyawa besi berasal dari korosi atau benda jatuh, selalu
dilakukan control pipa-pipa atau system kerja yang baik. Larutan yang
sudah terkontaminasi dapat dilakukan purifikasi.
Pengelupasan lapisan
Pembersihan permukaan benda yang kurang sempurna menyebabkan
penempelan lapisan seng kurang lekat dan mudah mengelupas. Lakukan
prosedur pembersihan dengan baik dan benar sehingga semua kerak,
kotoran, sisa-sisa minyak dan asam benar-benar hilang.
2.5.Korosi
Korosi (karat) gejala destruktif yang mempengaruhi semua logam.
Walaupun besi bukan logam pertama yang dimanfaatkan, tetapi besi paling
banyak digunakan dan paling awal menimbulkan korosi.
Pencegahan korosi atau karat sejak awal sampai sekarang, banyak
membebani peradaban manusia dikarenakan :
a. Biaya korosi sangat mahal, baik akibat korosi maupun pencegahannya.
b. Korosi sangat memboroskan sumber daya alam.
c. Korosi sangat membahayakan manusia, bahkan mendatangkan maut.
Definisi korosi adalah rusaknya suatu bahan atau menurunnya kualitas
bahan karena terjadi reaksi dengan lingkungan.
Kebanyakan proses korosi adalah melalui proses elektrokimia beberapa
secara kimiawi. Korosi terjadi pada logam, karena kebanyakan logam
ditemukan dialam dalam bentuk oksida atau logam cenderung kembali ke
keadaan pada saat ditemukan. Logam adalah konduktor listrik, sehingga
memungkinkan terjadi proses elektrokimia.
Plastik tidak ada kecenderungan kembali ke kondisi alam. Korosi pada
plastik terjadi karena reaksi dengan lingkungannya. Reaksi elektrokimia pada
korosi logam biasanya secara elektrokimia yaitu dari Anoda menuju Katoda.
Oksidasi adalah kehilangan elektron (terjadi di Anoda), sedangkan reduksi
2.5.1. Macam – Macam Korosi Yang Disebabkan Oleh Air Laut
Korosi dibedakan atau diklasifikasikan menurut penampakan
logam yang terkorosi, adapun macam – macam korosi adalah sebagai
berikut :
a. Korosi Merata
Adalah proses kimiawi atom elektrokimia berlangsung secara
diseluruh permukaan logam yang berhadapan dengan lingkungan
pengkorosi.
Korosi ini mudah dikontrol dengan cara coating, inhibitor
(memakai bahan kimia), proteksi katodik.
b. Korosi Pitting (kondisi pada air laut)
Adalah korosi dipermukaan benda kerja yang berbentuk
lubang – lubang karena sangat distruktif (bahaya), sulit dicek,
dapat menyebabkan runtuhnya konstruksi dengan tak terduga. Dan
untuk menghindari dipakai bahan – bahan yang tidak mempunyai
korosi pitting antara lain : baja tahan karat 304, baja tahan karat
316, tembaga, incoloy, besi tuang, kuningan, perunggu, titanium
dan masih banyak bahan yang tahan tehadap korosi pitting.
(Chamberlain J., Trethewey K.R., 1991)
2.5.2. Laju Korosi
Laju korosi untuk baja yang terendam dalam air maupun yang
a. Karbon dioksida.
Karbon dioksida sangat mudah larut dalam air dingin, dan
membentuk asam karbonat dengan pH 5,5 sampai 6.
b. Oksigen.
Oksigen akan meningkatkan efisiensi reaksi katoda dalam
kondisi – kondisi basa yang selalu dijumpai pada ketel – ketel baja.
Oksigen juga dapat menimbulkan sumuran atau peronggaan ketika
terlempar keluar dari air saat temperatur naik dan masuk kedalam
sistem.
c. Garam – garam magnesium dan kalsium.
Garam magnesium dan kalsium yang terlarut mengendap dari air
ketika menguap, membentuk selapis kerak pada permukaan
logam. Ketika kerak menebal, laju perpindahan panas menurun
sehingga efisiensi hilang dan mendatangkan resiko terjadinya
pelekukan atau distorsi serta terbentuknya endapan kerak kosong.
Mutu air juga merupakan peranan yang besar. Meningkatnya
laju aliran, khususnya ditempat terjadi olakan, juga meningkatkan
laju korosi.
Dalam air tawar, laju korosi sebesar 0,05 mm per tahun sudah
biasa, walaupun mungkin laju itu turun hingga 0,01 mm per tahun bila
endapan mengandung kapur sudah terbentuk. Dalam air laut laju korosi
rata – rata agaknya berada didaerah antara 0,1 – 0,15 mm per tahun
39
3. PENGAMATAN STRUKTUR MIKRO 4. PENGAMATAN STRUKTUR MAKRO
STUDI
PUSTAKA DATA HASIL PENGUJIAN
3.2. Bahan dan peralatan
Bahan yang digunakan dalam penelitian ini adalah plat baja karbon
rendah atau yang biasa digunakan pada lantai mobil tanpa motif.
Selain bahan, penelitian ini didukung dengan berbagai macam peralatan,
baik yang ada di laboratorium Universitas Sanata Dharma maupun yang
diluar Universitas Sanata Dharma seperti yang terlihat dibawah ini:
1. Alat penjepit/ ragum
2. Las karbit (sebagai alat pemotong)
3. Gergaji besi
4. Mesin milling
5. Peralatan elektroplating
6. Kamera digital
7. Pompa akuarium khusus buat air laut (satu set)
8. Akuaurium
9. Amplas waterproof (200, 500 & 1000) mesh
10. Mesin uji tarik (gambar terlampir)
11. Katalis
12. Resin
3.3. Pembuatan Benda Uji (Spesimen) 3.3.1. Uji Tarik
Untuk detail dimensi dari benda uji (spesimen) dibuat di
laboratorium proses produksi Universitas Sanata Dharma dengan
menggunakan mesin milling sesuai dengan dimensi di bawah ini:
Gambar 3.1 Benda Uji Tarik (spesimen)
B = 50 mm L = 250 mm A = 60 mm C = 20 mm
G = 50 mm W = 10 mm R = 8 mm
Adapun acuan pembuatan dimensi benda uji tarik, yaitu
menggunakan standarisasi ASTM A 370. Berikut merupakan tabel
satndarisasi ASTM A 370 (untuk benda uji plat). Seperti terlihat
pada gambar di bawah ini:
B A B
L
G
C
T
R
Gambar 3.2 standarisasi dimensi plat ASTM A370
Lembaran plat dibentuk sesuai dengan dimensi benda uji (spesimen)
seperti gambar diatas sebanyak 27 benda uji (spesimen). 3 benda uji
awal, 12 spesimen dilapisi seng dengan cara elektroplating, 12 benda
uji (spesimen) sisa tanpa dilapisi. Ke-27 benda uji (spesimen) ini
dibentuk mengacu pada standarisasi ASTM A370 untuk plat.
3.3.2. Pengamatan Struktur Mikro
Pembuatan benda uji mikro ini dilakukan di laboratorium logam
Universitas Sanata Dharma Yogyakarta. Bahan dipotong dengan
ukuran lebar ± 5 mm, dan panjang 20 mm. Total keseluruhan benda
uji mikro 16 spesimen, yaitu terdiri dari: 8 spesimen tanpa
3.3.3. Pengamatan Struktur Makro
Pengamatan struktur makro ini dengan cara pengambilan gambar
bentuk putus benda uji (setelah dilakuan pengujian tarik pada
spesimen) menggunakan kamera digital, sehingga didapat bentuk
patahan benda uji.
3.4. Bahan dan Pengujian 3.4.1. Uji Tarik
Pengujian tarik dimaksudkan untuk mendapatkan sifat mekanis
dari bahan yang kemudian dapat diketahui kekuatan maksimum
benda uji mengalami tarikan, dan regangan benda uji.
Adapun proses uji tarik sebagai berikut:
Mula-mula benda uji diukur menggunakan jangka sorong
(panjang benda uji, lebar benda uji, dan tebal benda uji)
Membuat tabel untuk mencatat data yang dihasilkan oleh
mesin uji tarik.
Benda uji dipasang pada penjepit atau “chuck” atas dan
bawah pada alat uji tarik. Penjepit bawah dinaikkan dan
diturunkan dengan kecepatan lambat, sehingga penjepit
benda uji dalam posisi yang tepat, diusahakan agar
kedudukan dari benda uji benar-benar vertikal, kemudian
Benda uji diberi beban tarik dengan kecepatan 10 mm/dtk
sehingga benda uji akan bertambah panjang dan sampai pada
saat benda uji tersebut akan putus. Putu yang diharapkan
berada pada bagian panjang ukur benda uji, apabila patah
terjadi di luar panjang ukur benda uji, pengujian tersebut
dinyatakan gagal. Apabila terjadi demikian maka pengujian
diulang dengan benda uji baru.
Data yang didapat kemudian dicatat selama pengujian tarik
(beban maksimum (Ft) dan pertambahan panjang (ΔL) )
dengan interval yang ditentukan.
Beban tarik maksimum dan Pertambahan panjang setelah
benda uji putus dicatat.
3.4.2. Pengamatan Struktur Mikro
Uji ini dimaksudkan untuk mendapatkan data kedalaman korosi.
Proses pengujian struktur mikro adalah sebagai berikut :
a) Permukaan benda uji yang telah dibentuk diamplas mulai dari
ukuran paling kasar sampai paling halus (200, 500 & 1000)
mesh.
b) Setelah benda uji rata dan halus, selanjutnya dipoles dengan
autosol dan digosok dengan kain sampai halus dan bekas
pengamplasan hilang sehingga permukaan benda uji mengkilap.
c) Pemotretan pertama dilakukan untuk kemudian diidentifikasi
d) Dilakukan pengetsaan dengan larutan NaOH pada permukaan
benda uji, kemudian diamkan selama 60 detik sambil
digoyang-goyang. Selanjutnya masukkan benda uji pada alkohol.
e) Permukaan benda uji yang dietsa NaOH dan alkohol akan
menunjukkan perubahan warna pada permukaan benda uji.
f) Permukaan yang telah dietsa diamati dibawah mikroskop logam
dan dilakukan pemotretan yang kedua, kemudian diidentifikasi.
3.4.3. Pengamatan Makro
Pada pengamatan struktur makro, yang dilakukan adalah
pemotretan rupa dari permukaan spesimen dengan menggunakan
kamera digital. Foto ini dimaksudkan untuk mewakili apa yang
terlihat oleh mata. Spesimen yang digunakan untuk uji makro ini
adalah spesimen dari hasil uji tarik.
3.4.4. Uji Berat
Pengujian ini dimaksudkan untuk mengetahui sifat bahan bila
mengalami korosi khusus untuk perubahan berat benda uji. Pada
benda uji dapat terlihat akan mengalami pertambahan berat atau
malah mengalami penurunan berat yang di akibatkan oleh korosi.
Pengujian berat ini dilakukan menggunakan timbangan digital
46 BAB IV
HASIL PENELITIAN DAN PEMBAHASAN
4.1. Hasil Uji Komposisi
Untuk hasil uji komposisi kimia, dilaksanakan di POLMAN Ceper
(Politeknik Manufaktur Ceper) Klaten - Jawa Tengah, dan hasil penelitian
uji komposisi kimia dapat dilihat pada halaman lampiran.
4.2. Pengujian Tarik
Dari data hasil pengujian tarik yang dilakukan dengan mesin uji tarik,
dihitung kekutan sekaligus regangan benda uji dengan rumus seperti di
bawah ini:
∆L : Pertambahan panjang (mm)
ε : Regangan (%)
Ft : Beban maksimum (kg)
t
: Kekuatan tarik (kg/mm2)
Tabel 4.1 Benda Uji Hasil Fabrikasi (tanpa elekroplating)
Tabel 4.2 Benda Uji Kontak Air Laut Selama 10 s/d 40 Hari Terelektroplating
Seng
1.1 1.58 9.52 15.04 50 665.80 12.5 44.26 0.25
1.2 1.58 9.53 15.06 50 683.50 14.6 45.39 0.29
1.3 1.58 9.95 15.72 50 670.80 12 42.67 0.24
Rata – rata 44.11 0.26
2.1 1.52 10.9 16.57 50 716.40 15.1 43.24 0.3
2.2 1.53 9.6 14.69 50 647.76 14.45 44.1 0.29
2.3 1.53 9.7 14.84 50 660.00 13.4 44.47 0.27
Rata – rata 43.94 0.29
3.1 1.53 9.7 14.84 50 634.50 12.7 42.75 0.25
3.2 1.53 10.51 16.08 50 725.50 14.2 45.12 0.28
3.3 1.58 10.4 16.43 50 701.50 12.3 42.69 0.25
Rata – rata 43.52 0.26
4.1 1.53 9.65 14.76 50 630.80 13.05 42.72 0.26
4.2 1.58 10.45 16.51 50 713.40 13.5 43.21 0.27
4.3 1.58 9.7 15.33 50 630.60 13.6 41.15 0.27
Gambar 4.1 Grafik Kekuatan Tarik Rata–rata Benda Uji Terelektroplating Seng
Gambar 4.2 Grafik Regangan Rata–rata Benda Uji Terelektroplating Seng
0.26 0.26
44.53 44.11 43.94 43.52 42.36
Tabel 4.3 Benda Uji Kontak Air Laut Selama 10 s/d 40 Hari Tanpa
1.1 1.58 10.45 16.51 50 693.2 12.4 41.98 0.25
1.2 1.58 9.97 15.75 50 672.8 13.75 42.71 0.28
1.3 1.58 9.9 15.64 50 649.6 13.9 41.53 0.28
Rata – rata 42.07 0.27
2.1 1.63 9.95 16.22 50 651.8 10.3 40.19 0.21
2.2 1.58 10.3 16.27 50 697.7 10.75 42.87 0.22
2.3 1.58 10.45 16.51 50 695.2 9.15 42.11 0.18
Rata – rata 41.72 0.20
3.1 1.54 10 15.40 50 651.2 8.6 42.29 0.17
3.2 1.58 9.51 15.03 50 675.8 10.5 44.98 0.21
3.3 1.68 10.4 17.47 50 622.9 9.7 35.65 0.19
Rata – rata 40.97 0.19
4.1 1.54 10.1 15.55 50 610.6 7.9 39.26 0.16
4.2 1.54 10.2 15.71 50 616.4 8.1 39.24 0.16
4.3 1.57 10.3 16.17 50 656.8 8.5 40.62 0.17
Gambar 4.3 Grafik Kekuatan Tarik Rata–rata Benda Uji Tanpa Terelektroplating
Gambar 4.4 Grafik Regangan Rata–rata Benda Uji Tanpa Terelektroplating
Gambar 4.5 Grafik Kekuatan Tarik Rata–rata Benda Uji
Gambar 4.6 Grafik Regangan Rata–rata Benda Uji
Keterangan:
a : benda uji fabrikasi
e : benda uji terelektroplating seng
te : benda uji tanpa terelektroplating
44.53 44.11
Pembahasan Uji Tarik:
Dari pengujian tarik yang dilakukan dilapangan, baik untuk baja yang
dilapisi seng dan baja yang tidak dilapisi mengalami penurunan tegangan
tarik yang tidak signifikan. Hasil regangan juga menunjukkan angka yang
tidak signifikan.
Perubahan mekanis yang tidak signifikan ini dikarenakan oleh waktu
benda uji kontak dengan air laut tidak terlalu memakan waktu yang lama.
Baja yang dilapisi dengan seng, memiliki angka kekuatan tarik yang
lebih tinggi dibandingkan dengan baja yang tidak dilapisi. Hal ini sekaligus
membuktikan bahwa baja yang dilapisi seng lebih tahan korosi
dibandingkan dengan baja yang tidak dilapisi.
Dari gambar 4.5 terlihat perbedaan kekuatan tarik baja karbon rendah
tanpa perlakuan maupun baja karbon rendah dengan perlakuan
elektroplating seng. Penurunan kekuatan tarik baja karbon rendah tanpa
perlakuan terkorosi 40 hari adalah sebesar 4,83 kg/mm2, sedangkan
penurunan kekuatan tarik baja karbon rendah terelektroplating seng terkorosi
40 hari adalah sebesar 2,17 kg/mm2. Hal ini disebabkan lapisan permukaan
kulit yang menipis, sehingga kekuatan permukaan kulit juga berkurang.
Regangan baja karbon rendah tanpa perlakuan terkorosi 40 hari sebesar
0,16%, sedangkan baja karbon rendah terelektroplating seng terkorosi 40
4.3. Pengamatan Struktur Mikro
Gambar 4.7 Benda Uji 3 (kontak air laut 30 hari)
tanpa perlakuan elektroplating
Pembahasan uji mikro
Berikut laju korosi melalui pengmatan struktur mikro (terlihat pada tabel
dibawah ini):
Tabel 4.4 Kedalaman Korosi
Benda Uji
Kedalaman Korosi
Tanpa Perlakuan (mm)
Kedalaman Korosi
Perlakuan Elektroplating seng
(mm)
1 -
-2 0,0023
-3 0,0034
4 0,0052 0,0021
Dari hasil uji mikro dengan perbesaran 50X pada gambar juga terlihat
bahwa korosi hanya masuk kedalam (laju korsi yang masuk ke bahan
terukur), tetapi tidak membentuk kristal yang baru.
Kedalaman korosi rata-rata baja karbon rendah tanpa perlakuan terkorosi
40 hari 0,0052 mm, sedangkan kedalaman korosi untuk baja dengan
perlakuan elektroplating seng terkorosi 40 hari 0,0021 mm. Data ini
sekaligus membuktikan bahawa baja karbon rendah dengan perlakuan
elektroplating seng lebih tahan korosi dibandingkan dengan baja karbon
rendah tanpa perlakuan.
4.4. Uji Berat
Berikut merupakan hasil timbang benda uji:
Tabel 4.5 Berat Benda Uji Tanpa Perlakuan Elektroplating
No 1.1 36,46 37,57 35,86
1.2 38,37 37,94 1.3 37,87 37,44
2.1 37,95 36,81 37,28
2.2 36,53 35,97
2.3 35,96 35,42
3.1 36,26 37,06 33,37
3.2 37,74 34,6
3.3 37,17 37,8
4.1 36,17 37,27 34,79
4.2 38,12 35,82
4.3 37,53 35,7
Tabel 4.6 Berat Benda Uji Dengan Perlakuan Elektroplating seng 1.1 37,8 35,5 37,75
1.2 33,65 33,6 1.3 35,05 34,96
2.1 33,82 35,18 33,79
2.2 38,12 38,05
2.3 33,61 33,58
3.1 33,86 36,64 35,5
3.2 38,03 36,3
3.3 38,04 37
4.1 35,83 35,55 35,07
4.2 35,41 35,13
4.3 35,4 35,2
Rata – rata 35,44 35,14 36,27 35,13
Apabila diolah menjadi penurunan berat rata-rata benda uji, dapat dilihat
pada tabel berikut:
Tabel 4.7 Penurunan berat benda uji
No
Benda uji
tanpa perlakuan (gr)
Benda uji
dengan perlakuan elektroplating (gr)
1 0,49 0,06
2 0,59 0,04
3 1,80 0,38
Pembahasan hasil uji berat
Pada benda uji terjadi penurunan berat baik itu benda uji terelektroplating
seng maupun tanpa perlakuan elektroplating. Hal tersebut membuktikan
bahwa benda uji mengalami abrasi yang disebabkan oleh air laut.
Dari tabel 4.7 Penurunan berat benda uji baja tanpa perlakuan terkorosi 40
hari sebesar 1,84 gram, sedangkan pada baja dengan perlakuan
elektroplating seng terkorosi 40 hari 0,41 gram. Data tersebut membuktikan
bahwa bahan karbon rendah dengan perlakuan elektroplating seng lebih
tahan terhadap penurunan berat bila dibandingkan dengan baja karbon
rendah tanpa perlakuan. Ini juga dapat diartikan bahwa baja karbon rendah
terelektroplating seng dapat meningkatkan ketahanan korosi.
4.5 Pengamatan Struktur Makro
Gambar uji makro setelah dilakukan pengujian tarik, dapat dilihat pada
gambar dibawah ini:
Gambar 4.9 benda uji (kontak air laut 10 hari) dengan perlakuan elektroplating
seng
Pembahasan Pengamatan Struktur Makro
Dari hasil uji makro dapat dilihat bentuk putus bahan setelah dilakukan uji
tarik dan kita dapat melihat bahwa terjadi korosi baik pada baja dengan
elektroplating seng, maupun baja tanpa perlakuan elektroplating.
Untuk korosi sendiri, benda uji tanpa perlakuan elektroplating lebih cepat
terjadi korosi, sedangkan benda uji dengan perlakuan elektroplating seng
58 BAB V PENUTUP 5.1. Kesimpulan
Setelah melakukan proses penelitian sifat fisis dan mekanis plat baja
karbon rendah dengan perlakuan elektroplating seng dan tanpa perlakuan
elektroplating kontak air laut selama 40 hari, penulis dapat menyimpulkan
beberapa hal:
1. Terjadi penurunan kekuatan tarik rata-rata sebesar 2,17 kg/mm2
atau
sebesar 0,049% pada baja terelektroplating seng. Benda uji tanpa
perlakuan mengalami penurunan kekuatan tarik rata-rata sebesar 4,83
kg/mm2
atau 0,11%.
2. Baja tanpa perlakuan elektroplating memiliki regangan rata-rata sebesar
0,16%, sedangkan baja dengan perlakuan elektroplating memiliki
regangan rata-rata sebesar 0,27%.
3. Kedalaman rata-rata korosi baja terelektroplating sebesar 0,0021 mm,
sedangkan baja karbon rendah tanpa perlakuan sebesar 0,0052 mm.
4. Penurunan berat rata-rata benda uji baja tanpa perlakuan sebesar 1,84 gram
atau sebesar 0,0057%. Untuk benda uji baja terelektroplating seng sebesar
0,41 gram atau 0,001%.
Pada pengamatan struktur makro dapat dilihat secara langsung bahwa baja
dengan perlakuan elektroplating seng lebih tahan korosi dibandingkan dengan
5.2. Saran
1. Untuk mendapatkan hasil yang maksimal, diperlukan kecermatan dalam
menggunakan sarana dan prasarana pendukung.
2. Dibutuhkan jangka waktu yang lebih lama melakukan penelitian untuk
mendapatkan hasil yang maksimal.
3. Pembuatan benda uji, harus dilakukan secermat mungkin, sehingga
dihasilkan data yang akurat.
Literatur dan studi pustaka sangat berguna untuk menambah referensi dan
60
DAFTAR PUSTAKA
Amanto, H. dan Daryanto, 1999, Ilmu Bahan, Bumi Aksara, Jakarta.
Chamberlain J. dan Trethewey K.R., 1991,Korosi: Untuk Mahasiswa Dan
Rekayasawan, Gramedia, Jakarta.
Hasnan, A.S., 2001, Mengenal Baja, www.oke.or.id, diakses tgl 12 Desember
2010.
Purwanto dan Huda, S., 2005,Teknologi Industri Elektroplating, BP UNDIP,
Semarang.
Surdia, T. dan Shinroku, S., 1999,Pengetahuan Bahan Teknik, Pradnya
Paramita, Jakarta.
Sucahyo, B., 1999,Ilmu Logam, PT. Tiga Serangkai Pustaka Mandiri,