POLA AKTIVITAS ENZIM LIGNOLITIK JAMUR TIRAM
(Pleurotus ostreatus) PADA MEDIA SLUDGE INDUSTRI KERTAS
ARIEF MUHAMMAD SIGIT
PROGRAM STUDI BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2008
ABSTRAK
ARIEF MUHAMMAD SIGIT. Pola Aktivitas Enzim Lignolitik Pleurotus
ostreatus pada
Media Sludge Industri Kertas. Dibimbing oleh
EMAN KUSTAMAN, TRI PANJI dan HAPPY WIDIASTUTI.
Sludge merupakan limbah padat terbesar dari industri kertas yang
jumlahnya melimpah dan belum dimanfaatkan secara optimal. Salah satu
alternatif yang dapat dilakukan dalam pemanfaatan limbah ialah dengan
menggunakan sludge sebagai media tumbuh jamur pelapuk putih (JPP).
Sludge
mempunyai kandungan karbon tinggi yang lebih sukar terdegradasi dibandingkan
dengan jenis polisakarida lainnya. Jamur tiram (Pleurotus ostreatus) merupakan
salah satu jenis JPP yang mampu merombak selulosa dan lignin. Kemampuan
tersebut tidak terlepas dari peran enzim ligninolitik yang dihasilkannya, yaitu
lakase (Lac), mangan peroksidase (MnP) dan lignin peroksidase (LiP). Penelitian
bertujuan mempelajari pola aktivitas enzim ligninolitik dua isolat jamur tiram,
jamur tiram Thailand (JTT) dan jamur tiram Bogor (JTB) pada media sludge dari
fase pembentukan miselia hingga fase setelah tubuh buah.
Media yang diuji, yaitu A) media serbuk gergaji tanpa suplemen, B) media
sludge tanpa suplemen, C) media campuran serbuk gergaji dan sludge dengan
perbandingan masing-masing 50% (v/v) tanpa suplemen, D) media serbuk gergaji
dengan tambahan suplemen, E) media sludge dengan tambahan suplemen,
F) media campuran serbuk gergaji dan sludge dengan perbandingan
masing-masing 50% (v/v) dengan tambahan suplemen. Hasil penelitian menunjukkan
bahwa aktivitas optimum LiP diperoleh dari JTT dalam media E yaitu sebesar
4,014 U/mL. Aktivitas optimum MnP diperoleh dari JTB dalam media E sebesar
4,394 U/mL. Aktivitas optimum lakase diperoleh dari JTT dalam media F sebesar
2,113 U/mL.
ABSTRACT
ARIEF MUHAMMAD SIGIT. The Pattern of Lignolytic Enzyme Activities of
Pleurotus ostreatus on the Sludge Media of Paper and Pulp Industry. Under the
direction of EMAN KUSTAMAN, TRI PANJI and HAPPY WIDIASTUTI
Sludge is the most produced solid waste from paper industries, abundantly
available and so far has not been managed optimally. As an alternative, to take
advantage from sludge, it can be used as grown media of oyster mushroom.
Sludge has a high content of carbon. that difficult to degrade compare to other
polysaccharide. Oyster mushroom (Pleurotus ostreatus), white-rot fungus, has the
ability to degrade cellulose and lignin. Species of the Pleurotus genus produced
three lignolytic enzymes −laccase (Lac), manganese-peroxidase (MnP), and lignin
peroxidase (LiP)− which have the capability to removed lignocellulose
preferentially. The aim of this study is to learn the pattern of lignolytic enzymes
activity, from both Thailand oyster mushroom (JTT) and Bogor oyster mushroom
(JTB), on sludge media from initiation of micellia until fruiting body phase.
The 6 types of media were tested: sawdust (A), sludge (B), a mixture of
sawdust and sludge with the proportion of 50 % each (v/v) (C), sawdust with
supplement (D), sludge with supplement (E), a mixture of sawdust and sludge
with the proportion of 50 % each (v/v) and with supplement (F). The results
showed that lignolytic enzymes activities reach optimum on first vegetatif phase.
The optimum activity of laccase reached 2,113 U/mL, this obtained from JTT that
grown in media F. The optimum activity of MnP reached 4,394 U/mL, this
obtained from JTB that grown in media E. The optimum activity of LiP reached
4,014 U/mL, this obtained from JTT that grown in media E.
POLA AKTIVITAS ENZIM LIGNOLITIK JAMUR TIRAM
(Pleurotus ostreatus) PADA MEDIA SLUDGE INDUSTRI KERTAS
ARIEF MUHAMMAD SIGIT
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Program Studi Biokimia
PROGRAM STUDI BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2008
Judul : Pola Aktivitas Enzim Lignolitik Jamur Tiram (Pleurotus ostreatus)
pada Media Sludge Industri Kertas
Nama : Arief Muhammad Sigit
NIM : G44103032
Disetujui
Komisi Pembimbing
Ir H Eman Kustaman
Ketua
Dr. Tri Panji
Dr. Happy Widiastuti
Anggota
Anggota
Diketahui
Dr. drh. Hasim, DEA
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
PRAKATA
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Esa karena
atas rahmat dan hidayah-Nya, penulis dapat menyelesaikan karya ilmiah ini.
Penelitian dilaksanakan di Laboratorium Balai Penelitian Bioteknologi
Perkebunan Indonesia (BPBPI). Tema yang dipilih dalam penelitian yang
dilaksanakan sejak bulan April 2007 ini adalah limbah padat sludge, dengan judul
Pola Aktivitas Enzim Lignolitik Jamur Tiram (Pleurotus ostreatus) pada Media
Sludge Industri Kertas.
Penulis mengucapkan terima kasih kepada Ir. H. Eman Kustaman, Dr. Tri
Panji dan Dr. Happy Widiastuti atas bimbingan dan saran-saran yang diberikan..
Di samping itu, penghargaan juga penulis sampaikan kepada peneliti dan seluruh
staf teknisi BPBPI yang telah membantu selama penelitian (Pak Yanto, Pak Mus,
Mbak Wulan, Mbak Ning, Mbak Irma, Mbak Iko, Mbak Urip, Ibu Ida, Mas Jefri,
Mas Ajit dan Devi) atas semua bantuannya. Ungkapan terima kasih juga
disampaikan kepada ayah, ibu, seluruh keluarga tercinta, serta teman-teman di lab
(Siska, Aried, Khairil dan Rio) yang telah memberikan saran dan dukungannya.
Kepada teman-teman seperjuangan (Erlank, Dika, Gilang, Willy dkk) terima kasih
atas kebersamaan, kehangatan dan kekompakannya.
Penulis menyadari penyusunan usulan penelitian ini tidak lepas dari
kesalahan dan kekurangan. Kritik dan saran yang membangun dari berbagai pihak
sangat diharapkan demi kesempurnaan pelaksanaan penelitian ini. Semoga karya
ilmiah ini bermanfaat bagi para pembaca dan bagi ilmu pengetahuan khususnya
bidang biokimia.
Bogor, Juli 2008
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 25 Oktober 1985 dari ayah
Untung Sugito dan ibu Sudjiati. Penulis merupakan anak ketiga dari empat
bersaudara. Tahun 2003 penulis lulus dari MA Darul Arqam Garut dan pada tahun
yang sama lulus seleksi masuk Institut Pertanian Bogor (IPB) melalui jalur
Undangan Seleksi Masuk IPB (USMI) pada Program Studi Biokimia, Fakultas
Matematika dan Ilmu Pengetahuan Alam.
Selama mengikuti perkuliahan, penulis pernah mengikuti kegiatan Praktik
Lapangan di Laboratorium Bioproses, Pusat Penelitian Bioteknologi-Lembaga
Ilmu Pengetahuan Indonesia (LIPI) Cibinong selama periode Juni sampai dengan
Agustus 2006 dengan judul Uji Sensitivitas Beberapa Galur Liar Dan Mutan
Monascus purpureus Dengan Antibiotik Higromisin B, Zeosin Dan Kanamisin.
Disamping itu penulis pernah aktif menjadi pengurus HIMPRO Kimia, Ikatan
Mahasiswa Kimia (IMASIKA) periode 2003/2004 dan Biokimia, Community of
DAFTAR ISI
Halaman
DAFTAR TABEL ... ix
DAFTAR GAMBAR ... ix
DAFTAR LAMPIRAN ... ..x
PENDAHULUAN ... 1
TINJAUAN PUSTAKA
Jamur Pelapuk Putih ... 1
Jamur Tiram (Pleurotus ostreatus) ... 2
Limbah Padat Sludge
Industri Kertas ... 2
Lignin ... 3
Enzim Yang Dihasilkan oleh Jamur Pelapuk Putih ... 4
BAHAN DAN METODE
Bahan dan Alat ... 7
Metode ... 7
HASIL DAN PEMBAHASAN
Pertumbuhan miselium jamur tiram ... 9
Aktivitas Enzim Lakase ... 9
Aktivitas Enzim Mangan Peroksidase ... 12
Aktivitas Enzim Lignin Peroksidase... 14
SIMPULAN DAN SARAN ... 16
DAFTAR PUSTAKA ... 16
DAFTAR TABEL
Halaman
1 Sifat kimia sludge industri kertas... 3
2 Enzim-enzim ligninolitik dan reaksi-reaksi utamanya... 4
3 Aktivitas MnP dan lakase pada sampel kompos selama siklus produksi jamur ... 5
DAFTAR GAMBAR
Halaman
1 Jamur tiram ... 2
2 Sludge industri kertas ... 3
3 Struktur lignin dan prekursornya ... 4
4 Struktur tiga jenis monolignol ... 4
5 Produktivitas lakase selama fermentasi padat menggunakan
Pycnoporussanguineus ... 5
6 Produksi MnP dengan waktu pemberian glukosa yang berbeda ... 6
7 Siklus katalitik lignin peroksidase ... 6
8 Aktivitas lignin peroksidase dari Phlebia radiata ... 7
9 Pertumbuhan miselium P.ostreatus pada media PDA ... 9
10 Pertumbuhan miselium P.ostreatus pada media biji sorgum ... 9
11 Pola aktivitas enzim lakase pada berbagai media yang diinokulasi JTT ... 10
12 Pola aktivitas enzim lakase pada berbagai media yang diinokulasi JTB ... 11
13 Pola aktivitas enzim MnP pada berbagai media yang diinokulasi JTT ... 13
14 Pola aktivitas enzim MnP pada berbagai media yang diinokulasi JTB ... 13
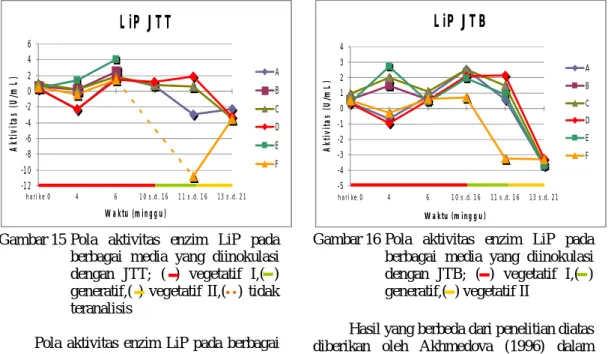
15 Pola aktivitas enzim LiP pada berbagai media yang diinokulasi JTT ... 15
DAFTAR LAMPIRAN
Halaman
1 Tahapan penelitian ... 20
2 Pembuatan media ... 21
3 Data enzim hari ke-0 ... 22
4 Data enzim empat minggu ... 23
5 Data enzim enam minggu ... 24
6 Data enzim fase primordia ... 25
7 Data enzim fase tubuh buah ... 26
1
PENDAHULUAN
Sludge merupakan limbah padat terbesar
dari industri kertas. Data Litbang PT KERTAS LECES menunjukkan bahwa saat ini produksi sludge mencapai 400 ton/hari. Limbah padat sludge jumlahnya melimpah dan sampai saat ini belum dimanfaatkan secara optimal sehingga dapat mencemari lingkungan. Pemanfaatan limbah padat organik tersebut diharapkan dapat menghasilkan nilai tambah sekaligus membantu pengelolaan lingkungan. Salah satu alternatif yang dapat dilakukan, yaitu dengan memanfaatkan sludge sebagai media tumbuh jamur pelapuk putih (JPP) untuk memperoleh enzim ligninolitik. Penggunaan enzim yang berasal dari mikroorganisme, pada masa yang akan datang, merupakan hal yang menjanjikan sebagai teknologi yang ramah lingkungan (Perez et al. 2002).
Limbah padat sludge mempunyai kandungan karbon tinggi. Senyawa karbon dalam sludge merupakan serat lignoselulosa, yang lebih sukar terdegradasi dibandingkan dengan jenis polisakarida lainnya (Reeves dan Schmidt 1994). Mikroorganisme yang paling berperan dalam proses degradasi lignin tersebut ialah jamur dari kelas Basidiomisetes. Jamur tiram (Pleurotus ostreatus) merupakan salah satu jenis jamur pelapuk putih (white rot
fungus) yang termasuk dalam kelompok
Basidiomisetes yang mampu merombak selulosa dan lignin.
Kemampuan jamur tiram dalam mendegradasi lignoselulosa tidak terlepas dari peran enzim ligninolitik yang dihasilkannya. Enzim ligninolitik terdiri atas lakase (benzenediol; oksigen reduktase, EC 1.10.3.2), mangan peroksidase (MnP, EC 1.11.1.13), dan lignin peroksidase (LiP, EC 1.11.1.14) (Gold dan Alic 1993). Biodelignifikasi dilakukan secara aerobik (Howard et al.. 2003) menggunakan enzim-enzim yang dihasilkan secara ekstraselular tersebut (Kirk dan Chang 1990, Dhouib et al. 2005). Sintesis dan sekresi enzim-enzim ini seringkali dipengaruhi oleh keterbatasan kadar karbon atau nitrogen. Produksi MnP dan LiP biasanya optimal pada waktu kandungan oksigen tinggi tetapi dapat ditekan oleh agitasi, sementara produksi lakase seringkali meningkat oleh agitasi, senyawaan aromatik dan pelarut organik (Dhouib et al. 2005).
Penambahan suplemen gipsum, kapur
dan dedak ke dalam media tumbuh jamur diperlukan untuk optimasi produksi enzim. Studi pustaka menunjukkan bahwa kapur
berfungsi mengontrol pH media tumbuh jamur agar sesuai dengan syarat tumbuh jamur. Kapur juga merupakan sumber kalsium. Gipsum berfungsi untuk mengokohkan media dan bahan penambah mineral (seperti kalsium dan sulfur). Dedak telah lama digunakan sebagai substrat alami dan dapat meningkatkan pertumbuhan miselium menjadi lebih tebal dan padat. Dedak memiliki kandungan karbon dan nitrogen yang tinggi (Yuniawati 2006). Dedak juga mengandung magnesium yang berfungsi mengaktifkan enzim, berperan dalam produksi energi formasi protein dan replikasi sel; dan mangan yang berperan pada beberapa enzim dan terlibat dalam metabolisme energi.
Isolat jamur tiram (P. ostreatus) yang digunakan dalam penelitian ini diuji kemampuannya untuk memproduksi enzim lakase, mangan peroksidase dan lignin peroksidase. Pola aktivitas ketiga enzim tersebut diamati mulai dari kolonisasi hingga perkembangan tubuh buah. Hasil penelitian yang dilaporkan Bonnen et al. (1994) menunjukkan bahwa pola aktivitas maksimum umumnya terlihat pada fase pembentukan koloni pada substrat dan menurun pada saat pembentukan tubuh buah, aktivitas enzim juga terlihat berbeda pada masing-masing periodenya. Oleh karena itu, penelitian ini bertujuan mempelajari pola aktivitas enzim ligninolitik dua isolat jamur tiram yang berasal dari taiwan (JTT) dan bogor (JTB) pada media sludge dari fase pembentukan miselia hingga fase setelah tubuh buah.
Hipotesis penelitian ini ialah aktivitas enzim akan mencapai optimum pada periode sebelum pembentukan tubuh buah. Penelitian diharapkan bermanfaat untuk mengetahui pola aktivitas enzim ligninolitik dari jamur tiram yang ditumbuhkan pada media sludge, sehingga diperoleh aktivitas enzim yang optimum pada periode yang tepat.
TINJAUAN PUSTAKA
Jamur Pelapuk Putih
Jamur pelapuk putih diketahui memiliki kemampuan unik yang secara efisien mendegradasi lignin menjadi CO2dan air, dan
meninggalkan warna putih dari selulosa (Cullen dan Kersten 1996). Hal ini dilakukan
sebagai upaya untuk memperoleh akses terhadap polimer-polimer karbohidrat yang terdapat pada dinding sel tanaman dan menggunakannya sekaligus sebagai sumber karbon dan energi. Jamur pelapuk kayu ini
2
biasanya tidak hanya membentuk koloni pada sampah hasil hutan dan pohon-pohon yang tumbang, tetapi juga pada pohon yang masih hidup (Eriksson et al. 1990 dalam Lankinen 2004).
Jamur pelapuk kayu sendiri dibagi menjadi jamur pelapuk putih, jamur pelapuk coklat dan jamur pendekomposisi sampah (Steffen 2003). Akan tetapi, satu-satunya jamur yang mampu secara efisien mendegradasi lignin ialah jamur pelapuk putih dari kelas basidiomikotina (Hatakka, 2001). Jamur Pelapuk Putih (JPP) dari kelas basidiomikotina, merupakan organisme yang bekerja efisien dan efektif dalam proses delignifikasi. Proses delignifikasi ini dimulai saat JPP menembus dan membentuk koloni dalam sel kayu lalu mengeluarkan enzim yang berdifusi melalui lumen dan dinding sel. Jamur ini menyerang komponen lignin dari kayu hingga menyisakan selulosa dan hemiselulosa yang tidak terlalu berpengaruh. Akibatnya, terjadi penurunan kekuatan fisik kayu dan pembengkakan jaringan kayu.
Hatakka et al. (1994 dalam Lankinen 2004) membagi jamur pembusuk kayu menjadi 3 kelompok berdasarkan pola enzim ligninolitik yang dihasilkannya: 1. jamur yang memproduksi LiP, MnP dan lakase, seperti
Phlebia Radiata
; 2. jamur yang memproduksi
MnP dan lakase, seperti Pleurotus ostreatus (Becker dan Sinitsyn 1993, Martínez et al. 1994, Giardina et al. 1996 dalam Lankinen 2004), Pleurotus eryngii (Martínez et al. 1996, Muñoz et al. 1997 dalam Lankinen 2004) and Dichomitus squalens (Eriksson et
al. 1990, Périé et al. 1996, 1998 dalam
Lankinen 2004); dan 3. jamur yang memproduksi LiP dan lakase.
Lignin modifying enzymes (LMEs)
diproduksi oleh jamur pelapuk putih selama proses metabolisme sekundernya berjalan, sementara oksidasi lignin tidak menyediakan energi yang cukup bagi jamur (Eggert et al. 1996 dalam Lankinen 2004). Proses sintesis dan sekresi enzim seringkali diinduksi oleh tingkat karbon atau nitrogen yang terbatas. Hal inilah yang mungkin menyebabkan JPP tergolong jamur yang sangat efisien dalam penggunaan nitrogen. Sebagai contoh kandungan nitrogen C. versicolcor saat ditumbuhkan pada media C:N dengan rasio 32:1 kira-kira sebesar 4%, namun saat ditumbuhkan pada media C:N rasio 1600:1 diperoleh 0,2% nitrogen. Hal ini menunjukkan dalam kondisi sedikit nitrogen, jamur lebih mengalokasikan nitrogen untuk memproduksi enzim ekstraselular dan komponen esensial
sel. Selain itu, jamur ini juga secara efisien mendaur ulang nitrogen di dalam miseliumnya (Deacon 2005).
Jamur Tiram (Pleurotus ostreatus)
Jamur tiram merupakan jamur kayu yang tumbuh berderet menyamping dan memiliki tubuh buah yang tumbuh mekar membentuk corong dangkal seperti kulit kerang (Djarijah 2001). Jamur tiram tumbuh secara alami di batang-batang kayu di hutan. Menurut sistematika, secara taksonomi jamur ini digolongkan dalam kelas Basidiomycetes, ordo Agaricales, famili Agaricaceae, dan genus Pleurotus (Pasaribu T et al. 2002). Jamur tiram (Pleurotus ostreatus) atau jamur tiram putih adalah jamur pangan dengan tudung berbentuk setengah lingkaran mirip cangkang tiram dengan bagian tengah agak cekung dan berwarna putih hingga krem. Jamur tiram masih satu kerabat dengan
Pleurotus eryngii atau King Oyster
Mushroom.
Gambar 1 Jamur tiram
Limbah Padat Sludge Industri Kertas
Limbah adalah bahan yang dihasilkan dalam suatu proses yang tidak berguna lagi untuk proses tersebut, yang bisa bersumber dari hasil aktivitas manusia maupun proses-proses alam dan atau belum mempunyai nilai ekonomi bahkan dapat mempunyai nilai ekonomi yang negatif. Limbah dibedakan menjadi tiga menurut bentuknya, yaitu limbah padat, cair, dan gas. Limbah padat merupakan salah satu bentuk limbah yang banyak terbuang ke lingkungan dan seringkali menimbulkan masalah bagi kehidupan manusia (Murtadho dan Said 1987).
Limbah padat sludge adalah contoh limbah hasil industri kertas yang banyak dibuang ke lingkungan. Limbah ini mengandung lignoselulosa yang merupakan hasil samping atau residu dari limbah hutan, industri pulp kertas, industri kayu, dan industri pertanian. Lignoselulosa sendiri merupakan bahan biopolimer dan komponen penyusun utama kayu dan tanaman bukan kayu yang berlimpah jumlahnya di alam.
3
Lignoselulosa merupakan komponen yang sukar terdegradasi dibandingkan dengan jenis polisakarida lainnya (Reeves dan Schmidt 1994).
Sludge industri kertas adalah limbah
dari proses berbahan baku kayu yang mengandung selulosa dan xylan sebagai penyusun dinding sel. Sludge industri kertas merupakan lumpur aktif yang diperoleh dari proses pengolahan air limbah, yang terdiri atas padatan 90% dan air 10%. Karakteristik dari
sludge industri kertas antara lain lembek,
strukturnya lunak seperti bubur, berwarna abu-abu keruh atau kehitaman, dan berbau tidak sedap. Sludge umumnya mengandung C/N yang tinggi. Tabel 1 menunjukkan karasteristik sludge industri kertas.
Limbah sludge juga dapat dijadikan sumber bahan organik alternatif. Hasil penelitian yang dilaporkan oleh Enny Widyati (2006) menunjukkan bahwa kompos sludge dapat meningkatkan pertumbuhan dan produktivitas tanaman dan jamur yang dibudidayakan. Sludge dapat dijadikan sumber bahan organik tanah (BOT) karena berasal dari proses industri yang menggunakan bahan baku kayu, sehingga sludge dapat menjadi sumber C bagi jamur.
Gambar 2 Sludge Industri Kertas Tabel 1 Sifat kimia sludge industri kertas
Variabel Nilai pH 8,75 C-organik 11,89 % N-total 1,00 % Mg 3,3 me/100 g K 2,65 me/100 g Fe 1,36 ppm Zn 0,88 ppm Cu 0,24 ppm Mn 1,64 ppm Sumber: (Widyati E 2006) Lignin
Lignin merupakan senyawa kompleks, tiga dimensi, polimer non-stereoregular yang disusun dari fenilpropanoid (Cullen dan Kersten 1996) dan merupakan bahan polimer alam terbanyak kedua setelah selulosa. Lignin
mengisi ruang-ruang kosong di antara selulosa, hemiselulosa dan komponen pektin di dalam dinding sel, dan secara kovalen terikat dengan hemiselulosa (en. wikipedia. org/ wiki/ Lignin 2007), selain juga berfungsi sebagai perekat atau penguat dinding sel. Lignin berperan sangat penting bagi tumbuhan sebagai sarana pengangkut air, nutrisi, dan metabolit dalam sel tumbuhan.
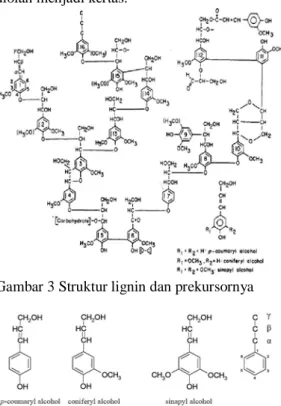
Lignin terbentuk dari gugus aromatik yang saling dihubungkan dengan rantai alifatik, terdiri atas 2-3 buah karbon, yang juga membentuk ikatan kovalen dengan polisakarida-polisakarida yang lain. Molekul lignin berikatan silang pada setiap molekul penyusunnya dengan jenis ikatan kimia yang berbeda. Unit fenil propana terikat satu sama lain dengan ikatan eter dan ikatan C-C, dengan persentasi ikatan eter lebih banyak. Gambar 3 memperlihatkan struktur lignin.
Tautan silang polimer lignin dengan komponen dinding sel yang lain memperkecil akses selulosa dan hemiselulosa terhadap enzim mikrobial, sehingga mereduksi kemampuan cerna enzim mikrobial tersebut. Oleh karena itu, lignin diduga mampu membantu menaikkan pertahanan tumbuhan melawan patogen dan hama. Contoh ini dapat dilihat pada banyak tersimpannya lignin dekat lokasi infeksi yang disebabkan oleh jamur.
Biosintesis lignin melibatkan polimerisasi radikal-radikal bebas yang merupakan prekursornya, dikenal juga sebagai monolignol. Tiga jenis monolignol yang utama (Gambar 4), yaitu koniferil alkohol, sinapil alkohol dan parakoumaril alkohol (sejumlah monolignol yang lain juga ada pada tumbuhan khusus atau dalam konsentrasi yang rendah). Proses ini diawali dengan sintesis monolignol, dengan bahan dasarnya ialah asam amino fenilalanin. Reaksi pertama berjalan bersamaan dengan jalur fenilpropanoid dan monolignol dianggap sebagai bagian dari kelompok ini. Tumbuhan yang berbeda menggunakan monolignol yang berbeda. Dikotiledonik lignin adalah campuran dari koniferil alkohol dan sinapil alkohol, dan monokotiledonik lignin adalah campuran dari tiga monolignol.
Monolignol disintesis di sitosol sebagai glukosida. Glukosa lalu ditambahkan ke monolignol agar dapat larut dalam air dan mengurangi sifat toksiknya. Glukosida lalu diangkut melalui sel membran ke apoplas, kemudian glukosa dihilangkan dan monolignol dipolimerisasi membentuk lignin (en. wikipedia. org/ wiki/ Lignin 2007). Polimerisasi dikatalisis oleh enzim oksidatif
4
membentuk radikal-radikal monolignol yang selanjutnya akan bergabung membentuk polimer lignin (en. wikipedia. org/ wiki/ Lignin 2007).
Kayu dengan kandungan lignin yang tinggi, bersifat tahan lama dan merupakan bahan baku yang baik bagi industri furnitur karena lignin menghasilkan lebih banyak energi saat dibakar dibanding selulosa. Namun pada industri kertas, lignin dalam kandungan tinggi membuat pulp menjadi kaku dan kekuatannya rendah sehingga lignin harus dihilangkan dari pulp terlebih dahulu sebelum diolah menjadi kertas.
Gambar 3 Struktur lignin dan prekursornya
Gambar 4 Struktur tiga jenis monolignol pada molekul lignin
Enzim yang Dihasilkan oleh Jamur Pelapuk Putih
Enzim adalah suatu biokatalisator yang sangat efektif untuk mempercepat perubahan kimia (Koolman dan Rohm 2000). Kerja kebanyakan enzim sangat spesifik terkait dengan tipe reaksi dan jenis reaktan yang dikatalisis oleh enzim. Pelczar et al. (1988) menggolongkan enzim dalam dua tipe utama yaitu enzim intraselular dan ekstraselular. Enzim intraselular berperan dalam mensintesis bahan-bahan selular dan menjalankan proses metabolisme untuk menyediakan energi bagi sel. Enzim ekstraselular berfungsi merubah nutrien yang terdapat di sekitarnya sehingga memungkinkan nutrien tersebut untuk memasuki sel.
Degradasi lignin adalah langkah yang sangat penting dalam siklus karbon (Cohen 2001), yang dimediasi oleh enzim oksidatif. Jamur pelapuk putih yang hidup pada bahan organik lignoselulosa mengeluarkan enzim ekstraselular yang bisa mendegradasi bahan tersebut sebagai nutrisinya, terutama lignin, sehingga disebut enzim ligninolitik. Sistem degradasi lignin pada jamur pelapuk putih melibatkan kerja enzim ekstraseluler yang diproduksi sendiri oleh jamur tersebut. Ada tiga jenis enzim ekstraseluler yang diproduksi oleh jamur pelapuk putih yang bersifat tidak selektif namun efektif dalam menyerang lignin. Enzim-enzim tersebut ialah lignin peroksidase (LiP), mangan peroksidase (MnP) dan lakase (Lac) (Howard et al.. 2003, Kirk et
al.. 1987) dan dikenal sebagai lignin modifying enzymes (LMEs). Jamur pelapuk
putih tidak bisa menggunakan lignin sebagai sumber energinya, sehingga proses degradasi tersebut diduga sebagai suatu cara agar selulosa yang terdapat didinding sel dapat diakses oleh JPP. Tabel 2 meringkas enzim ligninolitik, substrat serta reaksi-reaksinya. Tabel 2 Enzim-enzim ligninolitik dan reaksi-
reaksi utamanya Enzim Kofaktor Substrat,
perantara Reaksi Lignin peroksidase, LiP H2O2 Veratril alkohol Cincin aromatik dioksidasi menjadi radikal kation Mangan peroksidase, MnP H2O2 Mn, asam organik sebagai pengkelat Tiol,asam lemak tidak jenuh Mn(II) dioksidasi menjadi Mn(III); Mn(III) teroksidasi dikelat oleh senyawa fenolik menjadi radikal-radikal fenoksil; reaksi lainnya terjadi dengan adanya senyawa tambahan Versatil peroksidase, VP H2O2 Mn, veratril alcohol, Senyawaan yang sama untuk LiP dan MnP Mn(II) dioksidasi menjadi Mn(III), oksidati dari senyawa fenolik dan non-fenolik , dan dyes Lakase O2 Senyawa-aenyawa fenol; Senyawa-senyawa perantara, contoh: hidroksibenzot riazol atau ABTS Fenol dioksidasi menjadi radikal-radikal fenoksil; reaksi-reaksi lainnya terjadi dengan adanya perantara Glioksal oksidase, GLOX Glioksal, metil glioksal Glioksal dioksidasi menjadi asam glioksal; produksi H2O2 Aril alkohol oksidase, AAO Alkohol-alkohol aromatik (anisil, veratril alkohol) Alkohol-alkohol aromatik dioksidasi menjadi aldehid; produksi H2O2
Enzim lain yang memproduksiH2 O2 Kebanyakan senyawa organik O2 direduksi menjadi H2O2 Sumber: (Hatakka 2001)
5
Lakase
Enzim lakase (EC 1.10.3.2) merupakan enzim yang banyak mengandung tembaga oksidase dan mempunyai kemampuan untuk mengoksidasi senyawaan fenol. Lakase mengkonversi senyawaan fenol menjadi kuinin radikal dengan bantuan oksigen dan kemudian mengubahnya menjadi kuinon. Proses konversi ini juga menghasilkan beberapa substrat sampingan yang bermanfaat dalam proses degradasi. Lakase selain berperan dalam degradasi lignin (Hattaka 1994), juga berperan dalam proses pigmentasi, pembentukan badan buah, dan sporulasi pada JPP (Thurston 1994). Reaksi enzimatik pada lakase merupakan reaksi oksidasi yang menghasilkan satu elektron hasil oksidasi senyawa fenol dan mereduksi oksigen menjadi air (www. enzymeindia. com/ enzymes/ laccase. asp 2007).
Lakase banyak digunakan sebagai subjek penelitian dikarenakan lakase memiliki sifat spesifik yang rendah terhadap substrat-substratnya (Cavallazzi, et al.. 2004; Thurston, 1994). Hidrokuinin, katekol, guaiakol, 2,6-dimetoksifenol, p-fenildiamin dan siringaldazin merupakan substrat-substrat yang cukup bagus bagi lakase. Substrat kehilangan satu elektronnya dan biasanya terbentuk radikal fenoksi bebas (Thurston 1994) yang berperan sebagai intermediet. Elektron yang diambil oleh lakase, pada akhirnya akan ditransfer kembali ke oksigen untuk membentuk air (McGuirl dan Dooley 1999, Wong dan Yu 1999 dalam Couto dan Toca-Herrera 2006). Substrat tiruan lakase seperti ABTS (2,2`-azinobis-3-etilbenzthiazolin-6-sulfonat) dapat berperan sebagai mediator yang memungkinkan oksidasi komponen non-fenolik pada lignin yang tidak dapat dioksidasi oleh lakase sendiri (Bourbonnais dan Paice, 1990).
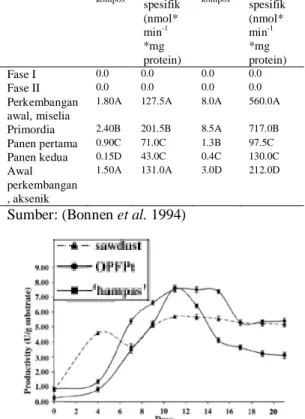
Bonnen et al. (1994) melakukan penelitian pendahuluan yang bertujuan mengetahui aktivitas lakase dan MnP selama siklus produksi jamur (Tabel 3). Bonnen melaporkan terjadinya peningkatan aktivitas enzim pada saat pembentukan miselia, baik pada lakase maupun MnP. Aktivitas ini mencapai maksimum pada saat perkembangan primordia jamur, dan mulai menurun aktivitasnya pada pembentukan tubuh buah.
Vikineswary et al. (2005) selanjutnya juga melaporkan hasil penelitiannya yang berkaitan dengan produktivitas lakase menggunakan Pycnoporus sanguineus.
Produktivitas lakase, terlihat pada Gambar 5, meningkat dengan cepat hingga aktivitas
maksimumnya tercapai setelah 11 hari fermentasi. Setelah itu, produktivitas lakase mulai menurun dengan cepat sampai akhir fermentasi selama 21 hari. Hanya fermentasi dengan OPFPt saja yang terlihat berlanjut dari hari ke-11 hingga hari ke-15. Apabila dilihat dari kolonisasi jamur terhadap media yang selesai dalam 11 hari fermentasi, terlihat bahwa produksi lakase terjadi pada awal pertumbuhannya.
Pemanfaatan lakase sangat luas diterapkan dalam berbagai bidang antara lain dalam proses bioremendiasi dan biodegradasi polutan organik pada tanah seperti klorofenol, dan polisiklik aromatik hidrikarbon, pada proses dekolorinasi dan detoksifikasi pada pewarna tekstil serta digunakan sebagai
bleaching pada proses biodeglinifikasi pada
pulp industri kertas.
Tabel 3 Aktivitas MnP dan lakase pada sampel kompos selama siklus produksi jamur. Sampel Kompos MnP Lakase U*g -1 kompos Akt spesifik (nmol* min-1 *mg protein) U*g -1 kompos Akt spesifik (nmol* min-1 *mg protein) Fase I 0.0 0.0 0.0 0.0 Fase II 0.0 0.0 0.0 0.0 Perkembangan awal, miselia
1.80A 127.5A 8.0A 560.0A
Primordia 2.40B 201.5B 8.5A 717.0B Panen pertama 0.90C 71.0C 1.3B 97.5C Panen kedua 0.15D 43.0C 0.4C 130.0C Awal perkembangan , aksenik 1.50A 131.0A 3.0D 212.0D
Sumber: (Bonnen et al. 1994)
Gambar 5 Produktivitas lakase dengan beragam substrat dari Pyc sanguineus.
Mangan Peroksidase
Enzim mangan peroksidase (MnP) (EC 1.11.1.13) juga merupakan enzim yang mengandung gugus heme peroksidase dan
6
menggunakan H2O2 untuk mengkatalisis
oksidasi dari Mn²+ ke Mn³+, proses ini selanjutnya mengoksidasi kembali substrat fenol. Aktifitas MnP dirangsang oleh asam organik yang berfungsi sebagai pengkelat atau penstabil Mn3+. Mekanisme reaksinya, pada keadaan awal mangan peroksidase dioksidasi oleh H2O2 membentuk MnP-senyawa I yang
dapat direduksi oleh Mn2+ dan senyawa fenol membentuk MnP-senyawa II.
Senyawa tersebut kemudian direduksi kembali oleh Mn2+, tetapi tidak oleh fenol, membentuk enzim keadaan awal dan produk (Wariish et al.. 1989). Adanya Mn2+ bebas sangat penting untuk menghasilkan siklus katalitik yang sempurna. MnP mampu mengoksidasi komponen fenolik dan non fenolik senyawa lignin, akan tetapi tidak mampu mengoksidasi unsur dengan potensial redoks yang tinggi, walaupun memiliki kerja yang sama dengan LiP. Gambar 6 memperlihatkan aktivitas mangan peroksidase (Xianghua et al. 2007).
Gambar 6 Produksi MnP dengan waktu pemberian glukosa yang berbeda Hasil penelitian Xianghua et al. (2007) mengindikasikan bahwa pemberian glukosa bisa menstimulasi produksi MnP. Lebih lanjut, Xianghua juga memaparkan bahwa penambahan gluksoa pada hari pertama tidak memperlambat munculnya aktivitas maksimum. Penambahan glukosa bahkan dapat menstimulasi pertumbuhan jamur dan meningkatkan produksi enzim secara konsekuen. Aktivitas puncak MnP yang diperoleh dengan pemberian glukosa terlihat pada hari ke-7, yang sama dengan kontrolnya. Glukosa, dalam hal ini tidak terakumulasi dalam media akan tetapi dikonsumsi selama pertumbuhan jamur.
Lignin Peroksidase
Enzim lignin peroksidase (LiP) (EC 1.11.1.14), tidak diproduksi oleh semua jamur pelapuk putih, namun merupakan
komponen kunci bagi jamur tersebut. Enzim ini mengandung gugus heme dengan potensial redoks yang tinggi dan memerlukan dua jenis metabolit agar dapat berfungsi dengan baik. Kedua jenis metabolit tersebut adalah hidrogen peroksida (H2O2) yang juga
diperlukan oleh MnP dan veratril alkohol (VA) yang digunakan sebagai mediator dalam reaksi redoks. LiP mengoksidasi gugus metoksil pada cincin aromatik dan mampu bekerja dengan substrat yang memiliki potensial redoks yang cukup tinggi.
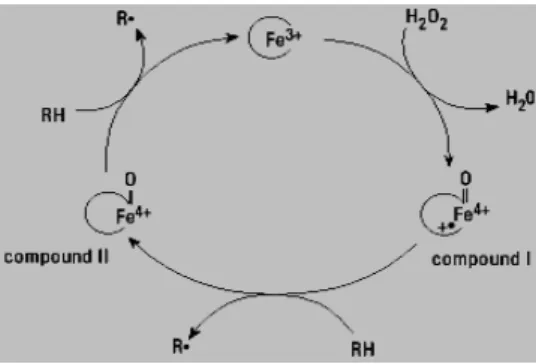
Enzim LiP memiliki siklus katalitik (Gambar 7) yang dinamakan mekanisme
ping-pong. Reaksi yang terjadi yakni H2O2
mengoksidasi enzim pada keadaan awal (resting enzyme) dengan dua elektron membentuk senyawa intermediet I, senyawa tersebut kemudian mengoksidasi substrat aromatik dengan menggunakan satu elektron membentuk senyawa intermediet II dan produk radikal bebas. Senyawa intermediet II yang dihasilkan dapat kembali mengoksidasi substrat lainya sehingga terbentuk enzim awal dan produk radikal bebas (Cullen dan Kersten 1996). Terbentuknya radikal bebas secara spontan atau bertahap inilah yang mengakibatkan lepasnya ikatan antar molekul dan beberapa inti pada cincin aromatik. Hasil dari penelitian aktivitas lignin peroksidase lainnya dapat dilihat pada Gambar 8.
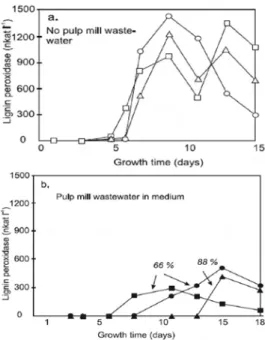
Lankinen (2004) mengungkapkan bahwa awal produksi LiP, terjadi kira-kira pada hari ke-9 dan 10 setelah dikultivasi dalam bioreaktor. Pola aktivitas tersebut terdeteksi dengan metode oksidasi veratril alkohol. Aktivitas enzim yang diperoleh juga lebih rendah pada media yang mengandung limbah kertas cair daripada media yang tidak mengandung limbah tersebut. Aktivitas enzim yang teramati dengan adanya limbah tersebut, juga kurang dari seperempatnya dibandingkan tanpa limbah.
Gambar 7 Siklus katalitik Lignin peroksidase, ion Fe berada pada heme
7
Gambar 8 Aktivitas lignin peroksidase dari
Phlebia radiata yang dikultivasi
dengan adanya glukosa, (a) tanpa limbah cair; (b) dengan limbah cair
BAHAN DAN METODE
Bahan dan Alat
Bahan yang digunakan dalam penelitian ini ialah isolat jamur Pleurotus ostreatus (dari daerah Bogor dan Thailand), kentang, gula pasir, bubuk agar, akuades, biji sorgum,
sludge, serbuk gergaji, dedak, kapur, gipsum,
bufer asetat 0.5 M pH 5.0, bufer fosfat pH 6.5, bufer Na-laktat 50 mM, ABTS 1 mM, guaiakol 4 mM, H2O2 1 mM dan 5mM,
MnSO4 1 mM, bufer asetat 0.05 M pH 5.0,
dan veratril alkohol 8 mM.
Alat yang digunakan, yaitu laminar air
flow cabinet, sentrifus Eppendorf 5417R,
autoklaf, spektrofotometer UV-Vis, tabung Eppendorf, pH meter, neraca analitik, cawan petri, parafilm, botol media, pipet volumetrik, mikropipet, mortar, pemanas, pengaduk magnetik dan peralatan gelas.
Metode Peremajaan P. ostreatus
Media PDA (Potatoes Dextrose Agar) steril dituang ke cawan petri yang steril di
laminar air flow cabinet secara aseptik. Media
setelah itu dibiarkan dingin hingga memadat. Setelah media PDA padat, isolat jamur P.
ostreatus (dari daerah Bogor dan Taiwan)
yang telah tersedia dipotong dadu kemudian dipindahkan satu potong ke dalam media PDA
secara aseptik. Setelah selesai, cawan petri disegel dengan parafilm dan diinkubasi selama sekitar satu minggu, hingga terbentuk miselia.
Pembuatan Inokulum P. ostreatus
Jamur yang telah tumbuh kemudian dipindahkan ke dalam media biji sorgum steril. Isolat jamur pada PDA dipotong dadu, kemudian dipindahkan 6 potong ke dalam media biji sorgum secara aseptik. Setiap isolat jamur dikulturkan dalam media biji sorgum. Setelah selesai, media biji sorgum lalu diinkubasi selama 1 bulan.
Pembuatan Media Produksi Enzim
Sludge dan serbuk gergaji ditimbang
pada wadah yang berbeda, kemudian dikondisikan sesuai perlakuan yang akan diberikan. Media dibagi ke dalam tiga kelompok, yaitu kelompok media sludge, kelompok media serbuk gergaji dan kelompok media yang merupakan campuran kedua macam bahan tersebut. Dua macam perlakuan yang diberikan yaitu perlakuan dengan suplemen (kapur, dedak dan gipsum), serta perlakuan tanpa suplemen. Masing-masing media dibuat untuk 1 kg bag log. Media sebelumnya dikomposkan terlebih dahulu sebelum dimasukkan dalam bag log.
Pengomposan media tumbuh jamur dibagi menjadi enam kelompok terpisah sesuai dengan perlakuan yang ditetapkan yaitu A) media serbuk gergaji tanpa suplemen B) media sludge tanpa suplemen C) media campuran serbuk gergaji dan sludge dengan perbandingan masing-masing 50% (v/v) tanpa suplemen D) media serbuk gergaji dengan tambahan suplemen dedak (12,5 %) , kapur (2,8 %) , dan gipsum (1,5 %) E) media
sludge dengan tambahan suplemen dedak
(12,5 %) , kapur (2,8 %) , dan gipsum (1,5 %) F) media campuran serbuk gergaji dan sludge dengan perbandingan masing-masing 50% (v/v) dengan tambahan suplemen dedak (12,5 %) , kapur (2,8 %) , dan gipsum (1,5 %).
Selanjutnya keenam kelompok media tersebut dikomposkan. Pengomposan dilakukan dengan cara menumpuk masing-masing media tanam setinggi ± 50 cm, lalu ditutup dengan lembaran plastik selama tiga hari. Setelah pengomposan, media kemudian dimasukkan ke dalam plastik tahan panas lalu ditutup dengan cincin pipa, diikat dengan karet gelang, disumbat dengan kapas dan ditutup dengan kertas. Seluruh media kemudian dipasteurisasi selama 8 jam pada suhu 65ºC, sebanyak dua kali dengan selang
8
waktu satu malam. Setiap perlakuan dilakukan 10 kali ulangan untuk setiap isolat.
Inokulasi Jamur Pada Baglog
Dua biakan jamur yang telah tumbuh pada media biji sorgum diaduk lalu diambil dua sendok makan dan diinokulasi secara aseptik ke dalam masing-masing media untuk setiap perlakuan. Setelah dilakukan penanaman kedua jenis jamur, pada seluruh media akan diperoleh 120 bag log, dengan pembagian 60 media untuk P.ostreatus dari Bogor dan 60 lainnya untuk P.ostreatus dari Thailand. Bag log yang telah diinokulasi kemudian diinkubasi selama ± 2 bulan hingga hifa tumbuh merata. Inkubasi dilakukan dengan cara menyimpan bag log di ruang inkubasi bersuhu 22-280C.
Ekstraksi Enzim
Proses ekstraksi dan analisis aktivitas enzim dibagi dalam dua tahap, yaitu tahap pertumbuhan miselia dan tahap tubuh buah. Tahap pertama dilakukan selama dua bulan, dengan selang waktu satu bulan yang dimulai sejak waktu inokulasi. Tahap kedua dimulai setelah tumbuh tubuh buah dengan selang waktu analisis setiap dua minggu, dikerjakan selama dua bulan. Sampel yang dianalisis merupakan sampel terbuang.
Biakan jamur yang telah tumbuh pada media sludge diambil 10 gram, kemudian digerus di dalam mortar bersama 20 mL bufer fosfat pH 7. Setelah halus, dimasukkan ke tabung eppendorf dan disentrifus dengan kecepatan 5000 rpm selama 10 menit pada suhu 0-4ºC. Supernatan lalu dipisahkan dari pelet dan dimasukkan ke tabung eppendorf yang lain. Proses sentrifus dilakukan lagi apabila supernatan yang diperoleh masih keruh, hingga diperoleh supernatan yang jernih/bebas kotoran. Supernatan yang diperoleh merupakan ekstrak kasar enzim yang kemudian akan dianalisis aktivitas enzimnya. Proses yang sama dikerjakan pula untuk media yang lain.
Analisis Aktivitas Enzim Lakase (Buswell
et al. 1995 dalam Fitria 2005)
Larutan sampel yang akan dianalisis dibuat dengan 0.4 mL filtrat enzim dicampur dengan 0.5 mL bufer asetat 0.5 M pH 5 dan 0.1 mL ABTS 1 mM. Campuran ini dimasukkan ke dalam kuvet kemudian dikocok. Setelah dikocok larutan diukur absorbannya pada panjang gelombang 420 nm dengan interval waktu 0 dan 30 menit.
Aktivitas enzim diukur berdasarkan persamaan berikut (Fitria 2005):
Aktivitas Enzim (U/mL)
= (At - Ao) x Vtotal (mL) x 109
maks x d x Venzim (mL) x t
maks = absorptivitas molar ABTS
(36000 M-1 cm-1) d = tebal kuvet (cm)
Satu unit aktivitas lakase didefinisikan sebagai jumlah enzim yang dibutuhkan untuk mengoksidasi 1 nmol ABTS per menit.
Analisis Aktivitas Enzim Mangan Peroksidase (MnP) (Kofujita et al. 1992 dalam Fitria 2005)
Sebanyak 0.1 mL bufer Na-laktat 50 mM pH 7, 0.1 mL H2O2 1 mM, 0.2 mL
MnSO4 1 mM, 0.1 mL guaiakol 4 mM, dan
0.3 mL akuades (campuran A) dimasukkan ke dalam kuvet berisi 0.2 mL filtrat enzim. Larutan ini dikocok lalu diukur absorbannya pada panjang gelombang 465 nm dengan interval waktu 0 dan 30 menit. Pengukuran aktivitas MnP diperoleh dengan melakukan reaksi dengan komposisi pereaksi yang sama dengan campuran A hanya saja tanpa penambahan MnSO4, sehingga akuades yang
ditambahkan pada reaksi ini sebanyak 0.5 mL (campuran B). Larutan ini kemudian diukur absorbannya pada panjang gelombang 465 nm dengan interval waktu 0 dan 30 menit. Aktivitas enzim diukur berdasarkan persamaan berikut (Fitria 2005).
Aktivitas Enzim (U/mL)
= (At - Ao) x Vtotal (mL) x 109
maks x d x Venzim (mL) x t
maks = absorptivitas molar guaiakol
(12100 M-1 cm-1) d = tebal kuvet (cm)
Aktivitas MnP setiap unit = Aktivitas enzim A – Aktivitas enzim B
Satu unit MnP sebanding dengan 1 nmol produk yang dihasilkan permenit.
Analisis Aktivitas Enzim Lignin Peroksidase (LiP) (Tien dan Kirk 1984 dalam Fitria 2005)
Sebanyak 0.2 mL filtrat enzim, 0.05 mL H2O2 5 mM, 0.1 mL veratril alkohol 8 mM,
0.2 mL bufer asetat 0.05 M pH 3, dan 0.45 mL akuades dimasukkan ke dalam kuvet kemudian dikocok. Larutan tersebut dibaca absorbannya pada panjang gelombang 310 nm dengan interval waktu 0 dan 30 menit. Aktivitas enzim diukur berdasarkan persamaan berikut (Fitria 2005):
9
Aktivitas Enzim (U/mL)
= (At - Ao) x Vtotal (mL) x 109
maks x d x Venzim (mL) x t
maks = absorptivitas molar veratril
alkohol (9300 M-1 cm-1) d = tebal kuvet (cm)
Satu unit LiP didefinisikan sebagai banyak enzim yang mengoksidasi 1 nmol substrat per menit.
HASIL DAN PEMBAHASAN
Pertumbuhan Miselium Jamur Tiram
Proses peremajaan isolat murni JPP dari kultur yang tersedia menggunakan media PDA. Peremajaan berlangsung hingga miselium tumbuh menutupi seluruh permukaan media agar. Hasil peremajaan kedua isolat jamur pada media PDA (Gambar 9) menunjukkan isolat jamur tiram Thailand (JTT) tumbuh lebih cepat dengan miselium yang lebih tebal dibandingkan dengan isolat jamur tiram Bogor (JTB).
Setelah miselium tumbuh menutupi media agar, isolat kemudian diinokulasi ke dalam media biji sorgum, sebagai inokulum sebelum dipindahkan ke dalam bag log. Hasil pertumbuhan kedua isolat pada media biji sorgum (Gambar 10) umumnya menunjukkan pertumbuhan miselium yang lebih tebal dan padat. Hasil yang diperoleh juga dapat menunjukkan perbedaan kecepatan tumbuh jamur di media PDA dan biji sorgum. Miselium isolat JTT tumbuh lebih cepat dalam menyelimuti seluruh media biji sorgum dibandingkan dengan pertumbuhan miselium JTB yang berlangsung lebih lambat. Miselium juga tumbuh lebih padat pada media biji sorgum dibandingkan dengan PDA. Hal ini diduga disebabkan oleh kandungan cadangan lemak dalam biji sorgum yang berguna untuk pertumbuhan.
Cadangan lemak dapat berfungsi sebagai sumber nutrisi, terutama sumber karbon, yang digunakan oleh jamur untuk mendukung pertumbuhannya, sehingga pada awal pertumbuhannya (2 minggu) miselium yang tumbuh pada media biji sorgum mendapat dorongan untuk tumbuh lebih banyak dibandingkan dengan PDA. Setelah miselium tumbuh merata, selanjutnya kedua jenis isolat diinokulasi ke media produksi. Analisis aktivitas enzim ligninolitik dilakukan selama periode inkubasi. Pengerjaan dimulai dari hari ke-0 (kontrol) hingga memasuki fase
setelah tubuh buah untuk setiap perlakuan (sekitar 5 bulan).
(a) (b)
Gambar 9 Pertumbuhan miselium P.ostreatus
pada media PDA, (a) isolat JTT dan
(b) isolat JTB, umur satu minggu
(a) (b)
Gambar 10 Pertumbuhan miselium
P.ostreatus pada media biji
sorgum (a) isolat JTT dan (b) isolat JTB
Aktivitas Enzim Lakase
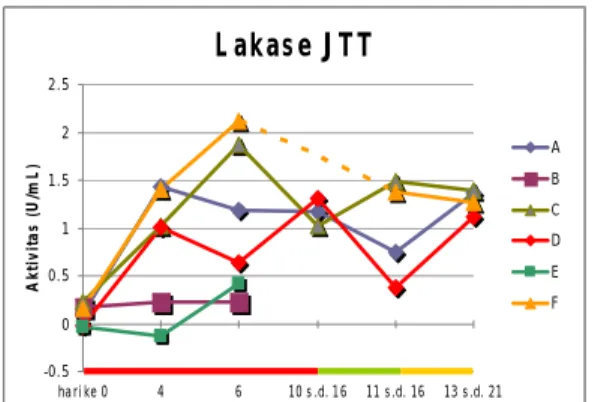
Aktivitas enzim ligninolitik dianalisis mulai hari ke-0 pada seluruh media. JPP umumnya hidup pada pH netral (Panji et al. 1996), sehingga analisis aktivitas enzim ligninolitik diawali dengan mengekstrak enzim pada medium menggunakan bufer fosfat pH 7. Aktivitas lakase, baik pada media yang tidak diberi tambahan suplemen maupun dengan penambahan, menunjukkan pengaruh positif yang meningkat hingga memasuki fase generatifnya pada media-media tersebut. Aktivitas lakase tertinggi ekstrak enzim kasar dari media A, B, C, D, E dan F yang diinokulasi JTT berturut-turut adalah sebesar 1,438, 0,222 1,870 1,428 0,412 dan 2,113 U/mL. Tabel lengkap hasil perhitungan dapat dilihat pada Lampiran.
Data yang diperoleh menunjukkan media A memberikan aktivitas maksimum enzim yang lebih tinggi dibandingkan dengan media B. Hasil analisis pada periode yang sama juga menunjukkan aktivitas enzim pada media A lebih tinggi dibandingkan dengan media C. Namun, apabila dibandingkan aktivitas maksimum enzimnya, penambahan serbuk gergaji ke dalam media sludge (media C) ternyata mampu memberikan hasil produksi enzim yang lebih tinggi, walaupun kurang efisien dari segi waktu produksi, dibandingkan dengan media A dan B. Hasil ini menunjukkan bahwa penambahan serbuk
10
gergaji ke dalam media sludge, dapat meningkatkan sekresi enzim lakase.
Data yang diperoleh juga menunjukkan media A mampu memproduksi enzim lakase dalam jumlah dan efisiensi waktu produksi yang lebih baik dibandingkan dengan media D. Hasil yang berbeda diperlihatkan oleh media B yang dibandingkan dengan media E. Media B memberikan waktu produksi aktivitas enzim yang lebih efisien, namun dari segi produksi, penambahan suplemen ke dalam media sludge (media E) memberikan aktivitas enzim yang lebih tinggi, walaupun suplementasi tetap tidak mampu mendukung pertumbuhan tubuh buah jamur. Peningkatan aktivitas juga terlihat pada media F, yang menunjukkan hasil yang lebih tinggi dibandingkan dengan media C. Interpretasi data ini menunjukkan bahwa suplementasi berpengaruh positif terhadap aktivitas enzim pada media E dan F. Suplementasi, berdasarkan hal ini, dapat digunakan dalam media sludge jika ingin memproduksi lakase dalam jumlah yang cukup banyak.
Pola aktivitas enzim lakase pada berbagai media yang diinokulasi dengan JTT dapat dilihat dalam Gambar 11. Dilihat dari pola aktivitas enzimnya, produksi lakase pada media A yang ditanami JTT mencapai puncak aktivitasnya pada waktu empat minggu setelah inokulasi. Setelah itu, aktivitasnya mulai menurun secara simultan hingga memasuki fase tubuh buah (sekitar 13 minggu). Penurunan aktivitas mungkin disebabkan jamur telah mendapatkan nutrisi yang diperlukan untuk pertumbuhan dengan cara mendegradasi media tempat tumbuhnya. Penurunan aktivitas enzim lakase diduga berhubungan dengan akumulasi produk metabolik jamur dalam media pertumbuhan yang mengakibatkan lakase terinaktivasi atau terhambat biosintesisnya; atau diakibatkan oleh kerja enzim proteolitik (Staszczak 1996 dalam Koroleva et al. 2002). Aktivitas enzim, selanjutnya terlihat meningkat pada waktu dua minggu setelah fase tubuh buah, yang mungkin disebabkan meningkatnya kebutuhan nutrisi untuk pertumbuhan jamur pada siklus selanjutya.
Pola aktivitas yang hampir sama dengan media A ditunjukkan pula oleh media C dan F. Pola aktivitas pada kedua media tersebut baru memperlihatkan aktivitas maksimum setelah enam minggu inkubasi. Pola aktivitas yang berbeda dengan media A, ditunjukkan oleh media D. Aktivitas enzim pada media ini juga terlihat memiliki dua kurva puncak selama pertumbuhannya. L akas e J T T -0.5 0 0.5 1 1.5 2 2.5 hari ke 0 4 6 10 s .d. 16 11 s .d. 16 13 s .d. 21 W aktu (ming g u) A k ti v it a s ( U /m L ) A B C D E F
Gambar 11 Pola aktivitas enzim lakase pada berbagai media yang diinokulasi dengan JTT; ( ) vegetatif I,( ) generatif,( ) vegetatif II,( ) tidak teranalisis
Aktivitas enzim selanjutnya juga terlihat meningkat kembali pada waktu dua minggu setelah fase tubuh buah. Pola aktivitas seperti ini diduga disebabkan pada awal pertumbuhannya, jamur masih mendapatkan nutrisi yang cukup dari suplemen yang ditambahkan ke dalam media. Oleh karenanya, jamur tidak memerlukan produksi enzim lakase dalam jumlah besar hingga memasuki fase primordia. Pola aktivitas pada media B dan E hanya dapat terlihat sampai enam minggu setelah inokulasi. Pola aktivitas pada kedua media ini tidak teramati seluruhnya karena tidak terbentuk tubuh buah. Pembentukan tubuh buah yang terhambat pada kedua media B dan E diduga karena kurangnya nutrisi yang terkandung dalam media, dalam hal ini sumber karbon. Sumber karbon diperlukan jamur untuk aktivitas metabolisme dan pertumbuhan miselium sehingga mampu mendukung pembentukan tubuh buah. Hal ini didukung karakteristik limbah sludge yang digunakan pada penelitian ini. Sludge yang digunakan merupakan limbah industri kertas berbahan baku kertas karton, sehingga diduga nutrisi yang terkandung pada media sludge sudah berkurang. Hasil analisis menunjukkan bahwa serbuk gergaji mengandung karbon (C) 47,70%, nitrogen (N) 0,29%; sedangkan
sludge mengandung karbon 40,24%, dan
nitrogen 0,32%. Oleh karena itu, penambahan serbuk gergaji, yang mengandung karbon yang lebih tinggi dibandingkan dengan media
sludge, ke dalam media sludge (media C)
terlihat dapat membantu jamur untuk mencapai fase tubuh buahnya.
Aktivitas enzim lakase pada JTB juga menunjukkan pengaruh positif yang
11
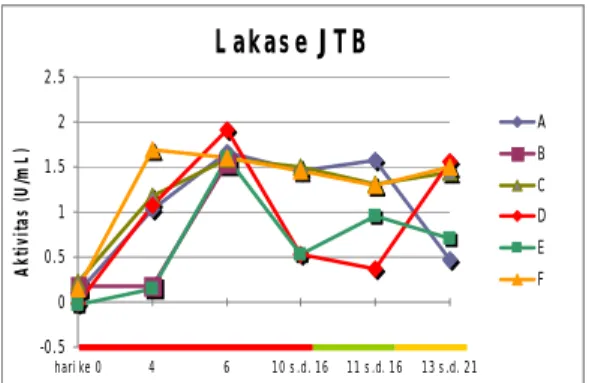
meningkat hingga memasuki fase generatifnya, baik pada media yang tidak diberi tambahan suplemen maupun dengan penambahan suplemen. Aktivitas maksimum lakase JTB A, B, C, D, E dan F berturut-turut sebesar 1,664, 1,542, 1,586, 1,905, 1,606 dan 1,697 U/mL. Tabel lengkap hasil perhitungan dapat dilihat pada Lampiran.
Data yang diperoleh menunjukkan media A mampu memberikan hasil produksi enzim maksimum yang lebih tinggi dibandingkan dengan media B dan C. Data yang diperoleh juga menunjukkan bahwa penambahan suplemen ke dalam media ternyata memberikan hasil yang lebih besar dibandingkan pada media tanpa penambahan suplemen (media A, B dan C). Peningkatan aktivitas setelah penambahan suplemen diperoleh dari media D, E dan F. Media D menunjukkan aktivitas enzim yang lebih tinggi dibandingkan dengan media A. Begitu pula dengan media E dibandingkan dengan media B. Media F yang dibandingkan dengan media C juga menunjukkan hal yang sama, baik pada periode yang sama maupun dibandingkan dengan aktivitas enzim maksimumnya. Media D dalam hal ini memperlihatkan hasil produksi enzim yang lebih tinggi dibandingkan yang lainnya, sedangkan media F lebih efisien dari segi waktu produksi enzim. Interpretasi dari data ini menunjukkan bahwa suplementasi berpengaruh positif terhadap aktivitas enzim pada media D, E dan F. Berdasarkan hal ini, maka suplementasi dapat digunakan untuk JTB dalam media sludge dan campuran sludge dengan serbuk gergaji, jika ingin memproduksi lakase dalam jumlah yang cukup banyak.
Pola aktivitas enzim lakase pada berbagai media yang diinokulasi dengan JTB dapat dilihat dalam Gambar 12. Produksi enzim lakase diseluruh media memperlihatkan pola aktivitas maksimum yang hampir seragam. Media A mencapai puncak aktivitasnya pada waktu enam minggu setelah inokulasi. Penurunan aktivitas sedikit terjadi pada fase primordia, namun kembali meningkat pada fase tubuh buah. Setelah itu, aktivitas enzimnya mulai menurun dengan cepat pada fase setelah tubuh buah (sekitar 15 minggu). Kemiripan pola aktivitas enzim ditunjukkan pada media A, B, dan E. Pada media B, analisis hanya sampai waktu enam minggu inkubasi karena tidak tumbuh tubuh buah; sedangkan pada media E, penurunan aktivitas yang tajam terjadi pada fase primordia. Pola aktivitas enzim yang mirip
juga diperlihatkan oleh media C, D dan F. Aktivitas maksimum JTB C dan D terlihat pada masa inkubasi enam minggu, sedangkan JTB F terlihat pada waktu empat minggu inkubasi. Aktivitas pada ketiga media ini mulai menurun secara simultan hingga memasuki fase tubuh buah.
Penelitian lain yang dikerjakan Bonnen
et al. (1994) menggunakan Agaricus bisporus
yang diinokulasi ke dalam media kompos, diperoleh aktivitas maksimum lakase sebesar 8,50 U/g kompos. Hasil aktivitas maksimum lakase paling tinggi dari media yang mengandung sludge pada penelitian ini, sebesar 2,113 U/mL atau hampir sebanding dengan 5,28 U/g kompos, masih lebih kecil bila dibandingkan dengan hasil yang diperoleh dari penelitian tersebut.
Secara umum, hampir seluruh aktivitas lakase (baik JTT maupun JTB), mencapai optimum pada tahap pertumbuhan miselia (sebelum pertumbuhan primordia). Hasil yang diperoleh ini sejalan dengan penelitian Bonnen et al. (1994), Ohga et al. (2001) dan Singh et al. (2003) dalam Machado dan Matheus (2006). Dalam studinya Machado dan Matheus (2006) menuliskan bahwa aktivitas terbesar lakase untuk sebagian besar fungi seperti Agaricus bisporus, Pleurotus
sajor-caju dan Lentinula edodes, umumnya
dapat teramati selama fase pembentukan koloni (miselium) pada substrat, sementara penurunan aktivitasnya terjadi pada awal pembentukan primordia. Bonnen et al. (1994), juga menyebutkan dalam penelitian lain yang menggunakan Agaricus bisporus, bahwa lakase memiliki aktivitas terbesar selama kolonisasi substrat dan pada awal perkembangan tubuh buah, sedangkan aktivitas terendahnya terjadi pada saat pematangan tubuh buah.
L akas e J T B -0.5 0 0.5 1 1.5 2 2.5 hari ke 0 4 6 10 s .d. 16 11 s .d. 16 13 s .d. 21 W a ktu (m in g g u) A k ti v it a s ( U /m L ) A B C D E F
Gambar 12 Pola aktivitas enzim lakase pada berbagai media yang diinokulasi dengan JTB; ( ) vegetatif I,( ) generatif,( ) vegetatif II
12
Hasil perhitungan menunjukkan bahwa JTT dan JTB, memiliki aktivitas lakase tertinggi pada saat fase awal pertumbuhannya. Aktivitas lakase tertinggi kedua isolat ini terjadi pada media dengan penambahan suplemen yang berupa dedak, gipsum dan kapur. Aktivitas tertinggi oleh JTT diperlihatkan pada media F, sedangkan JTB ditunjukkan pada media D. Apabila beberapa media tumbuh jamur diperbandingkan, media D yang diinokulasi JTB nampak memperlihatkan aktivitas enzim yang paling tinggi dibandingkan dengan yang lainnya dengan waktu enam minggu inkubasi. Perbandingan aktivitas maksimum lakase antara kedua isolat dipilih berdasarkan media yang dapat menunjukkan aktivitas hingga setelah fase tubuh buah pada kedua isolat.
Laporan dari Bonnen et al. (1994) juga melanjutkan bahwa aktivitas degradasi lignin dan kehilangan lignin dari kompos, meningkat pada saat awal produksi tubuh buah, dan menurun pada saat tubuh buah telah berkembang sepenuhnya Hal yang sama juga dilaporkan oleh Waksman dan Nissen (1932); dan Durrant et al. (1991). Hasilnya, tingkatan aktivitas lakase diduga berkorelasi langsung dengan aktivitas degradasi lignin dan kehilangan lignin dari substrat komposnya ketika dikolonisasi oleh A. bisporus. Aktivitas enzim maksimum yang lebih rendah pada media bersuplemen (seperti media D), dibandingkan dengan media tanpa suplemen, diduga terjadi karena terbentuknya senyawaan rekalsitran atau karena akumulasi sumber nutrisi yang berlebih. Kandungan fosfat dalam dedak (SNI 1992) dan gipsum yang ditambahkan diduga dapat membentuk Ca-fosfat yang bersifat rekalsitran, sehingga tidak dapat diserap jamur.
Aktivitas Enzim Mangan Peroksidase
Ada beberapa perlakuan pada kedua jenis isolat yang aktivitas enzim MnP-nya menunjukkan nilai negatif pada bulan pertama. Aktivitas negatif terjadi pada JTT yang ditumbuhkan dalam media B, C dan E; dan JTB yang ditumbuhkan dalam media D, E, dan F. Hal ini kemungkinan terjadi karena warna larutan hasil reaksi yang lebih pekat dibandingkan dengan kontrolnya, sehingga hasil pembacaan absorbansi memberikan hasil yang negatif, walaupun mungkin hasil sebenarnya positif. Penjelasan mengenai terjadinya hal ini masih belum diperoleh dari pustaka.
Aktivitas MnP yang disekresikan oleh
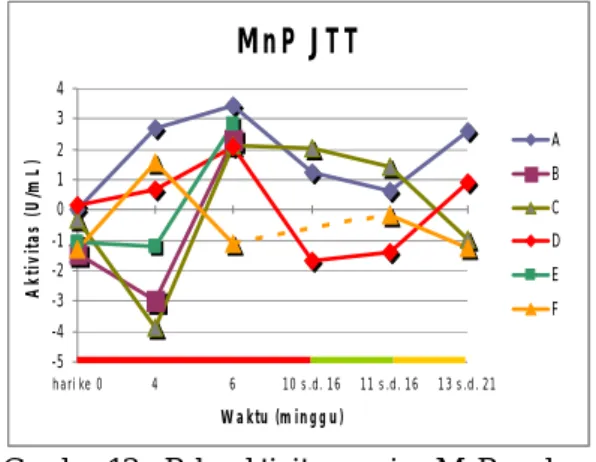
P.ostreatus pada kedua jenis isolat
menunjukkan pengaruh positif yang meningkat hingga memasuki fase generatifnya. Aktivitas maksimum MnP yang diinokulasi JTT pada media A, B, C, D, E dan F berturut-turut sebesar 3,416, 2,314, 2,121, 2,080, 2,851 dan 1,570 U/mL. Tabel lengkap hasil perhitungan dapat dilihat pada Lampiran. Data yang diperoleh menunjukkan media A pada JTT mampu memberikan hasil produksi enzim yang lebih tinggi dibandingkan dengan media B dan C. Media B juga menunjukkan aktivitas yang lebih tinggi dibandingkan dengan media C, walaupun media ini belum cukup dalam mendukung pertumbuhan tubuh buah. Hal ini menunjukkan media B dapat digunakan untuk memperoleh aktivitas enzim MnP yang cukup tinggi, namun tidak dapat digunakan untuk memproduksi tubuh buah jamur.
Selanjutnya, apabila media-media tersebut diperbandingkan, penambahan suplemen justru menurunkan aktivitas enzim MnP pada media serbuk gergaji saja atau serbuk gergaji ditambah sludge, sedangkan pada media sludge saja penambahan suplemen dapat meningkatkan aktivitas enzim MnP. Media A menunjukkan aktivitas enzim MnP yang lebih tinggi dibandingkan dengan media D. Hasil yang sama juga terjadi pada media C yang menunjukkan aktivitas enzim MnP yang lebih tinggi dibandingkan dengan media F. Peningkatan aktivitas setelah penambahan suplemen hanya diketahui terjadi pada media E yang dibandingkan dengan media B. Hasil ini menunjukkan suplementasi pada media
sludge dapat memberikan aktivitas enzim
MnP yang tinggi, walaupun belum mampu mendukung pertumbuhan tubuh buahnya.
Pola aktivitas enzim MnP pada berbagai media yang diinokulasi dengan JTT dapat dilihat pada Gambar 13. Produksi MnP pada media A mencapai puncak aktivitasnya dalam waktu enam minggu setelah inokulasi. Aktivitasnya lalu mulai menurun hingga akhirnya mengalami peningkatan kembali setelah melewati fase tubuh buahnya. Pola aktivitas seperti itu diperlihatkan juga oleh media C yang dibandingkan dengan media A. Media D, E dan F juga menunjukkan pola aktivitas yang hampir sama dengan media A. Aktivitas maksimum media D dan E tercapai pada waktu enam minggu, sedangkan media F dalam empat minggu. Perbedaan lainnya yang tampak adalah terjadinya penurunan aktivitas enzim MnP setelah tubuh buah terbentuk pada media C dan F. Pola aktivitas pada media B dan E hanya dapat terlihat sampai enam minggu setelah inokulasi.
13
MnP J T T
-5 -4 -3 -2 -1 0 1 2 3 4 hari ke 0 4 6 10 s .d. 16 11 s .d. 16 13 s .d. 21 Wa ktu (m ingg u) A k ti v it a s ( U /m L ) A B C D E FGambar 13 Pola aktivitas enzim MnP pada berbagai media yang diinokulasi dengan JTT; ( ) vegetatif I,( ) generatif,( ) vegetatif II,( ) tidak teranalisis
Aktivitas maksimum MnP yang diinokulasi JTB pada media A, B, C, D, E dan F berturut-turut ialah sebesar 5,923, 2,507, 3,912, 2,948, 4,394 dan 2,672 U/mL. Tabel lengkap hasil perhitungan dapat dilihat pada Lampiran. Media A pada JTB memberikan aktivitas enzim tertinggi dibandingkan dengan media B dan C. Perbandingan lebih lanjut juga menunjukan bahwa media tanpa penambahan suplemen dengan substrat yang sama (media A) ternyata mampu memberikan hasil yang lebih baik dibandingkan dengan media bersuplemen (media D), dengan hasil produksi yang diperoleh hampir dua kali lipatnya. Hasil yang sama juga terjadi pada media C yang dibandingkan aktivitas enzimnya dengan media F. Hasil ini menunjukkan suplementasi tidak terlalu berpngaruh terhadap aktivitas MnP pada media serbuk gergaji dan media campuran serbuk gergaji dan sludge.
Peningkatan aktivitas enzim setelah penambahan suplemen diketahui hanya terjadi pada media E yang dibandingkan dengan media B. Produksi enzim MnP pada media E hampir dua kali lipatnya dibandingkan dengan produksi pada media B. Apabila dibandingkan dengan media F pada periode yang sama, aktivitas maksimum enzim MnP pada media E menjadi hampir tiga kali lipatnya. Karakteristik dedak dan sludge yang memiliki kandungan mangan yang tinggi, yang dapat berfungsi sebagai kofaktor bagi enzim ini, diduga mampu membantu meningkatkan aktivitas enzim MnP.
Pola aktivitas enzim MnP pada berbagai media yang diinokulasi dengan JTB dapat dilihat pada Gambar 14. Pada media A yang diinokulasi dengan JTB, pola aktivitas yang
terlihat adalah meningkatnya produksi enzim dengan cepat hingga mencapai aktivitas maksimum pada masa enam minggu inkubasi. Setelah itu, aktivitasnya mulai menurun hingga pembentukan tubuh buah. Pola seperti ini terjadi pula pada media C, D, E dan F. Berbeda dengan media lainnya, media B mencapai aktivitas maksimumnya pada masa empat minggu setelah inokulasi, namun pada media ini tubuh buah tidak terbentuk.
Aktivitas enzim MnP pada penelitian ini berkebalikan dengan aktivitas enzim lakase. Penambahan suplemen terlihat tidak menyebabkan aktivitas MnP pada media menjadi lebih tinggi dibandingkan dengan perlakuan lainnya. Akan tetapi, media dengan penambahan suplemen umumnya tetap menunjukkan aktivitas enzim ligninolitik yang besar. Berbeda dengan penelitian Syafrizal (2007), yang menyebutkan, penambahan dedak pada media menyebabkan aktivitas MnP lebih tinggi dibanding pada perlakuan lainnya. Lebih jauh lagi, Syafrizal juga menyebutkan bahwa suplemen dedak berpotensi digunakan untuk meningkatkan sekresi enzim ligninolitik, terutama jika ingin terfokus pada produksi enzim mangan peroksidase dari JPP.
Apabila semua media tumbuh jamur dibandingkan, media A yang diinokulasi JTB nampak memperlihatkan aktivitas enzim yang paling tinggi dibandingkan dengan yang lainnya dengan waktu enam minggu inkubasi. Perbandingan aktivitas maksimum mangan peroksidase antara kedua isolat dipilih berdasarkan media yang menunjukkan aktivitas enzim hingga setelah fase tubuh buah pada kedua isolat. Pola aktivitas enzim MnP pada kedua media yang tidak teramati seluruhnya dikarenakan tubuh buah tidak terbentuk.
Gambar 14 Pola aktivitas enzim MnP pada berbagai media yang diinokulasi dengan JTB; ( ) vegetatif I,( ) generatif,( ) vegetatif II