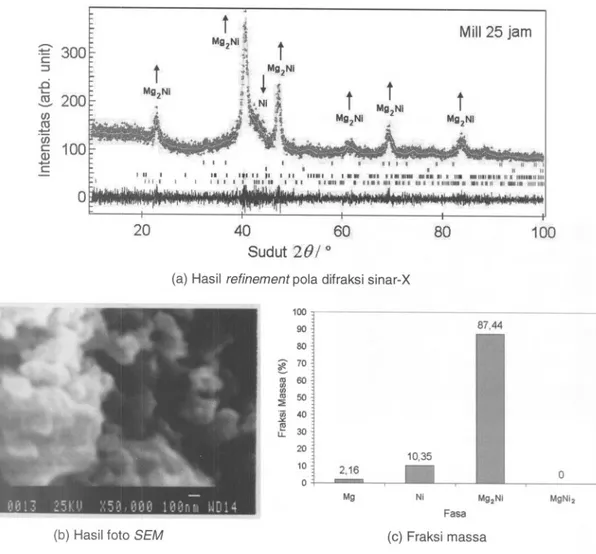
Analisis fasa dan strukturmikro paduan sistem Mg-Ni dan Mg-AI (Wisnu Ari Adi, S.Si.)
ANALISIS FASA DAN STRUKTURMIKRO
PADUAN SISTEM Mg-Ni DAN Mg-AI
Wisnu Ari Adi
Pusat Teknologi Bahan Industri Nuklir, BAT AN , Serpong
e-mail: [email protected]
ABSTRAK
ANALISIS FASA DAN STRUKTURMIKRO PADUAN SISTEM Mg-Ni DAN Mg-AI. Telah dilakukan sintesis dan karakterisasi paduan hidrida logam sistem Mg-Ni dan Mg-AI melalui metode mechanical alloying. Mechanical alloying adalah sebuah teknik pencampuran dari dua atau lebih logam yang menggunakan metode reaksi padatan (solid state reaction) dengan memanfaatkan proses deformasi untuk membentuk suatu paduano Alat yang digunakan adalah High Energy Milling SPEX 8000. Paduan hidrida logam sistem Mg-Ni dibuat melalui proses milling basah dengan variasi waktu milling selama 10 jam, 15 jam, 20 jam, dan 25 jam. Sedangkan paduan hidrida logam sistem Mg-AI dibuat dengan variasi waktu milling selama 10 jam, 20 jam, dan 30 jam. Hasil refinement pola difraksi sinar-X (XRD) menunjukkan bahwa serbuk Mg dan Ni yang dicampur dan dimilling selama 10 jam, 15 jam, 20 jam, dan 25 jam telah terjadi pertumbuhan fasa Mg2Ni yang berturut-turut sebesar 23,32%; 45,3%; 62,04%, dan 87,44%. Sedangkan pertumbuhan fasa Mg2AI3 setelah milling selama 10,20, dan 30 jam berturut-turut sebesar 71,82%; 90,73%; dan 96,19%. Dan hasil pengamatan dengan menggunakan Scanning Electron Microscope (SEM) menunjukkan bahwa pembentukan fasa baru terdiri dari em pat tahapan, yaitu proses pengecilan serbuk, proses penyatuan serbuk, proses pembentukan fasa baru, dan pengecilan butiran fasa baru. Disimpulkan bahwa mekanisme pembentukan Mg2Ni dengan metode mechanical alloying sangat bersesuaian dengan ilustrasi yang disampaikan oleh Benyamin dan Volin. Pembentukan awal paduan hidrida logam sistem Ni dan Mg-AI tampak pada waktu milling selama 10 jam. Waktu milling minimum untuk memperoleh fasa baru lebih dari 80% adalah selama di atas 25 jam, artinya semakin lama proses milling semakin banyak fasa baru yang terbentuk.
Kata kunci: Mechanical alloying, Mg2Ni, Mg2Ah.
ABSTRACT
THE ANALYSIS OF MICROSTRUCTURE AND PHASE ON THE Mg-Ni AND Mg-AI SYSTEM COMPOUND. The synthesis and characterization of Mg-Ni and Mg-AI compounds by using mechanical alloying technique have been performed. The mechanical alloying is a solid states reaction of some metal by using of deformation process to form a compound. The process of mechanical alloying used a SPEX 8000 High Energy Milling. The Mg and Ni powders are miXed and milled with the variation of milling time 10, 15, 20, and 25 hours. And the Mg and AI are milled with the variation of milling time during 10, 20, and 30 hours. The result of refinement of X-ray diffractions showed that the Mg2Ni phase already formed after milling of 10, 15, 20, and 25 hours are 23.32%, 45.3%, 62.04%, and 87.44%, respectively. And the Mg2Ah phase growth 71.82%, 90.73%, and 96.19% for the milling after 10, 20, and 30 hours, respectively. The result of Scanning Electron Microscope show that the formation of Mg-Ni and Mg-AI phase consist of four process, namely reduce powder size, welding predominance process, formation of new phase and reduce powder size of new phase. We conclude that mechanism of Mg2Ni formation by using mechanical alloying method is in accordance with Benyamin and Volin illustration. The first formation of Mg-Ni and Mg-AI phases are occurred after 10 hours of milling and the minimum milling time to growth more than 80% of the new phase is 25 hours, it's mean the long time of milling cause the new phase formation increase.
BABI
PENDAHULUAN
Energi adalah salah satu faktor utama yang sangat dibutuhkan dalam kehidupan
manusia dimuka bumi ini. Sumber energi yang paling besar selain matahari, berasal dari
bahan bakar berbasis fosil, seperti batubara, minyak bumi, dan gas alam. Ketersediaan
sumber energi ini sangat terbatas, sedangkan kebutuhan akan sumber energi terus
meningkat. Sumber energi berbasis fosil ini selain terbatas juga menimbulkan dampak negatif
yang cukup besar, yaitu dapat meningkatkan jumlah kandungan karbon dioksida di atmosfir
yang berakibat dapat meningkatkan suhu bumi (efek rumah kaca). Sehingga diperlukan
alternatif-alternatif pemecahan untuk dapat menghasilkan sumber energi baru yang dapat
bermanfaat untuk kehidupan manusia. Krisis energi dari bahan bakar fosil mendorong pesat
para peneliti untuk mengembangkan energi alternatif dari bahan hidrogen. Hidrogen
disamping merupakan salah satu alternatif yang dapat digunakan sebagai pengganti sumber
energi fosil, hidrogen juga terdapat melimpah di alam, ringan, bersih, ramah lingkungan dan
mudah diperbaharui.
Hidrogen, seperti halnya listrik, adalah energi karier yang juga harus diproduksi dari
sumber-sumber alam. Hidrogen dapat diproduksi dari gas alam dengan proses
reforming,siklus termokimia matahari, reaktor nuklir, maupun proses pemecahan air. Semua siklus
teknologi produksi hidrogen harus tidak melibatkan bahan bakar fosil dan hasil yang diperoleh
harus kompetitif di segala aspek dibanding dengan bahan bakar fosil. Namun disisi lain,
hidrogen ini memiliki kelemahan yaitu sangat reaktif mudah terbakar, dan meledak. Untuk itu
diperlukan cara untuk dapat menyimpan hidrogen ini dengan aman. Ada beberapa teknik
yang dilakukan untuk menyimpan hidrogen ini, diantaranya adalah bentuk penyimpanan
hidrogen secara tradisional yaitu mengkompres hidrogen ini dengan tekanan tinggi dalam
sebuah tabung atau lazim disebut dengan
Compressed HydrogenGas
(CHG),dijadikan
dalam bentuk cair yang disebut dengan
Liquid Hydrogen (LH),atau dengan cara menyimpan
di dalam sebuah logam yang kemudian dikenal dengan
Metal Hydride (MH)atau hidrida
logam [1-6]. Hal ini sudah dapat dilakukan dengan kapasitas yang besar, misalnya baterai
hidrogen.
Baterai hidrogen sudah cukup lama dikenal dan beredar di masyarakat sebagai
rechargeable battery
untuk menghidupkan komputer
laptop,ponsel, segala jenis peralatan
elektronik. Baterai ini dikenal sebagai baterai Ni-MH yang dapat digunakan untuk menyimpan
listrik [7].
Untuk keperluan
fuel cellmaupun kendaraan transport, penyimpanan hidrogen dalam
bentuk
on board storagemenjadi tantangan bagi para peneliti hingga sekarang. Tantangan
yang harus dijawab adalah bahwa diperlukan material yang mampu menyimpan hidrogen
dalam kondisi densitas yang lebih tinggi dibanding densitas hidrogen cairo Dan mengingat
keterbatasan volume kendaraan transportasi, hidrogen harus mampu menjalani siklus unjuk
kerja pada kondisi suhu 50°C hingga 120°C dengan tekanan 1 atm hingga10 atm. Untuk
maksud tersebut, diperlukan material yang ringan dan memiliki daya serap hidrogen yang
besar, karena sebuah kendaraan transport memerlukan sekitar 5 kg hingga 13 kg
H2[7].
Berbagai logam transisi dan paduannya dapat menyerap hidrogen membentuk ikatan
intersitial
dengan hidrogen dalam bentuk senyawa
binerdan
terner.Namun demikian, tidak
semua logam dapat dijadikan sebagai kandidat
on board storageuntuk kendaraan transpor.
Agar dapat berfungsi sebagai material
on board storagediperlukan beberapa persyaratan
yang harus dipenuhi.
Magnesium dan paduan magnesium dengan logam transisi lain merupakan bahan
penyimpan hidrogen yang cukup menjanjikan di masa yang akan datang karena kapasitas
serapan hidrogen yang cukup besar [8-10]. Magnesium dengan hidrogen akan membentuk
senyawa
hidridsebagai
MgH2yang mampu menampung hidrogen sebesar 7,6% berat
paduanoSelain hal itu, entalpi pembentukan senyawa hidrid ini cukup besar
(tJ.H= -75 kJ/mol)
membuat magnesium sangat menjanjikan untuk digunakan sebagai bahan penyimpan energi
panas, apalagi magnesium mudah didapat. Namun, ada kelemahan mendasar pada logam
magnesium sebagai bahan penyimpan energi, yaitu proses
hidriding-dehidridingberlangsung
sangat lamban,
butuh beberapa jam, dan berlangsung pada suhu 350°C hingga 400°C.
Tekanan gas hidrogen dalam kesetimbangannya dengan menggunakan
magnesium hidridsangat rendah sekitar 1 bar pada suhu 280°C. Sehingga secara termodinamik senyawa hidrid
harus berlangsung pada suhu rendah. Beberapa penyebab rendahnya kecepatan
Analisis fasa dan strukturmikro paduan sistem Mg-Ni dan Mg-AI (Wisnu Ari Adi, S.Si.)
hidroksida, dan rendahnya kecepatan disosiasi molekul hidrogen di permukaan logam. Salah satu cara untuk mengurangi beberapa kelemahan yang dimiliki oleh Mg tersebut adalah dengan menambahkan Mg dengan .Iogam transisi atau logam non transisi membentuk sebuah paduan
[11-12].
Metal hydride yang sedang dikembangkan dewasa ini adalah paduan berbasis
magnesium. Sintesis dari paduan berbasis magnesium ini telah banyak dilakukan oleh beberapa penelitian sebelumnya
[13-16].
Andreasen dan kawan-kawan telah berhasil membuat paduan paduan berbasis magnesium menggunakan Arc Melting. Namun teknik Arc Melting ini sangat sulit dilakukan khususnya di dalam lingkungan Argon [17]. Kendala utamadari sintesis paduan berbasis magnesium ini adalah ringannya serbuk-serbuk pembentuknya, sehingga pada saat busur Arc bersentuhan, serbuk-serbuk yang telah dipadatkan bersama tersebut berterbangan dan menyulitkan proses pelelehannya. Untuk diperlukan cara lain untuk dapat membuat paduan ini. Metode mechanical alloying ini diharapkan menjadi solusi yang paling sederhana untuk membuat paduan berbasis magnesium. Mechanical alloying
adalah sebuah teknik pencampuran yang merupakan sebuah metode reaksi padatan (solid
state reaction) dari beberapa logam (alloy) dengan memanfaatkan proses deformasi untuk
membentuk suatu paduano Prosesnya sangat mudah yaitu memadukan dua buah serbuk atau lebih melalui teknik milling.
Paduan metal hydride berbasis magnesium yang akan dibahas pada penelitian ini adalah sistem Mg-Ni dan Mg-AI. Paduan metal hydride sistem Mg-Ni memiliki kemampuan menyerap hidrogen yang sangat besar hingga
3,6%
berat, sedangkan sistem Mg-AI memiliki kemampuan penyimpanan hidrogen sebesar3,02%
berat hingga4,44%
berat dengan konsentrasi Mg sebesar40%
atom hingga58,6%
atom[18-22].
Absorpsi hidrogen untuk sistem Mg-Ni ini dapat menghasilkan paduan baru menjadi Mg2NiH4, sedangkan untuk sistem Mg-AI tidak. Mg-AI ini akan bereaksi secara tidak permanen membentuk paduan MgxAly.Kemudian setelah paduan ini bereaksi dengan hidrogen akan mengalami dekomposisi menjadi xMgH2 dan yAI. Sehingga dalam hal ini AI berfungsi sebagai mediator untuk mengikat Mg lebih banyak. Disamping itu untuk membentuk paduan MgH2 lebih sempurna perlu dilakukan pemanasan (ani~ pada saat proses hidriding berlangsung. Berdasarkan diagram fasa biner Mg-AI, bahwa paduan Mg-AI yang dapat terbentuk secara metastabil adalah paduan fasa ~- Mg2AI3 dan fasa y- Mg17A112
[23-25].
Untuk mendapatkan fasay-Mg17A112 dilakukan pemanasan pad a suhu antara
200°C
sampai400°C.
Namun hal yangsangat menarik untuk dipahami adalah proses pertumbuhan dan pembentukan fasa baru tersebut baik pada paduan metal hydride sistem Mg-Ni maupun Mg-AI. Jadi tujuan dari penelitian ini adalah untuk mengetahui dan memahami pertumbuhan fa sa baru pad a paduan
metal hydride sistem Mg-Ni dan Mg-AI.
BAB II TEORI
2.1. Hydrogen Storage
Mg-base dipilih karena dari hasil-hasil penelitian sebelumnya menunjukkan bahwa
magnesium mampu menyerap hidrogen cukup besar (mengandung 7,6% berat H2), disamping ringan, mudah diperoleh, dan harganya murah. Meskipun magnesium memiliki kapasitas tampung hidrogen yang besar, logam ini memiliki kelemahan mendasar, yaitu proses hidriding dan dehidriding berlangsung sangat lamban dan operasinya pada suhu yang relatif tinggi sekitar
350°C
hingga400°C.
Agar magnesium bisa dipromosikan sebagai material on board storage maka perlu dilakukan penelitian pembuatan paduan magnesium dengan logam lain sedemikian rupa sehingga diharapkan dapat menurunkan suhuhidriding-dehidriding menjadi sekitar
80°C
hingga150°C
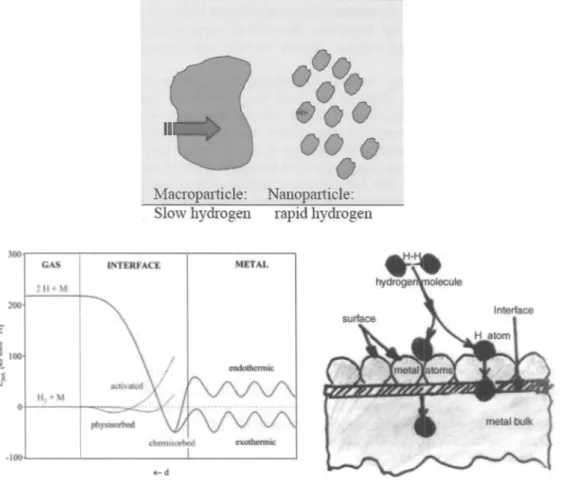
dengan tanpa mengurangi kapasitas tampungMacroparticle:
Slow hydrogen
Nanoparticle:
rapid hydrogen
:100 CASI INn:KFAca:METALI
:tU+\t I---200-
1
2
J
100I If •• \4 0 ·100 .-dGambar
2.1.
Proses dan mekanisme penyerapan hidrogen ke dalam hidrida logamHidrida logam yang dipersyaratkan untuk media penyimpan hidrogen agar memiliki kemampuan penyerapan hidrogen yang sangat tinggi adalah salah satunya memiliki ukuran butir (grain size) yang sangat keci!. Semakin kecil ukuran butirnya, semakin besar pula hidrogen yang dapat diserap oleh bahan tersebut seperti yang ditunjukkan pada Gambar 2.1. Menurut hasil penelitian Zaluska bahwa pengaruh dari ukuran butir dapat meningkatkan absorpsi hidrogen lebih banyak dan lebih cepat. Zaluska melaporkan bahwa Mg dengan ukuran butir 1 mm hanya mampu menyerap hidrogen kurang dari 0,5% berat dalam waktu 120 menit, dan Mg dengan ukuran butir 30 nm dapat menyerap hidrogen sebesar 6% berat dalam waktu yang sama.
Salah satu contoh baterai hidrogen yang sudah cukup lama dikenal dan beredar di masyarakat sebagai rechargeable battery untuk menghidupkan komputer laptop, ponsel, dan segala jenis peralatan elektronik. Baterai ini dikenal dengan sebutan baterai Ni-MH yang bisa digunakan untuk menyimpan listrik. Disamping itu ada beberapa contoh penggunaan
hydrogen storage untuk kendaraan bermotor. Di bawah ini diperlihatkan beberapa merek
mobil yang telah menggunakan bahan bakar hidrogen seperti yang ditunjukkan pada Gambar
2.2.
Analisis fasa dan strukturmikro paduan sistem Mg-Ni dan Mg-AI (Wisnu Ari Adi, S.Si.)
Gambar
2.2.
Beberapa contoh kendaraan bermotor yang menggunakan hidrogen2.2.
Metode Analisis Rietveld [26-29]
Metode tradisional untuk melakukan analisis kualitatif dan kuantitatif pada teknik Difraksi sinar-X biasanya melibatkan pengukuran intensitas dari puncak yang terpilih dan membandingkannya dengan data standar seperti International Committee Difraction Data
(ICDD). Bagaimanapun, metoda ini sangat membosankan, disamping memerlukan data
standar yang sangat bervariasi pada saat muncul keganjilan intensitas yang disebabkan oleh penyimpangan sudut. Sehingga terkadang hasil analisisnya sulit untuk dipertanggungjawabkan. Disamping itu pula metode ini tak dapat lagi memberikan hasil yang akurat jika terdapat banyak puncak-puncak yang saling tumpang tindih (overlap) sehingga akan menyebabkan hilangnya rincian informasi yang terkandung di dalam profil puncak difraksi terse but. Dengan demikian diperkenalkan metode baru untuk menganalisis profil multifasa dari pola difraksi serbuk.
Dasar untuk analisis profil multifasa dari pola difraksi serbuk secara lengkap pertama kali diperkenalkan oleh Rietveld tahun
1969.
Rietveld menunjukkan bahwa kemungkinan mereplika hasil sebuah pengukuran pol a difraksi dengan pola hitungan/kalkulasi. Kelebihannya adalah di kala terjadi kesalahan yang disebabkan oleh penyimpangan intensitas dari preparasi cuplikan atau ketidaksempurnaan model struktur cenderung akan meninggalkan sisa intensitas baik negatif maupun positif selama faktor-faktor dari kalkulasi tersebut tidak diubah oleh Taylor tahun1991.
Kemudian para peneliti lain seperti Hewat tahun1973,
Wiles dan Young tahun1981,
Will, Huang dan Parrish tahun1983,
Hill dan Howard tahun1986,
dan Taylor tahun1991
melengkapi hasil refinement program Rietveld ini dengan memberikan sebuah parameter kualitas.Setiap titik pada pola difraksi dipandang sebagai satu pengamatan tunggal yang kemungkinan mengandung kontribusi dari sejumlah refleksi Bragg yang berbeda. Pad a setiap posisi sudut atau setiap titik pada profil pol a difraksi, jumlah kontribusi intensitas akibat
overlap dapat dihitung berdasarkan nilai parameter-parameter yang didapat dengan asas
perhitungan Siroquant. Siroquant adalah suatu program analisis multi fasa jenis Rietveld yang
dapat mereplika pola difraksi hasil pengukuran/observasi dengan memanfaatkan least-square
fitting routine, yaitu melakukan penyesuaian faktor skala sampai pol a yang dihitung terbaik
mendekati pola difraksi yang terukur. Sehingga perbedaan yang dihasilkan dari pola difraksi observasi dan kalkulasi ditandai dengan derajat tingkat replikasinya. Derajat tingkat replika
(degree of fit) dilambanFkan dengan sebuah parameter statistik X2 (chi-squared). Idealnya
Namun program Rietveld versi Izumi (1994) memberikan parameter lain, dimana goodness of
fit yang dilambangkan dengan parameter S terbaik kurang dari 1,3.
2.2. 1. Prinsip Dasar
Prinsip dasar analisis Rietveld adalah mencocokkan (fitting) profil puncak perhitungan
terhadap profil puncak pengamatan. Pencocokan profil tersebut dilakukan dengan menerapkan prosedur perhitungan kuadrat terkecil non linear yang diberi syarat batas. Jadi analisis Rietveld tidak lain adalah problem optimasi fungsi non linear dengan pembatas
(constraints). Sehingga minimumkan fungsi obyektif dapat dinyatakan sebagai berikut :
(1 )
dengan w;C= 1/ Yi
(0))
dan
Yi(0)
berturut-turut adalah faktor bobot (weighting factor) danintensitas pengamatan (observation) pada posisi 20i. Sedangkan yi(c) merupakan intensitas perhitungan (calculation).
2.2.2. Persamaan Profil Pola Difraksi
Fungsi intensitas secara fisis yang dinyatakan :
(2)
dengan s, Fk(hk~, M, dan L berturut-turut adalah factor skala, factor struktur, multiplisitas, dan faktor Lorentz-polarization. Persamaan tersebut menyatakan bahwa banyaknya elektron akan didifraksikan hanya jika sudut hamburan (8) sama dengan sudut Bragg (Ok). Jadi fungsi intensitas tidak lain adalah persamaan intensitas garis. Namun pada kenyataannya bahwa pengukuran intensitas difraksi tersebut tidak terbentuk garis tetapi berupa puncak-puncak
Bragg yang melebar.
Berdasarkan hasil pengembangan program analisis Rietveld ini bahwa fungsi bentuk puncak merupakan fungsi pseudo-voigt yang telah dimodifikasi, yakni kombinasi linear dari fungsi Gauss dan fungsi Lorentz dengan tinggi puncak dan lebar penuh setengah tinggi puncak maksimum (FWHM) tidak sama. Fungsi pseudo-Voigt yang telah dimodifikasi dituliskan sebagai berikut :
(3) dengan
C~[(
4102
n
)y,
rH, (G)+ no-r;H,
(L)T
(4) (5) (6)Hk(G)
=
[U(tan
Ok_C,)2
+
V(tan
Ok
-Cs)+
W
y~
H (L)
=
Hk(G)
k
5
Pada persamaan-persamaan (3) hingga (6) di atas, y = fraksi komponen Gauss,
Analisis fa sa dan strukturmikro paduan sistem Mg-Ni dan Mg-AI (Wisnu Ari Adi, S.Si.)
dan
1-
A{ (20 - 20,
~n0,]
= laklor koreksi benluk puncak asimelris. Faklor koreksi bentuk asimetris perlu diberikan karena pad a sudut hamburan yang sangat rendah dan sangat tinggi, puncak-puncak difraksi menjadi tidak simetris akibat terbatasnya divergensi vertikal berkas. A = parameter asimetris dan t = konstanta yang diberi nilai +1,0 atau -1 tergantung pada apakah selisih(2e -
2ek) berturut-turut positif, nol atau negatif.Persamaan (5) menyatakan ketergantungan Hk(G) pada ek, U, V, dan W disebut parameter FWHM. Bila korelasi antara parameter-parameter FWHM sangat tinggi, maka
Cs
sebaiknya diberi nilai 0,6. Dalam persamaan (3) terdapat lima buah parameter varia bel yakni : U, V, W, y dan o. Fungsi bentuk puncak dapat diubah-ubah tergantung pada berapa nilai parameter y. Jika y= 1 bentuk puncak memenuhi fungsi Gauss dan bentuk puncak memenuhi fungsi Lorentz jika y diberi nilai O. Parameter variabel y memiliki daerah nilai:0 ~
r ~
1. Untukpola difraksi neutron, profil puncak difraksinya tepat memenuhi fungsi Gauss (y =1).
Dengan demikian nilai intensitas profile pola difraksi pada posisi 2ei dapat dihitung dengan mengalikan persamaan (1) dengan persamaan (3), setelah dikoreksi dengan fungsi latar belakang Yib(C) dan fungsi orientasi "preferred' ~, diperoleh :
Yi(C)
=
:LS\0
(hkl)12Mkp"L(ek)G(2e)
+
Yib(C) k(7)
I
melambangkan penjumlahan jika terdapat puncak-puncak Bragg yang saling tumpangk
tindih. Penjumlahan dilakukan terhadap semua refleksi yang dianggap masih dapat menyumbangkan intensitasnya pad a y;Cc).
2.3.
Mechanical Alloying[30 - 31]
Mechanical alloying adalah sebuah teknik pencampuran yang merupakan sebuah
metode reaksi padatan (solid state reaction) dari beberapa logam (alloy) dengan memanfaatkan proses deformasi untuk membentuk suatu paduano Proses mechanical
alloying ini sangat berbeda dengan teknik konvensional, misalkan proses pemanasan (heat
treatment) baik sintering maupun peleburan (melting) dan reaksi kimia. Derajat deformasi
yang dicapai pada teknik konvensional ini jauh lebih rendah dibandingkan dengan teknik
mechanical alloying [30-31].
\\
~ " Bola .' Ff Mendekat Bertumbukan-...
Bola BerpisahGambar 2.3. Proses tumbukan bola-bola dalam media milling [30].
Selama proses mechanical alloying, serbuk-serbuk Mg dan Ni secara periodik terjebak diantara bola-bola yang saling bertumbukan secara plastis terdeformasi. Akibatnya bola-bola yang saling bertumbukan tersebut menyebabkan perpatahan, kemudian terjadi penyatuan dingin (cold welding) dari serbuk-serbuk secara elementer seperti yang di iIIustrasikan pada Gambar 2.3.
Ketika waktu milling meningkat, fraksi volume unsur-unsur dari bahan dasar menurun, sedangkan fraksi volume paduan meningkat. Ukuran, bentuk, kerapatan serbuk, dan derajat kemurnian mempengaruhi hasil akhir paduano Ada empat tahapan dalam
Mg
Ni
(a) Tahap pertama (b) Tahap kedua (c) Tahap ketiga (d) Tahap keempat
Gambar
2.4.
Tahapan mechanical alloying menurut referensi Benyamin dan Volin [30].Tahap petama adalah proses perataan serbuk dari bentuk bulat menjadi bentuk pipih
(plat like) dan kemudian mengalami penyatuan (welding prodominance). Serbuk yang sudah
diratakan (bentuk pipih) disatukan membentuk sebuah lembaran (lamellar). Kemudian tahapan kedua adalah pembentukan serbuk pada arah yang sama (equiaXed), yaitu menyerupai lembaran berbentuk lebih pipih dan bulat. Perubahan bentuk ini disebabkan oleh pengerasan (hardening) dari serbuk. Tahap ketiga adalah orientasi penyatuan acak (welding
orientation) yaitu fragmen-fragmen membentuk sebuah partikel-partikel equaxed kemudian
disatukan dalam arah yang berbeda dan struktur lembaran mulai terdegradasi. Tahap keempat mechanical alloying ini adalah proses steady state (steady state processing),
struktur bahan perlahan-Iahan menghalus menjadi fragmen-fragmen, kemudian fragmen-fragmen tersebut disatukan dengan beberapa fragmen-fragmen yang lain dalam arah berlawanan.
BAB III METODE PERCOBAAN
3.1.
BahanPeralatan yang digunakan untuk metode mechanical alloying adalah High Energy
Milling (HEM) SpeX 8000 yang terdapat di laboratorium Bidang Karakterisasi dan Analisis
Nuklir (BKAN), Pusat Teknologi Bahan Industri Nuklir (PTBIN - BAT AN), dengan spesifikasi
normal speed
=
1500 rpm, run time=
90 men it, off time=
30 menit, dan on-off cycle=
1 kali,seperti yang ditunjukkan pada Gambar 1. HEM ini terdiri dari sebuah wadah (vial) yang di dalamnya terdapat bola-bola (ball mill) yang bergerak secara spin dan berfungsi untuk menghancurkan bahan tersebut. Vial ini terbuat dari bahan stainless steel (SS) dengan
bentuk seperti tabung dengan panjang 7,6 cm dan diameter luar 5,1 cm. Sedangkan ball mill
juga terbuat dari bahan stainless steel (SS) dengan diameter bola sebesar 12 mm. Paduan sistem Mg-Ni dibuat sebanyak 15 gram yang terdiri dari campuran antara Magnesium (Mg) dan Nickel (Ni). Magnesium Mg (produk Merck dengan tingkat kemurnian lebih dari 99,8%) dan nickel Ni (produk Merck dengan tingkat kemurnian lebih dari 99,0%), dengan perbandingan stokiometri unsur Mg : Ni =2 : 1. Sedangkan paduan sistem Mg-AI juga dibuat sebanyak 15 gram yang terdiri dari campuran antara Magnesium (Mg) dan Alumunium (AI). Alumunium berasal dari produk Merck dengan tingkat kemurnian lebih dari 99,0%, dengan perbandingan stokiometri unsur Mg : AI = 2 : 3.Dan berdasarkan teorema mesh ratio sama dengan 8, untuk massa cuplikan sebanyak 15 gram diperlukan massa bola-bola sejumlah 120 gram. Baik serbuk Mg - Ni maupun serbuk Mg - AI ini dicampur di dalam vial dan ditambahkan toluen untuk menghindari terjadinya oksidasi kemudian di milling.
3.2.
Tata
KerjaProses milling ini banyak digunakan untuk menghasilkan berbagai jenis bahan nanostruktur. Selain untuk menghasilkan butiran yang relatif kecil, milling ini juga menyebakan terbentuknya struktur yang metastabil. Pada penelitian ini, cuplikan Mg2Ni di
milling dengan variasi waktu milling selama 10 jam, 15 jam, 20 jam, dan 25 jam di suhu ruang
dalam lingkungan Argon. Pada penelitian ini cuplikan Mg-AI di milling dengan variasi waktu
Analisis fasa dan strukturmikro paduan sistem Mg-Ni dan Mg-AI (Wisnu Ari Adi, S.Si.)
a. High Energy Milling (HEM) dan vial
b. Alat difraktometer sinar-X (XRD) c. Alat Scanning Electron Microscope (SEM)
Gambar 3. 1. Peralatan preparasi dan karakterisasi cuplikan
Pengamatan strukturmikro cuplikan dilakukan dengan menggunakan SEM (Scanning
Electron Microscope) 515 Philip. Sedangkan pengamatan kualitas dan kuantitas fasa-fasa
yang ada di dalam cuplikan menggunakan peralatan X-Ray Diffractometer (XRD) merek
Philip, type PW 171O. Pengukuran pola difraksi cuplikan dengan berkas sinar-X dari tube
anode Cu dengan panjang gelombang, A = 1,5406 A, mode = continuous-scan, step size =
0,02°, dan time per step = 0,5 detik. Peralatan untuk sintesis dan karakterisasi diperlihatkan pada Gambar 3.1 .
Analisis profil difraktometer sinar-X yang diperoleh dilakukan dengan menggunakan perangkat lunak program RIETAN (Rietveld Analysis). Program RIETAN ini dibuat oleh Fuji Izumi pada tahun 1994 [26]. Langkah untuk menganalisis dengan menggunakan metode rietveld ini, yaitu dengan memasukkan dua jenis data. Data pertama adalah data instrumen yang berisikan parameter struktur kristal dan data kedua adalah data intensitas. Parameter struktur kristal adalah data masukan dari suatu model perhitungan yang diajukan sebagai standar acuan. Sedangkan data intensitas adalah data yang diperoleh dari hasil pengukuran menggunakan XRD. Hasil pengolahan dari program ini memberikan beberapa informasi, diantaranya adalah data parameter struktur kristal dalam satu sel satuan, data intensitas hasil perhitungan (calculation) dan pengamatan (observation), data jumlah fraksi massa yang diperoleh apabila lebih dari satu fasa, dan data refleksi Bragg yang muncul. Sedangkan karakterisasi SEM dan XRD ini dilakukan di Pusat Teknologi Bahan Industri Nuklir - BAT AN.
BAB IV HASIL DAN PEMBAHASAN
4.1. Analisis Fasa dan Strukturmikro Paduan Sistem Mg-Ni
Paduan Mg2Ni dibuat melalui reaksi padatan dengan menggunakan teknik
mechanical alloying dari pencampuran logam-Iogam penyusun, yaitu : Magnesium (Mg) dan
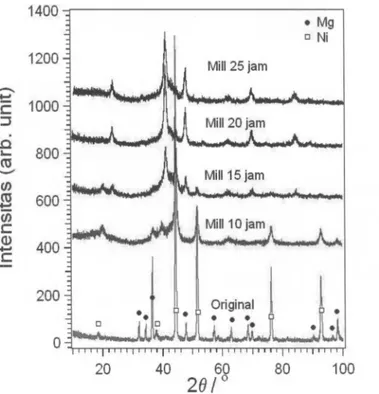
Nickel (Ni) dengan perbandingan stokiometri unsur Mg : Ni =2 : 3 yang di milling selama 0 jam, 10 jam, 15 jam, 20 jam, dan 25 jam. Gambar pola hasil pengukuran dengan difraksi sinar-X ditunjukkan seperti pada Gambar 4.1.
1400 1200
--:!::: 1000c:
:J
..a
800 ~ co'-"
corn 600-
'wQ)c:
400-
c:
200 0 • Mg o Ni Mill 25jam Mill 10jam 20 40 6020/0
80 100Gambar
4.1.
Pola difraksi sinar-X paduan sistem Mg-Ni sebelum dan setelah millingselama 10 jam, 15 jam, 20 jam, dan 25 jam.
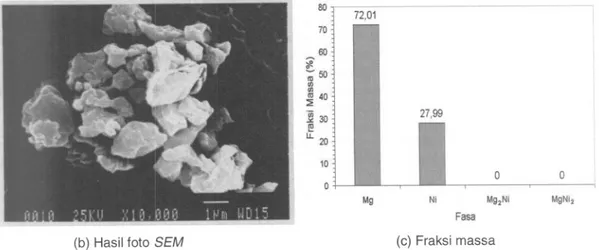
Karakterisasi awal dari dari bahan dasar, yiatu : serbuk Mg dan Ni ini ditunjukkan seperti pada Gambar 4.2.
120
.•.•....•. ~ 80 ::J.ri
I-~
40
(/) It] -·w c: Q)-
c: NISebelum Mill
) -.;, NI.
,-~
Mg ~NI NI )!
:..
i
Mg Mg1
- ~ ~ f NI ;: Mg :~ Mg MgMgj
Mg •• .I • !:.
'-'-"";.
~A-~.~~
(f:
I
r
.'-i1 II 1/ II ) I " "I , I I.
.
L
~I
r r10
2030
40
50
60
Sudut
2e/o 70 8090
100
Ana/isis fasa dan strukturmikro paduan sistem Mg-Ni dan Mg-A/ (Wisnu Ari Adi, S.Si.)
(b) Hasil foto SEM
80~ 72,01 70 80 ~~ 40';50'"'" ~30~ 1l.2Q 10 0 0 0 Mg Ni Mg2NiMgNi2 Fasa (C)Fraksi massa
Gambar 4.2. Karakterisasi bahan dasar yang terdiri dari serb uk Mg dan Ni
Pada awalnya campuran hanya terdiri dari serbuk Mg dan Ni yang masih berdiri sendiri-sendiri. Dari profil difraksi sinar-X menunjukkan bahwa campuran tidak mengandung impuritas dan hanya terdiri dari fasa Mg dan Ni.
Tahap petama adalah proses perataan serbuk dari bentuk bulat menjadi bentuk pipih
(plat like) dan kemudian mengalami penyatuan (welding prodominance). Serbuk yang sudah
diratakan (bentuk pipih) disatukan membentuk sebuah lembaran (lamellar). lIustrasi ini diperlihatkan pada Gambar 4.3.
Mill 10 jam
II IIJ
I • I 11 II
II I "1 II t. I II 11111' I 111111 1111" •• '" .,1 '11 II. "''''111'1' II' l.m.lIl1n
I I I I I IIItII I I I •111111III •• I •• II. , •••••• I' 'II.M ••••• II II _ I.111111111
500
~ 400'c
~ 300.c
~
200
en ~ lOOt " .• c:2
0
c: III I III I I I I ; -.t
Ni NI 10 1006080203040507090 Sudut20!
0(a) Hasil refinement pol a difraksi sinar-X..
_.-T
45 40 ~ 35:!J 30 '" ::¥'w 25 20 '"'" U: 15 10 5 0 Mg Ni Mg2NiMgNi2 Fasa(b) Hasil foto SEM
(c) Fraksi massa
Dari pengamatan foto SEM menunjukkan bahwa serbuk mulai mengecil dan sebagian diduga telah mengalami penyatuan. Hasil ini didukung dengan analisis profil difraksi sinar-X pada cuplikan yang telah di milling selama 10 jam. Tampak bahwa puncak-puncak
Mg dan Ni mulai menu run yang ditandai dengan simbol panah ke bawah (,J..). Dan tampak
mulai terjadi pertumbuhan puncak disekitar sudut 20°, 40°, dan 60° yang ditandai dengan simbol panah ke atas
(t).
Puncak-puncak ini diduga berasal dari fasa MgNi2 dan Mg2Ni. Hasilrefinement dari pola difraksi sinar-X ini menunjukkan bahwa terjadi pertumbuhan fasa MgNi2
dan Mg2Ni berturut-turut sebanyak 23,31% dan 17,63%. Penurunan puncak terbesar berasal dari fasa Mg. Hal ini disebabkan Mg merupakan bahan yang lunak, sehingga dapat dengan mudah dihancurkan. Oleh sebab itu Mg mudah mengalami amorfisasi dibandingkan dengan Ni.
Kemudian tahapan kedua adalah pembentukan serbuk pada arah yang sama
(equiaXed), yaitu menyerupai lembaran berbentuk lebih pipih dan bulat. Perubahan bentuk ini
disebabkan oleh pengerasan (hardening) dari serbuk seperti yang diperlihatkan pada Gambar
4.4.
200 III I 1111 .1 IIIII I 1'1II1'- 111111t ~, •• II I II III.' I I ••••••••••••• II I n. _1111.,.,11' 1111•• 11 I II II.".' 11••• 1111••• 1''''.1._ •.UII II_I.UUIII20401006080
Sudut
2()/o
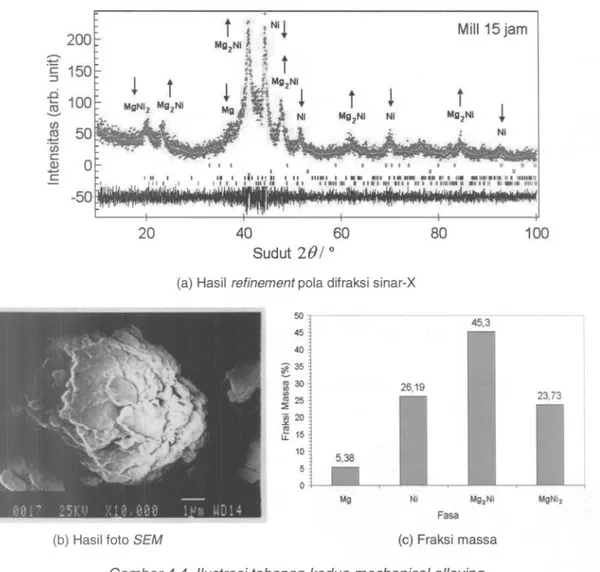
(a) Hasilrefinement pola difraksi sinar-X
-
-50]
--
45,3 45 40 ~35.
:}]3O '" ~ 25 -';20 -'"'" u:15 10 5 0 Mg Ni Mg,NiMgNi, Fasa(b) Hasil fotoSEM
(c) Fraksi massa
Gambar
4.4.
lIustrasi tahapan kedua mechanical alloying.Berdasarkan hasil foto SEM tampak sekali bahwa serbuk mulai lebih menyatu dan sudah tidak tampak lagi serbuk-serbuk Mg dan Ni, namun belum seluruhnya terdifusi membentuk fa sa baru. Hasil refinement pol a difraksi sinar-X hasil milling selama 15 jam menunjukkan bahwa terjadi penurunan puncak Mg dan Ni berturut-turut sebesar 7,18% dan 20,31 %, sedangkan terjadi pertumbuhan yang signifikan dari fasa MgNi2 dan Mg2Ni berturut-turut sebesar 6,1% dan 21,99%. Dari gambar pol a difraksi sinar-X tersebut tampak sekali bahwa sebagian puncak-puncak fasa Mg telah menghilang tinggal puncak tertinggi dari Mg yang masih muncul disekitar sudut 37°. Sedangkan puncak-puncak fasa Ni masih banyak terlihat walaupun intensitasnya mulai menurun secara signifikan. Hal ini berarti sebagian serbuk Mg telah bereaksi dengan Ni membentuk fasa MgNi2 dan Mg2Ni.
Analisis fa sa dan strukturmikro paduan sistem Mg-Ni dan Mg-AI (Wisnu Ari Adi, S.Si.) 400 ~ 300 ::J
.c
~ 200 en (IJ ~ 100 I:: Q)-
I:: De, 20 40 60 80 100 Sudut28/0(a) Hasilrefinement pola difraksi sinar-X70
j 62,04 60 ~50 ~ ~ 40 '" ~30""'"'" U:2O 10 0 Mg Ni Mg,NiMgNi, Fasa
--(b) Hasil fotoSEM (c) Fraksi massa
Gambar 4.5. lIustrasi tahapan ketiga mechanical alloying.
Tahap ketiga adalah orientasi penyatuan acak (welding orientation) yaitu fragmen-fragmen membentuk partikel-partikel equaXed kemudian disatukan dalam arah yang berbeda
dan struktur lembaran mulai terdegradasi. Ilustrasi pad a tahap ini diperlihatkan pada Gambar
4.5.
Berangkat dari hasil foto SEM pula tampak bahwa serbuk cenderung mulai menyatu membentuk fasa baru dan proses milling mulai mengecilkan ukuran serbuk dari fasa baru tersebut. Dari hasil pengukuran difraksi sinar-X menunjukkan puncak-puncak fasa Mg hampir hilang dan puncak-puncak fasa Ni hanya terlihat pada puncak tertinggi dari fa sa Ni, yaitu disekitar sudut 45° dengan nilai intensitasnya sangat rendah. Sedangkan fasa Mg2Ni tumbuh dengan sangat baik disekitar sudut 40°. Namun fasa MgNi2 pada tahap ini mulai menurun. Hal ini disebabkan bahwa fa sa MgNi2 ini dikenal dengan paduan yang memiliki sifat yang kurang stabil. Fasa MgNi2 ini diduga terdekomposisi menjadi Mg2Ni dengan mengikat Mg yang lebih banyak. Dari hasil refinement pola difraksi sinar-X hasil milling selama 20 jam ini menunjukkan bahwa terjadi penurunan puncak Mg, Ni, dan MgNi2 berturut-turut sebesar 0,6%, 12,69%, dan 4,65%, sedangkan terjadi pertumbuhan yang signifikan dari fasa Mg2Ni sebesar 16,74%.
Tahap keempat mechanical alloying ini adalah proses steady state (steady state
processing), struktur bahan perlahan-Iahan menghalus menjadi fragmen-fragmen, kemudian
fragmen-fragmen tersebut disatukan dengan fragmen-fragmen yang lain dalam arah berlawanan. lIustrasi pada tahap akhir ini diperlihatkan pada Gambar 4.6.
Pada tahap ini hampir keseluruhan telah terbentuk fasa Mg2Ni. Hal ini dapat dilihat dari hasil foto SEM yang menunjukkan serbuk dari fasa baru terse but semakin mengecil. Apabila ditinjau dari hasil pengukuran difraksi sinar-X, puncak-puncak fasa Mg sudah hilang. Hilangnya puncak-puncak fasa Mg ini bukan berarti bahwa kandungan fraksi volume dari Mg di dalam campuran berkurang, namun struktur kristal Mg sebagian telah rusak dan berubah menjadi
amari,
dan sebagian lagi telah bereaksi dengan Ni membentuk Mg2Ni. Dan fasa MgNi2 pada tahap ini telah mengalami transformasi fasa menjadi Mg2Ni dengan mengikat Mgyang lebih banyak. Namun akhir dari proses ini masih menyisakan sejumlah keeil puneak Ni yang diduga belum bereaksi dengan Mg untuk membentuk Mg2Ni. Dari hasil refinement pola difraksi sinar-X menunjukkan bahwa kandungan terakhir eampuran ini terdiri dari fasa Mg2Ni, Ni, dan Mg yang berturut-turut sebesar 87,44%; 10,35%; dan 2,16%.
t ~
Mg2NI!
t
;l
Mg2NI.' I
;; ,.I
t
t
t
: f&:1
-v.!
?
,,~~~;~~~~~.~
Mg2NI. Mg2NI Mg2NI~
I I' II I' I' 11 II II I
I •• II 1\
II I I'~II .' I II III •• I •••••• I' •••••• I" U•• UII.IIII1II ••II.IIII11
I I I I I 1111II I • I I I." •• II.'.' .1•• "' I
I"".' •...
II II _ ••IIUlIIiI:2 300
c
:J
.c
~
200
(/) IU +-' 'w C Q) +-' Co
I II I IIII20
" ,40
60
Sudut2B
/080
Mill 25 jam100
(a) Hasil refinement pola difraksi sinar-X
100 90 80 ~ 70 l'O 60 rJ) rJ)l'O 50 ::;; "w 40 Ot: !!1 30 u. 20 1~
L.;.;.6
Mg Fasa 87,44 o MgNI2(b) Hasil foto SEM (c) Fraksi massa
Gambar
4.6.
lIustrasi tahapan keempat mechanical alloying.Hasil ini menunjukkan bahwa makin lama proses milling fa sa metastabil dari MgNi2 mengalami transformasi fasa menjadi Mg2Ni yang stabi!. Dan tingginya fraksi massa dari fasa Mg2Ni mengakibatkan menurunnya fasa MgNi2 hingga kurang dari 1% dan menurunnya fasa Mg hingga kurang dari 3%. Jadi dengan proses milling basah ini sangat efektif selain melindungi euplikan berinteraksi dengan oksigen juga sangat membantu pembentukan fasa Mg2Ni dengan baik. Pembentukan awal paduan Mg2Ni tampak pada waktu milling selama 10 jam dan waktu milling minimum untuk memperoleh fasa Mg2Ni lebih dari 80% adalah selama 25 jam.
4.2.
Analisis Fasa dan Strukturmikro Paduan Sistem Mg-AIPaduan Mg2AI3 dibuat melalui reaksi padatan dengan menggunakan teknik
mechanical alloying dari peneampuran logam-Iogam penyusun, yaitu : Magnesium (Mg) dan
Alumunium (AI) dengan perbandingan stokiometri unsur Mg : AI=2 : 3 yang di-milling selama 10 jam, 20 jam, dan 30 jam. Gambar pola hasil pengukuran dengan difraksi sinar-X ditunjukkan seperti pada Gambar 4.7.
Berdasarkan hasil dari profil difraksi sinar-X pad a Gambar 4.7 menunjukkan bahwa pada awalnya sebelum milling eampuran tidak mengandung impuritas dan hanya terdiri dari fasa Mg dan Ni. Kemudian selama milling, terjadi proses mechanical alloying, yaitu
serbuk-serbuk Mg dan AI seeara periodik terjebak diantara bola-bola yang saling bertumbukan seeara plastis terdeformasi. Bola-bola yang saling bertumbukan tersebut menyebabkan
Analisis fasa dan strukturmikro paduan sistem Mg-Ni dan Mg-AI (Wisnu Ari Adi, S.Si.)
perpatahan, kemudian akan terjadi penyatuan dingin (cold welding) dari serbuk-serbuk secara elementer. Ketika waktu milling meningkat, fraksi volume unsur-unsur dari bahan dasar menurun, sedangkan fraksi volume paduan meningkat. Dengan demikian diduga bahwa pada Gambar 4.7 tampak adanya pertumbuhan fasa baru. Untuk itu perlu dilakukan identifikasi fasa awal, yaitu dengan mencocokkan puncak-puncak yang ada dengan Tabel Hanawalt. 2000 119 119 104 ~ 1500
S'
~ rn ~ 1000 ~ (I)-
c: 500 o 20 40 60 Sudut 2010 80 Mill 30 jam Mill 20 jam MiII10jam Sebelum Mill 100Gambar 4. 7. Pola difraksi sinar-X cuplikan Mg-AI sebelum dan setelah di milling
selama 10 jam, 20 jam, dan 30 jam.
Sedangkan hasil refinement pola difraksi sinar-X pada masing-masing proses milling di tunjukkan pada Gambar 4.8, Gambar 4.9, Gambar 4.10, dan Gambar 4.11, yang berturut-turut untuk profil XRD sebelum milling, hasil milling selama 10 jam, hasil milling selama 20 jam dan hasil milling selama 30 jam.
Gambar 4.8 menunjukkan bahwa kualitas bahan dasar baik Mg maupun AI masih sangat baik. Puncak tertinggi dari fasa Mg terdapat pada bidang (101), sedangkan puncak tertinggi dari fasa AI terdapat pada bidang (200). Dan jumlah fraksi massa yang diperoleh untuk fasa Mg dan AI berturut-turut sebesar 43,3% dan 56,7%. Hasil ini juga memberikan konfirmasi bahwa campuran yang terbentuk sesuai dengan komposisi stoikiometri yang diharapkan. AI
1~
1500-I
111 Mg I 101 ---j ~ 1000 ~ 500~ en:~~H
1
AI ~:t:
220 ~ l Q)-
s::: o 20 40 60 Sudut 2010 Sebelum Milling AI 311 1 Mg Mg 400 104 .."..~ Mg I I 11I AI I I I I ">---v -,--- 100 80Gambar 4.8. Refinement pola difraksi sinar-X cuplikan Mg-AI sebelum di-milling
Gambar 4.9 diperlihatkan hasil refinement pola difraksi sinar-X cuplikan yang di
milling selama 10 jam. Pad a Gambar 4.9, cuplikan setelah di-milling selama 10 jam, tampak
bahwa puncak-puncak Mg dan AI, terutama puncak tertinggi Mg bidang (101) pada sudut 36,39° dan AI bidang (200) pada sudut 44,49° mulai menu run yang ditandai dengan simbol
panah ke bawah (.J..). Dan tampak mulai terjadi pertumbuhan puncak disekitar sudut 38°, 43°,
63° dan 76° yang ditandai dengan simbol panah ke atas
(t).
Puncak-puncak ini merupakan puncak fasa Mg2A13• Hasil refinement dari pola difraksi sinar-X ini menunjukkan bahwa telah terjadi pertumbuhan fa sa Mg2AI3 sebesar 71 ,82% dan fa sa Mg dan AI menu run berturut-turut menjadi 6,37% dan 21,81 %. Penurunan puncak terbesar berasal dari fasa Mg.500 -I Milling 10 Jam 400 -I
rooJ
1
1
~ 200 Mg2A131 Mg2A131 :t::2
100~
311 AI 220J.~
t:
311 O~~I
I
II I
I
I
I I
I
I
..." 20 40 60 Sudut 281° 80 100Gambar 4.9. Refinement pola difraksi sinar-X cuplikan Mg-AI setelah milling 10jam
Hal ini disebabkan Mg merupakan bahan yang lunak, sehingga dapat dengan mudah dihancurkan. Oleh sebab itu Mg mudah mengalami amorfisasi dibandingkan dengan AI.
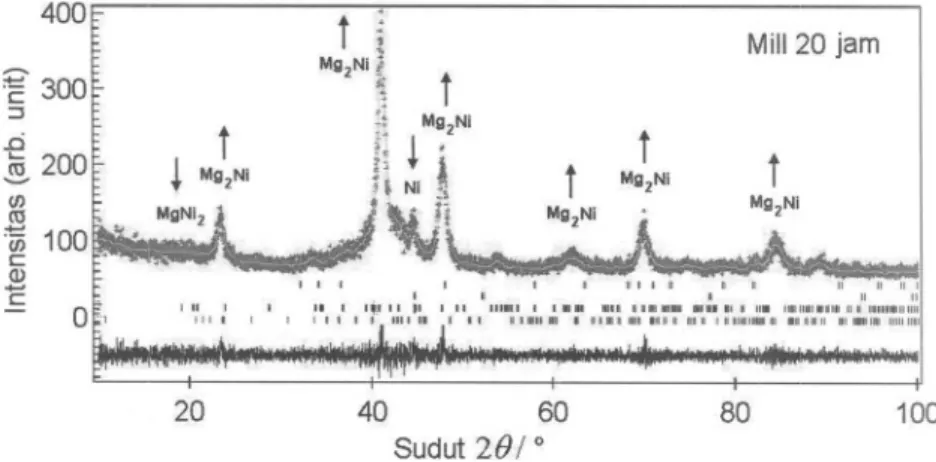
Gambar 4.10 diperlihatkan hasil refinement pol a difraksi sinar-X cuplikan yang
di-milling selama 20 jam.
400 300 .•....•• :J ro 200 .•....•. o
II
I
.1! .1!
II I
I I
I
I
I
I
I
I
---20 40 60 Sudut 281° 80 100Gambar 4.10. Refinement pola difraksi sinar-X cuplikan Mg-Alsetelah milling
20
jamHasil refinement pol a difraksi sinar-X hasil milling selama 20 jam pad a Gambar 4.10 menunjukkan bahwa sebagian puncak-puncak fasa Mg telah menghilang tinggal puncak tertinggi dari Mg bidang (101) yang masih muncul disekitar sudut 36,39° sedangkan puncak-puncak AI bidang (200), (220), dan (311) yang berturut-turut disekitar sudut 44,49°, 64,83°, dan 77,95°. Pertumbuhan fasa Mg2AI3 meningkat menjadi 90,73% dan fasa Mg dan AI menu run berturut-turut menjadi <1% dan 8,89%. Dari gambar pola difraksi sinar-X tersebut tampak puncak-puncak fasa AI masih banyak terlihat walaupun intensitasnya mulai menurun secara signifikan. Hal ini berarti sebagian serbuk Mg telah bereaksi dengan AI membentuk fasa Mg2A13.
Analisis fasa dan strukturmikro paduan sistem Mg-Ni dan Mg-AI (Wisnu Ari Adi, S.Si.)
Gambar 4.11 diperlihatkan hasil refinement pola difraksi sinar-X cuplikan yang
di-milling selama 30 jam.
500 -I Mg2AI3
!
111•
400 -Ii
i
~ 300 ~1
r~3i
200 \,.,~,~i
.1!
.11
Mg 101 .2! 100 r:: o II II
I I II
II II
I
I II
I
I I 20 40 60 Sudut 2()10 80 100Gambar 4. 11. Refinement pol
a
difraksi sinar-X cuplikan Mg-AI setelah milling 30 jam.Pada Gambar 4.11, dari hasil pengukuran difraksi sinar-X menunjukkan puncak-puncak fasa Mg sudah hilang dan puncak-puncak-puncak-puncak fasa AI diduga tinggal puncak tertinggi dari fasa AI tersebut bidang (200) pada sudut 44,49° dengan nilai intensitasnya sangat rendah. Sedangkan fasa Mg2AI3 tumbuh dengan sangat baik disekitar sudut 43° dengan fraksi massa sebesar 96,19%. lIustrasi pertumbuhan fasa Mg2AI3 ini diperlihatkan pada Gambar 4.12.
400
----~ 1200 ~ ~ 800 'wc
Q)-
c
Sebelum Mg di Mill 101 AI 111 500 ,--. ~ 400 ~ ~ 300 'w ~ 2001:
100
35
36
37
38
39
40
Sudut 28/°
(a) Sebelum milling
34 36 38 40
Sudut 28 /0
(b) Setelah milling 10 jam
400 ,--. ::i ~ 300 1/1 .J!! .~ 200 OJ
1:
100
MiII20jam 500 ,... ~ 400 ~ ~ 300 '00 ~ 2001:
100 Mill 30 jam 3436
38
40 Sudut 2e I0(c) Setelah milling 20 jam
40 34 36 38
Sudut 28I0
(d) Setelah milling 30 jam
Pada Gambar 4.12 tampak bahwa sebelum milling baik puncak Mg bidang (101) maupun terlihat sangat tajam. Kemudian setelah milling selama 10 jam baik puncak Mg (101) maupun puncak AI (111) mulai hancur ditandai dengan menu run dan melebarnya puncak Mg dan AI tersebut. Setelah milling selama 20 jam dan 30 jam, baik puncak Mg (101) maupun puncak AI (111) mulai menghilang. Hilangnya puncak-puncak fasa Mg ini bukan berarti bahwa kandungan fraksi volume dari Mg di dalam campuran berkurang, namun struktur kristal Mg sebagian telah rusak dan berubah menjadi amori, dan sebagian lagi telah bereaksi dengan AI membentuk Mg2A13. Namun akhir dari proses milling ini masih menyisakan sejumlah kecil puncak AI yang diduga belum bereaksi dengan Mg untuk membentuk Mg2AI3
sekitar kurang dari 5%. Dengan demikian proses mechanical alloying sangat efektif untuk
membuat paduan Mg2AI3 dengan waktu minimum milling selama
10
jam, artinya semakin lama proses milling semakin banyak fasa Mg2AI3 yang terbentuk. Komposisi terakhir fasaMg2AI3 yang terbentuk setelah milling selama 30 jam sebesar 96,19%, sisanya terdiri dari fasa Mg dan AI, yang masing-masing besarnya kurang dari 5%.
Analisis strukturmikro dari hasil foto SEM baik setelah milling 10 jam, 20 jam, dan 30 jam ditunjukkan pada Gambar 4.13. Hasil Gambar foto SEM tersebut menunjukkan bahwa cuplikan setelah milling
10
jam, partikel memiliki bentuk yang relatif sama dengan distribusi ukuran partikel yang ked I hampir merata di seluruh permukaan cuplikan walaupun masih ada beberapa ukuran partikel yang cukup besar. Hal ini menunjukkan bahwa proses penghancuran dari partikel Mg dan AI telah terjadi. Setelah milling 20 jam, tampak bahwa sebagian partikel-partikel kedl tersebut menyatu membentuk partikel yang lebih besar, sehingga jumlah partikel yang besar menjadi bertambah walaupun masih terdapat partikel-partikel kedl. Kemudian setelah milling selama 30 jam, jumlah partikel-partikel yang berukuran besar bertambah banyak dan hampir merata di seluruh permukaan cuplikan. Hal yang sangat menarik untuk di kaji dari hasil foto SEM ini adalah dengan bertambahnya waktu milling, idealnya bahwa ukuran partikel tersebut akan menjadi lebih kedl, namun yang terjadi adalah sebaliknya, bahwa ukuran partikel menjadi lebih besar. Hal ini diduga pada cuplikan telah terjadi pembentukan fa sa baru, yaitu hasil reaksi antara perpaduan partikel Mg dan AI. Namun hasil ini perlu adanya konfirmasi lebih lanjut dengan karakterisasi yang lain.(a) Fata SEM dari cuplikan Mg-AI setelah milling 10 jam
(b) Fata SEM dari cuplikan Mg-AI
setelah milling 20 jam
(c) Fata SEM dari cuplikan Mg-AI jam
setelah milling 30
Analisis fasa dan strukturmikro paduan sistem Mg-Ni dan Mg-AI (Wisnu Ari Adi, S.Si.)
Karakterisasi lain yang menunjang hasil pengamatan foto SEM tersebut adalah analisis fasa dari pola difraksi sinar-X masing-masing cuplikan. Hasil analisis dengan menggunakan program Rietveld menunjukkan bahwa baik cuplikan Mg-AI setelah milling
10
jam, 20 jam dan 30 jam, mengandung 3 fasa, yaitu fa sa Mg, fasa AI, dan fasa Mg2A13.
Berdasarkan hasil refinement dari profil difraksi sinar-X seperti yang terlihat pada Gambar 4.13 menunjukkan bahwa pad a awalnya sebelum milling campuran tidak mengandung impuritas dan hanya terdiri dari fasa Mg dan AI. Kemudian selama milling, terjadi proses
mechanical alloying, yaitu serbuk-serbuk Mg dan AI secara periodik terjebak diantara
bola-bola yang saling bertumbukan secara plastis terdeformasi. Akibat bola-bola yang saling bertumbukan tersebut menyebabkan perpatahan, kemudian terjadi penyatuan dingin (cold
welding) dari serbuk-serbuk secara elementer. Ketika waktu milling meningkat, fraksi volume
unsur-unsur dari bahan dasar menurun, sedangkan fraksi volume paduan meningkat.
Hasil perhitungan dengan menggunakan analisis Rietveld menunjukkan bahwa fraksi fasa Mg2AI3 meningkat seiring bertambahnya waktu milling seperti yang ditunjukkan pada Gambar 4.14. 60 120 - 50 100 ~ "'Tl ~ QJ
«
'" c:: 40 80 !!1. co :s: "00) C/I ___ Mg w ~ 30-e-
AI 60 C/I w co :s: -.k- Mg2AI3 C/I C/I co co '" ~ 20 '" 40 ~ 'w ~ :r. co U: 10 20 0 0 0 102030Waktu Milling Uam)
Gambar 4. 14. Pertumbuhan fraksi massa fasa Mg2AIs dengan meningkatnya waktu milling
Pad a Gambar 4.14 tampak bahwa hasil perhitungan fraksi massa komposisi fasa sebelum milling adalah 43,3% fasa Mg dan 56,7% fasa AI. Kemudian setelah milling 10 jam, fraksi massa fasa Mg dan AI mulai berkurang berturut-turut menjadi 6,37% dan 21,81%, sedangkan tumbuh fasa baru Mg2AI3 dengan fraksi massa sebanyak 71,82%. Apabila dikonfirmasi dengan hasil pengamatan foto SEM menunjukkan bahwa serbuk mulai mengecil dan sebagian diduga telah mengalami penyatuan. Setelah milling 20 jam, fraksi massa fasa Mg dan AI berkurang lagi berturut-turut menjadi < 1% dan 8,89%, sedangkan fraksi massa fasa Mg2AI3 meningkat menjadi 90,73%. Dari foto SEM menunjukkan bahwa serbuk mulai lebih menyatu dan serbuk-serbuk Mg dan AI sudah tidak tampak lagi, namun belum seluruhnya terdifusi membentuk fasa baru. Hingga pada akhirnya setelah milling 30 jam,
komposisi fraksi massa masing-masing fasa Mg, AI, dan Mg2AI3 berturut-turut menjadi 0,48%; 3,32%; dan 96,19%. Dari foto SEM, pada tahap ini hampir keseluruhan telah terbentuk fasa baru.
Hasil pengamatan SEM dan analisis fasa XRD ini didukung berdasarkan tinjauan secara mikrostruktural diantaranya adalah perhitungan ukuran kristalit dengan menggunakan formula Sheerer seperti yang ditunjukkan pada Gambar 4.15. Gambar 4.15 merupakan hasil perhitungan ukuran kristalit (grain size) masing-masing cuplikan dari sebelum di milling hingga setelah milling selama 30 jam.
60 ..-.. 50
E
c
~ 40 co .•... I/) .~ 30 :::t::c
~ 20 ::J ~ => 10 ..•...Fasa Mg2AI3 --- Fasa Mg-k-
Fasa AI o o 5 10 15 20 25 30 35Lama Milling Uam)
Gambar
4.15.
Ukuran kristalit cuplikan Mg-AI sebelum milling,setelah milling 10 jam, 20 jam, dan 30 jam
Pada awalnya sebelum di milling ukuran kristalit Mg sebesar 55 nm dan AI sebesar 41 nm. Setelah milling selama 10 jam, ukuran kristalit Mg dan AI berubah berturut-turut menjadi 4 nm dan 13 nm. Sedangkan muncul kristal baru Mg2AI3 dengan ukuran kristalit sebesar 3 nm. Pada tahap ini terjadi proses pengecilan ukuran kristal akibat efek milling. Ukuran kristalit baik Mg maupun AI yang sangat kecil ini memberikan peluang besar keduanya untuk bereaksi membentuk kristal baru, yaitu kristal Mg2A13. Kemudian milling
berikutnya, setelah 20 jam hingga 30 jam, ukuran kristalit dari Mg dan AI semakin mengecil ditandai dengan profil puncak XRD tampak semakin amort. Hal ini berarti bahwa baik kristal Mg dan AI telah rusak atau hancur. Sedangkan ukuran kristalit Mg2AI3 semakin membesar ditandai dengan semakin menajamkan profil puncak pada fasa ini. Hal ini berarti kristal
Mg2AI3 semakin tumbuh dengan baik.
BAB V KESIMPULAN
Dalam penelitian ini telah dilakukan sintesis paduan sistem Mg-Ni dan Mg-AI dengan menggunakan teknik mechanical alloying. Hasil refinement dari pol a difraksi sinar-X keduanya menunjukkan bahwa hasil fiffing antara observasi dan kalkulasi sudah cukup baik. Sehingga dari hasil sintesis terse but dapat disimpulkan sebagai berikut:
1.
Hasil mechanical alloying pad a paduan sistem Mg-Ni menunjukkan bahwa cuplikan terdiri dari 4 fasa, yaitu: fasa Mg, Ni, Mg2Ni, dan fasa MgNi2. Dan telah terjadi pertumbuhan fasa Mg2Ni pada milling selama 10 jam, 15 jam, 20 jam, dan 25 jam berturut-turut sebesar 23,32%; 45,3%; 62,04%, dan 87,44%. Sedangkan hasilmechanical alloying pad a paduan sistem Mg-AI menunjukkan bahwa cuplikan terdiri dari
3 fasa, yaitu : fasa Mg, AI, dan Mg2A13•Pertumbuhan fasa Mg2AI3 pada milling selama
10
jam, 20 jam, dan 30 jam berturut-turut sebesar 71 ,82%; 90,73%; dan 96,19%.
2. Dan hasil pengamatan dengan menggunakan Scanning Electron Microscope (SEM)
menunjukkan bahwa mekanisme pembentukan Mg2Ni dengan metode mechanical
alloying sangat bersesuaian dengan ilustrasi yang disampaikan oleh Benyamin dan
Volin. Pembentukan awal paduan Mg2Ni tampak pada waktu milling selama
10
jam, dan waktu milling minimum untuk memperoleh fasa Mg2Ni lebih dari 80% adalah selama 25 jam. Sedangkan untuk membuat paduan Mg2AI3 diperlukan waktu minimum millingsetelah
10
jam, artinya semakin lama proses milling semakin banyak fasa Mg2AI3 yang terbentuk.3. Hasil perhitungan fraksi mass a komposisi fa sa sebelum milling ukuran kristalit Mg dan AI berturut-turut adalah 55 nm dan 41 nm. Kemudian setelah milling selama 10 jam, fraksi massa fasa Mg dan AI mulai berkurang dengan ukuran kristalit mengecil, sedangkan
Analisis fasa dan strukturmikro paduan sistem Mg-Ni dan Mg-AI (Wisnu Ari Adi, S.Si.)
tumbuh fasa baru Mg2AI3 dengan fraksi massa sebanyak 71,82% dengan ukuran kristalit 3 nm. Serbuk mulai mengecil dan sebagian diduga telah mengalami penyatuan. Setelah
milling 20 jam, fraksi massa fasa Mg dan AI berkurang lagi dengan ukuran kristalit
semakin mengecil, sedangkan fraksi massa fasa M92AI3 meningkat dengan ukuran kristalit semakin bertambah besar. Serbuk mulai lebih menyatu dan sudah tidak tampak lagi serbuk-serbuk Mg dan AI, namun belum seluruhnya terdifusi membentuk fasa baru. Hingga pada akhirnya setelah milling 30 jam, komposisi fraksi massa masing-masing fasa Mg dan AI semakin hilang, sedangkan Mg2AI3 semakin dominan dengan ukuran krsitalit semakin membesar. Pada tahap ini hampir keseluruhan telah terbentuk fasa Mg2A13·
DAFT AR PUST AKA
[1] BORMAN, R, Hydrogen Storage Materials, http://www.hydrogen.html. 2006. [2] PYLE, W., Hydrogen Storage Materials, http://www.hydrogen.html. 2006 [3] B. ARNASON, T.I. SIGFUSSON, Int. J. Hydrogen Energy, 25 (2000) 389.
[4] ZUTEL, A., Materials for Hydrogen Storage, http://www.elsevier.com. 2006. [5] H. BUCHENER, R POVEL, Int. J. Hydrogen Energy, 7 (1982) 259.
[6] M. DORNHEIM, T. KLASSEN, R BORMANN, Hydrogen Storage Materials, Institute for
Materials Research, GKSS Research Center, Geesthacht, Germany, Browsing from internet.
[7] TETSUO SAKAI, ITUKI UEHARA, HIROSHI ISHIKAWA, Journal of Alloys and
Compounds, 293-295 (1999), 762-769.
[8] Y. FUKAI, The Metal-Hydrogen System - Basic Bulk Properties, Verlag, Berlin, 1993.
[9] HUANG, K. YVON, P. Fisher, J. Alloys Camp., 227(1995)121.
[10] G. LIANG, J. HUOT, S. BOILY, AV. NESTE, R SCHULTz, J. Alloys Camp.,
348(2003)319.
[11] B. ARNASON, T.I. SIGFUSSON, Int. J. Hydrogen Energy, 25 (2000) 389.
[12] ZALUSKA, L. ZALUSKI, J.O. STROM-OLSEN, J. Alloys Camp., 228(1999)217. [13] ZALUSKA et al., Appl. Phys. A, 72 (2001) 157-165 (review paper).
[14] ANDON INSANI, HADI SUWARNO, JOHNY WAHYUADI, WISNU ARI ADI, DAN EDDY S., Studi Difraksi Sinar-X pada Pembuatan Paduan Mg-Co-Ni yang Dibuat dengan Metode Pemaduan Mekanik (Mechanical Alloying), Jurnal Sains Materi Indonesia, ISSN:
1411-1098, Edisi Khusus Oktober 2006, 35-39.
[15] HADI SUWARNO, ANDON INSANI DAN WISNU ARI ADI, The X-ray Diffraction
Analyses on The Mechanical Alloying of The Mg2Ni Formation, Jurnal Teknologi Bahan
Nuklir, ISSN: 1907-2635, Volume 3, Nomor 2, Juni 2007,74-85.
[16] LEVINSON, D.W., MCPHERSON, D.J., Transactions of The American Society for Metal, 48, (1956) 689-705.
[17] ANDREASEN, A., SORENSEN, M.B., BURKARL, R, MOLLER, B., MOLENBROEK, AM., PEDERSEN, AS., ANDREASEN, J.W., NIELSEN, M.M., JENSEN, T.R,
J.
alloys Camps., Accepted.[18] LUO, H.L., CHAO, C.C., DUWES, P., Transactions of The Metallurgy Society of Aime,
230, (1964) 1488-1490.
[19] HAD I SUWARNO, WISNU A.A., ANDON I., International Conference Solid State Ionic
Proceeding, PTBIN, Serpong, 2007.
[20] WISNU ARI ADI, ANDON INSANI DAN HADI SUWARNO, Analisis Struktur Kristal
Paduan Mg2Ni Hasil Mechanical Alloying, Jurnal Sains Materi Indonesia, ISSN :
1411-1098, Volume 9, Nomor 2, Februari 2008,125-130.
[21] H. SUWARNO, W. ARI ADI, DAN A INSANI, New Synthesis Method of The Mg2Ni
Compound by Using Mechanical Alloying for Hydrogen Storage, Atom Indonesia, ISSN:
0126-1568, Volume 34, Nomor 2, July 2008, 69-78.
[22] WISNU ARI ADI, HADI SUWARNO, ANDON INSANI DAN NUSIN S., Mekanisme
Pembentukan Fasa Mg2Ni Dengan Metode Mechanical Alloying, Jurnal Sains Materi
Indonesia, ISSN: 1411-1098, Volume 10, Nomor 1, Oktober 2008, 60-65.
[23] BOUARICHA, S., DODELET, J.P., GUAY, D., HUOT, J., BOILY, S., SCHULZ, R,
[24] WISNU ARI ADI DAN HADI SUWARNO, Analisis Pembentukan Fasa _ -MgH2 Hasil Proses Hydriding Paduan Mg-AI, sedang dalam proses penerbitan di Jurnal Sains Materi
Indonesia.
[25] CRIVELLO, J.C., NOBUKI, T., KATO, S., ABE, M., KUJI, T., Journal of Advanced Science, vol. 19, 2007, 3-4.
[26] H.M. RIETVELD, J. Appl. Chryst. 2, 65, 1969.
[27] F. IZUMI, rigaku J.Q,1 , 1989.
[28] F. IZUMI, "A Rietveld-Refinement Program RIETAN-94 for Angle-Dispersive X-Ray and
Neutron Powder Diffraction", National Institute for Research in Inorganic Materials 1-1
Namiki, Tsukuba, Ibaraki 305, Japan, Revised on June 22, 1996.
[29] SUKIRMAN, E., Pengaruh Distribusi Kekosongan Oksigen pada Superkonduktivitas YBa2Cu307_X,Thesis Magister Pasca Sarjana Universitas Indonesia, 1991.
[30] HARRIS, J.R., Matemathical Modelling of Mechanical Alloying, Thesis submitted to The
University of Nottingham for the degree of Doctor of Physlosophy, September 2002.
[31] Mechanical Alloying, Casa Study, http://www.msm.cam.ac.uk/phase-trans/pubs/
![Gambar 2.2. Beberapa contoh kendaraan bermotor yang menggunakan hidrogen 2.2. Metode Analisis Rietveld [26-29]](https://thumb-ap.123doks.com/thumbv2/123dok/4547592.3303561/5.928.167.738.104.495/gambar-kendaraan-bermotor-menggunakan-hidrogen-metode-analisis-rietveld.webp)
![Gambar 2.3. Proses tumbukan bola-bola dalam media milling [30].](https://thumb-ap.123doks.com/thumbv2/123dok/4547592.3303561/7.918.141.626.775.927/gambar-proses-tumbukan-bola-bola-media-milling.webp)
![Gambar 2.4. Tahapan mechanical alloying menurut referensi Benyamin dan Volin [30].](https://thumb-ap.123doks.com/thumbv2/123dok/4547592.3303561/8.932.183.776.118.238/gambar-tahapan-mechanical-alloying-menurut-referensi-benyamin-volin.webp)