Minggu
ke
Pokok Bahasan
Tujuan Instruksional Umum
Tujuan Instruksional Khusus
Materi
Ref
.
1 1. Materi
2 X 50’
Pada akhir pokok bahasan ini mahasiswa diharapkan dapat : 1. Memahami pengertian materi,
penggolongannya dan hal-hal yang menyangkut materi dan perubahannya sebagai dasar dalam mempelajari kimia
Setelah mempelajari pokok bahasan ini mahasiswa dapat :
1. Menjelaskan pengertian materi dan memberikan contoh-contohnya
2. Menerangkan pengertian massa dan berat
3. Menjelaskan sifat fisika, sifat kimia, sifat ekstrinsik dan sifat intrinksik materi
4. Memahami perubahan-perubahan yang dapat terjadi pada materi beserta contoh-contohnya
5. Menerangkan perbedaan zat murni (unsur dan senyawa) dan campuran (homogen dan heterogen)
6. Menyebutkan dan menjelaskan hukum-hukum yang berkaitan dengan materi (hukum Kekekalan Massa, Hukum Perbandingan
1.1. Pengertian Materi 1.2. Massa dan Berat 1.3. Sifat Materi 1.4. Perubahan Materi 1.5. Klasifikasi Materi 1.6. Hukum-hukum yang berhubungan dengan materi 1.6.1. Hukum Kekekalan Massa 1.6.2. Hukum Perbandingan Tetap 1.6.3. Hukum Perbandingan Berganda
ke
.
2 & 3 2. Struktur Atom4 X 50’
Pada akhir pokok bahasan ini mahasiswa diharapkan dapat :
1. Menjelaskan partikel-partikel penyusun atom, menerangkan perkembangan model atom serta konfigurasi elektron dalam atom
Setelah mempelajari pokok bahasan ini mahasiswa dapat :
1. Menjelaskan Teori Atom Dalton 2. Menjelaskan partikel-partikel
penyusun atom (elektron, proton dan neuron) dan percobaan yang mendasari penemuan tersebut 3. Memahami dan menerangkan
Model Atom Thamson, Rutherford, Bohr dan Mekanika Kuantum
4. Menerangkan konfigurasi elektron dalam suatu atom dan aturan-aturan yang berlaku dalam konfigurasi elektron
2.1. Partikel Penyusun Atom 2.2. Perkembangan Model 2.2.1. Model Atom Thomson 2.2.2. Model Atom Rutherford 2.2.3. Model Atom Bohr 2.2.4. Model Atom Mekanika Kuantum 2.3. Konfigurasi Elektron 2.3.1. Aturan Aufbau 2.3.2. Aturan Hund 2.3.3. Larangan Pauli
Minggu
ke
Pokok Bahasan
Tujuan Instruksional Umum
Tujuan Instruksional
Khusus
Materi
Ref
.
4 3. Tabel Periodik2 X 50’
Pada akhir pokok bahasan ini mahasiswa diharapkan dapat :
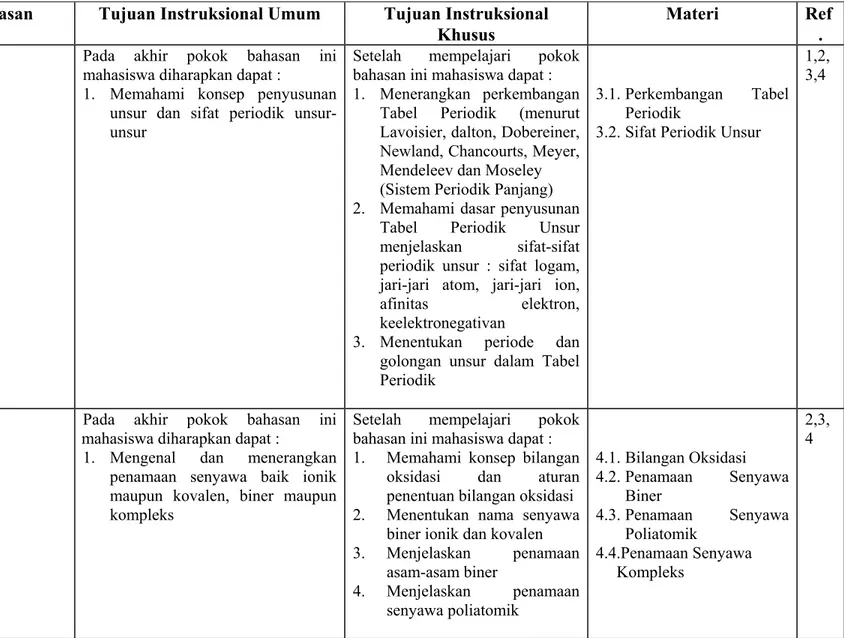
1. Memahami konsep penyusunan unsur dan sifat periodik unsur-unsur
Setelah mempelajari pokok bahasan ini mahasiswa dapat : 1. Menerangkan perkembangan
Tabel Periodik (menurut Lavoisier, dalton, Dobereiner, Newland, Chancourts, Meyer, Mendeleev dan Moseley (Sistem Periodik Panjang) 2. Memahami dasar penyusunan
Tabel Periodik Unsur menjelaskan sifat-sifat periodik unsur : sifat logam, jari-jari atom, jari-jari ion, afinitas elektron, keelektronegativan
3. Menentukan periode dan golongan unsur dalam Tabel Periodik
3.1. Perkembangan Tabel Periodik
3.2. Sifat Periodik Unsur
1,2, 3,4
5 4. Tata Nama Pada akhir pokok bahasan ini
mahasiswa diharapkan dapat :
1. Mengenal dan menerangkan
Setelah mempelajari pokok bahasan ini mahasiswa dapat :
1. Memahami konsep bilangan 4.1. Bilangan Oksidasi
2,3, 4
ke
Khusus
.
6 & 7 5. Ikatan Kimia4 X 50’
Pada akhir pokok bahasan ini mahasiswa diharapkan dapat :
1. Menerangkan macamikatan kimia 2. Menerangkan terjadinya ikatan
kimia
3. Menjelaskan bentuk molekul suatu senyawa
Setelah mempelajari pokok bahasan ini mahasiswa dapat : 1. Menjelaskan peranan elektron
valensi dalam pembentukan ikatan kimia
2. Memahami aturan Oktet menggunakan lambang Lewis dan membuat struktur Lewis untuk menggambarkan senyawa atau ion poliatomik 3. Memahami pengertian ikatan
ion dan ikatan kovalen serta perbedaan keduanya
4. Membedakan ikatan kovalen tunggal, kovalen rangkap dan kovalen koordinat serta memberikan contoh-contohnya
5. Menjelaskan penympangan aturan oktet dan terbentuknya resonansi
6. Memahami dan dapat membedakan ikatan polar dan non polar, serta memahami konsep keelektronegativan yang berkaitan dengan jenis ikatan kimia yang terbentuk 7. Menjelaskan bentuk-bentuk
molekul diatomik, triatomik, caturatom, pancaatom, dsb
5.1. Peranan Elektron dalam Pembentukan Ikatan Kimia
5.2. Peranan Elektron dalam Pembentukan Ikatan Kimia
5.3. Pembentukan Ikatan Ion 5.4. Pembentukan Ikatan Kovalen 5.4.1. Ikatan Kovalen Tunggal 5.4.2. Ikatan Kovalen Rangkap 5.4.3. Ikatan Kovalen Koordinat 5.5. Penyimpangan Aturan Oktet
5.5.1. Oktet Tak Lengkap 5.5.2. Oktet Berkembang 5.5.3. Species Ganjil 5.6. Resonansi
5.7. Kepoloran Ikatan dan Keelektronegativan 5.8. Bentuk Molekul
1,2, 3,4
Minggu
ke
Pokok Bahasan
Tujuan Instruksional Umum
Tujuan Instruksional
Khusus
Materi
Ref
.
8 6. Persamaan Kimia2 X 50’
Pada akhir pokok bahasan ini mahasiswa diharapkan dapat : 1. Memahami dan menjelaskan apa
yang disebut reaksi kimia
2. Menerangkan bagaimna suatu reaksi kimia dituliskan
3. Mengetahui prinsip utama dari reaksi kimia
Setelah mempelajari pokok bahasan ini mahasiswa dapat : 1. Menuliskan persamaan kimia
untuk menyatakan reaksi kimia
2. Menentukan koefisien reaksi pada persamaan kimia
3. Menerangkan pentingnya jumlah (kuntitatif) dalam persamaan kimia 4. Menyebutkan dan membedakan macam-macam reaksi kimia 6.1. Persamaan Kimia 6.2. Cara Menentukan Koefisiensi Reaksi 6.3. Jenis-jenis Reaksi Kimia 6.3.1. Reaksi Kombinasi 6.3.2. Reaksi Penguraian 6.3.3. Reaksi Pembakaran 6.3.4. Reaksi Pertukaran Tunggal 6.3.5. Reaksi Pertukaran Rangkap 6.3.6. Reaksi Netralisasi 1,2, 3,4 9 & 10 7. Stoikiometri 4 X 50’
Pada akhir pokok bahasan ini mahasiswa diharapkan dapat :
1. Mengenal dan menerangkan cara-cara pengukuran yang meliputi perhitungan zat dan campuran
Setelah mempelajari pokok bahasan ini mahasiswa dapat : 1. Menuliskan bilangan
Avogadro dan menerangkan arti dari satu mol senyawa 2. Memahami dan menjelaskan
konsep mol
7.1. Bilangan Avogadro 7.2. Konsep Mol
7.3. Massa Atom dan Massa Molekul
Minggu
ke
Pokok Bahasan
Tujuan Instruksional Umum
Tujuan Instruksional
Khusus
Materi
Ref
.
5. Mengerjakan hitungan yangberhubungan dengan larutan campuran dan larutan yang diencerkan atau dipekatkan 6. Membedakan rumus empirik
dan rumus molekul
7. Menentukan pereaksi pembatas dalam reaksi kimia 8. Mendefinisikan istilah-istilah
hasil teoritis, hasil nyata dan persen hasildari suatu reaksi kimia dan menghitung jumlahnya
9. Menghitung jumlah hasil reaksi bila dua atau lebih reaksi terjadi serentak atau berurutan
7.4. Reaksi Kimia dalam Larutan 7.4.1. Konsentrasi dalam Satuan Fisika Jumlah Solute persatuan volume larutan Persen Komposisi Massa Solute per massa solvent 7.4.2. Kosentrasi dalam Satuan Kimia 7.5. Rumus Empirik dan
Rumus Molekul
7.6. Hal-hal Kompleks dalam Reaksi Kimia 7.6.1. Pereaksi Pembatas 7.6.2. Hasol Teoritis, Hasil
Nyata dan Persen Hasil
7.6.3. Reaksi Serentak dan Berurutan
Minggu
ke
Pokok Bahasan
Tujuan Instruksional Umum
Tujuan Instruksional
Khusus
Materi
Ref
.
11 8. Termokimia
2 X 50’
Pada akhir pokok bahasan ini mahasiswa diharapkan dapat :
1. Mengetahui banyaknya energi yang dipertukarkan antara campuran reaksi dan keadaan sekelilingnya, khususnya energi kalor yang dapat digambarkan dalam persamaan kimia
Setelah mempelajari pokok bahasan ini mahasiswa dapat : 1. Membedakan bentuk energi
kalor dan kerja
2. Menerangkan pengertian entalpi reaksi dan perubahan entalpi reaksi
3. Membedakan reaksi eksoterm dan reaksi endotern
4. Membedakan entalpi reaksi untuk berbagai jenis reaksi (entalpi pembentukan, penguraian, pembakaran) 5. Menerangkan
hubungan-hubungan yang melibatkan entalpi
6. Memahami konsep dasar dan cara menentukan energi ikatan
7. Memahami pengertian dan ciri proses spontan dan tidak spontan
8.1. Termodinamika
8.2. Kalor dan Kalor Reaksi 8.3. Entalpi dan Perubahan
Entalpi
8.4. Reaksi Eksoterm dan Endoterm 8.5. Hukum-hukum yang berlaku dalam Termokimia 8.5.1. Sifat Ekstensif 8.5.2. Hukum Laplace 8.5.3. Hukum Hess 8.6. Energi Ikatan 8.7. Arah Proses 1,3, 4
ke
Khusus
.
12 9. Gas Pada akhir pokok bahasan ini
mahasiswa diharapkan dapat :
1. Memahami dan menerangkan sifat-sifat gas
Setelah mempelajari pokok bahasan ini mahasiswa dapat : 1. Menerangkan sifat-sifat fisis
gas
2. Memahami konsep Tekanan gas
3. Memahami dan menggunakan Hukum Boyle, Hukum Charles dan Hukum Avogadro untuk menyelesaikan soal-soal yang berkaitan dengan gas
4. Memahami konsep persamaan gas ideal dan menggunakannya dalam perhitungan
9.1. Sifat-sifat gas 9.2. Tekanan gas
9.3. Beberapa Hukum yang Berlaku pada gas 9.3.1. Hukum Boyle 9.3.2. Hukum Charles 9.3.3. Hukum Avogadro 9.4. Persamaan Gas Ideal
1, 4
Daftar Pustaka
1. Brady, James E., 1990, General Chemistry. Principles & Structure, fifh edition, John Wiley & Sons, New York
2. Holtzclaw, H.F. and W.r. Robinson, 1988, College Chemistry With Qualitative Analysis, eighth edition, D.C. Heath and Company, Lexington 3. Petrucci, R.H., 1990, Kimia Dasar, Prinsip dan Terapan Modern, Jilid 1 (terjemahan : Suminar dan Achmadi), Penerbit Erlangga, Jakarta 4. Tety Elida S., dkk., 1992, Pengantar Kimia, Penerbit Gunadarma, Jakarta