TUGAS PERANCANGAN PABRIK KIMIA
PRANCANGAN PABRIK BIOETANOL DARI ENCENG GONDOK
Disusun Oleh :
1. Eni Sumarsih 21030114120066
2. Reni Fatmawati 21030114120063 3. Richard Hartono 21030114120024
DEPARTEMEN TEKNIK KIMIA FAKULTAS TEKNIK UNIVERSITAS DIPONEGORO
BAB I
PENDAHULUAN
1.1. Latar Belakang
Eceng gondok (Eichhornia crassipes) merupakan gulma yang bersifat merugikan dan banyak ditemui di daerah perairan. Selain sebagai gulma, dalam jumlah yang besar enceng gondok akan mengakibatkan pendangkalan pada perairan seperti danau atau rawa khususnya di Rawa Pening. Eceng gondok berpotensi menghilangkan air permukaan sampai empat kali lipat jika dibandingkan dengan permukaan terbuka. Eceng gondok memiliki kecepatan tumbuh yang tinggi sehingga tumbuhan ini dianggap sebagai gulma yang dapat merusak lingkungan perairan. Eceng gondok dengan mudah menyebar melalui saluran air ke badan air lainnya.
Eceng gondok dapat tumbuh dengan cepat dan dapat mengakibatkan berbagai kesulitan seperti terganggunya transportasi, penyempitan sungai, dan permasalahan karena penyebarannya menutupi permukaan perairan. Kecepatan pertumbuhan eceng gondok di Rawa Pening mencapai 3,69% berat enceng gondok basah per hari (Widyanto, 1998), dan dalam waktu 30 hari, pertumbuhan eceng gondok sudah mencapai 110% lebih banyak daripada hari pertama. Dalam waktu 3–4 bulan saja, eceng gondok mampu menutupi lebih dari 70% permukaan rawa. Cepatnya pertumbuhan eceng gondok dan tingginya daya tahan hidup menjadikan tumbuhan ini sangat sulit dikendalikan. Keberadaan eceng gondok (Eichhornia crassipes) di perairan merupakan masalah bagi lingkungan perairan.
Untuk mengurangi permasalahan yang timbul akibat banyaknya eceng gondok di perairan, maka perlu dilakukan pemanfaatan terhadap ketersediaan eceng gondok yang sangat melimpah, salah satunya adalah pemanfaatan eceng gondok untuk pembuatan bioethanol. Eceng gondok dapat dimanfaatkan sebagai bahan baku untuk pembuatan bioethanol karena memiliki kandungan gula berupa selulosa. Selulosa merupakan homopolisakarida, dengan glukosa sebagai monomernya. Molekul selulosa berbentuk linier dan tak bercabang, dan terdiri
dari 10.000-15.000 unit D-glukosa (Lehninger, 2008). Perbedaan selulosa dengan amilosa yang juga polisakarida dari glukosa terletak pada konfigurasi residu glukosa penyusunnya. Selulosa tersusun dari residu-residu β-glukopiranosil yang dihubungkan dengan ikatan 1
à
4 (β1à
4), sedangkan amilosa oleh ikatan α1à
4. Selulosa dapat dihidrolisis menjadi glukosa dengan bantuan enzim selulase. Selulase merupakan kumpulan dari beberapa enzim yang bekerja bersama untuk hidrolisis selulosa. Mikroorganisme tertentu menghasilkan partikel yang dinamakan selulosom. Partikel inilah yang akan terdisintegrasi menjadi enzim-enzim, yang secara sinergis mendegradasi selulosa menjadi glukosa (Belitz dkk, 2008). Glukosa hasil hidrolisis selulosa ini kemudian difermentasi untuk menghasilkan bioethanol.Eceng gondok merupakan bahan baku potensial untuk dijadikan bioethanol karena ketersediaannya yang melimpah di Indonesia dan memiliki nilai ekonomis rendah. Di Rawa Pening, Kabupaten Semarang, eceng gondok dijual dengan harga berkisar Rp 2,800/Kg – Rp 3,500/Kg eceng gondok kering dan Rp 150/Kg- Rp 300/Kg eceng gondok basah. Potensi nilai tambah yang dihasilkan dalam pembuatan bioethanol dari eceng gondok cukup besar. Oleh karena itu, perancangan pabrik pembuatan bioethanol dari eceng gondok perlu dilakukan untuk mengetahui seberapa besar perkembangan potensi perkembangan industri ini di Indonesia
1.2 Tujuan
1. Untuk mengetahui spesifikasi bahan baku dan produk pembuatan bioetanol dari enceng gondok.
2. Untuk mengetahui dekripsi proses pembuatan bioetanol dari enceng gondok di suatu Industri
2. Untuk mengembangkan proses flow diagaram dari literatur 1.3 Manfaat
1. Dapat menjelaskan spesifikasi bahan baku dan produk pembuatan bioetanol dari enceng gondok
gondok
3. Dapat dan mampu mengembangakan proses flow diagram dari literatur
BAB II
TINJAUAN PUSTAKA
2.1 Eceng Gondok
Eceng gondok atau enceng gondok (Latin:Eichhornia crassipes) adalah salah satu jenis tumbuhan air mengapung. Selain dikenal dengan nama eceng gondok, di beberapa daerah di Indonesia, eceng gondok mempunyai nama lain seperti di daerah Palembang dikenal dengan nama Kelipuk, di Lampung dikenal dengan nama Ringgak, di Dayak dikenal dengan nama Ilung-ilung, di Manado dikenal dengan nama Tumpe. Eceng gondok pertama kali ditemukan secara tidak sengaja oleh seorang ilmuwan bernama Carl Friedrich Philipp von Martius, seorang ahli botani berkebangsaan Jerman pada tahun 1824 ketika sedang melakukan ekspedisi di Sungai Amazon Brasil. Eceng gondok memiliki kecepatan tumbuh yang tinggi sehingga tumbuhan ini dianggap sebagai gulma yang dapat merusak lingkungan perairan. Eceng gondok dengan mudah menyebar melalui saluran air ke badan air lainnya.
Gambar 1.1. Eceng Gondok
Pada tabel 1.2, (Anonymous, 1966) dalam penelitiannya terhadap eceng gondok dari Banjarmasin mengemukakan kandungan kimia tangkai eceng gondok tua yang segar.
Tabel 1.2. Kandungan Kimia Enceng Gondok Segar
Senyawa Kimia Presentase (%)
Air 92,6 Abu 0,44 Serat Kasar 2,09 Karbohidrat 0,17 Lemak 0,35 Protein 0,16 Fosfor 0,52 Kalium 0,42 Klorida 0,26 Alkanoid 2,22
Tabel 1.3. Kandungan Kimia Enceng Gondok Kering
Senyawa Kimia Presentase (%)
Selulosa 65
Pentosa 15
Lignin 20
2.2 Selulosa dan Enzim Selulase
Selulosa merupakan homopolisakarida, dengan glukosa sebagai monomernya. Molekul selulosa berbentuk linier dan tak bercabang, dan terdiri dari 10.000-15.000 unit D-glukosa (Lehninger, 2008). Perbedaan selulosa dengan amilosa yang juga polisakarida dari glukosa terletak pada konfigurasi residu glukosa penyusunnya. Selulosa tersusun dari residu-residu β-glukopiranosil yang dihubungkan dengan ikatan 1
à
4 (β1à
4), sedangkan amilosa oleh ikatan α1à
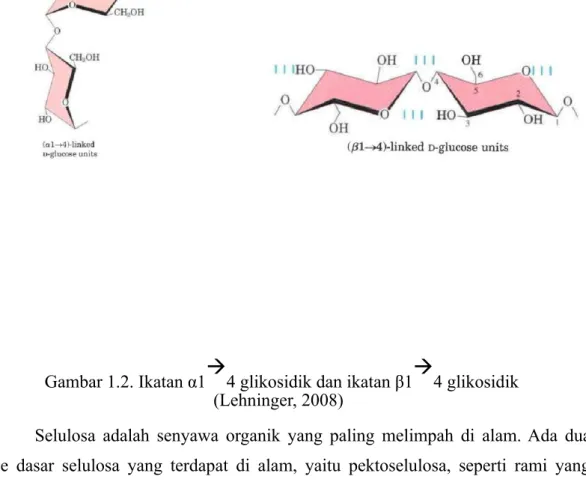
4. Akibatnya terdapat perbedaan yang kontras dalam hal struktur dan sifat fisik keduanya. Gambar 1.2 menunjukkan perbedaan ikatan glikosidik glukosa yang terdapat pada amilosa dan selulosa.Gambar 1.2. Ikatan α1
à
4 glikosidik dan ikatan β1à
4 glikosidik (Lehninger, 2008)Selulosa adalah senyawa organik yang paling melimpah di alam. Ada dua tipe dasar selulosa yang terdapat di alam, yaitu pektoselulosa, seperti rami yang mengandung 80% selulosa dan lignoselulosa yang terdiri dari selulosa, hemiselulosa, dan lignin. Sebagai senyawa utama penyusun dinding sel tanaman, selulosa mencakup sekitar 30% dari keseluruhan material tumbuhan (90% dari kapas dan 50% dari kayu merupakan selulosa.
Pemanfaatan selulosa telah dilakukan di berbagai bidang, di antaranya untuk produksi kertas, fiber, dan senyawa kimia turunannya untuk industri plastik, film fotografi, rayon, dan lainnya. Produk hidrolisis selulosa yaitu gula (glukosa) juga merupakan senyawa yang vital dalam industri bioproses. Oleh karena itu penggunaan selulosa sebagai sumber glukosa, di samping sebagai sumber energi terbarukan yang murah dan melimpah untuk berbagai keperluan semakin berkembang. Hidrolisis selulosa dapat dilakukan dengan menggunakan asam kuat maupun enzim selulase. Sebagai contoh, hewan herbivora dapat mengutilisasi selulosa sebagai bahan makanan karena memiliki rumen mikroflora untuk menghasilkan enzim selulase. Rumen mikroflora merupakan komunitas dari berbagai jenis mikroorganisme yang hidup di dalam perut hewan herbivora tersebut.
Selulase merupakan kumpulan dari beberapa enzim yang bekerja bersama untuk hidrolisis selulosa. Mikroorganisme tertentu menghasilkan partikel yang dinamakan selulosom. Partikel inilah yang akan terdisintegrasi menjadi
enzim-enzim, yang secara sinergis mendegradasi selulosa (Belitz dkk, 2008). Sedikitnya ada tiga enzim yang terlibat dalam degradasi atau hidrolisis selulosa, yaitu endo-β-glukanase, ekso-β-endo-β-glukanase, dan β-glukosidase. Nama lain dan fungsi dari enzim tersebut dalam hidrolisis selulosa dapat dilihat pada tabel 1.4.
Reaksi hidrolisis selulosa oleh selulase adalah sebagai berikut.
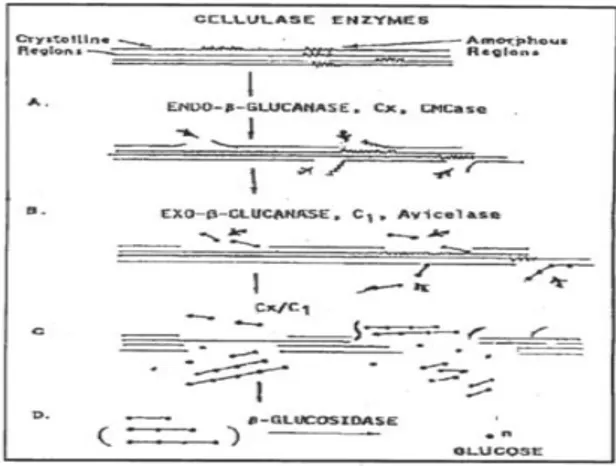
Tahapan-tahapan hidrolisis selulosa oleh selulase dapat dilihat pada Gambar 1.3. Faktor C1 sangat diinhibisi oleh produknya, sehingga selobiase
diperlukan agar hidrolisis selulosa dapat berlangsung. Selobiase juga diinhibisi oleh produknya, glukosa, sehingga hidrolisis sempurna selulosa hanya dapat dilakukan jika tersedia selobiase dalam jumlah besar atau glukosa yang terbentuk segera dipisahkan.
Gambar 1.3. Tahapan-Tahapan Hidrolisis Selulosa (Ghori, 2001) Tabel 1.4. Komponen Enzim di dalam Kompleks Enzim Selulase
(Belitz dkk, 2008)
EC No. Nama Sinonim Reaksi
3.2.1.4 Endo-β- Faktor Cx; Endohidrolisis ikatan
1,4-β-D-glukanase CMCase; 1,4-β-D- glukosidik, membentuk
glukan glukosa dan
3.2.1.91 Ekso- β- Faktor C1; Eksohidrolisis ikatan
1,4-β-D-glukanase avicelase; 1,4-β-D- glukosidik membentuk glukan selobiosa dari selulosa atau selobiohidrolase 1,4-β-glukooligosakarida. 3.2.1.21 β-glukosidase Selobiase; Hidrolisis residu β-D-glukosa
amygdalase terminal dalam β-glukan. 2.3 Bioethanol
Bioetanol merupakan bahan bakar yang bersih, hasil pembakaran menghasilkan CO2 dan H2O. Penambahan bahan yang mengandung oksigen
pada sistem bahan bakar akan mengurangi emisi gas CO yang sangat beracun dari sisa pembakaran. Aditif MTBE pada mulanya dipergunakan untuk meningkatkan nilai oktan, namun saat ini dilarang dipergunakan. MTBE dapat dideteksi dan menyebabkan pencemaran pada air tanah sehingga alkohol merupakan alternatif yang menarik untuk mengurangi emisi gas CO. Penggunaan alkohol murni dibanding dengan bensin secra umum akan mengurangi kadar CO2 hingga 13% karena merupakan hasil dari pertanian.
Seperti diketahui produk pertanian memerlukan gas CO2 untuk
metabolismenya. Bioetanol merupakan etanol yang diperoleh melalui proses fermentasi biomassa dengan bantuan mikroorganisme. Selain bioetanol dikenal pula gasohol, yang merupakan campuran bioetanol dengan premium. Misalnya gasohol E—10 mengandung bioetanol 10% dan sisanya premium. Bioetenol yang mengandung 35% oksigen dapat meningkatkan efesiensi pembakaran dan mengurangi emisi gas rumah kaca. Keuntungan lain dari bioetanol adalah nilai oktannya lebih tinggi dari premium sehingga dapat menggantikan fungsi bahan aditif seperti MTBE dan TEL. Bioetanol dapat langsung dicampur dengan premium pada berbagai komposisi sehingga dapat meningkatkan efesiensi dan emisi gas buang yang lebih ramah lingkungan.
2.4 Tahapan Proses 2.4.1 Pretreatment
Pretreatment biomassa lignoselulosa harus dilakukan untuk mendapatkan hasil yang tinggi di mana penting untuk pengembangan teknologi biokonversi dalam skala komersial. Sebagai contoh pretreatment yang baik dapat mengurangi
jumlah enzim yang digunakan dalam proses hidrolisis. Pretreatment dapat meningkatkan hasil gula yang diperoleh. Gula yang diperoleh tanpa pretreatment kurang dari 20%, sedangkan dengan pretreatment dapat meningkat menjadi 90% dari hasil teoritis. Tujuan dari pretreatment adalah untuk membuka struktur lignoselulosa agar selulosa menjadi lebih mudah diakses oleh enzim yang memecah polymer polisakarida menjadi monomer gula. Menurut (Sun & Cheng, dalam Isroi, 2008) pretreatment seharusnya memenuhi kebutuhan berikut ini :
a. meningkatkan pembentukan gula atau kemampuan menghasilkan gula pada proses berikutnya melalui hidrolisis enzimatik
b. menghindari degradasi atau kehilangan karbohidrat
c. menghindari pembentukan produk samping yang dapat menghambat proses hidrolisis dan fermentasi
d. biaya yang dibutuhkan ekonomis. 2.4.2 Hidrolisis
Proses hidrolisis terdiri dari tahap likuifikasi dan sakarifikasi. Tahap likuifikasi digunakan jamur Aspergillus niger yang menghasilkan enzim α-amilase untuk mendegradasi pati. Tahap sakarifikasi digunakan ragi Saccharomyces cerevisiae yang menghasilkan enzim glukoamilase untuk mengubah polisakarida menjadi gula yang dapat difermentasi (glukosa, galaktosa, manosa dan sebagainya). A. niger juga menghasilkan enzim selulase untuk mendegradasi selulosa. Beberapa mikroorganisme dapat melakukan fermentasi etanol dari substrat hasil degradasi eceng gondok, diantaranya Pichia stipitis NRLL Y-7124 (Nigam, 2002), ragi yang diisolasi dari bermacam-macam hidrosfer (Masami, dkk., 2008). Pada penelitian ini digunakan bakteri Zymomonas mobilis dan
Saccharomyces cerevisiae. 2.4.3 Fermentasi
Beberapa spesies mikroba dari kelompok yeast/khamir, bakteri dan fungi dapat memfermentasi karbohidrat menjadi ethanol dalam kondisi bebas oksigen. Mikroba melakukan fermentasi tersebut untuk mendapatkan omoge dan untuk
tumbuh. Reaksi yang terjadi dalam proses fermentasi pembuatan etanol adalah sebagai berikut :
C6H12O6
à
2 C2H5OH + 2 CO2Metode fermentasi untuk gula C6 telah diketahui dengan baik sejak paling tidak 6000 tahun yang lalu, ketika orang-orang Sumeria, Babylonia, dan Mesir mulai membuat bir dari nira. Mikroba yang sangat umum dimanfaatkan dalam proses fermentasi adalah ragi roti (Saccharomyces cereviseae) dan Zymomonas mobilis. Saccharomyces cereviseae memiliki banyak keunggulan antara lain adalah mampu memproduksi ethanol dari gula C6 (heksosa), toleran terhadap konsentrasi ethanol yang tinggi dan toleran terhadap senyawa inhibitor yang terdapat di dalam hidrolisat biomassa lignoselulosa (Olsson and Hahn-Hägerdal dalam Isroi,2008). Namun demikian, strain liar dari S. cerevieae tidak dapat memfermentasi gula C5 (pentose) seperti: xylosa, arabinosadan celloligosaccharides, menjadi salah satu kendala pemanfaatannya. Beberapa yeast diketahui dapat memfermentasi xylosa seperti: Pichia stipitis (Verduyn et al. dalam Isroi, 2008).
BAB III
DESKRIPSI PROSES
3.1. SPESIFIKASI BAHAN BAKU DAN PRODUK 3.1.1 Spesifikasi Bahan Baku 1. Eceng Gondok
¨ Wujud : padat
¨ Kenampakan : hijau tua
¨ Komposisi : selulosa 65 % berat
: pentosa15 % : lignin 20 %
(Anonymous, 1966) 2. Air
¨ Wujud : cairan
¨ Kenampakan : bening tidak berwarna
¨ Bau : tidak berbau
¨ Densitas : 0,994 gr/cc (pada 30oC) ¨ Turbidity : 10 ppm ¨ Oxygen consumed : 10 ppm ¨ Dissolved Oxygen : 0,1 ppm ¨ H2S : 3 ppm ¨ Total hardness : 40 ppm (Beatricx, 2010) 3. Aspergillus niger ¨ Kadar air : 50-70% ¨ Temperature : 35˚C-37˚C ¨ pH : 2,2-8,8 ¨ Kelembaban : 80-90%
4. Saccharomyces cerevisiae ¨ Kadar air : 4-6% ¨ Temperature : 28˚C-60˚C ¨ pH : 3,5-6,0 (Roehr, 2001) 3.1.3 Spesifikasi Produk
Produk yang dihasilkan adalah etanol.Etanol yang dihasilkan di industri dan akan digunakan sebagaibahan bakar harus didenaturasi agar tidak dijadikan bahan minuman. Pemerintah melalui Badan Standar Nasional (BSN) telah menetapkan Standar Nasional Indonesia (SNI) 7390:2008 tentang bioetanol terdenaturasi untuk gasohol. Oleh karena itu,pabrik ini akan membuat produk bioetanol sesuai dengan syarat mutu yang telah ditetapkan oleh BSN tersebut. Berikut adalah persyaratan mutu bioetanol terdenaturasi untuk gasohol menurut SNI tersebut di atas:
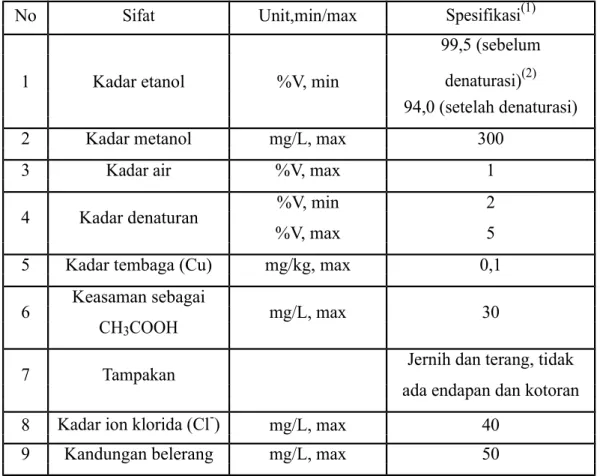
Tabel 2.1. Persyaratan Mutu Produk Etanol
No Sifat Unit,min/max Spesifikasi(1)
99,5 (sebelum
1 Kadar etanol %V, min denaturasi)(2)
94,0 (setelah denaturasi)
2 Kadar metanol mg/L, max 300
3 Kadar air %V, max 1
4 Kadar denaturan %V, min 2
%V, max 5
5 Kadar tembaga (Cu) mg/kg, max 0,1
6 Keasaman sebagai mg/L, max 30
CH3COOH
7 Tampakan Jernih dan terang, tidak
ada endapan dan kotoran
8 Kadar ion klorida (Cl-) mg/L, max 40
(S)
10 Kadar getah (gum), mg/100mL, max 5.0
dicuci
11 pHe 6,5-9,0
Berdasarkan persyaratan mutu yang ditentukan oleh SNI, maka pabrik ini akan membuat bioetanol dengan konsentrasi 99,5%.
3.2. KONSEP PROSES 3.2.1. Dasar Reaksi
Proses pembentukan etanol dari eceng gondok berlangsung dalam empat tahap, yaitu pretreatment lignoselulosa, proses hidrolisis selulosa menjadi glukosa, proses fermentasi glukosa menjadi etanol, dan proses pemekatan etanol dengan konsentrasi yang diharapkan 99%. Reaksi hidolisis selulosa menjadi glukosa bersifat endotermis (membutuhkan panas) dan irreversible. Reaksi yang terjadi pada proses hidrolisisselulosa adalah :
(C6H10O5)n+H2O
à
2C6H12O6Pertumbuhan inokulum dan reaksi fermentasi glukosa berlangsung pada kondisi aerob. Reaksi fermentasi bersifat eksotermis (melepaskan panas) dan irreversible. Reaksi berjalan di dalam fermentor dan bereaksi secara stokiometris dan untuk menjaga agar pH tetap konstan digunakan larutan buffer NH3.
Inokulum ditambahkan 2% dari volume media dan konversi reaksi glukosa sebesar 95%. Reaksi aerob pertumbuhan Saccharomyces cerevisiae adalah sebagai berikut :
C6H12O6 + 2,28 O2 + 2,08 NH3 → 4CH1,737N0,2O0,451 + 2CO2 + 5,92 H2O
Reaksi aerob proses fermentasi glukosa menjadi etanol : C6H12O6à
2C2H5OH + 2CO2ΔH= -78,414 kJ
Kondisi operasi: temperatur fermentasi 32°C, 1 atm, waktu 24 jam, pH 4-5.
Dari tinjauan termodinamika dapat diketahui sifat reaksi (endotermis dan eksotermis), pengaruh temperatur terhadap kesetimbangan reaksi. Data termodinamika reaksi fermentasi sebagai berikut :
ΔH˚f reaksi = ΔHof produk - ΔHof reaktan
ΔH˚f C6H12O6 = -1.264,0 kJ/mol
ΔH˚fC2H5OH = -277,698 kJ/mol
ΔH˚fCO2 = -393,509 kJ/mol
ΔH˚f reaksi = -78,414 kJ (eksotermis).
Reaksi bersifat dapat balik (reversible) dan searah (irreversible) dapat ditentukan secara termodinamika, yaitu berdasarkan persamaan Van’t Hoff.
=
Di mana : K = Konstanta kesetimbangan reaksi = panas reaksi T = Temperature
Terlihat semakin tinggi suhu maka konversi yang didapat akan semakin kecil. Ditinjau dari energy Gibbs ( ˚)
˚ = ˚ produk - ˚ reaktan = - 18606,57
˚ = - RT ln K
- 18606,57 = - 8,314 x 298 x ln K ln K = 7,51à K = 18,39 x 102
Dari perhitungan K di atas, diketahui bahwa harga K besar menunjukkan bahwa reaksi fermentasi glukosa menjadi etanol searah (irreversible) maka kenaikan suhu kurang berpengaruh terhadap konstanta kesetimbangan.
2.2.2. Kinetika Reaksi
Tinjauan kinetika pada reaktor sendiri dapat diketahui dengan persamaan Arhenius
k = Ae
-Ea/RTDari persamaan tersebut nampak bahwa semakin tinggi suhu maka konstanta kecepatan reaksi akan semakin besar, sehingga laju reaksi akan semakin cepat, karena semakin banyak molekul-molekul reaktan yang dapat melampaui energi aktivasi (sehingga banyak juga yang bisa bereaksi).
Hubungan antara nilai konstanta reaksi (k) dengan konversi (Xa), dapat diperoleh dari rumus sebagai berikut
Nilai k diperoleh, dimasukkan dalam persamaan :
Diasumsikan waktu (t) berlangsung 1 jam (3600 s), diperoleh :
T (suhu) K Xa (%) XA 283 0,000566971 87,01137 0,999898415 293 0,000587839 87,95137 0,999683247 303 0,000608708 88,82339 0,999084119 313 0,000629577 89,63234 0,997527935 323 0,000650448 90,38277 0,993740171 333 0,00067132 91,0789 0,985086309 343 0,000692192 91,72467 0,966583114 Apabila tinjauan thermodinamika dan kinetika digambardalam sebuah grafik maka akan diperoleh:
Titik suhu fermentasi optimal yaitu pada 305,2 K (32,2˚C) dengan konversi 99,8%.
3.3. DIAGRAM ALIR PROSES 3.3.1. Diagram Proses
Gambar 3.1. Flow Diagram Alir Proses (terlampir)
3.3.2. Langkah Proses
3.3.2.1. Tahap Pretreatment Eceng Gondok
Ada dua macam proses pretreatment yang dilakukan, yaitu pretreatment asam dan pemanasan. Asam yang digunakan adalah asam sulfat 2% (v/v).Sedangkan pemanasan menggunakan pressure tank pada suhu 121˚C selama 30 menit. Proses pretreatment asam dilakukan dengan menambahkan asam sulfat 2% (v/v) ke dalam eceng gondok, kemudian di mixing selama 7 jam. Selanjutnya suspensi eceng gondok dinetralkan dengan NaOH dan ditambah buffer asetat. Proses pretreatment pemanasan dilakukan dengan memanaskan eceng gondok pada suhu 121˚C selama 30 menit. Selanjutnya ditambah akuades dan buffer asetat.
3.3.2.2. Tahap Hidrolisis
Proses hidrolisis meliputi dua tahap, yaitu tahap likuifikasi dan sakarifikasi. Tahap likuifikasi dilakukan variasi seeding ratio jamur A. niger sebagai starter. Variasi seeding ratio sebesar 4/40 (v/v) dan 8/40 (v/v) dengan
waktu inkubasi dalam tahap likuifikasi selama dua hari. Selanjutnya dipanaskan pada suhu 90˚C selama 60 menit.Tahap sakarifikasi dengan ragi S. cerevisiae dengan waktu inkubasi selama satu hari. Selanjutnya dipanaskan pada suhu 60˚C selama 50 menit. Setelah dilakukan proses sakarifikasi, kadar glukosa diukur dengan metode Nelson-Somogyi. Pembuatan starter jamur A. niger dilakukan dengan menginokulasikan A. Niger dalam media PDB (Potato Dextrose Broth) kemudian di shaker pada suhu ruang selama 24 jam.
3.3.2.3. Tahap Fermentasi
Proses fermentasi ini dibagi menjadi beberapa tahap, yaitu tahap pembiakan ragi dan fermentasi.
a. Tahap Pembiakan Ragi
Tahap ini menggunakan tangki prefermentor yang dilengkapi pipa aliran udara dan pipa aliran air pendingin pada bagian luar dinding tangki.Tahap ini bertujuan untuk mengembangbiakkan ragi jenis Saccharomyces cereviseae dengan menggunakan media tetes. Untuk pembuatan larutan ragi, mula-mula diawali dengan cara memasukkan air proses bersuhu 15oC dan tetes 40obrix dari tangki pengendap tetes ke dalam tangki seeding dan mencampurnya hingga mencapai kekentalan sekitar 12-13obrix yang disertai aliran udara dari blower dengan fungsi ganda, yaitu untuk mempercepat tercampurnya tetes dengan air dan juga untuk konsumsi kebutuhan oksigen bagi ragi Saccharomyces cereviseae yang berlangsung pada suasana aerob. Selain itu juga menjaga suhu tangki konstan pada 30oC dengan mengalirkan air pada dinding luar tangki. Jika tidak dijaga, maka ragi sedang dikembangbiakkan akan terganggu kelangsungan hidupnya dan kemudian akan mati. Kemudian memasukkan ragi roti (yeast) yang telah dilarutkan dengan air secukupnya.Untuk nutrisinya, dimasukkan urea, diammonium phospat, dan ammonia. PHP juga ditambahkan ke dalam larutan ini dengan tujuan untuk mempertahankan pH agar tetap konstan yaitu 4,5-5. Dari hasil campuran ini didapatkan biakan ragi.Pada tangki pre-fermentor terdapat beberapa reaksi yaitu: reaksi hidrolisa, reaksi penguraian urea serta reaksi
pertumbuhan yeast. Asumsi pada reaksi hidrolisa adalah konversi yang terjadi 95%. Persamaan reaksi hidrolisa sebagai berikut :
(C6H10O5)n+H2O
à
C6H12O6Persamaan reaksi pada 95% konversi proses penguraian urea adalah : (NH2)2CO + H2O
à
2NH3 + H2OPersamaan reaksi untuk pertumbuhan yeast adalah :
C6H12O6 + 2,28 O2 + 2,08 NH3 → 4CH1,737N0,2O0,451 + 2CO2 + 5,92 H2O
Hr 298 = -3.582,667 kJ/kg b. Tahap Fermentasi
Tahap ini menggunakan tangki fermentor dengan dilengkapi pipa aliran udara dan pipa aliran air pendingin yang berasal dari air sungai untuk menjaga suhu fermentasi pada 30-32˚C. Fermentasi ini bertujuan untuk mendapatkan alkohol dengan kadar 8-9% atau lebih. Pertama-tama dimulai dengan sterilisasi tangki fermentor yang masih kosong dengan steam sampai suhu 121˚C lalu membiarkan suhu di dalam tangki turun sampai 30˚C. Setelah itu memasukkan air proses dengan suhu 30˚C, larutan tetes 40˚brix, proses fermentasi ini berjalan secara anerob. Selanjutnya biakan ragi yang telah dibiakkan pada tangki pre-fermentor dipompa masuk ke tangki pre-fermentor. Setelah itu, tetes 40˚brix dipompa masuk ke tangki dan proses berlangsung selama 24 jam. Untuk pH larutan ini dijaga sekitar 4,5-5. Untuk nutrisinya, dimasukkan urea, ammonium, dan diammonium phospat. Sedangkan turkey red oil ditambahkan sebagai anti foam untuk mencegah pembentukan foam selama proses terjadi. Hal ini dilakukan selama 15 menit setelah persiapan media pada tangki fermentor selesai. Kemudian dimasukkan ke dalam 2 tangki fermentor pada waktu yang disesuaikan dengan jam awal fermentasi. Tahap fermentasi ini berlangsung selama 24 jam hingga kadar alkohol mencapai 8,5-9% dan kekentalan 6,5-7˚brix. Setelah kadar alkohol sebesar 8,5-9% terpenuhi, larutan hasil fermentasi dipompa menuju separator untuk dipisahkan antara hasil fermentasi (cairan mash) dengan ragi (yeast cream). Separator ini menggunakan alat plate and frame filter press sehingga ragi (yeast cream) dan cairan hasil fermentasi (cairan mash) yang memilliki perbedaan massa jenis dapat dipisahkan. Ragi yang didapatkan masih dalam konsentrasi yang
tinggi.Dari hasil fermentasi tidak semuanya dipisahkan raginya, hanya sekitar 80-90% saja.Sisanya 10-20% tidak diambil raginya karena mengandung kotoran-kotoran sisa berupa endapan garam mineral.Hasil fermentasi yang telah dipisahkan ini langsung masuk ke tangki mash (mash tank).Selanjutnya didistilasi hingga menjadi alkohol prima (fine alkohol) dengan kadar mencapai 96,5%. Pada tahap fermentasi ini terjadi perubahan glukosa menjadi etanol dan air. Persamaan reaksi utamanya adalah :
C6H12O6
à
2C2H5OH + 2CO2Pada main fermentor selain terbentuk etanol, juga akan terbentuk produk samping. Hasil samping dalam persen berat (%gula) adalah sebagai berikut :
Asam asetat = 0,65% Fussel Oil = 0,85%
Asetaldehid = 0,05% (Prescot hal 128)
Reaksi samping yang terjadi pada main fermenter yaitu : C6H12O6
à
C3H8O3 + CH3CHO + CO22C6H12O6 + H2O
à
2C3H8O3 + CH3COOH+ C2H5OH + 2CO2Hr 298 = -1,358.1393 kJ/kg Komponen pada fussel oil meliputi :
Propanol = 12,5% Isobutyl alcohol = 15% Amyl alcohol = 30% Isoamyl alcohol = 32,5%
Etanol = 10% (Paturau hal 241)
3.3.2.4. Tahap Purifikasi
Pemisahan yang umum dilakukan untuk memisahkan etanol dari larutan fermentasi adalah distilasi. Pemisahan dan pemurnian etanol seringkali menjadi permasalahan tersendiri karena rendahnya konsentrasi etanol dalam curah fermentasi dan tuntutan kemurnian etanol yang tinggi agar dapat digunakan sebagai bahan bakar. Dengan demikian, proses pemisahan dan pemurnian dapat dikategorikan sebagai proses yang membutuhkan sejumlah besar energi. Broth
fermentasi masuk ke kolom distilasi untuk memisahkan zat-zat volatil seperti etanol, dan fussel oil hingga terpisah dari larutan (Roehr, 2001).
Tahap pemurnian selanjutnya adalah distilasi tahap kedua pada tekanan atmosfer dalam (atmospheric distillation column). Larutan etanol hasil distilasi pertama dimurnikan menjadi 95%-W/W etanol (azeotrop). Produk bawahnya adalah lutter water yang kemudian masuk ke pengolahan limbah. Campuran etanol-air membentuk azeotrop pada komposisi etanol 95% sehingga dehidrasi lebih lanjut untuk menghasilkan etanol fuel-grade dengan kemurnian 99,7% sudah tidak dapat dilakukan. Untuk itu dilakukan proses dehidrasi dengan membran pervaporasi.
Membran pervaporasi merupakan proses pemisahan campuran cair-cair menggunakan membran, permeat mengalami perubahan fasa dari fasa cair menjadi uap. Campuran azeotrop dapat dipisahkan dengan membran pervaporasi karena pemisahan dengan pervaporasi tidak didasarkan pada kesetimbangan uap-cair melainkan didasarkan pada perbedaan kelarutan sebagai wujud interaksi antara komponen campuran dengan membran. Membran yang biasa digunakan adalah membran tidak berpori (non-porous) dimana material membran terbuat dari PDMS (Poly Dimethyl – Siloxane) dan bersifat organofilik. Membran keramik lebih banyak digunakan daripada membran polimer karena membran ini tahan terhadap temperatur tinggi. Gaya dorong (driving force) pada pemisahan dengan membran pervaporasi adalah perbedaan konsentrasi dan tekanan parsial diantara kedua sisi membran.
3.3.2.5. Diagram Alir Proses Yang Dipilih
BAB IV
SPESIFIKASI ALAT DAN UTILITAS
4.1. SPESIFIKASI ALAT
4.1.1. Tangki Pre Treatment
Fungsi : Sebagai tempat perendaman dengan asam sulfat Kondisi operasi : 30˚C
Tekanan : 1 atm
4.1.2. Pompa
Kode : P-01
Fungsi : Mengalirkan Slurry dari Tangki Mashing menuju Tangki Sakarifikasi
4.1.3. Heat Exchanger
Kode : HE-101
Fungsi : Mentransfer supply panas utk kebutuhan reaksi saccarifikasi
Kondisi operasi : 65˚C
Tekanan : 1 atm
4.1.4. Fermentor
Kode : SSF-130
Fungsi : Sebagai tempat untuk terjadinya proses fermentasi utama
Kondisi operasi : 35˚C
Tekanan : 1 atm
4.1.5 Jaket Pendingin
Tipe : Jacket
Media Pendingin : Air
Bahan Konstruksi : Carbon Steel Grade C
4.1.7. Membran Pervorasi
Kode : M-330
Fungsi : Untuk memurnikan produk etanol hingga 99,5% v/v
4.1 5. Kolom Destilasi I
Kode : D-301
Fungsi : Memurnikan produk Etanol dari reaktor menjadi 85%
4.1.6. Kolom Destilasi II
Kode : D-311
Fungsi : Memurnikan produk etanol 95% mol 4.2. UTILITAS
Unit Pendukung proses atau utilitas adalah unit yang bertugas menyediakan sarana penunjang untuk menjamin kelancaran proses produksi. Pada perancangan pabrik bioetanol ini, utilitas yang diperlukan meliputi :
1. Unit penyediaan dan pengolahan air
Berperan dalam pengadaan dan pengolahan air sanitasi, air umpan boiler, dan air pendingin.
2. Unit penyediaan steam
Berperan dalam penyediaan steam untuk heat exchanger dan reboiler. 3. Unit penyediaan tenaga listrik
Sebagai penyedia tenaga listrik untuk tenaga penggerak peralatan proses dan untuk penerangan. Listrik disuplai dari PLN dan sebagai cadangan digunakan generator.
4. Unit penyediaan bahan bakar
Sebagai penyedia bahan bakar untuk peralatan proses.
PENUTUP
5.1 Kesimpulan
1. Untuk mengurangi permasalahan yang timbul akibat banyaknya eceng gondok di perairan, maka perlu dilakukan pemanfaatan terhadap ketersediaan eceng gondok yang sangat melimpah, salah satunya adalah pemanfaatan eceng gondok untuk pembuatan bioethanol.
2. Proses pembentukan etanol dari eceng gondok berlangsung dalam empat tahap, yaitu pretreatment lignoselulosa, proses hidrolisis selulosa menjadi glukosa, proses fermentasi glukosa menjadi etanol, dan proses pemekatan etanol dengan konsentrasi yang diharapkan 99%
3. Pertumbuhan inokulum dan reaksi fermentasi glukosa berlangsung pada kondisi aerob. Reaksi fermentasi bersifat eksotermis (melepaskan panas) dan irreversible Unit
4. Pendukung proses atau utilitas yang digunakan meliputi Unit penyediaan dan pengolahan air, Unit penyediaan steam ,Unit penyediaan tenaga listrik , dan Unit penyediaan bahan bakar.
5.2 Saran
Diharapkan dengan makalah tentang rancangan pabrik bioetanol dari enceng gondok dapat memberikan pengetahuan dan informasi bagi mahasiswa. Dan diharapkan mahasiswa bisa menganalisa, mendekripsikan proses dan mengembangkan proses flow diagram,