KARAKTERISTIK EKSTRAKSI FASA PADAT KOBALT(II) DAN NIKEL(II) MENGGUNAKAN BIOMASSA Azolla microphylla-SILIKA
DAN ELUEN LARUTAN HCl
CHARACTERISTIC OF SOLID PHASE EXTRACTION OF COBALT(II) AND NICKEL(II) UTILIZING BIOMASS OF Azolla microphylla-SILICA
AND ELUENT OF HCl SOLUTION
Danar Purwonugroho*, Darjito, Sri Wardhani, Rachmat Triandi Tjahjanto, Shabrina Adani Putri, Riski Achmad Maulana, Caesar Maulana, Yudistia Lingga Wati
Jurusan Kimia Fakultas MIPA Universitas Brawijaya Malang *E-mail: danar@ub.ac.id
ABSTRACT
Research on solid phase extraction of cobalt(II) and nickel(II) using biomass of Azolla microphylla-silica and eluent of HCl solution was performed. The purpose of this study was to determine the optimum conditions of solid phase extraction of cobalt(II) and nickel(II) using biomass of A. microphylla-silica, including adsorption pH, concentration of eluent, and the flow rate of the eluent. The optimum adsorption pH was determined by batch method using adsorbent size of 80-100 mesh. The result showed that the optimum adsorption pH of cobalt(II) as well as that of nickel(II) was pH 4. In the solid phase extraction experiment, 1.00 g of 20-40 mesh adsorbent was packed in mini column (cartridge) with a diameter of 10 mm and a length of 100 mm. Adsorption experiment was performed by passing 50 mL of metal ion solution of 0.5 mg/L pH 4 through the column at a flow rate of 1 mL/min. Metal ions retained in the column were eluted by passing 5 mL of HCl solution at various concentrations and flow rates. Solid phase extraction experiments were also conducted to evaluate the effect of sample volume on the metal ion recovery and the preconcentration factor of the metal ion solution. The results showed that the optimum conditions of solid phase extraction of cobalt(II) and nickel(II) using biomass A. microphylla-silica occured in the use of eluent with a concentration of 1 M at a flow rate of 0.5 mL/min. Solid phase exraction at a various of sample volume of 25-125 ml with the metal ion content of 0.025 mg resulted the recovery of metal ion of 94.78-98.93 % for cobalt(II) and 87.80-94,08 % for nickel(II), with the highest preconcentration factor of cobalt(II) and nickel(II) solution were 23.7 and 22.09 respectively.
Keywords: solid phase extraction, cartridge, cobalt (II), nickel (II), Azolla microphylla
ABSTRAK
Penelitian tentang ekstraksi fasa padat kobalt(II) dan nikel(II) menggunakan biomassa Azolla microphylla-silika dan eluen larutan HCl telah dilakukan. Tujuan penelitian ini adalah menentukan kondisi optimum ekstraksi fasa padat kobalt(II) dan nikel(II) menggunakan biomassa A. microphylla-silika, yang meliputi pH adsorpsi, konsentrasi eluen, serta laju alir eluen. pH optimum adsorpsi ditentukan dengan metode batch menggunakan adsorben ukuran 80-100 mesh. Hasil percobaan menunjukkan bahwa pH adsorpsi optimum kobalt(II) dan nikel(II) masing-masing adalah pH 4. Pada percobaan ekstraksi fasa padat, 1,00 g adsorben ukuran 20-40 mesh dikemas dalam kolom mini (cartridge) dengan ukuran diameter 10 mm dan panjang 100 mm. Percobaan adsorpsi dilakukan dengan mengalirkan 50 mL larutan ion logam 0,5 mg/L pH 4 melalui kolom dengan laju alir 1 mL/menit. Ion logam yang tertahan di dalam kolom dielusi
menggunakan 5 mL larutan HCl pada berbagai konsentrasi dan laju alir. Percobaan ekstraksi fasa padat juga dilakukan untuk mengkaji pengaruh volume sampel terhadap recovery dan tingkat pemekatan konsentrasi ion logam. Hasil penelitian menunjukkan bahwa kondisi optimum ekstraksi fasa padat kobalt(II) dan nikel(II) menggunakan biomassa A. microphylla-silika terjadi pada penggunaan eluen konsentrasi 1 M dengan laju alir 0,5 mL/menit. Ekstraksi fasa padat pada variasi volume sampel 25-125 mL dengan kandungan ion logam sebesar 0,025 mg menghasilkan recovery ion logam sebesar 98,93-94,78 % untuk kobalt(II) dan 94,08-87,8 % untuk nikel(II), dengan faktor pemekatan terbesar larutan kobal(II) dan nikel(II) masing-masing adalah 23,7 dan 22,09. Kata kunci: ekstraksi fasa padat, cartridge, kobalt(II), nikel(II), Azolla microphylla
1. PENDAHULUAN
Pencemaran air oleh logam berat merupakan permasalahan lingkungan yang paling serius dan mendapat perhatian sangat besar dari para peneliti di seluruh dunia. Logam berat yang mencemari lingkungan peraian, umumnya, berasal dari buangan limbah industri [1,2]. Metode yang banyak digunakan untuk pengolahan limbah logam berat di antaranya adalah pengendapan, adsorpsi, reduksi, koagulasi, dan filtrasi menggunakan membran [3]. Namun, metode tersebut dinilai tidak efektif atau terlalu mahal untuk pengolahan limbah dengan konsentrasi logam berat sekitar 100 mg/L [4]. Salah satu metode yang banyak dikembangkan untuk menurunkan konsentrasi logam berat dalam limbah adalah biosorpsi. Biosorpsi adalah proses adsorpsi menggunakan biomassa atau biopolimer sebagai adsorben [3]. Biosorpsi menggunakan biomassa dalam keadaan mati [4].
Biosorpsi dapat dilakukan dengan metode batch maupun metode kolom. Biosorpsi telah menjadi bagian penting dari ekstraksi fasa padat ion logam berat. Pada ekstraksi fasa padat, analit diekstraksi melalui proses adsorpsi, kemudian dielusi menggunakan pereaksi yang sesuai. Melalui proses ekstraksi fasa padat, konsentrasi analit dapat dipekatkan [5]. Ekstraksi fasa padat banyak dikembangkan untuk memekatkan konsentrasi ion logam berat yang dikaitkan dengan metode pengukuran tertentu, misalnya metode spektrofotometri serapan atom.
Biomassa yang banyak digunakan sebagai adsorben adalah biomassa tanaman. Kemampuan biomassa tanaman dalam mengikat ion logam berat difasilitasi oleh gugus fungsional seperti karboksil, hidroksil, sulfat, fosfat, dan amina [3]. Oleh sebab itu, tanaman dengan kandungan protein tinggi memiliki potensi yang besar untuk dapat dimanfaatkan sebagai adsorben pada biosorpsi logam berat. Pada biosorpsi dengan metode kolom, biomassa harus diamobilisasi pada matriks polimer untuk mendapatkan ukuran partikel yang mendukung sistem mengalir. Matriks polimer yang umum digunakan
untuk mendukung amobilisasi biomasa adalah silika, agar, poliakrilamid, polisulfon, dan alginat [6].
Azolla, tanaman paku-pakuan yang hidup mengambang di perairan, merupakan tanaman dengan kandungan protein yang relatif tinggi, yaitu 15,4 – 27,93 % [7]. Dua spesies Azolla tumbuh dengan baik di Indonesia, khususnya daerah Malang Jawa Timur, yaitu Azolla pinnata dan Azolla microphylla. Biomassa A. pinnata yang diamobilisasi pada polisilikat merupakan adsorben yang sangat baik untuk kromium(III), namum kromium(III) yang terikat oleh biomassa sulit didesorpsi [8]. Ekstraksi fasa padat terhadap kadmium(II) dan timbal(II) menggunakan biomassa A. microphylla-silika dan eluen larutan HCl 0,1 M dengan laju alir 1 mL/menit telah dilaporkan menghasilkan recovery ion logam sebesar 75,83 % untuk kadmium(II) dan sebesar 83,90 % untuk timbal(II) [9].
Penelitian ini mengkaji karakteristik ekstraksi fasa padat kobalt(II) dan nikel(II) menggunakan kolom mini (cartridges), adsorben biomassa A. microphylla-silika, dan eluen larutan HCl. Tujuan penelitian ini adalah menentukan kondisi optimum ekstraksi fasa padat kobalt(II) dan nikel(II) yang meliputi pH adsorpsi optimum, konsentrasi eluen optimum, dan laju alir eluen optimum. Pada penelitian ini dipelajari juga pengaruh volume sampel terhadap recovery dan tingkat pemekatan ion logam.
2. METODE PENELITIAN 2.1 Bahan Penelitian
Tanaman A. microphylla yang digunakan berasal dari Laboratorium Bioteknologi Universitas Muhammadiyah Malang. Bahan–bahan kimia yang digunakan dalam penelitian ini merupakan bahan berderajad pro analisa (p.a), yaitu CoCl2.6H2O, NiCl2.6H2O, HCl 37%, AgNO3, Na2SiO3, NaOH, BaCl2, H2SO4 96%, CH3COOH 100%.
2.2 Alat Penelitian
Alat-alat yang digunakan dalam penelitian ini yaitu: seperangkat alat gelas, kolom ukuran 200 x 50 mm, kolom 100 x 10 mm, selang infus, oven Fisher Scientific 655 F, ayakan 20, 40, 80, 100, 120, dan 150 mesh, pengocok listrik SM 25, sentrifuge Hittech EBAIII, timbangan mettler AE 50, pH meter, pengaduk magnet, dan spektrofotometer serapan atom SHIMADZU AA 6800.
2.3 Preparasi Adsorben Biomassa A. microphylla
Tanaman A. microphylla dicuci sampai bersih, kemudian dikeringkan dalam oven pada suhu 90 oC sampai massanya konstan. Biomassa kering ditumbuk, kemudian diayak menggunakan ayakan berukuran 120 mesh. Partikel yang lolos dari ayakan 120
mesh diayak lagi menggunakan ayakan berukuran 150 mesh. Partikel biomassa yang tertahan pada 150 mesh adalah biomassa yang digunakan pada penelitian ini. Biomassa berukuran 120-150 mesh dicuci dua kali menggunakan larutan HCl 0,01 M, kemudian dibilas dengan akuades hingga filtrat tidak membentuk endapan dengan larutan AgNO3. Biomassa 120-150 mesh dikeringkan dalam oven pada suhu 60 oC sampai massanya konstan.
2.4 Amobilisasi Biomassa pada Polisilikat
Asam sulfat 5 % sebanyak 75 mL dicampur dengan larutan natrium metasilikat 6 % dalam gelas kimia 500 mL sampai pH 2. Biomassa sebanyak 5 gram dimasukkan ke dalam larutan tersebut. Campuran diaduk dengan pengaduk magnet selama 15 menit. Larutan natrium metasilikat 6 % ditambahkan ke dalam gelas kimia sampai pH 7 sehingga terbentuk gel polisilikat yang keras dan biomassa teramobilisasi di dalamnya. Gel dicuci dengan akuades sampai filtrat tidak membentuk endapan dengan larutan BaCl2 0,1 M. Biomassa yang telah teramobilisasi dalam matrik polisilikat dikeringkan dalam oven pada suhu 60 oC sampai massa konstan. Biomassa Azolla microphylla-silika ditumbuk dan diayak untuk memperoleh ukuran 80-100 mesh dan 20-40 mesh.
2.5 Penentuan pH Adsorpsi Optimum
Adsorben biomassa A. microphylla-silika sebanyak 0,1 g disiapkan dalam erlenmeyer 250 mL. Larutan ion logam 100 mg/L dengan pH tertentu sebanyak 25 mL dimasukkan ke dalam erlenmeyer 250 mL yang berisi biomassa A. microphylla-silika. Suspensi dalam erlenmeyer dikocok menggunakan pengocok listrik dengan kecepatan 125 rpm selama 60 menit. Kemudian, suspensi disentrifugasi dengan kecepatan 3000 rpm selama 5 menit. Supernatan dipisahkan dan dimasukkan ke dalam botol sampel. Konsentrasi ion logam dalam supernatan ditentukan menggunakan spektrofotometer serapan atom.
2.6 Preparasi Kolom Mini
Disiapkan kolom mini dengan ukuran panjang 100 mm dan diameter 10 mm yang dilengkapi dengan alat pengatur laju alir. Bagian bawah kolom diberi glasswool untuk menahan adsorben. Ke dalam kolom dimasukkan 1 g adsorben biomassa-silika kemudian ditutup dengan glasswool. Kolom yang telah disiapkan dipasang vertikal pada statif. Kolom kedua dengan ukuran panjang 200 mm dengan diameter 50 mm yang dilengkapi pengatur laju alir dipasang di atas kolom pertama, untuk menampung fasa gerak. Sebelum digunakan untuk percobaan adsorpsi, adsorben yang berapa di dalam kolom
harus selalu terendam dalam larutan buffer dengan pH yang sesuai dengan pH optimum adsorpsi.
2.7 Percobaan Adsorpsi
Larutan ion logam dengan konsentrasi tertentu (1 mg/L; 0,5 mg/L; 0,33 mg/L; 0,25 mg/L; 0,2 mg/L) dan volume tertentu (25 mL; 50 mL; 75 mL; 100 mL; 125 mL) dialirkan melalui kolom mini dengan laju alir 1 mL/menit. Efluen sebanyak volume sampel yang dialirkan ditampung dalam gelas kimia. Konsentrasi ion logam dalam efluen ditentukan dengan spektrofotometer serapan atom.
2.8 Percobaan Desorpsi
Ion logam yang tertahan di dalam kolom didesorpsi menggunakan eluen larutan HCl. Sebanyak 5 mL larutan HCl dengan konsentrasi tertentu (0,8 M; 1 M; 1,2 M; 1,4 M) dialirkan melalui kolom dengan laju alir tertentu pula (0,5 mL/menit; 1 mL/menit; 1,5 mL/menit; 2 mL/menit; 2,5 mL/menit). Konsentrasi ion logam dalam efluen ditentukan dengan spektrofotometer serapan atom.
3. HASIL DAN PEMBAHASAN
3.1 Penentuan pH Adsorpsi Optimum
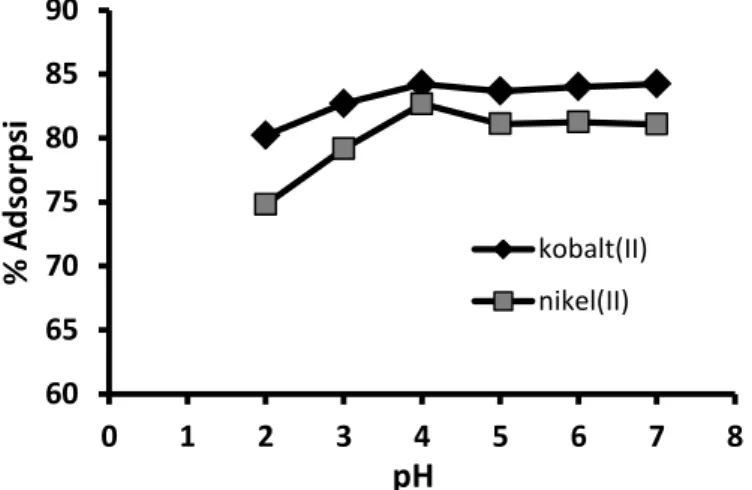
pH adsorpsi optimum ditentukan berdasarkan hasil percobaan pengaruh pH terhadap adsorpsi ion logam yang dilakukan dengan metode batch. Percobaan adsorpsi dilakukan menggunakan 0,10 g adsorben biomassa A. microphylla-silika dan 25 mL larutan ion logam 100 mg/L. Adsorpsi dilakukan pada variasi pH awal 2; 3; 4; 5; 6; dan 7. Hasil percobaan pengaruh pH terhadap adsorpsi ion logam disajikan pada Gambar 1.
Gambar 1. Pengaruh pH terhadap adsorpsi ion logam oleh biomassa A. microphylla-silika 60 65 70 75 80 85 90 0 1 2 3 4 5 6 7 8
%
A
d
so
rp
si
pH
kobalt(II) nikel(II)Gambar 1 menunjukkan bahwa adsorpsi ion logam, kobalt(II) maupun nikel(II), meningkat dari pH 2 sampai dengan pH 4. Adsorpsi kobalt(II) relatif tidak berbeda pada pH 4 – 7, sementara adsorpsi nikel(II) menurun dari pH 4 ke pH 5 dan relatif tetap pada pH 5 – 7. Berdasarkan uji ANOVA (α = 0,05) diperoleh informasi bahwa pH awal larutan berpengaruh nyata terhadap adsorpsi kobalt(II) maupun nikel(II) oleh biomassa A. microphylla-silika. Uji beda nyata terkecil (BNT) menunjukkan bahwa adsorpsi kobalt(II) pada pH 3 dan pH 4 berbeda nyata, sementara adsorpsi kobalt(II) pada pH 4, pH 5, pH 6, dan pH 7 tidak berbeda nyata, sehingga dapat disimpulkan bahwa pH optimum adsorpsi kobalt(II) adalah pH 4 dengan % adsorpsi kobalt(II) sebesar 84,21 %. Dengan cara yang sama diperoleh informasi bahwa pH adsorpsi optimum untuk adsorpsi nikel(II) terjadi pada pH 4 dengan % adsorpsi nikel(II) sebesar 82,67 %.
Pada proses biosorpsi, pH larutan dapat berpengaruh baik terhadap ion logam maupun biosorben. Dalam larutan, ion logam larut sebagai asam akua, [M(H2O)6]2+, yang bersifat asam Bronsted sebagaimana ditunjukkan oleh persamaan (1). Jika pH larutan dinaikkan maka terjadi peningkatan jumlah basa konjugat dari asam akua ion logam, [M(H2O)5(OH)]+, sehingga dapat menurunkan interaksi elektrostratik antara ion logam dengan gugus aktif anionik yang terdapat pada permukaan biosorben.
[M(H2O)6]2+(aq) + H2O(l) ⇄ [M(H2O)5(OH)]+(aq) + H3O+(aq) (1)
Karakteristik gugus aktif permukaan biomassa, terutama gugus asam lemah seperti gugus karboksil, sangat dipengaruhi oleh pH larutan. Pada pH rendah, gugus karboksil cenderung dalam keadaan terprotonasi, sementara pada pH semakin tinggi cenderung mengalami deprotonasi menjadi gugus karboksilat sebagaimana ditunjukkan oleh persamaan (2). Pada pH lebih besar dari pKa, semua gugus karboksil berubah menjadi gugus karboksilat dan berperan lebih besar sebagai gugus aktif permukaan pada adsorpsi ion logam kationik.
BIOMASSA-COOH + H2O ⇄ BIOMASSA-COO- + H3O+ (2)
Berdasarkan data pengaruh pH sebagaimana ditampilkan pada Gambar 1 dapat dinyatakan bahwa salah satu gugus aktif permukaan biomassa pada proses adsorpsi ion logam kationik adalah gugus karboksil yang mengikat ion logam kationik dengan mekanisme pertukaran kation. Fakta ini sekaligus memberikan informasi bahwa ion logam yang terikat oleh biomassa dapat didesorpsi menggunakan larutan asam.
3.2 Pengaruh Konsentrasi Larutan HCl Terhadap Recovery Ion Logam
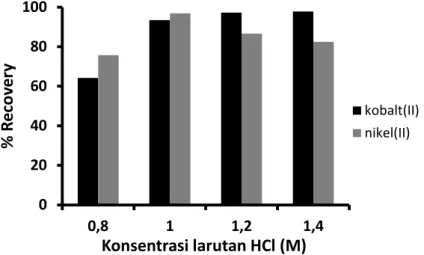
Pada percobaan adsorpsi diperoleh informasi bahwa hampir 100 % ion logam yang dialirkan melewati kolom tertahan di dalam kolom. Ion logam yang yang tertahan di dalam kolom didesorpsi menggunakan 5 mL larutan HCl berbagai konsentrasi dengan laju alir 0,5 mL/menit. Hasil percobaan pengaruh konsentrasi larutan HCl terhadap recovery ion logam ditampilkan pada Gambar 2.
Gambar 2. Pengaruh konsentrasi HCl terhadap recovery ion logam
Gambar 2 menunjukkan bahwa recovery ion logam, baik kobalt(II) maupun nikel(II), meningkat sangat tajam ketika konsentrasi larutan HCl ditingkatkan dari 0,8 M menjadi 1 M. Desorpsi kobalt(II) menggunakan larutan HCl 1,2 M dan 1,4 M sedikit meningkat dibanding dengan menggunakan larutan HCl 1 M. Sementara itu, desorpsi nikel(II) justru menurun ketika digunakan larutan HCl lebih dari 1 M. Berdasarkan hasil uji ANOVA (α = 0,05) diperoleh informasi bahwa konsentrasi HCl berpengaruh nyata terhadap recovery kobalt(II) maupun nikel(II). Pada penentuan kondisi optimum berdasarkan hasil uji BNT diperoleh informasi bahwa konsentrasi larutan HCl optimum untuk desorpsi kobalt(II) dan nikel(II) adalah 1 M.
3.3 Pengaruh Laju Alir Eluen Terhadap Recovery Ion Logam
Kajian pengaruh laju alir eluen bertujuan untuk mengetahui laju alir optimum yang diperlukan oleh eluen untuk mendesorpsi ion logam. Desorpsi ion logam dilakukan menggunakan larutan HCl 1 M. Hasil percobaan pengaruh laju alir eluen terhadap recovery ion logam disajikan pada Gambar 3.
Gambar 3 menunjukkan bahwa laju alir eluen berpengaruh terhadap recovery kobalt(II) dan nikel(II). Laju alir eluen berpengaruh terhadap waktu kontak antara eluen dengan ion logam yang terikat oleh adsorben. Semakin kecil laju alir semakin lama waktu
0 20 40 60 80 100 0,8 1 1,2 1,4
%
R
e
co
ve
ry
Konsentrasi larutan HCl (M)
kobalt(II) nikel(II)kontak antara eluen dengan ion logam yang terikat oleh biomassa sehingga peluang terjadinya pertukaran kation semakin besar. Laju alir eluen yang menghasilkan desorpsi ion logam terbesar adalah 0,5 mL/menit, dengan recovery kobalt(II) sebesar 95,24 % dan nikel(II) sebesar 91,18 %. Percobaan tidak dilakukan untuk laju alir eluen kurang dari 0,5 mL/menit, karena sangat sulit untuk mengatur laju alir kurang dari 0,5 mL/menit secara manual.
Gambar 3. Pengaruh laju alir eluen terhadap recovery ion logam
3.4 Pengaruh Volume Sampel Terhadap Recovery Ion Logam
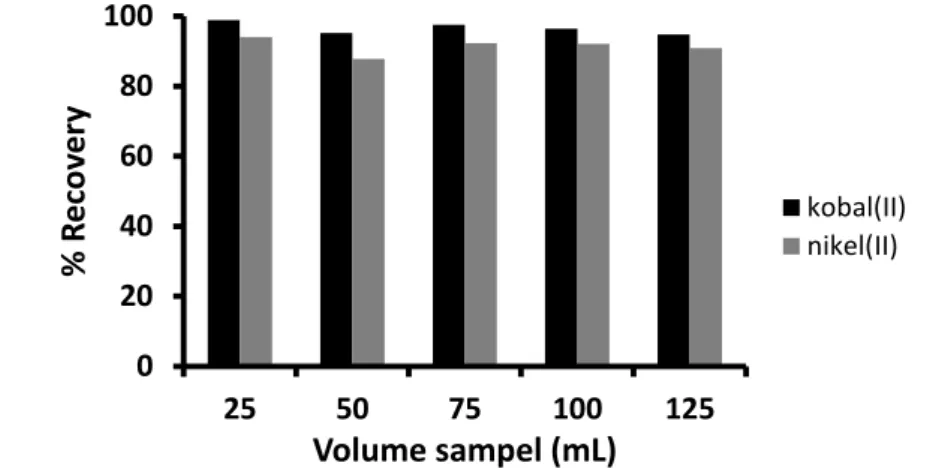
Percobaan adsorpsi dilakukan dengan mengalirkan 25 mL, 50 mL, 75 mL, 100 mL, dan 125 mL masing-masing mengandung 0,025 mg ion logam melalui kolom dengan laju alir 0,5 mL/menit. Ion logam yang tertahan di dalam kolom dielusi menggunakan 5 mL larutan HCl 1 M. Hasil percobaan pengaruh volume sampel terhadap recovery ion logam disajikan oleh Gambar 4.
Gambar 4. Pengaruh volume sampel terhadap recovery ion logam
Recovery ion logam, baik kobalt(II) maupun nikel(II), sedikit menurun ketika volume sampel ditingkatkan dari 25 mL sampai dengan 125 mL. Variasi volume sampel
0 20 40 60 80 100 0,5 1 1,5 2 2,5
%
R
e
co
ve
ry
Laju alir (mL/menit)
kobal(II) nikel(II) 0 20 40 60 80 100 25 50 75 100 125
%
R
e
co
ve
ry
Volume sampel (mL)
kobal(II) nikel(II)25-125 mL menghasilkan recovery sebesar 98,93-94,78 % untuk kobalt(II) dan 94,08- 87,8 % untuk nikel(II). Namun, berdasarkan hasil uji ANOVA (α = 0,05) diperoleh informasi bahwa volume sampel tidak berpengaruh nyata terhadap recovery ion logam.
4. KESIMPULAN
Berdasarkan hasil penelitian dan pembahasan yang telah disampaikan dapat ditarik kesimpulan bahwa kondisi optimum ekstraksi fasa padat kobal(II) dan nikel(II) menggunakan adsorben biomassa A. microphylla-silika dan eluen larutan HCl adalah: pH adsorpsi 4, konsentrasi eluen 1 M, dan laju alir eluen 0,5 mL/menit. Ekstraksi fasa padat pada variasi volume sampel 25-125 mL dengan kandungan ion logam sebesar 0,025 mg menghasilkan recovery ion logam yang tidak berbeda nyata yaitu 98,93-94,78 % untuk kobalt(II) dan 94,08-87,8 % untuk nikel(II), dengan faktor pemekatan tertinggi larutan kobalt(II) dan nikel(II) masing-masing sebesar 23,7 dan 22,09.
5. PUSTAKA
[1] M. Akbari, A. Hallajisani, A.R. Keshtkar, H. Shahbeig, S.A. Ghorbanian. Equilibrium and kinetic study and modeling of Cu(II) and Co(II) synergistic biosorption from Cu(II)-Co(II) single and binary mixtures on brown algae C. indica. Journal of Environmental Chemical Engineering. 2015; 3:140-149.
[2] A.M. Nazari, P.W. Cox, K.E. Waters. Biosorption of copper, nickel and cobalt ions from dilute solutions using BSA-coated air bubbles. Journal of Water Process Engineering. 2014; 3: 10-17.
[3] J. He, J.P. Chen. A comprehensive review on biosorption of heavy metals by algal biomass: Materials, performances, chemistry, and modelling simulation tools. Bioresource Technology. 2014; 160: 67-78.
[4] U. Farooq, J.A. Kozinski, M.A. Khan, M. Athar. Biosorption of heavy metal ions using wheat based biosorbents – A review of the recent literature. Bioresource Technology. 2010; 101: 5043-5053.
[5] P.H. Pacheso, R.A. Gil, S.E. Cerutti, P. Smichowski, L.D. Martinez. Biosorption: A new rise for elemental solid phase extraction methods. Talanta. 2011; 85: 2290-2300. [6] J.L. Gardea-Torresdey, G. de la Rosa, J.R. Peralta-Videa. Use of phytofiltration
technologies in the removal of heavy metals: A review*. Pure Appl. Chem. 2004; 76(4): 801-813.
[7] A. Chatterjee, P. Sharma, M. K. Ghosh, M. Mandal, P. K. Roy. Utilization of Azolla Microphylla as Feed Supplement for Crossbred Cattle. International Journal of Agriculture and Food Science Technology. 2013; 4(3): 207-2014.
[8] D. Purwonugroho, S. Wardhani, U. Andayani. Pemisahan Krom(III) dari Media Air Menggunakan Biomassa Azolla pinnata yang Diamobilisasi Pada Matriks Polisilikat. Natural. 2007; 11(3): 1-6.
[9] D. Purwonugroho, S. Wardhani, Darjito, D. A. Shandi, D. Chan. Biosorption of lead(II) and cadmium(II) by biomass of Azolla microphylla-silica in continuous system. Proceedings of International Conference on Basic Science, Malang. 2011; 312-314, 17-18 Feb 2011.