PATI-ALGINAT DARI EKSTRAKSI RUMPUT LAUT
COKLAT (
Sargassum sp.
) SEBAGAI MATERIAL
DRUG DELIVERY SYSTEM
SKRIPSI
MAWADDATUL KARIMAH
PROGRAM STUDI S1 KIMIA
DEPARTEMEN KIMIA
FAKULTAS SAINS DAN TEKNOLOGI
UNIVERSITAS AIRLANGGA
PATI-ALGINAT DARI EKSTRAKSI RUMPUT LAUT
COKLAT (
Sargassum sp.
) SEBAGAI MATERIAL
DRUG DELIVERY SYSTEM
SKRIPSI
MAWADDATUL KARIMAH
PROGRAM STUDI S1 KIMIA
DEPARTEMEN KIMIA
FAKULTAS SAINS DAN TEKNOLOGI
UNIVERSITAS AIRLANGGA
Skripsi ini tidak dipublikasikan, namun tersedia di perpustakaan dalam
lingkungan Universitas Airlangga. Diperkenankan untuk digunakan sebagai
referensi kepustakaan dengan pengutipan seijin penulis serta harus menyebutkan
Syukur Alhamdulillah atas segala rahmat, karunia dan hidayah yang telah diberikan oleh Allah SWT, sehingga penulis dapat menyelesaikan penulisan skripsi dengan judul “Pembuatan dan Karakterisasi Kapsul Pati-Alginat dari Ekstraksi Rumput Laut Coklat (Sargassum sp.) sebagai Material Drug Delivery System”. Naskah skripsi ini disusununtuk memenuhi persyaratan kelulusan dalam menempuh pendidikan S1-Kimia di Fakultas Sains dan Teknologi Universitas Airlangga.
Dalam penulisan naskah skripsi ini tidak lepas dari bantuan berbagai pihak. Oleh karena itu, dalam kesempatan ini penulis mengucapkan terima kasih kepada :
1. Ibu Siti Wafiroh, S.Si., M.Si. selaku dosen pembimbing I yang selalu memberikan bimbingan, nasehat dan motivasi selama penyusunan naskah skripsi ini.
2. Dr. Pratiwi Pudjiastuti, M.Si. selaku dosen pembimbing II yang selalu memberikan saran dan nasehat selama penulis menempuh studi S1-Kimia di Fakultas Sains dan Teknologi Universitas Airlangga.
3. Bapak Dr. Purkan, M.Si. selaku ketua Departemen Kimia Fakultas Sains dan Teknologi Universitas Airlangga atas saran, nasehat, dan motivasinya selama ini.
4. Ibu Dr. Nanik Siti Aminah, M.Si. selaku dosen wali yang selalu memberikan saran, nasehat, dan motivasi selama ini.
5. Ibu Dr. Alfinda Novi Kristanti dan Bapak Dr. Ir. Suyanto, M.Si. yang selalu memberikan saran, nasehat, dan motivasi selama ini.
6. Seluruh staf pengajar Departemen Kimia Fakultas Sains dan Teknologi Universitas Airlangga atas ilmu, bimbingan, dan saran yang telah diberikan. 7. Seluruh laboran dan karyawan di Laboratorium Kimia Fisik, Kimia Organik
dan Kimia Analitik.
8. Kedua orang tua dan semua keluarga yang selalu memberikan doa, semangat, dan dukungan moral kepada penulis selama ini.
9. Kementrian Agama RI yang telah memberikan beasiswa kepada penulis selama menempuh pendidikan S1.
10.Teman-teman prodi S1 Kimia angkatan 2012 yang selalu memberikan semangat kepada penulis selama mengerjakan skripsi ini
11.Teman-teman CSS MoRA Unair 2012 yang selalu memberikan motivasi kepada penulis selama mengerjakan skripsi ini
12.Teman-teman MTQ Unair yang selalu memberikan motivasi kepada penulis selama mengerjakan skripsi ini
13.Teman-teman skripsi kapsul Aulala, Niyyah dan Ulil yang selalu memberikan semangat, saran dan motivasi selama mengerjakan skripsi ini
berminat meneliti hal yang sama dan bermanfaat untuk masyarakat.
Surabaya, 13 Juli 2016 Penulis,
Ekstraksi Rumput Laut Coklat (Sargassum sp.) sebagai Material Drug Delivery System, skripsi ini di bawah bimbingan Siti Wafiroh, S.Si., M.Si. dan Dr. Pratiwi Pudjiastuti, M.Si., Departemen Kimia, Fakultas Sains dan Teknologi, Universitas Airlangga, Surabaya.
ABSTRAK
Penelitian tentang material drug delivery system mengalami perkembangan yang sangat cepat. Kapsul komersil dengan material gelatin merupakan kapsul yang banyak digunakan, namun kapsul gelatin ini mudah mengalami cracking. Oleh karena itu, perlu dilakukan pengembangan material
drug delivery salah satunya kapsul dari pati dan alginat dengan crosslinker STPP (sodium tripolyphosphat). Tujuan dari penelitian ini adalah membuat dan megkarakterisasi kapsul pati-alginat. Alginat yang digunakan adalah hasil dari ekstraksi rumput laut coklat jenis Sargassum sp. Metode yang digunakan adalah maserasi jalur asam alginat. Kedua bahan ini dikompositkan dengan 5 macam perbandingan yaitu (2:1), (3:2), (1:1), (1:2), (2:3). Karakterisasi yang dilakukan meliputi uji tarik, uji swelling air, uji disolusi, uji FTIR dan uji SEM. Kapsul pati-alginat optimal memiliki nilai stress, strain, modulus Young dan swelling air berturut-turut sebesar 8.018,18 kN/m2; 0,1225; 65.823,12 kN/m2 dan 248,12%.
Hasil uji disolusi kapsul yang mengandung ciprofloxacin pada pH 1,2; 4,5 and 6,8 selama 90; 2 dan 4 menit berturut-turut adalah 92%; 79% and 86%. Dengan demikian, kapsul dari komposit pati-alginat dapat digunakan sebagai drug delivery system.
Alginate Capsule from Extraction of Brown Algae (Sargassum sp.) as Material of Drug Delivery System, final project was under guidance of Siti Wafiroh, S.Si., M.Si. and Dr. Pratiwi Pudjiastuti, M.Si., Department of Chemistry, Faculty of Science and Technology, Airlangga University, Surabaya.
ABSTRACT
Research of material of drug delivery system has developed so fast. Commercial capsule with gelatin material is often consumed, but this capsule is easy to crack. Therefore, more drug release material development is needed. One of them is capsule from starch-sodium alginate using STPP (sodium tripolyphosphat) as crosslinker. The purposes of this research are to produce and characterise of starch-sodium alginate capsules. Alginate was extracted from brown algae (Sargassum sp.). The method was alginate acid pathway. Both of the materials were divided to 5 variation of compositions, (2:1), (3:2), (1:1), (1:2) and (2:3). The characterizations was performed by using tensile, water swelling, dissolution, FTIR and SEM tests. The optimum of starch-alginate capsules include stress, strain, modulus Young and swelling water values are 8,018.18 kN/m2; 0.1225; 65,823.12 kN/m2; 248.12%, respectively. The dissolution of
capsules contain of ciprofloxacin at pH 1.2; 4.5 and 6.8 for 90; 2 and 4 minutes are 92%; 79% and 86%, respectively. Based on this research, capsule from starch-alginate composite can be used as drug delivery system.
HALAMAN JUDUL ... i
LEMBAR PENYATAAN ... ii
LEMBAR PENGESAHAN ... iii
LEMBAR PEDOMAN PENGGUNAAN SKRIPSI ... iv
KATA PENGANTAR ... v
ABSTRAK ... vii
ABSTRACT ... viii
SURAT PERNYATAAN ORISINALITAS ... ix
DAFTAR ISI ... x
2.7 Prinsip Kerja Material Drug Delivery System ... 18
2.8 Karakterisasi Material Drug Delivery System ... 21
2.8.1 Fourier Transformed Infra Red(FTIR) ... 21
2.8.2 Scanning Electron Membrane(SEM) ... 23
2.8.3 Penentuan berat molekul polimer... 24
2.8.4 Uji swelling air ... 25
3.4 Prosedur Penelitian... 32
3.4.3 Karakterisasi natrium alginat ... .34
3.4.3.1 Penentuan berat molekul ... 34
3.4.3.2 Penentuan gugus fungsi dengan FTIR ... 34
3.4.4 Pembuatan komposit pati-alginat ... 35
3.4.5 Pencetakan kapsul pati-alginat ... 35
3.4.6 Karakterisasi kapsul pati-alginat ... 36
3.4.6.1 Uji mekanik ... 36
3.4.6.2 Uji kinerja... 36
3.4.6.3 Uji SEM ... 37
BAB IV HASIL DAN PEMBAHASAN ... 39
4.1 Hasil Ekstraksi Natrium Alginat dari Sargassum sp ... 39
4.2 Hasil Karakterisasi Natrium Alginat ... 43
4.2.1 Hasil uji penentuan berat molekul ... 43
4.2.2 Hasil uji FTIR ... 45
4.3 Hasil Pembuatan Komposit Pati-Alginat ... 47
4.4 Hasil Pencetakan Kapsul Pati-Alginat ... 48
4.5 Hasil Karakterisasi Kapsul Pati-Alginat ... 50
4.5.1 Hasil uji tarik ... 50
4.5.2 Hasil uji swelling air... 53
4.5.3 Hasil uji FTIR kapsul pati-alginat optimum ... 54
4.5.4 Hasil uji disolusi kapsul pati-alginat optimum... 57
4.5.5 Hasil uji SEM kapsul pati-alginat optimum ... 59
BAB V KESIMPULAN DAN SARAN ... 61
5.1 Kesimpulan ... 61
5.2 Saran ... 61
Nomor Judul Tabel Halaman
2.1 Karakteristik amilosa dan amilopektin ... 10
2.2 Karakteristik natrium alginat ... 13
2.3 Karakteristik sodium tripolyphosphate... 16
2.4 Kriteria dosis urutan daya toksisitas suatu bahan ... 17
4.1 Data spektra FTIR natrium alginat ... 45
4.2 Karakteristik kapsul pada masing-masing variasi ... 49
DAFTAR GAMBAR
4.1 Persamaan reaksi kimia pada saat proses demineralisasi ... 40
4.2 Pemisahan antara filtrat dan padatan setelah maserasi ... 40
4.3 Persamaan reaksi kimia natrium alginat dengan HCl ... 41
4.4 Persamaan reaksi kimia konversi asam alginat menjadi natrium alginat 41 4.5 Persamaan reaksi kimia oksidasi lignin oleh NaOCl ... 42
4.6 Serbuk natrium alginat ... 43
4.7 Grafik hubungan antara konsentrasi Na-alginat dan viskositas reduksi . 44 4.8 Hasil spektra natrium alginat ... 47
4.9 Kapsul pati-natrium alginat ... 48
4.10 Autograph ... 50
4.11 Diagram antara variasi komposisi membran dengan nilai stress ... 51
4.12 Diagram antara variasi komposisi membran dengan nilai strain ... 52
4.13 Diagram antara variasi komposisi membran dengan nilai modulus young53 4.14 Diagram antara variasi kapsul dengan nilai swelling air ... 53
4.15 Hasil spektra FTIR kapsul pati-alginat dan Na-alginat ekstraksi... 56
4.16 Hipotesis ikatan antara pati-STPP-alginat ... 57
4.17 Grafik hasil uji disolusi pH 1,2 ... 58
4.18 Grafik hasil uji disolusi pH 4,5 ... 59
4.19 Grafik hasil uji disolusi pH 6,8 ... 59
4.20 Morfologi permukaan membran kapsul pati-alginat dan kapsul komersil ... 60
Nomor Judul Lampiran
1. Pembuatan Larutan untuk Ekstraksi Natrium Alginat
2. Hasil Penentuan Viskositas dan Berat Molekul Natrium Alginat 3. Rendemen Hasil Ekstraski Natrium Alginat
4. Spektra FTIR Natrium Alginat Hasil Ekstraksi 5. Spektra FTIR Natrium Alginat Komersil
6. Spektra FTIR Natrium Alginat Campuran (Ekstraksi-Komersil) 7. Spektra FTIR Kapsul Pati-Natrium Alginat dengan crosslinker STPP 8. Hasil Pembuatan Komposit Pati – Alginat
9. Hasil Uji Tarik
BAB I PENDAHULUAN 1.1 Latar belakang
Kapsul sebagai drug delivery system dalam dunia farmasi sudah banyak digunakan sejak lama. Dalam pengembangannya, modifikasi swelling, cracking, hingga mekanisme pelepasan obat sudah banyak dilakukan (Bertrand, 2012). Beberapa macam metode drug delivery diantaranya secara oral, parenteral, lokal, rektal, transdermal dan inhalasi (Shargel et al., 2007).
Pemberian obat secara oral yaitu pemberian obat secara langsung melalui mulut, sedangkan parenteral yaitu pemberian obat melalui suntikan. Pemberian obat secara lokal yaitu obat diteteskan atau dioleskan secara langsung seperti obat tetes mata dan rektal yaitu pemberian obat melalui dubur. Transdermal yaitu pemberian obat melalui permukaan kulit seperti plester dan inhalasi yaitu pemberian obat dengan cara dihirup maupun disemprotkan melalui hidung atau mulut (Anief, 1995). Diantara macam-macam metode drug delivery, metode drug delivery secara oral merupakan metode yang paling diminati di masyarakat karena cara pemberian obat yang mudah, aman dan praktis (Shargel et al., 2007). Bentuk-bentuk obat yang dapat diberikan secara oral antara lain kapsul, tablet, sirup dan puyer. Pemberian obat tersebut disesuaikan dengan kebutuhan.
lebih tepat, tidak berbau dan hambar sehingga mudah untuk ditelan, dan release
dalam waktu yang sesuai (Saputra, 2014).
Kapsul pertama kali dibuat oleh J. C Lehuby pada tahun 1846 yang dikenal dengan kapsul gelatin (Augsburger, 2002). Berdasarkan sifatnya, kapsul gelatin dibedakan menjadi dua macam, yaitu cangkang kapsul gelatin lunak dan cangkang kapsul gelatin keras (Allen et al., 2011). Cangkang kapsul gelatin lunak biasanya plastis dengan bentuk bervariasi dengan packing yang tertutup. Umumnya isi kapsul ini berupa cairan, suspensi maupun pasta. Sedangkan cangkang kapsul gelatin keras umumnya berisi serbuk dengan satu macam bentuk yang umumnya lonjong yang terdiri dari dua bagian yaitu body dan cap
(Augsburger, 2002).
Pada umumnya, cangkang kapsul gelatin banyak digunakan di pasaran karena material dalam pembuatannya murah dan mudah diproduksi. Namun, material cangkang kapsul gelatin ini memiliki kelemahan yaitu kurang stabil dalam lingkungan berair sehingga waktu swelling dan cracking cenderung sangat cepat dan menyebabkan efek efikasi obat (Daberte, et al., 2011).
Modifikasi cangkang kapsul gelatin dapat berupa penambahan crosslinker
yang digunakan dalam drug delivery system harus biodegradable dan memiliki
biokompabilitas tinggi (Zhou, 2008).
Polimer telah banyak digunakan sebagai bahan pembuat material drug delivery system (Vilar et al., 2012). Berdasarkan kemampuannya untuk terdegradasi, drug delivery system dapat diklasifikasikan menjadi material polimer
nondegradable dan polimer biodegradable. Polimer biodegradable banyak dipilih sebagai drug delivery system agar aman dikonsumsi (Paolino et al., 2006).
Polimer alam yang berpotensi menjadi material drug delivery system
adalah pati. Penelitian tentang drug delivery system menggunakan pati telah dilakukan oleh Wang et al., (2010), Zhang et al., (2013), Lopez et al., (2013) dan Hosseini et al.,(2014), Fakharian et al., (2015), Marto et al., (2015), Lozano-Vazquez et al.,(2015) dan Mary and Sasikumar, (2015). Dalam penelitiannya, Wang et al., (2010) menggunakan komposit polimer pati – alginat sebagai bahan material local drug delivery system menggunakan bantuan crosslinker CaCl2.
Variasi rasio komposisi pati – alginat yang digunakan adalah (90:10), (70:30), (50:50) and (30:70) dan penambahan CaCl2 : etanol sebesar 50 : 50. Uji kontrol
release obat meningkat seiring dengan meningkatnya komposisi pati di dalam komposit pati – alginat. Hal ini menunjukkan potensi pati yang sangat besar dalam drug delivery system.
Lopez et al., pada tahun 2013 menguji release antioksidan tumbuhan
Pada hasil swelling, komposit pati-alginat memberikan hasil swelling yang stabil daripada alginat saja dan porositas kapsul alginat menurun seiring dengan meningkatnya pati yang ditambahkan. Namun dalam penelitian ini hasil release
kurang maksimal dan cenderung cepat karena kapsul yang dihasilkan terlalu tipis dengan porositas yang cukup tinggi. Hal ini mungkin dikarenakan tidak adanya
crosslinker yang ditambahkan sehingga tidak adanya penghubung antara pati dan alginat yang menyebabkan ketahanan mekanik rendah.
Modifikasi materi drug delivery system terbaru dengan pati dan alginat dilakukan oleh Mary and Sasikumar (2015). Dalam penelitiannya, drug delivery
diuji kinetika release dari antibiotik ciprofloxacin hydrochloride dengan cara in vitro. Variasi komposisi yang digunakan yaitu (1:1), (1:2), (1:3) dan (1:4). Setelah diamati selama 2 jam, hasil release tercepat yaitu pada komposisi pati – alginat 1:1 sebesar 65% dan release terlama yaitu pada perbandingan 1:4.
Dalam pembuatan material drug delivery system, selain pati dan alginat juga ditambahkan crosslinker yang berguna dalam menjembatani terjadinya ikatan antara dua gugus fungsi sehingga kinerja drug delivery system dapat meningkat (Giri, 2012). Jika crosslinker ditambahkan, maka tingkat swelling air membran dapat diperkecil dan kestabilannya meningkat. Crosslinker juga mempengaruhi besarnya kerapatan rantai polimer karena banyaknya tarikan yang dapat terjadi, sehingga mengurangi fleksbilitas dan menjadi kaku. Senyawa-senyawa
crosslinker antara lain glutaraldehid, sodium tripolyphosphate (STPP), N,N’-metilen-bis-akrilamida (MBA), asam oksalat, formaldehid, ion sulfat, ion fosfat, dan beberapa senyawa lainnya yang dapat berikatan dengan bahan utama membran (Berger et al., 2004).
Berdasarkan sifatnya, crosslinker dapat dibedakan menjadi kovalen dan ionik (Berger et al., 2004). Mekanisme yang paling tepat dalam menurunkan kebebasan molekul adalah ikatan silang kimia yang mengikat silang bersama rantai-rantai polimer melalui ikatan kovalen atau ikatan ion untuk membentuk suatu jaringan (Katz, 2008). Crosslinker kovalen seperti glutaraldehid, formaldehid dan asam oksalat. Sedangkan untuk crosslinker ionik contohnya
sodium tripolyphosphate (STPP) dan CaCl2.
menujukkan hasil yang tidak jauh berbeda, disarankan untuk menggunakan glutaraldehid dalam konsentrasi kecil guna meminimalisir efek toksik yang disebabkan oleh crosslinker tersebut.
Pieróg (2009) menguji pengaruh crosslinker ionik pada swelling hydrogel
kitosan. Crosslinker yang diujikan adalah asam sulfat (H2SO4), trisodium sitrat
(Na3C6H5O7), tripolifosfat dan natrium alginat. Variasi pH yang digunakan adalah
1.2, pH 7.4 dan pH 8.5. Pada uji swelling, kitosan murni memiliki nilai swelling
yang tinggi dan ketahanan mekanik yang rendah sementara kitosan-tripolifosfat memiliki nilai swelling yang rendah dan ketahanan mekanik yang tinggi. Hal ini mengindikasikan bahwa potensi tripolifosfat sebagai crosslinker sangat besar.
1.2Rumusan Masalah
Berdasarkan latar belakang yang telah diuraikan, dapat dirumuskan permasalahan sebagai berikut :
1. Dapatkah dibuat kapsul dari pati - alginat sebagai drug delivery system?
2. Bagaimana pengaruh variasi komposisi pati – alginat terhadap sifat mekanik drug delivery system?
3. Bagaimana kinerja material kapsul pati – alginat dibandingkan dengan kapsul dari bahan-bahan komersil?
1.3 Tujuan
1. Membuat kapsul dari pati-alginat sebagai drug delivery system
2. Mengetahui pengaruh variasi komposisi pati – alginat terhadap sifat mekanik drug delivery system
3. Mengetahui kinerja material kapsul pati – alginat dibandingkan dengan kapsul dari bahan-bahan komersil
1.4 Manfaat
Penelitian ini bermanfaat untuk pengembangan ilmu pengetahuan dan teknologi, khususnya di bidang kimia. Penelitian ini diharapkan menjadi salah satu informasi ilmiah dalam pengembangan material drug delivery system.
BAB II
TINJAUAN PUSTAKA 2.1Material Drug Delivery System
Penelitian tentang drug delivery system menggunakan bahan baku polimer alam sudah banyak dilakukan (Vilar et al., 2012). Polimer alam yang sering digunakan dalam pembuatan drug delivery system adalah kitosan yang diperoleh dari deasetilasi kitin. Salah satunya telah dilakukan oleh Tahtat, et al., (2013) dengan membuat material drug delivery system dari alginat - kitosan dengan bantuan crosslinker glutaraldehid untuk oral delivery insulin.
Selain kitosan, polimer alam lain yang berpotensi menjadi material drug delivery system adalah pati. Penelitian tentang drug delivery system menggunakan pati telah dilakukan oleh Wang et al., (2010), Zhang et al., (2013), Lopez et al., (2013) dan Hosseini et al., (2014), Fakharian et al., (2015), Marto et al., (2015) dan Lozano-Vazquez et al., (2015).
Menurut penelitian Wang et al., (2010) drug delivery system dibuat dengan cara mengkompositkan dua polimer alam yaitu pati dan alginat yang diperoleh dari ektraksi rumput laut coklat (Sargassum sp.). Hidrokoloid seperti alginat dapat memainkan peran penting dalam desain produk control-release. Hal ini menunjukkan alginat dari hasil ekstraksi rumput laut coklat (Sargassum sp.) sangat berpotensi menjadi material drug delivery system.
viskositas dan viskoplastisitas. Kemampuan release kapsul pati – karaginan sebanding dengan kapsul gelatin yang beredar di pasaran. Hal ini membuktikan bahwa potensi pati sangat besar dalam drug delivery system.
2.2Pati
Pati adalah karbohidrat kompleks yang tidak larut dalam air, berwujud bubuk putih, tawar dan tidak berbau. Pati merupakan karbohidrat dengan berat molekul tinggi yang terdapat pada tanaman dan mampu mensuplay 70 hingga 80% kalori yang dibutuhkan manusia dari bahan pangan yang dikonsumsi. Namun, selain sebagai sumber kalori utama, pati juga mempunyai sejumlah kegunaan pada makanan, seperti : sebagai bahan pelekat, pengikat, pembentuk lapisan, penstabil, pembentuk tekstur, pengental, dll (Mason, 2009). Kandungan amilosa merupakan bagian polimer linier dengan ikatan α-(1,4) unit glukosa.
Derajat polimerisasi amilosa berkisar antara 500 − 6.000 unit glukosa, bergantung pada sumbernya. Amilopektin merupakan polimer α-(1,4) unit glukosa dengan
rantai samping α-(1,6) unit glukosa. Dalam suatu molekul pati, ikatan α-(1,6) unit
glukosa ini jumlahnya sangat sedikit, berkisar antara 4 − 5%. Namun, jumlah molekul dengan rantai yang bercabang, yaitu amilopektin, sangat banyak dengan derajat polimerisasi 105 − 3x106 unit glukosa (Jacobs dan Delcour, 1998).
Ketika dipanaskan dalam air, amilopektin akan membentuk lapisan yang transparan, yaitu larutan dengan viskositas tinggi dan berbentuk lapisan-lapisan seperti untaian tali. Pada amilopektin cenderung tidak terjadi retrogradasi dan tidak membentuk gel, kecuali pada konsentrasi tinggi (Belitz dan Grosch, 2009).
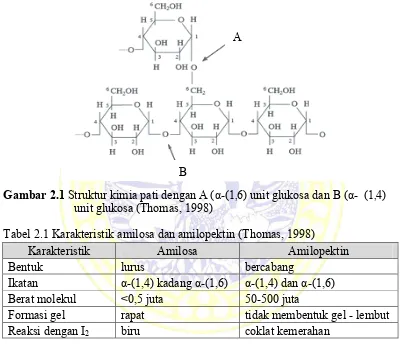
Gambar 2.1 Struktur kimia pati dengan A (α-(1,6) unit glukosa dan B (α- (1,4)
unit glukosa (Thomas, 1998)
Tabel 2.1 Karakteristik amilosa dan amilopektin (Thomas, 1998)
Karakteristik Amilosa Amilopektin
Bentuk lurus bercabang
Ikatan α-(1,4) kadang α-(1,6) α-(1,4) dan α-(1,6)
Berat molekul <0,5 juta 50-500 juta
Formasi gel rapat tidak membentuk gel - lembut
Reaksi dengan I2 biru coklat kemerahan
Pati dikenal sebagai polimer biodegradable dengan biocompability yang sempurna dan tidak toksik (Herman et al., 1989). Wang et al., (2010) juga mengkompositkan pati - alginat dalam sintesis material drug delivery system dan hasil penelitiannya menunjukkan uji control release meningkat seiring dengan meningkatnya komposisi pati dalam komposit pati – alginat. Mengkompositkan
A
alginat - pati sebagai pengembangan teknologi internal gelasi merupakan kombinasi yang cocok karena dapat meningkatkan efisiensi daripada menggunakan alginat sendiri (Martin et al., 2013). Hal ini mengindikasikan bahwa pati yang berpotensi besar dalam pengembangan drug delivery system.
2.3Alginat dari Ekstraksi Rumput Laut Coklat (Sargassum sp.)
Rumput laut coklat adalah salah satu jenis ganggang yang diklasifikasikan berdasarkan pigmen yang dihasilkan. Pigmen yang menyebabkan warna coklat pada rumput laut jenis ini adalah xantofil. Beberapa kandungan yang terdapat pada rumput laut coklat adalah alginat, yodium, vitamin E dan polifenol (Aslan, 1991). Beberapa spesies rumput laut coklat yaitu Colpmenia sinuosa, Lobophora variegate, Chnoospora implexa, Padina gymnospora, Sargassum tenerrium, dan
Dictyota dichotoma (Viswanathan and Nallamuthu, 2014).
Gambar 2.2Sargassum sp.
memiliki kemampuan adaptasi yang tinggi terhadap lingkungan dan memiliki masa tanam yang relatif pendek.
Malviya dan Srivastava (2011) telah meneliti tentang drug delivery system
dari bahan polimer alam alginat yang diektraksi dari rumput laut coklat (Sargassum sp.) yang dikombinasikan dengan kitosan. Dilakukan crosslink antara alginat dan kitosan secara ionik dengan perbandingan komposisi 1 : 1 menghasilkan material kompleks kitosan dan alginat. Polimer yang dihasilkan tidak rapuh, memiliki kekerasan yang baik, dan waktu desintegrasinya rendah sehingga dapat digunakan sebagai bahan drug delivery yang cepat terdesintegrasi. Hal ini menunjukkan alginat dari hasil ekstraksi rumput laut coklat (Sargassum sp.) sangat berpotensi menjadi material drug delivery system.
Berdasarkan penelitian Viswanathan pada tahun 2012, kandungan terbesar pada Sargassum sp. adalah alginat. Senyawa ini merupakan polimer murni dari asam uronat, tersusun dalam bentuk rantai linier panjang (Swift et al., 2014). Alginat telah banyak dimanfaatkan oleh berbagai industri sebagai bahan pengental (Bangun, 2001), Alga Sargassum sp. atau alga coklat merupakan salah satu genus Sargassum yang termasuk dalam kelas Phaeophyceae.
Kandungan terbesar dalam rumput laut coklat seperti Sargassum sp.
alginat (Jayanudin dkk, 2014). Namun yang larut dalam air hanya natrium alginat, kalium alginat dan ammonium alginat (Biopolymer F.M.C, 2003).
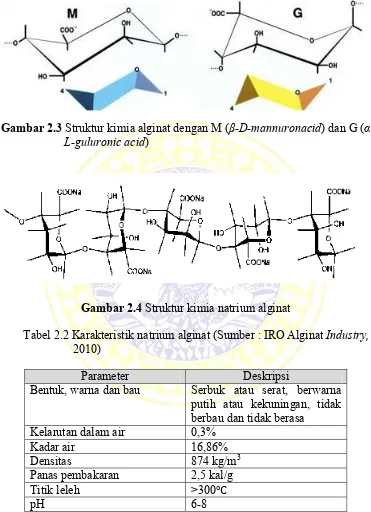
Gambar 2.3 Struktur kimia alginat dengan M (β-D-mannuronacid) dan G ( α-L-guluronic acid)
Gambar 2.4 Struktur kimia natrium alginat
Tabel 2.2 Karakteristik natrium alginat (Sumber : IRO Alginat Industry,
2010)
Parameter Deskripsi
Bentuk, warna dan bau Serbuk atau serat, berwarna putih atau kekuningan, tidak berbau dan tidak berasa
Kelarutan dalam air 0,3%
Kadar air 16,86%
Densitas 874 kg/m3
Panas pembakaran 2,5 kal/g
Titik leleh >300℃
Pada pH rendah, asam alginat mengarah pada pembentukan viskositas tinggi gel asam. Alginat juga mudah membentuk gel dengan adanya kation divalen sebagai ion kalsium (Tonnesen and Karlsen, 2002).
2.4Crosslinker pada Drug Delivery System
Cross link merupakan suatu metode yang dilakukan untuk mengurangi kelarutan membran dalam air (Ma, J and Sahai, Y., 2013). Penambahan
crosslinker berfungsi untuk menjembatani terjadinya ikatan antara dua gugus fungsi sehingga crosslinker dapat meningkatkan kinerja drug delivery system
(Giri, 2012). Ikatan yang terjadi dapat berupa ikatan kovalen maupun ionik. Jika
crosslinker ditambahkan maka tingkat swelling air membran dapat diperkecil dan kestabilannya meningkat. Senyawa-senyawa crosslinker antara lain glutaraldehid,
sodium tripoliphosphate (STPP), N,N’-metilen-bis-akrilamida (MBA), asam oksalat, formaldehid, ion sulfat, ion fosfat, dan beberapa senyawa lainnya yang dapat berikatan dengan bahan utama membran (Berger et al., 2004).
Berdasarkan sifatnya, crosslinker dapat secara kovalen dan ionik (Gunter, 1985). Mekanisme yang paling tepat dalam menurunkan kebebasan molekul adalah ikatan silang kimia yang mengikat silang bersama rantai-rantai polimer melalui ikatan kovalen atau ikatan ion untuk membentuk suatu jaringan (Katz, 2008). Glutaraldehid termasuk dalam crosslinker kovalen, contoh lainnya seperti formaldehid dan asam oksalat. Sedangkan untuk crosslinker ionik contohnya
sodium tripolyphosphate (STPP).
melalui modifikasi cross link secara kovalen (Giri, 2012). Beberapa crosslinker
yang berikatan secara kovalen adalah glutaraldehid, genipin, dan N,N’-metilen-bis-akrilamida (MBA).
Pada tahun 1998, Genta, menguji pengaruh glutaraldehid pada drug delivery system dengan bahan dasar kitosan. Matriks drug delivery system diuji secara in vitro dengan uji disolusi dengan larutan buffer fosfat pH 7.4 pada suhu 37℃. Hasil uji menunjukkan penambahan glutaraldehid bermanfaat dalam mengatur terurainya kitosan, variasi 7%-10% dan 15-25% glutaraldehid menujukkan hasil yang tidak jauh berbeda, disarankan untuk menggunakan glutaraldehid dalam konsentrasi kecil guna meminimalisir efek toksik yang disebabkan oleh crosslinker.
Pieróg (2009) membandingkan hasil swelling kitosan murni dan kitosan yang dimodifikasi dengan crosslinker tripolifosfat. Kitosan modifikasi memiliki ketahanan mekanik lebih kuat dengan waktu swelling yang rendah sedangkan kitosan memiliki ketahanan mekanik yang rendah dengan waktu swelling yang tinggi.
Cross link secara ionik juga banyak dilakukan pada material drug delivery system. Karakteristik kelarutan, rasio swelling, dan proses pelepasan obat pada material drug delivery system seringkali disebabkan oleh proses ionisasi dan protonasi gugus fungsi pada polimer yang digunakan. Untuk mengurang ionisasi dan protonasi tersebut, selain dengan penambahan material polimer lain, juga dapat ditingkatkan dengan crosslinker ionik seperti sodium tripolyphosphate
2.5Sodium tripolyphosphate (STPP)
Sodium tripolyphosphate merupakan senyawa anorganik dengan rumus molekul Na5P3O10 dan merupakan bentuk garam dari polyphosphat penta-anion
yang berikatan dengan triphosporic acid. Garam STPP berwarna putih dan terdapat dalam dua bentuk yaitu anhidrat dan hexahidrat.
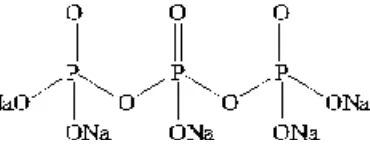
Struktur sodium tripolyphosphate (STPP) ditunjukkan pada Gambar 2.5
Gambar 2.5 Struktur kimia sodium tripolyphosphate
Tabel 2.3 Karakteristik sodium tripolyphosphate
Karakteristik Keterangan Berat molekul 367,87 g/mol
Densitas 2,52 g/cm3
Kelarutan dalam air 14,5 g/100 mL (25°C)
Bentuk Serbuk berwarna putih
Sodium tripolyphosphate dapat dibuat dengan cara mencampurkan Na2HPO4 dan NaH2PO4 dengan kondisi yang terkontrol (Greenwood, 1997).
Berikut reaksi yang terjadi :
2 Na2HPO4 + NaH2PO4 → Na5P3O10 + 2 H2O
Garam ini memiliki nilai toksisitas yang rendah dari hasil uji LD50 secara oral
sebesar > 1.000 mg/Kg berat badan (Boyd et al., 2001). LD50 (lethal dose)
kematian sampai 50% dari jumlah hewan yang di uji. Nilai LD50 digunakan untuk
mengelompokkan dosis toksik dari bahan kimia yang baru diproduksi.
Tabel 2.4 Kriteria dosis urutan daya toksisitas suatu bahan (per-berat badan manusia ~70 Kg) (Gosselin et al., 1984)
Kriteria Dosis
Praktis tidak toksik >15g/Kg Sedikit toksik 5-15 g/Kg Toksik sedang 0,5-5 g/Kg
Sangat toksik 50-500 mg/Kg Amat sangat toksik 5-50 mg/Kg
Super toksik <5 mg/Kg
2.6Metode Pencetakan Kapsul
Penemuan kapsul pertama kali yaitu oleh F.A.B Mothes, 1834. Pada awalnya kapsul memiliki bentuk lonjong dan hanya terdiri atas 1 bagian. Selanjutnya pada tahun 1846 dikembangkan kapsul yang terdiri atas 2 bagian cangkang oleh seorang farmasis dari Paris yang bernama J.C. Lehubby. Bentuk kapsul yang terdiri atas 2 cangkang ini masih digunakan hingga sekarang (Banker and Rhodes, 2002).
suhu 70-80 oC dan tertutupi dengan aluminium foil. Setelah rasio b/b pati dan
alginat telah didapatkan, selanjutnya ditentukan komposisi crosslinker yang akan ditambahkan. Untuk cangkang kapsul yang disertai crosslinker sodium tripolyphosphate (STPP), larutan STPP 2% ditambahkan pada komposisi campuran pati-alginat optimal yang sudah didapatkan dalam perbandingan tertentu. Penambahan dilakukan sebelum pemanasan larutan.
Proses pemanasan diakhiri ketika larutan campuran telah homogen. Campuran dituangkan pada dipping bath yang sudah dipanaskan pada rentang suhu 65-75 oC. Pencetakan dilakukan dengan pencelupan dipping pen yang sudah
terlebih dahulu dilumasi oleh pelumas makanan. Material yang menempel pada
dipping pen dikeringkan pada suhu ruang (Kristanto, 2014). 2.7Prinsip Kerja Material Drug Delivery System
Ada beberapa faktor yang mempengaruhi kinerja material drug delivery system, di antaranya morfologi permukaan kapsul, ukuran kapsul, ada tidaknya suatu plasticizer atau crosslinker, dan kesesuaian sifat fisikokimia obat dengan karakteristik dari polimer seperti hidrofobik atau hidrofilik, kemampuan dalam membentuk gel, dan juga kapasitas swelling air (Bansal, 2011).
yang ditambahkan maka tingkat kelunakan kapsul semakin tinggi, sedangkan penambahan crosslinker sebaliknya, semakin banyak crosslinker yang ditambahkan, maka ketahanan mekanik suatu kapsul yang diperoleh semakin tinggi. Sifat hidrofobik dan hidrofilik suatu polimer mempengaruhi dalam kinerja
drug delivery, kapsul yang terbuat dari polimer hidrofilik cenderung release lebih cepat karena kesesuaiannya dengan kondisi tubuh yang lebih dari 60% tersusun oleh air (Guyton and Hall, 2006). Kemampuan polimer dalam membentuk gel juga mempengaruhi kinerja suatu drug delivery, polimer yang mampu membentuk gel akan menghasilkan kapsul yang cenderung lunak dan tidak terlalu keras karena berasal dari sifat gel itu sendiri. Faktor lain yang mempengaruhi drug delivery suatu kapsul adalah kapasitas swelling air, polimer hidrofilik yang mempunyai ketahanan mekanik rendah akan mengalami swelling air yang cepat, begitupun sebaliknya.
Larutan buffer yang digunakan dalam disolusi disesuaikan dengan pH bagian tubuh yang akan dituju, seperti pada lambung maka larutan buffer yang digunakan adalah larutan dengan pH 1,2. Pada usus 12 jari digunakan larutan buffer dengan pH 4,5 (Ovesen et al., 1986) dan pH 6,8 untuk usus halus (Fallingborg, 1999).
Sementara itu, proses drug delivery secara umum dapat dibagi menjadi 3 mekanisme yaitu erosi, difusi, dan release melalui permukaan material (Bansal et al., 2011).
Pada mekanisme difusi, obat berdifusi keluar melalui sistem matriks. Inti obat dienkapsulasi dalam membran dalam hal ini berupa kapsul, sehingga difusi obat dapat dikendalikan kecepatan pelepasannya. Mekanisme pelepasan obat yang terjadi berawal dari terlarutnya obat di dalam membran dan diikuti oleh difusi dan terlepasnya obat dari permukaan pada sisi lain dari membran (Shargel et al.,
2007).
Pada proses erosi, polimer pada matriks akan mengalami erosi atau pengikisan karena terbentuk ikatan labil akibat reaksi yang terjadi secara hidrolisis maupun enzimatis. Seiring dengan terkikisnya polimer, maka obat akan dilepaskan ke dalam medium di sekitarnya (Shargel et al., 2007).
obat yang telah diserap tubuh akan diuraikan dengan sangat cepat dan menyebabkan terjadinya pemecahan. Dari tahap ini maka obat yang tersimpan di dalam material akan terserap oleh tubuh melalui lambung dan usus halus (Cairns, 2004).
Gambar 2.6 Skema release suatu obat (Fu, et al., 2010)
2.8Karakterisasi Material Drug Delivery System
Karakterisasi material drug delivery system dapat dilakukan menggunakan spektrofotometer Fourier Transformed Infra Red (FTIR), uji morfologi dengan
Scanning Electron Microscopy (SEM), penentuan berat molekul, uji swelling air, uji tarik, dan uji disolusi.
2.8.1 Fourier Trasform Infra Red (FTIR)
Tujuan utama pengujian dengan spektrofotometer FTIR adalah untuk mengetahui gugus fungsi yang terdapat pada suatu senyawa.
Spektroskopi FTIR adalah teknik pengukuran untuk mengumpulkan spektrum inframerah. Energi yang diserap sampel pada berbagai frekuensi sinar inframerah direkam, kemudian diteruskan ke interferometer. Secara umum, spektrofotometer FTIR sama seperti spektrofotometer IR, yang membedakan
Membran polimer
Zat terlarut
antara keduanya adalah sistem optik yang dikembangkan pada berkas sinar inframerah. Pada spektrofotometer FTIR, sistem optik yang digunakan adalah laser dan neon sedangkan pada spektofotometer IR adalah cermin diam dan nernst glower. Atom-atom dalam suatu molekul selalu bervibrasi. Bila radiasi sinar inframerah sesuai dengan frekuensi vibrasi dari atom-atom tersebut, maka akan terjadi serapan pada molekul dan terjadi transisi antara tingkat energi vibrasi dasar dengan tingkat energi vibrasi dalam keadaan tereksitasi. Tidak semua ikatan dalam molekul dapat menyerap energi inframerah meskipun memiliki frekuensi radiasi sesuai dengan gerakan ikatan. Ikatan-ikatan yang memiliki momen dipol dapat menyerap radiasi dari sinar inframerah ini (Sastrohamidjojo, 2001).
sehingga diperoleh spektrum IR yang menggambarkan besar % transmitan (%T) dan bilangan gelombangnya (cm-1) (Stuart, 2004).
Natrium alginat memberikan pita berupa O-H stretching pada daerah 3.242 cm-1 (Lawrie et al., 2007). Tidak jauh berbeda dari penelitian sebelumnya
yang dilakukan oleh Sankalia et al., (2005) bahwa stretch O-H natrium alginat muncul pada daerah 3.263,33 cm-1, karbonil 1.600,81 cm-1 dan karboksilat pada
1.000-1.400 cm-1. Sedangkan pada penelitian terbaru oleh Nagpal et al., 2013,
natrium alginat memberikan O-H stretching pada daerah 3.430,30 cm-1, karbonil
pada 1.616,03 cm-1 dan karboksilat pada 1416,39 cm-1.
Pada alginat, terdapat dua macam kandungan yaitu asam manuronat dan asam guluronat sehingga memberikan proporsi dan pita yang berbeda (Pereira et al., 2013). Berdasarkan hasil penelitian Sakugawa et al., (2014) rasio konsentrasi karakteristik tertentu M/G dari sampel alginat dapat disimpulkan dari intensitas relatif rasio dari dua band yaitu sebesar 1030/1080 cm-1 pada kalsium alginat dan
1.019/1.025 cm-1 pada mangan alginat. Absorbansi pada 1.030 cm-1 langsung
mencerminkan perubahan konsentrasi manuronat alginat dan 1.025 cm-1
dikaitkan dengan OH lentur dari guluronat. Rasio alginat M/G tentatif diperkirakan sekitar 1030/1080 cm-1 pada spektrum inframerah.
2.8.2 Scanning Electron Microscopy (SEM)
Suatu berkas elektron dengan energi kinetik sebesar 1-25 kV dan diameter 5 – 10 nm, diarahkan melewati suatu permukaan sampel yang dilapisi dengan film konduktor sehingga terjadi interaksi dengan berkas elektron dan menghasilkan sinyal (Mulder, 1996). Berkas elektron ini disebut elektron primer yang mempunyai energi tinggi sedangkan yang dipantulkan disebut elektron sekunder yang mempunyai energi rendah. Interaksi berkas elektron ini dengan sampel ini akan menghasilkan pola difraksi elektron (Nursanto dkk, 2011).
Sinyal yang dihasilkan dari penembakan elektron ditangkap oleh detektor lalu diteruskan ke monitor. Dari monitor diperoleh gambar yang khas yang menggambarkan permukaan atau penampang lintang dari sampel (Sutiani, 2009). 2.8.3 Penentuan Berat Molekul Polimer
Polimer merupakan unit monomer yang tersusun berulang-ulang (Patterson, 2012). Pada prinsipnya, polimer tersusun atas banyak polimer tak terbatas yang dihubungkan oleh ikatan kovalen kimia . Namun biasanya setiap monomer dibuat lebih dari 5 dan kurang dari 500 atom (Arndt, 2013).
Penentuan berat molekul rata-rata suatu polimer dapat ditentukan dengan viskometer Ostwald. Penentuan ini diawali dengan membuat variasi konsentrasi polimer dalam pelarut tertentu dan diukur waktu alirnya. Dari proses ini dapat dihitung viskositas spesifik dan viskositas reduksi dengan persamaan berikut :
ηsp = (t1−t0)
t0 .………...….. (1)
ηred = ηsp
Setelah itu dibuat grafik hubungan antara viskositas reduksi dan konsentrasi. Intercept yang diperoleh selanjutnya dimasukan dalam persamaan Mark Houwink-Sakurada yang ditunjukan oleh Persamaan 4.
ηred = [η] + k [η]2C………...………..….. (3)
η = K [Mv]a ……….………...………. (4)
Keterangan :
ηsp = viskositas spesifik
ηred = viskositas reduksi
t0 = waktu alir pelarut (s)
t1 = waktu alir akhir (s)
Mv = berat molekul polimer (g/mol) k = konstanta pelarut
a = tetapan spesifik polimer (Brandrup dan Immergut, 1989) 2.8.4 Uji Swelling air
kedua kekuatan ini sama besar. Berikut adalah persamaan untuk menghitung %
swelling air :
% 𝑠𝑤𝑒𝑙𝑙𝑖𝑛𝑔 = (Wbasah−W kering)
W kering 𝑥 100% ... (5)
Dengan W adalah massa basah dan massa kering membran (gram) (Kaban et al., 2006).
2.8.5 Uji Tarik
Dalam penentuan tingkat ketahanan material terhadap gaya luar, diperlukan uji mekanik berupa uji tarik. Adalah salah satu uji stress
(tegangan)-strain (regangan) mekanik yang bertujuan untuk mengetahui kekuatan bahan terhadap gaya tarik. Dalam pengujiannya, bahan uji ditarik sampai putus (Sukandi dan Santoso, 2014).
Uji tarik dapat dilakukan dengan menggunakan Autograph. Membran yang akan diuji dipotong dengan ukuran ± 6 x 1 cm dan dikaitkan pada alat
Autograph. Ujung-ujung membran dikaitkan dengan alat uji dan penarik dipasang pada satuan beban kgF (kilogram-Force). Membran ditarik dengan kecepatan 1 cm/menit hingga putus. Besar beban penarik dan perubahan panjang membran pada saat putus dicatat. Berikut adalah persamaan untuk menghitung stress, strain
l = panjang awal (cm) A = luas permukaan (cm2)
Δl = hasil selisih dari panjang awal dengan panjang akhir sebelum membran terputus (Sukandi dan Santoso, 2014).
2.8.6 Uji Disolusi
Disolusi merupakan suatu proses perpindahan molekul obat dari bentuk padat ke dalam suatu media berupa larutan. Uji disolusi bertujuan untuk mengetahui banyaknya zat aktif yang terlarut dan memberikan efek terapi di dalam tubuh. Kecepatan absorbsi obat tergantung pada pemberian yang dikehendaki dan juga harus dipertimbangkan frekuensi pemberiannya (Syamsuni, 2007).
Disolusi yang dilakukan untuk evaluasi bentuk kapsul ini berbeda dengan sediaan konvensional, baik dari segi alat maupun lamanya proses disolusi. Salah satu metode disolusi yang sangat baik, seperti yang dipublikasikan oleh Gohel et al., 2004. Dalam uji disolusi ini, digunakan gelas beker yang dimodifikasi dengan menambahkan suatu saluran tempat sampling yang menempel pada dasar
Gambar 2.7 Desain rangkaian alat disolusi (Gohel et al., 2004) Sampel yang akan
dianalisis
Magnetic stirrer
(75 rpm) 25 ml larutan pH
BAB III
METODOLOGI PENELITIAN 3.1 Tempat dan Waktu Penelitian
Penelitian ini dilaksanakan pada bulan Februari sampai Juli 2016. Penelitian dilaksanakan di Laboratorium Kimia Fisik, Departemen Kimia, Fakultas Sains dan Teknologi, Universitas Airlangga. Uji spektroskopi menggunakan FTIR dilaksanakan di Laboratorium Instrumen FMIPA Institut Teknologi Sepuluh November, uji tarik menggunakan Autograph dilaksanakan di Laboratorium Dasar Bersama (LDB) Farmasi Unair, uji morfologi menggunakan SEM dilaksanakan di Laboratorium Energi Institut Teknologi Sepuluh November dan Laboratorium Biosains Universitas Brawijaya Malang dan uji disolusi dilaksanakan di Laboratorium Kimia Universitas Surabaya.
3.2 Bahan dan Alat Penelitian 3.2.1 Bahan penelitian
Bahan-bahan yang digunakan dalam penelitian ini adalah tepung pati, rumput laut coklat (Sargassum sp.), akuades, asam klorida (HCl; 1% dan 10%), natrium hipoklorit (NaOCl; 4%), natrium karbonat (Na2CO3; 2%), isopropil
alkohol, kalium hidroksida (KOH; 0,1%), sodium tripolyphosphate (STPP) 2%, dan ciprofloxacin.
3.2.2 Alat – alat penelitian
3.3 Diagram Alir Penelitian
Ekstraksi natrium alginat dari rumput laut coklat (Sargassum sp.)
Diekstraksi dengan Na2CO3
2% selama 2 jam. Kemudian disaring dan diendapkan
dengan HCl 10% Dititrasi dengan Na2CO3 2% hingga
netral, ditambahkan NaOCl 4% hingga filtrat kuning bening
Filtrat dituang ke dalam isopropil alkohol, diaduk, didiamkan selama 30 menit, dikeringkan dan digiling
Sargassum sp. Dipotong-potong dan dicuci dengan akuades, direndam dalam KOH 0.1% dan dikeringkan
Sargassum sp. Direndam
Membuat kapsul pati – alginat (ekstraksi dan komersil) dengan perbandingan 1:1 ; 2:1 ; 3:2 ; 1:2 dan 2:3 dengan crosslinker STPP 2%
Stress Modulus Young Strain
Uji swelling
Kapsul pati-alginat optimum
3.4 Prosedur Penelitian 3.4.1 Preparasi reagen
1. Pembuatan larutan KOH 0,1 % (b/v)
Larutan dibuat dengan cara melarutkan 1 g KOH 85% dengan akuades pada gelas beaker 50 mL. Kemudian KOH yang telah larut dipindahkan ke dalam labu ukur 1000 mL dan ditambahkan akuades sampai tanda batas. 2. Pembuatan larutan HCl 1 % (v/v)
Larutan ini dibuat dengan cara diambil 27 mL larutan HCl 37% menggunakan gelas ukur, kemudian dipindahkan ke dalam labu ukur 1000 mL dan ditambahkan akuades sampai tanda batas.
3. Pembuatan larutan HCl 10 % (v/v)
Larutan ini dibuat dengan cara diambil 27 mL larutan HCl 37% menggunakan gelas ukur, kemudian dipindahkan ke dalam labu ukur 100 mL dan ditambahkan akuades sampai tanda batas.
4. Pembuatan larutan NaOCl 4% (v/v) dari NaOCl 12%
Larutan dibuat dengan cara diambil 33,3 mL NaOCl 12% menggunakan gelas ukur, kemudian dipindahkan ke labu ukur 100 mL dan ditambahkan akuades sampai tanda batas.
5. Pembuatan larutan Na2CO3 2% (b/v)
Larutan dibuat dengan cara melarutkan 2 g Na2CO3 99,9% dengan akuades
3.4.2 Ekstraksi natrium alginat dari Sargassum sp.
Metode ektraksi alginat yang digunakan dalam penelitian ini adalah hasil modifikasi dari jalur asam alginat yang dikembangkan oleh Balai Besar Riset Pengolahan Produk dan Bioteknologi Kelautan dan Perikanan, Jakarta. Sebelum dilakukan ekstraksi, rumput laut coklat (Sargassum sp.) dipotong kecil-kecil dan dicuci dengan akuades hingga bersih. Hasil potongan rumput laut yang telah dibersihkan direndam dalam KOH 0.1 % selama 1 jam dan dijemur sampai kadar air berkurang 15% (Husni dkk, 2012).
Ekstraksi alginat diawali dengan perendaman hasil rumput laut yang telah dikeringkan dengan HCl 1 %, perbandingan yang digunakan 1 : 30 (b/v) selama 1 jam. Kemudian rumput laut dinetralkan dengan cara dicuci dengan akuades berulang. Rumput laut netral diektraksi dengan Na2CO3 2% selama 2 jam dengan
perbandingan 1 : 30 (b/v) dan suhu dijaga antara 60° - 70° C. Filtrat hasil ekstraksi ditambahkan HCl 10% hingga pH 2.8 – 3.2 guna mengendapkan asam alginat (Husni dkk, 2012).
Selanjutnya ditambahkan Na2CO3 2% sampai pH netral dilakukan guna
3.4.3 Karakterisasi natrium alginat 3.4.3.1Penentuan berat molekul
Penentuan berat molekul natrium alginat yang telah disintesis yaitu dengan menggunakan viskometer Ostwald. Sebanyak 0,15 gram natrium alginat dilarutkan dalam akuades dan diencerkan dalam labu ukur 100 mL sampai tanda batas. Konsentrasi yang diperoleh adalah C yang selanjutnya diencerkan hingga diperoleh konsentrasi 0,1 C; 0,2 C; 0,3 C; dan 0,4 C. Sebanyak 5 mL masing-masing larutan ditentukan waktu alirnya (t) dengan menggunakan viskometer Ostwald. Ditentukan juga waktu alir akuades sebagai t0. Dari data tersebut
ditentukan viskositas spesifik dan reduksinya sesuai persamaan 1 dan 2. Selanjutnya dibuat grafik dimana sumbu x merupakan konsentrasi (C) dan sumbu y viskositas reduksi. Nilai intercept yang diperoleh dimasukan dalam persamaan 3 (Mark-Houwink Sakurada) sehingga diperoleh berat molekulnya.
3.4.3.2Penentuan gugus fungsi dengan FTIR
Natrium alginat dapat ditentukan gugus fungsinya menggunakan FTIR (Fertah et al., 2014). Teknik yang digunakan adalah pembentukan pelet KBr. Sebanyak 2 gram masing-masing sampel dihaluskan dan dicampur dengan KBr. Agar terbentuk lempengan tipis campuran ditekan dengan alat tekan hidrolik 10.000-15.000 Psi. Lempengan tipis dipasang dalam sel dan ditempatkan pada berkas jalannya sinar.
Alginat memberikan pita C=O pada daerah 1.612 cm-1 dan 1413 cm-1 C-H
(Mary and Sasikumar, 2015). Pada alginat, terdapat dua macam kandungan yaitu asam manuronat dan asam guluronat sehingga memberikan proporsi dan pitayang berbeda (Pereira et al., 2013). Rasio alginat M/G tentatif diperkirakan sekitar 1030/1080 cm-1 pada spektrum inframerah (Sakugawa et al., 2013).
3.4.4 Pembuatan komposit pati - alginat
Pembuatan komposit kapsul dari pati - alginat dilakukan dengan modifikasi metode yang dikembangkan oleh Dixit and Kulkarni (2012). Pada tahap awal, komposit dibagi menjadi 5 variasi perbandingan pati-alginat yaitu (2:1), (3:2), (1:1), (2:3) dan (1:2). Pada perbandingan (2:1), diambil 2,67 gram pati dan 1,33 gram alginat, kemudian dilarutkan dalam akuades 60 mL. selanjutnya ditambahkan STPP 2%. Lalu dihomogenkan dengan pengadukan disertai pemanasan sekitar 70-80℃ dengan ditutup menggunakan alumunium foil.
Selanjutnya, komposit didiamkan selama 24 jam. Setelah didiamkan, komposit dihomogenkan kembali, dilakukan pemanasan dan pengadukan dan diatur suhu sekitar 70℃ dengan kekentalan yang tepat, kemudian komposit dicetak menjadi kapsul dan sebagian dituangkan ke dalam cawan petri untuk dibuat membran guna uji tarik.
3.4.5 Pencetakan kapsul pati-alginat
Komposit yang telah dibuat dituangkan pada dipping bath yang sudah dipanaskan pada rentang suhu 65-75oC. Pencetakan dilakukan dengan pencelupan
3.4.6 Karakterisasi kapsul pati – alginat 3.4.6.1Uji mekanik
Uji mekanik terhadap komposit pati – alginat meliputi uji swelling air dan uji tarik.
1. Uji swelling air
Uji swelling air bertujuan untuk mengetahui kemampuan kapsul untuk menyerap air. Uji ini dilakukan dengan cara mengeringkan sampel membran dalam oven sehingga didapatkan berat kering membran (Wkering). Sampel
membran kering direndam dalam air kemudian ditimbang dan didapatkan berat basah membran (Wbasah). Selanjutnya % swelling ditentukan dengan persamaan 5.
(Kaban et al., 2006) 2. Uji tarik
Tingkat ketahanan material terhadap gaya luar ditentukan dengan uji tarik menggunakan Autograph. Membran yang akan diuji dipotong dengan ukuran 6 × 1 cm dan dikaitkan pada alat Autograph. Ujung-ujung membran dikaitkan dengan alat uji dan penarik dipasang pada satuan beban kilogram-Force. Membran ditarik dengan kecepatan 1 cm/menit hingga putus. Besar beban penarik dan perubahan panjang membran pada saat putus dicatat. Selanjutnya stress, strain, dan Modulus Young ditentukan dengan persamaan 6 sampai 8 (Sukandi dan Santoso, 2013). 3.4.6.2Uji kinerja
Uji disolusi bertujuan untuk mengetahui laju kelarutan zat aktif dari sediaan obat berada dalam tubuh untuk diabsorbsi (Hasibuan, 2011). Kapsul diisi dengan 100 mg ciprofloxacin kemudian dimasukkan dalam gelas beaker modifikasi kapasitas 100 ml yang berisi larutan buffer sebanyak 25 ml dengan pH 1,2; 4,5 dan 6,8 sebagai media disolusi. Selanjutnya alat dirangkai. Kapsul dibiarkan tenggelam dan pengaduk dijalankan dengan kecepatan 75 rpm dalam 15, 30, 45, 60, 75 dan 90 menit pada pH 1,2. Sedangkan variasi waktu yang digunakan pada pH 4,5 yaitu 20, 40, 60, 80, 100 dan 120 detik. Pada pH 6,8 yaitu 40, 80, 120, 160, 200 dan 240 detik. Sebanyak 10 mL larutan diambil untuk diukur absorbansinya. Untuk mempertahankan volume larutan, setiap pengambilan 10 mL sampel, ditambahkan 10 mL larutan pH ke dalam larutan (Gohel et al., 2004; Saifullah et al., 2007). Kemudian larutan yang telah diambil diuji konsentrasi ciprofloxacin yang dilepaskan menggunakan spektrofotometer UV-Vis dengan λmax 278 nm (Mary and Sasikumar, 2015) untuk pH 1,2.
Sedangkan untuk pH 4,5 pada λmax 272,5 nm dan pH 6,8 pada λmax 271 nm
(Gummadi et al., 2012). 3.4.6.3Uji SEM
BAB IV
HASIL DAN PEMBAHASAN 4.1 Hasil Ekstraski Natrium Alginat dari Sargassum sp.
Metode ekstraksi natrium alginat yang digunakan dalam penelitian ini merupakan metode yang dikembangkan oleh Balai Besar Pengolahan Produk dan Bioteknologi Kelautan dan Perikanan Jakarta melalui jalur asam alginat. Pada prosesnya, ekstraksi ini dibagi menjadi tiga tahap, yaitu delignifikasi, demineralisasi dan maserasi (Husni, dkk., 2012).
Pada tahap pertama, Sargassum sp. dicuci dengan air bersih guna menghilangkan pengotor dari sisa pasir laut yang tertinggal, kemudian ditimbang 100 gram dan dipotong kecil-kecil sekitar 2 cm. Pemotongan ini dilakukan agar mempercepat proses maserasi yang berlangsung. Setelah itu direndam dalam KOH pa 0,1% secukupnya selama 1 jam untuk degradasi lignin. Ibrahim et al., (2005) dalam Misson et al., (2009) mengemukakan bahwa lignin merupakan rantai dengan karbon-karbon terikat dan ikatan lainnya yang terdiri dari jaringan yang dihubungkan dengan polisakarida yang terdapat di dalam dinding sel. Kandungan lignin dalam Sargassum sp. sebesar 15,625% setiap gram (Anggarawati, 2012). Degradasi lignin dilakukan dengan cara ditambahkan basa seperti KOH, NaOH dan NH4OH (Julfana, et al., 2010). Setelah proses
perendaman selama 1 jam, Sargassum sp. dijemur di bawah sinar matahari sampai kadar airnya berkurang 15% (Husni, dkk., 2012).
Tahapan kedua adalah proses demineralisasi dengan cara Sargassum sp.
Sargassum sp. seperti atom Mg, Fe, Na dan Ca (Bachtiar, dkk., 2012). Kemudian
Sargassum sp. dinetralkan dengan akuades sampai mendekati pH 7.
Persamaan reaksi yang terjadi pada saat demineralisasi berlangsung ditunjukkan pada Gambar 4.1.
CaCO3(s) + 2HCl(aq) CaCl2(aq) + H2CO3(aq)
H2CO3(aq) H2O(aq) + CO2(g)
Gambar 4.1 Persamaan reaksi kimia pada saat proses demineralisasi (Anis, 2016) Proses ekstraksi tahap ketiga yaitu maserasi Sargassum sp. dengan larutan NaCO3 2% pada suhu 60-70% selama 2 jam. Tujuan penambahan NaCO3 2%
yaitu guna pembentukan natrium alginat dan terpisah dari senyawa lain yang terdapat dalam Sargassum sp. Setelah maserasi 2 jam, Sargassum sp. dipisahkan antara padatan dan filtratnya sesuai Gambar 4.2.
Gambar 4.2 Pemisahan antara filtrat dan padatan setelah maserasi
+ Na2CO3
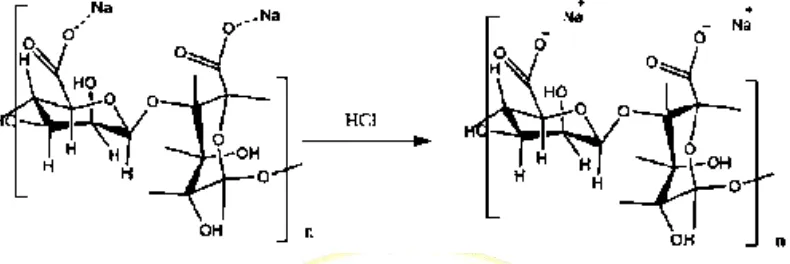
pada pH < 3,5 (Amalia, 2014). Persamaaan reaksi kimia natrium alginat dengan HCl terdapat pada Gambar 4.3.
Gambar 4.3 Persamaaan reaksi kimia natrium alginat dengan HCl (Sari, 2015) Selanjutnya asam alginat dikonversi menjadi natrium alginat kembali dengan cara ditambahkan sedikit demi sedikit NaCO3 2% disertai pengadukan
agar cepat larut hingga pH netral (Husni dkk., 2012). Persamaan reaksi kimia konversi asam alginat menjadi natrium alginat ditunjukkan pada Gambar 4.4
Gambar 4.4 Persamaan reaksi kimia konversi asam alginat menjadi natrium alginat (Sari, 2015)
Filtrat natrium alginat ditambah dengan NaOCl 4% sampai warna filtrat berubah dari coklat menjadi kuning bening. NaOCl merupakan bleaching agent
yang dapat mengoksidasi zat warna yang gelap menjadi warna yang lebih terang (Mushollaeni, et al., 2011). Persamaan reaksi yang terjadi pada saat bleaching
Gambar 4.5 Persamaan reaksi kimia oksidasi lignin oleh NaOCl (Sari, 2015) Filtrat bening dituangkan ke dalam gelas beaker yang berisi isopropil alkohol sehingga terbentuk serat putih kekuningan. Penambahan isopropil alkohol berfungsi untuk presipitasi (Basmal et al., 2013). Serat yang telah terbentuk dikeringkan di bawah sinar matahari, atau dengan cara lain menggunakan bantuan
Buchner untuk menyerap air agar lebih cepat kering. Setelah mengering, serat ditumbuk dengan mortar agar terbentuk serbuk natrium alginat putih kekuningan sesuai Gambar 4.6 dengan luas permukaan yang semakin besar. Ketika luas permukaan semakin besar, kecepatan serbuk untuk menjadi gel semakin besar. Rendemen yang dihasilkan sebesar 29%.
natrium alginat yang larut dalam air. Semakin tinggi suhu ekstraksi maka semakin tinggi hasil konversi. Namun, batas suhu optimal ekstraksi adalah 60℃, karena suhu yang terlalu tinggi menyebabkan natrium alginat terdegradasi (Jayanuddin, dkk., 2014).
Gambar 4.6 Serbuk natrium alginat 4.2 Hasil Karakterisasi Natrium Alginat
4.2.1 Hasil uji penentuan berat molekul
Natrium alginat dilarutkan dalam akuades untuk uji kelarutan. Serbuk natrium alginat tidak dapat terlarut sempurna dalam akuades dengan suhu kamar dan membentuk sedikit gel, sesuai dengan karakteristik natrium alginat yang larut dalam air hanya 0,3% (Viswanathan et al., 2014). Pada pemanasan 60-70℃ natrium alginat dapat terlarut sempurna (Jayanuddin, dkk., 2014).
Gambar 4.7 Grafik hubungan antara konsentrasi natrium alginat dan viskositas reduksi (𝝶red)
4.2.2 Hasil uji FTIR
Uji FTIR ini dilakukan untuk mengetahui gugus fungsi yang ada dalam natrium alginat. Natrium alginat hasil ekstraksi dikarakterisasi dengan instrumen FTIR dan dibandingkan dengan natrium alginat komersil dan campuran alginat ekstraksi-komersil. Data spektra FTIR natrium alginat ditunjukkan pada Tabel 4.1 Tabel 4.1 Data spektra FTIR natrium alginat
Jenis
bending 1031,95 1031,95 1030,02 1029,99
C-O-C
stretching 1091,75 1091,75 1093,67 1091,71
Na dalam isomer
alginat 1413,87 1415,80 1413,87 1415,75
Dari spektra FTIR yang di atas dapat diketahui bahwa FTIR natrium alginat ekstraksi relatif sama dengan natrium alginat komersil dan natrium alginat literatur karena nilai bilangan gelombang tidak ada perbedaan yang signifikan. Begitupula hasil bilangan gelombang campuran alginat ekstraksi dan komersil.
Gugus hidroksil/O-H stretching natrium alginat ekstraksi muncul pada bilangan gelombang 3446,91 cm-1, sedangkan pada natrium alginat komersil 3437,26 cm-1,
bilangan gelombang 3446,79 cm . Gugus karbonil (C=O) untuk natrium alginat ekstraksi terdapat pada bilangan gelombang 1629,90 cm-1, sedangkan pada
natrium alginat komersil 1616,40 cm-1, campuran natrium alginat ekstraksi dan
komersil 1612,54 cm-1 dan literatur 1614,42 cm-1. Senyawa lain yang terdapat
dalam natrium alginat adalah asam manuronat yang ditandai dengan O-H bending
pada panjang gelombang 1029,9 cm-1 dan asam guluronat yang ditandai dengan
C-O-C stretching pada panjang gelombang 1091,71 cm-1. Hal ini berdasarkan
penelitian Sakugawa (2004) dalam Pereira (2013), gugus O-H bending dan C-O-C
stretching berturut-turut terdapat pada panjang gelombang 1030 dan 1080 cm-1.
Pada natrium alginat hasil ekstraski dan komersil, gugus O-H bending dan C-O-C
stretching muncul pada panjang gelombang yang sama yaitu 1031,95 cm-1
dan1091,75 cm-1, sedangkan pada campuran natrium alginat ekstraksi dan
komersil yaitu 1030,02 dan 1093,67 cm-1 Menurut literatur, Natrium yang
berikatan dengan isomer alginat terdapat pada bilangan gelombang 1415,75 cm-1,
sedangkan pada hasil ekstraksi dan komersil terdapat pada 1413,87 cm-1 dan
1415,80 cm-1 dan campuran 1413,87 cm-1. Jadi, secara keseluruhan gugus fungsi
Gambar 4.8 Hasil spektra natrium alginat 4.3 Hasil Pembuatan Komposit Pati-Natrium Alginat
Komposit pati-natrium alginat sebagai drug delivery dibentuk dalam bentuk kapsul. Komposit dibuat dengan 5 variasi yaitu A, B, C, D, E dengan perbandingan pati : natrium alginat masing-masing 2 : 1; 3 : 2; 1 : 1; 1 : 2 dan 2 : 3. Selain itu juga ditambahkan crosslinker berupa STPP sebanyak 2% (b/v).
Crosslinker berfungsi untuk peningkatan kekuatan ikatan antara pati dan natrium alginat. Pelarut yang digunakan adalah akuades. Dalam proses pelarutan juga dilakukan pemanasan agar komposit homogen dengan cepat dan tidak ada gelembung udara yang terjebak. Pemanasan dilakukan pada rentang suhu optimal 70-80℃ untuk mendapatkan komposit dengan kekentalan yang tepat. Pemilihan
4000 3500 3000 2500 2000 1500 1000 500
%T
Bilangan Gelombang (cm-1)
Alginat Komersil Alginat Ekstraksi
suhu di atas suhu optimal menyebabkan kerusakan pada komposit karena terjadi degradasi polimer yang menyebabkan turunnya viskositas sehingga diperoleh hasil cetakan kapsul yang tipis (Jayanuddin, dkk., 2014).
4.4 Hasil Pencetakan Kapsul Pati-Alginat
Proses pencetakan kapsul diawali dengan persiapan berupa pemanasan
dipping bath menggunakan penangas air dan pengolesan dipping pen dengan pelumas makanan. Pemanasan ini berguna untuk penghilangan gelembung udara yang mungkin terjebak ketika proses pencetakan. Sedangkan pengolesan pelumas makanan berfungsi agar memudahkan pengambilan hasil cetakan kapsul setelah dikeringkan. Komposit yang telah homogen dicetak dengan cara dituang pada
dipping bath dan dibiarkan untuk beberapa saat sampai kekentalan tepat. Kemudian dipping pen dicelupkan pada dipping bath yang telah berisi komposit. Pencelupan dilakukan beberapa kali hingga didapatkan ketebalan kapsul yang tepat. Selanjutnya dikeringkan di udara bebas untuk mengurangi kadar air dalam kapsul. Setelah kering, kapsul dilepas dan dianalisis kinerjanya.
Tabel 4.2 Karakteristik kapsul pada masing-masing variasi Perbandingan
Komposisi Karakteristik Kapsul Gambar
A (2 : 1) tidak beraturan, plastis Lembek (++), bentuk (+)
B (3 : 2) Plastis (++), halus, kuat
C (1 : 1) Sedikit plastis, halus
D (2 : 3) Kaku, kuat, halus
E (1 : 2) Sangat kaku, kuat, bentuk tidak beraturan
bersifat plastis. Kapsul C memiliki tekstur lebih kuat dari kapsul B namun keplastisitasannya berkurang. Hal ini membuktikan bahwa semakin besar penambahan natrium alginat maka kapsul semakin kaku. Pada kapsul D, tekstur beraturan, kuat, sedikit plastis. Sedangkan pada kapsul E, kapsul sangat kaku, kuat namun tekstur tidak beraturan.
4.5 Hasil Karakterisasi Kapsul Pati-Alginat 4.5.1 Uji tarik
Membran komposit pati-alginat masing-masing variasi komposisi diuji mekanik berupa uji tarik menggunakan Autograph seperti pada Gambar 4.10.
Gambar 4.10Autograph
Pada uji tarik, membran dipotong dengan ukuran 6 x 1 cm sehingga diperoleh nilai gaya (kgF) dan pertambahan panjang yang diperoleh sampai sebelum putus (∆𝑙). Kemudian dilakukan analisis data untuk mendapatkan nilai
Gambar 4.11 Diagram antara variasi komposisi membran dengan nilai stress
Diagram nilai stress ditunjukkan pada Gambar 4.11. perbandingan di atas merupakan perbandingan pati : natrium alginat. Menurut diagram di atas, semakin banyak penambahan alginat maka menaikkan nilai stress. Tegangan atau stress ini menunjukan gaya maksimal yang dapat bekerja pada setiap satuan luas permukaan membran (Anis, 2016).Nilai stress mengalami kenaikan ketika cukup banyak natrium alginat yang ditambahkan, hal ini terjadi karena kandungan L-guluronat pada alginat yang berperan utama dalam proses pembentukan gel. Pembentukan gel sendiri terjadi karena adanya rantai panjang polimer alginat yang saling berikatan. Selain itu, sifat alginat yang sedikit larut dalam air sehingga strukturnya cukup stabil.
Nilai strain komposit A dan B cukup besar karena plastisitas yang disebabkan oleh pati cukup memberi pengaruh. Plastisitas pada membran membuat nilai pertambahan panjang semakin besar sehingga didapatkan hasil
Gambar 4.12 Diagram antara variasi komposisi membran dengan nilai strain
Setelah diperoleh nilai stress dan strain, diperoleh nilai Modulus Young.
Nilai Modulus Young menunjukkan ukuran kekakuan suatu material. Diagram
Modulus Young ditunjukkan oleh Gambar 4.13. Komposit dengan penambahan pati yang cukup banyak memiliki nilai Modulus Young yang kecil karena sifat plastisitasnya yang besar. Sedangkan penambahan alginat membuat komposit semakin kaku dan mengurangi sifat plastis. Komposit D (2:3) mencapai nilai optimum karena nilai stress dan strain yang saling mendukung, setelah mencapai optimum, Modulus Young mengalami penurunan.
0
Gambar 4.13 Diagram antara variasi komposit pati-alginat dengan nilai Modulus Young
4.5.2 Hasil uji swelling air
Uji swelling air bertujuan untuk mengetahui kemampuan kapsul untuk menyerap air. Diagram hasil uji swelling air ditunjukkan dalam Gambar 4.14.