C - 198
KARAKTERISASI ABU DASAR PLTU PAITON: PENGARUH PERLAKUAN MAGNET, HCl, DAN FUSI DENGAN NaOH
A.M. Faridah1, N. Widiastuti1,2, D. Prasetyoko1,2
1)
Laboratorium Riset Kimia Material dan Energi
2)
Laboratorium Energi, Pusat Studi Energi e-mail: arif10@mhs.chem.its.ac.id
Institut Teknologi Sepuluh Nopember (ITS), Surabaya, 6011
Abstrak-Logam berat limbah abu dasar sangat berbahaya bagi lingkungan. Abu dasar (BA) telah dimanfaatkan sebagai bahan konstruksi jalan, semen dan lainnya, tetapi jumlahnya masih melimpah. Komposisi utama abu dasar adalah silika (SiO2), alumina (Al2O3), besi (Fe), kalsium (Ca) dan karbon
(C). Pada penelitian ini ditunjukkan perubahan karakter Abu Dasar PLTU Paiton dengan penghilangan Fe dan Ca serta pemisahan SiO2 dan Al2O3 dengan C yang masih dipertahankan. Penghilangan Fe
menggunakan magnet, sedangkan Ca dengan asam klorida (HCl). Pemisahan SiO2 dan Al2O3 dilakukan
dengan mereaksikan abu dasar dengan natrium hidroksida (NaOH). Pada penelitian ini dilakukan variasi rasio NaOH/BA yaitu: 0,8; 1,0; 1,2 dan 1,4 dalam atmosfir nitrogen (N2) untuk mempertahankan C-nya.
Campuran NaOH/BA membentuk garam sehingga bisa mengikat SiO2 dan Al2O3. Pemisahan keduanya
dari Na dilakukan melalui pelarutan campuran dengan akuademin. Padatan dari setiap perlakuan dikarakterisasi menggunakan fourier transform infra red (FTIR), X-ray diffraction (XRD) dan X-ray fluorescence (XRF). Berdasarkan karakterisasi dengan FTIR dan XRD didapati bahwa puncak Fe fasa hematit (Fe2O3) dan Ca fasa kalsit (CaCO3) tidak ditemukan lagi. Hasil karakterisasi XRF menunjukkan
Fe2O3 berkurang dari 37,5 menjadi 10,6%, sedangkan CaO dari 19,0 menjadi 6,68%. Pada hasil
pemisahan SiO2 dan Al2O3 data FTIR menunjukkan adanya puncak SiO2 yang berarti sudah terpisahkan
dari abu dasar, sedangkan Al2O3 tidak terdeteksi.
Abstrack.Heavy metals in bottom ash is environmentally problem. Bottom ash (BA) has been used as road construction materials, cement and others. Nevertheless the basic amount of waste ash is still abundant. The main composition of bottom ash are silica (SiO2), alumina (Al2O3), iron (Fe), calcium (Ca)
and carbon (C). In the research have been shown the influence of Fe and Ca metal removal and separation of SiO2 and Al2O3 on the character of bottom ash PLTU Paiton with C which is still
maintained. Removal of Fe and Ca metal by magnet separation and hydrochloric acid (HCl) respectively. Both of them are separated by reacting with sodium hydroxide (NaOH). In this study, variations in the ratio of NaOH/BA are 0.8, 1.0, 1.2 and 1.4 in an atmosphere of nitrogen (N2) to maintain the carbon.
Mixturing of NaOH/BA formalize the salt, so that it can bind to SiO2 and Al2O3 from the bottom ash. The
separation of SiO2 and Al2O3 of Na through dissolution of the mixturing with aquademin. So that the
solids from each treatment were characterized using the fourier transform infra red (FTIR), X-ray diffraction (XRD) and X-ray fluorescence (XRF). Characterization with FTIR and XRD show that peaks of Fe as Fe2O3 and Ca as CaCO3 disappear again. XRF data show that Fe2O3 of bottom ash less from 37.5
to 10,6%, whereas CaO is from 19,0 to 6,68%. The result of SiO2 and Al2O3 separation show that FTIR
data that peak of SiO2 appear, it is mean that SiO2 have been extracted, but Al2O3 nodetection.
C - 199
PENDAHULUANAbu dasar (bottom ash/ BA) batubara PLTU Paiton dihasilkan sekitar 1-2 juta ton pertahun (Prijatama dan Sumarnadi, 1996). Hal itu sangat berbahaya karena dapat mencemari lingkungan. Abu Dasar PLTU Paiton memiliki komposisi kimia utama yaitu: silikon (Si) 24,10 % berat, aluminium (Al) 6,80 % berat, besi (Fe) 33,59 % berat, dan kalsium (Ca) 26,30 % berat (Yanti, 2009). Abu dasar telah banyak dimanfaatkan seperti: sebagai bahan dasar konstruksi jalan, produksi semen (Astrup et al., 2007) dan zeolit seperti zeolit A (Chareonpanich et al., 2011). Saat ini, pemanfaatan abu dasar paling menarik adalah dalam manajemen sampah dimana abu dasar sering digunakan sebagai pengisap (absorben) untuk beberapa polutan dalam air (Gupta et al., 2005; Gupta et al., 2006; Gupta et al., 2004; Mittal et al., 2005; Gupta et al., 2006; Mittal et al., 2006; Mittal et al., 2006; Mittal et al., 2006; Dincer et al., 2007; Mittal et al., 2007; Mittal et al., 2008; Mittal et al., 2008).
Berdasarkan beberapa penelitian di atas dilakukan penelitian tentang karakterisasi Abu Dasar PLTU Paiton melalui penghilangan Fe dan Ca menggunakan magnet dan HCl. Variasi konsentrasi NaOH pada reaksi fusi menjadi parameter utama pada penelitian ini sebagai variabel yang akan menunjukkan pengaruhnya terhadap karakter abu dasar PLTU Paiton.
METODE PENELITIAN Alat dan bahan
Bahan-bahan kimia yang digunakan dalam penelitian ini adalah: Abu Dasar PLTU Paiton, asam klorida (HCl), natrium hidroksida (NaOH), akuades dan akuademin. Peralatan yang digunakan dalam penelitian ini meliputi: peralatan gelas seperti labu takar, alat refluks, magnet, gelas pengaduk, gelas beker, pompa vakum, furnace tubular.
PROSEDUR
Penghilangan Logam Besi (Fe)
Abu dasar yang telah diayak pada ayakan berukuran 60 sampai 120 mesh
ditimbang sebanyak 25 g, kemudian dicampur dengan 1 L akuades lalu dimasukkan magnet seperator dan diaduk dengan stirer magnetik 300 rpm. Pemisahan Fe dilakukan selama 1 jam dengan 6 kali perlakuan. Abu dasar bebas Fe2O3 difiltrasi dan dikeringkan dalam oven
dengan temperatur 105 oC selama 24 jam. Abu dasar bebas Fe2O3 ditimbang sampai konstan
setelah diletakkan dalam desikator. Penghilangan Logam Ca dengan HCl
Abu dasar bebas Fe ditimbang sebanyak 10 g lalu dicampurkan dalam 300 mL HCl 12 M selama 4 jam. Filtrat hasil reaksi dengan HCl dianalisa menggunakan AAS dan residunya dianalisa dengan XRF.
Reaksi Fusi dengan NaOH
Abu dasar batubara dan NaOH yang sudah digerus dicampurkan dengan perbandingan massa tertentu ke dalam stainles steel krusibel hingga rata. Campuran dimasukkan furnace tubular untuk dilakukan reaksi fusi pada suhu 750 oC selama 1 jam. Jumlah perbandingan komposisi NaOH dan abu dasar dapat dilihat pada Tabel 1. Setelah peleburan campuran didinginkan, digerus dan dibuat suspensi dengan penambahan 127,5 mL air deionisasi campuran hasil peleburan diikuti oleh pengadukan dengan laju sekitar 200 rpm dan pemeraman (aging) selama 24 jam dalam botol polietilen pada suhu kamar. Selanjutnya campuran yang telah diperam tersebut disaring dan diambil ekstrak supernatannya sebagai larutan sumber Si dan Al. Kandungan Si dan Al terlarut pada ekstrak tersebut dianalisis dengan Inductively Coupled Plasma Optical Emission Spectrometer (ICP-OES). Residu hasil peleburan Si/Al dikarakterisasi dengan XRF.
Tabel 1. Perbandingan komposisi NaOH dan Abu dasar
Rasio NaOH/ Abu
Dasar (g)
NaOH (g) Abu Dasar (g)
0,8 12 15
1,0 15 15
1,2 18 15
C - 200
HASIL DAN PEMBAHASANPreparasi
Abu dasar dikarakterisasi dengan XRF dan XRD terlebih dahulu sebelum diperlakukan untuk mengetahui komposisi kimia yang terkandung. Adanya komposisi kimia akan mempengaruhi karakter abu dasar. Selain itu, karakterisasi dengan XRD dilakukan untuk mengetahui fasa amorf dan kristalinnya. Fasa amorf pada abu dasar akan mengekstrak Si/ Al lebih banyak dibanding fasa kristalin, karena fasa amorf lebih tidak stabil ikatan strukturnya dibanding fasa kristalin sehingga akan lebih mudah bereaksi atau lebih reaktif terhadap aktivasi alkali (Querol dkk., 1997). Komposisi kimia abu dasar dapat dilihat pada Tabel 2. Difragtogram XRD abu dasar dapat dilihat pada Gambar 1.
Komposisi kimia abu dasar yang paling besar dari Tabel 2 adalah hematit (Fe2O3) yaitu 37,5 % dan kalsiun oksida (CaO)
adalah, sedangkan silika (SiO2) dan alumina
(Al2O3) masing-masing adalah 31,80 dan
6,30% berat. Fe
2O3 dalam abu dasar akan
berpengaruh negatif terhadap pembentukan zeolit, karena menghambat proses kristalisasi dan menurunkan kristalinitas material yang dihasilkan (Voughan, 1999). Kandungan CaO juga berpengaruh terhadap pembentukan material, dimana konsentrasi kalsium yang tinggi dapat mengarahkan pada percepatan kecepatan reaksi (Hemming and Berry, 1988). Tabel 2. Komposisi abu dasar hasil analisis
XRF dalam prosen berat massa Logam Oksida Prosentase (%) Logam Oksida Prosentase (%) Al2O3 6,30 TiO2 1,26 SiO2 31,80 V2O5 0,06 P2O5 0,72 MnO 0,35 K2O 0,77 Fe2O3 37,5 CaO 19,00 CuO 0,06 Penghilangan Logam Fe
Logam Fe dalam abu dasar akan mengalami dekomposisi selama fusi (Voughan, 1999). Komposisi abu dasar setelah perlakuan dengan pemisahan magnetik dapat dilihat pada Tabel 3. Perbandingan antara abu
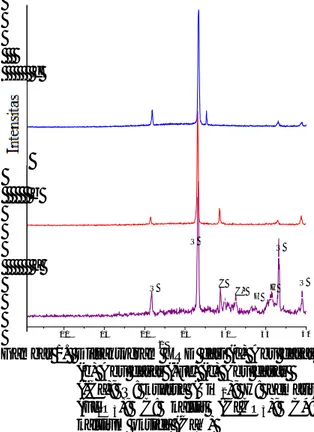
dasar awal dan setelah perlakuan dengan pemisahan magnetik ditunjukkan dengan pola difraksi sinar-X pada Gambar 1. Gambar 1 menunjukkan bahwa pemisahan magnetik menyebabkan perubahan intensitas puncak difraksi abu dasar terutama pada puncak kuarsa (SiO
2) 2θ= 26,64 o
, dimana abu dasar hasil pemisahan magnetik puncaknya lebih tinggi. Peningkatan intensitas puncak difraksi tersebut akibat abu dasar mengalami perubahan kandungan kimianya setelah pemisahan magnetik terutama akibat pengurangan kandungan besinya sehingga terjadi peningkatan kandungan kuarsanya. Perubahan ini sesuai dengan hasil pada Tabel 3, dimana hematit menurun dari 37,5 menjadi 20,90 % berat.
Tabel 3. Komposisi abu dasar setelah penghilangan Fe dalam fasa Fe2O3
dari hasil analisis XRF dalam prosen berat massa Logam Oksida Prosentase (%) Logam Oksida Prosentase (%) Al2O3 1,00 TiO2 1,20 SiO2 23,20 V2O5 0,04 P2O5 1,40 MnO 0,25 K2O 0,98 Fe2O3 20,90 CaO 24,70 CuO 0,21
Penghilangan Logam Kalsium (Ca)
Komposisi abu dasar setelah perlakuan dengan asam klorida (HCl) dapat dilihat pada Tabel 4. Perbandingan antara abu dasar awal dan setelah perlakuan dengan HCl ditunjukkan dengan pola difraksi sinar-X pada Gambar 1. Tabel 4. Komposisi abu dasar setelah
penghilangan logam Ca dalam fasa CaO dan CaCO3 dari hasil analisis
XRF dalam prosen berat massa Logam Oksida Prosentase (%) Logam Oksida Prosentase (%) Al2O3 1,00 TiO2 2,03 SiO2 68,30 V2O5 0,05 P2O5 3,30 MnO 0,12 K2O 1,40 Fe2O3 10,60 CaO 6,68 CuO 0,34
C - 201
Q H 10 15 20 25 30 35 40 2 Q Q Q H C*Gambar 1 menunjukkan bahwa reaksi dengan HCl menyebabkan berkurangnya puncak Ca dalam fasa kalsit (CaCO3). Selain itu pada
Gambar 1 juga ditunjukkan bahwa intensitas puncak difraksi abu dasar pada puncak kuarsa (SiO
2) 2θ = 26,64 o
semakin tinggi. Hal itu menunjukkan bahwa kadungan kalsit pada abu dasar semakin sedikit dan kandungan logam oksida lainnya dalam abu dasar pun semakin berkurang sehingga kuarsanya menjadi semakin terbebas dari logam oksida.
Perubahan kandungan kalsit dari abu dasar setelah pemisahan magnetik hingga reaksi dengan HCl sesuai dengan hasil pada Tabel 4 dimana kalsit berkurang dari meningkat dari 24,70 menjadi 6,68 % berat. Hubungan antara abu dasar pada setiap perlakuan dengan perubahan komposisi kimia dapat dilihat pada Gambar 2.
c
b
a
Gambar 1. Difraktogram XRD dari (a) Abu dasar (b) Abu dasar (-Fe) (c) Abu dasar (-Ca); Q: kuarsa (SiO2); H: hematit
(Fe2O3); C: kalsit (CaCO3); C*:
kalsium oksida (CaO)
Komposisi awal abu dasar yang utama adalah yang utama adalah mineral kuarsa (SiO2).
Gambar 1 menunjukkan bahwa tingkat kristalinitas kuarsa semakin meningkat dengan berkurangnya kandungan Fe2O3 dan CaCO3,
sebagaimana yang ditunjukkan oleh pola difraksi
pada 2θ= 20,86º; 26,64º; 36,54º; 39,47º (PDF 46-1045) untuk kuarsa (SiO2). Fasa lain yang
tampak yaitu hematit (Fe2O3) yang ditunjukkan
oleh pola difraksi pada 33,15º; 35,61º (PDF 33-0664) dan kalsit (CaCO3)dengan (PDF 05-0586)
pada 29,40º dan 31,42º, begitu pula korundum (Al2O3) muncul puncak walaupun intensitasnya
sangat rendah hanya sekitar 0,2-0,5 %. Hal itu didukung oleh data XRF yang menunjukkan kandungan korundum dalam abu dasar hanya 6,30 % berat. Selain mengandung fasa kristalin, abu dasar kering diperkirakan juga mengandung fasa amorf yang ditunjukkan oleh gundukan (hump) pada baseline difraktogram antara 20 hingga 40°. Berdasarkan data difraktogram tersebut, tampak bahwa abu dasar kering yang digunakan dalam penelitian ini mengandung fasa kristalin kuarsa, hematit dan kalsit.
0 10 20 30 40 50 60 70 80 AD AD (-Fe) AD (-Ca)
Perlakuan Abu Dasar
P ro se n ta se (% )
Preparasi Abu Dasar (AD)
SiO2 Al2O3 Fe2O3 CaO
Gambar 2. Hubungan antara setiap perlakuan abu dasar dengan perubahan komposisi kimia
Gambar 2 menunjukkan peningkatan prosentase silika pada setiap perlakuan, sedangkan logam oksida lainnya semakin menurun. Hal ini disebabkan karena kandungan logam oksida lain seperti hematit dan kalsit yang dapat mengganggu kestabilan silika semakin berkurang. Kandungan alumina dalam abu dasar sangat kecil sehingga pada proses pemisahan magnetik ikut terpisah dan mudah berekasi dengan HCl dan sehingga semakin berkurang.
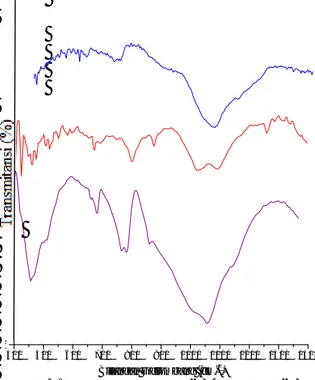
Hasil karakterisasi FTIR pada Gambar 3 juga menunjukkan bahwa abu dasar yang telah C
C - 202
diperlakukan dengan pemisahan magnetik dan reaksi dengan HCl menunjukkan puncak Si-O-Si pada bilangan gelombang 1080 dan 455 cm-1 semakin tinggi intensitasnya. Hal itu berarti bahwa adanya mineral kuarsa dalam abu dasr semakin murni. Data karakterisasi ini sesuai dengan yang disampaikan Davis et al.(1999); O’’zcan et al. (2005); Martins et al. (2007); Sprynsky et al. (2008) bahwa spektra paling kuat adalah pada bilangan gelombang 1065 cm−1 yang dikarenakan adanya vibrasi internal tetrahedron Si–O–Si dan Si–O–Al; pada pita 785 cm−1 direpresentasikan adanya vibrasi ikatan karbonat yang berarti terdapat kalsit atau kalsit dengan magnesium; Pita pada 455 cm−1 merupakan vibrasi ikatan Si–O–Si.Gambar 3. Spektra FTIR dari (a) Abu dasar (b) Abu dasar (-Fe) (c) Abu dasar (-Ca) Variasi rasio NaOH/ abu dasar
Reaksi fusi pada penelitian ini dilakukan dengan mencampurkam abu dasar batubara hasil perlakuan awal (reaksi dengan HCl) dengan NaOH sebagai aktivatornya. Alkali fusi ini dilakukan dengan memvariasikan komposisi campuran NaOH dan abu dasar (NaOH/BA) dengan perbandingan 0,8 ; 1,0 ; 1,2 ; 1,4. Parameter tetapnya adalah abu dasar dengan massa 15 g sedangkan NaOH mengikuti (lihat
Tabel 1). Natrium Hidroksida (NaOH) yang digunakan berfungsi sebagai mineralizer yang dapat meningkatkan proses pelarutan. Fenomena disebabkan karena kapasitas air murni sebagai pelarut seringkali tidak mampu melarutkan Si dan Al dalam proses pelarutan abu dasar pada temperatur tinggi.
Hasil yang didapatkan dari perlakuan alkali fusi adalah yang disebut massa fusi. Massa fusi yang diperoleh semakin meningkat dengan meningkatnya rasio NaOH/ BA. Fenomena ini diperkuat dengan hasil yang dilakukan sebelumnya, dimana ternyata dengan metode pemisahan magnetik hanya mampu mengurangi kandungan besi sekitar 16,6 % dari berat awal (lihat Tabel 3) dan Ca berkurang sampai perlakuan reaksi dengan HCl berkurang sekitar 18,20 % (lihat Tabel 4). Hubungan antara variasi rasio NaOH/ BA dan perubahan komposisi kimia pada residu hasil pelarutan reaksi fusi dapat dilihat pada Gambar 4.
0 10 20 30 40 50 60 0,8 1 1,2 1,4 Rasio NaOH P ro se n ta se (% )
Hasil Residu Reaksi Fusi dengan NaOH
SiO2 Al2O3 Fe2O3 CaO
Gambar 4. Hubungan antara variasi rasio NaOH/AD dengan perubahan komposisi kimia
Gambar 2 menunjukkan penurunan jumlah silika dan alumina dan penurunan hematit serta kalsit. Hal itu berarti bahwa semakin besar konsentrasi atau rasio NaOH/BA maka semakin banyak silika dan alumina yang terekstrak karena adanya kandungan Na sebagai garam yang terlarut dalam air. Perubahan tersebut diikuti dengan kenaikan prosentase hematit dan kalsit dikarenakan semakin banyak yang terdekomposisi dengan semakin besarnya rasio
400 500 600 700 800 900 1000 1100 1200 1300 1400
0.0
C - 203
QM C
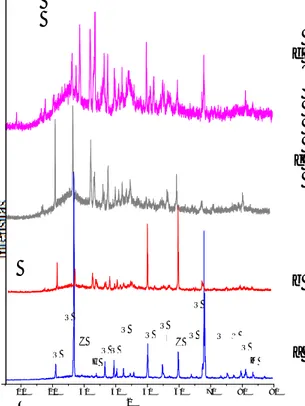
NaOH/ abu dasar. Hal itu diperkuat juga oleh data hasil XRD yang dapat dilihat pada Gambar 4.
d
c
b
a
Gambar 4. Difraktogram XRD dari variasi rasio NaOH/ BA (a) 0,8 (b) 1,0 (c) 1,2 (d) 1,4; Q: kuarsa (SiO2); M:
korundum (Al2O3); H: hematit
(Fe2O3); C: kalsit (CaCO3)
Kristalinitas kuarsa terjadi semakin tinggi dengan semakin kecilnya rasio NaOH/BA, sedangkan semakin meningkatnya rasio NaOH/BA menyebabkan material semakin amorf. Material yang amorf dikarenakan semakin tingginya kandungan logam lain seperti hematit dan kalsit, sehingga menjadikan material atau sampel semakin tidak stabil amorf. Sebagaimana yang disebutkan oleh Hemming dan Berry (1988) bahwa kandungan CaO dengan konsentrasi kalsium yang tinggi dapat mengarahkan pada percepatan kecepatan reaksi.
KESIMPULAN
1. Kandungan logam hematit dan kalsit semakin berkurang dengan perlakuan pemisahan magnetik dan reaksi HCl.
2. Kandungan kuarsa semakin meningkat dengan perlakuan pemisahan magnetik dan reaksi HCl.
3. Peningkatan rasio NaOH/AD menurunkan kandungan kuarsa pada residu hasil reaksi fusi.
4. Penurunan rasio NaOH/AD menurunkan kandungan mineral hematit dan kalsit pada residu hasil reaksi fusi
UCAPAN TERIMA KASIH
Penulis mengucapkan banyak terima kasih kepada komponen di Laboratorium Energi: XRD, XRF.
DAFTAR PUSTAKA
Dincer, A.R., Gunes, Y., and Karakaya, N., 2007, Coal-Based Bottom Ash (CBBA) Waste Waterial as Adsorbent for Removal of Textile Dye Stuffs from Aqueous Solution, J. Hazard. Mater. 141. p. 529–535.
Gupta, V.K., Mittal, A., Gajbe, V., 2005, Adsorption and Desorption Studies of Water Soluble Dye, Quinoline Yellow, using Waste Waterials, J. Colloid Interf. Sci. 284.p.89–98. Gupta, V.K., Mittal, A., Krishnan, L., and Mittal,
J., 2006, Adsorption Treatment and Recovery of the Hazardous Dye, Brilliant Blue FCF, over Bottom Ash and De-oiled Soya, J. Colloid Interf. Sci. 293. p.16–26. Gupta, V.K., Mittal, A., Krishnan, L., and Gajbe,
V., 2004, Adsorption Kinetics and Column Operations for the Removal and Recovery of Malachite Green from Wastewater using bottom ash, Sep. Purif. Technol. 40 (2004) 87–96.
Gupta, V.K., 2006, Removal and Recovery of the Hazardous Azo Dye Acid Orange 7 through Adsorption over Waste Materials: Bottom Ash and De-oiled Soya, Ind. Eng. Chem. Res. 45. p.1446–1453.
Hemmings, R. T. and Berry, E. E., 1988, On the Glass in Coal Fly Ashes: Recent Advances, in: Fly Ash and Coal Conversion By-Products : Characterization, Utilization, and Disposal, Materials Research Society, Mc Carthy, Massachusetts, Vol. IV, 3-38. Q Q Q Q Q Q M C Q Q 10 20 30 40 50 60 70 80 90 2 Q Q Q H
C - 204
Mittal, A., Kurup (Krishnan), L., and Gupta,V.K., 2005, Use of Wastematerials—Bottom Ash and De-oiled Soya, as Potential Adsorbents for the Removal of Amaranth from Aqueous Solutions, J. Hazard. Mater. 117. p.171–178.
Mittal, A., Mittal, J., and Kurup, L., 2006, Adsorption Isotherms, Kinetics and Column Operations for the Removal of Hazardous Dye, Tartrazine from Aqueous Solutions using Waste Materials—Bottom Ash and De-oiled Soya, as Adsorbents, J. Hazard. Mater. 136. p. 567–578.
Mittal, A., Mittal, J., Kurup, and Batch, L., 2006, Bulk Removal of Hazardous Dye, Indigo Carmine from Castewater through Adsorption, J. Hazard. Mater. 137. p.591– 602.
Mittal, A., Mittal, J., Kurup, L., and Singh, A.K., 2006, Process Development for the Removal and Recovery of Hazardous Dye Erythrosine from Wastewater by Waste Materials— Bottom Ash and De-oiled Soya as Adsorbents, J. Hazard. Mater. 138. p.95– 105.
Mittal, A., Malviya, A., Kaur, D., Mittal, J., and Kurup, L., 2007, Studies on the Adsorption Kinetics and Isotherms for the Removal and Recovery of Methyl Orange from Wastewaters using Waste Materials, J. Hazard. Mater. 148 . p. 229–240.
Mittal, A., Gajbe, V., and Mittal, J., 2008, Removal and Recovery of Hazardous Triphenylmethane Dye, Methyl Violet through Adsorption over Granulated Waste Materials, J. Hazard. Mater. 150. p.364– 375.
Mittal, A., Gupta, V.K., Malviya, A., and Mittal, J., 2008, Process Development for the Batch and Bulk Removal and Recovery of a Hazardous, Water-Soluble Azo Dye (Metanil Yellow) by Adsorption over Waste Materials (Bottom Ash and De-oiled Soya), J. Hazard. Mater. 151. 821–832.
Prijatama,H. dan Sumarnadi, E.T., 1996, Mengubah Limbah Menjadi Rupiah: Pemanfaatan Limbah Abu Batubara PLTU, Prosiding Pemaparan Hasil Litbang Ilmu Pengetahuan Teknik, Bandung.
Querol, X., Alastuey, A., López-Soler, A., Plana, F., Andrés, J.M., Juan, R., Ferrer, P. dan Ruiz, C.R., 1997, A Fast Method For Recycling Fly Ash: Microwave-Assisted Zeolite Synthesis. Environment Science and Technology, 31 (9), p. 2527–2533.
Vaughan, D., 1999. Crystal Engineering: The Design and Application of Functional Solid. Kluwer Academic Publishers, Netherlands, pp. 451–472.