UJI TOKSISITAS SUBKRONIS INFUSA DAUN SIRIH MERAH (Piper
crocatum Ruiz & Pav) PADA TIKUS : STUDI TERHADAP GAMBARAN
MIKROSKOPIS JANTUNG DAN KADAR SGOT DARAH
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Diajukan oleh:
Ignasius Kuncarli
NIM: 098114080
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
UJI TOKSISITAS SUBKRONIS INFUSA DAUN SIRIH MERAH (Piper
crocatum Ruiz & Pav) PADA TIKUS : STUDI TERHADAP GAMBARAN
MIKROSKOPIS JANTUNG DAN KADAR SGOT DARAH
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Diajukan oleh: Ignasius Kuncarli NIM: 098114080
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
ii
Persetujuan Pembimbing
UJI TOKSISITAS SUBKRONIS INFUSA DAUN SIRIH MERAH (Piper
crocatum Ruiz & Pav) PADA TIKUS : STUDI TERHADAP GAMBARAN
MIKROSKOPIS JANTUNG DAN KADAR SGOT DARAH
SKRIPSI
Yang diajukan oleh:
Ignasius Kuncarli
NIM: 098114080
telah disetujui oleh
Pembimbing Utama
vi
HALAMAN PERSEMBAHAN
Ketika semuanya padam, di mana harapan yang ada telah tiada,,,
Yakinlah, cahaya sekecil apapun dapat menjadi Harapan,,
Seperti Lilin kecil, yang selalu menerangi ketika tak ada cahaya,,
Semua hal yang kupunya, aku persembahkan kepada,,
Tuhan Yesus dan Bunda Maria, yang selalu bersamaku di segala moment
Bapak dan Ibuku, Nicolas Kun dan B. Esti Sumarni, serta adikku, (alm.) Mario E Kuntoro dan Sintia Putri Kunesta yang selalu memberikan yang terbaik
Semua saudara, teman, rekan yang memberikan pembelajaran tiap kali kita bertemu
vii
PRAKATA
Puji syukur penulis panjatkan kepada Tuhan Yang Maha Esa atas berkat dan rahmat-Nya, sehingga penulis dapat menyelesaikan skripsi yang berjudul “Uji Toksisitas Subkronis Infusa Daun Sirih Merah (Piper crocatum Ruiz & Pav) Merah Pada Tikus : Studi Terhadap Gambaran Mikroskopis Jantung Serta Kadar SGOT Darah”. Penyususnan skripsi ini sebagai salah satu syarat memperoleh gelar Sarjana Farmasi (S. Farm) Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
Penulis sangat menyadari bahwa laporan skripsi ini tidak akan terselesaikan tanpa bantuan dari berbagai pihak. Oleh karena itu, pada kesempatan ini perkenankan penulis mengucapkan terimakasih kepada :
1. Dekan Fakultas Farmasi Universitas Sanata Dharma, yang telah memimpin, menyelenggarakan, pendampingan dan tuntunan selama perkuliahan.
2. Prof. Dr. C. J. Soegihardjo, Apt., selaku Dosen Penguji skripsi yang telah
banyak memberi masukan dan saran kepada penulis.
3. Ibu Phebe Hendra, M.Si., Ph.D., Apt. selaku Dosen Penguji skripsi yang telah
banyak memberi masukan dan saran kepada penulis.
viii
5. Ibu Rini Dwiastuti, M.Si., Apt selaku Kepala Laboratorium Fakultas Farmasi yang telah memberikan izin dalam penggunaan semua fasilitas laboratorium untuk kepentingan penelitian skripsi ini.
6. Bapak Yohanes Dwiatmaka, M.Si., yang telah memberikan bantuan dalam
determinasi tanaman sirih merah (Piper crocatum Ruiz & Pav.) dan juga bersedia memberikan tanaman tersebut untuk digunakan dalam penelitian skripsi ini.
7. Bapak Heru, Bapak Parjiman, Bapak Kayat, Bapak Wagiran, selaku laboran Laboratorium Fakultas Farmasi yang telah banyak memberikan bantuan selama proses pelaksanaan penelitian.
8. Rekan satu kelompok sirih merah (Piper crocatum), Yuningsih Wulan Oei, Hertarinda, dan Thomas Catur Y atas kerjasama, saran dan motivasi dalam pengerjaan skripsi ini.
9. Sahabat-sahabatku, Reza Eka Putra, Yulio Nur Aji, Joseph Singgih, Felix
Pradana, Jati Panantya, Herman Gunawan, F. Eki Suprabawati, Rosalia Kony, Christine Herdyana, Nanda Chris Nurcahyanti, Theresia Garri, Veronika Dita Ayuningtyas, Apriliawati Galuh, Evy Veny Veronica, Lukas Surya atas kebersamaan, motivasi serta saran yang telah diberikan.
10. Kristin Yunita, yang telah memberikan waktu, saran, motivasi, dan
kebersamaan dalam pelaksanaan penelitian ini.
ix
12. Semua pihak yang terlibat baik langsung maupun tidak langsung yang namanya tidak dapat disebutkan satu persatu dalam penyusunan skripsi ini.
Penulis menyadari bahwa masih banyak terdapat kesalahan dalam penyusunan skripsi ini. Oleh karena itu, penulis mengharapkan kritik dan saran yang membangun demi hasil yang lebih baik. Penulis berharap semoga skripsi ini dapat bermanfaat bagi perkembangan ilmu pengetahuan khususnya di bidang farmasi, serta semua pihak, baik mahasiswa, lingkungan akademis, maupun masyarakat.
Yogyakarta, Juli 2013
x
DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
PERNYATAAN KEASLIAN KARYA ... iv
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH ... v
HALAMAN PERSEMBAHAN ... vi
PRAKATA ... vii
DAFTAR ISI ... x
DAFTAR TABEL ... xv
DAFTAR GAMBAR ... xvi
DAFTAR LAMPIRAN ... xviii
INTISARI ... xix
ABSTRACT ... xx
BAB I. PENGANTAR ... 1
A. Latar Belakang ... 1
1. Perumusan masalah ... 4
2. Keaslian penelitian ... 4
3. Manfaat penelitian ... 5
a. Manfaat teoretis ... 5
xi
B. Tujuan Penelitian ... 5
1. Tujuan umum ... 5
2. Tujuan khusus ... 6
BAB II. PENELAAHAN PUSTAKA... 7
A. Tanaman Sirih Merah (Piper crocatum Ruiz & Pav.) ... 7
1. Taksonomi dan morfologi daun sirih merah ... 7
2. Penggunaan tumbuhan ... 8
3. Kandungan kimia…… ... 9
a. Flavonoid ... 9
b. Tanin ... 9
c. Minyak atsiri ... 10
B. Infusa ... 10
1. Pengertian ... 10
2. Cara pembuatan ... 10
C. Toksikologi ... 11
1. Pengertian ... 11
2. Wujud dan sifat efek toksik ... 11
3. Uji toksisitas subkronis dan kronis ... 12
D. Jantung. ... 12
1. Anatomi jantung ... 12
2. Histologi jantung ... 13
xii
E. Aminotransferase ... 15
F. Keterangan Empiris ... 16
BAB III. METODE PENELITIAN... 17
A. Jenis dan Rancangan Penelitian ... 17
B. Variabel Penelitian ... 17
1. Variabel utama ... 17
a. Variabel bebas ... 17
b.Variabel tergantung ... 17
2. Variabel pengacau ... 17
a. Variabel pengacau terkendali ... 17
b. Variabel pengacau tidak terkendali ... 18
C. Definisi Operasional 1. Infusa daun sirih merah ... 18
2. Kriteria efek toksisitas ... 18
D. Bahan Penelitian ... 18
E. Alat dan Instrumen Penelitian ... 19
1. Alat pembuatan serbuk ... 19
2. Alat pembuatan infusa ... 19
3. Alat uji toksisitas ... 19
F. Tata Cara Penelitian ... 19
1. Determinasi tanaman ... 19
xiii
3. Pembuatan serbuk daun sirih merah ... 20
4. Penetapan kadar air serbuk daun sirih merah ... 20
5. Penetapan dosis infusa daun sirih merah ... 20
6. Penetapan dosis aquadest sebagai kontrol negative ... 21
7. Pembuatan infusa daun sirih merah ... 22
8. Penyiapan hewan uji ... 22
9. Pengelompokan hewan uji ... 22
10. Prosedur pelaksanaan toksisitas subkronis ... 23
11. Prosedur pembedahan ... 23
12. Histopatologi jantung ... 24
13. Pengamatan ... 24
a. Pengamatan berat badan hewan uji ... 24
b. Pengukuran asupan pakan hewan uji ... 25
c. Pengukuran asupan minum hewan uji ... 25
14. Analisis data ... 25
a. Pengukuran kadar SGOT darah... 25
b. Pengukuran berat badan tikus ... 26
c. Pengukuran asupan pakan dan minum tikus ... 26
d. Pembacaan preparat histopatologi jantung ... 27
BAB IV. HASIL DAN PEMBAHASAN ... 28
A. Determinasi Tanaman Sirih Merah ... 28
xiv
C. Kadar SGOT Darah Tikus Jantan Akibat Pemberian
Infusa Daun Sirih Merah ... 29
D. Kadar SGOT Darah Tikus Betina Akibat Pemberian Infusa Daun Sirih Merah ... 32
E. Perubahan Histopatologi Jantung Tikus Jantan dan Betina Akibat Pemberian Infusa Daun Sirih Merah ... 35
F. Perubahan Berat Badan Tikus Jantan dan Betina Akibat Pemberian Infusa Daun Sirih Merah ... 38
G. Asupan Minum Tikus Jantan dan Betina Akibat Pemberian Infusa Daun Sirih Merah ... 41
H. Asupan Pakan Tikus Jantan dan Betina Akibat Pemberian Infusa Daun Sirih Merah ... 43
BAB V. KESIMPULAN DAN SARAN ... 45
A. Kesimpulan ... 45
B. Saran ... 45
DAFTAR PUSTAKA ... 46
LAMPIRAN ... 49
xv
DAFTAR TABEL
Halaman Tabel I. Uji Paired T-test pada tikus jantan tiap kelompok
perlakuan serta nilai p kadar SGOT ... 30 Tabel II. Uji Paired T-test pada tikus betina tiap kelompok
perlakuan serta nilai p kadar SGOT ... 33 Tabel III. Hasil pembacaan preparat organ jantung pada tikus jantan ... 36 Tabel IV. Hasil pembacaan preparat organ jantung pada tikus betina ... 36 Tabel V. Purata berat badan ± SE tikus jantan akibat pemberian
infusa daun sirih merah ... 39 Tabel VI. Purata berat badan ± SE tikus betina akibat pemberian
xvi
DAFTAR GAMBAR
Halaman Gambar 1. Daun sirih merah. ... 8 Gambar 2. Histopatologi normal otot jantung, pengecatan hematoksilin
eosin, perbesaran 400x ... 14 Gambar 3. Gambaran mikroskopis otot jantung tikus Wistar setelah
diberi paparan arus listrik secara langsung, pengecatan
hematoksilin eosin, perbesaran 400x ... 14 Gambar 4. Diagram batang rata-rata pengaruh pemberian infusa daun
sirih merah terhadap kadar SGOT darah tikus jantan antar
kelompok perlakuan ... 31 Gambar 5. Diagram batang rata-rata pengaruh pemberian infusa daun
sirih merah terhadap kadar SGOT darah tikus betina antar
kelompok perlakuan ... 34
Gambar 6. Preparat organ jantung pada jantan dosis infusa daun sirih
merah 3.105 g/KgBB dengan perbesaran 400x ... 37 Gambar 7. Grafik perubahan berat badan tikus jantan selama
pemberian infusa daun sirih merah ... 39 Gambar 8. Grafik perubahan berat badan tikus betina selama
pemberian infusa daun sirih merah ... 40 Gambar 9. Grafik asupan minum tikus jantan akibat pemberian infusa
xvii
Gambar 10.Grafik asupan minum tikus betina akibat pemberian infusa
daun sirih merah ... 42 Gambar 11.Grafik asupan pakan tikus jantan akibat pemberian infusa
daun sirih merah ... 43 Gambar 12. Grafik asupan pakan tikus betina akibat pemberian infusa
xviii
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Foto daun sirih merah.. ... 50
Lampiran 2. Foto infusa daun sirih merah.. ... 50
Lampiran 3. Foto pembedahan tikus yang telah diberikan perlakuan ... 51
Lampiran 4. Foto organ tikus.. ... 51
Lampiran 5. Perhitungan penetapan peringkat dosis infusa daun sirih merah pada kelompok perlakuan. ... 52
Lampiran 6. Perhitungan rendemen serbuk daun sirih merah... 53
Lampiran 7. Perhitungan konversi dosis infusa daun sirih merah untuk manusia... 54
Lampiran 8. Perhitungan dosis aquadest sebagai kontrol negatif.. ... 55
Lampiran 9. Surat pengesahan determinasi tanaman sirih merah.. ... 56
Lampiran 10. Surat ethics committee approval... 57
Lampiran 11. Analisis statistik kadar SGOT darah pre dan post pada tikus jantan melalui uji Paired T-Test.. ... 58
Lampiran 12. Analisis statistik kadar SGOT darah post tikus jantan.. ... 59
Lampiran 13. Analisis statistik kadar SGOT darah pre dan post pada tikus betina melalui uji paired t-test.. ... 61
Lampiran 14. Analisis statistik kadar SGOT darah post tikus betina. ... 62
Lampiran 15. Analisis statistik berat badan tikus jantan... 65
Lampiran 16. Analisis statistik berat badan tikus betina... 66
xix
INTISARI
Sirih merah (Piper crocatum) adalah salah satu tanaman dimanfaatkan masyarakat sebagai obat tradisional. Untuk mengetahui tingkat keamanannya dikonsumsi jangka panjang, maka diuji toksisitas subkronis. Penelitian bertujuan mengetahui hubungan spektrum efek toksik infusa dengan perubahan kadar SGOT dan histopatologi jantung.
Penelitian bersifat eksperimental murni, rancangan penelitian acak lengkap pola searah. Sebanyak 40 tikus galur Wistar (20 jantan dan 20 betina), 2-3 bulan dibagi acak dalam 4 kelompok, yaitu kelompok kontrol aquadest dan kelompok perlakuan dosis 1,38 ; 2,07 ; 3,105 g/KgBB. Metodenya yaitu pengukuran kadar SGOT darah tikus secara subkronis dengan pemberian infusa sirih merah selama 28 hari, kekerapan pemberian sehari sekali. Sebelum perlakuan, pada hari pertama, SGOT darah diukur. Pada hari ke-28, setelah perlakuan, darah seluruh tikus diambil melalui sinus orbitalis untuk pengukuran kadar SGOT darah yang akan dianalisis dengan one way anova dan sebagian tikus dibedah guna melihat kerusakan pada jantung.
Hasil penelitian menunjukkan perubahan tidak bermakna, pada kadar SGOT dan berat badan ketika diberikan infusa daun sirih merah selama 28 hari. Pembacaan preparat organ jantung tikus tidak menunjukkan perubahan spesifik yang teramati setelah pemejanan.
Disimpulkan pemberian infusa daun sirih merah tidak berpengaruh terhadap kadar SGOT darah hewan uji dan juga tidak menimbulkan kerusakan yang berarti pada organ jantung.
xx
ABSTRACT
Red betel (Piper crocatum) is one of the plants used in traditional medicine. To determine the level of long-term security consumed, the subchronic toxicity test. The research aims to investigate the relationship spectrum of toxic effects of infusion with levels of SGOT and histopathological changes in the heart.
Research is purely experimental, randomized study design complete unidirectional pattern. A total of 40 Wistar rats (20 males and 20 females), 2-3 months were divided randomly into 4 groups: control group and the treatment group dose aquadest 1.38; 2.07; 3.105 g / KgBW. The method is the measurement of blood levels of SGOT subchronic rats by administration of red betel infusion for 28 days, the frequency of once-daily administration. Prior to treatment, on the first day, SGOT measured blood. On day 28, after the treatment, all the mice blood drawn through orbital sinus for measurement of blood levels of SGOT to be analyzed by one way ANOVA and partially dissected mice to see damage to the heart.
The results showed no significant changes, the levels of SGOT and body weight when given a red betel leaf infusion for 28 days. Reading of rat cardiac preparations showed no specific changes were observed after pemejanan.
The conclusion that administration of red betel leaf infusion has no effect on levels of SGOT blood test animals and also do not cause significant damage to heart.
1
BAB I PENGANTAR
A. Latar Belakang
Tanaman sirih merah (Piper crocatum) merupakan salah satu tanaman obat yang daunnya telah lama dikenal mempunyai khasiat obat untuk meyembuhkan berbagai penyakit. Efek farmakologis sirih merah sebagai antioksidan dan antibakteri merupakan potensi yang mungkin dapat digunakan untuk penyembuhan luka (Manoi, 2007). Kandungan kimia tanaman sirih merah belum diteliti secara detil. Menurut Werdhany, Marton, dan Setyorini (2008), daun sirih merah memiliki kandungan kimia antara lain : minyak atsiri, hidroksikavikol, kavikol, kavibetol, allylprokatekol, karvakrol, eugenol, p-cymene,
cineole, caryfelen, kadimen estragol, terpena, dan fenil propada. Selain itu, juga banyak mengandung senyawa fitokimia seperti alkaloid, saponin, tanin, dan flavonoid.
2
desinfektan dan antijamur, sangat baik jika digunakan sebagai obat kumur dan keputihan (Ningrum dan Murtie, 2013).
Beberapa penelitian tentang daun sirih merah sebagai obat telah dilakukan, yaitu sebagai imunomodulator, memiliki sifat sebagai anti inflamasi, anti fungi, anti diare, analgetik dan masih banyak lagi. Penelitian yang dilakukan oleh Salim (2006) pada rebusan sirih merah dengan dosis 20 g/KgBB memiliki efek antihiperglikemia dengan menurunkan kadar glukosa darah tikus diabetes galur Sprague-Dawley yang telah diinduksi aloksan tetrahedrat dari 17,76 % - 40,17 %. Minyak atsiri pada daun sirih merah berpengaruh terhadap penurunan berat badan dan berpotensi sebagai pelangsing aromaterapi (Utami, 2011).
Namun, belum ada penelitian guna mengetahui pengonsumsian daun sirih merah dalam jangka waktu yang lama. Sehingga diperlukan uji toksisitas. Tujuan uji toksisitas adalah untuk mengetahui spektrum efek toksik serta hubungan dosis dan toksisitas pada pemberian berulang dalam jangka waktu tertentu. Umumnya pengukuran toksisitas dapat dilakukan secara in vivo yang menggunakan hewan percobaan. Pada uji toksisitas akut yang dilakukan oleh Salim (2006), rebusan daun sirih merah tidak memiliki toksisitas hingga dosis 20 g/KgBB. Hingga saat ini, belum ada penelitian mengenai potensi ketoksikan sirih merah jika digunakan dalam jangka waktu yang lama.
sering digunakan dalam masyarakat dalam mengonsumsi obat tradisional. Selain itu, cara pembuatannya yang mudah sehingga masyarakat bisa melakukannya.
Secara umum, fungsi jantung adalah memompa darah dari jantung ke seluruh bagian tubuh dan menampungya kembali setelah dibersihkan oleh paru-paru. Jika terdapat penurunan fungsi jantung, misalnya terjadi infeksi otot jantung, dapat mempengaruhi kebutuhan oksigen serta nutrisi yang dibutuhkan seluruh tubuh (Herman, 2009).
Pada nekrosis otot jantung, protein intraseluler akan masuk dalam ruang interstitial dan masuk ke sirkulasi sistemik melalui mikrovaskuler lokal dan aliran limfatik. Profil kadar petanda biokimia terhadap waktu pengambilan di sirkulasi perifer bergantung pada berat molekulnya, lokasi dalam sel dan karakterisitik pelepasannya dan kecepatan aliran vaskuler atau limfatik dan klirens sistemik. Protein – protein intraseluler meliputi salah satunya aspartate aminotransferase (AST) atau serum glutamic oxaloacetic transaminase (SGOT) diperkenalkan sebagai salah satu petanda biokimia kerusakan otot jantung (Samsu, Sargowo, 2007).
mana penelitian ini adalah salah satu uji toksisitas subkronis infusa daun sirih merah.
1. Perumusan masalah
Berdasarkan uraian pada latar belakang, maka dapat dirumuskan berbagai permasalahan dalam penelitian ini, yaitu :
a. Seberapa besar efek toksik (perubahan biokimia dan struktural) infusa daun sirih merah terhadap kerusakan jantung yang dinilai dari perubahan kadar SGOT dan histopatologi jantung ?
b. Apakah terdapat hubungan kekerabatan antara dosis infusa daun sirih merah (Piper crocatum) dengan spektrum efek toksik pada kadar SGOT dan histopatologi jantung ?
2. Keaslian penelitian
Sepengetahuan penulis penelitian yang telah ada sebelumnya yaitu : a. Potensi Rebusan Daun Sirih Merah (Piper crocatum) Sebagai senyawa
Antihiperglikemia Pada Tikus Putih Galur Sprague-Dawley, menunjukkan bahwa tidak ada kematian pada tikus putih galur Sprague-Dawley yang diujikan untuk mengetahui toksisitas akut pada rendaman ekstrak etanol daun sirih merah dengan dosis 20 g/kg BB (Salim, 2006).
fagositosis makrofag peritoneal mencit yang diinduksi dengan bakteri Lysteria monocytogenes baik pada parameter indeks fagositosis, persen
fagositosis maupun efisiensi fagositosisnya (Hartini, Wahyuono, Widyarini, Yuswanto, 2013).
Sejauh penelusuran penulis mengenai penelitian dan jurnal di berbagai pustaka, belum ada penelitian mengenai toksisitas subkronis infusa sirih merah (Piper crocatum Ruiz & Pav.) terhadap histopatologi jantung dan SGOT darah tikus jantan dan betina.
3. Manfaat penelitian
a. Manfaat teoretis. Hasil penelitian ini diharapkan dapat menjadi awal bagi
perkembangan pengetahuan mengenai efek toksik daun sirih merah (Piper crocatum).
b. Manfaat praktis. Penelitian ini dapat memberikan informasi kepada masyarakat mengenai wujud efek toksik toksisitas subkronis infusa daun sirih merah (Piper crocatum) terhadap kadar SGOT darah dan histopatologi jantung.
B. Tujuan Penelitian 1. Tujuan umum
2. Tujuan khusus
a. Mengungkapkan perbedaan gambaran mikroskopis jantung dan kadar SGOT darah, tikus Wistar setelah pemberian infusa daun sirih merah (Piper crocatum) secara subkronik.
7
BAB II
PENELAAHAN PUSTAKA
A. Daun Sirih Merah (Piper crocatum Ruiz & Pav.) 1. Taksonomi dan morfologi daun sirih merah
Kingdom : Plantae (Tumbuhan)
Subkingdom : Tracheobionta (Tumbuhan berpembuluh) Super Divisi : Spermatophyta (Menghasilkan biji) Divisi : Magnoliophyta (Tumbuhan berbunga) Kelas : Magnoliopsida (berkeping dua / dikotil) Sub Kelas : Magnoliidae
Ordo : Piperales
Famili : Piperaceae (suku sirih-sirihan)
Genus : Piper
keunguan, panjang 2,1–6,2 cm, pangkal tangkai daun pada helaian daun agak ketengah sekitar 0,7–1 cm dari tepi daun bagian bawah. Karakter morfologi daun sirih merah dengan nama ilmiah P.crocatum adalah mempunyai bentuk daun yang cukup bervariasi antara daun muda (fase muda) dan daun pada cabang yang akan menghasilkan alat reproduksi (fase dewasa). Saat muda umumnya mempunyai bentuk daun menjantung – membulat telur dan pada fase dewasa (siap menghasilkan alat reproduksi) terjadi perubahan bentuk daun dari membulat telur – melonjong (Astuti, 2011). Gambar daun sirih merah dapat dilihat pada
gambar 1.
Gambar 1. Daun Sirih Merah (Plantamor, 2011).
2. Penggunaan tumbuhan
3. Kandungan kimia a. Flavonoid
Flavonoid merupakan golongan polifenol sehingga memili sifat kimia
senyawa fenol, yaitu bersifat agak asam sehingga dapat larut dalam basa. Karena memiliki sejumlah gugus hidroksil, flavonoid merupakan senyawa polar sehingga pada umumnya flavonoid larut dalam pelarut polar seperti etanol, metanol, butanol, aseton, air dan sebagainya. Menurut berbagai literature, flavonoid, sebagai derivate dari fenol, dapat menyebabkan rusaknya susunan dan perubahan mekanisme permeabilitas dari dinding sel bakteri sehingga dikatakan memiliki sifat antibakteri (Handayani, 2006). Flavonoid berfungsi sebagai pigmen pemberi warna pada bunga dan buah. Flavonoid berfungsi sebagai pigmen pemberi warna pada bunga dan buah (Mills, 2000).
b. Tanin
c. Minyak atsiri
Minyak atsiri disebut juga minyak eteris adalah minyak yang bersifat mudah menguap, yang terdiri dari campuran yang mudah menguap, dengan komposisi dan titik didih berbeda-beda. Setiap substansi yang dapat menguap memiliki titik didih dan tekanan uap tertentu dan dalam hal ini dipengaruhi oleh suhu. Pada umumnya tekanan uap yang rendah dimiliki oleh persenyawaan yang memiliki titik didih tinggi (Guenther, 2006).
B. Infusa 1. Pengertian
Infusa merupakan sediaan cair yang dibuat dengan mengekstraksi simplisia nabati dengan air pada suhu 90 derajat celcius selama 15 menit. Infus merupakan cara yang paling sederhana untuk membuat sediaan herbal dari bahan lunak seperti daun dan bunga (Direktorat Obat Asli Indonesia, 2010).
2. Cara pembuatan
C. Toksikologi 1. Pengertian
Menurut Doull dan Bruce semua senyawa adalah racun, tidak satupun yang bukan racun, takaran atau dosis yang tepatlah yang membedakan racun dan obat. Berdasarkan pernyataan tersebut maka dapat disimpulkan, toksikologi adalah ilmu yang mempelajari pengaruh kuantitatif zat kimia atas sistem biologi, dan yang paling terpenting bagaimana zat kimia tersebut berbahaya bagi sistem biologi (Donatus, 2005).
2. Wujud dan sifat efek toksik
Wujud efek toksik sesuatu racun dapat berupa perubahan biokimia, fungsional, dan struktural. Berbagai perubahan ini memiliki ciri yang khas, yakni terbalikkan atau tak terbalikkan. Jenis wujud perubahan biokimia tidak menunjukkan bukti secara langsung terhadap patologi organ, apabila mekanisme homeostatis normal makhluk hidup masih dapat bekerja maka perubahan biokimia bersifat timbal balik (Donatus, 2005).
3. Uji toksisitas subkronis dan kronis
Pemeriksaan toksisitas diperlukan untuk mengetahui berapa dosis yang dapat menyebabkan keracunan sehingga dapat diketahui jumlah penggunaan dosis yang tepat. Tingkat dosis yang dapat menyebabkan keracunan ditentukan dengan Letal Dosis 50 (LD50). LD50 adalah dosis dari suatu bahan yang menyebabkan 50% kematian dalam suatu populasi. Dengan melihat hubungan efektifitas dosis dalam bentuk rasio LD50, maka dapat diketahui batas keamanan pemakaian suatu zat atau obat. Semakin besar nilai indeks terapi suatu obat, maka semakin aman obat tersebut. Sebaliknya akan semakin berbahaya suatu obat jika indeks terapinya kecil (Depkes, 2000).
Percobaan ini termasuk uji toksisitas jangka panjang, mencakup pemberian obat secara berulang selama 1-3 bulan untuk percobaan sub kronis dan selama 3-6 bulan untuk percobaan kronis. Tujuan dari percobaan toksisitas jangka panjang ini adalah menguji keamanan obat dengan melalui serangkaian percobaan terhadap hewan. Pada percobaan toksisitas ini segala perubahan berupa akumulasi, toleransi, metabolisme dan kelainan khusus di organ atau sistem organ tertentu harus dipelajari. Dan pada waktu tertentu sebagian hewan harus dimatikan untuk mengetahui pengaruh bertahap obat terhadap organ (Lu, 1991).
D. Jantung 1. Anatomi jantung
seimbang). Fungsi utama jantung adalah mendorong darah agar dapat mengalir dengan lancer di dalam pembuluh pada sistem sirkulasi ke seluruh tubuh (Herman, 2009).
Secara anatomis, jantung merupakan organ yang mempunyai rongga di dalamnya. Rongga di dalam jantung ini terdiri dari empat ruangan, yaitu dua rongga ruang atrium di sebelah atas dan dua ruang ventrikel di sebelah bawah. Secara fungsional, jantung manusia terdiri atas dua bagian yang terpisah, yaitu bagian kanan dan kiri. Jantung bagian kanan dan kiri masing-masing terdiri pula atas dua ruang pompa yang berdenyut, yaitu atrium dan ventrikel. Jadi, secara fungsional, juga ada empat ruang pompa pada jantung, yaitu atrium kanan, ventrikel kanan, atrium kiri dan ventrikel kiri (Herman, 2009). Ventrikel mempunyai dinding yang lebih tebal dan jauh lebih kuat jika dibandingkan dengan atrium, khususnya ventrikel kiri yang harus memompakan darah keluar ke seluruh organ tubuh melalui sirkuit sistemik (Campbell, 2004).
2. Histologi jantung
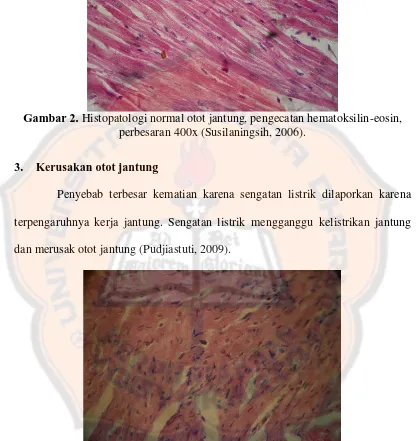
Gambar 2. Histopatologi normal otot jantung, pengecatan hematoksilin-eosin, perbesaran 400x (Susilaningsih, 2006).
3. Kerusakan otot jantung
Penyebab terbesar kematian karena sengatan listrik dilaporkan karena terpengaruhnya kerja jantung. Sengatan listrik mengganggu kelistrikan jantung dan merusak otot jantung (Pudjiastuti, 2009).
Gambar 3. Gambaran mikroskopis otot jantung tikus Wistar setelah diberi paparan arus listrik secara langsung, pengecatan hematoksilin-eosin, perbesaran
400x (Pudjiastuti,2009).
di lapisan superficial epikardium. Selain itu, terdapat berkas miokardium yang meregang diselingi miokardium yang hiperkontraksi (Pudjiastuti, 2009).
E. Aminotransferase
Serum aminotransferase merupakan enzim intraseluler yang dikeluarkan dari hepatosit yang luka dan sangat berguna sebagai penanda dari jaringan hati yang luka (inflamasi atau nekrosis sel). Serum aminotransferase terdiri dari 2 macam, yaitu :
1. Aspartate aminotransferase (AST, SGOT [serum glutamic oxaloacetic transaminase]), ditemukan di sitosol dan mitokondria. Terdapat di liver,
tulang otot, jantung, ginjal, otak dan pankreas.
2. Alanin aminotransferase (ALT, SGPT [serum glutamic pyruvic transaminase]), ditemukan di sitosol. Konsentrasi tertinggi terdapat di
liver (lebih sensitif dari AST untuk inflamasi liver dan hepatosit nekrosis)
(Friedman, Keeffe, 2011).
SGOT adalah enzim yang memiliki aktivitas metabolisme yang tinggi, ditemukan di jantung, hati, otot rangka, ginjal, otak, limfa, pankreas dan paru-paru. Penyakit yang menyebabkan perubahan, kerusakan atau kematian sel pada jaringan tersebut akan mengakibatkan terlepasnya enzim ini ke sirkulasi. Nilai normal kadar SGOT dalam tubuh manusia adalah 5-35 U/L (Direktur Pelayanan Kefarmasian, 2011).
dilepaskan oleh sel yang rusak atau mati karena umur yang sudah tua sehingga dapat ditemukan di dalam plasma darah. Bila kadar enzim di dalam darah meningkat menunjukkan peningkatan jumlah sel yang rusak atau mati, atau proliferasi sel (penambahan jumlah sel dalam jumlah banyak). Sel-sel tertentu memiliki enzim plasma dalam jumlah yang banyak dibandingkan dengan sel lainnya. SGOT atau Aspartat transaminase (AST) banyak terdapat di dalam sel jantung, sel hati (liver), otot rangka, ginjal, dan sel darah merah. Kadar normal SGOT atau AST normal pada laki-laki adalah 17 U/L sedangkan pada wanita 5-15 U/L. Kadar SGOT atau AST dalam darah meningkat 10-100 kali lipat dibandingkan dengan kadar normal bila terjadi infark jantung, hepatitis, nekrosis, terganggunya sirkulasi darah sehingga terjadi syok atau hipoksemia (Djojodibroto, 2003)
F. Keterangan Empiris
17
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Jenis penelitian ini adalah penelitian eksperimental murni dengan rancangan acak pola searah. Eksperimental murni adalah penelitian dengan cara mengendalikan variabel pengacau. Rancangan acak merupakan cara menetapkan sampel yang digunakan dalam penelitian dengan pengacakan agar setiap sampel memperoleh kesempatan yang sama untuk dapat masuk ke dalam kelompok perlakuan dan kelompok kontrol. Pola searah ditunjukkan dengan diberikannya perlakuan yang sama pada kelompok perlakuan, yaitu pemberian infusa daun sirih merah secara per oral dengan dosis yang berbeda.
B. Variabel Penelitian 1. Variabel utama
a. Variabel bebas : Dosis infusa daun sirih merah.
b. Variabel tergantung : Kadar SGOT serta hisotopatologi jantung setelah pemberian infusa daun sirih merah.
2. Variabel pengacau
b. Variabel pengacau tak terkendali : Kondisi patologis dan fisiologis hewan uji.
C. Definisi Operasional 1. Infusa
a. Infusa yang dianalisis merupakan ekstraksi simplisia daun sirih merah
(Piper crocatum) sejumlah 20 g dalam 100 mL pada suhu 900C dengan aquadest, selama 15 menit
b. Dosis infusa daun sirih merah yang diberikan pada kelompok perlakuan yaitu sejumlah mg serbuk daun sirih merah yang dibuat dalam bentuk infusa sebesar 1,38 ; 2,07 ; 3,105 g/KgBB.
2. Kriteria efek toksisitas subkronis meliputi histopatologi jantung dan kadar SGOT
a. Kadar SGOT darah adalah enzim yang memiliki aktivitas metabolisme
yang tinggi, ditemukan di jantung, hati, otot rangka, ginjal, otak, limfa, pankreas dan paru-paru.
b. Preparat jantung yang diamati adalah bagian sel dan jaringan dari organ
jantung tikus jantan dan betina dengan pengecatan hematoksilin dan eosin.
D. Bahan Penelitian
Bahan yang digunakan pada penelitian ini adalah empat puluh tikus putih galur Wistar di mana 20 jantan dan 20 betina berumur 2-3 bulan, berat badan 100 – 200 gram. Daun sirih merah diambil yang masih muda diperoleh dari Bapak
minum dan sebagai pelarut dalam pembuatan infusa. Pelet BR-2 untuk asupan pakan.
E. Alat dan Instrumen Penelitian Alat – alat yang digunakan dalam penelitian ini adalah
1. Alat-alat pembuatan serbuk kering daun sirih merah antara lain : mesin penyerbuk (blender), timbangan, oven.
2. Alat-alat pembuatan infusa daun sirih merah antara lain : bekker glass,
timbangan, batang pengaduk, gelas ukur, panci infusa, heater, stopwatch, kain flanel.
3. Alat-alat uji toksisitas antara lain : kandang tikus (metabolic cage), timbangan, bekker glass, jarum suntik per oral, spuit injeksi, Eppendorf, pipa kapiler (haematokrit).
F. Tata Cara Penelitian 1. Determinasi tanaman
Determinasi dilakukan di Laboratorium Farmakognosi Fitokimia Fakultas Farmasi Universitas Sanata Dharma Yogyakarta hingga ke tingkat spesies dan disahkan oleh Bapak Yohanes Dwiatmaka, M. Si.
2. Pengumpulan bahan uji
pucuk dan pangkal daun. Daun yang diperoleh berasal dari Pak Yohanes Dwiatmaka M.Si., pada bulan Maret 2013 di Bantul.
3. Pembuatan serbuk daun sirih merah
Daun sirih merah yang telah dipetik, dicuci, dikeringkan, kemudian dimasukkan ke dalam oven dengan suhu ± 50oC selama 24 jam. Daun yang telah kering kemudian diserbuk dan diayak dengan menggunakan ayakan no. 30, dan dilakukan perhitungan rendemen serbuk daun sirih merah.
Rendemen serbuk daun sirih merah dihitung dengan menggunakan
rumus : (Sharief, 2006).
4. Penetapan kadar air serbuk daun sirih merah
Penetapan kadar air menggunakan metode gravimetri dengan bantuan alat Moisture Balance. Dimasukkan ±5 g serbuk daun sirih merah ke dalam alat, kemudian diratakan. Timbang bobot zat sebagai bobot sebelum pemanasan (bobot a) panaskan pada suhu 1100C selama 30 menit. Setelah itu, ditimbang bobot zat setelah pemanasan (bobot b). Selisih bobot a dan bobot b merupakan kadar air yang diselidiki.
5. Penetapan dosis infusa daun sirih merah
70 Kg. Konversi manusia (70 kg ke tikus 200 g) = 0,018 (Laurence and Bacharach, 1964).
Dosis untuk 200g tikus = 0,018 x 23g = 0,414g/200g BB = 2,07x10-3g/g BB = 2,07 g/Kg BB
Dalam penelitian ini dibuat 3 peringkat dosis, dengan cara menggunakan kelipatannya. Angka kelipatan yang digunakan sebesar satu setengah kalinya, sehingga diperoleh tiga peringkat dosis yaitu 1,38 ; 2,07 ; 3,105 g/kgBB.
6. Penetapan dosis aquadest sebagai kontrol negatif
Untuk penentuan dosis aquadest digunakan dosis tertinggi untuk mengetahui jumlah volume maksimum yang diberikan kepada hewan uji. Dosis tertinggi 3,105 g/kgBB, berdasarkan rumus didapatkan volume maksimum, yaitu :
D x BB = C x V
3,105g/Kg BB x 200g = 20% x V V = 3,105 mL/200g BB
Maka dosis aquadest adalah : V = 0,015525 mL/g BB
7. Pembuatan infusa daun sirih merah
Sebanyak 20 g serbuk daun sirih merah direbus selama 15 menit dengan 100 mL aquadest, pada suhu 900C sambil sesekali diaduk. Setelah dingin, larutan disaring dengan kain flanel dan di tambahkan volumenya dengan aquadest hingga 100 mL. Konsentrasi infusa yang didapat adalah 20%. Pemilihan konsentrasi 20 % didasarkan pada tingkat serbuk yang bisa dibasahi oleh aquadest sebanyak 100 mL.
8. Penyiapan hewan uji
Hewan uji yang digunakan terdiri dari tikus jantan dan betina, galur Wistar, umur 2- 3 bulan, berat badan 100 – 200 g, berjumlah 40 ekor (20 jantan dan 20 betina) disiapkan dan ditempatkan dalam metabolic cage. Setiap metabolic cage berisi satu tikus. Tiga hari sebelum dilakukan perlakuan hewan uji
diadaptasikan pada metabolic cage.
9. Pengelompokan hewan uji
10. Prosedur pelaksanaan toksisitas subkronis
Sediaan uji berupa infusa daun sirih merah diberikan pada hewan uji sesuai dosis pemberian dengan kekerapan pemberian satu kali sehari selama 28 hari pada tikus jantan dan betina dengan tetap diberi makan dan minum. Pada awal masa uji yaitu pada hari I, darah semua tikus diambil melalui sinus orbital mata, ditampung pada Eppendorf berisi heparin untuk diambil serum darah kemudian dilakukan pengukuran kadar SGOT darah tikus. Pengukuran kadar SGOT darah dilakukan di Parahita Medical Lab. Pemberian infusa daun sirih merah dilakukan selama 28 hari pada setiap kelompok perlakuan sesuai dengan peringkat dosis. Pada hari ke-29 darah semua tikus diambil melalui vena orbital mata, ditampung pada Eppendorf berisi heparin untuk diambil serum darah kemudian dilakukan pengukuran kadar SGOT darah tikus. Pada hari ke-29 juga dilakukan pembedahan setengah dari hewan uji baik jantan maupun betina untuk dilakukam pemeriksaan histopatologi. Kemudian pada hari ke-42 (14 hari setelah 28) dilakukan pembedahan hewan uji yang tersisa untuk melihat reversibilitas.
11. Prosedur pembedahan
sampai bagian leher menggunakan gunting bedah. Kemudian, ambil dan pisahkan masing-masing organ menggunakan gunting bedah dengan bantuan pinset, pastikan tiap-tiap organ tidak tercampur, kemudian organ tersebut dicuci dengan NaCl 0,9% kemudian dimasukkan ke dalam pot organ yang sesuai antara label tikus yang dibedah dengan label yang ada di pot organ. Sisa organ tikus yang tidak terpakai dimasukkan ke dalam kantong plastik dan ditutup rapat agar tidak ada bau yang keluar, kemudian di kubur.
12. Histopatologi jantung
Organ jantung diambil dengan cara nekropsi setelah tikus mati. Selanjutnya pembuatan preparat histopatologi tersebut secara berurutan difiksasi di dalam larutan buffer netral formalin, trimming, dehidrasi, infiltrasi dengan parafin, diiris dengan mikrotom dan diwarnai dengan hematosilin-eosin (HE). Pewarnaan dilakukan dengan cara menginkubasi preparat otot dengan larutan
Mayer’s hematoxilyn selama 5 menit, kemudian diinkubasi dalam larutan eosin
0,5% yang sudah ditambah asam asetat (100 : 1).
13. Pengamatan
a. Pengamatan berat badan hewan uji
b. Pengukuran asupan pakan hewan uji
Hewan uji diberikan asupan pakan setiap hari sebanyak 20 g dan dilakukan penggantian pakan setiap harinya. Cara mengukur besarnya asupan pakan tikus yaitu dengan menimbang pakan yang diberikan pada hari pertama, kemudian pada hari kedua pakan yang masih tertinggal pada wadah ditimbang. Selisih penimbangan antara berat pakan hari kedua dengan berat badan hari pertama, dihitung sebagai asupan makanan yang dihabiskan pada hari pertama.
c. Pengukuran asupan minun hewan uji
Hewan uji diberikan minum berupa aquadest sebanyak 150 mL. Minuman diberikan dalam wadah botol kaca yang diberi pipa seperti tabung reaksi yang diberi lubang pada ujungnya. Pengukuran asupan minum hewan uji dilakukan dengan cara memasukkan 150 mL air pada wadah dihari pertama, kemudian pada hari kedua jumlah sisa air yang masih terdapat dalam botol dihitung. Air minum yang dihabiskan tikus pada hari pertama dihitung dengan mengurangkan jumlah air minum yang diberikan pada hari pertama dengan jumlah air minum sisa pada hari kedua.
14. Analisis data
a. Pengukuran kadar SGOT darah
Data kadar SGOT darah tikus dianalisis dengan uji Kolmogorov Smirnov untuk melihat distribusi data tiap kelompok. Apabila distribusi
Way ANOVA) dengan taraf kepercayaan 95% , kemudian dilanjutkan
dengan uji Scheffe untuk mengetahui perbedaan masing-masing kelompok jika nilai p < 0,05 (menunjukkan perbedaan bermakna). Apabila hasil analisis dengan uji Kolmogorov Smirnov data menunjukkan distribusi yang tidak normal maka analisis dilanjutkan dengan analisis non parametrik, yaitu Kruskal Walis untuk melihat perbedaan kadar SGOT darah antar kelompok, dilanjutkan dengan uji Mann Whitney untuk mengetahui perbedaan uji tiap kelompok. Untuk mengetahui ada tidaknya perbedaan bermakna sebelum dan sesudah perlakuan dilakukan uji paired-T test untuk tiap kelompok.
b. Pengukuran berat badan tikus
Pengukuran berat badan tikus sebagai data pendukung dalam penelitian ini. Pengukurannya dengan dihitung purata kenaikan berat badan pada hari ke 0, 7, 14, 21, dan pada hari ke 28. Data perubahan berat yang telah didapatkan, selanjutnya dianalisis dengan menggunakan General Linier Model dengan metode multivariate. Guna menentukan
jumlah purata tiap perlakuan, maka dilanjutkan dengan analyze compare means dengan metode means.
c. Pengukuran asupan pakan dan minum tikus
d. Pembacaan preparat histopatologi jantung
28
BAB IV
HASIL DAN PEMBAHASAN
Penelitian ini bertujuan untuk mengetahui ada tidaknya potensi efek toksik yang ditimbulkan infusa daun sirih merah. Penelitian ini secara khusus bertujuan untuk mengungkapkan spektrum efek toksik (perubahan biokimia dan struktural) infusa daun sirih merah terhadap perubahan histopatologi jantung, kadar SGOT serta mengetahui kekerabatan antara dosis dengan spektrum efek toksik.
A. Determinasi Tanaman Sirih Merah
Determinasi tanaman dilakukan untuk menentukan jenis tanaman apa yang peneliti gunakan dalam penelitian. Hal itu dikarenakan tanaman memiliki berbagai macam varietas. Determinasi dilakukan dengan mencocokkan tanaman pada hasil determinasi tanaman sirih merah yang telah dilakukan oleh Martinus Supriyadi Krisyanto.
Hasil determinasi menyimpulkan bahwa tanaman sirih merah yang digunakan dalam penelitian ini adalah benar tanaman sirih merah dengan nama ilmiah Piper crocatum Ruiz & Pav. yang telah disahkan oleh Bapak Yohanes Dwiatmaka, M.Si., dapat dilihat pada lampiran 9.
B. Serbuk dan Kadar Air Daun Sirih Merah
diserbuk dengan mesin penyerbuk Retsch bv, diayak dengan ayakan nomor 30. Tujuan dari pengayakan ini adalah untuk mendapatkan ukuran serbuk yang seragam. Dengan ukuran serbuk yang seragam, maka kemampuan difusi air dalam menarik senyawa daun sirih merah seragam juga. Dari penyerbukkan dan pengayakan tersebut didapatkan sejumlah 230,18 g serbuk daun sirih merah, lalu dilakukan perhitungan rendemen. Perhitungan rendemen dilakukan untuk mengetahui serbuk daun sirih merah yang diperoleh dari daun sirih merah basah. Rendemen yang didapatkan sebesar 23,018% b/b.
Selanjutnya serbuk diuji kadar airnya untuk memenuhi syarat serbuk yang baik, yaitu tidak lebih dari 10% (Menteri Kesehatan RI, 1994). Penetapan kadar air ini menggunakan metode gravimetri. Prinsip dari metode ini yaitu analisis kuantitatif berdasarkan berat tetapnya (berat konstan) (Sudjadi, 2010). Dari serbuk sirih merah yang dibuat diperoleh kadar air sebesar 9,48 %, dari hasil tersebut, serbuk yang dihasilkan telah memenuhi syarat Menteri Kesehatan.
C. Kadar SGOT Darah Tikus Jantan Akibat Pemberian Infusa Daun Sirih Merah
Terdapat empat kelompok perlakuan dalam penelitian ini, yaitu kelompok kontrol aquadest 15,525 g/KgBB sebagai kontrol pelarut dan kelompok perlakuan infusa daun sirih merah, dosis 1,38 ; 2,07 ; 3,105 g/KgBB. Penggunaan aquadest sebagai kelompok kontrol bertujuan untuk melihat pengaruh aquadest
sebagai pelarut infusa daun sirsih merah terhadap kadar SGOT darah pada pemberian secara subkronis.
Selama 28 hari, kadar SGOT darah pada tiap kelompok diukur ketika pre dan post pemberian infusa daun sirih merah. Selanjutnya, dianalisis dengan uji Paired T-test. Uji ini dilakukan karena karena subyek uji yang digunakan sama,
namun diberi perlakuan yang berbeda serta melihat signifikansi terdapat pengaruh pemberian infusa daun sirih merah yang bermakna pada pre dan post perlakuan di tiap kelompok perlakuan.
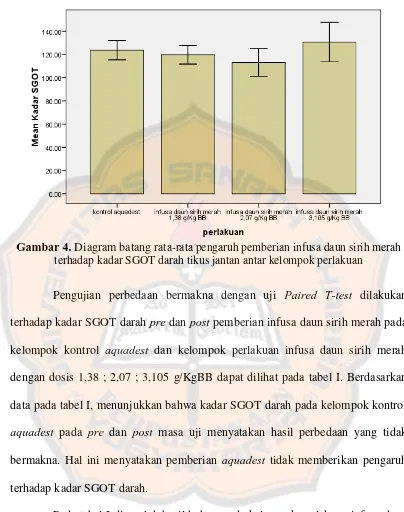
Gambar 4. Diagram batang rata-rata pengaruh pemberian infusa daun sirih merah terhadap kadar SGOT darah tikus jantan antar kelompok perlakuan
Pengujian perbedaan bermakna dengan uji Paired T-test dilakukan terhadap kadar SGOT darah pre dan post pemberian infusa daun sirih merah pada kelompok kontrol aquadest dan kelompok perlakuan infusa daun sirih merah dengan dosis 1,38 ; 2,07 ; 3,105 g/KgBB dapat dilihat pada tabel I. Berdasarkan data pada tabel I, menunjukkan bahwa kadar SGOT darah pada kelompok kontrol aquadest pada pre dan post masa uji menyatakan hasil perbedaan yang tidak
bermakna. Hal ini menyatakan pemberian aquadest tidak memberikan pengaruh terhadap kadar SGOT darah.
merah yang dibandingkan dengan kelompok kontrol aquadest juga menunjukkan perbedaan tidak bermakna.
Selanjutnya kadar SGOT darah post pemberian infusa daun sirih merah selama 28 hari dianalisis menggunakan varian satu arah (One Way Anova). Hal ini bertujuan guna melihat adakah pengaruh pemberian infusa daun sirih merah pada kelompok perlakuan infusa daun sirih merah yang dibandingkan terhadap kelompok perlakuan kontrol aquadest.
Hasil analisis varian satu arah terhadap kadar SGOT darah post pemberian infusa daun sirih merah diperoleh nilai probabilitas sebesar 0,767 (p>0,05). Hal ini menandakan perbedaan yang tidak bermakna antar kelompok perlakuan. Pada gambar 4 terdapat diagram batang yang menunjukkan bahwa tidak terdapat hubungan antara spektrum efek toksik dengan dosis infusa daun sirih merah.
Untuk lebih melihat spektrum efek toksik dengan lebih jelas dapat dilakukan uji subkronis infusa daun sirih merah terhadap tikus jantan dan betina dalam jangka waktu yang lebih panjang yaitu selama 90 hari.
D. Kadar SGOT Darah Tikus Betina Akibat Pemberian Infusa Daun Sirih Merah
diterapkan sama pada tikus betina. Pemeriksaan kadar SGOT darah tikus betina dilakukan sebelum (pre) dan setelah (post) 28 hari pemberian infusa daun sirih merah dan dianalisis dengan menggunakan uji Paired T-test. Uji ini dilakukan karena subjek uji yang digunakan sama namun memiliki perlakuan berbeda, bertujuan mengetahui pengaruh pemberian infusa daun sirih merah terhadap kadar SGOT darah tikus betina pada pre dan post perlakuan ditiap kelompok perlakuan.
Tabel II. Uji Paired T-test pada tikus betina tiap kelompok perlakuan serta nilai p kadar SGOT
Kelompok Perlakuan Kadar SGOT Darah (mg/dl) Nilai p Pre
(Rerata±SE) Post (Rerata±SE) I Kontrol aquadest
15,525 g/KgBB 138,18 ±12,79 92,14 ± 4,50 0,984 TB
II IDSM 1,38
g/KgBB 112,66 ± 3,87 108,00 ± 8,06 0,606 TB
III IDSM 2,07
g/KgBB 116,34 ± 6,48 101,44 ± 10,28 0,097 TB
IV IDSM 3,105
g/KgBB 122,73 ± 11,92 93,32 ± 3,57 0,442 TB
Ket. : TB = Berbeda tidak bermakna (nilai p>0,05) B = berbeda bermakna (nilai p<0,05)
Gambar 5. Diagram batang rata-rata pengaruh pemberian infusa daun sirih merah terhadap kadar SGOT darah tikus betina antar kelompok perlakuan
Selanjutnya kadar post SGOT darah diuji dengan analisis varian satu arah (One Way Anova). Hasil uji varian satu arah terhadap kadar SGOT darah setelah pemberian infusa daun sirih merah selama 28 hari mendapatkan nilai probabilitas sebesar 0,376 (p>0,05). Menunjukan bahwa terdapat perbedaan yang tidak bermakna antara kelompok kontrol aquadest dan kelompok perlakuan infusa daun sirih merah. Pada gambar 5 terdapat diagram batang yang menunjukkan hasil bahwa tidak adanya kekerabatan antara spektrum efek toksik dengan dosis.
Hal ini dapat dikarenakan adanya mekanisme untuk memelihara kadar SGOT darah untuk tetap dalam keadaan normal. Namun, untuk lebih melihat spektrum efek toksik dengan lebih jelas dapat dilakukan uji subkronis infusa daun sirih merah terhadap tikus jantan dan betina selama 90 hari.
E. Perubahan Histopatologi Jantung Tikus Jantan dan Betina Akibat Pemberian Infusa Daun Sirih Merah
Tujuan penelitian ini adalah untuk melihat spektrum efek toksik infusa daun sirih merah terhadap histopatologi jantung pada tikus jantan dan betina, maka dilakukan pemeriksaan terhadap histopatologi jantung tikus jantan dan betina untuk mengungkapkan spektrum efek toksik tersebut selama 28 hari, serta 14 hari setelah pemejanan guna melihat reversibilitas yang terjadi. Uji reversibilitas dilakukan untuk mengetahui keterbalikan efek toksik yang terjadi
Tabel III. Hasil pembacaan preparat organ jantung pada tikus jantan
Tidak ditemukan adanya perubahan spesifik yang teramati. Susunan sel dan jaringan tampak normal.
Tidak ditemukan adanya perubahan spesifik yang teramati. Susunan sel dan jaringan tampak normal.
IDSM 1,38 g/Kg BB
Tidak ditemukan adanya perubahan spesifik yang teramati. Susunan sel dan jaringan tampak normal.
Tidak ditemukan adanya perubahan spesifik yang teramati. Susunan sel dan jaringan tampak normal.
IDSM 2,07 g/Kg BB
Tidak ditemukan adanya perubahan spesifik yang teramati. Susunan sel dan jaringan tampak normal.
Tidak ditemukan adanya perubahan spesifik yang teramati. Susunan sel dan jaringan tampak normal.
IDSM 3,105 g/Kg BB
Tidak ditemukan adanya perubahan spesifik yang teramati. Susunan sel dan jaringan tampak normal.
Tidak ditemukan adanya perubahan spesifik yang teramati. Susunan sel dan jaringan tampak normal.
Keterangan :IDSM = Infusa Daun Sirih Merah
Tabel IV. Hasil pembacaan preparat organ jantung pada tikus betina
Kelompok
Tidak ditemukan adanya perubahan spesifik yang teramati. Susunan sel dan jaringan tampak normal.
Tidak ditemukan adanya perubahan spesifik yang teramati. Susunan sel dan jaringan tampak normal.
IDSM 1,38 g/Kg BB
Tidak ditemukan adanya perubahan spesifik yang teramati. Susunan sel dan jaringan tampak normal.
Tidak ditemukan adanya perubahan spesifik yang teramati. Susunan sel dan jaringan tampak normal.
IDSM 2,07 g/Kg BB
Tidak ditemukan adanya perubahan spesifik yang teramati. Susunan sel dan jaringan tampak normal.
Tidak ditemukan adanya perubahan spesifik yang teramati. Susunan sel dan jaringan tampak normal.
IDSM 3,105 g/Kg BB
Tidak ditemukan adanya perubahan spesifik yang teramati. Susunan sel dan jaringan tampak normal.
Tidak ditemukan adanya perubahan spesifik yang teramati. Susunan sel dan jaringan tampak normal.
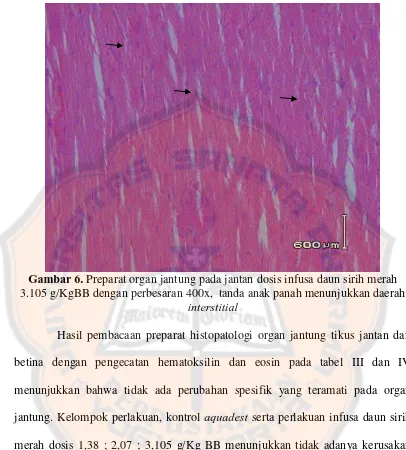
Gambar 6. Preparat organ jantung pada jantan dosis infusa daun sirih merah 3.105 g/KgBB dengan perbesaran 400x, tanda anak panah menunjukkan daerah
interstitial
lebih melihat spektrum efek toksik dengan lebih jelas dapat dilakukan uji subkronis infusa daun sirih merah terhadap tikus jantan dan betina selama 90 hari.
F. Perubahan Berat Badan Tikus Jantan dan Betina Akibat Pemberian Infusa Daun Sirih Merah
Tabel V. Purata berat badan ± SE tikus jantan akibat pemberian infusa daun sirih
Gambar 7. Grafik perubahan berat badan tikus jantan selama pemberian infusa daun sirih merah
Keterangan:
Tabel VI. Purata berat badan ± SE tikus betina akibat pemberian infusa daun
Keterangan : IDSM = Infusa daun sirih merah SE = Standar Error
Gambar 8. Grafik perubahan berat badan tikus betina selama pemberian infusa daun sirih merah
Keterangan:
Dosis 1 = kelompok pemberian infusa daun sirih merah 1.38 g/Kg BB Dosis 2 = kelompok pemberian infusa daun sirih merah 2,07 g/Kg BB Dosis 3 = kelompok pemberian infusa daun sirih merah 3,105 g/Kg BB Kontrol = kontrol aquadest 15,525 g/Kg BB
berat badan tikus yang tertinggi. Hasil analisis dengan uji General Linear Model (metode Multivariate) terhadap perubahan berat badan tikus jantan menunjukkan hasil yang berbeda bermakna antara kelompok perlakuan dan kontrol aquadest, sedangkan pada tikus betina menunjukkan hasil yang tidak berbeda bermakna antara kelompok perlakuan dan kontrol aquadest. Terjadinya perubahan berat badan dapat dikarenakan proses pertumbuhan yang dialami oleh tikus jantan maupun betina dan adanya pengaruh dari pemberian infusa daun sirih merah.
Gambar 7 menunjukkan grafik perubahan berat badan tikus dengan profil yang sama, artinya dengan pertambahan umur tikus jantan juga diikuti dengan pertambahan berat badan tikus jantan. Begitu juga grafik yang ditunjukkan pada gambar 8, grafik perubahan berat badan tikus betina dengan profil yang sama, hal ini menunjukkan bahwa tiap kelompok perlakuan terjadi peningkatan berat badan pada hari ke 28.
G. Asupan Minum Tikus Jantan Dan Betina Akibat Pemberian Infusa Daun Sirih Merah
Gambar 9. Grafik asupan minum tikus jantan akibat pemberian infusa daun sirih merah
Keterangan :
Dosis 1 = kelompok pemberian infusa daun sirih merah 1.38 g/Kg BB Dosis 2 = kelompok pemberian infusa daun sirih merah 2,07 g/Kg BB Dosis 3 = kelompok pemberian infusa daun sirih merah 3,105 g/Kg BB Kontrol = kontrol aquadest 15,525 g/Kg BB
Gambar 10. Grafik asupan minum tikus betina akibat pemberian infusa daun sirih merah
Keterangan :
Dosis 1 = kelompok pemberian infusa daun sirih merah 1.38 g/Kg BB Dosis 2 = kelompok pemberian infusa daun sirih merah 2,07 g/Kg BB Dosis 3 = kelompok pemberian infusa daun sirih merah 3,105 g/Kg BB Kontrol = kontrol aquadest 15,525 g/Kg BB
menunjukkan peningkatan dan penurunan, namun tidak menunjukkan hasil perbedaan yang bermakna.
H. Asupan Pakan Tikus Jantan Dan Betina Akibat Pemberian Infusa Daun Sirih Merah
Asupan pakan adalah salah satu data pendukung dalam uji toksisitas. Kita dapat memantau keadaan berat badan tikus melalui jumlah asupan pakan yang dikonsumsi oleh tikus.
Gambar 11. Grafik asupan pakan tikus jantan akibat pemberian infusa daun sirih merah
Keterangan :
Gambar 12. Grafik asupan pakan tikus betina akibat pemberian infusa daun sirih merah
Keterangan :
Dosis 1 = kelompok pemberian infusa daun sirih merah 1.38 g/Kg BB Dosis 2 = kelompok pemberian infusa daun sirih merah 2,07 g/Kg BB Dosis 3 = kelompok pemberian infusa daun sirih merah 3,105 g/Kg BB Kontrol = kontrol aquadest 15,525 g/Kg BB
Pada gambar 11, menunjukkan grafik pola makan tikus jantan normal, untuk semua kelompok perlakuan. Walau terdapat perbedaan pada kelompok perlakuan dosis 1.38 g/KgBB di mana pada awal percobaan terdapat adanya penurunan asupan pakan, tetapi tidak menunjukkan perbedaan yang berarti.
45
BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
1. Dalam penelitian ini, tidak didapatkan adanya spektrum toksik infusa daun
sirih merah selama 28 hari terhadap perubahan kadar SGOT darah di mana menunjukkan hasil perbedaan tidak bermakna serta perubahan pada gambaran histopatologi jantung yang tidak teramati perubahan yang spesifik.
2. Tidak terdapat hubungan antara dosis infusa daun sirih merah dengan spektrum efek toksik pada perubahan kadar SGOT darah dan histopatologi jantung.
B. Saran
1. Perlu dilakukan peningkatan pemberian infusa daun sirih merah dari 28 hari menjadi 90 hari guna mengetahui seberapa besar efek toksik yang ditimbulkan.
DAFTAR PUSTAKA
Ahadi, M.R., 2003, Kandungan Tanin Terkondensasi dan Laju Dekomposisi pada Serasah Daun Rhizospora mucronata lamk pada Ekosistem Tambak Tumpangsari, Purwakarta, Jawa Barat, Skripsi, Institut Pertanian Bogor, Bogor.
Astuti, 2011, KARAKTERISTIK MORFOLOGI DAUN SIRIH MERAH: Piper crocatum Ruitz & Pav dan Piper porphyrophyllum, Pusat Konservasi Tumbuhan Kebun Raya Bogor LIPI, Berk. Penel. Hayati Edisi Khusus: 7A (83–85).
Campbell, N.A., 2004. BIOLOGI Edisi Kelima Jilid 3. Jakarta ; Erlangga.
DepKes, 2000, Parameter Standar Umum Ekstrak Tumbuhan Obat, Direktorat Jenderal Pengawasan Obat Dan Makanan. Jakarta, pp. 88.
Direktorat Obat Asli Indonesia, 2010, Acuan Sediaan Herbal, volume kelima, Badan Pengawas Obat dan Makanan Republik Indonesia, Jakarta.
Direktur Pelayanan Kefarmasian, 2011, Pedoman Interpretasi Data Klinik, Departemen Kesehatan RI, Jakarta, pp.59.
Djojodibroto, R.D., 2003, Seluk Beluk Pemeriksaan Kesehatan (General Medical Check Up), Pustaka Populer Obor, Jakarta, pp. 59-60.
Donatus, I.A., 2005, Toksikologi Dasar, Universitas Gadjah Mada, Yogyakarta, pp.1, 187, 145- 164, 193-194.
Friedman, L.S., Keeffe, E.B., 2011, Handbook of Liver Disease, ed.3th, Elsevier Health Sciences, Indiana University, p.3-4.
Guenther, E.et al., Penerjemah: S. Ketaren, 2006, Minyak Atsiri, Jilid 1, Penerbit Universitas Indonesia, UI Press Jakarta.
Handayani, T., 2006, Pengaruh Daya Anti Bakteri Ekstrak Daun Teh Segar (Camelia sinensis) terhadap Streptococcus alpha, Jurnal Persatuan Dokter Gigi Indonesia Agustus 2006 : pp. 50.
Hartini, Y.S., Wahyuono, S., Widyarini, S., Yuswanto, Ag., 2013, Uji Aktivitas Fagositosis Makrofag Senyawa Kode Pc-2 dari Daun Sirih Merah (Piper crocatum Ruiz & Pav.) Secara In-vivo, Seminar Nasional Tumbuhan Obat Indonesia ke-44, Stifi Bhakti Pertiwi Palembang, Palembang.
Kondo, M., K. Kita, & H. Yokata, 2006, Evaluation of fermentation characteristics and nutrive value of green tea waste ensiled with by – product mixture for ruminants. Asain – Aust. J. Anim., Sci. 19 : 533-540. Laurence, J., Bacharach, M., 1964, Analytical Toxicology, CRC Press,
Philadelphia.
Lu, F.C., 1991, Toksikologi Dasar Asas, Organ Sasaran dan Penilaian Risiko, diterjemahkan oleh Nugroho,E., Edisi kedua. UI Press, Jakarta.
Manoi, F. 2007. Sirih merah sebagai tanaman obat multifungsi.
http://litbang.deptan.go.id, diakses tanggal 5 November 2012.
Menteri Kesehatan RI, 1994, Persyaratan Obat Tradisional, Menteri Kesehatan Republik Indonesia, Jakarta.
Mills, S., 2000, Principles and Pratice of Phytotherapy Modern Herbal Medicine, London : Churchill Livingstone, pp. 31-32.
Ningrum, K. E., & Murtie, M., 2013, Tumbuhan Sakti Basmi Berbagai Penyakit, Penerbit Dunia Sehat, Jakarta Timur, pp. 4.
Plantamor, 2011, Sirih Merah Piper crocatum Ruiz & rav,
http://www.plantamor.com/index .php?plant=2092, diakses tanggal 5 November 2012.
Pudjiastuti, A., 2009, Perbedaan Kerusakan Otot Jantung Tikus Wistar Akibat Paparan Arus Listrik Secara Langsung Dan Melalui Media Air, Laporan Penelitian, Fakultas Kedokteran Universitas Diponegoro, Semarang.
Salim, A., 2006, Potensi Rebusan Daun Sirih Merah (Piper crocatum) Sebagai Senyawa Antihiperglikemia Pada Tikus Putih Galur Sprague-Dawley, Skripsi,11, Institut Pertanian Bogor, Bogor.
Samsu, N., Sargowo, D., 2007, Sensitivitas dan Spesifisitas Troponin T dan I pada Diagnosis Infark Miokard Akut, Majalah Kedokteran Indonesia, Vol. 57, 365.
Sharief, D.A., 2006, Optimasi Proses Ekstraksi dan Pengeringan Semprot Pada Teh Hijau Instan, Institut Pertanian Bogor, Bogor.
Sudewo, B., 2005, Basmi Penyakit dengan Sirih Merah, AgroMedia, Jakarta, pp. 35-38.
Susilaningsih, N., CD Praktikum Histologi 1, Bagian Histologi, Fakultas Kedokteran, Universitas Diponegoro; 2006.
Utami, M.R., 2011, Fraksinasi Senyawa Aktif Minyak Atsiri Daun Sirih Merah (Piper Cf. Fragile. Benth) Sebagai Pelangsing Aromaterapi Secara In Vivo, Tesis, 28, Institut Pertanian Bogor, Bogor.
LAMPIRAN
Lampiran 1. Foto daun sirih merah
Lampiran 3. Foto pembedahan tikus yang telah diberikan perlakuan
Lampiran 5. Perhitungan penetapan peringkat dosis infusa daun sirih merah pada kelompok perlakuan
Dosis terapi infusa daun sirih merah adalah 23 g/70Kg BB untuk manusia 70 Kg. Konversi manusia (70 kg ke tikus 200 g) = 0,018 (Laurence and Bacharach, 1964).
Dosis untuk 200g tikus = 0,018 x 23g = 0,414g/200g BB = 2,07x10-3g/g BB = 2,07 g/Kg BB
Lampiran 6. Perhitungan rendemen serbuk daun sirih merah
Dari 1Kg daun sirih merah basah didapatkan 230,18g daun sirih merah kering. Maka, diperoleh rendemen sebesar :
Untuk perhitungan kadar air menggunakan metode gravimetric, maka
digunakan rumus :
Replikasi I Replikasi II Replikasi III
Bobot awal (g) 5,000 5,001 5,027
Bobot akhir (g) 4,467 4,542 4,594
Kadar air (%) 10,66 9,18 8,61
Lampiran 7. Perhitungan konversi dosis infusa daun sirih merah untuk manusia
Angka konversi Tikus 200 g ke manusia 70 kg = 56,0
Dosis untuk manusia = Dosis untuk tikus 200 g x (angka konversi ke manusia)
Dengan dasar tersebut maka ditetapkan dosis infusa daun sirsak untuk manusia : 1. Infusa daun sirih merah 1,38 g/Kg BB
0,00138 g/g x 200 g = 0,276/ 200g BB
0,276 g/ 200gBB x 56,0 = 15,456 g/ 70 kgBB manusia 2. Infusa daun sirih merah 2,07 g/Kg BB
0,00207 g/g x 200 g = 0,414/ 200g BB
0,414 g/ 200gBB x 56,0 = 23,184g/ 70 kgBB manusia 3. Infusa daun sirih merah 3,105 g/Kg BB
0,003105g/g x 200 g = 0,621/ 200g BB
Lampiran 8. Perhitungan dosis aquadest sebagai kontrol negatif Untuk penentuan dosis aquadest digunakan dosis tertinggi untuk mengetahui jumlah volume maksimum yang diberikan kepada hewan uji. Dosis tertinggi 3,105 g/kgBB, berdasarkan rumus didapatkan volume maksimum yaitu :
D x BB = C x V 3,105g/Kg BB x 200g = 20% x V
V = 3,105 ml/200g BB Maka dosis aquadest adalah : V = 0,015525 ml/g BB
Lampiran 11. Analisis statistik kadar SGOT darah pre dan post pada tikus jantan melalui uji Paired T-Test
Lampiran 12. Analisis statistik kadar SGOT darah post pada tikus jantan
Normal Parametersa Mean 121.7850 Std. Deviation 25.24673 Most Extreme Differences Absolute .141 Positive .141 Negative -.103 Kolmogorov-Smirnov Z .629 Asymp. Sig. (2-tailed) .824
a. Test distribution is Normal.
Oneway Lower Bound Upper Bound
kontrol aquadest 5 1.2364E2 18.60196 8.31905 100.5426 146.7374 96.00 140.60
ANOVA
Kadar SGOT
Sum of Squares df Mean Square F Sig.
Between Groups 809.090 3 269.697 .382 .767
Within Groups 11301.456 16 706.341
Total 12110.546 19
Lampiran 14. Analisis Statistik Kadar SGOT Darah Post Tikus Betina
Normal Parametersa Mean 98.7250
Std. Deviation 15.94972
Most Extreme Differences Absolute .186
Positive .186
Negative -.089
Kolmogorov-Smirnov Z .830
Asymp. Sig. (2-tailed) .496
a. Test distribution is Normal.
Descriptives
ANOVA
Kadar SGOT
Sum of Squares df Mean Square F Sig.
Between Groups 829.865 3 276.622 1.105 .376
Within Groups 4003.612 16 250.226
Total 4833.477 19
Lampiran 15. Analisis Statistik Berat Badan Tikus Jantan
Case Processing Summary
Cases
Included Excluded Total
N Percent N Percent N Percent Kontrol aquadest Mean 1.4221E2 1.6015E2 1.7749E2 1.8850E2 2.0353E2
Std. Error of
Mean 6.40218 4.24547 3.10294 3.84503 3.45677 Infusa daun sirih
merah 1,38 g/kgBB
Mean 1.4907E2 1.5735E2 1.7376E2 1.9429E2 2.0911E2 Std. Error of
Mean 1.96608 2.96596 5.46459 7.00195 7.46729 Infusa daun sirih
merah 2,07 g/kgBB
Mean 1.2705E2 1.4236E2 1.6475E2 1.8284E2 1.9568E2 Std. Error of
Mean 8.37097 3.06958 4.53803 6.68441 8.10240 Infusa daun sirih
merah 3,105 g/kgBB
Mean 1.1651E2 1.3013E2 1.4778E2 1.6346E2 1.7783E2 Std. Error of
Mean 4.84507 5.61920 5.74856 6.77363 6.56475 Total Mean 1.3371E2 1.4750E2 1.6595E2 1.8227E2 1.9654E2
Std. Error of
Between-Subjects Factors
Value Label N
kelompok_perlakuan 1 Kontrol
aquadest 5
b. The statistic is an upper bound on F that yields a lower bound on the significance level.