BAB II
TINJAUAN PUSTAKA
2.1 Diabetes Melitus
DM merupakan suatu kelompok penyakit metabolik dengan karakteristik hiperglikemia yang terjadi karena kelainan sekresi insulin, kerja insulin atau kedua-duanya.1
2.1.1 Klasifikasi DM1
1. Tipe 1: Destruksi sel beta, umumnya menjurus ke defisiensi insulin absolut.
- Autoimun - Idiopatik
2.Tipe 2: Bervariasi, mulai yang dominan resistensi insulin disertai defisiensi insulin relatif sampai yangdominan defek sekresi insulin disertai resisten insulin.
3.Tipe lain: Defek genetik fungsi sel beta, defek genetik kerja insulin, penyakit eksokrinpankreas, endokrinopati, karena obat atau zat kimia, infeksi, sebab imunologi yang jarang, sindromgenetik lain yang berkaitan dengan DM.
4.Diabetes mellitus Gestasional. 2.1.2 Diagnosis1
Diagnosis DM ditegakkan atas dasar pemeriksaan kadar glukosa darah.Pemeriksaan glukosa darah yang dianjurkan adalah pemeriksaan glukosa
secara enzimatik dengan bahan plasma darah vena. Pemantauan hasil pengobatan dapat dilakukan dengan menggunakan pemeriksaan glukosa darah kapiler dengan
glukometer. Diagnosis tidak dapat ditegakkan atas dasar adanya glukosuria. Berbagai keluhan dapat ditemukan pada penyandang DM. Kecurigaan adanya DM perlu dipikirkan apabila terdapat keluhan seperti:
- Keluhan klasik DM : poliuria, polidipsia, polifagia, dan penurunan berat
- Keluhan lain: lemah badan, kesemutan, gatal, mata kabur, dan disfungsi ereksi pada pria, serta pruritus vulva pada wanita.
Kriteria Diagnosis DM
- Pemeriksaan glukosa plasma puasa ≥126 mg/dl. Puasa adalah kondisi
tidak ada asupan kalori minimal 8 jam
- Pemeriksaan glukosa plasma ≥200 mg/dl 2 jam setelah Tes Toleransi
Glukosa Oral (TTGO) dengan beban glukosa 75 gram.
- Pemeriksaan glukosa plasma sewaktu ≥200 mg/dl dengan keluhan klasik.
- Pemeriksaan HbA1c ≥6,5% dengan menggunakan metode yang
terstandararisasi oleh National Glycohaemoglobin Standarization Program (NGSP)
2.1.3 Penatalaksanaan DM1
Tujuan penatalaksaan secara umum adalah meningkatkan kualitas hidup penyandang diabetes.
Tujuan penatalaksanaan :
- Tujuan Jangka pendek : menghilangkan keluhanDM, memperbaiki
kualitas hidup dan mengurangi risiko komplikasi akut
- Tujuan Jangka panjang : mencegah dan menghambat progresivitas
penyulit mikroangiopati dan makroangiopati
- Tujuan akhir pengelolaan adalah turunnya morbiditas dan mortalitas DM.
Untuk mencapai tujuan tersebut perlu dilakukan pengendalian glukosadarah, tekanan darah, berat badan, dan profil lipid melalui pengelolaan pasien secara komprehensif
Ada 4 pilar penatalaksaan DM : 1. Edukasi
2.1.4 Metformin1
Terapi farmakologis pada penderita DM diberikan bersamaan dengan pengaturan makan dan latihan jasmani (gaya hidup sehat). Terapi farmakologis terdiri dari obat oral dan bentuk suntikan.
Metforminmempunyai efek utama mengurangi produksi glukosa hati (glukoneogenesis) dan memperbaiki ambilan glukosa dijaringan perifer.
Metformin merupakan pilihan pertama pada sebagian besar kasus DM Tipe2. Dosis metformin diturunkan pada pasien dengan gangguan fungsi ginjal (GFR 30-60 ml/menit/1,75m2). Metformin tidak boleh diberikan pada beberapa keadaan seperti: GFR<30 ml/menit/1,73 m2, adanya gangguan hati berat, serta pasien-pasien dengan kecenderungan hipoksemia (misalnya penyakit serebrovaskular, sepsis, renjatan, PPOK, gagal jantung (NYHA FC III-IV). Efek samping yang mungkin berupa gangguan saluran pencernaan seperti halnya gejala dispepsia.
2.1.5 Patogenesis DM Tipe 2
Glucolipotoxicity dapat dinyatakan sebagai suatu penentu yang utama
penyebab DM Tipe 2. Secara umum, Glucolipotoxicity merupakan kombinasi dari
glucotoxicity dan lipotoxicity yang mana kedua hal tersebut terjadi secara
bersamaan.15
Glucotoxicity merupakan peningkatan kadar gula darah secara konstan
(hiperglikemi) yang menyebabkan dampak kerusakan dari fungsi sel β dan
nantinya akan menurunkan sekresi insulin. Sama halnya dengan sejumlah lipid
tertentu (lipotoxicity), FFAa juga telah dikenal meregulasi sekresi insulin, namun
peningkatan yang kronis FFAa di plasma juga akan menyebabkan gangguan
fungsi sel β.16
Selain itu, hiperglikemi juga dapat menimbulkan reactive oxygen species
(ROS), dimana sel-sel ini telah dikenal sangat rentan terhadap stres oksidatif sel β karena memiliki tingkat sederhana enzim-enzim antioksidan.19,20
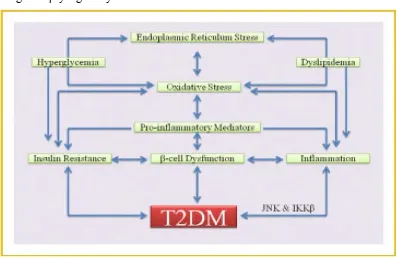
Stress oksidatif menghasilkan dan melepaskan mediator pro inflamasi (sitokin dan kemokin), yang telah diketahui keterlibatannya terhadap gangguan fungsi sel β yang menyebabkan resistensi insulin dan inflamasi .
Gambar 2.1 Beberapa faktor patogenik yang menyebabkan dan berperan dalam patogenesis DM Tipe 264
2.1.5.1Faktor-faktor yang menimbulkan terjadinya inflamasi jaringan pada DM Tipe 2
Walaupun banyak respon patogen yang terlibat dalam menginduksi resistensi insulin akibat inflamasi dan memblok sekresi insulin dari sel β, namun
hiperglikemi, dislipidemia dan stress oksidatif dianggap terlibat secara langsung dalam inflamasi jaringan yang khusus.
2.1.5.1.1 Hiperglikemi
β.41
Kadar gula darah yang tinggi yang memasuki sel β dari pankreas,akan merangsang berbagai mediator proinflamasi seperti IL-1b, TNF-a, IL-6 dll.42 2.1.5.1.2 Dislipidemia
Istilah dislipidemia digunakan ketika nilai dari lipid berubah karena respon terhadap resistensi insulin dan kelebihan nutrisi. Efek perubahan konsentrasi lipid pada sel β bergantung pada profil lipid tertentu. Saturated fatty acids (palmitate) dapat menyebabkan pro-apoptosis di sel β, dilain hal monosaturated fatty acids (oleates) melindungi sel β dari bahaya efek saturated fatty acids dan glukosa.Akibat peningkatan resistensi insulin dijaringan perifer, jumlah FFAa juga meningkat. Sekali jumlah sirkulasi dari FFAs bertambah, FFAs kemudian bermigrasi ke sel β pankreas yang menyebabkan kerusakan sel β melalui induksi sekresi dari IL-1b.44Very low density lipoproteins (VLDL) dan low density lipoproteins (LDL) sangat berbahaya dan bertindak sebagai pro apoptosis dari sel β sama seperti saturated fatty acids, dilain hal high density lipoprotein (HDL) melindungi sel β dari bahaya.45
2.1.5.1.3 Stres oksidatif
Bagaimana peran stress oksidatif dalam patogenesis DM Tipe 2 dikenal cukup baik. Stres oksidatif dapat menyebabkan kerusakan jaringan bersamaan dengan hiperglikemi yang kronis. Beberapa faktor yang menyebabkan stres oksidatif (mediator proinflamasi, hiperglikemi, dislipidemia, gangguan toleransi glukosa, resistensi insulin, hipoksia, kurangnya aktifitas) dapat merusak struktur dan fungsi dari sel β di islet pankreas.Stres oksidatif juga berpotensi membangkitkan ROS bersama dengan sitokin proinflamasi dan kemokin disekitar selβ.36
2.1.5.2 Respon inflamasi yang berpotensi sebagai dasar patogenesis DM Tipe 2 2.1.5.2.1 Hipoksia
yang kemungkinan besar dipengaruhi oleh potensi ER redox dan menurunkan konsentrasi ATP dan menyebabkan kematian sel β.29
2.1.5.2.2 Transcriptional pathways
Ada banyak jalur metabolik yang menyebabkan resistensi insulin pada di jaringan perifer. Proses metabolik merangsang terjadinya inflamasi dan stres yang menginduksi kinase seperti IkB kinase-b (IKKb) dan JUN N-terminal kinase
(JNK). Kedua kinase tersebut diketahui berperan dalam patogenesis DM Tipe 2.30 IKKb berpotensi mengaktifkan nuclear factor-kB (NF-kB) yang menginduksi sitokin proinflamasi (TNF-α dan IL-1b) di hati dan jaringan adipose. Sitokin-sitokin ini yang menyebabkan resistensi insulin di jaringan perifer.31Dilain hal, JNK berpotensi mengaktifkan transcription factor-2 (ATF2) dan ELK1. Walaupun mekanisme JNK mempengaruhi faktor transkripsi belum jelas, tapi beberapa penelitian eksperimen telah dilakukan untuk mengetahui perannya dalam proses inflamasi.vSelain jalur NF-kB dan JNK, FFAs dan advanced glycation end-products (AGEs) dapat menimbulkan resistensi insulin dan menyebabkab DM Tipe2 melalui aktifasi toll like receptors (TLRs) dan reseptor terhadap AGEs.32 2.1.5.2.3 Sitokin-sitokin
Yang paling menjanjikan dari berbagai macam faktor patofisiologi DM Tipe 2 adalah jumlah dari sitokin proinflamasi seperti IL-1b, TNF-α dan IL-6. Sitokin-sitokin ini dilepaskan dari jaringan adipose dan merangsang terjadinya inflamasi tidak hanya pada jaringan yang sesuai tetapi juga pada sel β dari islet pankreas dan menyebabkan terjadinya resistensi insulin.33Awalnya, hal tersebut untuk mengantisipasi mekanisme inflamasi dari sel β yg mengalami apoptosis yang terjadi karena hiperglikemi.34 Selanjutnya, mekanisme tersebut diteliti oleh
Proses autostimulasidari IL-1b mungkin dapat dicegah dengan memblok aktifitas NF-kB dan atau mengurangi sinyal IL-1R1 terhadap IL-1b .Karena itu rangsangan dari IL-1b karena glukosa dan FFAs dapat dicegah dengan memblok sinyal IL-1R. Lebih lanjut lagi rangsangan terhadap terhadap sel β untuk memproduksi IL-1b, juga meningkatkan produksi nitric oxide dan menyebabkan reduksi kosentrasi ATP di mitokondria yang menyebabkan disfungsi sel β dan menurunkan sekresi insulin.Selain IL-1b, TNF-α juga berperan penting dalam menyebabkan resistensi insulin, obesitas dan inflamasi.TNF-α mengatur aktivitas jalur IKKb/NF-kB dan JNK dalammeregulasi resistensi insulin. Produksi yang berlebihan dari TNF-α di jaringan adipose menyebabkan resistensi insulin di jaringan perifer dengan menginduksi terjadinya inflamasi dan apoptosis sel β di pankreas.37-39
Sitokin-sitokin proinflamasi dapat berpotensi menyebabkan inflamasi dijaringan perifer sama dengan di islets pankreas. IL-1Ra adalah satu-satunya sitokin antiinflamasi alamiah.IL-1Ra diekspresikan di kelenjar pankreas pada individu normal. Namun ekspresi Il-1 Ra menurun pada pasien DM Tipe 2 yang nantinya akan menyebabkan peningkatan kemampuan IL-1b untuk merusak islets pankreas.36,40
2.1.5.2.4 Kemokin
Adiposit mensekresi berbagai kemokin. Telah diperlihatkan bahwa jaringan adipose pada orang obesitas mensekresi kemokin lebih banyak dibandingkan pada pasien yang tidak obesitas.61Ada beberapa tipe dari kemokin sepertiCCL2 (MCP1), CCL3,(MIP-1a), CCL6, CCL7, CCL8, dan CCL9. Semua kemokin
dihasilkan dari jaringan adipose, islets di pankreas dan sel endotel. Beberapa penelitian eksperimen telah mengobservasi bahwa kemokin berperan penting
2.1.5.3 Innate immune system
Innate immune system atau sistem imun alamiah adalah sistem pertama
pertahanan tubuh memerangi infeksi mikroba,cedera fisik dan cedera kimia.
Konsep pengaktifan dari innate imunity mendasari patofisiologi dari DM
Tipe2, resistensi insulin, aterosklerosis, sudah ditegakkan oleh beberapa
penelitian.24,25
Sejumlah reaksi terjadi untuk mencegah kerusakan jaringan, mengisolasi
dan menghancurkan sumber infeksi dan mengaktifkan proses penyembuhan untuk
mengembalikan hemostasis, terdiri dari proses penyembuhan luka, menghindari
dan mengisolasi ancaman.26
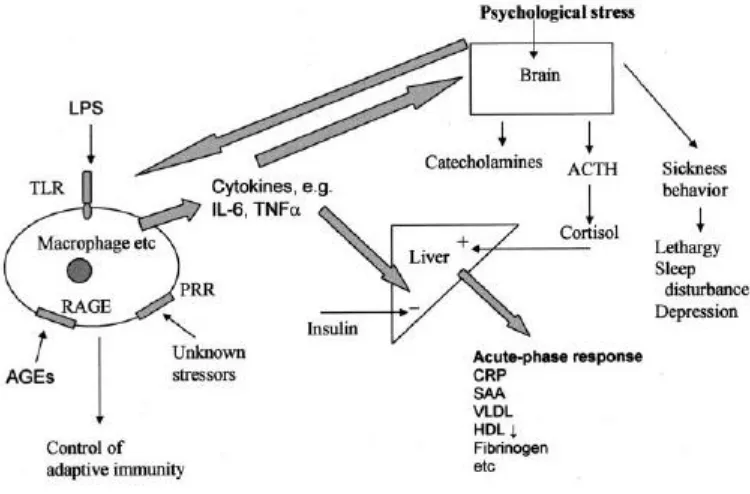
Gambar 2.2 Komponen-komponen dari sistem imun alamiah (Innate immune system)10
Sentinel cells seperti makrofag mendeteksi lingkungan yang memiliki
potensi bahaya dari infeksi,zat-zat kimia dan makanan oleh PRRs (Pattern
recognition receptors) dengan mengaktifkan jalur signal dan pelepasan
dari TLR-4, yang dapat mengenali LPS (lipopolysaccharide) dari bakteri dan reseptor terhadap AGEs (Advanced Glication Endproduct).
Sitokin-sitokin merangsang produksi protein fase akut dari hati dan juga
merangsang otak untuk melepaskan hormon adrenocorticotropic (cortisol dari
kelenjar adrenal) dan mengaktifkan sistem saraf simpatis melalui pelepasan
katekolamin.Stress Psikologis juga dapat menyebabkan respon fase akut melalui
persyarafan sel-sel yang memproduksi sitokin dan melalui aktivasi sistem saraf
simpatis dan reseptor adrenergik di makrofag. Sitokin pusat merangsang “sickness
behavior” diantaranya letargi, perubahan pola tidur dan depresi.The innate immune system juga mengontrol sistem imun adaptasi melalui ekspresi
costimulatory molecule yang diperlukan untuk antigen presentation, SAA dan
serum amyloid A.26
Studi tentang aturan dari innate immunity telah menemukan pentingnya
respon terhadap cedera pada penyakit metabolik. Setiap pertimbangan yang
digunakan pada terapi DM Tipe 2 mungkin dibayangkan sebagai suatu jalan untuk
membuktikan respon terhadap cedera, dengan cara diet (menurunkan terjadinya
cedera), olahraga ( suatu cara untuk melatih respon terhadap suatu cedera oleh
microinjury yang berulang),metformin dan DPP-IV inhibitors ( dengan efek anti
inflamasinya yang sudah diketahui dengan baik) atau insulin ( pusat regulasi dari
inflamasi). Respon model terhadap cederaini sebaiknya diuji dimasa depan
sebagai suatu langkah perkembangan strategi baru dari terapi gangguan
metabolik.
2.2 C-Reaktive Protein (CRP)
2.2.1 Definisi
kuantitatif dimana dapat mengukur kadar sampai < 0,2– 0,3 mg/L.46Dengan nilai rujukan dikatakan low <1.0mg/L, moderate 1.0-3.0 mg/L dan high>3.0mg/L.
CRP merupakan marker inflamasi yang diproduksi dan dilepas oleh hati dibawah rangsangan sitokin-sitokin seperti IL-6,Interleukin 1 (IL-1), dan Tumor
Necroting Factor α (TNF-α).47
. Beberapa obat seperti colchicine dapat menghambat produksi CRP
sedangkan obat immunosupresif seperti kortikosteroid dan yang lainnya atau obat anti radang (Non Steroid Anti Inflamation Drug) tidak dapat menghambat sekresinya.47
2.2.2 Sintesis CRP
Sintesis CRP di hati berlangsung sangat cepat setelah ada sedikit rangsangan, konsentrasi serum meningkat diatas 5mg/L selama 6-8 jam dan mencapai puncak sekitar 24-48 jam. Waktu paruh dalam plasma adalah 19 jam dan menetap pada semua keadaan sehat dan sakit, sehingga satu-satunya penentu konsentrasi CRP di sirkulasi adalah menghitung sintesa IL-6 dengan demikian menggambarkan secara langsung intensitas proses patologi yang merangsang produksi CRP. Kadar CRP akan menurun tajam bila proses peradangan atau kerusakan jaringan mereda dan dalam waktu sekitar 24-48 jam telah mencapai nilai normal kembali .Kadar CRP stabil dalam plasma dan tidak dipengaruhi variasi diurnal.46-48
2.2.3 Fungsi Biologis CRP
Fungsi dan peranan CRP di dalam tubuh ( in vivo ) belum diketahui
seluruhnya, banyak hal yang masih merupakan hipotesis. Meskipun CRP bukan suatu antibodi, tetapi CRP mempunyai berbagai fungsi biologis yang menunjukkan peranannya pada proses peradangan dan mekanisme daya tahan tubuh terhadap infeksi.46
Beberapa hal yang diketahui tentang fungsi biologis CRP ialah:46,49 1. CRP dapat mengikat C-polisakarida (CPS) dari berbagai bakteri melalui
2. CRP dapat meningkatkan aktivitas dan motilitas sel fagosit seperti granulosit dan monosit/makrofag
3. CRP dapat mengaktifkan komplemen baik melalui jalur klasik mulai dengan C1q maupun jalur alternatif.
4. CRP mempunyai daya ikat selektif terhadap limfosit T. Dalam hal ini diduga CRP memegang peranan dalam pengaturan beberapa fungsi
tertentu selama proses keradangan.
5. CRP mengenal residu fosforilkolin dari fosfolipid, lipoprotein membrane sel rusak, kromatin inti dan kompleks DNA-histon.
6. CRP dapat mengikat dan mendetoksikasi bahan toksin endogen yang terbentuk sebagai hasil kerusakan jaringan.
2.2.4 Inflamasi dan Respon Fase Akut
Inflamasi merupakan mekanisme proteksi yang terbatas terhadap trauma atau invasi mikroba dengan reaksi yang menghancurkan atau membatasi bahan yang berbahaya dan merusak jaringan.Inflamasi diperlukan tubuh untuk mempertahankan diri dari berbagai bahaya yang mengganggu keseimbangan tetapi juga dapat memperbaiki kerusakan struktur serta gangguan fungsi jaringan.Reaksi inflamasi termasuk dalam respons imun nonspesifik. Bila terjadi inflamasi, sel-sel sistem imun yang tersebar di seluruh tubuh akan bergerak ke lokasi infeksi beserta produk-produk yang dihasilkannya.50
Selama respon ini berlangsung terjadi 3 proses yang penting yaitu:
Peningkatan aliran darah ke daerah infeksi
Peningkatan permeabilitas kapiler akibat retraksi sel-sel endotel yang
mengakibatkan molekul-molekul besar dapat menembus dinding vaskuler
Migrasi leukosit ke vaskuler
neutrofilia dan protein fase akut. Proses inflamasi akan berjalan terus sampai antigen dapat disingkirkan.45
Sejumlah protein plasma secara bersama disebut protein-protein fase akut. Protein-protein ini menunjukkan peningkatan dramatis dalam menanggapi mediator-mediator yang bertindak sebagai tanda bahaya dini.45
Suatu sifat utama dari CRP adalah kemampuannya mengikat ( dengan pola
yang bergantung dengan kalsium ) sejumlah mikroorganisme yang mengandung fosforilkolin dalam membran mereka, kompleks yang berguna untuk mengaktifkan komplemen ( melalui jalur klasik ). Ini mengakibatkan deposisi C3b diatas permukaan mikroba yang kemudian diopsonisasi untuk perlekatan pada fagosit.Aktivasi komplemen berikutnya adalah terjadinya penarikan dan pemacuan neutrofil, fagosit yang telah aktif terikat pada mikroba yang telah diselaputi oleh C3b melalui permukaan reseptor C3b dan kemudian menelan mereka. CRP juga diikat C1q dan karenanya dapat mengaktifkan komplemen atau bekerja sebagai opsonin melalui interaksi dengan reseptor C1q pada fagosit.51,52
Peningkatan sintesis CRP akan meningkatkan viskositas plasma sehingga laju endap darah juga akan meningkat. Adanya CRP yang tetap tinggi menunjukkan infeksi yang tetap persisten.45,52
2.2.5 Pemeriksaan Kadar CRP
2.2.5.1 Prinsip dan Metode Pemeriksaan
Pada penentuan CRP, maka CRP dianggap sebagai antigen yang akan
ditentukan dengan menggunakan suatu antibodi spesifik yang diketahui (antibodi anti-CRP). Dengan suatu antisera yang spesifik, CRP (merupakan antigen yang
larut) dalam serum mudah dipresipitasikan.46
Jadi pada dasarnya, penentuan CRP dapat dilakukan dengan cara, yaitu:
Tes presipitasi: Sebagai antigen ialah CRP yang akan ditentukan, dan
sebagai antibodi adalah anti-CRP yang telah diketahui
Tes aglutinasi pasif: Antibodi disalutkan pada partikel untuk menentukan
Uji ELISA: Dipakai teknik Double Antibody Sandwich ELISA. Antibodi
pertama (antibodi pelapis) dilapiskan pada fase padat, kemudian ditambahkan serum penderita. Selanjutnya ditambahkan antibodi kedua (antibodi pelacak) yang berlabel enzim. Akhirnya ditambahkan substrat, dan reagen penghenti reaksi. Hasilnya dinyatakan secara kuantitatif.
Imunokromatografi: Merupakan uji Sandwich imunometrik. Pada tes ini,
antibodi monoklonal terhadap CRP diimobilisasi pada membran selulosa nitrat di garis pengikat. Bila ditambahkan serum yang diencerkan sampai ambang atas titer rujukannya pada bantalan sampel maka CRP dalam sampel akan diisap oleh bantalan absorban menuju bantalan konjugat, dan akan diikat oleh konjugat (antibodi monoklonal) pertama, berlabel emas koloidal. Selanjutnya CRP yang telah mengikat konjugat akan diisap oleh bantalan absorban menuju ke garis pengikat yang mengandung antibodi monoklonal kedua terhadap CRP (imobile) sehingga berubah warna menjadi merah. Sisanya yang tidak terikat pada garis pengikat akan bergerak menuju garis kontrol yang mengandung antibodi anti tikus yang mengikat sisa konjugat yang tidak terikat pada garis pengikat. Konjugat yang tidak terikat dibersihkan dari membran dengan larutan pencuci yang selanjutnya diisap oleh membran absorban. Bila kadar CRP lebih tinggi daripada ambang atas titer rujukannya, akan terbentuk warna merah coklat pada garis pengikat di membran yang intensitasnya berbanding lurus dengan kadar CRP dalam serum. Pembacaan hasil secara kuantitatif.
Imunoturbidimetri: Merupakan cara penentuan yang kualitatif. CRP dalam
serum akan mengikat antibodi spesifik terhadap CRP membentuk suatu
kompleks immun. Kekeruhan (turbidity) yang terjadi sebagai akibat ikatan tersebut diukur secara fotometris. Konsentrasi dari CRP ditentukan secara kuantitatif dengan pengukuran turbidimetrik.
2.2.5.2Hal-hal yang dapat mempengaruhi hasil pemeriksaan CRP
chron’s, sindrom reiter’s, sindrom vaskulitis, lupus eritematosus, nekrosis jaringan atau trauma.Obat-obatan yang dapat menurunkan kadar CRP seperti colchicines
dan statin.45,46
2.3 Puguntano dan inflamasi
Berdasarkan penelitian Juwita (2009)., diketahui bahwa tumbuhan puguntano mengandung senyawa kimia golongan alkaloid, flavonoid, tanin dan steroid/triterpenoid.13Hal ini juga sesuai dengan studi Harahap dkk. yang
menemukan bahwa ekstrak etanol daun puguntano yang diperoleh dari metode perkolasi dan sokletasi memiliki kandungan fitokimia yang sama yaitu
flavonoid,saponin, tannin, glikosida, dan steroid/terpenoid.53Diduga senyawa cucurbitacin dalam glikosida yang terkandung pada tumbuhan inilah yang memberikan efek penurunan kadar gula darah pada serbuk simplisia Puguntano tersebut.14
Salah satu golongan senyawa kimia yang bertanggung jawab untuk efek antiinflamasi adalah steroid/triterpenoid. Sehingga diduga steroid inilah yang memberikan efek antiinflamasi dari daun puguntano tersebut.Efek antiinflamasi dari senyawa steroid/triterpenoid berhubungan dengan kemampuannya yang dapat menghambat kerja enzimatik fosfolipase sehingga mencegah pelepasan mediator proses peradangan, yaitu asam arakhidonat dan metabolitnya seperti prostaglandin (PG), leukotrien(LT), tromboksan dan prostasiklin sehingga terjadinya peradangan lebih lanjut dapat dihidari (Siswandono dan Soekardjo,1995). Efek samping yang sering timbul akibat pemakaian obat-obat sintesis dihindari dengan penggunaan ekstrak yang terdiri dari berbagai macam komponen senyawa kimia, yang diharapkan interaksi antara komponen-komponen tersebut dapat meniadakan efek samping.13
Flavonoid merupakan fenol bioaktif dengan berat molekul rendah dan memiliki peran dalam sintesis sel.54Dalam keterkaitannya dengan diabetes
pelepasan insulin dan meningkatkan uptake ion Ca2+.56Studi lain menemukan bahwa flavonoid merupakan komponen fenol dengan aktifitas biologi yang luas dan memiliki efek pada diabetes melalui inhibisinya pada enzim α-glukosidase atau pencegahan absorpsi glukosa dan atau memperbaiki toleransi glukosa.57Studi terakhir menunjukkan phenolic fitokimiapada tannin merupakan inhibitor α -amilase dan α-glukosidase, dengan efek yang kuat pada inhibisi α-glukosidase dan efek ringan pada α-amilase sehingga dapat digunakan untuk mencegah lonjakan gula darah post-prandial dengan efek yang minimal.57
Studi yang terakhir mendapatkan secara observasi klinis serbuk simplisia daun puguntano mempunyai efek dalam menurunkan kadar gula darah pada pasien diabetes mellitus dengan dosis 2 g, 3 kali sehari selama 14 hari yang diberikan secara oral dalam bentuk seduhan.14
Studi lain pun telah menyimpulkan bahwa n –hexane ekstrak dari daun picria fel –terrae lour merupakan obat anti diabetes yang efektif . Dimana zat ini memiliki kemampuan menurunkan nilai glukosa darah dan reduksi selama 10 hari sebesar 44.47% pada mencit.58
2.3.1 Pembuatan ekstrak
Metode: perkolasi Pelarut: etanol 70% .
Cara: sebanyak 300 g serbuk simplisia dimasukkan ke dalam bejana bertutup dan dibasahi dengan sejumlah cairan penyari etanol 50%, dimaserasi selama 3 jam.
Massa dipindahkan sedikit demi sedikit ke dalam perkolator, kemudian cairan penyari dituangkan secukupnya sampai terdapat selapis cairan penyari di atas
2.3.2 Pembuatan sediaan kapsul ekstrak daun puguntano
Kapsul ekstrak daun Puguntano dibuatdengan dosis 100 mg dan dicampur dengan bahan pengisi sampai bobot kapsul 500 mg digunakan cangkang kapsul nomor 0.
Setiap kapsul mengandung:
R/ Ektrak daun Puguntano 100 mg Amylum manihot 5 % Amylum maydis 2,5 % Sakarum laktis qs Cara :
Ekstrak kental daun Puguntano ditimbang lalu digerus sedikit demi sedikit dengan bahan pengisi dan bahan pengering/pegembang (amylum manihot, amylum maydis dan sakarum laktis) sehingga diperoleh massa yang kompak, kemudian dibuat granul dengan mengayak massa tersebut. Dikeringkan di lemari pengering selama 1 jam sehingga diperoleh granul kering. Diayak kembali dan dicampur dengan sakarum laktis sampai mencapai bobot yang sesuai.Kemudian dimasukkan ke dalam cangkang kapsul dengan bantuan alat pengisi kapsul.
Evaluasi penyimpangan bobot sediaan kapsul ekstrak daun puguntano dilakukan dengan cara berikut :
Cara :
Ditimbang 20 kapsul, kemudian ditimbang lagi kapsul satu persatu.Keluarkan isi
semua kapsul, timbang seluruh bagian cangkang kapsul. Perbedaan dalam persen bobot isi tiap kapsul terhadap bobot rata-rata tiap isi kapsul tidak boleh lebih dari