LAMPIRAN 1
DATA HASIL PERCOBAAN
1.1 DATA HASIL PERCOBAAN
Untuk larutan logam berat Cd, Fe dan Zn memiliki konsentrasi awal sebesar 12,5 ppm.
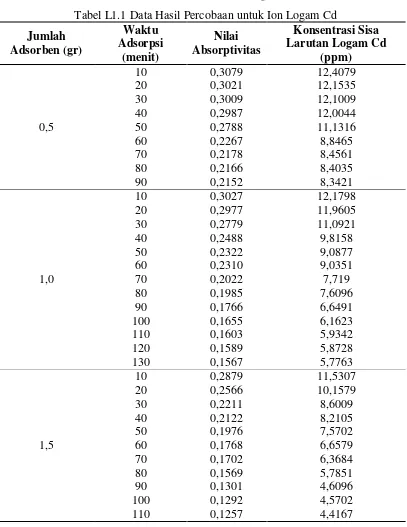
1.1.1 Data Hasil Percobaan Untuk Ion Logam Cd
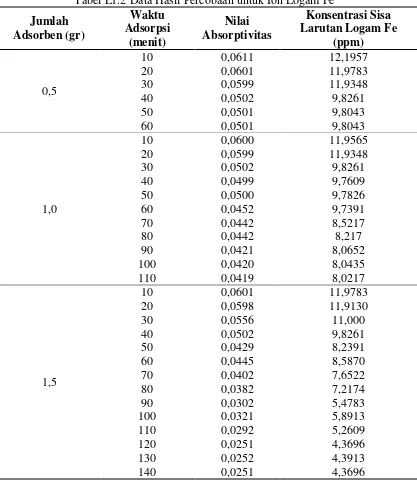
1.1.2 Data Hasil Percobaan Untuk Ion Fe
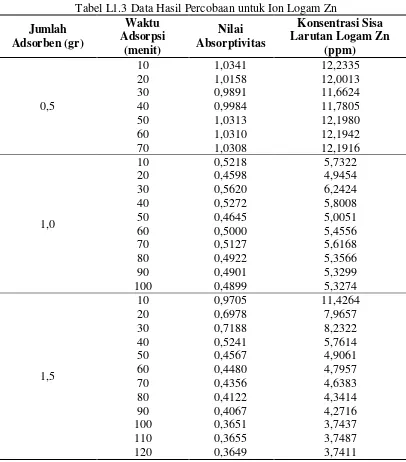
1.1.3 Data Hasil Percobaan Untuk Ion Logam Zn
1.2 DATA HASIL PERHITUNGAN
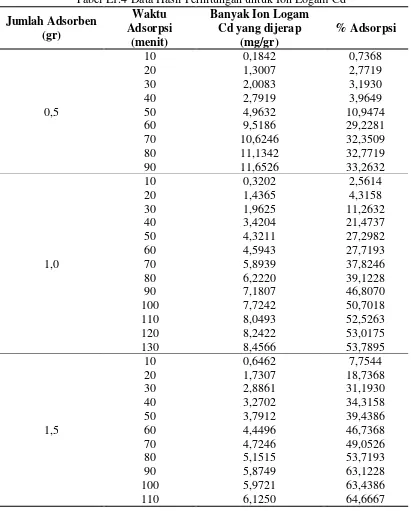
1.2.1 Data Hasil Perhitungan Ion Logam Cd
1.2.2 Data Hasil Perhitungan Ion Logam Fe
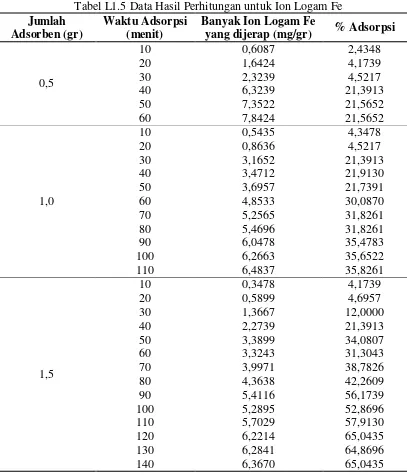
Tabel L1.5 Data Hasil Perhitungan untuk Ion Logam Fe Jumlah
Adsorben (gr)
Waktu Adsorpsi (menit)
Banyak Ion Logam Fe
yang dijerap (mg/gr) % Adsorpsi
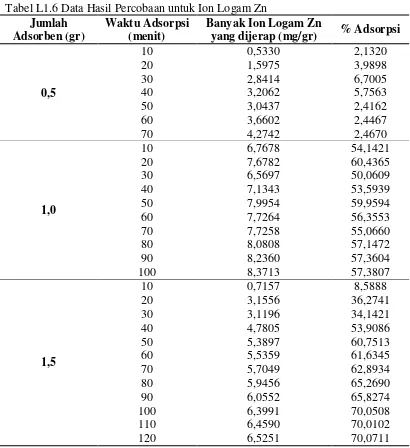
1.2.3 Data Hasil Perhitungan Ion Logam Zn Tabel L1.6 Data Hasil Percobaan untuk Ion Logam Zn
Jumlah Adsorben (gr)
Waktu Adsorpsi (menit)
Banyak Ion Logam Zn
yang dijerap (mg/gr) % Adsorpsi
LAMPIRAN 2
CONTOH HASIL PERHITUNGAN
2.1 PERHITUNGAN BANYAK ION LOGAM YANG DIJERAP
Dari persamaan 3.1 dapat dihitung jumlah ion logam yang dijerap oleh adsorben. Maka untuk contoh perhitungan jumlah logam yang dijerap akan diambil contoh yaitu ion logam Fe pada waktu adsorpsi 20 menit dan jumlah
2.2 PERHITUNGAN PERSENTASE ADSORPSI
Dalam perhitungan persentase adsorpsi digunakan persamaan 4.1. Maka untuk contoh perhitungan persentase adsorpsi akan diambil contoh ion logam Fe pada waktu adsorpsi 20 menit dan jumlah adsorben 0,5 gram.
% Adsorpsi = Co- C
Co x 100% (4.1)
% Adsorpsi = ( 12,5-11,9783
12,5 ) ppm x 100%
= 0,041739 x 100%
= 4,1739%
2.3 PERHITUNGAN KINETIKA ADSORPSI
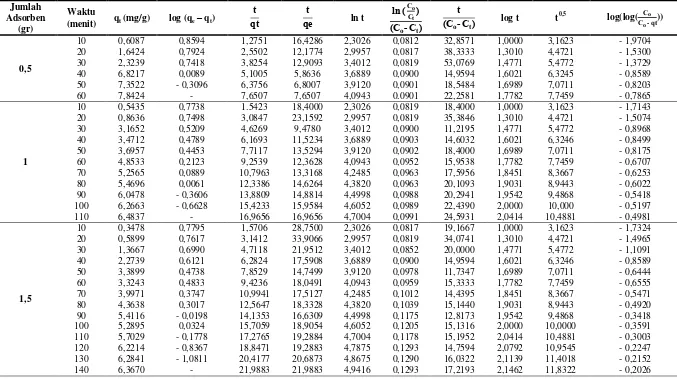
Untuk contoh perhitungan kinetika adsorpsi maka digunakan data dari ion logam Fe. Diplot hasil yang diperoleh sehingga akan didapatkan persamaan kinetika adsorpsi yang sesuai untuk penjerapan ion logam Fe dengan adsorben cangkang telur bebek. Data untuk penentuan kinetika adsorpsi penjerapan ion logam Fe dapat dilihat pada tabel L2.1.
Persamaan Orde Satu Semu Lagergen
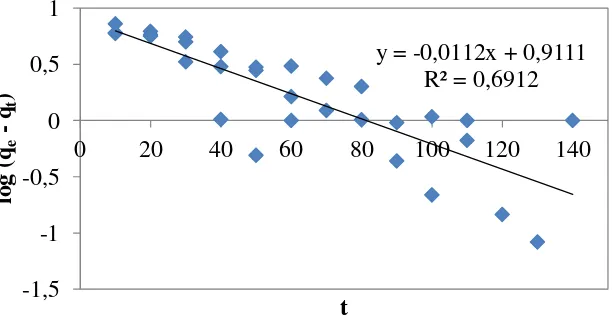
Diplot kurva log (qe – qt) vs t dengan slope adalah k1. Kurva log (qe
– qt) vs dapat dilihat pada gambar L2.1.
Gambar L2.1 Plot Kinetika Orde Satu Semu Lagergen untuk Penjerapan Ion Logam Fe
Dari gambar L2.1 diperoleh persamaan kinetika orde satu semu Lagergen adalah y = -0,0112x + 0,9111 dengan R2 = 0,6912. Maka untuk mencari nilai dari k1 dapat dilihat pada cara berikut:
Maka nilai k1 sebesar 0,0258 L/menit.
Persamaan Orde Dua
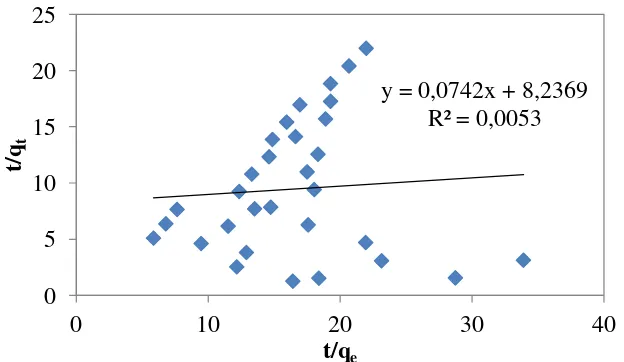
Diplot kurva t vs t dengan intersep adalah k. Kurva tvs t dapat dilihat pada gambar L2.2.
Gambar L2.2 Plot Kinetika Orde Dua untuk Penjerapan Ion Logam Fe
Dari gambar L2.2 diperoleh persamaan kinetika orde dua adalah y = 0,0742x + 8,2369 dengan R2 = 0,0053. Maka untuk mencari nilai dari k dapat dilihat pada cara berikut:
h = k. qeq cal2
h = 0,0007. (13,4771)2 h = 0,1271
Maka nilai k sebesar 0,0007 gr/mmol.menit. Untuk laju adsorpsi diperoleh nilai h sebesar 0,1271 mg/gr.menit.
Persamaan Difusi Intra Partikel
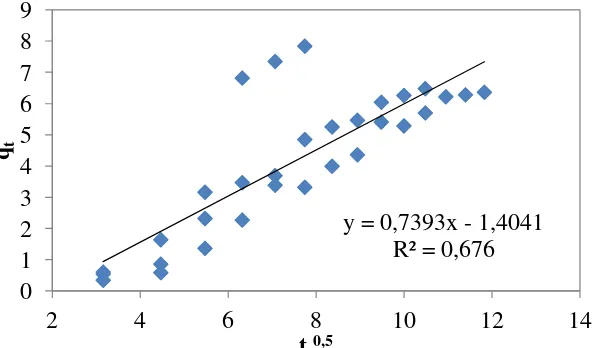
Diplot kurva qt vs t0,5 dengan slope adalah ki. Kurva qt vs t0,5 dapat dilihat pada gambar L2.3.
Gambar L2.3 Plot Kinetika Difusi Intra Partikel untuk Penjerapan Ion Logam Fe
Dari gambar L2.3 diperoleh persamaan kinetika orde dua adalah y = 0,7393x – 1,4041 dengan R2 = 0,676. Maka untuk mencari nilai dari ki dapat dilihat pada cara berikut:
Persamaan Bangham
Diplot kurva log(log( Co
Co- t
))
vs log t dengan slope adalah km. Kurvalog(log( Co
Co- t
))
vs log t dapat dilihat pada gambar L2.4.Gambar L2.4 Plot Kinetika Bangham untuk Penjerapan Ion Logam Fe
Dari gambar L2.4 diperoleh persamaan kinetika orde dua adalah y = 1,4373x – 3,2605 dengan R2 = 0,9508. Maka untuk mencari nilai dari km dapat dilihat pada cara berikut:
Gambar L2.5 Plot Kinetika Elovisch untuk Penjerapan Ion Logam Fe
Dari gambar L2.5 diperoleh persamaan kinetika orde dua adalah y = 2,499x – 5,6087 dengan R2 = 0,7124. Maka untuk mencari nilai dari ɑ dan ß dapat dilihat pada cara berikut:
Persamaan Langmuir - Hinshelwood
Gambar L2.6 Plot Kinetika Langmuir - Hinshelwood untuk Penjerapan Ion Logam Fe
Dari gambar L2.6 diperoleh persamaan kinetika Langmuir - Hinshelwood adalah y = -0,0008x + 0,1134 dengan R2 = 0,2365. Maka untuk mencari nilai dari ko dan k1 dapat dilihat pada cara berikut:
ko = nilai intersep disebabkan nilai koefisien korelasi atau R2 yang telah mendekati nilai 1.
2.4 PERHITUNGAN ISOTHERM ADSORPSI
Untuk contoh perhitungan isotherm adsorpsi digunakan data dari ion logam Fe. Dari hasil yang diperoleh dapat ditabelkan pada tabel L2.2.
Tabel L2.2 Data Penentuan Isotherm Adsorpsi
Ce qe log Ce log qe ln qe ln Ce ɛ2 Ce / qe
Nilai ɛ2 diperoleh dengan menggunakan persamaan 2.7:
ɛ = RT ln(1 + 1
Ce) (2.7)
Diplot kurva isotherm yang dapat mewakili penjerapan ion logam Fe. Trial I (Isotherm Langmuir)
Diplot Ce
Dari gambar L2.7 diperoleh persamaan isotherm Langmuir adalah
Trial II (Isotherm Freundlich)
Untuk isotherm Freundlich akan diplot kurva log Ce vs log qe. Kurva tersebut akan memberikan nilai intersep adalah log k dan slope adalah
1
n. Kurva isotherm Freundlich dapat dilihat pada gambar L2.8.
Dari gambar L2.8 diperoleh persamaan isotherm Freundlich adalah
Trial III (Isotherm Tempkin)
Isotherm Tempkin memiliki kurva qe vs ln Ce dengan intersep adalah
B1 ln Kt dan slope adalah B1. Kurva isotherm Tempkin dapat dilihat pada gambar L2.9.
Pada Gambar L2.9 diperoleh persamaan isotherm Tempkin adalah y = 1,4456 x + 4,0837. Maka dapat dihitung nilai B1 dan Kt dengan cara sebagai berikut:
B1 = nilai intersep B1 = 1,4456
B1 ln Kt = 4,0837 1,4456 ln Kt = 4,0837 ln Kt = 4,0837
1,4456
ln Kt = 2,8249 Kt = e2,8249
Kt = 16,8596
Dari perhitungan diperoleh nilai B1 sebesar 1,4456 mg/gr dan Kt sebesar 16,8596. Nilai B1 dapat diperoleh nilai b dengan cara sebagai berikut:
B1 =
T b
1,4456 = 8,3145 kJ/kmol.K . 301,15 K
b
b = 8,3145 kJ/kmol.K . 301,15 K
1,4456
b = 1.732,0916 kJ/kmol
Trial IV (Isotherm DKR)
Gambar L2.10 Kurva Isotherm DKR untuk Ion Logam Fe yang Dijerap oleh Adsorben Cangkang Telur Bebek
Dari gambar L2.10 diperoleh persamaan isotherm DKR yaitu y = -0,0000007 x + 2,0201. Maka dapat dihitung nilai Xm dan ß dengan cara sebagai berikut:
Dari hasil perhitungan diperoleh nilai Xm (kapasitas penjerapan maksimum) sebesar 7,5391 mg/gr dan ß (koefisien aktivitas) sebesar -0,0000007mol2/J2.
Trial V (Isotherm BET)
Isotherm BET memiliki kurva Ce vs dengan intersep adalah
Gambar L2.11 Kurva Isotherm BET untuk Ion Logam Fe yang Dijerap oleh Adsorben Cangkang Telur Bebek
Dari perhitungan diperoleh nilai KB sebesar 4,8191 dan Cs sebesar 7,1586 mg/L.
LAMPIRAN 3
FOTO HASIL PENELITIAN
3.1 FOTO PERCOBAAN ADSORPSI LOGAM BERAT
Gambar L3.1 Foto Larutan Logam Berat yang Dibuat
Gambar L3.3 Tempat Penempatan Sampel yang akan Diuji dengan AAS
3.2 FOTO PERALATAN YANG DIGUNAKAN
Gambar L3.5 Peralatan AAS yang Digunakan
Gambar L3.7 Pipa Penyalur Gas