IKATAN DAN STRUKTUR MOLEKUL :
Gaya antarmolekul, Cairan dan Padatan
Diantara 112 unsur yang dikenal, sebagian besar berupa padatan pada kondisi 25oC
dan 1 atm. Hanya 11 unsur berupa gas pada kondisi ini ( H2, N2, O2 F2 Cl2 dan 6 gas
mulia), dan 2 unsur berupa cairan (Hg dan Br2), walaupun 2 unsur lainnya (Cs dan Ga)
meleleh hanya pada temperatur yang agak tinggi. Banyak senyawa berupa gas (CO2 dan
CH4) dan cairan (H2O), akan tetapi sebagian besar senyawa berupa padatan.
Pada bab ini akan diterangkan beberapa hal yang menarik tentang fasa cair dan
padatan, seperti mengapa tubuh kita merasa dingin apabila berkeringat, bagaimana air
tubuh dapat mempengaruhi cuaca sekitar (local climate), mengapa karbon murni berupa
intan keras dan grafit, dan mengapa banyak senyawa padatan membentuk bentuk kristal
yang indah.
1 KEADAAN MATERI DAN TEORI KINETIKA MOLEKUL
Teori kinetika molekul gas mengasumsikan, bahwa jarak antar atom atau molekul
gas sangat berjauhan dan antar partikel ini dianggap saling independen. Akibatnya,
sifat-sifat gas pada sebagian besar kondisi dapat ditentukan dengan menggunakan persamaan
gas ideal PV = nRT. Akan tetapi cairan dan padatan tidak sesederhana fasa gas. Partikel
pada fasa cair dan padat saling berdekatan, karena terjadi gaya tarik antar partikel, dimana
gaya ini untuk gas diabaikan.
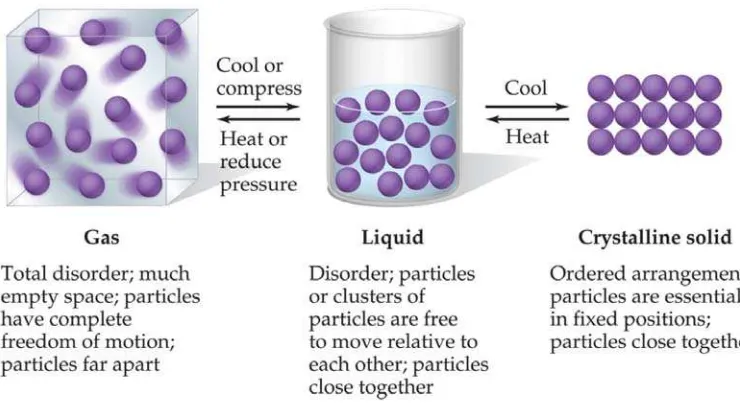
Perbedaan masing-masing keadaan materi ditinjau dari tingkat partikulat, dapat
diterangkan dengan membandingkan volume yang ditempati oleh masing-masing keadaan
materi dengan jumlah molekul yang sama. Suatu wadah berisi 300 mL nitrogen cair. Bila
semua cairan ini diuapkan, gas nitrogen yang terbentuk dapat mengisi balon yang sangat
besar (> 200 L) sampai tekanan 1 atm pada temperatur kamar. Antar molekul gas terdapat
ruang ruang kosong, sedangkan pada cairan molekulnya sangat berdekatan, bahkan saling
bersentuhan.
Pada perubahan dari fasa cair ke gas disertai dengan perubahan volume yang
sangat besar. Sebaliknya pada perubahan dari fasa padat menjadi cair tidak disertai dengan
perubahan volume yang besar. Atom-atom di dalam cairan saling berikatan dengan
kekuatan yang hampir sama dengan atom di dalam padatan. Gas mudah dikompresi, yaitu
atau padat sukar dikompresi, partikelnya akan saling tolak menolak untuk didekatkan.
Campuran udara-bahan bakar di dalam mesin mobil dikompresi terlebih dahulu dengan
faktor 10 sebelum dibakar. Sebaliknya volume air cair hanya berubah sebesar 0,005 %
setiap perubahan tekanan 1 atm.
Gambar 13.1 Perubahan dari gas, cair ke padat.
Teori kinetika molekul gas mengasumsikan, bahwa antar molekul gas hanya
terdapat gaya tarik menarik yang sangat lemah. Gaya tarik antar molekul atau antar ion -
molekul pada cairan atau padatan jauh lebih kuat. Gaya tarik yang kuat ini menyebabkan
antar molekul saling berikatan, sehingga cairan (dan padatan bila dalam bentuk bubuk)
dapat dituang dari wadah satu ke wadah lainnya dan cairan dapat membentuk tetesan.
Oleh karena pentingnya peranan gaya antarmolekul pada cairan dan padatan, maka pada
bab berikut ini akan dibicarakan mengenai gaya antarmolekul.
13.2 GAYA ANTARMOLEKUL
Berbagai tipe gaya antarmolekul terdapat pada Tabel 13.1. Gaya antarmolekul tersebut
meliputi interaksi antara ion dan molekul polar, antar molekul polar, dan antar molekul
nonpolar. Perlu dicatat, bahwa semua gaya ini berasal dari gaya tarik elektrostatik, yaitu
gaya tarik antara muatan positif dan negatif. Gaya antarmolekul sangat berperan di dalam
banyak proses, terutama dalam hal energi yang berkaitan dengan berbagai perubahan
keadaan suatu materi (padat, cair, gas). Juga berkaitan langsung dengan titik leleh, titik
didih dan entalpi penguapan, yaitu sifat yang membutuhkan energi untuk mengatasi gaya
Tabel 13.1 Gaya antarmolekul
Jenis Interaksi Faktor dasar yang berperan dalam energi interaksi
Ion – dipol Muatan ion ; momen dipol
Dipol – dipol Momen dipol
Dipol – dipol induksi Momen dipol, polarizability
Dipol induksi – dipol
induksi Polarizability
Umumnya, gaya antarmolekul tidak sekuat gaya ikatan intramolekul. Kebanyakan energi
ikatan kovalen berkisar antara 100 sampai 400 kJ/mol. Gaya tarik antar ion di dalam
senyawa ionik lebih besar, biasanya berkisar antara 700 sampai 1100 kJ/mol. Sebagai
acuan kasar, gaya antarmolekul umumnya 15% (atau kurang) dari energi ikatan.
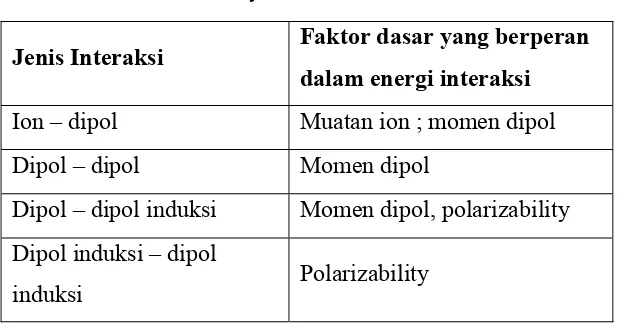
Interaksi antara ion dan molekul dengan dipol permanen
Adanya distribusi elektron ikatan di dalam molekul seringkali menghasilkan dipol
momen permanen. Molekul dengan dipol ini memiliki kutub positif dan negatif. Bila
molekul polar dan senyawa ionik dicampur, kutub negatif dari dipol akan berikatan
dengan kation positif, dan sebaliknya kutub positif dengan anion. Kekuatan gaya tarik
antara ion positif atau negatif dengan molekul polar lebih lemah dibandingkan dengan
gaya tarik antara ion-ion, tetapi lebih besar dibandingkan dengan gaya antarmolekul
lainnya. Gaya tarik ion-dipol dapat diungkapkan dengan hukum Coulomb berikut :
(n+e)(n-e) Gaya ~
d2
Dari persamaan di atas, gaya tarik bergantung pada :
- Jarak antara ion dan dipol ; makin dekat jarak antara ion dan dipol, gaya tarik semakin
kuat.
- Kekuatan dipol ; makin besar kekuatan dipol, gaya tarik semakin kuat.
Contoh interaksi antara ion dengan molekul polar adalah pembentukan ion terhidrasi di
dalam larutan air. Bila senyawa ionik dilarutkan dalam air, ion positif dan negatif
dikelilingi oleh molekul air yang polar (Gambar 13.2).
Gambar 13.2 Gaya tarik antara ion dengan kutub positif dan negatif kuat.
Energi yang berkaitan dengan hidrasi ion disebut energi solvasi atau lebih spesifik
disebut entalpi hidrasi. Nilai energi solvasi atau entalpi hidrasi suatu ion tidak dapat diukur
langsung, tetapi nilainya dapat ditentukan. Solvasi atau hidrasi ion Na digambarkan oleh
reaksi berikut :
Na+ (g) + x H2O (ℓ) → [Na(H2O)x]+(aq) (x kemungkinan = 6)
∆Hreaksi = - 405 kJ
Energi gaya tarik bergantung pada 1/d, d adalah jarak antara pusat ion dengan
muatan kutub yang berlawanan. Berarti, semakin besar jari-jari ion, entalpi hidrasi
semakin kurang eksoterm.
Tabel 13.2 Entalpi hidrasi kation logam alkali
Kation jari-jari ion Entalpi hidrasi
(pm) (kJ/mol)
Na+ 116 - 405
K+ 152 - 321
Rb+ 166 - 296
Cs+ 181 - 263
Entalpi hidrasi dari ion H+ sekitar – 1090 kJ/mol. Nilai yang besar ini disebabkan ion H+
berukuran sangat kecil. Oleh karena ion H+ terhidrasi sering diformulasikan sebagai ion
H3O+, walaupun struktur sebenarnya lebih rumit.
Garam terhidrasi seringkali dijumpai di dalam ilmu kimia. Contoh BaCl2.2H2O dan
CoCl2.6H2O. Kadang-kadang molekul air menempati ruang kosong di dalam kisi kristal,
tetapi seringkali kation dari garam tersebut berasosiasi langsung dengan molekul air.
Contoh senyawa CoCl2.6H2O lebih baik dituliskan sebagai [Co(H2O)4Cl2].2H2O (Gambar
13.3).
Gambar 13.3. Gambar [Co(H2O)4Cl2].2H2O yang berwarna coklat
Empat dari enam molekul H2O berikatan dengan ion Co2+ dengan gaya tarik ion-dipol, 2
molekul H2O lainnya di dalam kisi.
Soal 13.1 : Energi hidrasi
Jelaskan mengapa entalpi hidrasi Na+ (- 405 kJ/mol) sedikit lebih negatif dibandingkan
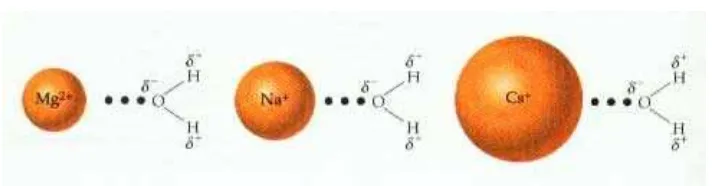
dengan Cs+ (- 263 kJ/mol), sedangkan Mg2+ jauh lebih negatif (- 1922kJ/mol)
dibandingkan dengan Na+ atau Cs+.
Kekuatan atraksi ion-dipol bergantung pada ukuran ion bermuatan dan besarnya dipol dan
berbanding terbalik pada jarak keduanya. Jari-jari ion Na+ = 116 pm, Cs+ = 181 pm, dan
Mg2+ = 86 pm. Dari harga jari-jari tersebut jarak antara pusat muatan positif ion logam dan
kutub negatif dari dipol air : Mg2+ < Na+ < Cs+
Gambar 13.4. Jarak antar pusat ion logam dengan dipol negatif molekul air
Energi hidrasi berbanding terbalik ( energi hidrasi Mg2+ paling negatif. Selain itu, Mg2+
memiliki muatan 2+, sedangkan ion lainnya bermuatan 1+. Ini berarti entalpi hidrasi Mg2+
lebih negatif dibandingkan dengan kedua ion lainnya.
Interaksi antar molekul dengan dipol permanen
Apabila molekul polar bertemu dengan molekul polar yang sejenis atau berbeda, kedua
molekul tsb. dapat berinteraksi. Kutub positif dari molekul yang satu berikatan dengan
kutub negatif dari molekul yang lain (Gambar 13.5).
Gambar 13.5. Atraksi dipol - dipol
Terjadinya atraksi dipol-dipol mempunyai efek yang penting terhadap sifat zat.
Pentingnya gaya tarik antarmolekul terhadap penguapan cairan atau kondensasi gas. Pada
kedua proses tersebut terjadi perubahan energi. Penguapan membutuhkan tambahan panas
(entalpi penguapan ∆H vap.). Nilai energi penguapan adalah positif, artinya penguapan
merupakan proses endoterm. Perubahan entalpi untuk proses kondensasi, kebalikan proses
Entalpi penguapan mengukur kekuatan gaya tarik antarmolekul dalam keadaan cair. Untuk mengubah dari fasa cair menjadi gas, dibutuhkan tambahan energi untuk
mengatasi gaya tarik antarmolekul, sehingga molekul terpisah dan lolos menjadi uap.
Semakin kuat gaya tarik antarmolekul cairan, semakin besar pula energi yang dibutuhkan
untuk memisahkan molekul. Berarti senyawa polar memiliki nilai entalpi penguapan yang
lebih besar dibandingkan senyawa nonpolar dengan massa yang sama.
Titik didih cairan juga berkaitan dengan gaya tarik antarmolekul. Bila temperatur dinaikan, molekul mendapatkan tambahan energi kinetika sampai akhirnya setelah
mencapai titik didihnya molekul mempunyai energi kinetika yang cukup untuk mengatasi
gaya tarik antarmolekul. Makin kuat gaya tarik antarmolekul, titik didih semakin tinggi.
Gaya antarmolekul juga mempengaruhi kelarutan. Pengamatan secara kualitatif terhadap kelarutan adalah ”like dissollves like”. Artinya molekul polar larut dalam pelarut polar,
dan molekul nonpolar larut dalam pelarut nonpolar. Molekul polar tak dapat larut dalam
pelarut nonpolar atau molekul nonpolar tak dapat larut dalam pelarut polar.
Contoh : air dan etanol (C2H5OH) dapat dicampur dalam segala perbandingan
membentuk campuran homogen. Sebaliknya air sangat tidak larut dalam gasolin.
Perbedaan ini disebabkan karena air merupakan molekul polar, sedangkan molekul
hidrokarbon di dalam gasolin ( misalkan oktana C8H18) adalah nonpolar. Interaksi antara
air-etanol cukup kuat, sehingga energi untuk memutuskan ikatan air berasal dari energi
atraksi antara 2 molekul polar. Sebaliknya, atraksi antara air-hidrokarbon adalah lemah.
Molekul hidrokarbon tak dapat merusak atraksi air-air yang kuat.
Ikatan hidrogen
Hidrogen fluorida dan beberapa senyawa lainnya dengan ikatan O-H atau N-H
mempunyai kekecualian sifat. Hal ini dapat dilihat dari hasil pengujian titik didih senyawa
hidrogen dari unsur golongan 4A sampai 7A. Umumnya, titik didih senyawa hidrogen
dengan unsur segolongan bertambah dengan semakin besarnya massa molar.
Contoh : titik didih senyawa hidrogen dari unsur golongan 4A (CH4, SiH4, GeH4, SnH4).
Efek yang sama juga terlihat pada molekul yang lebih berat , yaitu senyawa hidrogen dari
unsur golongan 5A, 6A, dan 7A. Akan tetapi titik didih NH3, H2O dan HF sangat
menyimpang dari ketentuan yang berdasarkan massa molar. Titik didih NH3 dan HF jauh
lebih besar daripada yang diharapkan berdasarkan massa molar.
Oleh karena titik didih suatu zat bergantung terhadap kekuatan gaya tarik
tarik antarmolekul yang kuat. Gaya tarik tsb. disebabkan oleh adanya ikatan hidrogen,
yaitu interaksi dipol-dipol khusus yang menyangkut ikatan polar H-X.
Gambar 13.6. Ikatan hidrogen
Ikatan dipol ditimbulkan sebagai akibat adanya perbedaan kelektronegatifan antara
atom-atom yang berikatan. Keelektronegatifan N (3,0), O (3,5), dan F (4,0) merupakan
yang tertinggi dari semua unsur, sedangkan keelektronegatifan hidrogen jauh lebih rendah
(2,1). Adanya perbedaan keelektronegatifan yang besar berarti ikatan N-H, O-H, dan F-H
sangat polar. Pada ikatan antara H dengan N, O, atau F, unsur yang memiliki
keelektronegatifan lebih besar relatif bermuatan negatif, sedangkan atom hidrogen relatif
bermuata positif.
Gaya Dispersi : Interaksi dipol induksi
Gaya dispersi terdapat dalam semua molekul. Gaya tersebut bersifatnya
elektrostatik dan berasal dari atraksi dipol induksi. Gaya ini dapat menerangkan
bagaimana molekul nonpolar seperti iodine I2, dapat berubah menjadi padatan pada
temperatur kamar atau bagaimana I2 dapat larut dalam air atau etanol.
Besarnya kekuatangaya dispersi dimulai dari molekul yang sangat lemah sampai
sangat kuat . Contoh pada HCl, sekitar 20% dari gaya antarmolekulnya adalah atraksi
dipol-dipol dan 80% nya adalah gaya dispersi.
Interaksi antara molekul polar dengan nonpolar
Kelarutan oksigen dalam air sangat kecil, dengan konsentrasi sekitar 10 ppm ( atau sekitar
0,001% berat). Hal ini penting untuk diketahui, karena mikroorganisme menggunakan
oksigen untuk merubah zat organik yang larut dalam air menjadi senyawa yang lebih
sederhana. Jumlah oksigen yang dibutuhkan untuk mengoksidasi sejumlah zat organik
disebut BOD (biological oxygen demand). Air yang sangat tercemar mengandung
Molekul O2 yang nonpolar dapat larut dalam air yang polar, karena molekul polar
seperti air dapat menginduksi atau menciptakan dipol pada molekul yang tidak memiliki
dipol permanen. Gambar 13.7 menggambarkan molekul air yang polar dapat menginduksi
dipol pada molekul nonpolar seperti O2.
Gambar 13.7 Induksi dipol air dengan molekul O2.
Pada awalnya, awan elektron pada molekul O2 (gas) terdistribusi secara merata
diantara kedua atom oksigen.Bila kutub negatif pada molekul H2O mendekati O2, awan
elektron O2 akan terdistorsi. Molekul O2 menjadi polar, karena molekul air yang polar
dapat menginduksi dipol di dalam O2 yang nonpolar. Akibatnya molekul H2O dan O2
dapat saling tarik menarik walaupun lemah. Oksigen dapat larut dalam air karena ada gaya
tarik antara dipol permanen dengan dipol induksi (gaya dipol/dipol induksi).
Proses menginduksi dipol disebut polarisasi, dan derajat awan elektron suatu atom (misalkan Ne atau Ar) atau molekul (misalkan O2, N2, atau I2) dapat didistorsikan
untuk membentuk dipol bergantung pada polarizability atom atau molekul. Elektron valensi dari atom atau molekul yang besar, seperti I2, dapat dipolarisasi atau didistorsi
lebih mudah dibandingkan dengan elektron pada atom atau molekul yang lebih kecil,
seperti He atau H2. Pada atom atau molekul yang lebih kecil, elektron valensi lebih dekat
ke inti dan lebih kuat terikat oleh inti. Umumnya, untuk senyawa deret analog, seperti
halogen atau alkana, semakin besar massa molar molekul semakin besar polarizability.
Kelarutan beberapa gas di dalam air dapat dilihat pada Tabel 13.3
Tabel 13.3 Kelarutan beberapa gas dalam air
Gas Massa molar Kelarutan pada 20OC
(g/mol) (g gas/100 g air)
H2 2,01 0,000160
N2 28,0 0,000190
Bila massa molar gas semakin besar, polarizability awan elektron makin besar, dipol
makin mudah diinduksi, dan kekuatan interaksi dipol/dipol induksi bertambah. Berarti
kelarutan zat nonpolar dalam zat polar umumnya meningkat dengan makin besarnya
massa.
Interaksi antar molekul nonpolar
Iodine I2, pada STP berupa padatan, hal ini disebabkan karena antar iodine yang nonpolar
terdapat gaya antarmolekul . Kekuatan gaya ini dapat dilihat dari nilai entalpi penguapan
zat pada titik didih. N2, O2, dan CH4 mempunyai gaya antarmolekul yang sangat lemah,
sehingga mempunyai titik didih dan entalpi penguapan yang sangat rendah. I2 dan benzena
mempunyai gaya antarmolekul yang kuat, sehingga mempunyai titik didih dan entalpi
penguapan tinggi.
∆H (penguapan) Titik didih
Senyawa (kJ/mol) (OC)
N2 5,58 - 196
O2 6,82 - 183
I2 41,95 185
CH4(metana) 8,2 - 161,5
C6H6(benzena) 30,7 80,1
Dua molekul nonpolar dapat saling tarik menarik, hal ini akibat elektron di dalam atom
atau molekul yang selalu melakukan gerakan yang konstan. Umumnya, awan elektron
disekitar atom adalah bulat (Gambar 13.8). Bila dua atom atau molekul nonpolar saling
mendekati, maka akan timbul gaya tolak atau gaya tarik, masing-masingnya antara
elektron-elektron atau elektron-inti dan menyebabkan terjadinya distorsi awan elektron
membentuk dipol induksi yang tak permanen. Dipol induksi ini menyebabkan gaya tarik
antarmolekul. Berarti, gaya tarik antarmolekul nonpolar dalam cairan dan padatan adalah
Gambar 13.8 Interaksi dipol induksi
Perlu ditekankan kembali, gaya dispersi terdapat pada semua molekul polar
maupun nonpolar. Akan tetapi, antara molekul nonpolar hanya terdapat gaya dispersi.
Soal 13.2 Gaya antarrmolekul
Gaya antarrmolekul apakah yang bekerja pada : (a) metana (CH4) cair, (b) campuran air
(H2O) dan metanol (CH3OH) (c) Larutan litium klorida (LiCl) dalam air. Serta buat urutan
kekuatan interaksinya.
Jawab:
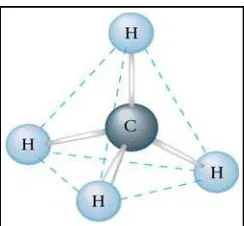
(a) Metana CH4 merupakan molekul kovalen sederhana. Berdasarkan struktur Lewisnya
metana berupa molekul tetrahedral dan nonpolar. Berarti molekul metana berinteraksi
melalui gaya dipol induksi (Gambar 13.9).
Gambar 13.9a. Geometri molekul CH4.
(b). Air dan metanol, keduanya polar dan mempunyai ikatan O-H. Berarti keduanya
Gambar 13.9b. Ikatan hidrogen
(c). LiCl merupakan senyawa ionik yang terdiri dari ion Li+ dan Cl-. Air adalah molekul
polar, berarti gayanya adalah ion-dipol.
Urutan kekuatan interaksinya :
CH4 cair < H2O dan CH3OH < LiCl dalam H2O
13.3 SIFAT CAIRAN Entalpi penguapan
Penguapan merupakan proses endoterm, karena diperlukan energi untuk mengatasi gaya
tarik antarmolekul. Energi panas yang dibutuhkan untuk menguapkan cairan disebut
entalpi penguapanmolar ∆HOvap(dalam satuan kilojoule per mol).
penguapan
Cairan uap
Energi panas diserap oleh cairan
Bila antara molekul uap dan permukaan cairan terjadi kontak, molekul uap akan kembali
masuk ke dalam fasa cair, dan proses ini disebut kondensasi. Kondensasi merupakan proses eksoterm, dilepaskan energi ke lingkungan. Nilai entalpi kondensasi sama dengan
entalpi penguapan tetapi berlawanan tanda. Contoh : Entalpi kondensasi 1 mol air pada
100OC = - 40,7 kJ, maka entalpi penguapan 1 mol air pada 100OC = + 40,7 kJ.
Terdapat hubungan antara titik didih, entalpi penguapan, dan massa molar.Titik
didih cairan nonpolar (seperti hidrokarbon, gas di udara, dan halogen) bertambah dengan
semakin besarnya massa atom atau massa molekul, karena gaya dispersi antarmolekul
semakin besar. Alkana juga menunjukan kecenderungan yang sama. Titik didih dan
entalpi penguapan hidrogen halida (HX, dimana X = Cl, Br dan I) makin besar dengan
bertambahnya massa molar. Untuk molekul tersebut, bekerja gaya dipol-dipol dan gaya
dispersi dimana semakin besar massa molar gaya dispersi semakin berperan. Harga entalpi
Soal 13.3 : entalpi penguapan
Bila 1,00 L air diuapkan di dalam pan pada 100OC, berapa panas yang dibutuhkan untuk
menguapkan air tersebut ?. ∆Hvap air = + 40,7 kJ/mol pada 100oC.
Jumlah energi yang dibutuhkan untuk penguapan = 53,2 mol X
mol
(ekivalen dengan ¼ energi yang dihasilkan dari makanan setiap hari).
Bila kita berolahraga dengan kuat, tubuh akan berkeringat. Untuk proses penguapan panas
yang dibutuhkan diambil dari tubuh, akibatnya tubuh merasa dingin. Bila uap air di udara
berkondensasi menjadi air hujan, maka panas yang dilepaskan 2,0x108 kJ. Panas ini
ekivalen dengan panas dari 50 ton dinamit.
Tekanan uap
Bila suatu cairan ditempatkan dalam wadah tertutup, cairan akan menguap sampai
akhirnya dicapai kecepatan penguapan sama dengan kecepatan kondensasi. Keadaan ini
disebut kesetimbangan dinamik.
Cairan ↔ uap
Pada wadah terbuka, uap yang terbentuk berdifusi menjauhi permukaan cair,
kesetimbangan tak pernah terjadi dan uap terus terbentuk hingga semua cairan menguap.
Saat kesetimbangan cair – uap telah dicapai, tekanan yang dihasilkan oleh uap
Gambar 13.11 Tekanan uap
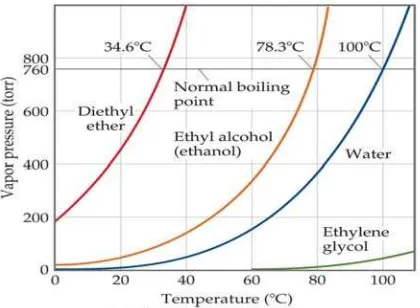
Tekanan uap semakin besar dengan semakin meningkatnya temperatur (Gambar 13.12).
Semakin tinggi temperatur, semakin banyak molekul yang memiliki energi untuk berubah
menjadi uap. Oleh karena itu tekanan uap semakin besar apabila temperatur dinaikan.
Contoh pada 25OC tekanan uap air 24 mm Hg, sedangkan pada 60OC adalah 149 mm Hg.
Gambar 13.12 Kurva tekanan uap
Soal 13.4 : tekanan uap
Bila sebanyak 2,00 L air ditempatkan dalam ruangan tertutup dengan volume 4,33x104 L,
kemudian diamati jumlah air yang menguap. Apakah semua air akan menguap pada
temperatur 25OC ?. (Pada 25OC, densitas air 0,997 g/mL dan tekanan uap 23,8 mm Hg).
Jawab :
Pertama, harus dihitung jumlah air yang harus menguap dalam ruangan 4,33x104 pada
25oC, sehingga menghasilkan tekanan 23,8 mm Hg. Dengan menggunakan hukum gas
Berarti hanya separuh air yang dibutuhkan untuk menghasilkan tekanan uap sebesar 23,8
mm Hg pada ruangan tsb. dan 25OC.
Hubungan antara tekanan uap cairan dengan temperatur dinyatakan dengan
persamaan Clausius-Clapeyron :
ℓn P = - (∆Hvap / RT) + C
P = tekanan uap T = temperatur Kelvin R = konstanta gas
∆Hvap = entalpi penguapan cairan
C = konstanta
Persamaan ini digunakan untuk menentukan ∆Hvap. Plot ℓn P terhadap 1/T, menghasilkan
garis lurus dengan slope - (∆Hvap / R).
Titik didih
Bila air ditempatkan dalam beaker terbuka, maka massa dari udara akan menekan
permukaan air. Dengan pemanasan, semakin banyak uap air yang tebentuk dan akan
mendorong molekul udara menjauhi permukaan. Akhirnya pada temperatur tertentu
tekanan uap cairan sama dengan tekanan udara. Pada keadaan ini, gelembung uap mulai
terbentuk di dalam cairan dan cairan mendidih.
Titik didih suatu cairan adalah temperatur saat tekanan uap sama dengan tekanan
luar. Bila tekanan luar 1 atm, disebut titik didih normal. Terdapat hubungan antara titik didih normal, tekanan uap dan gaya antarmolekul.
Titik didih normal air 100OC, dan dibeberapa tempat di Amerika air mendidih pada
temperatur sangat mendekati 100OC. Pada tempat yang lebih tinggi seperti Salt Lake City,
mempunyai tekanan udara sekitar 650 mmHg, sehingga air mendidih pada temperatur
95OC. Memasak makanan lebih lama matang di Salt Lake City dibandingkan di New
37
normal boiling point is the temperature at which a liquid boils under one atm of pressure.
liquid
pressure = 1 atm
vapor pressure = 1 atm
BOILING
Gambar 5.13 Titik didih
Temperatur dan tekanan kritis
Dari kurva tekanan uap pada Gambar 13.12, terlihat seolah-olah tekanan uap akan terus
naik tanpa batas, padahal tidak demikian. Pada temperatur dan tekanan tertentu, batas
antarmuka cair dan uap hilang. Titik ini disebut titik kritis. Temperatur pada titik kritis disebut temperatur kritis dan tekanannya disebut tekanan kritis. Zat yang berada pada
kondisi kritis disebut fluida superkritis, yaitu seperti gas pada tekanan tinggi yang densitasnya sama dengan cairan, sementara viskositasnya tetap mirip gas.
Untuk sebagian besar zat, titik kritis terjadi pada kondisi temperatur dan tekanan
tinggi. Contoh, air mempunyai temperatur kritis 374OC dan tekanan kritis 217,7 atm
(Tabel 13.5). Pada tekanan tinggi, molekul air ditekan hingga jaraknya berdekatan seperti
pada cairan. Akan tetapi pada temperatur tinggi, berarti molekul – molekul ini
mempunyai energi kinetika yang cukup untuk mengatasi gaya tarik antarmolekul. Berarti,
fluida kritis mempunyai susunan molekul yang kuat dan rapat seperti cairan, tetapi gaya
tarik antarmolekul yang merupakan karakteristik cairan lebih kecil daripada energi
kinetika partikel.
Fluida superkritis, seperti air dan CO2, sangat berguna sekali karena mempunyai
kemampuan untuk melarutkan material yang secara normal tak larut. Fluida superkritis
CO2 tidak larut dalam air dan senyawa polar lainnya seperti gula, tetapi larut dalam
minyak nonpolar yang merupakan senyawa yang menyebabkan rasa dan bau dalam
makanan. Oleh karena itu, sekarang perusahaan makanan menggunakan superkritis CO2
untuk mengekstrak kafein dari kopi.
Senyawa TK (OC) PK (atm)
CH4 (metana) - 82,6 45,4
C2H6 (etana) 32,3 49,1
C3H8 (propana) 96,7 41,9
C4H10 (butana) 152,0 37,3
CCl2F2 (CFC-12) 111,8 40,9
NH3 132,4 112,0
H2O 374,0 217,7
CO2 30,99 72,8
SO2 157,7 77,8
The Critical Phenomenon of SF6
T < Tc T > Tc T ~ Tc T < Tc
11.8
Gambar 13.14. Fluida superkritis SF6.
Tegangan permukaan, aksi kapiler dan viskositas
Molekul di dalam cairan, mengalami interaksi dengan semua molekul yang
mengelilinginya. Sebaliknya, molekul pada permukaan cairan hanya berinteraksi dengan
molekul yang berada di bawah permukaan (Gambar 13.15). Akibatnya, molekul
permukaan mengalami gaya tarik ke bawah, dan permukaan menjadi tegang seolah cairan
mempunyai kulit. Kekuatan kulit cairan ini, di ukur besarannya melalui besarnya
Properties of Liquids
Surface tensionis the amount of energy required to stretch or increase the surface of a liquid by a unit area.
Strong
shape that liquids form when dropping through the air: The molecules are all being pulled toward the center.
Gambar 13.16 Tetesan cairan
Adanya tegangan permukaan menyebabkan tetesan air berbentuk bulat, karena bulatan
mempunyai luas permukaan yang lebih kecil dibandingkan bentuk lainnya dengan volume
yang sama.
Aksi kapiler sangat berkaitan dengan tegangan permukaan. Bila sebuah pipa kapiler dicelupkan ke dalam air, maka air akan naik di dalam pipa kapiler, seperti halnya
air naik dalam secarik kertas. Oleh karena gelas terdapat ikatan Si-O yang polar, maka
molekul air yang juga polar akan mengalami gaya adhesi dengan gelas. Gaya adhesi yang
kuat ini akan berkompetisi dengan gaya kohesi antar molekul air. Berarti sebagian molekul
air akan menempel pada gelas dan sebagian lain antar molekul air, membentuk jembatan
kembali ke air. Tegangan permukaan air (dari gaya kohesi) cukup kuat untuk menarik
cairan naik di dalam pipa kapiler. Gaya ini menyebabkan permukaan air cekung di dalam
gelas atau dalam tabung reaksi.
Beberapa cairan mempunyai gaya kohesi yang lebih besar dibandingkan gaya adhesi
dengan gelas. Contoh air raksa, permukaan cairan akan turun di dalam pipa kapiler dan
Viskositas adalah tahanan cairan untuk mengalir. Bila air dituang dari gelas, gelas akan kosong dengan cepat. Sebaliknya, bila yang dituang adalah madu, gelas akan kosong
dalam waktu yang lebih lama. Selain gaya antarmolekul, ada faktor lain yang
mempengaruhi viskositas. Contoh olive oil yang terdiri dari rantai atom karbon dan
oksigen yang sangat panjang memiliki viskositas 70 kali lebih besar dibandingkan dengan
etanol, molekul kecil yang hanya terdiri dari 2 atom karbon, 5 atom hidrogen dan 1 atom
oksigen. Molekul natural oil yang panjang, lentur dan saling berkaitan satu sama lain,
semakin panjang rantainya, semakin berkaitan satu sama lain dan viskositas makin besar.
Juga makin panjang molekul, gaya antarmolekul semakin besar, karena semakin banyak
atom yang saling tarik menarik.
Soal 13.5 Viskositas
Gliserol (HOCH2CHOHCH2OH) digunakan dalam kosmetik. Apakah viskositas gliserol
lebih besar atau lebih kecil dibandingkan dengan etanol CH3CH2OH ?.
13.4 LOGAM DAN PADATAN IONIK
Banyak jenis padatan dijumpai di sekitar kita, seperti terlihat pada Gambar 13.24.
Gambar 13.24.
a. Garam, NaCl, padatan ionik.
b. Aluminium, padatan logam.
c. Silikon, kerangka padatan.
d. Botol semprot, polietilen,
padatan amorf.
Kimia zat padat merupakan ilmu
pengetahuan yang maju pesat, karena berkaitan dengan pengembangan material baru.
Kisi kristal dan unit sel atom logam
Molekul gas dan cairan bergerak secara kontinyu dan random, juga berotasi dan
Molekul, atom atau ion padatan tak dapat bergerak (walaupun bervibrasi dan
kadang-kadang berotasi), sehingga susunan atom atau molekulnya membentuk pola yang teratur.
Tabel 13.6 Struktur dan sifat dari berbagai tipe zat padat
________________________________________________________________________ _
Tipe Contoh Unit Struktur
Ionik NaCl, K2SO4, CaCl2 Ion positif dan negatif
(NH4)3PO4
Logam Besi, Perak, Tembaga, Atom logam (ion logam positif
yang
logam paduan dikelilingi oleh lautan elektron
Molekul H2, O2, I2, H2O, CO2, CH4 Molekul saling berikatan dengan
Ikatan kovalen
Kerangka Grafit, Intan, Kuarsa. Atom berikatan membentuk
kerang ka satu, dua atau tiga dimensi
Amorf Gelas, polietilen, nilon Kerangka yang berikatan
kovalen
(Glassy) tanpa aturan dan batasan tertentu
Struktur padatan dapat digambarkan sebagai kisi atom, ion atau molekul tiga
dimensi. Unit berulang terkecil dari susunan atom, ion atau molekul dalam kristal padat
disebut unit sel.
Gambar 13.17. Unit sel dari padatan datar dua dimensi yang terbentuk dari lingkaran atom
Struktur makroskopik kristal dari susunan atom yang indah menyatakan bahwa kristal
tersebut mempunyai suatu simetri dalam, simetri adalah merupakan ion-ion yang ikut serta
membentuk padatan. Struktur padatan dapat digambarkan dalam kisi tiga dimensi atom,
ion atau molekul. Untuk menggambarkan struktur, perlu digambarkan dahulu unit sel nya.
Bagi padatan kristal, unit sel adalah bagian terkecil dari unit pengulangan yang
Umumnya dalam kisi kristal terdapat beberapa unit sel yang mungkin terbentuk. Contoh
pada Gambar 13.17, segi empat pada gambar di atas adalah unit sel. Kisi keseluruhan
dibangun dari gabungan unit sel secara sisi dengan sisi (edge to edge). Unit sel juga
mencerminkan ”stoikiometri” padatan. Unit sel segi empat (hijau), terdiri dari seperempat
dari empat buah bulatan putih dan satu bulatan hitam, sehingga total terdiri dari 1 bulatan
putih dan 1 bulatan hitam per unit sel. Unit sel dari kisi kristal dua dimensi lainnya juga
dapat dengan mudah digambarkan, seperti segi empat (merah), yang terdiri dari satu
lingkaran putih penuh, atau jajaran genjang (kuning).
Secara konvensional unit sel digambarkan dengan meletakkan atom atau ion pada
titik-titik kisi, yaitu pada sudut-sudut kubus atau bentuk geometrik lainnya yang menyusun
unit sel. Kisi kristal tiga dimensi dapat dibangun dari gabungan unit sel tiga dimensi,
seperti blok bangunan (building block). Ada 7 macam unit sel (Gambar 13.18), yaitu
kubus, tetragonal, ortorombik, trigonal, heksagonal, monoklinik dan triklinik.
11.4
Gambar 13.18 Unit sel dari 7 sistim kristal
Unit sel yang paling sederhana adalah kubus. Selanjutnya hanya akan dibicarakan unit sel
kubus. Ada 3 buah unit sel kubus, yaitu primitive atau kubus sederhana (sc), kubus
41
unit cells:
contains 2 atoms contains 1 atomGambar 13.19 Unit sel kubus
Ketiganya memiliki 8 atom atau ion sejenis pada pojok unit sel kubus. Akan tetapi pada
struktur bcc dan fcc selain kedelapan partikel tersebut, terdapat tambahan partikel sejenis .
Pada struktur bcc terdapat tambahan partikel pada pusat bidang kubus, sedangkan pada
struktur fcc terdapat tambahan 6 partikel, masing-masing pada pusat sisi kubus.
Logam-logam memiliki struktur kubus, contoh struktur bcc : Logam-logam alkali, struktur fcc : nikel,
tembaga, aluminium.
Saat unit sel kubus sederhana (bc) bergabung membentuk kristal 3 dimensi,
masing-masing partikel pojok mengadakan sharing dengan 8 kubus (Gambar 13.20). Oleh
karena itu, hanya 1/8 bagian dari masing-masing partikel pojok berkontribusi di dalam
unit sel. Berarti jumlah partikel di dalam unit sel kubus bc = (8 pojok kubus)(1/8
masing-masing partikel pojok di dalam unit sel) = 1 partikel per unit sel.
Shared by 8 2
unit cells
Shared by unit cells
Gambar 13.20. Penggunaan Atom pada kubus pusat sudut dan muka
Pada struktur fcc, selain memiliki 8 partikel pojok juga terdapat 6 partikel pada
pusat sisi kubus. Masing-masing partikel pada pusat sisi kubus dipakai bersama dengan
kubus lainnya. Artinya, masing-masing menyumbangkan ½ partikel per sisi kubus. Berarti
jumlah partikel berpusat muka di dalam unit sel fcc = (6 sisi kubus)(1/2 partikel di dalam
unit sel) = 3 partikel berpusat muka per unit sel. Total ada 4 atom atau ion per unit sel, 1
berasal dari kontribusi atom atau ion pojok ditambah 3 dari kontribusi atom atau ion pada
pusat muka.
Teknik x-ray crystallography dapat digunakan untuk menentukan struktur
kristalin. Setelah struktur diketahui, kemudian dikombinasikan dengan informasi yang
diperoleh dari percobaan lain untuk menghitung parameter yang sangat berguna yakni
jari-jari atom.
Soal 13.6 Penentuan jari-jari atom dari pengukuran kisi kristal.
Aluminium memiliki densitas 2,699 g/cm3 dengan struktur fcc. Hitunglah jari-jari atom
aluminium.
Jawab :
Tahapan dalam menyelesaikan soal di atas :
Tahap 1 : menghitung massa unit sel
26,98 g 1 mol 4 atom
Massa unit sel = --- X --- X --- = 1,792x10-22 g 1 mol 6,022x1023 unit sel
Tahap 2 : Menghitung volume unit sel
1,792x10-22 g 1 cm3
Volume unit sel = --- X --- = 6,640x10-23 cm3 / unit sel 1 unit sel 2,699 g
Tahap 3 : Menghitung Menghitung panjang rusuk unit sel
Panjang rusuk unit sel = 3 6,640x10-23 cm3 = 4,049x10-8 cm
Tahap 4 : Menghitung jari-jari atom
Atom pusat menyentuh masing-masing atom pojok, sehingga jarak diagonal pada sisi = 4x
jari-jari bulatan atom.
Diagonal sisi sel = 4 x (jari-jari atom Al)
Jarak diagonal dapat dicari dari segitiga ;
(Jarak diagonal)2 = (rusuk)2 + (rusuk)2 = 2 x (rusuk)2
Jarak diagonal = 2x ( rusuk)
= 2x (4,049x10-8 cm) = 5,727x10-8 cm
Jarak diagonal dibagi 4 = jari-jari atom :
(5,727x10-8 cm)
Jari-jari atom Al = --- = 1,432x10-8 cm 4
= 143,2 pm
Contoh 13.7 Struktur besi padat
Besi memiliki densitas 7,8740 g/cm3, dan jari-jari atom besi 126 pm. Buktikan bahwa
struktur besi padat adalah kubus berpusat bidang (bcc).
Jawab :
Unit sel bcc mengandung 2 atom. Apabila dengan menggunakan data densitas besi dan
jari-jari atom didapatkan 2 atom per unit sel, berarti unit selnya adalah bcc.
Step 1. Mencari panjang rusuk kubus
(Jarak diagonal bidang kubus)2 = (rusuk sel)2 + (diagonal sisi)2
= 3 X (rusuk sel)2
• Jarak diagonal bidang kubus = 3 X (rusuk sel)
Jarak diagonal bidang kubus = 4 X jari-jari atom
Gambar diagonal kubus = 4 x jari-jari atom
4 X jari-jari atom = 3 X (rusuk sel)
4 X jari-jari atom 4 X 126 pm
Panjang rusuk sel = = = = 291 pm = 2,91 X 10-8 cm 3 3
Step 2. Menghitung volume unit sel (kubus)
Volume unit sel = (2,91 x 10-8 cm)3 = 2,46 x 10-23 cm3
Step 3. Menghitung massa unit sel
7,8740 g
Massa unit sel = (2,46 x 10-23 cm3) X = 1,94 X 10-22 g Cm3
Step 4. Menghitung massa atom besi, kemudian dibandingkan dengan massa unit sel 55,85 g 1 mol
Massa 1 atom Fe = X = 9,274 X 10-23 g / atom 1 mol 6,022 X 1023 atom
1,94 X 10-22 g / unit sel
--- = 2,09 atom per unit sel 9,274 X 10-23 g / atom
Struktur dan formula padatan ion
Penentuan kisi dan jumlah dan lokasi hole merupakan kunci untuk mengerti hubungan
antara struktur kisi dengan formula garam.
Contoh senyawa ionik CsCl (Gambar 13.21)
18 Other types of forces holding solids together:
ionic:
There are no individual molecules here.
“charged ions stuck together by their charges”
Gambar 13.21 Struktur kristal CsCl, ZnS dan CaF2
Ion Cl membentuk unit sel kubus sederhana, sedangkan ion Cs menempati hole yang
berada pada pusat kubus. Berarti pada kisi ini ion Cs+ dikelilingi oleh 8 ion Cl- tetangga
terdekat.
Contoh NaCl
NaCl Structure
Gambar 13.22 Struktur Natrium klorida
Ion Cl- tersusun di dalam unit sel fcc, dan ion Na+ tersusun dengan cara teratur diantara
ion Cl-. Masing-masing ion Na+ dikelilingi oleh 6 ion Cl- membentuk geometri oktahedral
(Gambar 13.31c). Dengan demikian ion Na+ berada dalam struktur oktahedral.
13.5 MATERIAL PADAT JENIS LAIN
Sejauh ini yang dibicarakan adalah struktur logam dan padatan ionik sederhana. Berikut
ini, akan dibicarakan mengenai kategori padatan lainnya, yaitu padatan molekular, padatan
network dan padatan amorf.
Molecular solid
Molekul kovalen, seperti H2O dan CO2 pada kondisi tertentu berada dalam keadaan padat.
Pada senyawa ini, molekulnya (bukan atom atau ion) sejajar dengan susunan teratur dalam
Gambar 13.23. Struktur es
Bagaimana molekul tersusun di dalam kisi kristal bergantung pada bentuk molekul
dan tipe gaya antarmolekul. Molekul cenderung menyusun diri dengan cara yang paling
efisien, yaitu tersusun untuk mengisi ruangan secara efisien, jadi sedekat mungkin, dan
berurutan atau sejajar yang memaksimalkan gaya tarik antarmolekul. Struktur air dibangun
untuk mendapatkan gaya tarik antarmolekul maksimum melalui ikatan hidrogen. Molekul
asam organik seringkali padatannya berupa dimer, yaitu dua molekul yang dihubungkan
dengan ikatan hidrogen.
Jaringan Padatan (Network Solid)
”Network solid” atau jaringan padatan, adalah zat yang tersusun dari jejaring atom-atom
21
Covalent Network: (diamonds, quartz) very
1.54 Å
3.35 Å 1.42 Å
strong.
What type of hybridization is present in each?
Gambar 13.24. (a) Padatan molekul (b) Network solid
Padatan Amorf
Karakteristik dari padatan kristal murni (logam, padatan ionik, padatan molekul)
adalah meleh pada temperatur tertentu. Contoh: air meleh pada 0oC, aspirin pada 135oC,
timbal pada 327,5oC, dan NaCl pada 801oC. Bila dipanaskan es pada 0oC mulai meleleh
dan temperatur tetap pada 0 oC sampai semua padatan telah berubah menjadi cair. Hanya
setelah semua es meleleh, temperatur akan naik kembali. Oleh karena nilainya spesifik dan
reprodusibel, sehingga titik leleh sering digunakan untuk mengidentifikasi senyawa kimia.
Banyak padatan yang sering dijumpai sehari-hari tidak mempunyai sifat tsb.
Sebagai contoh gelas. Bila gelas dipanaskan, akan meleleh pada range temperatur yang
luas. Sifat ini sangat berguna bagi artisans dan craftsmen yang dapat menciptakan produk
An amorphous soliddoes not possess a well-defined arrangement and long-range molecular order.
A glass is an optically transparent fusion product of inorganic
materials that has cooled to a rigid state without crystallizing
Crystalline quartz (SiO2)
Non-crystalline
quartz glass 11.7
Gambar 13.25. Padatan kristal kuarsa SiO2 dan amorf SiO2.
13.6 SIFAT FISIKA ZAT PADAT
Titik leleh padatan atau titik beku cairan adalah temperatur saat fasa padat dan cairan berada dalam kesetimbangan. Transformasi padatan menjadi cair (pelelehan)
membutuhkan energi yang disebut entalpi fusion (kilojoule per mol).
Energi panas yang diabsorbsi saat pelelehan = Entalpi fusi = ∆Hfusi
Energi panas yang dilepaskan saat membeku = Entalpi kristalisasi = - ∆Hfusi
Titik leleh yang rendah berarti harga entalpi fusionnya juga rendah, sebaliknya titik leleh
M liquid is the temperature at which the solid and liquid phases coexist in equilibrium
Gambar 13.26. Pelelehan
Tabel 13.7 Titik leleh dan entalpi pelelehan beberapa padatan
Senyawa Titik Leleh
Padatan molekular : Molekul nonpolar
O2 - 219 0,440
F2 - 220 0,510 Hanya gaya dispersi
Cl2 - 102 6,41
Br2 - 7,2 10,8
Padatan molekular : Molekul Polar
HCl - 114 1,99
HBr - 87 2,41 Ketiga molekul HX memiliki gaya
dipol-dipol dan gaya dispersi yang
bertambahnya ukuran dan massa
molar
HI - 51 2,87
H2O 0 6,02 Ikatan Hidrogen
Padatan Ionik
NaF 996 33,4 Semua padatan ionik memiliki
extended ion – ion interaction.
NaCl 801 28,2 Catatan : Trendnya sama seperti
untuk energi kisi.
NaBr 747 26,1
NaI 660 23,6
Dari tabel 13.7 di atas terlihat bahwa :
(1) Logam yang memiliki titik leleh rendah, seperti logam alkali dan merkuri, memiliki
entalpi fusion yang rendah pula.
(2) Logam transisi mempunyai harga titik leleh dan entalpi fusi yang tinggi. Tungsten (W)
memiliki titik leleh tertinggi dan entalpi fusion tertinggi diantara semua unsur kecuali
carbon. Oleh karena itu, tungsten digunakan sebagai filamen dalam lampu pijar.
Sampai sekarang tak ada material yang sebaik W sejak ditemukan lampu pijar tahun
1908.
(3) Zat nonpolar yang membentuk molekul padat memiliki titik leleh rendah. Pada deret
molekul tersebut, titik leleh makin besar dengan semakin besarnya ukuran dan massa
molar. Semakin besar massa molar, gaya dispersi semakin besar. Akibatnya semakin
besar jumlah energi dibutuhkan untuk memutuskan gaya intermolekul dalam padatan,
hal ini tercermin dari semakin meningkatnya harga entalpi fusi.
(4) Titik leleh senyawa ionik lebih tinggi dibandingkan dengan titik leleh padatan molekul,
karena gaya ion-ion dalam padatan ionik sangat kuat dan energi kisi besar. Oleh karena
gaya ion-ion bergantung pada ukuran ion (seperti halnya pada muatan ion), maka ada
korelasi antara energi kisi dengan logam atau halogen dalam tabel periodik. Dengan
bertambahnya ukuran kation dari Li+ ke Cs+, energi kisi senyawa kation dengan halida
yang sama berkurang. Demikian pula semakin besar ukuran ion halida dari F- ke I-,
energi kisi dengan semakin besarnya ukuran ion, diikuti dengan berkurangnya titik
leleh dan entalpi fusi.
Sublimasi adalah perubahan langsung dari padatan menjadi gas.
Padat → gas energi panas yang dibutuhkan = ∆Hsublimasi
Sublimasi , seperti juga fusion dan penguapan, merupakan proses endoterm. Air yang
mempunyai entalpi sublimasi 51 kJ/mol, dapat diubah dengan sangat cepat dari padatan es
menjadi uap air. Contoh sifat ini adalah pada lemari es yang bebas dari terbentuknya
bunga es. Selama waktu tertentu, kompartemen pendingin (freezer) sedikit dihangatkan.
Molekul air yang dilepaskan dari permukaan es (tekanan uap es 4,60 mm Hg pada 0oC)
dihilangkan oleh arus udara yang ditiupkan ke dalam pendingin.
S
to sublime 1 mole of a solid.
ΔHsub = ΔHfus+ ΔHvap
( Hess’s Law)
Gambar 13.27. Sublimasi
Contoh 13.10 Panas penguapan dan pelelehan
Rubbing alcohol (2-propanol) membeku pada temperatur – 89,5oC dan mendidih pada
82,3oC. Berapa panas yang dibutuhkan untuk melelehkan 10,0 gram 2-propanol pada –
89,5oC, kemudian cairan yang terbentuk dipanaskan sampai titik didihnya, dan selanjutnya
diuapkan pada temperatur yang sama, ∆Hfusi = 5,37 kJ/mol ; kapasitas panas spesifik
Jawab :
Step 1 : panas yang dibutuhkan untuk melelehkan 10,0 g 2-propanol padat pada – 89,5oC.
10.0 g X
Step 2 : Panas yang dibutuhkan untuk menghangatkan cairan dari 89,5oC sampai 82,3oC.
10,0 g X
Step 3 : Panas yang dibutuhkan untuk menguapkan cairan pada 82,3oC.
10,0 g X
Diagram Fasa digunakan untuk mengilustrasikan kaitan antara fasa suatu materi dengan
temperatur dan tekanan.
E
Gambar 13.29 Diagram fasa air
Pada diagram fasa air dapat dilihat bahwa,
Garis A-D : pada kombinasi P dan T terjadi kesetimbangan fasa uap-cair
Garis A-B : pada kombinasi P dan T terjadi kesetimbangan fasa cair - padat
Garis dari titik A sampai ke titik D, menunjukkan adanya kesetimbangan antara fasa cair
dan uap, yang juga sama dengan kurva tekananan uap air. Titik didih air 100oC, yaitu
temperatur dimana tekanan uap nya adalah 1 atm.
Titik A, adalah titik dimana ketiga fasa berada dalam kesetimbangan, dan titik ini disebut
titik tripel. Titik tripel air terjadi pada P = 4,58 torr dan T = 0,0098oC.
Garis kesetimbangan padat-cair (A-B) untuk air memiliki slope negatif. Karena pada garis
ini tidak berhubungan dengan tekanan uap maka tekanan hanya tergantung pada tekanan
luar. Semakin besar tekanan luar, titik leleh semakin kecil. Setiap kenaikan tekanan 1 atm,
terjadi penurunan titik leleh air sebesar 0,01oC. Hal ini disebabkan karena volume es lebih
besar dibandingkan air, akibat struktur kisi es yang lebih terbuka dibandingkan air. Contoh
es akan meleleh bila diberi tekanan (Gambar 13.30).
Gambar 13.30. Struktur 3-dimensi es
(a). Es meleleh bila diberi tekanan. Suatu kawat tipis diletakan di atas es dan kedua ujung
kawat diberi beban. Tekanan yang yang dilakukan kawat terhadap es menyebabkan es
akan meleleh dan akhirnya kawat lolos melalui es.
(b). Model komputer permukaan es ( molekul air digambarkan dengan bulatan yang lebih
besar). Molekul pada layer 1 bervibrasi lebih cepat dibandingkan dengan pada layer 2
dan layer dibagian lebih dalam. Molekul air pada permukaan lebih bersifat cair
Kita dapat bermain ski atau skating di atas es, karena permukaan es agak meleleh
akibat tekanan pisau skating atau ski, atau permukaan es meleleh akibat panas yang terjadi
akibat gesekan/friksi. Akan tetapi alasan tersebut kurang memuaskan karena hanya dengan
berdiri atau meluncur di atas es dapat menghasilkan tekanan atau temperatur yang cukup
tinggi untuk terjadinya pelelehan. Keterangan yang lebih baik adalah molekul air pada
permukaan bervibrasi dengan cepat, sehingga permukaan es meleleh. Lapis pertama dan
kedua hampir seperti cairan (liquid-like) dan dengan alasan ini maka kita dapat bermain
ski atau skating di atas es.
Diagram fasa untuk CO2 terdapat pada Gambar 13.31. Perbedaan dengan diagram
fasa air adalah garis kesetimbangan padat-cair untuk CO2 memiliki slope positif. Densitas
CO2 padat lebih besar dibandingkan dengan CO2 cair, sehingga CO2 padat akan tenggelam
dalam wadah berisi CO2 cair. CO2 padat mengalami sublimasi langsung menjadi CO2 gas
pada temperatur kamar (pada 1 atm). Dengan alasan ini , maka CO2 disebut dry ice ;
terlihat seperti es tetapi tidak meleleh.
11.9
Effect of Increase in Pressure on the Melting Point of Ice and the Boiling Point of Water
![Gambar 13.3. Gambar [Co(H2O)4Cl2].2H2O yang berwarna coklat](https://thumb-ap.123doks.com/thumbv2/123dok/1755753.1582985/5.595.129.496.357.510/gambar-gambar-co-h-cl-yang-berwarna-coklat.webp)