PENGARUH PEMBERIAN PADA TIKUS JANTAN
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
PEMBERIAN AKUT JUS WORTEL (Daucus carota
PADA TIKUS JANTAN WISTAR : KAJIAN TERHADAP OR DAN KADAR KREATININ SERUM
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh : Daryono Thejo NIM : 068114073
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
2009
Daucus carota L.)
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
ii SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh : Daryono Thejo NIM : 068114073
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
Walaupun seseorang
tetapi malas dan tid
maka sesungguhnya,
lebih baik orang yan
tetapi berjuang dengan pe
Semoga Sang Triratna
Semoga semua makhluk hidup berbahagia
Papa dan Mam
v
HALAMAN PERSEMBAHAN
Walaupun seseorang hidup seratus tahun
tetapi malas dan tidak bersemangat,
maka sesungguhnya,
lebih baik orang yang hidup hanya sehari
berjuang dengan penuh semangat
(Dhammapada 112)
Semoga Sang Triratna selalu melindungi
ua makhluk hidup berbahagia
Karya ini kupersembahkan untuk :
Papa dan Mama atas dukungan moral dan materialnya
Kakak atas dukungan intelektualny
Keluarga besarku atas dukungan sem
Novianti atas doa dan sukacita yang diberikan
Sahabat dan teman-teman Almamaterku 20
yang telah memberikan semangat dan dukungan
Karya ini kupersembahkan untuk :
oral dan materialnya
Kakak atas dukungan intelektualnya
s dukungan semangatnya
n sukacita yang diberikan
Almamaterku 2006 FST
Nama
Nomor Mahasiswa
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma
PENGARUH PEMBERIAN PADA TIKUS JANTAN DAN KADAR KREATININ
Dengan demikian, saya Dharma, hak untuk mengelolanya dalam ben mempublikasikannya tanpaperlu meminta izin
selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini yang saya buat dengan sebenarnya. Dibuat di Yogyakarta
Pada tanggal : 19 Desember 2009
Yang menyatakan
( Daryono Thejo )
vi : Daryono Thejo Nomor Mahasiswa : 068114073
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul:
PEMBERIAN AKUT JUS WORTEL (Daucus
PADA TIKUS JANTAN WISTAR: KAJIAN TERHADAP OR DAN KADAR KREATININ SERUM
demikian, saya memberikan kepada Perpustakaan Universitas untuk menyimpan, mengalihkan dalam bentuk
mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas, mempublikasikannya di Internet atau media lain untuk kepentingan
meminta izin dari saya maupun memberikan royalti selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini yang saya buat dengan sebenarnya. Dibuat di Yogyakarta
Pada tanggal : 19 Desember 2009
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan
aucus carota L.)
: KAJIAN TERHADAP ORGAN GINJAL
vii PRAKATA
Puji syukur kepada Tuhan Yang Maha Esa karena dengan kasih setianya,
penulis dapat menyelesaikan skripsi berjudul “Pengaruh Pemberian Akut Jus
Wortel (Daucus carota L.) Pada Tikus Jantan Wistar : Kajian Terhadap Organ
Ginjal dan Kadar Kreatinin Serum” sebagai salah satu syarat untuk menyelesaikan
program pendidikan S1 dan mendapatkan gelar S.Farm di Fakultas Farmasi,
Universitas Sanata Dharma Yogyakarta.
Penulis mengucapkan terima kasih kepada semua pihak yang telah
memberikan dukungan, motivasi, dan memberikan saran hingga terselesaikannya
skripsi ini, terutama kepada :
1. Ibu Rita Suhadi M.Si., Apt. selaku Dekan Fakultas Farmasi, Universitas
Sanata Dharma Yogyakarta,
2. Bapak Yosef Wijoyo, M.Si., Apt. selaku Dosen Pembimbing skripsi yang
selalu meluangkan waktu untuk memberikan bimbingan, pengetahuan, dan
motivasi selama penelitian dan penyusunan skripsi ini,
3. Ibu Phebe Hendra, M.Si., Ph.D., Apt. selaku Dosen Penguji yang telah
meluangkan waktunya untuk menguji dan memberikan arahan demi
sempurnanya skripsi ini,
4. Bapak Dr. C.J. Soegihardjo, Apt. selaku Dosen Penguji yang telah
meluangkan waktunya untuk menguji dan memberikan arahan demi
sempurnanya skripsi ini,
5. Ibu drh. Reny Kusumastuti, M.P., selaku Dosen yang membimbing dan
data skripsi ini,
7. Bapak Parjiman, Bapak
banyak membantu selama penelitian ini,
8. Pius dan Thomas ya
Terima kasih atas pertolongan yang kalian berikan.
9. Semua angkatan 2006 ter
per satu, yang telah membantu selama penyelesaian skripsi ini.
Penulis menyadar
Oleh karena itu, penulis
skripsi ini. Akhir kata
perkembangan ilmu dan berbagai pihak.
viii
Parjiman, Bapak Heru, dan Bapak Kayat selaku laboran
banyak membantu selama penelitian ini,
Thomas yang membantu dalam menekropsi (membunuh)
Terima kasih atas pertolongan yang kalian berikan.
Semua angkatan 2006 terlebih kelas FST dan pihak yang tidak disebutkan s
per satu, yang telah membantu selama penyelesaian skripsi ini.
Penulis menyadari bahwa skripsi ini masih banyak terdapat
itu, penulis mengharapkan saran dan kritik demi pen
Akhir kata besar harapan skripsi ini dapat bermanfaat
perkembangan ilmu dan berbagai pihak.
Yogyakarta, 26
selaku laboran yang telah
(membunuh) subyek uji.
tidak disebutkan satu
per satu, yang telah membantu selama penyelesaian skripsi ini.
terdapat kekurangan.
demi penyempurnaan
dapat bermanfaat bagi
November 2009
Penulis
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan
tidak memuat karya atau
dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
ix
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang s
karya atau bagian karya orang lain, kecuali yang telah
dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Yogyakarta, 26 November 2009 skripsi yang saya tulis ini
yang telah disebutkan
dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Yogyakarta, 26 November 2009
Penulis
x
tikus jantan Wistardan kadar kreatinin serumnya.
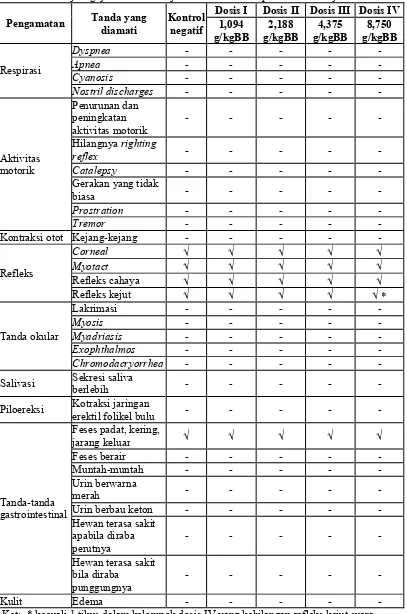
Metode penelitian yang digunakan adalah eksperimental murni dengan rancangan acak lengkap pola searah. Obyek uji yang digunakan adalah jus wortel yang terbagi dalam empat peringkat dosis, yaitu 1,094; 2,188; 4,375 dan 8,750 g/kgBB yang diberikan secara peroral ke subyek uji. Subyek uji yang digunakan adalah tikus jantan galur Wistar sebanyak 30 ekor dengan umur 60-90 hari, dan berat 100-200 gram. Subyek uji dibagi dalam 5 kelompok perlakuan, masing-masing kelompok terdapat 6 ekor tikus, yaitu : kelompok I sebagai kelompok kontrol negatif diberi diberi air putih merk “Aqua” 25 ml/kgBB, kelompok II-V sebagai kelompok perlakuan diberi jus wortel dalam 4 peringkat dosis.
Data hasil pengamatan kemudian diolah dengan analisis statistik Kruskal-Wallisuntuk rasio berat organ ginjal, kadar kreatinin serum praperlakuan, dan kadar kreatinin serum pascaperlakuan (1 hari dan 14 hari), Two-Way Anova untuk analisis profil kenaikan berat badan, Paired t-test untuk analisis kadar kreatinin serum pascaperlakuan banding praperlakuan, dan Unpaired t-test untuk analisis kadar kreatinin serum pascaperlakuan 1 hari banding 14 hari.
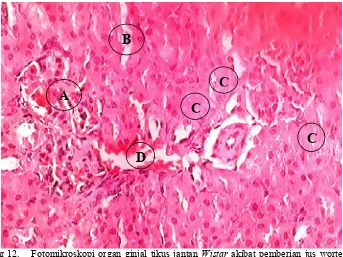
Hasil penelitian menunjukkan bahwa jus akut wortel memiliki efek toksik pada ginjal yang kemungkinan disebabkan ketoksikan dari bentuk autooksidasi beta karoten dalam wortel, ditunjukkan dengan adanya hemorrhagic, nekrosis tubulus dan glomerulus pada ginjal, namun tidak sampai mematikan subyek uji (LD50 semu). Sifat efek toksik pada organ ginjal mulai mengalami pemulihan. Kadar kreatinin serum antara perlakuan jus wortel dengan kontrol negatif berbeda tidak bermakna. Kadar kreatinin serum pada penelitian ini tidak berkorelasi dengan kondisi ginjal.
xi
ABSTRACT
The aims of this study is to determine safety use of carrot juice (Daucus carota L.) thats determine the acute toxicity of carrot juice orally expressed by LD50 values, the effect to the kidney organ Wistar male rats and serum creatinine levels.
Research method used is a pure experimental with one-way randomized completely design. Test object used is carrot juice which is divided in 4 doses ranking, namely 1.094; 2.188; 4.375 and 8.750 g/kgBB the peroral given to test subjects. Test subjects used were male rats of Wistar strain 30 rats with age 60 – 90 days, and weighting 100 – 200 grams. Test subjects were divided into 5 treatment groups, each group consist of 6 rats, namely: group I as a negative control group were given water brand "Aqua" 25 ml/kgBB, group II-V in the treatment group were given carrot juice in 4 rating doses.
Observation data was processed with statistical analysis Kruskal-Wallis for kidney organ weight ratios, serum creatinine levels pretreatment, and serum creatinine levels posttreatment (1 day and 14 days), Two-Way Anova for profile changes in weight analysis, Paired t-test for analysis of serum creatinine levels posttreatment versus pretreatment, and Unpaired t-test for analysis of serum creatinine levels posttreatment 1 day versus 14 days.
The results showed that the carrot juice has acute toxic effects on the kidney is probably due toxicity of autooxydation form of beta carotene in carrots, indicated by a hemorrhagic, necrotic tubules and glomerulus of the kidney, but not to kill the test subject (pseudo LD50). Toxic effects to kidney organ are starting to recover. Serum creatinine levels between carrot juice treatment and a negative control treatment showed no significant difference between them. Serum creatinine levels in this study did not correlate with kidney conditions.
xii
HALAMAN JUDUL ... ii
HALAMAN PERSETUJUAN PEMBIMBING ... iii
HALAMAN PENGESAHAN ... iv
HALAMAN PERSEMBAHAN ... v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPERLUAN AKADEMIS ... vi
PRAKATA... vii
PERNYATAAN KEASLIAN KARYA ... ix
INTISARI ... x
ABSTRACT... xi
DAFTAR ISI... xii
DAFTAR TABEL... xviii
DAFTAR GAMBAR ... xix
DAFTAR LAMPIRAN... xxiv
BAB I PENGANTAR... 1
A. Latar Belakang ... 1
1. Permasalahan ... 3
2. Keaslian penelitian... 4
xiii
B. Tujuan Penelitian ... 9
1. Tujuan umum ... 9
2. Tujuan khusus ... 9
BAB II PENELAAHAN PUSTAKA ... 10
A. Tanaman Wortel... 10
1. Sistematika tanaman ... 10
2. Nama sinonim ... 10
3. Nama daerah ... 10
4. Morfologi ... 10
5. Kultivar wortel ... 11
6. Kandungan kimia ... 12
7. Khasiat ... 12
B. Beta Karoten ... 12
C. Toksikologi ... 16
1. Definisi toksikologi... 16
2. Asas umum toksikologi... 16
a. Kondisi efek toksik ... 16
b. Mekanisme aksi efek toksik... 17
c. Wujud efek toksik ... 17
d. Sifat efek toksik ... 18
3. Jenis uji toksikologi ... 18
a. Uji ketoksikan tak khas ... 19
xiv
a. Pemilihan spesies hewan... 20
b. Cara pemberian ... 20
c. Dosis dan jumlah hewan ... 20
d. Faktor lingkungan ... 21
e. Pengamatan dan pemeriksaan ... 22
3. Penggolongan LD50... 22
E. Ginjal... 23
1. Definisi dan fungsi ... 23
2. Anatomi dan fisiologi ginjal ... 23
3. Fotomikroskopi ginjal ... 25
a. Korteks ... 25
b. Medula ... 26
c. Pelvis... 26
4. Nefrotoksikan... 26
a. Glomerulus (glomerulonefropati) ... 27
b. Nefropati tubulus proksimal ... 27
c. Nefropati tubulus distal... 28
F. Kreatinin ... 28
1. Definisi... 28
xv
3. Fungsi kreatinin serum... 29
BAB III METODE PENELITIAN ... 30
A. Jenis dan Rancangan Penelitian ... 30
B. Variabel Penelitian dan Definisi Operasional... 30
1. Variabel penelitian ... 30
a. Variabel bebas... 30
b. Variabel tergantung... 30
2. Variabel pengacau terkendali... 30
3. Variabel pengacau tak terkendali... 31
4. Definisi operasional ... 31
C. Alat atau Instrumen Penelitian... 31
D. Bahan atau Materi Penelitian ... 32
1. Subyek uji ... 32
2. Sediaan uji... 32
3. Kontrol negatif ... 32
4. Formalin 10%... 32
5. Pakan dan minum subyek uji ... 32
6. Garam NaCl fisiologis ... 32
E. Tata Cara Peneltitian... 33
1. Determinasi tanaman wortel (Daucus carota L.) ... 33
2. Pengelompokan subyek uji ... 33
3. Penanganan subyek uji... 33
xvi
8. Pengukuran kadar kreatinin serum... 38
a. Pengukuran kadar kreatinin serum praperlakuan... 38
b. Pengukuran kadar kreatinin serum pascaperlakuan ... 38
9. Histopatologi organ ginjal... 39
a. Pengambilan dan pengamatan histopatologi... 39
b. Pembuatan preparat histopatologi... 39
c. Pemeriksaan histopatologi organ ginjal ... 40
F. Analisis Hasil ... 40
BAB IV HASIL DAN PEMBAHASAN ... 42
A. Determinasi Tanaman Wortel ... 42
B. Pengamatan Gejala-Gejala Klinis ... 43
C. Potensi Ketoksikan Akut Jus Wortel (LD50)... 45
D. Pengamatan Makroskopis dan Mikroskopis Ginjal ... 45
1. Analisis hasil histopatologis 24 jam ... 50
2. Analisis hasil histopatologis 14 hari ... 57
E. Analisis Berat Rasio Organ Ginjal... 67
F. Analisis Kadar Kreatinin Serum ... 68
1. Kreatinin serum praperlakuan... 68
2. Kreatinin serum pascaperlakuan ... 69
xvii
H. Analisis Berat Pakan dan Minum ... 73
BAB V KESIMPULAN DAN SARAN ... 76
A. Kesimpulan ... 76
B. Saran ... 76
DAFTAR PUSTAKA ... 78
LAMPIRAN... 82
xviii
Tabel 2. Gejala klinis dalam uji ketoksikan akut ... 37
Tabel 3. Gejala-gejala klinis tikus jantan Wistar akibat pemberian
akut jus wortel... 44
Tabel 4. Hasil pemeriksaan makroskopis organ ginjal tikus jantan
Wistar akibat pemberian akut jus wortel... 46
Tabel 5. Hasil pemeriksaan histopatologi organ ginjal tikus jantan
Wistarakibat pemberian akut jus wortel... 47
Tabel 6. Berat rasio organ ginjal ... 67
Tabel 7. Kadar kreatinin serum praperlakuan ... 69
Tabel 8. Kadar kreatinin serum pascaperlakuan banding
praperlakuan... 70
Tabel 9. Kadar kreatinin serum kelompok pascaperlakuan H-1 dan
H-14 ... 70
Tabel 10. Kadar kreatinin serum pascaperlakuan H-1 banding
xix
DAFTAR GAMBAR
Gambar 1. Struktur beta karoten... 13
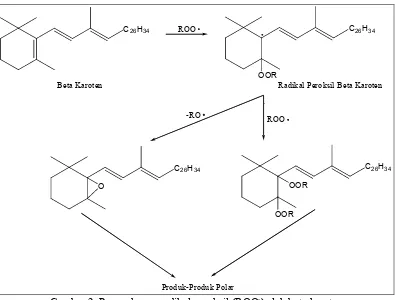
Gambar 2. Penangkapan radikal peroksil (ROO.) oleh beta karoten ... 13
Gambar 3. Struktur beta apo-8’-karotenal, salah satu produk degradasi oksidatif dari beta karoten... 15
Gambar 4. Struktur ginjal ... 24
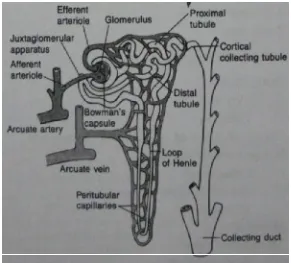
Gambar 5. Struktur nefron ... 24
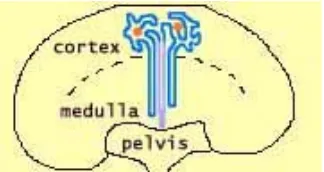
Gambar 6. Bagian-bagian ginjal ... 25
Gambar 7. Bagian korteks ... 25
Gambar 8. Bagian Medula ... 26
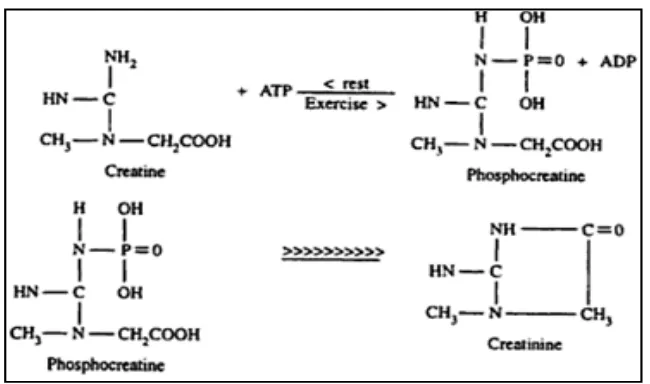
Gambar 9 Mekanisme pembentukan kreatinin ... 29
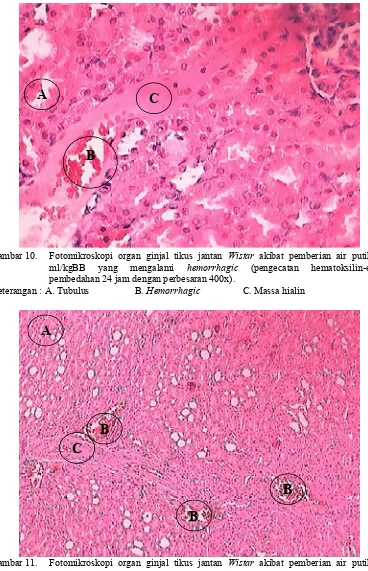
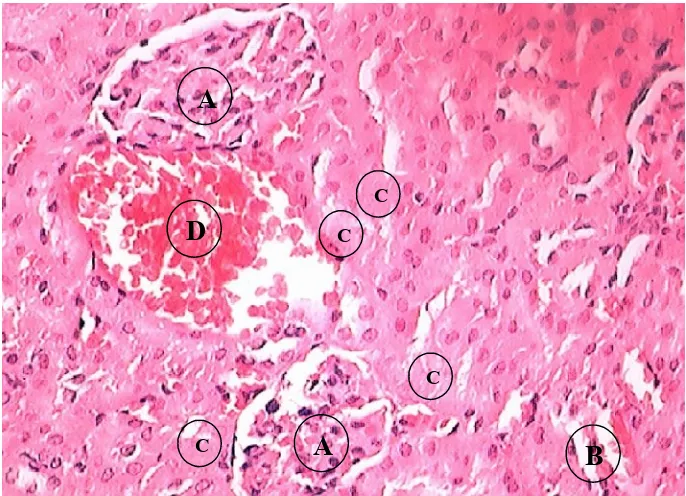
Gambar 10. Fotomikroskopi organ ginjal tikus jantan Wistar akibat pemberian air putih 25 ml/kgBB yang mengalami hemorrhagic (pengecatan hematoksilin-eosin pembedahan 24 jam dengan perbesaran 400x) ... 51
Gambar 11. Fotomikroskopi organ ginjal tikus jantan Wistar akibat pemberian air putih 25 ml/kgBB yang mengalami hemorrhagic (pengecatan hematoksilin-eosin pembedahan 24 jam dengan perbesaran 100x) ... 51
xx
hematoksilin-eosin pembedahan 24 jam dengan perbesaran
400x) ... 53
Gambar 14. Fotomikroskopi organ ginjal tikus jantan Wistar akibat
pemberian jus wortel dosis 2,188 g/kgBB yang mengalami
nekrosis glomerulus fokal menuju multifokal (pengecatan
hematoksilin-eosin pembedahan 24 jam dengan perbesaran
100x) ... 54
Gambar 15. Fotomikroskopi organ ginjal tikus jantan Wistar akibat
pemberian jus wortel dosis 4,375 g/kgBB yang mengalami
nekrosis tubulus multifokal (pengecatan hematoksilin-eosin
pembedahan 24 jam dengan perbesaran 400x) ... 55
Gambar 16. Fotomikroskopi organ ginjal tikus jantan Wistar akibat
pemberian jus wortel dosis 4,375 g/kgBB yang mengalami
nekrosis glomerulus multifokal (pengecatan
hematoksilin-eosin pembedahan 24 jam dengan perbesaran 100x)... 55
Gambar 17. Fotomikroskopi organ ginjal tikus jantan Wistar akibat
pemberian jus wortel dosis 8,750 g/kgBB yang mengalami
nekrosis tubulus multifokal menuju diffuse (pengecatan
hematoksilin-eosin pembedahan 24 jam dengan perbesaran
xxi
Gambar 18. Fotomikroskopi organ ginjal tikus jantan Wistar akibat
pemberian jus wortel dosis 8,750 g/kgBB yang mengalami
nekrosis glomerulus multifokal (pengecatan
hematoksilin-eosin pembedahan 24 jam dengan perbesaran 100x)... 57
Gambar 19. Fotomikroskopi organ ginjal tikus jantan Wistar akibat
pemberian air putih 25 ml/kgBB yang mengalami
hemorrhagic (pengecatan hematoksilin-eosin pembedahan
14 hari dengan perbesaran 100x) ... 58
Gambar 20. Fotomikroskopi organ ginjal tikus jantan Wistar akibat
pemberian jus wortel dosis 1,094 g/kgBB yang mengalami
nekrosis tubulus fokal menuju multifokal (pengecatan
hematoksilin-eosin pembedahan 14 hari dengan perbesaran
400x) ... 59
Gambar 21. Fotomikroskopi organ ginjal tikus jantan Wistar akibat
pemberian jus wortel dosis 1,094 g/kgBB yang mengalami
nekrosis glomerulus fokal menuju multifokal (pengecatan
hematoksilin-eosin pembedahan 14 hari dengan perbesaran
100x) ... 60
Gambar 22. Fotomikroskopi organ ginjal tikus jantan Wistar akibat
pemberian jus wortel dosis 2,188 g/kgBB yang mengalami
nekrosis tubulus multifokal (pengecatan hematoksilin-eosin
xxii
eosin pembedahan 14 hari dengan perbesaran 100x)... 61
Gambar 24. Fotomikroskopi organ ginjal tikus jantan Wistar akibat
pemberian jus wortel dosis 4,375 g/kgBB yang mengalami
nekrosis tubulus multifokal menuju diffuse (pengecatan
hematoksilin-eosin pembedahan 14 hari dengan perbesaran
400x) ... 62
Gambar 25. Fotomikroskopi organ ginjal tikus jantan Wistar akibat
pemberian jus wortel dosis 4,375 g/kgBB yang mengalami
nekrosis glomerulus multifokal (pengecatan
hematoksilin-eosin pembedahan 14 hari dengan perbesaran 100x)... 63
Gambar 26. Fotomikroskopi organ ginjal tikus jantan Wistar akibat
pemberian jus wortel dosis 8,750 g/kgBB yang mengalami
nekrosis tubulus multifokal menuju diffuse (pengecatan
hematoksilin-eosin pembedahan 14 hari dengan perbesaran
400x) ... 64
Gambar 27. Fotomikroskopi organ ginjal tikus jantan Wistar akibat
pemberian jus wortel dosis 8,750 g/kgBB yang mengalami
nekrosis glomerulus multifokal (pengecatan
xxiii
Gambar 28. Grafik kenaikan berat badan tikus jantan Wistar akibat
pemejanan akut jus wortel... 73
Gambar 29. Grafik rata-rata jumlah pakan tikus jantan Wistar per
harinya... 74
Gambar 30. Grafik rata-rata jumlah minum tikus jantan Wistar per
xxiv
Lampiran 2. Gambar jus wortel konsentrasi 35% dan 4,376% ... 82
Lampiran 3. Foto blender ... 82
Lampiran 4. Foto ruang pemeliharaan... 83
Lampiran 5. Foto timbangan ... 83
Lampiran 6. Foto pengambilan sampel darah ... 83
Lampiran 7. Foto proses pembedahan... 84
Lampiran 8. Penentuan dosis dari konsentrasi ... 84
Lampiran 9. Konversi dari dosis terendah ke konsentrasi terendah ... 84
Lampiran 10. Perhitungan pemberian volume pada tikus ... 84
Lampiran 11. Konversi dosis tertinggi ke manusia 70 kg ... 85
Lampiran 12. Pengamatan gejala klinis kontrol negatif “Aqua”
(25 ml/kgBB) ... 86
Lampiran 13. Pengamatan gejala klinis dosis I Jus Wortel
(1,094 g/kgBB) ... 87
Lampiran 14. Pengamatan gejala klinis dosis II Jus Wortel
(2,188 g/kgBB) ... 88
Lampiran 15. Pengamatan gejala klinis dosis III Jus Wortel
(4,375 g/kgBB) ... 89
Lampiran 16. Pengamatan gejala klinis dosis IV Jus Wortel
xxv
Lampiran 17. Berkas pemeriksaan histopatologis organ ginjal
tikus jantan Wistar... 91
1
Sejak ribuan tahun yang lalu, obat dan pengobatan tradisional sudah ada
di Indonesia, jauh sebelum pelayanan kesehatan formal dengan obat-obatan
modernnya dikenal masyarakat. Pengobatan tradisional dengan memanfaatkan
tumbuhan berkhasiat obat merupakan pengobatan yang dimanfaatkan dan diakui
masyarakat dunia, yang menandai kesadaran untuk kembali ke alam (back to
nature) adalah untuk mencapai kesehatan yang optimal dan untuk mengatasi
berbagai penyakit secara alami (Wijayakusuma, 2000).
Pengobatan tradisional pada umumnya lebih aman daripada obat-obatan
modern. Walaupun begitu, obat tradisional harus hati-hati dalam penggunaannya.
Beberapa tanaman yang digunakan dalam pengobatan tradisional dalam jumlah
sedikit merupakan obat, tetapi akan berubah menjadi racun bila dipakai dalam
jumlah berlebihan (Werner, 1989).
Salah satu contoh tanaman obat tradisional adalah wortel. Tanaman ini
sering dikonsumsi masyarakat dengan diolah menjadi sayur ataupun dibuat jus.
Menurut penelitian yang telah dilakukan, wortel dapat digunakan sebagai obat
anti inflamasi (Hapsari, 2003; Widarsih, 2003; Rasmandani, 2004; Kristama,
2007), analgesik (Putra, 2003; Widhianata, 2007), dan hepatoprotektif (Nuraeni,
2003; Widari, 2004). Menurut Dalimartha (2007) dan Hutapea (1993) wortel juga
2
tekanan darah tinggi dan untuk kesehatan mata, dimana zat yang dicurigai
berkhasiat adalah beta karoten.
Menurut Wijayakusuma (2000), penggunaan tanaman obat tradisional
dalam pengobatan tradisional di Indonesia dianggap kuno, tidak ilmiah, tidak
rasional karena tidak dilakukan uji farmakologi, toksisitas, uji klinik, dan berbagai
uji lainnya, sehingga khasiat dan keamanannya masih diragukan. Oleh karena itu
perlu diuji toksisitas akut jus wortel.
Toksisitas akut merupakan uji yang dilakukan dengan memberikan zat
kimia yang sedang diuji sebanyak satu kali dalam jangka waktu 24 jam (Lu,
1995). Penelitian ketoksikan akut mencakup semua organ, namun dalam
penelitian ini hanya dipilih satu organ saja, yaitu ginjal. Hal ini dikarenakan arah
dari penelitian ini lebih mengenai pengaruh pemberian akut jus wortel (Daucus
carota L.) terhadap organ ginjal, karena pengaruh pemberian akut jus wortel bisa
berefek positif atau justru berefek negatif (toksik). Selain itu ginjal merupakan
organ sasaran utama dari efek toksik (Lu, 1995) sehingga mengundang
ketertarikan peneliti untuk meneliti apakah jus wortel dapat bersifat toksik
terhadap organ ginjal yang akan diperiksa kondisi ginjalnya secara makroskopik
dan mikroskopik (histopatologi).
Selain melihat perubahan struktural (histopatologi) yang terjadi pada
organ ginjal, penelitian ini juga dilakukan pengukuran terhadap kadar kreatinin
serum untuk melihat pengaruh pemberian akut jus wortel terhadap perubahan
biokimiawi dalam tubuh dan bagaimana hubungannya terhadap organ ginjal.
menghasilkan energi yang akan mengalir lewat darah menuju ke ginjal untuk
diekskresikan. Apabila terjadi gangguan fungsi pada ginjal, akan mengurangi
ekskresi kreatinin dan akan berakibat terjadi peningkatan kadar kreatinin serum
sehingga kreatinin serum dapat menggambarkan kondisi ginjal (Fischbach and
Dunning, 2004). Karena hal itulah maka dilakukan penelitian mengenai pengaruh
pemberian akut jus wortel (Daucus carota L.) pada tikus jantan Wistar : kajian
terhadap organ ginjal dan kadar kreatinin serum.
1. Permasalahan
Berdasarkan latar belakang yang telah dikemukakan, permasalahan yang
muncul adalah :
a. Berapa besar potensi ketoksikan akut jus wortel yang dinyatakan dengan
kisaran Median Lethal Dosage (LD50) ?
b. Bagaimana gejala, wujud, sifat dan mekanisme efek toksik dari jus wortel ?
c. Bagaimana pengaruh pemberian akut jus wortel terhadap organ ginjal pada
tikus Wistar ?
d. Bagaimana pengaruh pemberian akut jus wortel terhadap kadar kreatinin
serum pada tikus Wistar?
e. Apakah terdapat suatu korelasi antara kondisi organ ginjal dengan kadar
4
2. Keaslian penelitian
Beberapa penelitian mengenai khasiat dan keamanan tanaman wortel
adalah sebagai berikut :
a. Daya Anti Inflamasi Infus Umbi Wortel (Daucus carota L.) Pada Mencit
Jantan (Hapsari, 2003).
Infusa umbi wortel (Daucus carota L.) mempunyai daya anti inflamasi yang
ditunjukkan dengan kemampuan infusa umbi wortel dalam mengurangi
pembengkakan akibat pemberian injeksi karagenin 1% secara subplanar. Daya
anti inflamasi air perasan umbi wortel dosis dosis 4,75; 9,5; 19; dan 38
g/kgBB berturut-turut adalah sebesar 38,62%; 67,43%; 54,47%; 26,25%.
b. Daya Anti Inflamasi Perasan Umbi Wortel (Daucus carota L.) Pada Mencit
Putih Jantan (Widarsih, 2003).
Air perasan umbi wortel (Daucus carota L.) mempunyai daya anti inflamasi
yang ditandai dengan penurunan bobot udema akibat pemberian injeksi
karagenin 1% secara subplanar. Daya anti inflamasi air perasan umbi wortel
dosis 1,25; 2,5; 5; 10; dan 20 ml/kgBB berturut-turut adalah sebesar 19,01%;
46,41%; 103,71%; 75,39%; dan 53,58%.
c. Efek Hepatoprotektif Air Perasan Umbi Wortel (Daucus carota L.) Terhadap
Mencit Jantan Terinduksi CCl4(Nuraeni, 2003).
Air perasan umbi wortel (Daucus carota L.) mempunyai efek hepatoprotektif
terhadap mencit jantan terinduksi CCl4. Efek hepatoprotektif ditandai dengan
menurunnya aktivitas GPT-serum dan menurunnya derajat kerusakan sel hati
dosis 0,14; 0,392; 1,162; 3,50; 10,50 dan 31,50 ml/kgBB berturut-turut adalah
sebesar 10,53%; 12,83%; 18,87%; 28,26%; 35,70% dan 77,12%.
d. Efek Analgesik Air Perasan Umbi Wortel (Daucus carota L.) Pada Mencit
Putih Betina (Putra, 2003).
Air perasan umbi wortel (Daucus carota L.) mempunyai kemampuan
analgesik pada mencit putih betina. Efek analgesik air perasan umbi wortel
dosis 1,25; 2,5; 5; 10; dan 20 ml/kgBB secara berturut-turut adalah sebesar
29,72%; 43,68%; 67,36%; 60,74%, dan 31,18%.
e. Daya Anti Inflamasi Sari Umbi Wortel (Daucus carotaL.) Pada Mencit Putih
Jantan (Kajian Terhadap Lama Masa Pemberian) (Rasmandani, 2004).
Lama masa pemberian mempengaruhi daya anti inflamasi sari umbi wortel
(Daucus carota L.) pada mencit jantan yang ditunjukkan bahwa pemberian
sari umbi wortel secara berlebihan dapat menurunkan daya anti inflamasi sari
umbi wortel. Pemberian sari umbi wortel dosis 5 ml/kgBB hari ke-1 sampai
hari ke-4 menunjukkan penurunan berat rata-rata udema kaki mencit, namun
pada hari ke-5 dan ke-6 mengalami peningkatan berat rata-rata udema kaki
mencit dibanding hari sebelumnya.
f. Efek Hepatoprotektif Perasan Umbi Wortel (Daucus carota L.) Pada Mencit
Jantan Terinduksi Parasetamol : Kajian Berdasarkan Perbedaan Tempat
Tumbuh (Widari, 2004).
Perasan umbi wortel (Daucus carota L.) dosis 1,47 ml/kgBB pada tempat
6
hepatoprotektif yang berbeda terhadap mencit jantan terinduksi parasetamol
dosis 250 mg/kgBB.
g. Pengaruh Perlakuan Perasan Umbi Wortel (Daucus carota L.) Secara
Subkronis Terhadap Gambaran Histopatologis Ginjal Tikus Putih (Adita,
2006).
Perasan umbi wortel (Daucus carotaL.) memiliki potensi efek toksik terhadap
organ ginjal tikus putih bila digunakan dalam waktu jangka pendek, yaitu
selama 14 hari berturut-turut. Wujud efek toksiknya berupa hemorrhagic,
erosi epitel tubulus, dan peradangan. Sifat efek toksiknya terbalikkan pada
tikus jantan dan bersifat tak terbalikkan pada tikus betina.
h. Pengaruh Perlakuan Perasan Umbi Wortel (Daucus carota L.) Secara
Subkronis Terhadap Gambaran Histopatologis Hepar Tikus Putih Jantan dan
Betina (Mayana, 2006).
Perasan umbi wortel (Daucus carotaL.) memiliki potensi efek toksik terhadap
organ hati tikus putih bila digunakan dalam waktu jangka pendek, yaitu
selama 14 hari berturut-turut. Wujud efek toksiknya berupa hyperemia
multifokal, hemorrhagic, dan degenerasi melemak. Sifat efek toksiknya tak
terbalikkan pada tikus jantan dan betina.
i. Pengaruh Perlakuan Perasan Umbi Wortel (Daucus carota L.) Secara
Subkronis Terhadap Gambaran Histopatologis Ovarium Tikus Putih (Sunu,
2006).
Perasan umbi wortel (Daucus carotaL.) dosis 8,53 ml/kgBB memiliki potensi
jangka pendek, yaitu selama 14 hari berturut-turut. Wujud efek toksik berupa
kerusakan ovarium dan penghambatan oogenesis. Sifat efek toksiknya adalah
tak terbalikkan.
j. Pengaruh Perlakuan Perasan Umbi Wortel (Daucus carota L.) Secara
Subkronis Terhadap Gambaran Histopatologis Organ Lambung dan Usus
Halus Tikus Putih (Lingganingsih, 2006).
Perasan umbi wortel (Daucus carota L.) dosis 3,41 ml/kgBB mempunyai
spektrum efek toksik terhadap organ lambung tikus putih jantan, sedangkan
dosis 8,53; 21,33; dan 53,32 ml/kgBB mempunyai spektrum efek toksik
berupa erosi epitel lapisan mukosa dan peradangan pada organ lambung tikus
putih jantan dan betina. Perasan umbi wortel tidak mempengaruhi terjadinya
spektrum efek toksik pada organ usus halus. Sifat efek toksiknya pada organ
lambung bersifat terbalikkan.
k. Efek Analgesik Jus Umbi Wortel (Daucus carota L.) Pada Mencit Putih
Betina (Widhianata, 2007).
Jus umbi wortel (Daucus carota L.) terbukti mempunyai khasiat analgesik
dengan metode rangsang kimia pada mencit putih betina. Efek analgesik jus
umbi wortel dosis 0,5; 1; 2; 4; dan 8 g/kgBB secara berturut-turut adalah
sebesar 17,71%; 27,04%; 36,77%; 56,02%; dan 41,25%.
l. Efek Anti Inflamasi Ampas Wortel (Daucus carota L.) Pada Kelinci Putih
8
Pemberian ampas wortel (Daucus carota L.) selama 3 dan 4 hari pada kelinci
putih betina memiliki efek anti inflamasi yang ditandai dengan penurunan
mean skor eritema.
m. Toksisitas Akut Sari Wortel (Daucus carota L.) Kajian terhadap Organ
Lambung, Ginjal, dan Hati pada Mencit Putih Betina Galur Balb/c (Karlina,
2009)
LD50 semu > 16,7 ml/kgBB. Terjadi radang pada lambung dan ginjal yang
bersifat terbalikan, serta nekrosis pada organ hati (24 jam setelah perlakuan).
Terjadi peningkatan aktivitas ALT yang bermakna tetapi tidak untuk kadar
kreatinin serum.
n. Pengaruh Pemberian Akut Jus Wortel (Daucus carota L.) Pada Tikus Jantan
Wistar : Kajian Terhadap Organ Hati dan Aktivitas Serum Glutamic Pyruvic
Transaminase(SGPT) (Novianti, 2009).
Pemberian Akut Jus Wortel pada konsentrasi jus wortel sebanyak 35%
memberikan hasil berupa LD50 semu > 8,750 g/kgBB, menyebabkan
perubahan struktural pada sel hati seperti nekrosis, degenerasi hidrofik, dan
pembentukan jaringan fibroblast, yang mulai mengalami pemulihan organ
hati. Jus wortel tidak menyebabkan perubahan aktivitas SGPT. Aktivitas
SGPT dalam penelitian ini tidak berkorelasi dengan kerusakan sel hati.
Berdasarkan pustaka yang ditemukan, telah banyak dilakukan pengujian
terhadap tanaman wortel. Namun, penulis tidak menemukan adanya penelitian
tentang Pengaruh Pemberian Akut Jus Wortel (Daucus carota L.) Pada Tikus
3. Manfaat penelitian
a. Manfaat teoritis
Data-data ilmiah yang diperoleh dari penelitian ini diharapkan dapat
berguna untuk pengembangan penggunaan jus wortel dalam pengobatan.
b. Manfaat metodologis
Diharapkan metode penelitian ini dapat digunakan sebagai acuan untuk
penelitian berikutnya yang berhubungan dengan jus wortel.
c. Manfaat praktis
Penelitian ini diharapkan dapat memberikan informasi keamanan
penggunaan jus wortel kepada masyarakat.
B. Tujuan Penelitian 1. Tujuan umum
Mengetahui apakah terdapat pengaruh pemberian akut jus wortel pada
tikus jantan Wistarterhadap organ ginjal dan kadar kreatinin serum.
2. Tujuan khusus
Penelitian ini digunakan untuk menetapkan seberapa besar potensi
ketoksikan akut jus wortel pada tikus jantan Wistar yang dinyatakan dengan
kisaran LD50, untuk mengetahui gejala, wujud, sifat dan mekanisme efek toksik
jus wortel, untuk mengetahui pengaruh pemberian akut jus wortel terhadap organ
ginjal dan kadar kreatinin serum pada tikus jantan Wistar, dan untuk mengetahui
apakah terdapat suatu korelasi antara kondisi organ ginjal dengan kadar kreatinin
10 BAB II
PENELAAHAN PUSTAKA A. Tanaman Wortel 1. Sistematika tanaman
Sistematika tanaman wortel adalah sebagai berikut :
Kingdom : Plantae
Divisi : Spermatophyta
Subdivisi : Angiospermae
Kelas : Dicotyledoneae
Bangsa : Umbelliflorae
Suku : Apiaceae
Marga : Daucus
Jenis : Daucus carota L. (Hutapea, 1993)
2. Nama sinonim
Tanaman wortel memiliki nama sinonim : Daucus sativus (Dalimartha,
2007).
3. Nama daerah
Tanaman wortel memiliki nama daerah yaitu : Boktel dalam bahasa
Sunda, Wortel dalam bahasa Jawa, dan Ortel dalam bahasa Madura (Hutapea,
1993).
4. Morfologi
Tanaman wortel termasuk suku Apiaceae. Bentuk tanaman ini berupa
tanaman ini sekitar 1 sampai 1,5 meter dihitung dari ujung daun hingga ujung
umbinya.
Bagian-bagian yang terdapat pada tanaman wortel terdiri dari :
a. Batang : Tegak, bulat, berbulu, hijau.
b. Daun : Majemuk, menyirip, bersilang, lonjong, tepi bertoreh,
ujung runcing, pangkal berlekuk, panjang 15-20 cm,
lebar 10-13 cm, pertulangan menyirip, hijau.
c. Bunga : Majemuk, bentuk cawan, di ujung batang, tangkai
silindris, hijau, kelopak lonjong, lima helai, hijau,
benang sari silindris, panjang ± 3 mm, putih, kepala sari
bulat, kuning, tangkai putik silindris, kepala ptik bulat,
kuning, makota bentuk bintang, halus, putih.
d. Umbi : Buni, lonjong, diameter ± 3 mm, coklat.
e. Biji : Lonjong, putih.
f. Akar : Tunggang, membentuk umbi, oranye (Hutapea, 1993).
5. Kultivar wortel
Berdasarkan bentuk umbinya, wortel dibagi menjadi tiga kultivar, yaitu :
a. Tipe imperator, yaitu golongan wortel yang bentuk umbinya bulat panjang
dengan ujung runcing, hingga mirip bentuk kerucut.
b. Tipe chantenay, yaitu golongan wortel yang bentuk umbinya bulat panjang
dengan ujung tumpul dan tidak berakar serabut.
c. Tipe nantes, yaitu golongan wortel yang memiliki bentuk umbi tipe peralihan
12
6. Kandungan kimia
Dalam 100 g wortel segar mengandung 37.000 kalori; 1,1 g protein, 0,9 g
serat; 36 mg kalsium; 1,2 mg Fe; 4,2 mg karoten; 0,06 mg tiamin; 0,05 mg
riboflavin; 0,7 mg niasin; dan 8 mg vitamin C (Ashari, 2006). Kandungan lainnya
adalah pada umbinya mengandung saponin dan polifenol (Hutapea, 1993).
7. Khasiat
Tanaman wortel memiliki berbagai macam khasiat :
a. Memperkuat fungsi hati.
b. Sebagai antiseptik.
c. Sebagai laksatif (Dalimartha, 2007).
d. Sebagai penurun tekanan darah tinggi.
e. Untuk menjaga kesehatan mata (Hutapea, 1993).
Selain itu manfaat lain dari wortel adalah bersifat sebagai diuretik
(memperlancar kencing) sehingga dapat mendorong keluar sisa metabolisme sel
tubuh yang tidak berguna melalui ginjal (Dalimartha, 2007).
B. Beta Karoten
Beta karoten merupakan salah satu dari 600 komponen karotenoid yang
banyak ditemukan dalam tanaman. Karotenoid merupakan senyawa isoprenoid
C40 dan tetraterpenoid yang terdapat dalam plastida jaringan tanaman, baik yang
melakukan fotosintesis maupun tidak. Dalam kloroplas, karotenoid berperan
Gambar 1. Struktur beta karoten (Watson, 2002)
Beta karoten biasanya digunakan sebagai suplemen nutrisi maupun
prekursor vitamin A (Buring and Hennekens, 1993). Namun, perannya lebih
penting adalah dalam detoksifikasi berbagai bentuk oksigen. Beta karoten bersifat
larut dalam lemak dan berfungsi sebagai peredam singlet oksigen dan radikal
bebas (Krinsky, 1989).
C26H34 C26H34
OOR
C26H34
OOR OOR ROO
C26H34 O
Produk-Produk Polar
Beta Karoten Radikal Peroksil Beta Karoten
ROO
-RO
Gambar 2. Penangkapan radikal peroksil (ROO.) oleh beta karoten
(Kennedy and Liebler, 1992)
Hasil penelitian epidemiologis terkait beta karoten menyatakan bahwa
subjek yang banyak mengkonsumsi buah-buahan dan sayuran dengan kandungan
14
dan penyakit kardiovaskuler (Peto, Buckley, and Sporn, 1981). Penelitian lain
juga menyatakan bahwa asupan tinggi beta karoten dari sayuran dan buah-buahan
menekan resiko beberapa penyakit ganas termasuk kanker prostat (Williams,
Boileau, Clinton, and Erdman, 2000).
Namun di sisi lain, beta karoten dapat berperan sebagai prooksidan, yang
dimodulasi oleh Fe dalam jaringan. Ditemukan bahwa pemberian beta karoten
pada tikus yang telah diberi canthaxanthin (suplemen yang mengandung Fe) dapat
menyebabkan penyerapan Fe meningkat sehingga akan menyebabkan
pembentukan kompleks karotenoid dengan Fe yang dapat larut dalam lumen usus,
kemudian mencegah efek penghambatan polifenol pada absorpsi Fe (Garcia,
1998).
Menurut Masotti, Casali, and Galeotti (1988), beta karoten dapat bersifat
sebagai antitumor atau agen tumor-promoting. Ketika aktivitas prooksidan terjadi
dalam sel yang telah mengalami transformasi (perubahan), senyawa tersebut akan
berpotensi sebagai antioksidan. Namun ketika aktivitas prooksidan beta karoten
terjadi dalam sel normal, akan dihasilkan kerusakan oksidatif yang menekan
integritas sel dan menginduksi transformasi neoplastik.
Beta karoten memiliki potensi sebagai antioksidan dan prooksidan. Salah
satu bentuk prooksidan dari beta karoten adalah beta apo-8’-karotenal yang
merupakan salah satu produk oksidasi dari beta karoten karena pada kadar
oksigen yang tinggi beta karoten dapat mengalami autooksidasi. Bentuk ini
apabila tidak segera dinetralkan oleh tokoferol (vitamin E) dan asam askorbat
Di dalam tubuh, beta karoten akan dioksidasi oleh 15,15’-dioxygenase
menjadi dua molekul retinal yang kemudian dioksidasi menjadi asam retinoat
(Redmond, T.M., Gentlemen, S., Duncan, T., Yu, S., Wiggert, B., Gantt, E., et al.,
2000). Asam retinoat berfungsi sebagai agen kemopreventif, menghambat
karsinogenesis khususnya di jaringan paru (Patrick, 2000). Akan tetapi, beta
karoten juga dapat mengalami degradasi oksidatif menjadi beta apo-8’, 10’, 12’,
dan 14’-karotenal yang dapat memicu metabolisme asam retinoat. Dengan
demikian akan menyebabkan penurunan kadar asam retinoat dalam jaringan dan
dapat menyebabkan terjadinya proliferasi sel dan pembentukan kanker (Siems,
Sommerburg, Schild, Augustin, Langhans, and Wiswedel, 2002). Meski
demikian, ada keuntungan yang dapat diperoleh dari sifat beta karoten sebagai
prooksidan, yaitu dapat membunuh sel tumor. Karotenoid berperan sebagai agen
oksidatif yang selektif terhadap sel tumor (Null, 2000).
H O
16
C. Toksikologi 1. Definisi toksikologi
Toksikologi adalah ilmu yang mempelajari aksi berbahaya zat kimia atas
sistem biologi. Takrif ini menunjukkan bahwa obyek yang dipelajari dalam
toksikologi adalah antaraksi zat kimia atau senyawa asing dengan sistem biologi
atau makhluk hidup, dimana pusat perhatiannya terletak pada pengaruh berbahaya
bahan racun itu atas kehidupan makhluk hidup (Donatus, 2001).
2. Asas umum toksikologi
a. Kondisi efek toksik
Kondisi efek toksik adalah berbagai keadaan atau faktor yang dapat
mempengaruhi keefektifan absorpsi, distribusi, dan eliminasi zat beracun di dalam
tubuh, sehingga menentukan keberadaan zat kimia utuh atau metabolitnya dalam
sel sasaran serta toksisitasnya atau keefektifan antaraksinya dengan sel sasaran
(Loomis, 1978).
Kondisi efek toksik dari suatu senyawa tergantung pada dua hal yaitu :
kondisi pemejanan dan kondisi makhluk hidup. Kondisi pemejanan antara lain
meliputi jenis pemejanan (akut, subkronis, atau kronis), jalur pemejanan
(intravaskuler atau ekstravaskuler), lama dan kekerapan pemejanan, saat
pemejanan, dan takaran atau dosis pemejanan. Sedangkan kondisi makhluk hidup
meliputi keadaan normal (misalnya berat badan, umur, suhu tubuh, kecepatan
pengosongan lambung, kecepatan aliran darah, status gizi, kehamilan, genetika,
jenis kelamin, ritme sirkadian, ritme diurnal), dan keadaan tidak normal (misalnya
b. Mekanisme aksi efek toksik
Berdasarkan sifat dan tempat kejadiannya, mekanisme aksi efek toksik
zat kimia dibagi menjadi dua yaitu mekanisme luka intrasel dan mekanisme luka
ekstrasel. Mekanisme luka intrasel adalah luka sel yang diawali oleh aksi racun
pada tempat aksi di dalam sel sasaran, oleh karena itu mekanisme ini sering
disebut mekanisme langsung atau primer. Sedangkan mekanisme luka ekstrasel
adalah zat racun pada awalnya bereaksi di lingkungan luar sel dengan akibat
terjadinya luka di dalam sel, oleh karena itu mekanisme ini sering disebut
mekanisme tidak langsung atau sekunder (Donatus, 2001).
c. Wujud efek toksik
Wujud efek toksik dapat berupa perubahan biokimia, fungsional dan
struktural. Namun tidak berarti bahwa efek toksik zat beracun sepenuhnya dapat
terpisah dengan tegas ke dalam 3 wujud dasar efek toksik, melainkan sering
merupakan campuran, karena ketiganya merupakan suatu proses yang saling
berkaitan (Donatus, 2001).
1) Perubahan biokimia
Jenis wujud efek toksik ini berkaitan dengan respon dan perubahan atau
kekacauan biokimia terhadap luka sel, akibat antaraksi zat racun dan sel sasaran
yang sifatnya terbalikkan.
2) Perubahan fungsional (fisiologi)
Jenis wujud efek toksik ini merupakan jenis efek toksik yang berkaitan
dengan antaraksi zat beracun dengan sel sasaran atau tempat aktif enzim yang
18
3) perubahan struktural (histopatologi)
Jenis wujud efek toksik ini berkaitan dengan perubahan morfologi sel
yang akhirnya terwujud sebagai kekacauan struktural. Sehubungan dengan
masalah ini, terdapat respon histopatologi dasar sebagai tanggapan terhadap luka
sel, yakni degenerasi, proliferasi, dan inflamasi atau perbaikan (Donatus, 2001).
d. Sifat efek toksik
Sifat efek toksik dapat berupa antaraksi terbalikkan (reversible) dan
antaraksi yang tidak terbalikkan (irreversible) (Donatus, 2001).
1) Antaraksi yang terbalikkan (reversible)
Antaraksi ini merupakan efek toksik yang ditimbulkan oleh racun akan
segera hilang bila pemejanan dengan racun terhadap makhluk hidup dihentikan
dan kondisi dari sel sasaran atau reseptornya akan kembali ke keadaan normal.
2) Antaraksi yang tidak terbalikkan (irreversible)
Antaraksi ini merupakan efek toksik yang ditimbulkan oleh racun tidak
akan segera hilang bila pemejanan dengan racun terhadap makhluk hidup
dihentikan karena terjadi penumpukan efek toksik dan kerusakannya yang terjadi
pada reseptor bersifat menetap sehingga reseptor tidak akan bisa kembali ke
keadaan normal (Donatus, 2001).
3. Jenis uji toksikologi
Pada umumnya uji toksikologi terbagi menjadi dua golongan yaitu uji
a. Uji ketoksikan tak khas
Uji yang dirancang untuk mengevaluasi keseluruhan atau spektrum efek
toksik sesuatu senyawa pada aneka ragam jenis subyek uji. Termasuk dalam
golongan uji ketoksikan tak khas adalah :
1) Uji ketoksikan akut
Uji ini dirancang untuk menentukan efek toksik suatu senyawa yang
terjadi dalam waktu yang singkat setelah pemejanan atau pemberiannya dengan
takaran tertentu dan biasanya pengamatan dilakukan 24 jam.
2) Uji ketoksikan subkronis
Uji ketoksikan suatu senyawa yang diberikan dengan dosis berulang pada
subyek uji tertentu selama kurang dari tiga bulan.
3) Uji ketoksikan kronis
Uji ketoksikan kronis serupa dengan uji ketoksikan subkronis.
Perbedaannya terletak pada lamanya pemberian atau pemejanan takaran dosis
senyawa uji dan masa pengamatan serta pemeriksaannya.
b. Uji ketoksikan khas
Uji yang dirancang untuk mengevaluasi secara rinci efek yang khas
sesuatu senyawa pada aneka ragam jenis subyek uji, termasuk golongan uji
ketoksikan khas ini adalah uji potensiasi, kekarsinogetikan, kemutagenikan,
20
D. Toksisitas Akut 1. Definisi
Uji toksisitas akut dilakukan dengan memberikan zat kimia yang sedang
diuji sebanyak satu kali dalam jangka waktu 24 jam (Lu, 1995).
2. Rancangan percobaan
a. Pemilihan spesies hewan
Secara umum, dalam penentuan nilai LD50 digunakan subyek uji berupa
tikus dan mencit. Hewan ini dipilih karena murah, mudah didapat, dan mudah
ditangani. Selain itu terdapat banyak data toksikologi tentang jenis hewan ini,
suatu fakta yang mempermudah perbandingan toksisitas zat kimia (Lu, 1995).
Penentuan LD50 sebaiknya dilakukan pada kedua jenis kelamin, juga pada
hewan dewasa dan yang masih muda, karena kerentanannya mungkin berbeda
(Lu, 1995).
b. Cara pemberian
Secara umum toksikan harus diberikan melalui jalur yang biasa
digunakan pada manusia. Jalur oral paling sering digunakan pada manusia. Bila
akan diberikan per oral, zat tersebut harus diberikan dengan sonde (Lu, 1995).
c. Dosis dan jumlah hewan
Untuk menentukan LD50secara tepat, perlu dipilih suatu dosis yang akan
membunuh sekitar separuh jumlah hewan-hewan itu, dosis lain yang akan
membunuh lebih dari separuh (kalau bisa kurang dari 90%), dan dosis ketiga yang
akan membunuh kurang dari separuh (kalau bisa lebih dari 10%) dari
sekurang-kurangnya tiga diantaranya akan berada dalam rentang dosis yang
dikehendaki (Lu, 1995).
Secara umum, LD50 akan lebih tepat bila digunakan lebih banyak hewan
untuk tiap dosis dan bila rasio antara dosis yang berurutan lebih kecil. Banyak
peneliti menggunakan 40-50 subyek uji per LD50 dan memilih rasio 1,2-1,5 (Lu,
1995). Namun, Weil (1952) menyarankan penggunaan empat hewan untuk tiap
dosis dan rasio sebesar 2,0 antara dosis yang berurutan. Belakangan ini diajukan
prosedur uji sederhana yang lain (Bruce, 1985) yang menggunakan hanya enam
sampai sembilan hewan untuk setiap uji.
d. Faktor lingkungan
Faktor lingkungan dapat mempengaruhi respon hewan terhadap zat kimia
yang diberikan antara lain :
1) Pengandangan hewan dapat mempengaruhi LD50 suatu bahan kimia, namun
nilai LD50 untuk kebanyakan bahan kimia hanya sedikit dipengaruhi oleh faktor
ini (Lu, 1995). Subyek uji seharusnya dikandangkan dalam kelompok berdasarkan
jenis kelamin atau dikandangkan sendiri-sendiri, tergantung dari spesies dan
ukuran tubuh hewan tersebut (Hayes, 2001).
2) Jenis kandang (berlubang-lubang atau padat) dan jenis bahan alas kandang
juga dapat mempengaruhi reaksi hewan terhadap toksikan (Lu, 1995).
3) Suhu lingkungan juga dapat mempengaruhi efek toksik begitu juga dengan
kelembaban relatif, dimana bila kelembaban relatif ruangan tinggi maka dapat
22
ruangan yang optimal untuk subyek uji adalah 22 ± 3oC dan kelembaban
relatifnya 30-70% (Hayes, 2001).
4) Pola makan minum dan kualitasnya harus terstandarisasi. Tujuannya adalah
agar subyek uji mendapatkan makanan dan minuman yang bernutrisi lengkap dan
bebas dari kontaminan sehingga keadaan fisiologi dan metabolisme subyek uji
selama penelitian tetap dalam kondisi normal (Hayes, 2001).
e. Pengamatan dan pemeriksaan
Setelah toksikan diberikan, jumlah hewan yang mati (jika ada) dan waktu
kematiaannya harus diamati untuk memperkirakan LD50. Yang lebih penting lagi,
tanda-tanda toksisitasnya harus dicatat. Jangka waktu pengamatan harus cukup
panjang dan biasanya 7-14 hari tetapi dapat jauh lebih lama (Lu, 1995).
Autopsi harus dilakukan pada semua hewan yang mati dan pada beberapa
hewan yang hidup, terutama hewan yang tampak sakit pada akhir percobaan.
Autopsi dapat memberikan informasi yang berharga tentang organ sasaran,
terutama bila kematian tidak terjadi segera setelah pemberian zat kimia.
Diperlukan juga pemeriksaan histopatologik organ tubuh dan jaringan tertentu
(Lu, 1995).
3. Penggolongan LD50
Penggolongan potensi ketoksikan akut pada hewan dapat dilihat pada
Tabel 1. Potensi ketoksikan akut zat kimia pada hewan (Lu, 1995)
Kriteria LD50(mg/kg)
1. Luar biasa toksik 5 atau kurang
2. Sangat toksik 5 – 50
3. Cukup toksik 50 – 500
4. Sedikit toksik 500 – 5000
5. Praktis tidak toksik 5000 – 15000
6. Relatif kurang berbahaya Lebih dari 15000
E. Ginjal 1. Definisi dan fungsi
Ginjal adalah organ yang berfungsi untuk menyingkirkan buangan
metabolisme normal dan mengekskresi xenobiotik dan metabolitnya. Ginjal
merupakan organ sasaran utama dari efek toksik (Lu, 1995). Ginjal rentan
terhadap banyak zat kimia. Kerentanan ini disebabkan posisinya dalam sirkulasi
cairan badan yaitu fungsi ekskresinya berhubungan erat sekali dengan darah dan
zat yang terkandung di dalamnya (Koeman, 1987).
2. Anatomi dan fisiologi ginjal
Struktur yang menonjol dalam ginjal adalah nefron, kira-kira berjumlah
1,3 x 106. Tiap nefron terdiri atas glomerulus dan serangkaian tubulus.
Glomerulus dialiri darah oleh sistem kapiler bertekanan tinggi yang menghasilkan
ultrafiltrat dari plasma. Filtrat yang terkumpul dalam kapsul Bowman mengalir
melalui tubulus berkelok proksimal, ansa Henle, dan tubulus distal, dan kemudian
mengalir lewat kumpulan tubulus ke dalam piala ginjal dan dibuang sebagai urin
24
Gambar 4. Struktur ginjal (Klaassen, 2001)
3. Fotomikroskopi ginjal
Secara fotomikroskopi organ ginjal, ginjal terbagi menjadi tiga bagian,
yaitu : korteks, medula, dan pelvis (gambar 6)(King, 2007).
Gambar 6. Bagian-bagian ginjal (King, 2007)
a. Korteks
Korteks adalah bagian terluar dari organ ginjal. Korteks terdapat bagian
yang dinamakan renal corpuscle dan terhubung dengan tubulus yang memiliki
fungsi untuk memproduksi filtrat dari plasma darah oleh glomerulus dan
menerima filtrat plasma dari glomerulus untuk memproses lebih lanjut menjadi
urin oleh tubulus. Renal corpuscle terbagi menjadi glomerulus, kapsul bowman,
dan ruang bowman. Sedangkan tubulus terbagi menjadi tubulus proksimal dan
tubulus distal (gambar 7) (King, 2007).
Gambar 7. Bagian korteks (King, 2007)
26
b. Medula
Medula merupakan bagian tengah dari ginjal setelah korteks. Fungsi dari
bagian ini adalah untuk menciptakan kondisi garam hipertonik sehingga bisa
mengabsorpsi air yang masih dibutuhkan tubuh. Bagian ini terbagi menjadi
lengkung henle dan collecting duct(gambar 8)(King, 2007).
Gambar 8. Bagian Medula (King, 2007) Keterangan : ts = lengkung henle bersegmen tipis
dt = lengkung henle bersegmen tebal cd = collecting duct
c. Pelvis
Pelvis adalah bagian dalam dari ginjal setelah medula. Fungsi dari bagian
ini adalah menerima urin hasil pemrosesan pada bagian korteks dan medula untuk
diteruskan lebih lanjut ke ureter (King, 2007).
4. Nefrotoksikan
Ginjal merupakan gudang penyimpanan racun yang poten, karena
memiliki kapasitas yang tinggi untuk mengikat zat kimia. Keadaan ini mungkin
eliminasi, berturut-turut metabolisme dan ekskresi racun dari dalam tubuh
(Donatus, 2001).
Kelompok utama nefrotoksikan adalah logam berat, antibiotik, analgesik,
dan hidrokarbon berhalogen tertentu. Semua bagian nefron secara potensial dapat
dirusak oleh efek toksikan. Beratnya beberapa efek beragam dari satu perubahan
biokimia atau lebih sampai kematian sel, dan efek ini dapat muncul sebagai
perubahan kecil pada fungsi ginjal atau gagal ginjal total (Lu, 1995).
Efek toksik zat beracun terhadap ginjal dapat diklasifikasikan
berdasarkan lokasinya sebagai berikut :
a. Glomerulus (Glomerulonefropati)
Glomerulus merupakan organ target yang jarang dipengaruhi oleh bahan
beracun. Organ ini dapat dipengaruhi oleh bahan beracun baik secara langsung
maupun tidak langsung. Salah satu perubahan glomerulus adalah perubahan
permeabilitasnya terhadap protein-protein plasma (Glaister, 1986).
b. Nefropati tubulus proksimal
Karena terjadi absorpsi dan sekresi aktif tubulus proksimal, kadar
toksikan pada tubulus proksimal sering lebih tinggi. Selain itu, kadar sitokrom
P-450 pada tubulus proksimal lebih tinggi untuk mendetoksifikasi atau
mengaktifkan toksikan. Dengan demikian, tempat ini sering merupakan sasaran
efek toksik (Lu, 1995).
Nefrotoksisitas yang terjadi di tubulus proksimal dapat berupa
28
tergantung dari tempat dan luasnya luka. Kelainan tubulus proksimal ini dapat
berupa hidrofik, inklusi, dan nekrosis (Glaister, 1986).
c. Nefropati tubulus distal
Efek toksik yang sering ditemui pada tubulus distal adalah kristaluria,
dan nekrosis papilla ginjal. Hal tersebut berhubungan dengan fungsi tubulus distal
dalam mengatur keseimbangan air, elektrolit, dan asam basa (Glaister, 1986).
F. Kreatinin 1. Definisi
Kreatinin adalah produk samping pemecahan fosfokreatin otot dalam
menghasilkan energi (Fischbach and Dunning, 2004).
2. Mekanisme pembentukan kreatinin
Kreatin adalah derivat atau turunan asam amino yang diperoleh dari
makanan (khususnya daging merah) dan juga dibentuk di liver dari asam amino
arginin, glisin, dan metionin. Kreatin kemudian ditangkap oleh otot tubuh
membentuk fosfokreatin, yang merupakan senyawa fosfat berenergi tinggi.
Fosfokreatin yang dipecah akan menyediakan cadangan energi (ATP). Ketika otot
digunakan secara berlebihan maka produksi fosfokreatin juga akan berlebih,
karena menyiapkan cadangan energi untuk siap digunakan oleh otot agar mampu
bekerja lebih keras lagi. Namun oleh karena jumlah fosfokreatin yang berlebih ini,
akan dihasilkan produk samping yaitu kreatinin (hasil siklisasi fosfokreatin) yang
Gambar 9. Mekanisme pembentukan kreatinin (Pasquale, 2000)
Kreatinin diproduksi dalam kecepatan yang konstan tergantung dari
massa otot seseorang dan kemudian dibuang dari tubuh melalui ginjal. Jumlah
produksi kreatinin ini konstan apabila jumlah massa otot juga dalam keadaan yang
konstan (Fischbach and Dunning, 2004).
3. Fungsi kreatinin serum
Kreatinin merupakan hasil samping pemecahan fosfokreatin yang tidak
bermanfaat lagi bagi tubuh dan akan mengalir lewat darah menuju ke ginjal untuk
diekskresikan. Apabila terjadi gangguan fungsi pada ginjal, akan mengurangi
ekskresi kreatinin dan akan berakibat terjadi peningkatan kadar kreatinin dalam
darah (kreatinin serum). Oleh karena itulah kadar kreatinin serum dapat
menggambarkan kondisi ginjal (Fischbach and Dunning, 2004).
Kadar kreatinin serum akan meningkat di atas ambang normal jika
penurunan fungsi ginjal mencapai 50%; oleh karenanya kreatinin serum bukan
merupakan indikator sensitif untuk kerusakan gejala ringan sampai sedang
(Rubenstein, Wayne, and Bradley, 2003). Uji kreatinin menunjukkan kelainan
30 BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian Pengaruh Pemberian Akut Jus Wortel (Daucus carota L.)pada
Tikus Jantan Wistar : Kajian Terhadap Organ Ginjal dan Kadar Kreatinin Serum
termasuk dalam penelitian eksperimental murni dengan rancangan acak lengkap
pola searah.
B. Variabel Penelitian dan Definisi Operasional 1. Variabel penelitian
a. Variabel bebas :
Dosis jus wortel, yaitu sejumlah (gram) jus wortel tiap satuan kgBB
subyek uji yang bersangkutan.
b. Variabel tergantung :
Toksisitas akut oral jus wortel, ditunjukkan dengan jumlah kematian
subyek uji, gejala efek toksik, sifat efek toksik, wujud efek toksik (dilihat dari
gambaran histopatologi subyek uji), mekanisme efek toksik, dan kadar kreatinin
serum pada subyek uji yang menggambarkan sehat tidaknya fungsi ginjal subyek
uji yang terpejan jus wortel.
2. Variabel pengacau terkendali
Suhu dan kelembaban ruangan, jenis dan jumlah pakan dan minum,
3. Variabel pengacau tak terkendali
Kondisi patologis subyek uji.
4. Definisi operasional
Jus wortel adalah sejumlah gram wortel yang diblender sampai sehalus
mungkin dan diambil sari beserta ampas di dalamnya untuk diberikan kepada
subyek uji.
Konsentrasi jus wortel yang diberikan ke subyek uji adalah konsentrasi
tertinggi dari jus wortel yang konsistensinya masih berbentuk jus pada umumnya
dan bisa diberikan ke subyek uji melewati lubang injeksi spluit oral.
C. Alat atau Instrumen Penelitian
1. Kandang subyek uji berukuran 35 cm x 26 cm x 12 cm.
2. Neraca analitik atau Analytical balance (Scout Pro, tipe SPS2001F, made in
USA).
3. Blender (Philips, Type HR 2815/A, Holland).
4. Alat-alat gelas (Pyrex) seperti bekkerglass, gelas ukur, dan labu takar.
5. Spuit oral, volume 5 ml (Terumo Syringe, MD 21921).
6. Pipa kapiler (Micro Haematocrit Tubes).
7. Microtube1,5 ml
8. Seperangkat alat bedah (Gold Cross, Stainless Steel).
9. Pemeriksaan preparat histopatologi subyek uji menggunakan mikroskop
32
D. Bahan atau Materi Penelitian 1. Subyek uji
Subyek uji yang digunakan berupa tikus jantan Wistar dengan kisaran
umur 60 sampai 90 hari dan dengan berat badan 100 - 200 gram yang diperoleh
dari Usaha Dagang Tikus WistarBantul, Yogyakarta.
2. Sediaan uji
Sediaan uji yang digunakan adalah jus wortel. Wortel dalam penelitian
ini memiliki bentuk umbi bulat panjang dengan ujung tumpul yang merupakan
tipe chantenay yang diperoleh dari Desa Soko Muntilan dengan waktu panen pada
bulan September 2009.
3. Kontrol negatif
Kontrol negatif berupa air putih merk “Aqua” dengan sumber mata air
dari Klaten.
4. Formalin 10%
Formalin dibeli dari Aldrich Lab dengan konsentrasi 37 % dan perlu
diencerkan menjadi formalin 10%.
5. Pakan dan minum subyek uji
Pakan dan minuman yang diberikan kepada subyek uji adalah pakan
merk “AD-5” dan air putih merk “Aqua”.
6. Garam NaCl fisiologis
Garam NaCl fisiologis diperoleh dari Laboratorium Biofarmasetika
E. Tata Cara Penelitian 1. Determinasi tanaman wortel (Daucus carota L.)
Tanaman wortel dideterminasi dengan menyesuaikan ciri-ciri yang ada
dengan buku acuan “Atlas Tumbuhan Obat Indonesia” karangan Dalimartha
(2007) dan “Inventaris Tanaman Obat Indonesia” karangan Hutapea (1993).
2. Pengelompokan subyek uji
Subyek uji sebanyak 30 ekor tikus jantan Wistar dikelompokkan secara
acak ke dalam 5 kandang, masing – masing kandang terdiri dari 6 ekor tikus. Tiap
kandang mewakili 1 kelompok perlakuan.
3. Penanganan subyek uji
Setelah dikelompokkan, subyek uji diadaptasikan selama kurang lebih 2
minggu dengan kondisi pemeliharaan pada ruangan yang bersuhu 25oC dengan
jenis dan jumlah pakan dan minum yang dikontrol. Setiap kandang diberi alas
berupa sekam padi yang diganti dan dibersihkan kandangnya setiap hari. Selama
masa 2 minggu ini, keadaan subyek uji diamati meliputi berat badan, pengamatan
tingkah laku, jumlah intake per hari makan dan minum setiap kandang, bentuk
dan warna kotoran dan dibandingkan antar subyek uji. Pakan diberikan pada
wadah makanan yang terbuat dari kaca. Wadah ini diisi sejumlah makanan dan
keesokan harinya, sisa makanan ditimbang. Demikian halnya pada jumlah air
minum. Air minum diberikan melalui botol dengan takaran tertentu kemudian
34
4. Orientasi penetapan konsentrasi jus wortel (Daucus carota L.)
Umbi wortel dicuci dengan air hingga bersih. Umbi wortel kemudian
dipotong dengan ukuran 3 cm x 0,2 cm x 1 cm. Kemudian wortel ditimbang 60 g,
70 g, 80 g, 90 g dan 100 g dan diblender selama 5 x 1 menit dengan ditambahkan
air sampai volume 200 ml. Jumlah gram ini digunakan untuk melihat konsistensi
jus yang masih dapat melewati jarum injeksi per oral. Berdasarkan hasil orientasi
yang dilakukan diperoleh konsentrasi jus maksimal adalah 35%.
5. Orientasi penetapan dosis jus wortel (Daucus carota L.)
Dosis terendah yang digunakan merupakan dosis yang secara teknis
masih dapat diberikan pada subyek uji sebatas volume minimal yang masih dapat
terskala oleh injeksi per oral dan jika dikonversikan menjadi jus, dosis terendah
tersebut masih berwujud seperti jus (tidak terlalu encer). Dosis tertinggi yang
digunakan merupakan dosis yang secara teknis dapat diberikan pada subyek uji
sebatas volume maksimal injeksi per oral. Berdasarkan hasil orientasi yang
dilakukan diperoleh dosis terendah 1,094 g/kgBB dan dosis tertinggi 8,750
g/kgBB. Dosis terendah dan tertinggi kemudian dihitung untuk menentukan
peringkat dosis II dan III dengan faktor perkalian tetap dua (2x). Peringkat dosis
terendah sampai tertinggi dari pemejanan jus wortel ini adalah sebagai berikut :
Dosis I (terendah) = 1,094 g/kgBB
Dosis II = 2,188 g/kgBB
Dosis III = 4,375 g/kgBB
6. Pemejanan jus wortel
Satu hari sebelum pemejanan, subyek uji dipuasakan namun tetap diberi
minum. Kelompok I digunakan sebagai kontrol, hanya diberi air merk “aqua”,
yaitu 25 ml/kgBB. Kelompok II-V dipejankan dengan jus wortel. Kelompok II
diberi dosis 1,094 g/kgBB. Kelompok III diberi dosis 2,188 g/kgBB. Kelompok
IV diberi dosis 4,375 g/kgBB. Kelompok V diberi dosis 8,750 g/kgBB.
7. Pengamatan
Pengamatan dilakukan dengan mengamati gejala-gejala klinis, perubahan
berat badan, jumlah asupan makan dan minum perhari, jumlah subyek uji yang
mati, kadar kreatinin serum praperlakuan dan pascaperlakuan, penimbangan berat
ginjal, dan pemeriksaan makroskopis dan mikroskopis (histopatologi) organ
ginjal. Keterangan lebih jelasnya dapat dilihat di bawah ini :
a. Pengamatan gejala klinis (tabel 2) dilakukan secara intensif pada 3 jam
pertama setelah pemejanan jus wortel. Hari berikutnya, pengamatan bisa
dilakukan sekali sehari sampai hari ke-14.
b. Perubahan berat badan dilakukan dengan cara penimbangan berat badan pada
hari ke-0 (pertama) sampai hari ke-14 (terakhir).
c. Perubahan jumlah makan dan minum perhari pada hari ke-0 (pertama) sampai
hari ke-14 (terakhir).
d. Jumlah subyek uji yang mati (bila ada) pada masing-masing kelompok uji 24
jam setelah pemejanan.
e. Penimbangan berat organ ginjal setelah subyek uji dinekropsi pada hari ke-1
36
f. Pengambilan darah subyek uji dilakukan sebelum pemejanan subyek uji
(praperlakuan) dan setelah pemejanan (pascaperlakuan) untuk mendapatkan
kadar kreatinin serumnya.
g. Pemeriksaan makroskopis organ ginjal dilakukan setelah subyek uji
dinekropsi pada hari ke-1 (setengah populasi) dan hari ke-14 (setengah
populasi) dan diamati bentuk, warna, dan konsistensi ginjalnya. Setelah itu
dilakukan pengamatan mikroskopis organ ginjal setelah organ ginjal dibuat
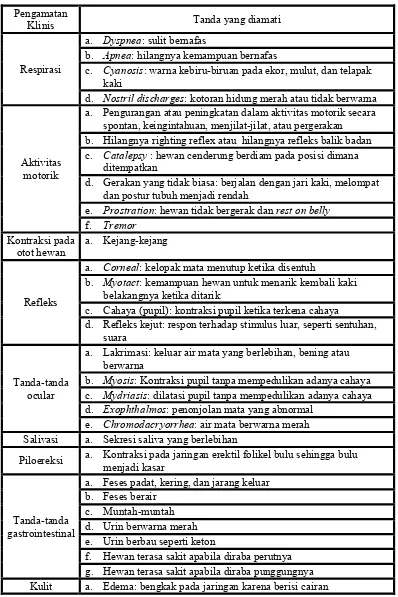
Tabel 2. Gejala klinis dalam uji ketoksikan akut Pengamatan
Klinis Tanda yang diamati
Respirasi
a. Dyspnea: sulit bernafas
b. Apnea: hilangnya kemampuan bernafas
c. Cyanosis: warna kebiru-biruan pada ekor, mulut, dan telapak kaki
d. Nostril discharges: kotoran hidung merah atau tidak berwarna
Aktivitas motorik
a. Pengurangan atau peningkatan dalam aktivitas motorik secara spontan, keingintahuan, menjilat-jilat, atau pergerakan
b. Hilangnya righting reflex atau hilangnya refleks balik badan c. Catalepsy: hewan cenderung berdiam pada posisi dimana
ditempatkan
d. Gerakan yang tidak biasa: berjalan dengan jari kaki, melompat dan postur tubuh menjadi rendah
e. Prostration: hewan tidak bergerak dan rest on belly
f. Tremor
Kontraksi pada otot hewan
a. Kejang-kejang
Refleks
a. Corneal: kelopak mata menutup ketika disentuh
b. Myotact: kemampuan hewan untuk menarik kembali kaki belakangnya ketika ditarik
c. Cahaya (pupil): kontraksi pupil ketika terkena cahaya
d. Refleks kejut: respon terhadap stimulus luar, seperti sentuhan, suara
Tanda-tanda ocular
a. Lakrimasi: keluar air mata yang berlebihan, bening atau berwarna
b. Myosis: Kontraksi pupil tanpa mempedulikan adanya cahaya c. Mydriasis: dilatasi pupil tanpa mempedulikan adanya cahaya d. Exophthalmos: penonjolan mata yang abnormal
e. Chromodacryorrhea: air mata berwarna merah Salivasi a. Sekresi saliva yang berlebihan
Piloereksi a. Kontraksi pada jaringan erektil folikel bulu sehingga bulu menjadi kasar
Tanda-tand