EVALUASI PENANDAA
BEREDAR DI APOTEK KOTA YOGYAKAR STANDAR BADAN PEN
EVALUASI PENANDAAN KEMASAN OBAT TRADISIONAL YANG BEREDAR DI APOTEK KOTA YOGYAKARTA BERDASARKAN STANDAR BADAN PENGAWAS OBAT DAN MAKANAN (BPOM)
PERATURAN MENTERI KESEHATAN, ASSSOCIATION OF ASIA NATION (ASEAN),DAN WORLD HEALTH
ORGANIZATION (WHO)
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Farmasi
ASAN OBAT TRADISIONAL YANG YAKARTA BERDASARKAN
(BPOM), ASSSOCIATION OF THE
ii
EVALUASI PENANDAAN KEMASAN OBAT TRADISIONAL YANG BEREDAR DI APOTEK KOTA YOGYAKARTA BERDASARKAN STANDAR BADAN PENGAWAS OBAT DAN MAKANAN (BPOM),
PERATURAN MENTERI KESEHATAN, ASSSOCIATION OF THE SOUTH EAST ASIA NATION (ASEAN),DAN WORLD HEALTH
ORGANIZATION (WHO)
Skripsi yang diajukan oleh : Novia Tri Purnamasari
NIM : 088114125
telah disetujui oleh
Pembimbing Utama
iii
Pengesahan Skripsi Berjudul
EVALUASI PENANDAAN KEMASAN OBAT TRADISIONAL YANG BEREDAR DI APOTEK KOTA YOGYAKARTA BERDASARKAN STANDAR BADAN PENGAWAS OBAT DAN MAKANAN (BPOM),
PERATURAN MENTERI KESEHATAN, ASSSOCIATION OF THE SOUTH EAST ASIA NATION (ASEAN),DAN WORLD HEALTH
ORGANIZATION (WHO)
Oleh :
Novia Tri Purnamasari NIM : 088114125
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi
Universitas Sanata Dharma Pada tanggal : ...
Mengetahui Fakultas Farmasi Universitas Sanata Dharma
Dekan,
Ipang Djunarko, M.Sc.,Apt.
Pembimbing utama : Tanda Tangan
Ipang Djunarko, M.Sc.,Apt. ………..
Panitia Penguji :
1. Ipang Djunarko, M.Sc.,Apt. ………..
2. Prof. Dr. C. J. Sugihardjo., Apt. ………..
Kupersembahkan
Allah SWT atas segala berkat s
Bapak, Ibu, dan Kakak
Teman
Semua orang yang mengasihiku
iv
Kupersembahkan karya kecil ini untuk :
atas segala berkat serta pencurahan
rahmat-Bapak, Ibu, dan Kakak-kakakku tercinta
Teman-teman dan almamaterku
Semua orang yang mengasihiku
v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan di bawah ini, saya mahasiswa Universitas Sanata Dharma:
Nama : Novia Tri Purnamasari
Nomor mahasiswa : 088114125
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul :
Evaluasi Penandaan Kemasan Obat Tradisional yang Beredar di Apotek Kota Yogyakarta Berdasarkan Standar Badan Pengawas Obat dan Makanan (BPOM), Peraturan Menteri Kesehatan, Asssociation of the South East Asia Nation (ASEAN),dan World Health Organization (WHO)
beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan kepada Perpustakaan Universitas Sanata Dharma hak untuk menyimpan, mengalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas, dan mempublikasikan di internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalti kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini saya buat dengan sebenarnya.
Dibuat di Yogyakarta Pada tanggal : 23 Mei 2012
Yang Menyatakan
vi
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang saya tulis ini tidak memuat karya atau bagian karya orang lain, kecuali yang telah disebutkan dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Apabila di kemudian hari ditemukan indikasi plagiarisme dalam naskah ini, maka saya bersedia menanggung segala sanksi sesuai peraturan perundang-undangan yang berlaku.
Yogyakarta, 23 Mei 2012
Penulis
vii PRAKATA
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Esa atas berkat, rahmat dan kasih karunia yang telah diberikanNya sehingga penulis dapat menyelesaikan penulisan skripsi yang berjudul “Evaluasi Penandaan Kemasan Obat Tradisional yang Beredar di Apotek Kota Yogyakarta Berdasarkan Standar Badan Pengawas Obat dan Makanan (BPOM), Peraturan Menteri Kesehatan, Asssociation of the South East Asia Nation (ASEAN), dan World Health Organization (WHO)”
dengan baik sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi (S.Farm.) pada Fakultas Farmasi, Universitas Sanata Dharma Yogyakarta.
Penulis menyadari bahwa keberhasilan penulisan skripsi ini tidak terlepas dari bantuan serta dukungan dari berbagai pihak secara langsung maupun tidak langsung baik berupa moral, materiil maupun spiritual. Oleh sebab itu, penulis menghaturkan banyak terima kasih kepada :
1. Dekan Fakultas Farmasi, Universitas Sanata Dharma yang telah memberikan ijin untuk melakukan penelitian ini, dan telah memberikan dukungan selama penyusunan skripsi ini.
2. Ipang Djunarko, M.Sc., Apt. selaku Dosen Pembimbing yang dengan sabar membimbing dan memberikan arahan, saran, kritikan serta dukungan kepada penulis selama proses penelitian dan penulisan skripsi.
viii
4. Pengelola apotek Kota Yogyakarta yang telah memberikan ijin untuk melakukan penelitian di Apotek.
5. Sukmana Derta yang selalu memberikan motivasi, doa, dorongan, serta bantuan kepada peneliti dalam menyelesaikan skripsi.
6. Teman skripsiku Sekar Dewi yang telah saling menguatkan, memberikan semangat dan bantuan kepada peneliti serta bersama-sama menjalani suka dan duka selama menjalankan penelitian ini.
7. Sahabat-sahabatku tersayang Fransisca Dian P., Angela Vita, Ika Puji R., Vivi Christiani, Stefany Putri H., Stephanie Irena, Syafada Rizma, Alfiari Novita, Andri Ani, Suriadi, dan masih banyak lagi yang telah memberikan semangat dan banyak bantuan sehingga skripsi ini dapat terselesaikan dengan baik. 8. Teman-teman kelas B 2008, FKK B 2008, terima kasih atas kebersamaannya
dan pengalaman yang tak terlupakan dan luar biasa selama menjalani kuliah dan praktikum serta dorongan semangat yang telah diberikan kepada peneliti selama penyusunan skripsi ini.
9. Teman-teman KKN XLII Kelompok 12 yang telah memberikan perhatian, semangat, dan warna baru dalam hidup peneliti dalam menyelesaikan naskah. 10. Teman-teman dari angkatan 2006-2011 yang penulis kenal yang telah
memberikan perhatian dan semangat kepada penulis dalam menyelesaikan naskah.
ix
Penulis menyadari bahwa tidak ada yang sempurna dalam kehidupan ini. Oleh karena itu, penulis sangat mengharapkan kritik dan saran agar skripsi ini dapat menjadi lebih baik. Akhir kata, penulis berharap semoga skripsi ini dapat bermanfaat untuk menambah pengetahuan bagi yang membutuhkan.
xi F. Logo Kelompok Obat Tradisional………... G. Standar dan Peraturan yang Terkait Penandaan Obat Tradisional H. Landasan Teori……….. I. Hipotesis...
xii
BAB IV HASIL DAN PEMBAHASAN... A. Persentase Kesesuaian Obat Tradisional Berdasarkan Standar
BPOM, Peraturan Menteri Kesehatan, ASEAN, Dan WHO…… B. Persentase Kesesuaian Penandaan Produk Obat Tradisional
Terhadap Setiap Kriteria Standar BPOM, Peraturan Menteri Kesehatan, ASEAN, Dan WHO………... BAB V KESIMPULAN DAN SARAN... A. Kesimpulan... B. Saran... DAFTAR PUSTAKA... LAMPIRAN... BIOGRAFI PENULIS...
34
34
xiii
DAFTAR TABEL
Halaman Tabel I. Informasi yang harus dicantumkan pada kemasan obat
tradisional, obat herbal terstandar, dan fitofarmaka berdasarkan standar BPOM………... Tabel II. Informasi yang harus dicantumkan pada kemasan obat
tradisional berdasarkan standar Peraturan Menteri Kesehatan………... Tabel III. Informasi yang harus dicantumkan pada kemasan obat
tradisional berdasarkan standar ASEAN……… Tabel IV. Informasi yang harus dicantumkan pada kemasan obat
tradisional berdasarkan standar WHO………...
21
22
23
xiv
Produk Obat Tradisional Terhadap Standar BPOM……... Gambar 5. Diagram Batang Persentase Modus Tingkat Kesesuaian
Produk Obat Tradisional Terhadap Standar Peraturan Menteri Kesehatan……….. Gambar 6. Diagram Batang Persentase Modus Tingkat Kesesuaian Produk Obat Tradisional Terhadap Standar ASEAN…… Gambar 7. Diagram Batang Persentase Modus Tingkat Kesesuaian
Produk Obat Tradisional Terhadap Standar WHO……… Gambar 8. Diagram Batang Persentase Kesesuaian Produk Jamu
Terhadap Setiap Kriteria Standar BPOM………... Gambar 9. Diagram Batang Persentase Kesesuaian Produk Obat
herbal terstandar Terhadap Setiap Kriteria Standar BPOM………. Gambar 10. Diagram Batang Persentase Kesesuaian Produk Fitofarmaka Terhadap Setiap Kriteria Standar BPOM…...
xv
Gambar 11. Diagram Batang Persentase Kesesuaian Produk Jamu Terhadap Setiap Kriteria Standar Peraturan Menteri Kesehatan……….. Gambar 12. Diagram Batang Persentase Kesesuaian Produk Obat
Herbal Terstandar Terhadap Setiap Kriteria Standar Peraturan Menteri Kesehatan……… Gambar 13. Diagram Batang Persentase Kesesuaian Produk
Fitofarmaka Terhadap Setiap Kriteria Standar Peraturan Menteri Kesehatan……… Gambar 14. Diagram Batang Persentase Kesesuaian Produk Jamu
Terhadap Setiap Kriteria Standar ASEAN…………... Gambar 15. Diagram Batang Persentase Kesesuaian Produk Obat
Herbal Terstandar Terhadap Setiap Kriteria Standar ASEAN………. Gambar 16. Diagram Batang Persentase Kesesuaian Produk
Fitofarmaka Terhadap Setiap Kriteria Standar ASEAN………. Gambar 17. Diagram Batang Persentase Kesesuaian Produk Jamu
Terhadap Setiap Kriteria Standar WHO……… Gambar 18. Diagram Batang Persentase Kesesuaian Produk Obat
xvi
Gambar 19. Diagram Batang Persentase Kesesuaian Produk
xvii DAFTAR LAMPIRAN
Lampiran 1. Evaluasi Penandaan Produk Jamu Berdasarkan Standar BPOM……… Lampiran 2. Evaluasi Penandaan Produk Obat Herbal Terstandar
Berdasarkan Standar BPOM……….. Lampiran 3. Evaluasi Penandaan Produk Fitofarmaka Berdasarkan
Standar BPOM………... Lampiran 4. Evaluasi Penandaan Produk Jamu Berdasarkan Standar
Peraturan Menteri Kesehatan………. Lampiran 5. Evaluasi Penandaan Produk Obat Herbal Terstandar
Berdasarkan Standar Peraturan Menteri Kesehatan…... Lampiran 6. Evaluasi Penandaan Produk Fitofarmaka Berdasarkan
Standar Peraturan Menteri Kesehatan……… Lampiran 7. Evaluasi Penandaan Produk Jamu Berdasarkan Standar
ASEAN……….. Lampiran 8. Evaluasi Penandaan Produk Obat Herbal Terstandar
Berdasarkan Standar ASEAN……… Lampiran 9. Evaluasi Penandaan Fitofarmaka Berdasarkan Standar
ASEAN……….. Lampiran 10. Evaluasi Penandaan Produk Jamu Berdasarkan Standar
xviii
Lampiran 11. Evaluasi Penandaan Produk Obat Herbal Terstandar Berdasarkan Standar WHO……… Lampiran 12. Evaluasi Penandaan Produk Fitofarmaka Berdasarkan
Standar WHO………... Lampiran 13. Surat ijin penelitian dari Dinas Perizinan……….
113
xix
INTISARI
Evaluasi penandaan kemasan obat tradisional diperlukan agar setiap produk yang beredar melakukan penandaan sesuai dengan standar yang ada sehingga dapat memberikan jaminan mutu terhadap konsumen. Penelitian ini bertujuan untuk mengetahui informasi dari obat tradisional yang beredar di apotek Kota Yogyakarta yang memenuhi standar penandaan kemasan BPOM, Peraturan Menteri Kesehatan, ASEAN dan WHO.
Penelitian merupakan penelitian noneksperimental dengan rancangan observasional deskriptif evaluatif yang bersifat retrospektif. Data yang diperoleh melalui pengamatan langsung pada kemasan obat tradisional.
Hasil penelitian menunjukkan bahwa tidak semua obat tradisional memenuhi standar penandaan kemasan BPOM, Peraturan Menteri Kesehatan, ASEAN dan WHO. Berdasarkan standar BPOM, kriteria yang hanya dicantumkan oleh sebagian produk jamu, obat herbal terstandar, dan fitofarmaka adalah bentuk sediaan, nama dan alamat pemberi atau penerima kontrak, kontraindikasi, efek samping, interaksi obat, dan info khusus babi, alkohol, dan pemanis buatan. Berdasarkan standar Peraturan Menteri Kesehatan, kriteria yang hanya dicantumkan oleh sebagian produk jamu, obat herbal terstandar, dan fitofarmaka adalah kontraindikasi. Berdasarkan standar ASEAN, kriteria yang hanya dicantumkan oleh sebagian produk jamu, obat herbal terstandar, dan fitofarmaka adalah bentuk sediaan, nama dan alamat pemegang otorisasi pemasaran, dan info khusus alkohol dan penggunaan eksternal. Berdasarkan standar WHO, kriteria yang hanya dicantumkan oleh sebagian produk jamu, obat herbal terstandar, dan fitofarmaka adalah kontraindikasi dan lama pemberian.
.
xx ABSTRACT
An evaluation of traditional medicine packaging marking is required for the marking of each available product in accordance with existing standards so that it can provide quality assurance to the consumer. This study aims to get information about the traditional medicines which are available in the pharmacies in Yogyakarta whether they meet the marking standards of the packaging of BPOM, Regulation of the Minister of Health, ASEAN and WHO.
The study was non experimental using an observational study with descriptive evaluative design which is retrospective. The data obtained through direct observation on the packaging of traditional medicine.
The results showed that not all traditional medicine packaging meets the labeling standards of BPOM, Regulation of the Minister of Health, ASEAN and WHO. Based on the BPOM standard, criteria that just listed by some jamu, obat herbal terstandar, and fitofarmaka is the dosage form, name and address of the giver or the recipient of a contract, contraindication, side effects, drug interactions, and specific information content of pig, alcohol, and an artificial sweetener. Based on the Regulation of the Minister of Health, criteria that just listed by some jamu, obat herbal terstandar, and fitofarmaka is the contraindication. Based on the ASEAN standard, criteria that just listed by some jamu, obat herbal terstandar, and fitofarmaka is the dosage form, address of the marketing authorization holder, and specific information content of alcohol and external use. Based on the WHO, criteria that just listed by some jamu, obat herbal terstandar, and fitofarmakais the contraindication and duration for each.
1 BAB I
PENGANTAR
A. Latar Belakang
Obat tradisional merupakan bahan atau ramuan bahan atau ramuan yang berupa bahan tumbuhan, bahan hewan, bahan mineral, sediaan sarian (galenik) atau campuran dari bahan-bahan tersebut yang secara turun temurun digunakan untuk pengobatan, dan dapat diterapkan sesuai dengan norma yang berlaku di masyarakat (Dewan Perwakilan Rakyat RI, 2009). Obat herbal atau obat tradisional yang telah berkembang di Indonesia dibagi menjadi 3 kelompok, yaitu jamu, obat herbal terstandar, dan fitofarmaka. Jamu merupakan obat tradisional yang klaim khasiatnya berdasarkan pengalaman empiris yang telah berlangsung dalam kurun waktu yang sangat lama. Obat herbal terstandar adalah obat herbal yang simplisisianya telah dilakukan standarisasi dan uji praklinik. Fitofarmaka adalah obat herbal yang paling tinggi standarisasinya dibandingkan dengan jamu dan obat herbal terstandar karena pada fitofarmaka telah dilakukan uji klinik secara lengkap (Direktorat Jenderal Pengawas Obat dan Mananan RI, 2004).
wajib memiliki ijin edar dari Kepala Badan Pengawas Obat dan Makanan (Direktorat Jenderal Pengawas Obat dan Makanan RI, 2005).
Menurut survei, kasus yang paling sering muncul adalah dari penandaan atau pelabelan obat tradisional. Hasil survei yang diadakan Yayasan Pemberdayaan Konsumen Kesehatan Indonesia (YPKKI) dan majalah TEMPO bahwa obat tradisional masih banyak yang tidak mencantumkan nomor registrasi, mencantumkan tanda pendaftaran yang fiktif dan menggunakan senyawa kimia sintesis. Hanya 3 dari 11 sampel jamu yang mencantumkan nomor registrasi sesuai dengan standar Departemen Kesehatan. Empat merek lainnya menampilkan tanda pendaftaran fiktif alias tidak sesuai dengan standar resmi. Sisanya, 4 merek jamu, tergolong liar karena tidak dibubuhi tanda registrasi apa pun (Chamim, Wiyana, Cahyani, dan Rulianto, 2001). Menurut operasi gabungan tahun 2004 yang dilakukan Badan Pengawas Obat dan Makanan (BPOM), temuan kasus obat tradisional tanpa ijin edar sebanyak 83,5% dan 16,5% mengandung bahan kimia obat (Tim Redaksi InfoPOM, 2005).
DIY/Jateng/Kalbar/Kalteng, dan belum pernah mengikuti diklat sejenis. Dalam pelatihan ini peserta akan mempelajari tentang pengetahuan umum tentang kemasan yang meliputi pengertian, jenis dan pemilihan bahan kemasan, apa yang wajib ada dalam kemasan, desain kemasan, pengenalan mesin kemasan, teknologi kemasan, praktek pengemasan (Balai Diklat Industri, 2012).
Evaluasi penandaan menggunakan standar BPOM, Peraturan Menteri Kesehatan, ASEAN, dan WHO perlu dilakukan dengan tujuan untuk perlindungan konsumen. Semakin terbukanya pasar nasional sebagai akibat dari proses globalisasi ekonomi harus tetap menjamin peningkatan kesejahteraan masyarakat serta kepastian mutu dan keamanan barang dan atau jasa yang diperoleh di pasar. Konsumen mempunyai hak untuk mendapatkan kenyamanan, keamanan, dan keselamatan dalam mengkonsumsi barang dan atau jasa, sedangkan pelaku usaha atau produsen berkewajiban untuk menjamin mutu barang dan atau jasa yang diproduksi dan diperdagangkan berdasarkan ketentuan standar mutu yang berlaku (Dewan Perwakilan Rakyat RI, 1999).
penyimpanan, dan info khusus babi, alkohol, dan pemanis buatan. Kriteria yang terdapat pada standar ASEAN tetapi tidak terdapat pada standar WHO antara lain nama dan alamat pemegang otorisasi pemasaran, rute administrasi beserta petunjuk penggunaan, dan info khusus alkohol dan penggunaan eksternal, sedangkan kriteria yang terdapat pada standar WHO tetapi tidak terdapat pada standar ASEAN adalah lama pemberian.
produk yang termasuk ke dalam dua kelompok tersebut digunakan sebagai sampel, sedangkan untuk kelompok jamu karena jumlahnya tidak diketahui secara pasti maka setiap apotek diambil 7 produk dan dengan merk yang berbeda.
1. Permasalahan
Pada penelitian ini terdapat beberapa permasalahan yang harus dievaluasi, yaitu:
a. Apakah semua produk obat tradisional yang beredar di Apotek Kota Yogyakarta telah melakukan penandaan sesuai dengan standar BPOM, Peraturan Menteri Kesehatan, ASEAN, dan WHO ?
b. Seperti apakah kesesuaian penandaan produk obat tradisional terhadap setiap kriteria standar BPOM, Peraturan Menteri Kesehatan, ASEAN, dan WHO ?
2. Keaslian penelitian
Berdasarkan data penelusuran penelitian tentang evaluasi penandaan kemasan obat tradisional yang beredar di Apotek Kota Yogyakarta berdasarkan standar BPOM, Peraturan Menteri Kesehatan, ASEAN, dan WHO sejauh ini belum pernah dilakukan. Pernah dilakukan penelitian sejenis yang dilakukan oleh (Prilianti, 2008) dengan judul Evaluasi Kerasionalan Produk Obat Anti Jerawat yang Tergolong Kosmetik, Obat Bebas, dan Obat Bebas Terbatas yang Beredar di
Makanan HK.00.05.4.1745 dan terdapat 100% produk yang memenuhi kerasionalan kelengkapan informasi menurut WHO dan Perauran Pemerintah RI nomor 72 tahun 1998. Persamaan pada penelitian ini dengan penelitian yang peneliti lakukan sebelumnya adalah dalam hal kajian pokok yang diteliti, yaitu mengenai evaluasi sediaan farmasi di Apotek berdasarkan standar, sedangkan perbedaannya terletak pada jenis sediaan farmasi, jenis standar yang digunakan untuk mengevaluasi, dan tahun penelitian yang dilakukan peneliti. Pada penelitian sebelumnya sediaan farmasi yang menjadi objek penelitian adalah obat jerawat, sedangkan pada penelitian ini adalah obat tradisional.
3. Manfaat penelitian
a. Manfaat teoritis. Penelitian ini diharapkan dapat memberikan informasi kesesuaian obat tradisional yang beredar di Apotek Kota Yogyakarta berdasarkan standar penandaan kemasan BPOM, Peraturan Menteri Kesehatan, ASEAN, dan WHO.
B. Tujuan Penelitian
1. Tujuan umum
Penelitian ini dilakukan dengan tujuan untuk mengetahui informasi dari obat tradisional yang beredar di Apotek Kota Yogyakarta yang memenuhi standar penandaan kemasan BPOM, Peraturan Menteri Kesehatan, ASEAN dan WHO.
2. Tujuan khusus
a. Mengetahui apakah obat tradisional yang beredar di Apotek Kota Yogyakarta telah memenuhi standar penandaan kemasan berdasarkan BPOM, Peraturan Menteri Kesehatan, ASEAN, dan WHO.
8 BAB II
PENELAAHAN PUSTAKA
A. Penandaan (Pelabelan)
Menurut Keputusan Kepala Badan Pengawas Obat dan Makanan
HK.00.05.41.1384 tahun 2005, penandaan adalah keterangan yang lengkap mengenai khasiat, keamanan dan cara penggunaan serta informasi lain yang dianggap perlu untuk dicantumkan pada etiket dan atau brosur yang disertakan pada jamu, obat herbal terstandar, dan fitofarmaka (Direktorat Jenderal Pengawas Obat dan Makanan RI, 2005).
Menurut Peraturan Departemen Kesehatan Republik Indonesia No.246/Menkes/Per/V/1990, penandaan adalah tulisan atau gambar yang dicantumkan pada pembungkus, brosur, wadah atau etiket, yang disertakan pada obat tradisional dan berfungsi memberikan informasi tentang obat tradisional (Departemen Kesehatan Republik Indonesia, 1990).
Setiap informasi tentang suatu produk dapat dilihat dari label yang tertera pada kemasan. Label dapat didefinisikan sebagai tulisan, tag, gambar atau pengertian lain yang ditulis, dicetak, distensil, diukir, dihias atau dicantumkan dengan cara apapun dan dapat memberikan kesan dari suatu produk yang terdapat
pada suatu wadah atau kemasan (Siagian, 2002). Label merupakan bagian dari
(1) Label dapat mengidentifikasi produk atau merek,
(2) label mempromosikan produk dengan menarik perhatian konsumen melalui
warna dan grafik menarik yang memberikan petunjuk visual bagi produk yang sesungguhnya,
(3) label menggambarkan produk melalui informasi tentang kandungan nutrisi,
petunjuk penggunaan cara membuang yang tepat, dan keamanan (Soegoto, 2009).
B. Kemasan
Saat akan membeli suatu produk dalam kemasan, hal yang pertama kali dilihat oleh konsumen adalah kemasan produk. Kemasan adalah barang yang dipakai untuk mewadahi atau membungkus makanan yang berhubungan langsung dengan isi, termasuk penutupnya (Direktorat Jenderal Pengawas Obat dan Makanan RI, 1991). Menurut Peraturan Departemen Kesehatan Republik Indonesia Nomor: 722/Menkes/Per/IX/88, kemasan eceran adalah kemasan berlabel dalam ukuran yang sesuai untuk konsumen, tidak ditujukan untuk industri pengolahan makanan (Departemen Kesehatan Republik Indonesia, 1988).
Menurut Peraturan Pemerintah RI nomor 72 tahun 1998, kemasan sediaan farmasi dan alat kesehatan adalah bahan yang digunakan untuk mewadahi dan/atau membungkus sediaan farmasi dan alat kesehatan baik yang bersentuhan langsung maupun tidak. Pengemasan sediaan farmasi dan alat kesehatan dilaksanakan dengan menggunakan bahan kemasan yang tidak membahayakan kesehatan manusia dan/atau dapat mempengaruhi berubahnya persyaratan mutu, keamanan, dan kemanfaatan sediaan farmasi dan alat kesehatan. (Dewan Perwakilan Rakyat RI, 1998).
C. Apotek
Menurut PP No. 51 tahun 2009, tugas dan fungsi Apotek, yaitu :
a. Tempat pengabdian profesi seorang apoteker yang telah mengucapkan sumpah jabatan apoteker;
b. Sarana yang digunakan untuk melakukan pekerjaan kefarmasian;
c. Sarana yang digunakan untuk memproduksi dan distribusi sediaan farmasi, antara lain obat, bahan baku obat, obat tradisional, dan kosmetika;
d. Sarana pembuatan dan pengendalian mutu sediaan farmasi, pengamanan, pengadaan, penyimpanan dan pendistribusi atau penyaluran obat, pengelolaan obat, pelayanan obat atas resep dokter, pelayanan informasi obat, serta pengembangan obat, bahan obat dan obat tradisional (Dewan Perwakilan Rakyat RI, 2009).
D. Obat Tradisional 1. Definisi
Menurut Peraturan Departemen Kesehatan Republik Indonesia Nomor: 246/Menkes/Per/V/1990, obat tradisional adalah bahan atau ramuan bahan yang berupa bahan tumbuhan, bahan hewan, bahan mineral, sediaan sarian (galenik) atau campuran dari bahan tersebut, yang secara turun-temurun telah digunakan untuk pengobatan berdasarkan pengalaman (Departemen Kesehatan Republik Indonesia, 1990).
tersebut yang secara turun temurun digunakan untuk pengobatan, dan dapat diterapkan sesuai dengan norma yang berlaku di masyarakat (Dewan Perwakilan Rakyat RI, 2009).
Menurut Badan Pengawas Obat dan Makanan Republik Indonesia No: HK.00.05.4.2411, obat tradisional adalah bahan atau ramuan bahan yang berupa bahan tumbuhan, bahan hewan, bahan mineral, sediaan sarian (galenik) atau campuran dari bahan tersebut, yang secara turun-temurun telah digunakan untuk pengobatan berdasarkan pengalaman (Direktorat Jenderal Pengawas Obat dan Makanan RI, 2004).
Menurut WHO Traditional Medicine Strategy 2002-2005, obat
tradisional adalah istilah yang komprehensif yang digunakan untuk merujuk baik
untuk bentuk obat tradisional seperti obat tradisional Cina (Traditional Chinese
2. Sediaan obat tradisional
a. Rajangan, yaitu sediaan obat tradisional berupa potongan simplisia, campuran simplisia, atau campuran simplisia dengan sediaan galenik yang penggunannya dilakukan dengan pendidihan atau penyeduhan dengan air panas (Departemen Kesehatan Republik Indonesia, 1994).
b. Serbuk, yaitu sediaan obat tradisional berupa butiran homogen dengan derajat halus yang cocok; bahan bakunya berupa simplisia sediaan galenik, atau campurannya (Departemen Kesehatan Republik Indonesia, 1994). c. Pil, yaitu sediaan padat obat tradisional berupa massa bulat; bahan
bakunya berupa serbuk simplisia, sediaan galenik, atau campurannya (Departemen Kesehatan Republik Indonesia, 1994).
d. Dodol atau jenang, yaitu sediaan padat obat tradisional; bahan bakunya berupa serbuk simplisia, sediaan galenik atau campurannya (Departemen Kesehatan Republik Indonesia, 1994).
e. Pastiles, yaitu sediaan padat obat tradisional berupa lempengan pipih umumnya berbentuk segi empat; bahan bakunya berupa serbuk simplisia, sediaan galenik, atau campurannya (Departemen Kesehatan Republik Indonesia, 1994).
f. Kapsul, yaitu sediaan obat tradisional yang terbungkus cangkang keras
atau lunak; bahan bakunya berupa serbuk simplisia, sediaan galenik, atau campurannya (Departemen Kesehatan Republik Indonesia, 1994).
rata atau cembung, terbuat dari sediaan galenik dengan atau tanpa bahan tambahan (Departemen Kesehatan Republik Indonesia, 1994).
h. Cairan obat dalam, yaitu sediaan obat tradisional berupa larutan emulsi atau suspense dalam air; bahan bakunya berasal dari serbuk simplisia atau sediaan galenik dan digunakan sebagai obat dalam (Departemen Kesehatan Republik Indonesia, 1994).
i. Sari jamu, yaitu cairan obat dalam, dengan tujuan tertentu diperbolehkan
mengandung etanol. Kadar etanol tidak lebih dari 1% v/v pada suhu 20°C
dan kadar methanol tidak lebih dari 0,1% jika dihitung terhadap kadar etanol (Departemen Kesehatan Republik Indonesia, 1994).
j. Parem, pilis dan tapel, yaitu sediaan padat obat tradisional; bahan bakunya
berupa serbuk simplisia, sediaan galenik, atau campurannya dan digunakan sebagai obat luar (Departemen Kesehatan Republik Indonesia, 1994).
k. Koyok, yaitu sediaan obat tradisional berupa pita kain yang cocok dan tahan air yang dilapisi dengan serbuk simplisia dan atau sediaan galenik, digunakan sebagai obat obat luar dan pemakaiannya ditempelkan pada kulit (Departemen Kesehatan Republik Indonesia, 1994).
l. Cairan obat luar, yaitu sediaan obat tradisional berupa larutan suspense
m. Salep/krim, yaitu sediaan setengah padat yang mudah dioleskan, bahan bakunya berupa sediaan galenik yang larut atau terdispersi homogen dalam dasar salep/krim yang cocok dan digunakan sebagai obat luar (Menteri Kesehatan, 1994).
n. Teh, yaitu sediaan obat tradisional dapat dibuat secara produk tunggal dan campuran dengan bahan lain. Produk tunggal dibuat dari tanaman obat yang telah dikeringkan, kemudian dikemas dalam kantong kertas. Sementara jenis sediaan obat tradisional berupa teh dapat dibuat secara campuran dari beberapa serbuk tanaman yang telah dikeringkan. Penggunaannya dilakukan dengan cara diseduh air mendidih (Rukmana,
2003).
E. Klasifikasi Obat Tradisional
Obat tradisional dapat dikelompokkan menjadi beberapa macam
berdasarkan Keputusan Badan Pengawas Obat dan Makanan RI No:
HK.00.05.4.2411, berdasarkan cara pembuatannya serta jenis klaim penggunaan dan tingkat pembuktian khasiat, obat bahan alam di Indonesia dikelompokkan menjadi:
a. Jamu
b. Obat herbal terstandar
1. Jamu
Jamu adalah obat tradisional Indonesia yang secara turun temurun telah digunakan untuk pengobatan dan diterapkan berdasarkan pengalaman (Direktorat Jenderal Pengawas Obat dan Makanan RI, 2004). Berdasarkan Keputusan Badan Pengawas Obat dan Makanan RI No: HK.00.05.4.2411 pasal 2, yaitu jamu harus memenuhi kriteria aman sesuai dengan persyaratan yang ditetapkan, klaim khasiat dibuktikan berdasarkan data empiris, dan memenuhi persyaratan mutu yang berlaku; jenis klaim penggunaan sesuai dengan jenis pembuktian tradisional dan tingkat pembuktiannya, yaitu tingkat pembuktian umum dan medium dan jenis klaim penggunaan harus diawali dengan kata-kata “secara tradisional digunakan untuk …”, atau sesuai dengan yang disetujui pada pendaftaran (Direktorat Jenderal Pengawas Obat dan Makanan RI, 2004).
2. Obat herbal terstandar
Obat herbal terstandar merupakan sediaan obat bahan alam yang telah dibuktikan keamanan dan khasiatnya secara ilmiah dengan uji pra klinik dan bahan bakunya telah distandarisasi. Obat herbal terstandar harus memenuhi kriteria sebagai berikut.
(a.) Aman sesuai dengan persyaratan yang ditetapkan, (b.) klaim khasiat dibuktikan secara ilmiah atau pra klinik.
(d.) memenuhi persyaratan yang berlaku (Direktorat Jenderal Pengawas Obat dan Makanan RI, 2004).
Jenis klaim penggunaan sesuai dengan tingkat pembuktian, yaitu tingkat pembuktian umum dan medium (Direktorat Jenderal Pengawas Obat dan Makanan RI, 2004).
3. Fitofarmaka
Fitofarmaka merupakan sediaan obat bahan alam yang telah dibuktikan keamanan dan khasiatnya secara ilmiah dengan uji pra klinik dan uji klinik, bahan baku dan produk jadinya telah distandarisasi. Fitofarmaka harus memenuhi kriteria sebagai berikut.
(a.) Aman sesuai dengan persayaratan yang ditetapkan, (b.) klaim khasiat harus dibuktikan berdasarkan uji klinik,
(c.) telah dilakukan standarisasi terhadap bahan baku yang digunakan dalam produk jadi, dan
(d.) memenuhi persyaratan mutu yang berlaku (Direktorat Jenderal Pengawas Obat dan Makanan RI, 2004).
F. Logo Kelompok Obat Tradisional
Berdasarkan Keputusan Kepala Badan Pengawas Obat dan Makanan tentang ketentuan pokok pengelompokan dan penandaan obat bahan alam Indonesia, pada pasal 5 menyatakan bahwa kelompok jamu untuk pendaftaran
baru harus mencantumkan logo dan tulisan “JAMU”. Logo berupa “RANTING
DAUN TERLETAK DALAM LINGKARAN” yang dicetak dengan warna hijau di atas warna putih atau warna lain yang menyolok kontras dengan warna
logo, dan ditempatkan pada bagian atas sebelah kiri dari
wadah/pembungkus/brosur. Tulisan “JAMU” harus jelas dan mudah dibaca,
dicetak dengan warna hitam di atas dasar warna putih atau warna lain yang
menyolok kontras dengan tulisan “JAMU”.
Gambar 1. Logo Jamu
(Direktorat Jenderal Pengawas Obat dan Makanan RI, 2004).
Pada pasal 7 disebutkan bahwa obat herbal terstandar harus
mencantumkan logo dan tulisan “OBAT HERBAL TERSTANDAR”. Logo
berupa “JARI-JARI DAUN (3 PASANG) TERLETAK DALAM
LINGKARAN” yang dicetak dengan warna hjau di atas dasar warna putih atau warna lain yang menyolok kontras dengan warna logo dan ditempatkan pada
bagian atas sebelah kiri dari wadah/pembungkus/brosur. Tulisan “OBAT
warna hitam di atas dasar warna putih atau warna lain yang menyolok kontras
dengan tulisan “OBAT HERBAL TERSTANDAR”.
Gambar 2. Logo Obat Herbal Terstandar
(Direktorat Jenderal Pengawas Obat dan Makanan RI, 2004). Pada pasal 8, kelompok Fitofarmaka sebagaimana dimaksud harus
mencantumkan logo dan tulisan “FITOFARMAKA”. Logo berupa “JARI-JARI
DAUN (YANG KEMUDIAN MEMBENTUK BINTANG) TERLETAK DALAM LINGKARAN” yang dicetak dengan warna hijau di atas warna putih atau warna lain yang menyolok kontras dengan warna logo dan ditempatkan pada
bagian atas sebelah kiri dari wadah/pembungkus/brosur. Tulisan
“FITOFARMAKA” harus jelas dan mudah dibaca, dicetak dengan warna hitam diatas dasar warna putih atau warna lain yang menyolok kontras dengan tulisan “FITOFARMAKA”.
Gambar 3. Logo fitofarmaka
(Direktorat Jenderal Pengawas Obat dan Makanan RI, 2004).
memberikan informasi yang konsisten sesuai dengan peraturan masing-masing Negara (Prilianti, 2008).
1. Keputusan Kepala Badan Pengawas Obat dan Makanan
a. Berdasarkan Keputusan Kepala Badan Pengawas Obat dan Makanan HK.00.05.23.0279 tahun 2002 tentang pencantuman asal bahan tertentu, kandungan alkohol, dan tanggal kadaluwarsa pada penandaan atau label obat, obat tradisional, suplemen makanan, dan pangan :
Pasal 3 menjelaskan bahwa obat, obat tradisional, dan suplemen makanan, dan pangan yang mengandung bahan tertentu harus mencantumkan asal dan keterangan bahan tertentu tersebut pada komposisi penandaan atau label dan mencantumkan tulisan “Bersumber Babi” dalam kontak dengan warna putih pada pada penandaan label (Direktorat Jenderal Pengawas Obat dan Makanan RI, 2002). Pasal 6 menjelaskan tentang penulisan tanggal kadaluwarsa, yaitu tanggal ditulis dengan angka, bulan ditulis dengan huruf, dan tahun ditulis dengan angka (Direktorat Jenderal Pengawas Obat dan Makanan RI, 2002).
b. Berdasarkan Keputusan Kepala Badan Pengawas Obat dan Makanan HK.00.05.41.1384 tahun 2005 tentang kriteria dan tata laksana pendaftaran obat tradisional, obat herbal terstandar dan fitofarmaka :
warna; Brosur yang mencantumkan informasi mengenai obat tradisional, obat herbal terstandar, dan fitofarmaka (Direktorat Jenderal Pengawas Obat dan Makanan RI, 2005).
Tabel I. Informasi yang Harus Dicantumkan pada Kemasan Obat Tradisional Berdasarkan Standar BPOM
No.
Informasi yang harus dicantumkan Pembungkus/bungkus luar
1. Nama obat tradisional/obat herbal
terstandar/fitofarmaka √
2. Bentuk sediaan √
3. Besar kemasan √
4. Komposisi √
5. Logo obat tradisional/obat herbal
terstandar/fitofarmaka √
6. Nama pendaftar √
7. Alamat pendaftar √
Nama industri negara asal/pemberi
lisensi/penerima kontrak √
Alamat industri negara asal/pemberi
lisensi/penerima kontrak √
√ = informasi harus dicantumkan
2. Peraturan Menteri Kesehatan
Berdasarkan Peraturan Menteri Kesehatan Nomor:
246/Menkes/Per/V/1990 tentang ijin usaha obat tradisional dan pendaftaran obat tradisional informasi yang harus dicantumkan pada kemasan adalah sebagai berikut:
Tabel II. Informasi yang Harus Dicantumkan pada Kemasan Obat Tradisional Berdasarkan Peraturan Menteri Kesehatan
No Informasi yang harus dicantumkan
1. Nama obat tradisional atau nama dagang
2. Logo
3. Komposisi (ditulis dengan tata nama latin)
4. Bobot, isi atau jumlah obat tiap wadah
5. Dosis pemakaian
6. Khasiat atau kegunaan
7. Kontra indikasi (bila ada)
8. Kadaluwarsa
9. Nomor pendaftaran (nomor ijin edar)
10. Nomor kode produksi
11. Nama industri atau alamat sekurang-kurangaya nama kota dan kata
“INDONESIA"
12. Untuk obat tradisional lisensi harus dicantumkan juga nama dan alamat
industri pemberi lisensi; sesuai dengan yang disetujui pada pendaftaran.
13. Ditulis dalam bahasa Indonesia dengan huruf latin.
Sumber: Departemen Kesehatan Republik Indonesia, 1990.
3. ASEAN
Berdasarkan ASEAN- The final list of the harmonized labeling
Tabel III. Informasi yang Harus Dicantumkan pada Kemasan Obat Tradisional Berdasarkan Standar ASEAN
No Informasi yang harus dicantumkan
1. Nama produk
2. Logo
3. Bentuk sediaan
4. Komposisi bahan aktif dengan tata nama latin dan kekuatan bahan aktif
5. Nomor batch
6. Manufaktur dan tanggal kadaluwarsa atau hanya tanggal kadaluwarsa 7. Rute administrasi
8. Penggunaan dan indikasi penggunaan 9. Kondisi penyimpanan
10. Negara registrasi / properti / nomor pemberitahuan (jika berlaku) 11. Nama dan alamat produsen
12. Nama dan alamat pemegang otorisasi pemasaran 13. Peringatan (jika ada)
14. Besar kemasan
15.
Pernyataan khusus: - Kandungan alkohol
- Untuk penggunaan eksternal (untuk obat tradisional) 16. Bahasa nasional dan / atau bahasa Inggris
Sumber: ASEAN, 2011.
4. WHO (World Health Organization)
Berdasarkan WHO-Regulatory Situation of Herbal Medicines A
Tabel IV. Informasi yang Harus Dicantumkan pada Kemasan Obat Tradisional Berdasarkan Standar WHO
No Informasi yang harus dicantumkan
1. Label jelas dan mudah dibaca
2. Ditulis dalam bahasa Indonesia / latin utuk senyawa aktif
3. Ditandai dengan emblem khusus misal daun
4. Nomor pendaftaran (nomor ijin edar)
5. Nama dan alamat perusahaan
6. Komposisi
7. Indikasi
8. Petunjuk penggunaan dan dosis
9. Lama pemberian
10. Peringatan
11. Kontraindikasi
12. Penyimpanan
13. Tanggal kadaluwarsa
14. Kode produksi (nomor batch)
Sumber: WHO, 1998.
H. Landasan Teori
personalia yang menangani. Penerapan CPOTB merupakan persyaratan kelayakan dasar untuk menerapkan sistem jaminan mutu yang diakui dunia internasional. Selain itu, obat tradisional juga harus memenuhi Kriteria dan Tata Laksana Pendaftaran Obat Tradisional, Obat Herbal Terstandar dan Fitofarmaka.
Semua produk obat tradisional yang beredar di Apotek Kota Yogyakarta merupakan produk yang terjamin mutu dan kualitasnya karena di bawah pengawasan BPOM sehingga informasi yang terdapat pada kemasan obat tradisional minimal memenuhi persyaratan kriteria dari BPOM.
I. Hipotesis
26 BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian mengenai evaluasi penandaan kemasan obat tradisional yang beredar di Apotek Kota Yogyakarta berdasarkan standar BPOM, Peraturan Menteri Kesehatan, ASEAN, dan WHO merupakan penelitian non eksperimental dengan rancangan observasional deskriptif evaluatif yang bersifat retrospektif.
Disebut penelitian non eksperimental karena pada penelitian ini dilakukan observasi terhadap variabel subjek menurut keadaan apa adanya, tanpa manipulasi atau intervensi peneliti (Pratiknya, 2001), dan disebut penelitian observasional karena menggunakan teknik pendekatan guna mendapatkan data primer dengan cara langsung mengamati objek datanya (Jogiyanto, 2008). Rancangan penelitian disebut deskriptif evaluatif karena tujuan penelitian, yaitu memberikan gambaran informasi dan evaluasi mengenai obat tradisional yang telah memenuhi standar BPOM, Peraturan Menteri Kesehatan, ASEAN, dan WHO (Notoatmodjo, 2002). Penelitian ini bersifat retrospektif karena data yang digunakan dalam penelitian ini berupa informasi yang sudah melekat pada produk obat tradisional yang beredar.
B. Variabel Penelitian
1. Variabel bebas (independent)
Adalah tingkat pengetahuan produsen.
2. Variabel tergantung (dependent)
Adalah jumlah kriteria yang memenuhi standar BPOM, Peraturan Menteri Kesehatan, ASEAN dan WHO.
C. Definisi Operasional
Berikut ini adalah batasan mengenai penelitian yang akan dilakukan. 1. Evaluasi yang dimaksud adalah menilai adanya informasi yang tercantum pada kemasan produk obat tradisional kemudian dibandingkan dengan informasi menurut BPOM HK.00.05.41.1384 tahun 2005, Peraturan Menteri Kesehatan Nomor: 246/Menkes/Per/V/1990, ASEAN, dan WHO.
2. Penandaan merupakan tulisan atau gambar yang dicantumkan pada kemasan yang disertakan pada obat tradisional, yang memberikan informasi tentang obat tradisional tersebut. Standar penandaan yang digunakan untuk mengevaluasi
adalah berdasarkan BPOM, Peraturan Menteri Kesehatan Nomor:
246/Menkes/Per/V/1990, ASEAN, dan WHO.
a) Menurut BPOM HK.00.05.41.1384 tahun 2005 kriteria yang harus tercantum
dalam penandaan meliputi nama obat tradisional/obat herbal
nomor ijin edar, nomor batch, batas kadaluwarsa, klaim penggunaan, kontraindikasi, efek samping, interaksi obat, cara penyimpanan, dan informasi sesuai ketentuan yang belaku.
b) Peraturan Menteri Kesehatan Nomor: 246/Menkes/Per/V/1990 tentang izin usaha obat tradisional dan pendaftaran obat tradisional, yang harus tercantum dalam penandaan meliputi nama obat tradisional atau nama dagang, komposisi, bobot, isi atau jumlah obat tiap wadah, dosis pemakaian, khasiat atau kegunaan, kontraindikasi (bila ada), kadaluwarsa, nomor pendaftaran, nomor kode produksi, nama industri atau alamat sekurang-kurangaya nama kota dan kata “Indonesia", dan ditulis dalam bahasa indonesia dengan huruf latin.
c) Berdasarkan ASEAN-The final list of the harmonized labeling requirements
for TMHS yang harus tercantum dalam penandaan meliputi nama produk, bentuk
sediaan, komposisi bahan aktif dan kekuatan bahan aktif, nomor batch,
manufaktur dan tanggal kadaluwarsa atau hanya tanggal kadaluwarsa , rute administrasi, penggunaan dan indikasi penggunaan, kondisi penyimpanan , negara registrasi/properti/nomor pemberitahuan (jika berlaku), nama dan alamat produsen, nama dan alamat pemegang otorisasi pemasaran, peringatan (jika ada), ukuran pengemas, pernyataan khusus, yaitu untuk penggunaan eksternal dan kandungan alkohol, bahasa nasional dan/atau bahasa inggris dan latin untuk nama-nama bahan aktif (tanama-naman atau hewan).
Indonesia/latin, ditandai dengan emblem khusus misal daun, nomor pendaftaran, nama dan alamat perusahaan ,komposisi, indikasi, metode penggunaan dan dosis, lama pemberian, peringatan, kontraindikasi, penyimpanan, tanggal kadaluwarsa, dan kode produksi.
3. Dalam penelitian ini obat tradisional adalah obat yang termasuk golongan jamu, obat herbal terstandar, dan fitofarmaka.
4. Apotek yang digunakan dalam pengambilan sampel untuk penelitian adalah Apotek di Kota Yogyakarta yang memberikan ijin penelitian.
5. Nama pendaftar yang dimaksud adalah nama produsen yang mendaftar.
D. Subjek Penelitian dan Teknik Sampling
Subjek pada penelitian ini, yaitu Apotek di Kota Yogyakarta yang memberikan ijin penelitian. Objek pada penelitian ini adalah obat tradisional yang meliputi jamu, obat herbal terstandar, dan fitofarmaka. Yang termasuk kriteria inklusi, yaitu Apotek di Kota Yogyakarta yang memberikan ijin penelitian dan obat tradisional dalam negeri yang tergolong jamu, obat herbal terstandar, dan fitofarmaka. Yang termasuk kriteria eksklusi, yaitu Apotek di Kota Yogyakarta yang tidak memberikan ijin penelitian, obat tradisional import, obat tradisional lisensi, obat yang tidak tergolong jamu, obat herbal terstandar, dan fitofarmaka.
produk. Pada kelompok fitofarmaka dan obat herbal terstandar jumlahnya hanya sedikit, maka sampel yang ada akan diambil semua, yaitu fitofarmaka sebanyak 5 produk dan obat herbal terstandar sebanyak 19 produk.
Menurut Gay (1976) dan kemudian dikutip oleh Sevilla, pengambilan sampel untuk bahan penelitian deskriptif adalah 10% dari populasi. Untuk populasi yang sangat kecil diperlukan minimal 20% (Sevilla, 1993).
Jumlah Apotek di kota Yogyakarta berdasarkan data Dinas Kesehatan Kota Yogyakarta tahun 2011 sebanyak 126 Apotek. Jumlah Apotek yang digunakan untuk pengambilan sampel sebanyak 20% x 126 Apotek = 25,2 Apotek. Hasil tersebut dapat dibulatkan menjadi 25 Apotek. Dalam menentukan
lokasi penelitian dan pengambilan sampel digunakan teknik non random (non
probability sampling). Sampling dilakukan dengan metode purposive sampling, yaitu pengambilan sampel didasarkan atas pertimbangan tertentu yang dibuat oleh peneliti sendiri berdasarkan ciri atau sifat populasi. Dalam menentukan ciri atau sifat populasi pada penelitian ini dengan cara menggunakan kriteria inklusi dan eksklusi. Sampel yang termasuk dalam kriteria inklusi yang selanjutnya digunakan sebagai objek penelitian.
E. Alat atau Instrumen Penelitian
Instrument penelitian yang digunakan adalah lembar pengambilan data
(check list). Check list adalah suatu daftar untuk mencocokan yang berisi nama
subjek dan beberapa gejala serta identitas lainnya dari sasaran pengamatan
informasi pada kemasan produk obat tradisional terhadap standar BPOM, Peraturan Menteri Kesehatan, ASEAN, dan WHO. Selain itu untuk perhitungan data digunakan kalkulator dan program Microsoft Excel.
F. Lokasi Penelitian
Lokasi yang akan digunakan dalam penelitian ini adalah 25 Apotek yang tersebar di Kota Yogyakarta.
G. Tata Cara Penelitian
1. Analisis situasi
Analisis situasi dengan melakukan perijinan dan observasi lokasi di Apotek Kota Yogyakarta. Perijinan dilakukan dengan memberikan surat pengantar dari Universitas Sanata Dharma kepada Dinas Perijinan untuk mendapatkan surat ijin penelitian di 25 Apotek yang terpilih. Surat tersebut kemudian akan diberikan kepada setiap pengelola Apotek. Observasi dilakukan dengan melihat informasi yang tertera pada kemasan obat tradisional.
2. Pengambilan data
Data diambil dengan mengamati penandaan, yaitu informasi yang tertera pada kemasan obat tradisional yang meliputi jamu, obat herbal terstandar, dan
fitofarmaka, kemudian dimaksukkan dalam lembaran check listyang berisi daftar
menggunakan 4 standar, yaitu dari BPOM, Peraturan Menteri Kesehatan, ASEAN, dan WHO.
H. Analisis Hasil
1. Kesesuaian Obat Tradisional Berdasarkan Standar BPOM, Peraturan Menteri Kesehatan, ASEAN, dan WHO
Masing-masing produk pada kelompok jamu, obat herbal terstandar, dan fitofarmaka dihitung persentase kelengkapan informasinya berdasarkan standar BPOM, Peraturan Menteri Kesehatan, ASEAN dan WHO. Setelah itu selanjutnya dihitung persentase rata-rata kesesuaian kelompok jamu, obat herbal terstandar, dan fitofarmaka terhadap masing-masing standar. Data kualitatif yang diperoleh dibahas dalam bentuk uraian dan secara deskriptif dalam bentuk gambar diagram.
Perhitungan persentase setiap produk adalah sebagai berikut:
Setelah didapatkan persentase setiap produk, kemudian dikelompokkan berdasarkan nilai persentasenya dan dilihat persentase yang paling sering muncul atau persentase modus.
2. Kesesuaian Penandaan Produk Obat Tradisional Terhadap Setiap Kriteria Standar BPOM, Peraturan Menteri Kesehatan, ASEAN, dan WHO
34 BAB IV
HASIL DAN PEMBAHASAN
A. Persentase Kesesuaian Obat Tradisional Berdasarkan Standar BPOM, Peraturan Menteri Kesehatan, ASEAN, dan WHO
Obat tradisional dibagi menjadi tiga kelompok, yaitu jamu, obat herbal terstandar dan fitofarmaka. Ketiga kelompok tersebut memiliki jenis klaim penggunaan dan tingkat pembuktian khasiat yang berbeda-beda. Jamu klaim khasiat dibuktikan berdasarkan data empiris, obat herbal terstandar keamanan dan khasiatnya dibuktikan secara ilmiah dengan uji pra klinik dan bahan bakunya telah distandarisasi, sedangkan fitofarmaka keamanan dan khasiatnya dibuktikan secara ilmiah dengan uji pra klinik dan uji klinik, serta bahan baku dan produk jadinya telah distandarisasi. Jamu dan obat herbal terstandar tingkat pembuktiannya umum dan medium sedangkan fitofarmaka tingkat pembuktiannya medium dan tinggi (Direktorat Jenderal Pengawas Obat dan Makanan RI, 2004).
Setiap produk obat tradisional yang beredar harus memenuhi standar mutu yang berlaku. Mutu obat tradisional tidak hanya dilihat dari cara pembuatannya akan tetapi juga penandaannya. Di Indonesia terdapat dua standar yang mengatur terkait penandaan obat tradisional, yaitu Peraturan Menteri Kesehatan dan BPOM sedangkan standar internasional yang mengatur antara lain adalah ASEAN dan WHO.
Produk obat tradisional berkualitas akan memberikan jaminan mutu untuk konsumennya. Jaminan mutu tersebut dapat dilakukan dengan memberikan penandaan yang sesuai dengan standar.
1. Standar BPOM
Gambar 4. Diagram Batang
Berdasarkan gambar tingkat kesesuaian jamu 68,75%, dan fitofarmaka fitofarmaka paling tinggi, pembuktiannya adalah medium telah dilakukan standarisasi kualitasnya lebih tinggi
Jenderal Pengawasan Obat dan Makan Persentase tingkat
tinggi dari pada kelompok ketiga kelompok obat herbal ada yang melampaui 70%. kriteria informasi yang harus dikarenakan terdapat 2 produk
0%
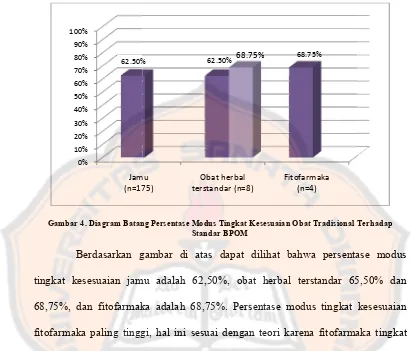
. Diagram Batang Persentase Modus Tingkat Kesesuaian Obat Tradisional Terhadap Standar BPOM
Berdasarkan gambar di atas dapat dilihat bahwa persentase suaian jamu adalah 62,50%, obat herbal terstandar 65,50
fitofarmaka adalah 68,75%. Persentase modus tingkat kese tinggi, hal ini sesuai dengan teori karena fitofarmaka
adalah medium dan tinggi. Selain itu pada kelompok fitofarmaka standarisasi bahan baku dan produk jadinya, sehingga mutu
tinggi dari pada jamu dan obat herbal terstandar. (Direktorat n Obat dan Makanan RI, 2004).
se tingkat kesesuaian kelompok obat herbal terstandar kelompok jamu, atau dapat dikatakan sesuai dengan teori.
obat herbal terstandar, persentase tingkat kesesuaiannya ui 70%. Rendahnya persentase kesesuaian tersebut dikare yang harus dicantumkan cukup rinci dan banyak. terdapat 2 produk yang diambil di Apotek merupakan stock
Jamu
ian Obat Tradisional Terhadap
sehingga dimungkinkan be obat tradisional tidak ada sehingga dapat dikatakan penandaan BPOM.
2. Standar Peraturan Menteri Secara tingkatan
BPOM namun kriteria standar Kesehatan belum terdapat
BPOM sudah terdapat pengelompokan terstandar dan fitofarmaka.
pengelompokan khusus antara pembeda adalah dari segi
Peraturan Menteri Kesehatan tetap digunakan
Gambar 5. Diagram Batang 0%
dimungkinkan belum sesuai dengan standar yang ada. Ketiga kelompok tidak ada yang memiliki persentase modus yang mencapa
dikatakan bahwa tidak semua produk jamu memenuhi
Standar Peraturan Menteri Kesehatan
tingkatan Peraturan Menteri Kesehatan lebih tinggi dari kriteria standar BPOM jauh lebih lengkap. Pada Peraturan
terdapat pengelompokan obat tradisional sedangkan terdapat pengelompokan obat tradisional, yaitu jamu, obat
fitofarmaka. Secara umum dalam penandaan tidak khusus antara ketiga kelompok obat tradisional dan yang
dari segi logo, oleh karena itu pada penelitian ini ri Kesehatan tetap digunakan untuk mengevaluasi.
. Diagram Batang Persentase Modus Tingkat Kesesuaian Obat Tradisional Terhadap Standar Peraturan Menteri Kesehatan penelitian ini standar
Berdasarkan gambar di atas dapat dilihat bahwa fitofarmaka memiliki persentase modus kesesuaian paling besar, yaitu 91,67% dan 100%, jamu 91,67% dan obat herbal terstandar 91,67%. Persentase kesesuaian kelompok jamu dan obat herbal terstandar adalah sama, yaitu sebesar 91,67%. Dilihat dari gambar 4. dan gambar 5. persentase modus tingkat kesesuaian ketiga kelompok obat tradisional terhadap standar Peraturan Menteri Kesehatan terlihat lebih besar dibandingkan dengan kesesuaian terhadap standar BPOM. Hal ini dikarenakan kriteria standar yang ditetapkan oleh BPOM lebih banyak dan lebih rinci. Kriteria yang terdapat pada standar BPOM tetapi tidak terdapat pada standar Peraturan Menteri Kesehatan antara lain bentuk sediaan, nama dan alamat pemberi/penerima kontrak, efek samping, interaksi obat, dan info khusus terkait kandungan babi, alkohol dan pemanis buatan. Menurut gambar 5. diatas, tidak semua kelompok obat tradisional memiliki persentase modus yang mencapai 100%. Hal ini menunjukkan bahwa tidak semua produk obat tradisional memenuhi standar Peraturan Menteri Kesehatan.
3. Standar ASEAN
Suplemen Kesehatan Indonesia InfoPOM, 2008). Harmonisasi industri obat tradisioanal. ini, sebuah produk yang bereda melakukan registrasi kembali, keberadaan harmonisasi bisa dengan bebas masuk tradisional Indonesia harus dikuasai produk dari ASEA merupakan kriteria yang
produk obat tradisional harus benar
Gambar 6. Diagram Batang
Berdasarkan gambar tingkat kesesuaian yang
0%
Kesehatan Indonesia (APSKI) hadir sebagai observer (Tim Harmonisasi ASEAN ini tentunya sangat menguntungkan tradisioanal. Melalui kesamaan regulasi di negara-negara produk yang beredar di Indonesia dapat beredar di ASEAN tan
registrasi kembali, namun di sisi lain terdapat juga ancaman harmonisasi ini. Produk-produk sejenis dari anggota ASEAN
masuk ke Indonesia. Untuk itu, industri jamu dan obat harus memperkuat daya saing agar pasar domestik dari ASEAN ini. Kriteria standar yang ditetapkan kriteria yang dibuat seragam untuk wilayah Asia Tenggara produk obat tradisional harus benar-benar memperhatikan kualitas dan mutu.
. Diagram Batang Persentase Modus Tingkat Kesesuaian Obat Tradisional Terhadap Standar ASEAN
gambar di atas dapat dilihat bahwa persentase kesesuaian yang paling tinggi adalah kelompok fitofarmaka
Jamu beredar di ASEAN tanpa perlu juga ancaman dari
ian Obat Tradisional Terhadap
87,5%, kemudian jamu sebesar 75%, dan obat herbal terstandar sebesar 68,75%. Persentase kelompok fitofarmaka yang paling tinggi menandakan bahwa kelompok fitofarmaka paling memenuhi kriteria standar dibandingkan dengan jamu dan obat herbal terstandar. Kelompok obat herbal terstandar memiliki persentase kesesuaian lebih rendah dari pada jamu, hal ini dikarenakan pada kelompok obat herbal terstandar tidak ada produk yang mencantumkan nama dan alamat pemegang otorisasi pemasaran. Jumlah kriteria standar yang ditetapkan oleh ASEAN sama dengan standar BPOM, namun jika dilihat dari gambar 4. dan gambar 6. persentase modus tingkat kesesuaian terhadap standar ASEAN lebih tinggi dibandingkan dengan standar BPOM. Hal ini dikarenakan pada standar BPOM ada kriteria kontraindikasi, interaksi obat, dan efek samping sedangkan pada standar ASEAN tidak ada. Berdasarkan gambar 6. dapat dilihat bahwa ketiga kelompok obat tradisional tidak ada yang memiliki persentase modus yang mencapai 100%, sehingga dapat dikatakan bahwa tidak semua produk obat tradisional memenuhi standar penandaan ASEAN.
4. Standar WHO
Gambar 7. Diagram Batang
Berdasarkan gambar kesesuaian tertinggi adalah terstandar dengan 86,67 dilihat dari tingkatan mutu
herbal terstandar, dan fitofarmaka. persentase tingkat kesesuaian dikarenakan adanya kriteria terstandar mencantumkan produk yang mencantumkan herbal terstandar menjadi gambar 7. dari ketiga
persentase modus yang mencapai memenuhi standar WHO.
. Diagram Batang Persentase Modus Tingkat Kesesuaian Obat Tradisional Terhadap Standar WHO
gambar di atas dapat dilihat bahwa persentase modus tertinggi adalah fitofarmaka dengan 93,33%, kemudian obat
86,67%, dan jamu dengan 80%. Ini sesuai dengan teori tingkatan mutu urutan dari yang paling tinggi adalah fitofarmaka,
dan fitofarmaka. Kelompok obat herbal terstandar mempunyai kesesuaian lebih tinggi dibandingkan dengan kelompok a kriteria lama pemberian. Dua dari 8 produk obat mencantumkan lama pemberian sedangkan pada jamu hanya 5
antumkan, sehingga persentase rata-rata tingkat kesesuaian obat menjadi lebih tinggi dibanding persentase jamu.
ketiga kelompok obat tradisional tidak ada yang
yang mencapai 100% atau tidak semua produk obat tradisional memenuhi standar WHO. kemudian obat herbal dengan teori bahwa fitofarmaka, obat terstandar mempunyai kelompok jamu produk obat herbal
B. Persentase Kesesuaian Penandaan Produk Obat Tradisional Terhadap Setiap Kriteria Standar BPOM, Peraturan Menteri Kesehatan, ASEAN, dan WHO
Banyaknya obat tradisional yang beredar sekarang ini membuat konsumen terkadang bingung untuk memilih produk mana yang akan dibeli. Sebagai seorang konsumen seharusnya benar-benar selektif dalam memilih obat tradisional karena tidak sedikit produk obat tradisional yang beredar tidak memenuhi standar. Hal ini dapat dilihat dari temuan kasus obat tradisional tanpa ijin edar sebanyak 83,5% (Direktorat Jenderal Pengawasan Obat dan Makanan RI, 2005). Temuan kasus tersebut menandakan bahwa banyak obat tradisional yang beredar banyak yang tidak memiliki ijin edar. Pencantuman ijin edar menjadi sangat penting karena tanpa adanya ijin edar kualitas dan mutu obat tradisional tidak terjamin.
Menurut Peraturan Pemerintah RI nomor 72 tahun 1998, penandaan dan informasi suatu sediaan farmasi dan alat kesehatan bertujuan untuk melindungi konsumen dari informasi yang tidak obyektif, tidak lengkap, dan menyesatkan. Penandaan dan informasi tidak hanya berupa tulisan akan tetapi dapat berupa gambar, warna ataupun ketiganya atau bentuk lain yang disertakan pada kemasan atau dimasukkan dalam kemasan atau merupakan bagian dari wadah dan kemasannya (Dewan Perwakilan Rakyat RI, 1998).
dari suatu produk. Indikasi perlu dicantumkan pada produk obat tradisional supaya konsumen bisa memilih produk obat tradisional yang tepat untuk digunakan. Untuk produk yang tergolong obat herbal dan fitofarmaka harus mencantumkan indikasi karena obat herbal tertandar telah melalui uji pra klinik dan fitofarmaka telah melalui uji klinik. sedangkan produk yang tergolong jamu mencantumkan klaim khasiat kegunaan produk. jenis klaim penggunaan harus diawali dengan kata-kata “secara tradisional digunakan untuk …”, atau sesuai dengan yang disetujui pada pendaftaran (Direktorat Jenderal Pengawas Obat dan Makanan RI, 2004). Klaim khasiat tidak boleh menggunakan kata-kata: super, ultra, istimewa, top, tokcer, cespleng, manjur dan kata-kata lain yang semakna yang menyatakan khasiat dan kegunaan berlebihan atau memberi janji bahwa obat tradisional tersebut pasti menyembuhkan atau dengan kata lain klaim khasiat tidak boleh menyesatkan (Departemen Kesehatan Republik Indonesia,1990).
Efek samping obat adalah efek yang tidak diinginkan yang mungkin terjadi selama proses terapi. Tanda peringatan dan efek samping obat tradisional dicantumkan pada produk obat tradisional supaya konsumen berhati-hati dalam menggunakan produk obat tradisional. Pada kenyataannya tidak semua obat tradisional yang beredar mencantumkan efek samping, karena mungkin memang obat tradisional tersebut tidak menimbulkan efek samping.
Nomor ijin edar merupakan nomor yang menunjukkan bahwa suatu produk yang beredar sudah didaftarkan. Di Indonesia, produk yang beredar harus mendapatkan ijin edar dari BPOM. Produk yang tidak mencantumkan ijin edar tidak dapat dijamin kualitas, mutu, dan keamanannya.
Nomor batch (kode produksi) merupakan nomor yang menunjukkan suatu produk dalam satu kali produksi yang mempunyai sifat dan mutu yang seragam. Sistem penandaan pada nomor kode produksi harus dapat memastikan diketahuinya bulan, batch yang keberapa dalam bulan tersebut serta tahun dan jumlah pembuatan pada masing-masing batch. Dengan diketahuinya asal usul produk jadi tersebut akan mempermudah tindak lanjut pengawasannya (Departemen Kesehatan Republik Indonesia, 1991).
tradisional tersebut sehingga penggunaan obat tradisional mempunyai khasiat sesuai dengan tujuan terapinya.
1. Standar BPOM
Berdasarkan standar BPOM terdapat 16 kriteria informasi yang harus dicantumkan dan tidak semua kriteria terpenuhi 100%.
a. Jamu
Kelompok jamu memiliki produk yang sangat banyak jumlahnya melebihi obat herbal terstandar dan fitofarmaka. Pembuatannya relatif lebih sederhana dan murah dibandingkan dengan obat herbal terstandar dan fitofarmaka sehingga tidak jarang produk yang tergolong jamu tidak memenuhi standar.
Gambar 8. Diagram Batang Persentase Kesesuaian Produk Jamu Terhadap Setiap Kriteria Standar BPOM
Berdasarkan gambar di atas dapat terlihat bahwa tidak semua kriteria selalu dicantumkan sesuai dengan ketetapan standar yang ada. Ada kriteria-kriteria tertentu yang jarang dicantumkan pada kemasan produk. Semua produk
jamu 100% mencantumkan nama produk, besar kemasan, komposisi, nama dan alamat pendaftar, nomor ijin edar, tanggal kadaluwarsa, dan indikasi.
Pada kriteria logo 99% produk mencantumkan dan 1% produk tidak mencantumkan. Ini berarti ada produk yang tidak mencantumkan logo padahal logo merupakan komponen penanda yang penting. Melalui logo konsumen dapat membedakan produk jamu dengan obat yang lainnya sehingga dapat memilih obat yang sesuai. Sebesar 96,57% dari 175 produk jamu mencantumkan nomor batch dan ada 3% atau 9 produk yang tidak mencantumkannya.
Sebesar 82,56% produk mencantumkan bentuk sediaan dan 17,44% produk tidak mencantumkan. Bentuk sediaan juga komponen yang penting dalam penandaan. Dengan mencantumkan bentuk sediaan konsumen dapat memilih bentuk sediaan yang diinginkan. Misalnya ada konsumen yang tidak bisa minum obat dalam bentuk sediaan pil maka akan memilih yang bentuk sediaan sirup. Dengan dicantumkannya bentuk sediaan pada kemasan akan membantu konsumen agar tidak salah pilih obat karena tidak jarang ada pasien yang sungkan untuk bertanya.
Sebesar 46% produk mencantumkan kondisi penyimpanan dan 54% tidak mencantumkan. Dari persentase tersebut terlihat bahwa lebih banyak produk jamu yang tidak mencantumkan. Pencantuman kondisi penyimpanan diperlukan agar konsumen mengetahui bagaimana cara menympan jamu yang tidak habis sekali pakai dapat tetap terjaga stabilitasnya.
0%, dan info khusus kandungan babi, alkohol, dan pemanis buatan sebesar 2%. Dapat dikatakan 95% produk tidak mencantumkan nama dan alamat pemberi atau penerima kontrak, 93% tidak mencantumkan kontraindikasi, 98% tidak mencantumkan efek samping, 100% tidak mencantumkan interaksi obat dan 98% tidak mencantumkan info khusus kandungan babi, alkohol, dan pemanis buatan. Dapat dilihat bahwa persentase kesesuaian terhadap kelima kriteria tersebut sangat rendah sehingga dapat dikatakan bahwa lebih banyak produk jamu yang tidak mencantumkan.
Produk jamu yang tidak mencantumkan nama dan alamat pemberi atau penerima kontrak kemungkinan karena produk tersebut diproduksi oleh industrinya sendiri dan pekerjaan pembuatannya tidak dilimpahkan pada industri lain. Pemberi kontrak adalah industri di bidang obat tradisional yang melimpahkan pekerjaan pembuatan obat tradisional, obat herbal terstandar dan fitofarmaka berdasarkan kontrak. Penerima kontrak adalah industri di bidang obat tradisional atau industri farmasi yang menerima pekerjaan pembuatan obat tradisional, obat herbal terstandar dan fitofarmaka berdasarkan kontrak (Direktorat Jenderal Pengawasan Obat dan Makanan RI, 2005).
Albi Gura®. Produk yang memiliki tingkat kesesuaian terendah dengan persentase sebesar 50% , yaitu Mushamus®dan Black Vito®.
b. Obat herbal terstandar
Jumlah obat herbal terstandar yang telah terdaftar ada 19 produk (ITB, 2011) namun pada penelitian hanya diperoleh 8 produk saja.
Gambar 9. Diagram Batang Persentase Kesesuaian Produk Obat Herbal Terstandar Terhadap Setiap Kriteria Standar BPOM
Berdasarkan gambar di atas dapat dilihat bahwa persentase tingkat kesesuaian 100% untuk nama produk, besar kemasan, komposisi, nama dan alamat pendaftar, nomor ijin edar, nomor batch, dan indikasi. Berbeda dengan kelompok jamu, persentase kesesuaian untuk kriteria tanggal kadaluwarsa dan logo obat herbal terstandar tidak 100% akan tetapi 75%. Kelompok obat herbal terstandar yang secara kualitas lebih baik dari jamu seharusnya memiliki persentase tingkat kesesuaian yang lebih tinggi dari pada kelompok jamu.
Sebesar 25% produk obat herbal terstandar yang tidak mencantumkan logo karena produk yang ada di Apotek merupakan stock lama jadi kemungkinan belum sesuai dengan standar yang berlaku sekarang.
Persentase kesesuaian untuk nomor batch kelompok obat tradisional lebih tinggi dibandingkan dengan kelompok jamu. Persentase kesesuaian terhadap kriteria bentuk sediaan adalah 75% dan lebih rendah dari pada kelompok jamu. Persentase kesesuaian terhadap kriteria kontraindikasi dan penyimpanan masing-masing adalah 12,50% dan 62,50%, sedangkan untuk kriteria nama dan alamat pemberi atau penerima kontrak, efek samping, interaksi obat, dan info khusus kandungan babi, alkohol, dan pemanis buatan adalah 0% atau semua produk tidak mencantumkan. Produk obat herbal terstandar yang memiliki tingkat kesesuaian paling tinggi terhadap setiap kriteria standar BPOM dengan persentase sebesar 68,75% adalah Lelap®dan Diapet®. Produk yang memiliki persentase terendah sebesar 56,25% adalah Virjint®.
c. Fitofarmaka