BAB II
TINJAUAN PUSTAKA
A. Penelitian Terdahulu
Penetapan kadar atenolol dalam plasma manusia dan cairan biologis
lainnya antara lain Kromatografi Cair Kinerja Tinggi (KCKT) (Yilmaz et al, 2012), Kromatografi Cair-Spektrofotometri Massa (LC
MS-MS) (Lwin et al, 2017), Elektroforesis kapiler (CE) (Arias et al, 2001), dan Kromatografi Gas-Spektrofotometri massa (GC-MS) (Yilmaz, 2009). Berdasarkan penelitian dengan menggunakan KCKT, hasil yang didapatkan yaitu nilai linearitas dari atenolol r = 0,99 yang menunjukan linearitas. Nilai presisi intra-day dan inter-day untuk atenolol dalam plasma kurang dari 6,1 dan akurasi lebih baik dari 5,5%. Nilai LOD 1,5 dan LOQ 5 ng/mL. Recovery rata-rata atenolol dalam plasma adalah 98,4% (Yilmaz et al, 2012). Pada LC
MS-MS, Atenolol menunjukkan rentang linier dari 1-800 ng/mL (r2 = 0,9995), presisi CV 15% dan recovery analit (kisaran 80-100%) tercapai
B. Landasan Teori
1. Atenolol
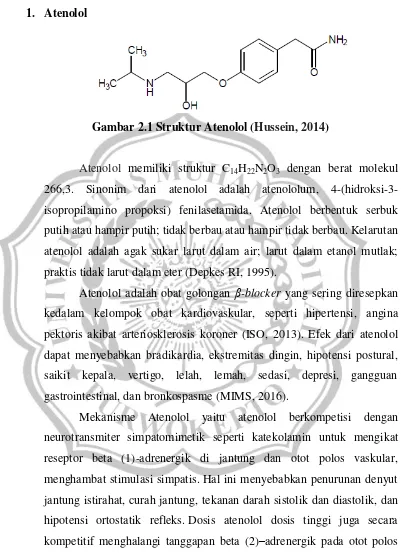
Gambar 2.1 Struktur Atenolol (Hussein, 2014)
Atenolol memiliki struktur C14H22N2O3 dengan berat molekul 266,3. Sinonim dari atenolol adalah atenololum, 4-(hidroksi-3-isopropilamino propoksi) fenilasetamida. Atenolol berbentuk serbuk putih atau hampir putih; tidak berbau atau hampir tidak berbau. Kelarutan atenolol adalah agak sukar larut dalam air; larut dalam etanol mutlak; praktis tidak larut dalam eter (Depkes RI, 1995).
Atenolol adalah obat golongan β-blocker yang sering diresepkan kedalam kelompok obat kardiovaskular, seperti hipertensi, angina pektoris akibat arteriosklerosis koroner (ISO, 2013). Efek dari atenolol dapat menyebabkan bradikardia, ekstremitas dingin, hipotensi postural, saikit kepala, vertigo, lelah, lemah, sedasi, depresi, gangguan gastrointestinal, dan bronkospasme (MIMS, 2016).
Mekanisme Atenolol yaitu atenolol berkompetisi dengan neurotransmiter simpatomimetik seperti katekolamin untuk mengikat reseptor beta (1)-adrenergik di jantung dan otot polos vaskular, menghambat stimulasi simpatis. Hal ini menyebabkan penurunan denyut jantung istirahat, curah jantung, tekanan darah sistolik dan diastolik, dan hipotensi ortostatik refleks. Dosis atenolol dosis tinggi juga secara kompetitif menghalangi tanggapan beta (2)–adrenergik pada otot polos bronkial dan vaskular (Rawashdeh, 2013).
sirkulasi sistemik. Tingkat puncak darah mencapai antara 2 dan 4 jam setelah dikonsumsi. Tidak seperti propanolol atau metoprolol, atenolol mengalami sedikit atau tidak ada metabolisme di dalam hati dan bagian yang diserap dieliminasi pada ginjal. Lebih dari 85% dosis intravena dieksreksi di urin dalam waktu 24 jam dibandingkan dengan 50% pada dosis oral. Hanya sejumlah sedikit (6-16%) yang terikat protein, sehingga menghasilkan tingkat obat pada plasma yang relatif konsisten. Waktu paruh eliminasi atenolol adalah 6-7 jam. Berdasarkan tingkat puncak pemberian intravena dicapai dalam waktu 5 menit. Clearance kreatinin kurang dari 35 mL/min/1,73 m2 (Wander et al, 2009).
2. Cairan Biologis
Cairan biologis adalah cairan yang terdapat di dalam tubuh, antara lain darah, urine, salifa dan lainnya. Penggunaan plasma dalam darah untuk analisis lebih sering digunakan karena jumlah obat lebih banyak terbebas atau terikat protein plasma. Darah merupakan sampel yang paling baik untuk identifikasi senyawa obat atau zat aktif lainnya baik untuk tujuan kualitatif ataupun kuantitatif. Plasma lebih sering digunakan daripada serum pada analisis obat, karena dapat disentrifugasi dengan segera, sedangkan pembentukan serum membutuhkan lebih banyak waktu (Smyth, 1992). Plasma biasanya digunakan untuk analisis klinis ataupun deteksi kandungan analit tertentu karena kandungan komponen darahnya lebih sedikit dibandingkan darah utuh yang memiliki matriks biologi yang sangat kompleks, sehingga lebih menguntungkan untuk analisis dan meminimalisir kegagalan ataupun kesalahan dalam analisis (Pearce, 2006).
3. KLT (Kromatografi Lapis Tipis)-Densitometri
kaca, pelat aluminium, atau pelat plastik. Kromatografi planar dapat dikatakan sebagai bentuk terbuka dari kromatografi kolom.
Fase gerak yang dikenal sebagai pelarut pengembang akan bergerak sepanjang fase diam karena pengaruh kapiler pada pengembangan secara menaik (ascending), atau karena pengaruh gravitasi pada pengembangan secara menurun (descending). KLT dalam pelaksanaannya lebih mudah dan lebih murah dibandingkan dengan kromatografi kolom. Sistem yang paling sederhana pada fase gerak KLT adalah campuran 2 pelarut organik karena daya elusi campuran kedua pelarut tersebut dapat mudah diatur sedemikian rupa sehingga pemisahan dapat terjadi secara optimal. Beberapa petunjuk dalam memilih dan mengoptimasi fase gerak:
a. Fase gerak harus mempunyai kemurnian yang sangat tinggi karena KLT merupakan teknik yang sensitif
b. Daya elusi fase gerak harus diatur sedemikian rupa sehingga harga Rf terletak antara 0,2-0,8 untuk memaksimalkan pemisahan
c. Untuk pemisahan dengan menggunakan fase diam polar seperti silika gel, polaritas fase gerak akan menentukan kecepatan migrasi solut yang berarti menentukan nilai Rf
d. Solut-solut ionik dan solut-solut polar lebih baik digunakan campuran fase geraknya, seperti air dan metanol dengan perbandingan tertentu.
Fase diam yang digunakan dalam KLT merupakan penjerap berukuran kecil dengan diameter partikel antara 10-30 µm. Semakin kecil ukuran rata-rata partikel fase diam dan semakin sempit kisaran ukuran fase diam, maka semakin baik kinerja KLT dalam hal efiseinsinya dan resolusinya. Penjerap yang paling sering digunakan adalah silika dan serbuk selulosa, sementara mekanisme sorpsi yang utama pada KLT adalah partisi dan adsropsi.
Jika sampel yang digunakan terlalu banyak maka akan menurunkan resolusi. Penotolan sampel yang tidak tepat akan menyebabkan bercak yag menyebar dan puncak ganda.
Bejana KLT dijenuhkan dengan uap fase garak. Tinggi fase gerak dalam bejana harus dibawah lempeng yang telah berisi totolan sampel. Bejana KLT harus tertutup rapat dan sedapat mungkin volume fase gerak sedikit mungkin, akan tetapi harus mampu mengelusi lempeng sampai ketinggian lempeng yang telah ditentukan. Ada beberapa teknik untuk melakukan pengembangan dalam KLT, yaitu pengembangan menaik (ascending), pengembangan dengan menurun (descending), melingkar, dan mendatar.
Bercak pemisahan pada KLT umumnya bercak yang tidak berwarna. Untuk penentuannya dapat dilakukan secara kimia, fisika dan biologi. Cara kimia yang biasanya digunakan adalah dengan mereaksikan bercak dengan suatu pereaksi melalui cara penyemprotan sehingga bercak menjadi jelas. Cara fisika yang digunakan untuk menampakkan bercak adalah dengan pencacahan radioaktif dan fluoresensi sinar ultraviolet. Fluoresensi sinar ultraviolet terutama untuk senyawa yang dapat berfluoresensi, membuat bercak akan terlihat jelas. Jika senyawa tidak dapat berfluoresensi maka bahan penyerapnya akan diberikan indikator yang berfluoresensi, dengan demikian bercak akan kelihatan hitam sedangkan latar belakangnya akan kelihatan berfluoresensi. Melakukan scanning pada permukaan lempeng dengan menggunakan densitometri.
KLT digunakan secara luas untuk analisis solut-solut organik terutama dalam bidang biokimia, farmasi, klinik, forensik, baik untuk analisis kuantitatif dengan cara membandingkan nilai Rf solut dengan nilai Rf senyawa baku atau untuk analisis kualitatif.
a. Analisis Kualitatif
KLT dapat digunakan untuk uji identifikasi senyawa baku. Parameter pada KLT yang digunakan untuk identifikasi adalah nilai Rf. Dua senyawa dikatakan identik jika mempunyai nilai Rf yang sama jika diukur pada kondisi KLT yang sama.
b. Analisis Kuantitatif
Ada 2 cara yang digunakan untuk analisis kuantitatif dengan KLT. Pertama, bercak diukur langsung pada lempeng dengan menggunakan ukuran luas atau dengan teknik densitometri. Cara kedua adalah dengan mengerok bercak lalu menetapkan kadar senyawa yang terdapat dalam bercak tersebut dengan metode analisis yang lain, seperti metode spektrofotometri (Gandjar, 2007).
4. Validasi Metode Analisis
a. Selektivitas (Spesifisitas)
b. Linearitas
Linearitas adalah kemampuan metode analisis yang memberikan respon yang secara langsung atau dengan bantuan transformasi matematika yang baik, proporsional terhadap konsentrasi analit dalam sampel. Parameter adanya hubungan linier digunakan koefisien korelasi r pada analisis regresi linier Y = a + bX. Hubungan linier yang ideal dicapai jika nilai b = 0 dan r = +1 atau –1 bergantung pada arah garis, sedangkan nilai a menunjukkan kepekaan analisis terutama instrumen yang digunakan (Harmita, 2004).
Berdasarkan persamaan regresi linear yang didapatkan, ditentukan apakah ada korelasi yang bermakna antara kedua besaran yang diukur. Untuk itu perlu dihitung besarnya koefisien korelasi (r) dan dibandingkan dengan r-tabel (r-kritik). Apabila r-hitung lebih kecil daripada r-tabel maka dikatakan korelasi tidak bermakna dan persamaan regresi tidak dapat digunakan untuk mengitung besaran yang dicari. Sebaliknya apabila r-hitung lebih besar dari r-tabel maka korelasi bermakna (signifikan) dan besaran yang dicari dapat dihitung dengan persamaan regresi yang ada (Gandjar, 2007).
c. Batas Deteksi (LOD) dan Batas Kuantitasi (LOQ)
LOD =
LOQ =
SD adalah standar deviasi dari respon dan b adalah slope dari kurva baku (Gandjar, 2007).
d. Presisi
Presisi adalah ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual, diukur melalui penyebaran hasil individual dari rata-rata jika prosedur diterapkan secara berulang pada sampel-sampel yang diambil dari campuran yang homogen.
Rumus pehitungan koefisien variasi: SD =
RSD =
Nilai RSD antara 1-2% biasanya dipersyaratkan untuk senyawa-senyawa aktif dalam julah yang banyak, sedangkan untuk senyawa-senyawa dengan kadar sekelumit, RSD berkisar 5-15% (Gandjar, 2007)
e. Akurasi
Akurasi adalah ukuran yang menunjukkan derajat kedekatan hasil analis dengan kadar analit yang sebenarnya. Kecermatan dinyatakan sebagai persen perolehan kembali (recovery) analit yang ditambahkan. Recovery dihitung dengan membandingkan kadar yang terukur dengan penambahan baku terhadap kadar teoritis.
akurasi sangat tergantung kepada konsentrasi analit dalam matriks sampel dan pada keseksamaan metode (RSD). Rentang kesalahan yang diijinkan pada setiap konsentrasi analit pada matriks (Harmita, 2004) dapat dilihat pada tabel 2.1
Tabel 2.1 Rentang Kesalahan Analit pada matriks sampel
(%)
Rata-rata yang diperoleh (%)
100 98-102
> 10 98-102
> 1 97-103
> 0,1 95-105
0,01 90-107
0,001 90-107
0,000.1 (1 ppm) 80-110
0,000.01 (100 ppb) 80-110
0,000.001 (10 ppb) 60-115
0,000.000.1 (1 ppb) 40-120