LAPORAN PRAKTIKUM KIMIA FISIKA II
SEMESTER GANJIL 2015/2016
SOL LIOFIL
NAMA : Shafira NurhasanahNIM : 1137040064
KELAS : 5/B
KELOMPOK : 3 (Hijau)
JURUSAN KIMIA
FAKULTAS SAINS DAN TEKNOLOGI
UIN SGD BANDUNG
Tanggal Praktikum : 1 Oktober 2015 Tanggal Laporan : 12 Oktober 2015
PERCOBAAN 2 SOL LIOFIL
I. TUJUAN
- Mengetahui sifat sol liofil
- Menentukan titik isoelektrik melalui pengamatan viskositas II. DASAR TEORI
Sistem koloid adalah sistem berfasa dua, fasa yang satu terdispersi di dalam fasa yang lain. Bila sebagai fasa terdispersi berupa zat padat dan medium pendispersinya berupa cairan maka sistem koloid ini disebut sol. Dalam sistem ini, partikel-partikel fasa terdispersi tidak menggumpal atau mengendap. Hal ini disebabkan karena sol mempunyai kestabilan tertentu. Berdasarkan kestabilan itu dapat dibedakan menjadi dua jenis sol liofil fan sol liofob.
Kestabilan sol liofob disebabkan adanya lapisan rangkap listrik pada antar muka partikel dan medium pendispersinya. Permukaan partikel-partikel terdispersi dapat mengadsorpsi ion-ion tertentu sehingga akan memiliki muatan listrik sejenis dan akan saling tolak-menolak antar sesamanya. Jadi adanya sedikit elektrolit akan menstabilkan sol liofob. Kestabilan sol liofil terutama disebabkan oleh karena partikel zat tersolvavi (mempunyai selubung molekul zat pelarut pada permukaannya, bila pelarut/medium pendispersi berupa air disebut terhidrasi). Sol liofil terbentuk antara lain bila gelatin atau protein dimasukkan ke dalam air. Protein adalah polimer dari asam amino dan bersifat amfoter. Secara umum rumus molekul zat ini dinyatakan sebagai:
HOOC-R-NH2
Dalam lingkungan asam, protein terionisasi bermuatan positif: HOOC-R-NH2 + H+ HOOC-R-NH3
Dalam lingkungan basa, protein terionisasi bermuatan negatif: HOOC-R-NH2 + OH- -OOC-R-NH2 + H2O
Jadi terbentuknya partikel protein yang bermuatan positif atau negatif bergantung pada pH. pH pada saat muatan negatif molekul protein setimbang dengan muatan positifnya dikenal sebagai titik isoelektrik. Pada titik isoelektrik berbagai sifat listrik atau transport protein mencapai harga minimum atau maksimum. Yang mencapai nilai minimum antara lain adalah viskositas, hantaran listrik, laju elektroforesis, rotasi optik, tekanan osmosis, pengembunan dan kepekaan terhadap pengendapan dengan alkohol. Sedangkan yang mencapai harga maksimum misalnya kecepatan sedimentasi dan pembentukan busa.
III. ALAT DAN BAHAN
Alat Ukuran Jumlah
Gelas kimia 150 mL 6 buah
Piknometer 25 mL 1 buah
Visometer Oswald - 1 buah
Pipet tetes - 3 buah
Botol semprot - 2 buah
Bunsen - 1 buah
Kaki tiga + kasa - 1 buah
Spatula - 2 buah
Pipet ukur 10 mL 2 buah
Gelas ukur 25 mL 1 buah
Filler - 2 buah pH meter - 1 buah Statif - 1 buah Bahan Jumlah Gelatin 3 gram Larutan Na2HPO4 0,2 M 25,83 mL
Larutan asam sitrat 0,1 M 34.17 mL
Aquades secukupnya
IV. CARA KERJA
Gelatin dimasukkan ke dalam 6 gelas kimia masing-masing 0,5 gram kemudia ditambahkan larutan Na2HPO4 0,2 M dan larutan asam sitrat 0,1 M dengan komposisi:
pH Larutan Na2HPO4 0,2 M (mL) Larutan asam sitrat 0,1 M (mL)
2,2 0,2 9,8 3,0 2,06 7,94 4,0 3,86 6,14 5,0 5,15 4,85 6,0 6,32 3,68 7,0 8,24 1,76
aduk larutan hingga gelatin larut, jika perlu lakukan pemanasan agar seluruh gelatin larut dan encerkan larutan hingga 50 mL. Tentukan pH larutan dengan menggunakan pH meter dan tentukan viskositas larutan-larutan gelatin tersebut dengan menggunakan air sebagai standar serta tentukan pula rapat massa larutan tersebut.
V. HASIL PENGAMATAN Wpikno kosong=20,55 gram Wpikno+air=45,61 gram ρ air(T =270C )=0,9967 g mL η air
(
T =270C)=
0,870 x 10−6m 2 s t viskositas air 1=0,40 s t viskositas air 2=0,48 st viskositas air rata−rata=0,44 s
pH Wpikno+larutan W (gram) pH larutan+gelatin Viskositas (s) Viskositas rata-rata 1 2 2,2 Pikno+larutan pH 2,2 45,86 2,1 0,60 0,62 0,61 3,0 Pikno+larutan pH 3,0 45,94 3,0 0,61 0,60 0,605 4,0 Pikno+larutan pH 4,0 46,0 4,0 0,55 0,56 0,555 5,0 Pikno+larutan pH 5,0 46,02 5,0 0,64 0,62 0,63 6,0 Pikno+larutan pH 6,0 46,10 6,1 0,63 0,66 0,645 7,0 Pikno+larutan pH 7,0 46,16 7,0 0,65 0,66 0,655
VI. PENGOLAHAN DATA
1) Menentukan volume viknometer
Vpikno=(Wpikno+air)−(Wpikno kosong ) ρ air
¿45,61 g−20,55 g
0,99678 g mL
¿25,14 mL
ρ larutan=(Wpikno+larutan)−(Wpikno kosong ) ρ air ρ larutan( pH 2,2)=45,86 g−20,55 g25,14 mL =1,0067 g mL ρ larutan( pH 3,0)=45,94 g−20,55 g25,14 mL =1,0099 g mL ρ larutan( pH 4,0)=46,00 g−20,55 g25,14 mL =1,0123 g mL ρ larutan( pH 5,0)=46,02 g−20,55 g25,14 mL =1,0131 g mL ρ larutan( pH 6,0)=46,10 g−20,55 g25,14 mL =1,0160mLg ρ larutan( pH 7,0)=46,16 g−20,55 g25,14 mL =1,0186mLg
3) Menentukan viskositas larutan untuk masing-masing pH η larutan=ρ larutan x η air x t laruan
ρ air x t air η larutan(pH 2,2)= 1,0067 g mLx 0,870 x 10 −6m2 s x 0,61 s 0,9967 g mLx 0,44 s ¿1,2182 x 10−6m 2 s η larutan ( pH 3,0)= 1,0099 g mLx 0,870 x 10 −6m2 s x 0,605 s 0,9967 g mLx 0,44 s ¿1,2120 x 10−6m 2 s
η larutan ( pH 4,0 )= 1,0123 g mLx 0,870 x 10 −6m2 s x 0,555 s 0,9967 g mLx 0,44 s ¿1,1145 x 10−6m2 s η larutan(pH 5,0)= 1,0131 g mLx 0,870 x 10 −6m2 s x 0,63 s 0,9967 g mLx 0,44 s ¿1,2661 x 10−6m 2 s η larutan ( pH 6,0)= 1,0160 g mLx 0,870 x 10 −6m2 s x 0,6455 s 0,9967 g mLx 0,44 s ¿1,3000 x 10−6m 2 s η larutan(pH 7,0)= 1,0186 g mLx 0,870 x 10 −6m2 s x 0,655 s 0,9967 g mLx 0,44 s ¿1,3235 x 10−6m 2 s 4) Grafik pH terhadap viskositas
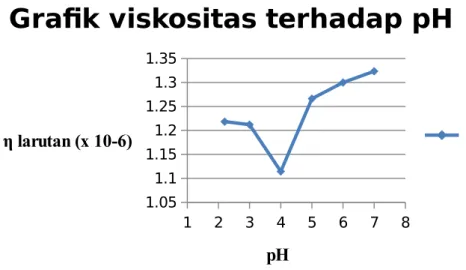
1 2 3 4 5 6 7 8 1.05 1.1 1.15 1.2 1.25 1.3 1.35
Grafik viskositas terhadap pH
pH η larutan (x 10-6) 5) Titik isoelektrik y=a x2 +bx +c x1 = 3 y1 = 1,2120 x 10-6 x2 = 4 y1 = 1,1145 x 10-6 x3 = 5 y1 = 1,2661 x 10-6 Persamaan 1,2120=a(3)2+b (3)+c ...(1) 1,1145=a(4)2 +b (4 )+c ...(2) 1,2661=a (5)2 +b (5 )+c ...(3)
a. Eliminasi c pada persamaan (1) dan (2) 1,2120 x 10−6 =9 a+3 b+c ...(1) 1,1145 x 10−6 =16 a+4 b+c - ...(2) 0,0975 x 10−6=−7 a−b ...(4)
b. Eliminasi c pada persamaan (2) dan (3) 1,1145 x 10−6=16 a+4 b+c
...(2) 1,2661 x 10−6=25 a+5 b +c - ...(3) −0,1615 x 10−6=−9 a−b
...(5)
c. Eliminasi b pada persamaan (4) dan (5)
−0,1615 x 10−6=−9 a−b - ...(5) 0,2590 x 10−6=2a a=0,2590 x 10 −6 2 =0,1295 x 10 −6
d. Substitusi a pada persamaan (4) 0,0975 x 10−6=−7 a−b ...(4) 0,0975 x 10−6=−7 (0,1295 x 10−6)−b 0,0975 x 10−6=−0,9065 x 10−6−b b ¿−0,9065 x 10−6−0,0975 x 10−6 b ¿−1,0040 x 10−6
e. Substitusi a dan b pada persamaan (1)
1,2120 x 10−6=9 a+3 b+c ...(1) 1,2120 x 10−6=9(0,1295 x 10−6)+3(−1,0040 x 10−6)+c 1,2120 x 10−6=1,1655 x 10−6+(−3,0120 x 10−6)+c c ¿1,2120 x 10−6−1,1655 x 10−6+3,0120 x 10−6 c ¿3,0585 x 10−6 f. Mencari nilai x y ¿a x2+bx+c 0,1295 x 10−6¿x2+
(−1,0040 x 10
−6)
x +c 1,2120 x 10−6=¿ x=−b 2a= −(−1,0040 x 10−6)
2(
0,1295 x 10−6)
¿1,0040 x 10 −6 0,2590 x 10−6 ¿3,8764 g. Mencari nilai yy=−(b 2 −4 ac) 4 a ¿−{
(
−1,0040 x 10 −6)
2 −4(
0,1295 x 10−6) (
3,0585 x 10−6)
} 4(
0,1295 x 10−6)
¿−{(−1,0080 x 10 −6)
−1,5843 x 10−6} 0,5180 x 10−6 ¿2,5923 x 10 −12 0,5180 x 10−6 ¿5,0044 x 10−6 VII. PEMBAHASAN VIII. KESIMPULANDari percobaan kali ini dapat disimpulkan bahwa:
- Sol liofil memiliki sifat yang stabil dan menyukai air, daya serap terhadap mediumnya kuat serta viskositasnya lebih besar dari mediumnya, terdiri dari zat organik dan tidak mudah menggumpal.
- Titik isoelektriknya dihasilkan pada posisi dengan pH 3, pH 4, dan pH 5 IX. JAWABAN TUGAS DAN PERTANYAAN
TUGAS
1. Tentukan viskositas sol liofil pada bermacam-macam pH! Jawab pH Viskositas (mpas) 2,2 1,2182 3 1,2120 4 1,1145 5 1,2661 6 1,3000 7 1,3235
2. Buat grafik antara viskositas terhadap pH! Jawab
1 2 3 4 5 6 7 8 1.05 1.1 1.15 1.2 1.25 1.3 1.35
Grafik viskositas terhadap pH
pH η larutan (x 10-6)
3. Tentukan titik isoelektrik dari grafik dengan cara interpolasi! Jawab
Titik isoelektrik terjadi pada pH 3, pH 4 dan pH 5
PERTANYAAN
1. Sebutkan sifat-sifat khusus suatu dispersi koloid ! apa perbedaan dengan larutan? Jawab
Sifat khusus dispersi koloid adalah berubah wujud dalam bentuk cairan, dipengaruhi suhu dan memiliki fasa terdispersi dan fasa pendispersi, sedangkan larutan merupakan campuran yang homogen antara zat terlarut dan zat pelarut.
2. Faktor-faktor apa saja yang menentukan kestabilan sol liofob dan sol liofil? Jawab
Faktor-faktor yang mempengaruhi kestabilan sol liofob karena adanya lapisan rangkap listrik pada antar muka partikel dan medium oendispersinya, sedangkan kestabilan sol liofil karena partikel zat padat tersolvasi atau mempunyai selubung molekul zat pada permukannya.
3. Apa arti ion-zwitter ? nyatakan ax (aktifitas ion hydrogen) pada titik isoelektrik dengan suatu persamaan.
Jawab:
Zwitter merupakan molekul yang memiliki dua muatan (positif dan negatif) sekaligus pada proten gugus hidroksinya cenderung membentuk ion negatif, sedangkan pada gugus aminnya akan membentuk ion positif.
4. Bagaimana besarnya viskositas sol liofil bila dibandingkan dengan liofob? Mengapa demikian?
Jawab
Viskositas sol liofob lebih besar dibandingkan viskositas sol liofil karena liofob yang memiliki sifat membenci larutan, membuat kekentalannya meningkat dan hal tersebut berbanding lurus terhadap viskositas.
X. DAFTAR PUSTAKA
Atkins, PW. 1083. Kimia Fisika. Jakarta: Erlangga
Giles, R, V. 1984. Mekanisme Fluida dan Hidrolika. Jakarta: Erlangga Kusuma, S. 1983. Pengetahuan Bahan-Bahan Kimia. Jakarta: Erlangga Soekardjo. 22002. Kimia Dasar. Yogyakarta: UGM Press