SPEKTROFOTOMETRI DERIVATIF ULTRAVIOLET
UNTUK PENENTUAN KADAR KAFEIN DALAM MINUMAN
SUPLEMEN DAN EKSTRAK TEH
FEBRI NERSYANTI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2006
ABSTRAK
FEBRI NERSYANTI. Spektrofotomeri Derivatif Ultraviolet untuk Panentuan Kadar Kafein dalam Minuman Suplemen dan Ekstrak Teh. Dibimbing oleh DEDEN SAPRUDIN dan RUDI HERYANTO.
Metode spektrofotometri derivatif ultraviolet (SDUV) yang relatif murah, cepat, dan dapat dipercaya dikembangkan untuk analisis kuantitatif kafein dalam minuman suplemen dan teh tanpa pemisahan dari matriksnya. Hasil penentuan kadar kafein yang diperoleh dari metode SDUV dibandingkan dengan hasil kuantifikasi kafein dengan metode kromatografi cair kinerja tinggi (KCKT).
Kuantifikasi kafein secara SDUV dilakukan berdasarkan pengukuran amplitudo puncak ke garis dasar pada panjang gelombang 274 nm untuk minuman suplemen dan 293 nm untuk teh. Hasil analisis kafein secara SDUV terhadap minuman suplemen dan teh menunjukkan kadar berturut-turut sebesar 335.99 ppm, dan untuk teh sebesar 1.91%. Hasil analisis kafein secara KCKT terhadap minuman suplemen dan teh menunjukkan kadar berturut-turut sebesar 333.91 ppm dan 1.74%. Analisis secara statistik dengan menggunakan uji t menunjukkan tidak adanya perbedaan yang nyata pada minuman suplemen, namun pada teh terdapat perbedaan yang nyata. Uji F dari kedua contoh tidak menunjukkan perbedaan yang nyata.
Uji linearitas pada metode SDUV untuk minuman suplemen dan teh menghasilkan koefisien korelasi (r) masing-masing sebesar 0.9995 dan 0.9991 pada kisaran 2- 10 ppm. Nilai simpangan baku relatif untuk uji ketelitian pada minuman suplemen sebesar 1.26% dan teh sebesar 4.71%. Nilai perolehan kembali adalah 99.17-101.25% untuk minuman suplemen dan 99.50-106.75% untuk teh. Limit deteksi pada minuman suplemen sebesar 0.18 ppm dan pada teh sebesar 0.58 ppm. Nilai limit kuantisasi pada minuman suplemen sebesar 0.54 ppm dan pada teh sebesar 1.76 ppm.
ABSTRACT
FEBRI NERSYANTI. Ultraviolet Spectrophotometry Derivative for the Quantification of Caffeine in Energy Drink and Tea. Supervised by DEDEN SAPRUDIN and RUDI HERYANTO.
The relative cheap, fast, and reliable ultraviolet derivative spectrophotometry (UVDS) method was developed for quantitative determination of caffeine in the energy drink and tea without elimination of the matrix. Caffeine analysis using UVDS method was compared with high pressure liquid chromathography (HPLC) method.
Caffeine quantification using UVDS method was based on the measurement of peak to baseline amplitude at the wavelength of 274 nm for energy drink and at 293 nm for tea. Caffeine analysis using UVDS method on the energy drink and tea showed the concentration of 335.99 ppm and 1.91%, respectively. Caffeine analysis using HPLC method on the energy drink and tea showed the concentration of 333.91 ppm and 1.79%, respectively. Statistical analysis by t test for energy drink did not show difference between the two methods and for tea showed difference between the two methods. F test for two samples did not show difference between the two methods.
The linearity test of the UVDS method presented a correlation coefficient (r) of 0.9995 for energy drink and 0.9991 for tea in the range 2-10 ppm. Relative standard deviation were 1.26% for energy drink and 4.71% for tea. Recovery were 99.17-101.25% for energy drink and 99.50-106.75% for tea. The limit of detection were 0.18 ppm for energy drink, 0.58 ppm for tea. The limit of quantification were 0.54 for energy drink and 1.76 ppm for tea.
SPEKTROFOTOMETRI DERIVATIF ULTRAVIOLET
UNTUK PENENTUAN KADAR KAFEIN DALAM MINUMAN
SUPLEMEN DAN EKSTRAK TEH
FEBRI NERSYANTI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2006
Judul : Spektrofotometri Derivatif Ultraviolet untuk Penentuan Kadar Kafein dalam Minuman Suplemen dan Ekstrak Teh
Nama : Febri Nersyanti NRP : G44201012
Menyetujui:
Pembimbing I, Pembimbing II,
Drs. Deden Saprudin, M.Si. Rudi Heryanto, S.Si, M.Si.
NIP 132126040 NIP 132311929
Mengetahui:
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Institut Pertanian Bogor
Dr. Ir. Yonny Koesmaryono, M.S
NIP 131473999
PRAKATA
Puji syukur penulis panjatkan ke hadirat Allah SWT atas rahmat dan karunia-Nya, sehingga karya ilmiah ini berhasil diselesaikan. Karya ilmiah yang berjudul
Spektrofotometri Derivatif Ultraviolet untuk Penentuan Kadar Kafein dalam Minuman Suplemen dan Ekstrak Teh ini disusun berdasarkan penelitian yang
dilakukan penulis sejak bulan Juli hingga Januari 2006 di Laboratorium Kimia Analitik Departemen Kimia Institut Pertanian Bogor, Pusat Studi Biofarmaka Institut Pertanian Bogor, dan Balai Budidaya Air Tawar Sukabumi.
Selama melaksanakan penelitian hingga penulisan karya ilmiah, penulis banyak mendapat bantuan dan bimbingan berharga dari berbagai pihak. Oleh karena itu, penulis mengucapkan terima kasih terutama kepada Bapak Drs. Deden Saprudin, M.Si dan Bapak Rudi Heryanto, S.Si, M.Si, selaku pembimbing atas segala saran, pengarahan, dan ilmunya kepada penulis. Bapak Mohammad Rafi S.Si yang telah banyak membantu mengatasi kesulitan penulis dan kepada program hibah kompetisi A2 yang telah mendanai penelitian ini. Ucapan terima kasih yang tak terhingga penulis ucapkan kepada keluarga besar penulis atas doa, semangat, cinta dan kasih sayangnya. Penghargaan dan terima kasih penulis sampaikan kepada Om Em, Bapak Ridwan, Bapak Manta, dan Bapak Kosasih.
Terima kasih juga penulis sampaikan kepada sahabat satu tim, Sri, Sekar, Mas Heri, dan teman-teman kimia angkatan 38 atas bantuan, semangat, dan dorongannya, serta semua pihak yang tidak dapat disebut satu per-satu.
Semoga karya ilmiah ini bermanfaat.
Bogor, Maret 2006
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 18 Februari 1983 dari ayah Ir. Sugiarto dan ibu Sri Widji Hartati. Penulis merupakan anak pertama dari dua bersaudara.
Tahun 2001 penulis lulus dari SMU Negeri 1 Tambun dan pada tahun yang sama lulus seleksi masuk IPB melalui jalur Undangan Seleksi Masuk IPB. Penulis memilih Program Studi Kimia, Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam.
Selama mengikuti perkuliahan, penulis menjadi asisten untuk mata kuliah Kimia Analitik II pada tahun ajaran 2004/2005 dan Kimia Analitik I pada tahun ajaran 2005/2006. Pada bulan Juni sampai Agustus 2004 penulis mengikuti Praktik Lapangan di PT Indofarma (Persero) Tbk, Cikarang Barat, Bekasi.
DAFTAR ISI
Halaman
DAFTAR TABEL………... viii
DAFTAR GAMBAR………... viii
DAFTAR LAMPIRAN………... ix
PENDAHULUAN………... 1
TINJAUAN PUSTAKA Kafein... 1
Spektrofotometri Ultraviolet... 2
Spektrofotometri Derivatif Ultraviolet (SDUV)... 2
Filter Penghalusan Savitzky-Golay... 3
Kromatografi Cair Kinerja Tinggi (KCKT)... 3
Pengembangan dan Validasi Metode... 3
BAHAN DAN METODE Bahan dan Alat... 4
Metode Penelitian... 4
HASIL DAN PEMBAHASAN Penentuan Parameter Metode SDUV... 5
Validasi Metode Analisis SDUV... 8
Perbandingan Hasil Analisis antara Metode SDUV dan KCKT... 9
SIMPULAN DAN SARAN Simpulan... 10
Saran... 10
DAFTAR PUSTAKA... 10
DAFTAR TABEL
Halaman
1 Konsentrasi standar kafein dan amplitudo spektrum pada kondisi optimum... 7
2 Hasil uji presisi untuk minuman suplemen dan eksrak teh... 8
3 Perolehan kembali untuk minuman suplemen dan ekstrak teh... 8
4 Waktu retensi dari kromatogram... 9
5 Kadar kafein dalam minuman suplemen dan teh dengan metode KCKT... 9
6 Perbandingan hasil penentuan kafein antara metode SDUV dan KCKT... 9
DAFTAR GAMBAR
Halaman 1 Struktur kafein... 12 Spektrum turunan dari absorpsi pita Gauss... 3
3 Spektrum standar dan contoh pada konsentrasi 4 ppm... 5
4 Spektrum standar dan contoh (6 ppm) pada kondisi awal (a), pada turunan pertama (b), dan turunan kedua (c)... 6
5 Spektrum standar (4 ppm) dan contoh (4 ppm) pada turunan pertama (a), dan pada turunan kedua (b)... 6
6 Kurva standar untuk minuman suplemen (a) teh (b) dengan rentang konsentrasi 2-10 ppm... 7
DAFTAR LAMPIRAN
Halaman
1 Bagan alir penelitian... 13
2 Uji ANOVA dari standar pada laju penyapuan 100, 200, 400, 800, dan 1200 nm/menit... 14
3 Uji ANOVA dari standar di derivat 2 pada laju penyapuan 100, 200, dan 400 nm/menit... 14
4 Penentuan kadar dari minuman suplemen dan teh dengan metode SDUV... 14
5 Data hasil uji akurasi dengan metode SDUV...………... 15
6 Data hasil uji linearitas, limit deteksi, dan limit kuantisasi... 16
7 Kromatogram standar kafein 400 ppm...………... 17
8
Kromatogram minuman suplemen...………... 179
Kromatogram teh...………... 1810 Penentuan kadar dari minuman suplemen dan teh dengan metode KCKT... 19
1
PENDAHULUAN
Latar Belakang
Kafein adalah salah satu jenis alkaloid yang banyak terdapat di daun teh (Camellia
sinensis), biji kopi (Coffea arabica), dan biji
coklat (Theobroma cacao) (Coffeefag 2001). Kafein memiliki efek farmakologis yang bermanfaat secara klinis, seperti menstimulasi susunan syaraf pusat, relaksasi otot polos terutama otot polos bronkus, dan stimulasi otot jantung (Coffeefag 2001). Berdasarkan efek farmakologis tersebut seringkali kafein ditambahkan dalam jumlah tertentu ke minuman suplemen. Efek samping dari penggunaan kafein secara berlebihan (overdosis) dapat menyebabkan gugup, gelisah, tremor, insomnia, hiperestesia, mual, dan kejang (Farmakologi Fakultas Kedokteran UI 2002).
Beberapa metode sudah dikembangkan dalam penentuan kadar kafein. Metode-metode tersebut adalah Metode-metode titrasi (British Pharmacopeia 1993), spektrofotometri (AOAC 1999), kromatografi gas (AOAC 1999) dan kromatografi cair kinerja tinggi (USP 1996; Altun 2001). Dibandingkan ketiga metode tersebut, metode spektrofotometri merupakan metode yang relatif cepat, murah, dan umum digunakan. Dalam perkembangannya spektrofotometri terbagi menjadi spektrofotometri konven-sional dan spektrofotometri derivatif. Metode spektrofotometri konvensional memiliki keterbatasan, yaitu tidak dapat digunakan secara langsung untuk analisis secara kuantitatif maupun kualitatif dari contoh yang memiliki matriks kompleks, sehingga harus dilakukan pemisahan analat dari matriks (El-Sayed et al. 2001). Pemisahan kafein dari matriks dapat menjadi sumber kesalahan analisis dan memperpanjang waktu analisis. Oleh karena itu, diperlukan metode lain yang lebih cepat, murah dengan tingkat ketelitian dan ketepatan yang tinggi, serta dapat mengatasi efek matriks tanpa harus memisahkannya terlebih dahulu.
Beberapa peneliti telah melaporkan pengembangan dari metode spektrofotometri konvensional untuk mengatasi hal tersebut, seperti penentuan kafein di dalam minuman (Alpdogan et al. 2000), asam askorbat pada sayuran (Aydogmus et al. 2001), penentuan losartan di dalam sediaan farmasi (Ansari et
al. 2004), penentuan total flavonoid dari
ekstrak tanaman Brazilian (Rolim et al. 2005, siap terbit) dan lain-lain.
Pengaruh matriks dan alat spektro-fotometer yang berbeda menyebabkan perbedaan hasil analisis. Oleh karena itu, untuk penentuan kafein yang terkandung di dalam minuman suplemen dan ekstrak teh dengan menggunakan spektrofotometer UV-Vis Hitachi 2800 perlu dilakukan validasi atau pengujian terhadap kinerja analitiknya. Pengujian kinerja analitik diperlukan untuk menjamin keabsahan dan keakuratan data hasil analisis. Parameter-parameter yang digunakan antara lain linearitas, presisi, akurasi, limit deteksi, dan limit kuantisasi. Tujuan penelitian ini adalah mengembangkan metode spektrofotometri derivatif ultraviolet untuk penentuan kadar kafein dalam minuman suplemen dan ekstrak teh. Hipotesis penelitian ini adalah metode spektrofotometri derivatif ultraviolet untuk penetapan kadar kafein dalam minuman suplemen dan ekstrak teh memiliki validitas yang tinggi.
TINJAUAN PUSTAKA
Kafein
Kafein merupakan salah satu jenis alkaloid yang terdapat pada tumbuhan. Kafein dapat disebut juga sebagai tein (Farmakologi Fakultas Kedokteran UI 2002). Kafein termasuk salah satu derivat xantin yang mengandung gugus metil. Kafein atau 1,3,7-trimetilxantin dengan rumus molekul C8H10N4O2 yang terdapat pada
Gambar 1. Kafein memiliki sifat fisis seperti berbentuk kristal dengan warna putih, memiliki titik leleh 234o C, larut dengan air (15 mg/ml)
dan kloroform, serta memiliki rasa agak pahit (British Pharmacopeia 1993). N N N N H3C O CH3 O CH3
Gambar 1 Struktur kafein.
Penelitian membuktikan bahwa kafein memiliki efek sebagai stimulasi sel syaraf pusat, otot jantung, dan meningkatkan diuresis (Farmakologi Fakultas Kedokteran UI 2002), sehingga kafein dapat bermanfaat secara klinis. Pengaruh tersebut timbul pada pemberian kafein 85-250 mg. Jika dosis pemberian kafein ditingkatkan, maka akan menyebabkan gugup, gelisah, tremor, insomnia, hiperestesia, mual, dan kejang (Farmakologi Fakultas Kedokteran UI 2002). Intensitas efek kafein ini berbeda
2
untuk setiap organ (Farmakologi Fakultas Kedokteran UI 2002). Berdasarkan FDA (Food Drug Administrasion) diacu dalam Liska (2004), dosis kafein yang diizinkan antara 100-200 mg. Kombinasi tetap kafein dengan analgetik seperti aspirin digunakan untuk pengobatan sakit kepala (Farmakologi Fakultas Kedokteran UI 2002; Liska 2004).
Minuman suplemen umumnya mengan-dung kafein. Formula dari minuman suplemen ini selain mengandung zat aktif juga mengandung plasebo. Plasebo ialah senyawa yang tidak mengandung zat aktif, senyawa ini umumnya dihubungkan sebagai bahan tambahan farmasetik, seperti bahan pengisi, pengental, pembawa, zat penstabil, zat pengawet, zat pemberi rasa, dan zat pemanis (Ansel 1989).
Tanaman teh berdasarkan taksonomi termasuk golongan divisi: Spermatophyta, sub divisi: Angiospermae, kelas: Magnoliopsida, subkelas: Dilleniidae, ordo: Theales, suku: Theaceae, genus: Camellia, spesies: sinensis. Jenis teh sangat beragam, begitu juga dengan kualitas hasil olahannya. Namun, umumnya jenis teh dibagi menjadi tiga berdasarkan waktu dari lamanya proses fermentasi yaitu, teh hijau dibuat tanpa melalui proses fermentasi, teh oolong dihasilkan melalui proses semi fermentasi, dan teh hitam dibuat melalui proses fermentasi. Kandungan dalam teh beraneka ragam antara lain kafein, teofilin, vitamin K, vitamin C, vitamin A, vitamin B (B1, B2, B6), K, Na, Mn, Cu, F, flavonoid, dan tanin (MLDI 2000). Kadar kafein dalam daun teh sekitar 2%, (Farmakologi Fakultas Kedok-teran UI 2002; Hesse 2002).
Spektrofotometri Ultraviolet
Suatu berkas sinar jika melewati suatu medium yang bersifat homogen, maka sebagian dari cahaya datang akan diabsorpsi, sebagian lagi dipantulkan, dan sisanya akan ditransmisikan dengan efek intesitas murni. Berdasarkan hukum Lambert-Beer dapat diketahui hubungan antara absorbansi, tebal sel, konsentrasi, dan intesitas cahaya. Hukum Beer dapat diterapkan hanya untuk radiasi monokromatik dan memiliki sifat dasar sebagai spesies penyerap yang tidak berubah sepanjang jangkauan konsentrasi yang diteliti (Harris & Bashford 1987)
A = ε c b = log Io/I
Keterangan:
A : Absorbansi
ε : Absortivitas molar (l/mol cm)
b : Ketebalan benda yang dilewati cahaya (cm) c : Konsentrasi analat (mol/l)
Spektrofotometri Derivatif Ultraviolet (SDUV)
Metode SDUV merupakan perkembangan dari spektrofotometri konvensional yang memerlukan peralatan optik, elektronik, dan metode matematika untuk menghasilkan turunan spektrum (Owen 1996). Metode SDUV dapat digunakan untuk contoh yang memiliki matriks kompleks, sehingga penentuan baik secara kuantitatif maupun kualitatif dapat dilakukan tanpa harus melakukan pemisahan antara analat dengan matriksnya. Metode ini dapat digunakan untuk menentukan panjang gelombang maksimum pada kurva yang lebar secara akurat dengan melakukan penurunan spektrum. Metode ini memiliki kelebihan, yaitu dapat menghasilkan sidik jari yang lebih baik dibandingkan dengan spektrum absorpsi yang umumnya, menghasilkan absobansi maksimum dari pita yang lebar, serta dapat meningkatkan daya pisah dari spektrum yang mengalami tumpang tindih (O’Haver 1979; Harris & Bashford 1987; Ansari et al. 2004).
Penurunan data spektrum dilakukan dengan metode matematika yaitu dengan memplot
slope atau gradient (Skujins et al. 1986) dari
serapan dengan nilai panjang gelombang (Owen 1996). Rumus yang digunakan adalah sebagai berikut: Orde nol : A = f (λ) Orde pertama :
dλ
dA
= ƒ'(λ) Orde kedua : 2 2dλ
A
d
= ƒ''(λ) Orde ke-n : n ndλ
A
d
= ƒ'n(λ)Penentuan secara kuantitatif dari senyawa memenuhi hukum Lambert-Beer baik pada spektrum asli (zero order), maupun pada spektrum turunan. Pada spektrofotometri derivatif ultraviolet, hukum Lambert-Beer menyatakan bahwa konsentrasi analat berhubungan secara linear terhadap amplitudo pada panjang gelombang tertentu (Popovic et al
3
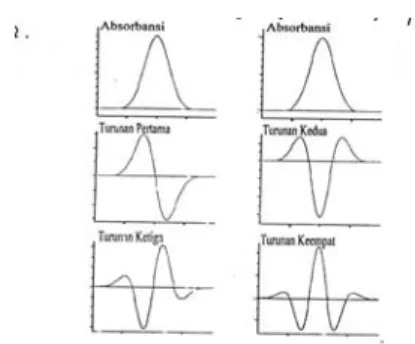
1999). Spektrum turunan lebih kompleks dibandingkan dengan spektrum aslinya, seperti ditunjukkan pada Gambar 2.
Gambar 2 Spektrum turunan dari absorpsi pita Gauss.
Pada spektrum orde nol, konsentrasi analat sebanding dengan absorbans pada panjang gelombang tertentu. Pada spektrum turunan, konsentrasi analat sebanding dengan amplitudo. Jenis-jenis amplitudo dalam spektroskopi derivatif ultraviolet adalah DL
(amplitudo pada puncak tertinggi ke puncak lain), Ds (amplitudo pada puncak ke puncak
lain), dan Dz (amplitudo dari puncak ke garis
nol). Untuk membuat kurva kalibrasi, maka dipilih amplitudo yang memberikan linearitas terbaik (Skujins et al. 1986).
Filter Penghalusan Savitzky-Golay
Kemampuan untuk menemukan puncak absorpsi pada orde turunan yang lebih tinggi sangat ditentukan oleh signal to noise ratio (S/N) pada data spektrum asli. Hal yang terpenting adalah meminimalkan noise tanpa mengurangi informasi yang ada. Oleh karena itu, perlu dilakukan proses penghalusan data (smoothing) selama penurunan spektrum.
Filter penghalusan Savitzky-Golay dengan
menggunakan metode kuadrat terkecil sehingga menghasilkan fungsi baru yang dinamakan least-squares digital polynomial
smoothing filters (Skujins et al. 1986). Proses
penghalusan secara polinomial merupakan perluasan prinsip dari moving average dengan modifikasi pada vektor titik berat.
Penghalusan Savitzky Golay umumnya digunakan pada spektrofotometri. Adanya penghalusan yang terlalu besar akan mengakibatkan penyimpangan pada spektrum yaitu dengan menurunnya inten-sitas dan pemisahan (Brereton 2003).
Kromatografi Cair Kinerja Tinggi (KCKT)
Salah satu metode pemisahan komponen-komponen campuran yang cuplikannya dalam keadaan kesetimbangan diantara dua fase yaitu fase diam yang dapat menahan cuplikan dan fase gerak yang dapat membawa cuplikan disebut metode kromatografi.
Pada penentuan kafein digunakan metode USP 1996. Pengukuran dilakukan dengan detektor ultraviolet pada panjang gelombang 280 nm, volume injeksi 10 μl, laju alir 1.0 ml/menit dan kolom C18 dengan fasa gerak
merupakan campuran dari dapar natrium asetat trihidrat dengan asetonitril. Metode ini merupakan kromatografi fase balik, hal ini dkarenakan fase diam bersifat non-polar dan fase gerak bersifat polar (Christian 2004).
Pengembangan dan Validasi Metode Analisis
Validasi adalah proses untuk membuktikan metode analisis dapat diterima untuk tujuan yang diharapkan (Green 1996). Berdasarkan Departemen Kesehatan (2001), validasi ialah suatu tindakan pembuktian dengan cara yang sesuai bahwa tiap bahan, prosedur, kegiatan, sistem, dan perlengkapan atau mekanisme yang digunakan dalam produksi dan pengawasan akan senatiasa mencapai hasil yang diinginkan.
Parameter-parameter yang digunakan dalam penetapan validasi, yakni limit deteksi, limit kuantisasi, linearitas, akurasi, presisi, spesifiktivitas, robustness (SAC-SINGLAS 2002; Chan et al. 2004).
Linearitas
Linearitas sebagai suatu prosedur analisis yang mampu memberikan hasil (misal absorbans) yang sebanding dengan konsentrasi (jumlah analat) di dalam contoh (ICH diacu dalam Chan et al. 2004). Pada pengukuran dengan menggunakan spektrofotometer UV-Vis maka konsentrasi analat akan berbanding lurus dengan absorban. Hal tersebut sesuai dengan hukum Beer. Persamaan linearitas yang digunakan ialah Y = a + bX. Syarat pene-rimaan validasi untuk uji linearitas adalah (r) ≥ 0.9995 (AOAC).
Presisi
Presisi suatu prosedur analisis menujukkan ukuran kedekatan nilai sederet pengukuran dari beberapa contoh yang serba sama pada kondisi yang telah ditentukan (Chan et al. 2004). Presisi dalam metode kimia analisis dinyatakan dalam % SBR. Presisi dapat dibagi menjadi dua, yakni keterulangan (repeatability) dan ketertiruan
4
(reproducibility) (SAC-SINGLAS 2002). Keterulangan merupakan presisi yang dihitung dari hasil penetapan ulangan dengan menggunakan metode, operator, peralatan, laboratorium, dan waktu yang sama. Sedangkan, ketertiruan menunjukkan presisi yang dihitung dari hasil penetapan ulangan dengan menggunakan metode yang sama, tetapi dilakukan oleh operator, peralatan, laboratorium, dan waktu yang berbeda. Kriteria % SBR menurut AOAC adalah sangat teliti (% SBR < 1), teliti (% SBR = 1-2), sedang (% SBR = 2-5), dan tidak teliti (% SBR > 5).
Akurasi
Akurasi prosedur analisis menunjukkan kedekatan nilai yang sebenarnya dan nilai yang terukur. Analisis kimia dari suatu sampel dapat dikatakan tepat jika nilai yang diperoleh dekat dengan nilai absolut atau nilai yang sebenarnya. Akurasi biasanya dilaporkan sebagai persen perolehan kembali (recovery) yang diharapkan berada pada selang 80-110% (AOAC).
Limit deteksi dan limit kuantisasi
Limit deteksi ialah konsentrasi terendah analat dalam sampel yang dapat dideteksi dan ditentukan berbeda nyata secara statistika dari pengukuran blanko (Green 1996; SAC-SINGLAS 2002). Sedangkan, limit kuantisasi ialah konsentrasi terendah dari analat yang masih dapat dideteksi pada tingkat presisi dan akurasi yang layak (Green 1996; SAC-SINGLAS 2002). Penentuan limit deteksi dan limit kuantisasi dapat dilakukan dengan pendekatan berdasarkan sinyal ke noise, serta plot rata-rata blanko ke kurva kalibrasi standar (SAC-SINGLAS 2002).
BAHAN DAN METODE
Alat dan Bahan
Bahan-bahan yang digunakan ialah standar kafein, akuabides, asetonitril, natrium asetat trihidrat, asam asetat glasial, minuman suplemen, dan teh komersil. Kedua contoh diperoleh dari beberapa pasar swalayan yang terdapat di Bogor.
Alat-alat yang digunakan ialah spektrofotometer UV-Vis Hitachi 2800, piranti lunak UV-solutions versi-2 Hitachi, KCKT Thermofiniggan yang dilengkapi dengan detektor UV (280 nm) dan kolom C8
(Chromosorb), 1 set peralatan komputer, filter
millex HV 0,22 μm, filter vacuum dengan
porositas 0,45 μm, syringe, kuvet, dan peralatan kaca.
Metode Penelitian
Analisis Kuantitatif Kafein dengan SDUV
Preparasi larutan stok standar. Larutan
standar dibuat dengan menimbang kafein sebesar 0.01 g, kemudian dilarutkan dalam akuabides hingga volumenya 100 ml. Konsentrasi larutan stok standar diperoleh adalah 100 ppm. Kurva kalibrasi diperoleh dengan membuat serangkaian standar dengan konsentrasi 2, 4, 6, 8, dan 10 ppm. Lalu diukur dengan spektrofotometri derivatif UV pada laju penyapuan 100, 200, 400, 800, dan 1200 nm/menit.
Preparasi contoh. Minuman suplemen
dilarutkan dalam akuabides dengan konsentrasi 5 ppm.Bahan simplisia kering teh sebanyak 1 g dididihkan dengan akuabides sebanyak 50 ml hingga volume mencapai 25 ml. Ekstrak disaring dan ditepatkan volumenya menjadi 50 ml (Alpdogan et al. 2000). Lalu teh dan minuman suplemen dilarutkan dalam akuabides dengan konsentrasi 5 ppm. Kedua larutan ini dianalisis dengan metode spektrofotometri UV pada laju penyapuan 100, 200, 400, 800, dan 1200 nm/menit. Kemudian baik standar maupun sampel dilakukan overlay, lalu diproses menggunakan kemometrik sehingga diperoleh kondisi optimum dan λ yang tepat.
Analisis kuantitatif dengan KCKT
Analisis penentuan kadar kafein yang terkandung pada sampel menggunakan KCKT merupakan metode USP yang dimodifikasi. Pengukuran dilakukan dengan detektor UV pada panjang gelombang 280 nm, volume injeksi 10 μl, laju alir 1.0 ml/menit dan kolom C8.
Preparasi fasa gerak. Natrium asetat trihidrat
ditimbang sebanyak 1.36 g, lalu dimasukkan ke labu takar 1000 ml. Kemudian dilarutkan dengan 100 ml air dan dikocok hingga larut. Asam asetat glasial sebanyak 5 ml ditambahkan, lalu dilarutkan dengan air hingga volumenya 1000 ml. Asetonitril sebanyak 70 ml dimasukkan ke labu takar 1000 ml, kemudian
5
dilarutkan dengan dapar yang telah dibuat hingga volumenya 1000 ml.
Preparasi larutan stok standar kafein.
Standar kafein ditimbang sebanyak 0.1 g, kemudian dilarutkan dalam fasa gerak hingga volumenya 100 ml. Konsentrasi larutan stok standar diperoleh adalah 1000 ppm. Kurva kalibrasi diperoleh dengan membuat serangkaian standar dengan konsentrasi 400 ppm.
Preparasi contoh. Bahan simplisia kering
teh 1 g dididihkan dengan akuabides sebanyak 50 ml hingga volume mencapai 25 ml. Ekstrak disaring dan ditepatkan volumenya menjadi 50 ml. Untuk minuman suplemen tidak dilakukan preparasi. Kedua larutan diinjeksikan ke dalam kolom KCKT.
Validasi Metode Analisis Spektrofotometri Ultraviolet Derivatif
Linearitas. Deret standar dibuat pada
konsentrasi 2, 4, 6, 8, dan 10 ppm dengan cara membuat 3 seri larutan standar. Persamaan linear yang digunakan ialah Y = a + bX serta linearitasnya diketahui dari nilai koefisien korelasi (r). Koefisien korelasi (r) dirumuskan sebagai berikut:
r =
{
(
)(
)
}
(
)
(
)
(
(
)
2)
i i 2 i i i Y Y Σ X X Σ Y Yi X Xi Σ − − − − Keterangan: r = koefisien korelasiXi = konsentrasi zat aktif masing-masing
contoh
x
= konsentrasi zat aktif rata-rataYi = respons detektor masing-masing contoh Y = respons detektor rata-rata
Presisi. Larutan contoh disiapkan untuk
konsentrasi 5 ppm dibuat enam kali ulangan dan dianalisasi pada waktu yang bersamaan untuk mendapatkan keterulangan. Penentuan presisi berdasarkan penentuan SBR.
SB =
(
)
1 n X X Σ 2 i i − − SBR = X SB . 100% Keterangan: SB = simpangan baku SBR = simpangan baku relatifXi = kadar kafein tiap ulangan X = kadar kafein rata-rata n = banyaknya ulangan
Akurasi. Larutan stok masing-masing contoh
dibuat dengan konsentrasi kafein sebesar 100 ppm dan larutan stok standar 100 ppm. Sebanyak 0.3 ml sampel dipindahkan ke dalam labu takar 10 ml dan ditambahkan larutan standar kafein masing-masing sebanyak 0.1, 0.3, dan 0.5 ml kemudian ditepatkan volumenya dengan akuabides. Masing-masing penambahan standar dilakukan sebanyak 3 kali ulangan. Penentuan akurasi dengan menentukan nilai persen perolehan kembali (%PK).
%PK = teori ditemukan umlah Jumlah J x100%
Limit deteksi dan limit kuantisasi. Parameter
limit deteksi dan limit kuantisasi ditentukan dari kurva standar. Rumus yang digunakan adalah
LoD = 3.3 x SB S LoQ = 10 SB
S
SB adalah simpangan baku dari intersep dan S merupakan kemiringan dari kurva standar.
HASIL DAN PEMBAHASAN
Penentuan Parameter Metode SDUV
Serapan spektrum dari standar kafein, minuman suplemen, dan teh diperlihatkan di Gambar 3. Serapan contoh lebih besar dibandingkan dengan standar pada konsentrasi yang sama yaitu 4 ppm. Hal ini dapat dikarenakan pada contoh terkandung matriks yang dapat memberikan serapan pada panjang gelombang yang sama. Metode spektro-fotometri konvensional tidak dapat digunakan pada kondisi tersebut, karena akan menye-babkan perolehan hasil yang tidak akurat.
Absorbans 200 250 300 350nm 0.0 0.5 1.0 1.5 2.0 2.5 λ
Gambar 3 Spektrum standar dan contoh pada konsentrasi 4 ppm.
Keterangan : hitam = standar,
merah = minuman suplemen, dan biru = ekstrak teh.
6
Pada penentuan kafein dengan SDUV dilakukan pencarian kondisi optimum. Parameter yang digunakan untuk penentuan kondisi optimum ialah laju penyapuan (scan
speed), orde turunan (derivative order), orde
penghalusan (smoothing), dan jumlah jendela (number of point). Pemilihan kondisi optimum untuk laju penyapuan berdasarkan waktu yang dibutuhkan untuk melakukan
scanning, namun tanpa mengurangi
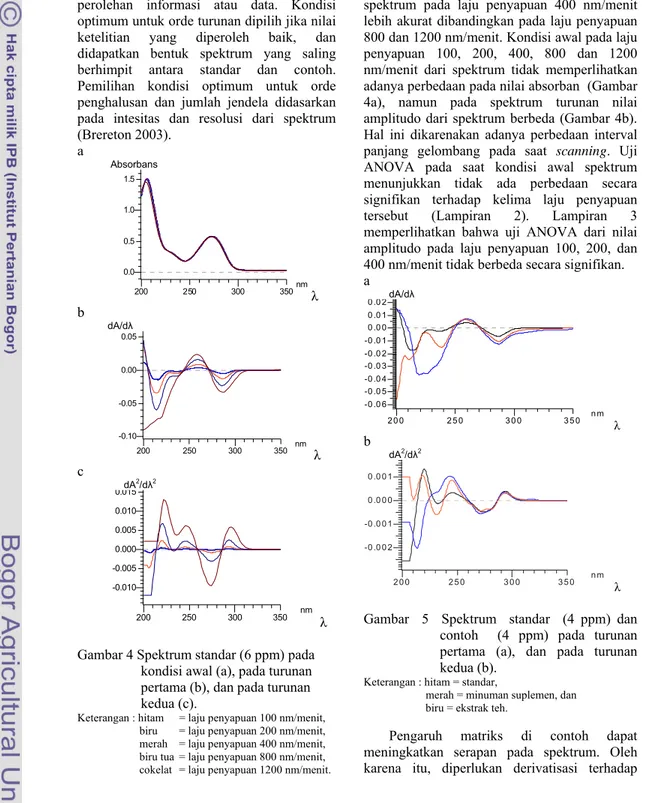
perolehan informasi atau data. Kondisi optimum untuk orde turunan dipilih jika nilai ketelitian yang diperoleh baik, dan didapatkan bentuk spektrum yang saling berhimpit antara standar dan contoh. Pemilihan kondisi optimum untuk orde penghalusan dan jumlah jendela didasarkan pada intesitas dan resolusi dari spektrum (Brereton 2003). a Absorbans 200 250 300 350nm 0.0 0.5 1.0 1.5 λ
b dA/dλ 200 250 300 350 nm -0.10 -0.05 0.00 0.05 λ c dA2/dλ2 200 250 300 350 nm -0.010 -0.005 0.000 0.005 0.010 0.015 λ
Gambar 4 Spektrum standar (6 ppm) pada kondisi awal (a), pada turunan pertama (b), dan pada turunan kedua (c).
Keterangan : hitam = laju penyapuan 100 nm/menit, biru = laju penyapuan 200 nm/menit, merah = laju penyapuan 400 nm/menit, biru tua = laju penyapuan 800 nm/menit, cokelat = laju penyapuan 1200 nm/menit.
Kondisi awal dilakukan penentuan terhadap besarnya laju penyapuan yang akan digunakan. Laju penyapuan yang akan diuji yaitu 100, 200, 400, 800, dan 1200 nm/menit. Laju penyapuan 400 nm/menit merupakan kondisi optimum untuk melakukan scanning spektrum dari kafein. Hal ini dikarenakan pada laju penyapuan 400 nm/menit waktu pembacaan lebih cepat dibandingkan pada laju penyapuan 100 dan 200 nm/menit. Selain itu, perolehan informasi dari spektrum pada laju penyapuan 400 nm/menit lebih akurat dibandingkan pada laju penyapuan 800 dan 1200 nm/menit. Kondisi awal pada laju penyapuan 100, 200, 400, 800 dan 1200 nm/menit dari spektrum tidak memperlihatkan adanya perbedaan pada nilai absorban (Gambar 4a), namun pada spektrum turunan nilai amplitudo dari spektrum berbeda (Gambar 4b). Hal ini dikarenakan adanya perbedaan interval panjang gelombang pada saat scanning. Uji ANOVA pada saat kondisi awal spektrum menunjukkan tidak ada perbedaan secara signifikan terhadap kelima laju penyapuan tersebut (Lampiran 2). Lampiran 3 memperlihatkan bahwa uji ANOVA dari nilai amplitudo pada laju penyapuan 100, 200, dan 400 nm/menit tidak berbeda secara signifikan. a dA/dλ 2 0 0 2 5 0 3 0 0 3 5 0 n m -0 .0 6 -0 .0 5 -0 .0 4 -0 .0 3 -0 .0 2 -0 .0 1 0 .0 0 0 .0 1 0 .0 2 λ b dA2/dλ2 2 0 0 2 5 0 3 0 0 3 5 0 n m -0 .0 0 2 -0 .0 0 1 0 .0 0 0 0 .0 0 1 λ
Gambar 5 Spektrum standar (4 ppm) dan contoh (4 ppm) pada turunan pertama (a), dan pada turunan kedua (b).
Keterangan : hitam = standar,
merah = minuman suplemen, dan biru = ekstrak teh.
Pengaruh matriks di contoh dapat meningkatkan serapan pada spektrum. Oleh karena itu, diperlukan derivatisasi terhadap
7
spektrum untuk mengurangi efek matriks yang terkandung di dalam contoh. Gambar 5(a) menunjukan orde turunan pertama. Pada orde turunan pertama spektrum standar dan contoh tidak berhimpit. Hal ini dapat dikarenakan, matriks yang terkandung pada contoh belum dapat dihilangkan, sehingga diperlukan orde turunan yang lebih tinggi untuk menghilangkan efek matriks (Alpdogan et al. 2000).
Gambar 5(b) menunjukkan spektrum pada orde turunan kedua. Pada turunan orde kedua diperoleh pola spektrum yang berhimpit antara standar dan contoh pada panjang gelombang 270 hingga 350 nm. Hal ini berarti, bahwa adanya himpitan menandakan hanya serapan kafein saja yang terjadi pada panjang gelombang tersebut. Orde turunan kedua menghasilkan himpitan antara spektrum standar dengan contoh. Oleh karena itu, orde turunan kedua dipilih sebagai kondisi optimum untuk analisis kuantitatif dari minuman suplemen dan ekstrak teh dengan menggunakan spektrofotometer UV-Vis Hitachi 2800. Orde turunan yang lebih tinggi tidak dipilih, karena semakin tinggi orde turunan maka penurunan S/N akan semakin besar. Semakin kecil nilai S/N menyebabkan noise sulit dibedakan dari analat (Owen 1996). Panjang gelombang yang digunakan untuk analisis minuman suplemen dan ekstrak teh masing-masing ialah 274 nm dan 293 nm. Perbedaan panjang gelombang pada kedua contoh dikarenakan bedanya kandungan dari kedua contoh. Penentuan amplitudo dilakukan dari puncak ke garis nol, sehingga dinamakan metode DZ
(amplitude zero) atau peak to zero (Fell AF et al. 1981; Skujins et al. 1986).
Proses penghalusan spektrum dengan menggunakan filter bertujuan untuk
menghilangkan noise dan mempertahankan perbandingan antara sinyal dengan noise (S/N) sesuai spektrum pada kondisi awal. Teknik yang digunakan untuk penghalusan spektrum adalah Savitzky-Golay, teknik ini umumnya digunakan pada spektrofotometri. Proses penghalusan yang terlalu tinggi dapat mengurangi intensitas dan resolusi pada spektrum, sedangkan apabila terlalu rendah maka noise masih terdapat di dalam spektrum. Jumlah jendela dapat memberikan pengaruh terhadap spektrum. Semakin besar nilai dari jumlah jendela dapat menyebabkan intensitas dan resolusi spektrum semakin menurun sehingga dapat terjadi penyimpangan di dalam analisis kuantitatif (Brereton 2003). Oleh karena itu, penentuan
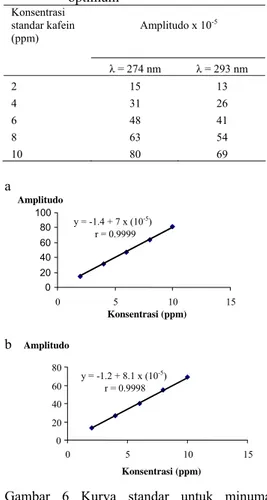
orde penghalusan dan jumlah jendela yang tepat sangat penting untuk mencapai tujuan analisis kuantitatif. Penentuan kafein pada minuman suplemen dan ekstrak teh digunakan orde penghalusan 2 dengan jumlah jendela untuk minuman suplemen dan ekstrak teh masing-masing ialah 25 dan 27. Jumlah jendela dari kedua contoh berbeda dikarenakan kedua sampel memiliki matriks yang tidak sama. Tabel 1 Konsentrasi standar kafein dan
amplitudo spektrum pada kondisi optimum Konsentrasi standar kafein (ppm) Amplitudo x 10-5 λ = 274 nm λ = 293 nm 2 15 13 4 31 26 6 48 41 8 63 54 10 80 69 a b
Gambar 6 Kurva standar untuk minuman suplemen (a), kurva standar untuk ekstrak teh (b) dengan rentang konsentrasi 2 hingga 10 ppm. Persamaan kurva standar dibuat dengan membuat plot hubungan antara konsentrasi dan amplitudo puncak ke garis nol (Dz).
Berdasar-kan Tabel 1 diperoleh persamaan garis kurva standar (Gambar 6), dan diperlihatkan adanya hubungan yang linear antara konsentrasi standar dengan amplitudo hal ini sesuai dengan hukum Lambert-Beer. Persamaan garis kurva standar untuk minuman suplemen yaitu Y = -1.2 + 8.1 X (x 10-5) dengan nilai regresi sebesar 0.9999.
y = -1.4 + 7 x (10-5) r = 0.9999 0 20 40 60 80 100 0 5 10 15 Konsentrasi (ppm) Amplitudo y = -1.2 + 8.1 x (10-5) r = 0.9998 0 20 40 60 80 0 5 10 15 Konsentrasi (ppm) Amplitudo
8
Sedangkan, untuk ekstrak teh yakni Y = -1.2 + 7 X (x 10-5) dan nilai regresi sebesar
0.9998. Tabel 3 dan 4 memperlihatkan kadar dari masing-masing contoh. Berdasarkan Lampiran 4 diperoleh kadar dari minuman suplemen yaitu sebesar 335.99±3.64 ppm, dan untuk ekstrak teh sebesar 1.91± 0.09%(b/b).
Validasi Metode Analisis SDUV
Validasi metode SDUV dilakukan untuk mengevaluasi unjuk kerja metode SDUV karena metode SDUV merupakan metode baru yang dikembangkan untuk analisis kuantitatif kafein di dalam minuman suplemen dan ekstrak teh. Suatu metode dikatakan valid jika memenuhi batas penerimaan parameter validasi yang berlaku. Parameter validasi yang ditentukan antara lain presisi, akurasi, linearitas, limit deteksi, dan limit kuantisasi.
Tabel 2 Hasil uji presisi untuk minuman suplemen dan ekstrak teh
Kandungan kafein Ulangan minuman suplemen (ppm) ekstrak teh (%)(b/b) 1 339.1 1.96 2 339.1 1.79 3 339.1 1.85 4 339.1 1.84 5 330.9 2.02 6 330.9 2.02 x±batasgalat 335.99±3.64 1.91±0.09 SB 4.24 0.09 SBR 1.26 4.71
Uji presisi digunakan larutan contoh 5 ppm. Kadar dari masing-masing contoh diharapkan menunjukkan hasil yang berdekatan, sehingga SBR yang diperoleh kurang dari atau sama dengan 2.00%. Semakin kecil nilai SBR, maka ketelitian semakin besar dan sebaliknya semakin besar nilai SBR yang diperoleh, maka semakin kecil ketelitian. Berdasarkan Tabel 2, nilai SBR untuk minuman suplemen sebesar 1.26% dan untuk ekstrak teh nilai SBR yang didapat sebesar 4.71%. Hal ini menunjukkan bahwa nilai presisi untuk analisis minuman suplemen adalah teliti berdasarkan kriteria yang telah ditetapkan AOAC (1993), karena nilai SBR minuman suplemen terdapat pada kisaran 1 hingga 2%. Ketelitan yang tinggi menunjukkan bahwa setiap hasil analisis yang dilakukan secara berulang memiliki
nilai yang tidak jauh berbeda. Pada ekstrak teh nilai presisi yang diperoleh memiliki ketelitian yang cukup, karena nilai SBR terdapat dikisaran 2 hingga 5%. Kadar kafein pada ekstrak teh yang diperoleh memiliki nilai yang beragam, sehingga SBR yang dihasilkan relatif besar. Hal ini, dikarenakan untuk memperoleh kafein yang terkandung di teh diperlukan preparasi terlebih dahulu yaitu dengan mengekstrak, sehingga dapat menyebabkan adanya galat yang mempengaruhi hasil analisis.
Tabel 3 Perolehan kembali untuk minuman suplemen dan ekstrak teh
Contoh Jumlah teori (ppm) Jumlah ditemukan (ppm) % Perolehan kembalia Minuman suplemen 4 4.05 101.25 6 5.95 99.17 8 8.01 100.13 Ekstrak teh 4 4.27 106.75 6 6.11 101.83 8 7.96 99.50 a : rataan ulangan
Parameter akurasi (Tabel 3) dilakukan dengan menambahkan standar yang telah diketahui konsentrasinya. Berdasarkan Lam-piran 5 diperoleh nilai perolehan kembali untuk minuman suplemen sebesar 99.17% hingga 101.25%, sedangkan untuk ekstrak teh ialah 99.50% hingga 106.75%. Nilai perolehan kembali dari masing-masing contoh sesuai dengan nilai kriteria yang telah ditetapkan oleh AOAC (1993), yaitu sebesar 98 hingga 110%. Hal ini dapat dinyatakan bahwa kedua contoh memiliki ketepatan yang tinggi, yaitu hasil pengukuran dekat dengan nilai yang sebenarnya.
Nilai linearitas diperlihatkan dengan kurva standar yang merupakan hubungan antara amplitudo dengan konsentrasi standar antara 2 hingga 10 ppm. Persamaan garis dari kurva standar untuk minuman suplemen adalah Y = -1.5 + 7.52 X (x 10-5) dengan nilai regresi
sebesar 0.9995, dan untuk ekstrak teh ialah Y = -1.87 + 6.3 X (x 10-5) dengan nilai regresi
sebesar 0.9991. Nilai regresi dari kedua persamaan garis tersebut mendekati nilai satu, sehingga dapat dikatakan kurva memiliki kelinearan yang tinggi. Hal ini menunjukkan bahwa terdapat hubungan antara konsentrasi dengan amplitudo. Minuman suplemen sesuai dengan nilai regresi yang telah ditetapkan oleh AOAC (1993) yaitu sebesar 0.9995, namun untuk ekstrak teh tidak sesuai dengan kriteria dari AOAC (1993).
9
Berdasarkan Lampiran 6 limit deteksi dari minuman suplemen ialah 0.18 ppm dan untuk teh sebesar 0.58 ppm. Hal ini berarti pada konsentrasi tersebut sinyal dapat dibedakan dengan noise. Nilai dari limit kuantisasi untuk minuman suplemen sebesar 0.54 ppm, sedangkan untuk ekstrak teh sebesar 1.76 ppm, artinya dalam kadar kafein yang relatif sedikit metode SDUV memberikan ketelitian dan ketepatan yang baik.
Perbandingan Hasil Analisis Antara Metode SDUV dengan KCKT
Tabel 4 Waktu retensi dari kromatogram
Keterangan Waktu retensi (menit) Standar 400 ppm 18.080 Minuman suplemen 1a 18.157 Minuman suplemen 2 a 18.183 Minuman suplemen 3 a 18.185 Ekstrak teh 1 a 18.077 Ekstrak teh 2 a 18.068 Ekstrak teh 3 a 18.073 Keterangan: a Ulangan
Metode KCKT digunakan sebagai referensi untuk analisis kafein pada minuman suplemen dan ekstrak teh. Waktu retensi (waktu yang diperlukan untuk tinggal di dalam kolom) untuk senyawa kafein adalah ± 18 menit. Kromatogram standar kafein dan kromatogram dari minuman suplemen dan teh masing-masing terdapat dalam Lampiran 7, 8, dan 9. Konsentrasi standar yang digunakan pada analisa KCKT sebesar 400 ppm. Data kromatogram standar dan contoh disajikan pada Tabel 4.
Tabel 5 Kadar kafein dalam minuman suplemen dan ekstrak teh
Ulangan Minuman suplemen (ppm) Teh (%) (b/b) 1 332.52 1.71 2 334.73 1.84 3 334.47 1.68
x
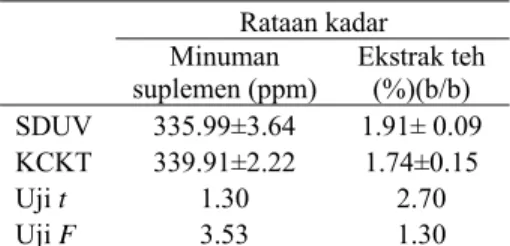
± batas galat 333.91± 2.22 1.74 ± 0.15 SB 1.21 0.08 SBR (%) 0.36 4.68Berdasarkan perhitungan yang terdapat dalam Lampiran 10 diperoleh kadar kafein di minuman suplemen dan ekstrak teh masing-masing sebesar 339.91±2.22 ppm dan 1.74±0.15% (b/b). Data kadar dari minuman
suplemen dan teh diperlihatkan pada Tabel 5. Hasil kadar minuman suplemen hampir sama dengan yang tercantum pada label minuman dan metode SDUV. Tetapi, untuk ekstrak teh nilai kadar yang diperoleh berbeda dengan nilai yang terdapat pada pustaka, yaitu 2% (Farmakologi Fakultas Kedokteran UI 2002; Hesse 2002). Hal ini dapat dikarenakan perbedaan dari jenis teh yang digunakan, daerah tanam, dan kondisi tanah.
Metode analisis spektrofotometri derivatif ultraviolet dibandingkan dengan KCKT menggunakan analisis statistika seperti uji F dan uji t. Uji F digunakan untuk mengetahui ketelitian dari kedua metode tersebut dengan membandingkan dua ragam, sedangkan uji t digunakan untuk membandingkan nilai rataan. Ragam adalah ukuran yang menggambarkan besarnya perbedaan antara satu pengukuran dengan pengukuran lainnya. Tabel 6 memperlihatkan nilai dari uji F dan uji t (Lampiran 11) dari minuman suplemen dan ekstrak teh.
Tabel 6 Perbandingan hasil penentuan kafein antara metode SDUV dan KCKT
Rataan kadar Minuman
suplemen (ppm) Ekstrak teh (%)(b/b) SDUV 335.99±3.64 1.91± 0.09 KCKT 339.91±2.22 1.74±0.15 Uji t 1.30 2.70 Uji F 3.53 1.30
Fteori pada selang kepercayaan 95% 5.786
tteori pada selang kepercayaan 95% 2.365
Nilai Fhitung dan thitung dari minuman
suplemen menunjukkan kurang dari nilai Fteori
dan tteori. Hal ini menunjukkan bahwa metode
SDUV dan KCKT untuk minuman suplemen memiliki ragam dan nilai rataan yang sama. Baik metode SDUV maupun KCKT dapat digunakan untuk penentuan kadar kafein pada minuman suplemen, karena dari hasil pengujian secara statistik kedua metode tidak memberikan perbedaan secara signifikan.
Uji F untuk teh memberikan hasil Fhitung
kurang dari nilai Fteori, sedangkan untuk uji t
nilai thitung lebih besar dibandingkan nilai tteori.
Metode SDUV dan KCKT untuk penentuan kafein di teh memiliki nilai ragam yang sama, namun nilai rataan kadar kafein dari kedua metode berbeda secara signifikan. Hal ini berarti metode SDUV untuk penentuan kafein pada teh tidak dapat digunakan, karena metode tersebut tidak dapat menghilangkan efek matriks yang terkandung pada ekstrakteh.
10
SIMPULAN DAN SARAN
Simpulan
Efek matriks yang terkandung pada minuman suplemen dapat direduksi, sehingga menghasilkan nilai yang sesuai dengan kriteria AOAC pada masing-masing parameter validasi. Hal tersebut juga dibuktikan dengan uji statistik, untuk membandingkan nilai ragam (uji F) dan rataan (uji t) hasil kuantifikasi kafein menggunakan metode SDUV dan metode KCKT, kedua uji statistik menunjukkan bahwa kedua metode tidak berbeda nyata. Metode SDUV dapat digunakan untuk kuantifikasi kafein pada minuman suplemen dan kondisi optimum yang diperoleh adalah laju penyapuan 400 nm/menit, orde turunan 2, orde penghalusan 2 dengan jumlah jendela 25. Kadar kafein yang terdapat di dalam minuman suplemen sebesar 335.99 ppm.
Pada ekstrak teh pengaruh matriks tidak dapat direduksi dengan baik. Oleh karena itu, nilai yang diperoleh untuk parameter presisi dan linearitas kurang sesuai dengan kriteria yang telah ditetapkan oleh AOAC. Uji F menunjukkan tidak adanya perbedaan secara signifikan antara metode SDUV dengan metode KCKT, namun uji t menunjukkan terdapat perbedaan yang nyata dari kedua metode. Oleh karena itu, metode SDUV belum dapat digunakan untuk kuantifikasi kafein pada teh. Kadar kafein yang terkandung pada ekstrak teh sebesar 1.91 % (b/b).
Saran
Pengujian terhadap parameter validasi yang lain juga perlu dilakukan seperti uji ketahanan (robustness), spesifiktivitas, dan ketertiruan (reproducibility). Selain itu, pada ekstrak teh perlu dilakukan pencarian metode SDUV yang lebih baik untuk analisis kadar kafein, sehingga pengaruh matriks dapat dihilangkan.
DAFTAR PUSTAKA
Alpdogan G, Karabina K, Sungur S. 2000.
Derivative spectrophotometric determination of caffeine in some beverages. Turk J Chem 26:295-302. American Pharmaceutical Association. 1982.
Handbook of Nonprescription Drugs.
Washington: American Pharmaceutical Association Pr.
Ansari M, Kazemipour M, Baradaran M, Jalalizadeh H. 2004. Derivative spectrophotometric method for determination of losartan in pharmaceutical formulation. J Pharmaco & Therapeuti 3: 21-25.
Ansel HC. 1989. Pengantar Bentuk Sediaan
Farmasi. Ed ke-4. Farida Ibrahim;
penerjemah. Jakarta: Universitas Indonesia Pr. Terjemahan dari Introduction to
Pharmaceutical Dosage Forms.
[AOAC]. Association Official of Analytical Chemistry. 1993. AOAC Peer-Verified
Methods Program. Maryland: AOAC
International.
[AOAC]. Association Official of Analytical Chemistry. 1999. Official Methods of
Analysis of AOAC International. Maryland:
AOAC International.
Aydogmus Z, Cetin SM, Ozgur MU. 2001. Determination of ascorbid acid in vegetables by derivative spectrophotometry. Turk J Chem 26:
697-704.
Brereton RG. 2003. Data Analysis for the
Laboratory and Chemical Plant. England: J
Wiley.
British Pharmacopeia. 1993. British
Pharmamacopeia. Jilid 1. London: British
Pharmacopeia.
Chau FT, Liang Y, Gao J, Shao X. 2004.
Chemometrics from Basics of Wavelet Transform. New Jersey: J Wiley.
Chan CC. 2004. Potency Method Validation. Di dalam: Chan CC, Lee YC, Lam H, Zhang XM, editor. Analytical Method Validation
and Instrument Performance Verification.
New Jersey: J Wiley. hlm. 11-26.
Christian GD. 2004. Analytical Chemistry. Ed ke-6. New Jersey: River Street Hoboken. hlm. 604-617
Coffeefag. 2001. Frequently Asked Questions about Caffeine. http://coffeefag.com// [19 Jan 2006]
[Depkes] Departemen Kesehatan, POM. 2001.
Petunjuk Operasional Penerapan CPOB.
Jakarta: Depkes.
El-Sayed AY, Hussein AG. 2003.Second and First Derivative of Phosphate and Silicate in Detergents and Waters by First-Derivative Spectrophotometry. Anal 126: 1810-1815.
Fell AF, Jarvie JR, Stewart MJ. 1981. Analysis for Paraquat by Second and Fourth Derivative Spectroscopy. Clin Chem 27/2: 286-292.
11
[FKUI] Farmakologi Fakultas Kedokteran UI. 2002. Farmakologi dan Terapi. Ed ke-4. Jakarta: Gaya Baru.
Garcia PL, Santoro RM, Hackman K, Singh AK. 2005. Development and validation of a HPLC and a UV derivative spectrophotometric methods for determination of hydroquinone in gel and cream preparations. J Pharm & Bio Anal, siap terbit.
Green JM. 1996. A practical guide to analytical method validation. Anal Chem (68): 305A-309A
Harris DA, CL Bashford. 1987.
Spectrophotometry and Spectroflurometry: a practical and
approach. Oxford: IRL Pr.
Hendayana S, Kadarohman A, Sumarna AA, Supriatna A. 1994. Kimia Analitik
Instrumen. Semarang: IKIP Semarang
Pr.
Hesse M. 2002. Alkaloid: Nature’s Curse or
Blessing. Jerman: Willey-vch.
Liska K. 2004. Drugs and The Body with
Implication for Society. Ed ke-7. New
Jersey: Pearson.
Miller JN, Miller JC. 2000. Statistics and
Chemometrics for Analytical Chemistry.
Harwon: Pearson Prentice Hall.
[MLDI] Mailing List Dokter Indonesia. 2000. Teh dan Khasiatnya. www.mldi.or.id. [19 Jan 2006]
Munson JW. 1991. Analisis Farmasi Kimia
Modern. Harjana; penerjemah. Surabaya:
Airlangga University Press. Terjemahan dari Pharmaceutical Analysis Modern Methods.
Owen T. 1996. Fundamentals of UV-Visible
Spectroscopy. Waldbornn:
Hewlett-Packard.
O’Haver TC. 1979. Potential clinical application of derivative and wavelength modulation spectropho-tometry. Clin
Chem. 25: 1584-1553.
Popovic GV, Pfendt LB, Stefanovic VM. 2000. Analytical application of derivative spectrophotometri. J Serb
Chem Soc 65:457-472.
Rolim A, et al. 2005. Total flavonoids quantification from O/W with extract of Brazilian plants. Intl J Pharmaceutical, siap terbit.
[SAC-SINGLAS] Singapore Accreditation
Council-Singapore Laboratory Accreditation Scheme. 2002. Method
validation for chemical testing. Singapura: Spring Singapore. 01:1-9.
Skujins S. 1986. UV Instrument at Work. Switzerland: Varian AG.
Siswandono, Bambang Soekarjo. 1995. Kimia
Medisinal. Surabaya: Universitas Airlangga
Pr.
[USP] United States Pharmacopeia. 1996. The
United States Pharmacopeia. Ed Asian.
12
13
Lampiran 1 Bagan alir penelitian
Standar kafein contoh ekstrak teh dan
minuman suplemen
Metode spektrofotometri derivatif ultraviolet
Metode Referensi US Pharmacopiea
Preparasi standar dan contoh
Penentuan kecepatan penyapuan, orde turunan,
orde penghalusan, dan jumlah jendela
Penentuan kurva standar dari DL, DS, dan DZ
Penentuan kadar kafein dalam contoh
Uji statistika
14
Lampiran 2 Uji ANOVA dari standar pada laju penyapuan 100, 200, 400, 800, dan 1200 nm/menit Analysis of Variance Source DF SS MS F P Factor 4 0.0016 0.0004 0.01 1.000 Error 350 20.5931 0.0588 Total 354 20.5947
Individual 95% CIs For Mean Based on Pooled StDev
Level N Mean StDev ---+---+---+--- Sc 100 71 0.2149 0.2418 (---*---) Sc 200 71 0.2141 0.2416 (---*---) Sc 400 71 0.2159 0.2421 (---*---) Sc 800 71 0.2117 0.2430 (---*---) Sc 1200 71 0.2100 0.2443 (---*---) ---+---+---+--- Pooled StDev = 0.2426 0.175 0.210 0.245
Lampiran 3 Uji ANOVA dari standar di derivat 2 pada laju penyapuan 100, 200, dan 400nm/menit Analysis of Variance Source DF SS MS F P Factor 2 0.0000010 0.0000005 1.07 0.345 Error 225 0.0001086 0.0000005 Total 227 0.0001096
Individual 95% CIs For Mean Based on Pooled StDev
Level N Mean StDev --+---+---+---+---- Sc 100 76 -2.6E-05 2.00E-04 (---*---) Sc 200 76 -2.3E-05 2.00E-04 (---*---) Sc 400 76 -1.7E-04 1.17E-03 (---*---)
--+---+---+---+---- Pooled StDev = 6.95E-04 -0.00030 -0.00015 0.00000 0.00015
Lampiran 4 Penentuan kadar dari minuman suplemen dan teh dengan metode SDUV
Minuman suplemen Teh Ulangan Amplitudo λ = 274 (x 10-5) Amplitudo λ = 293 (x 10-5) 1 40 34 2 40 34 3 40 33 4 40 30 5 40 31 6 39 31
Persamaan garis untuk minuman suplemen : Y = -1.2 + 7 X (x 10-5) nilai regresi sebesar 0.9999
Contoh perhitungan ulangan 1 (Y= 40 x 10-5) : Y = -1.2 + 8.1 X (x 10-5)
40 x 10-5 = 1.2 + 8.1 X (x 10-5) X = 5.09 ppm
15
Lanjutan Lampiran 4 Penentuan kadar dari minuman suplemen dan teh dengan metode SDUV Faktor pengencer =
ml
0.5
ml
3
ml 10 ml 10×
× =1.5
100 Kadar (mg) =ml
1000
1.5
L 1 ml 150 100 ppm 5.09×
× × × = 339.07 ppm Rataan kadar =6
87 . 330 87 . 330 07 . 39 3 07 . 339 339.07 339.07+ + + + + = 329.67 ppm Batas galat (selang kepercayaan 95%) =
n SD t ×
=
9 93 . 0 571 . 2 ×=
0.79Persamaan garis untuk teh :
Y = -1.2 + 7 X (x 10-5) nilai regresi sebesar 0.9998
Contoh perhitungan ulangan 1 (Y= 34 x 10-5) : Y = -1.2 + 7 X (x 10-5)
34 x 10-5 = 1.2 + 7 X (x 10-5)
X = 5.03 ppm Bobot daun teh = 1.0069 g = 1006.9 mg
Faktor pengencer =
ml
0.5
ml
2.5
ml 10 ml 10×
× = 80 Kadar (%) (b/b) =ml
1000
mg
1006.9
L 1 ml 50 80 ppm 5.03 × × × x 100% = 1.96 % Rataan kadar =
6
100% . 2.02) 2.02 1.84 1.85 1.79 1.96 ( + + + + + = 1.91% Batas galat (selang kepercayaan 95%) =
n SD t ×
=
6 09 . 0 571 . 2 ×=
0.09Lampiran 5 Data hasil uji akurasi dengan metode SDUV
Contoh Jumlah ditambahkan (ppm) Jumlah ditemukan (ppm) % Perolehan kembalia Minuman suplemen 4 4.05 101.25 6 5.95 99.17 8 8.01 100.13 Ekstrak teh 4 4.27 106.75 6 6.11 101.83 8 7.96 99.50 a : rataan ulangan
16
Lanjutan Lampiran 5 Data hasil uji akurasi dengan metode SDUV % Perolehan kembali = ×100% teori Jumlah ditemukan Jumlah % Perolehan kembali = 100% 4 09 . 4 × ppm ppm = 101.25%
Lampiran 6 Data hasil uji linearitas, limit deteksi, dan limit kuantisasi
Persamaan kurva standar yang diperoleh untuk minuman suplemen (λ = 274 nm) Ulangan 1 Y = - 1.5 + 7.85 X (x 10-5) r = 0.9999 Ulangan 2 Y = -1 + 7.5 X (x 10-5) r = 1 Ulangan 3 Y = -2 + 7.2 X (x 10-5) r = 0.9986 Rataan Y = -1.5 + 7.52 (x 10-5) r = 0.9995 σ = 4.08 x 10-6 Limit deteksi = S σ × 3 . 3 Limit deteksi = 5 -6 10 52 . 7 10 4.08 3 . 3 − × × × Limit deteksi = 0.18 ppm Limit kuantisasi = S σ × 10 Limit kuantisasi = 52 . 7 408 . 0 10× Limit kuantisasi = 0.54 ppm
Persamaan kurva standar yang diperoleh untuk teh (λ = 293 nm) Ulangan 1 Y = - 2.7 + 6.75 X (x 10-5) r = 0.9999
Ulangan 2 Y = -0.3 + 6.05 X (x 10-5) r = 0.9987 Ulangan 3 Y = -2.6 + 6.1 X (x 10-5) r = 0.9988 Rataan Y = -1.87 + 6.3 (x 10-5) r = 0.9991 σ = 1.109 x 10-5
Ulangan 1 Ulangan 2 Ulangan 3 Amplitudo (x 10-5) Amplitudo (x 10-5) Amplitudo (x 10-5)
λ = 274 nm λ = 293 nm λ = 274 nm λ = 293 nm λ = 274 nm λ = 293 nm 14 11 14 11 12 9 30 24 29 24 28 23 46 38 44 37 41 34 61 51 59 49 54 45 77 65 74 59 71 59
17
Lanjutan Lampiran 6 Data hasil uji linearitas, limit deteksi, dan limit kuantisasi Limit deteksi = S σ × 3 . 3 Limit deteksi = 5 5 10 3 . 6 10 109 . 1 3 . 3 − − × × × Limit deteksi = 0.58 ppm Limit kuantisasi = S σ × 10 Limit kuantisasi = 5 5 10 3 . 6 10 109 . 1 10 − − × × x Limit kuantisasi = 1.76 ppm
Lampiran 7 Kromatogram standar kafein 400 ppm
Lampiran 8 Kromatogram minuman suplemen (a) ulangan 1, (b) ulangan 2, dan (c) ulangan 3
18
Lanjutan Lampiran 8 Kromatogram minuman suplemen (a) ulangan 1, (b) ulangan 2, dan (c) ulangan 3
(b)
(c)
Lampiran 9 Kromatogram teh (a) ulangan 1, (b) ulangan 2, dan (c) ulangan 3
19
Lanjutan Lampiran 9 Kromatogram teh (a) ulangan 1, (b) ulangan 2, dan (c) ulangan 3
(b)
(c)
Lampiran 10 Penentuan kadar dari minuman suplemen dan teh dengan metode KCKT
Ulangan
Luas puncak kromatogram Kadar
Minuman suplemen Teh Minuman suplemen (mg) Teh (%) (b/b)
1 15864935 16379784 49.88 1.71
2 15970647 17649917 50.21 1.84
3 15957198 16081873 50.17 1.68 Luas puncak (A) kromatogram standar 400 ppm = 19084638
Contoh perhitungan ulangan 1 minuman suplemen Cstandar x Acontoh = Ccontoh x Astandar
Ccontoh =
dar
As
Acontoh
dar
Cs
tan
tan
×
20
Lanjutan Lampiran 10 Penentuan kadar dari minuman suplemen dan teh dengan metode KCKT Ccontoh =
19084638
15864935
400
ppm
×
Ccontoh = 332.52 ppm Rataan kadar =3
) 47 . 334 73 . 334 52 . 332 ( + + ppm = 333.91 ppmBatas galat (selang kepercayaan 95%) =
n SD t ×
=
3 207 . 1 182 . 3 ×=
2.21 ppmLampiran 11 Uji t dan F
Two-Sample T-Test and CI: SDUV 1, KCKT1 (minuman suplemen)
Two-sample T for SDUV 1 vs KCKT1
N Mean StDev SE Mean SDUV 1 6 335.99 0.639 0.26 KCKT1 3 333.91 1.207 0.10
Difference = mu SDUV 1 - mu KCKT1 Estimate for difference: 0.367
95% CI for difference: (-0.321, 1.054)
T-Test of difference = 0 (vs not =) T-Value = 1.30 P-Value = 0.240 DF = 6
Fhitung =
2
SB
1
SB =0.181
0.639 = 3.53Two-Sample T-Test and CI: SDUV 2, KCKT 2 (ekstrak teh)
Two-sample T for SDUV 2 vs KCKT 2
N Mean StDev SE Mean SDUV 2 6 1.9139 0.0985 0.040 KCKT 2 3 1.7467 0.0814 0.047
Difference = mu SDUV 2 - mu KCKT 2 Estimate for difference: 0.1672
95% CI for difference: (-0.0046, 0.3390)
T-Test of difference = 0 (vs not =):T-Value = 2.70 P-Value = 0.054 DF = 4
Fhitung =