ABSTRAK
Daun Binahong (Anredera cordifolia (Ten.) Steenis ) merupakan tanaman yang banyak dimanfaatkan sebagai obat herbal. Sediaan dari daun binahong banyak dijumpai di pasaran. Tujuan dari penelitian ini adalah untuk membandingkan kadar flavonoid total serta potensi antioksidan (IC50) serbuk simplisia daun binahong dan sediaan daun binahong yang beredar di pasaran. Ekstraksi dilakukan dengan cara maserasi dengan menggunakan pelarut etanol 70%. Penentuan kadar flavonoid total dan uji potensi antioksidan dilakukan secara spekktrofotometri UV-Vis. Penetapan kadar flavonoid total menggunakan natrium asetat dan alumunium klorida (AlCl3) sebagai pereaksi dan untuk penetapan potensi antioksidan menggunakan DPPH
(1,1-difenil-2-fikrilhidrazil) sebagai radikal bebas. Kadar flavonoid total serbuk simplisia daun binahong sebesar
21,180% dan sediaan daun binahong yang beredar di pasaran antara 5,888% sampai 13,019%. Serbuk simplisia daun binahong dan sediaan daun binahong yang beredar di pasaran memiliki IC50 lebih dari 1000 ppm. Hasil dari penelitian tersebut menunjukkan bahwa kadar falavonoid daun binahong lebih besar dibandingkan sediaan daun binahong di pasaran.
Kata Kunci : Daun Binahong (Anredera cordifolia Ten. Steenis), sediaan daun binahong di pasaran, flavonoid, antioksidan dan DPPH
ABSTRACT
Binahong leaf (Anredera cordifolia (Ten.) Steenis) is the plants often used as medical herb. The pharmaceutical of the leaf binahong can be found on the market. The purpose of the research were compared the total amount of flavonoid and potential of antioxidant (IC50) simplicial powder of binahong leaf and pharmaceutical binahong leaf on the market. Extraction was done by maceration method, using ethanol 70%. Detemination of total flavonoid content and potential of antioxidant used spechtrofotometry UV-Vis. Determination of total flavonoid content used natrium acetat and alumunium chloride as reagent and test potential of antioxidant used DPPH (1,1-difenil-2-fikrilhidrazil) as free radical . Total flavonoid content of the binahong leaf amounted 21,1801% and pharmaceutical binahong leaf on the market between 5,888% to 13,0194%. The potential of antioxidant binahong leaf and pharmaceutical binahong leaf on the market more than 1000 ppm. The result of the researche show that the total amount of flavonoid from binahong leaf bigger than the pharmaceutical of binahong leaf on the market.
Keyword: Binahong leaf (Anredera cordifolia (Ten.) Steenis), pharmaceutical of binahong leaf on the market, flavonoid, antioxidant, and DPPH
PENDAHULUAN
Tanaman binahong merupakan salah satu tanaman obat yang berpotensi untuk dikembangkan, karena hampir semua bagian dari tanaman binahong seperti umbi, batang dan daun dapat digunakan dalam terapi herbal (Usman, 2010). Bagian tanaman yang paling sering digunakan atau dimanfaatkan untuk kesehatan atau sebagai obat adalah bagian daun. Berdasarkan hasil penelitian, senyawa metabolit sekunder yang terdapat
dalam daun binahong antara lain steroid, alkaloid, flavonoid, saponin, polifenol dan tannin (Mustikasari, dkk. 2012 ). Daun binahong diketahui berpotensi sebagai
antioksidan, karena salah satunya
mengandung flavonoid (Widya, 2013 dan Mustikasari 2012). Pada saat ini telah banyak beredar produk sediaan herbal dari daun binahong misalnya sediaan kapsul daun binahong. Kandungan berkhasiat serta
potensi antioksidan didalam sediaan daun binahong tersebut belum banyak diketahui.
Antioksidan adalah senyawa yang mampu menangkal atau meredam dampak negatif oksidan atau radikal bebas dalam tubuh. Radikal bebas merupakan senyawa asing yang dapat merusak sistem imunitas tubuh. Selain itu, Radikal bebas yang berlebih didalam tubuh dapat mengganggu produksi DNA, lapisan lipid pada dinding sel, mempengaruhi pembuluh darah, dan produksi prostaglandin sehingga dapat memicu timbulnya berbagai penyakit seperti memicu tumbuhnya sel kanker (Suryanto, 2009). Pembentukan radikal bebas dapat dicegah dengan antioksidan. Antioksidan
bekerja dengan cara mendonorkan
elektronnya kepada senyawa yang bersifat oksidan sehingga aktivitas senyawa oksidan itu dapat dihambat (Winarsi, 2007).
Penelitian ini menganalisis kadar flavonoid total dan potensi antioksidan daun binahong dibandingkan dengan sediaan daun
binahong yang beredar di pasaran,
menggunakan metode spektrofotometri UV-Vis. Umumnya senyawa flavonoid terdapat pada tumbuhan dalam bentuk glikosida sehingga senyawa ini bersifat polar dan termasuk senyawa fenolik alam yang
potensial sebagai antioksidan
(Markham,1988). Pelarut yang cocok untuk ekstraksi senyawa ini adalah etanol 70 % (Harborne, 1987). Ekstraksi daun binahong
dilakukan dengan metode maserasi
menggunakan etanol 70%. Berdasarkan
Penelitian sebelumnya ekstrak daun
binahong dibuat dengan cara maserasi dengan pelarut etanol 96% (Umar, 2012; Widya, 2013). Mustikasari dkk, 2012
menarik senyawa flavonoid dan
menganalisis potensi antioksidan ekstrak
daun binahong dengan menggunakan
ekstrak yang diperoleh dengan cara maserasi bertingkat dengan menggunakan pelarut etil asetat dan etanol 70%. Hasil penelitian ekstrak etanol daun binahong memberikan IC50 sebesar 75,26 ppm, sedangkan ekstrak etil asetat memberikan IC50 sebesar 93,62 ppm. Oleh karena itu, pada penelitian ini digunakan pelarut etanol 70% sebagai pelarut pengekstraksi. Penetapan kadar flavonoid dilakukan dengan pereaksi AlCl3 dengan pembanding kuersetin. Pengujian aktivitas antioksidan dilakukan dengan
menggunakan metode DPPH dengan
pembanding larutan vitamin C murni.
METODE KERJA
Waktu dan Tempat Penelitian
Penelitian telah dilaksanakan pada bulan Februari sampai Mei 2016 bertempat
di Laboratorium Farmasi Fakultas
Matematika dan Ilmu Pengetahuan Alam, Universitas Pakuan Bogor.
Alat dan Bahan
Alat yang digunakan dalam
penelitian ini, antara lain, alumunium foil, alat penggiling (grinder), alat gelas, balp, corong, mesh 40, moisture balance, pipet ukur, pipet tetes, tanur, timbangan analitik, spektrofotometer.
Bahan yang digunakan dalam penelitian ini adalah sediaan daun binahong yang beredar di pasaran, daun binahong (Anredera cordifolia), air suling, etanol 70 %, etanol 96% p.a, metanol, kuersetin, Vitamin C, 1,1-difenil-2-fikrilhidrazil (DPPH), Na-asetat, alumunium klorida (AlCl3), asam klorida (HCl) , Bouchardart LP, Mayer LP, ammonia (NH3), eter, etil asetat, gelatin, Natrium klorida (NaCl) kloroform (CHCl3), Na asetat, Besi (III) klorida (FeCl3), serbuk Zn P, serbuk Mg P.
Pengumpulan dan Determinasi Tanaman
Bahan yang digunakan dalam penelitian ini berasal dari daun binahong yang diperoleh dari Kebun Percobaan Biologi Fakultas MIPA Universitas Pakuan, Bogor dan sediaan daun binahong yang telah beredar di Pasaran diperoleh dari berbagai toko obat herbal yang terdapat dari daerah Bogor dan sekitarnya seperti daerah Pasar Anyar dan Pasar Bogor. Daun binahong yang digunakan dalam penelitian ini telah
dideterminasi di Pusat Konservasi
Tumbuhan Kebun Raya – LIPI, Bogor.
Pembuatan Simplisia dan Ekstrak Penyediaan simplisia
Daun Binahong yang telah
dikumpulkan, masing-masing dibersihkan
dari kotoran-kotoran yang menempel
(sortasi basah) lalu dicuci dengan air mengalir sampai bersih, kemudian ditiriskan
untuk menghilangkan air sisa-sisa
pencucian. Daun binahong yang telah bersih dan bebas air pencucian lalu dikeringkan di
dalam oven pada suhu 400C lalu dibersihkan kembali dari kotoran yang mungkin tidak hilang pada saat sortasi basah (sortasi
kering). Simplisia kering tersebut
selanjutnya digrinder hingga menjadi simplisia serbuk lalu diayak dengan ayakan
mesh 40 kemudian ditimbang untuk
mendapatkan bobot akhir simplisia, lalu simpan dalam wadah kering dan bersih. Rendemen simplisia dapat dihitung dengan rumus :
Persiapan Pembuatan Ekstrak
1. Pembuatan Ekstrak Daun Binahong
Daun binahong sebanyak 5g
diekstraksi dengan pelarut etanol 70% dengan penyari 1:10 dengan cara maserasi selama 3 hari interval waktu pengocokkan 6 jam sekali selama 15 menit, kemudian disaring. Filtrat didiamkan selama 24 jam lalu dienaptuangkan, kemudian dimasukkan ke dalam labu ukur 50 mL dan diencerkan sampai batas. Diperoleh ekstrak cair (KemenKes. 2011).
2. Pembuatan Ekstrak dari Sampel yang Diperoleh dari Pasaran
Serbuk kapsul daun binahong sebanyak 5g diekstraksi dengan pelarut etanol 70% dengan penyari 1:10 dengan cara maserasi selama 3 hari interval waktu pengocokkan 6 jam sekali selama 15 menit, kemudian disaring. Filtrat didiamkan
selama 24 jam lalu dienaptuangkan,
kemudian dimasukkan ke dalam labu ukur 50 mL dan diencerkan sampai batas. Diperoleh ekstrak cair (KemenKes. 2011).
Penetapan Karakteristik Simplisia Penetapan Kadar Air
Penetapan kadar air simplisia daun binahong dan sediaan daun binahong yang
ada di pasaran dilakukan dengan
menggunakan alat moisture balance.
Sebelum digunakan alat terlebih dahulu ditara dengan akurasi dan temperatur sesuai dengan jumlah simplisia yang akan diujikan. Serbuk simplisia daun binahong sebanyak 1 gram disimpan di atas punch, diratakan sampai menutupi permukaan punch lalu ditutup, setelah 10 menit proses selesai maka persen kadar air dari simplisia akan tertera secara otomatis pada layar moisture balance (penentuan dilakukan duplo). Kadar air
simplisia pada umumnya yaitu tidak lebih dari 5 %.
Penetapan Kadar Abu
Lebih kurang 2g serbuk simplisia ditimbang seksama, dimasukkan kedalam krus silikat yang telah dipijarkan dan ditara lalu diratakan. Dipijarkan perlahan-lahan pada suhu ±600ºC hingga arang habis, didinginkan dan ditimbang. Jika dengan cara
ini arang tidak dapat dihilangkan,
ditambahkan air panas, lalu disaring melalui kertas saring bebas abu. Sisa abu dan kertas saring dipijarkan dalam krus yang sama. Filtrat dimasukkan ke dalam krus, diuapkan, dipijarkan hingga bobot tetap dan ditimbang. Dihitung kadar abu terhadap bahan yang telah dikeringkan di udara (DepKes RI, 2000).
Kadar abu = (bobot krus+bobot abu)−bobot krusbobot simplisia x 100 %
Uji fitokimia
Ekstrak daun binahong (Anredera
cordifolia), serbuk simplisia daun binahong
dan serbuk kapsul daun binahong yang telah diperoleh diuji secara fitokimia. Uji ini merupakan uji kimia kualitatif menggunakan pereaksi yang spesifik. Uji fitokimia yang dilakukan terhadap serbuk simplisia dan ekstrak daun binahong serta sediaan daun binahong yang ada di pasaran meliputi:
Uji Alkaloid
Sebanyak ± 500 mg sampel ditambah dengan 1 mL asam klorida 2 N dan 9 mL air suling, dipanaskan di atas penangas air selama 2 menit, didinginkan
kemudian disaring, 3 tetes filtrat
dipindahkan pada kaca arloji, kemudian ditambahkan 2 tetes pereaksi Bouchardat LP, jika pada kedua percobaan tidak terjadi endapan, maka serbuk tidak mengandung alkaloid.
Adanya alkaloid ditunjukkan
dengan terbentuk endapan menggumpal berwarna putih atau kuning yang larut dalam metanol dengan pereaksi Mayer LP
dan dengan pereaksi Bouchardat LP
terbentuk endapan berwarna coklat sampai hitam (DepKes RI, 1980).
Uji Saponin
Sebanyak ± 500 mg sampel dimasukkan ke dalam tabung reaksi, ditambahkan 10 mL air panas, didinginkan dan kemudian dikocok kuat-kuat selama 10
detik (jika zat yang diperiksa berupa sediaan cair, diencerkan 1 mL sediaan yang diperiksa dengan 10 mL air dan dikocok kuat-kuat selama 10 detik). Reaksi positif jika terbentuk buih yang mantap selama tidak kurang dari 10 menit, setinggi 1 cm sampai 10 cm. Pada penambahan 1 tetes asam klorida 2 N buih tidak hilang (DepKes RI, 1980).
Uji Tanin
Sebanyak ± 20 mg sampel
ditambahkan etanol sampai sampel terendam semuanya. Kemudian sebanyak 1 mL larutan dipindahkan kedalam tabung reaksi dan ditambahkan 2-3 tetes larutan FeCl3 1%.
Hasil positif ditunjukkan dengan
terbentuknya warna hitam kebiruan atau hijau (Sastrawan, dkk. 2013).
Sebanyak ± 20 mg sampel
ditambahkan air sampai sampel terendam semuanya, kemudian dipanaskan ± selama 5 menit. Kemudian 1 mL larutan dipindahkan kedalam tabung reaksi dan ditambahkan 2-3 tetes gelatin 1 % persen, lalu ditambahkan natrium klorida (NaCl) 10%. Hasil positif menunjukkan terbentuknya endapan putih (Kumoro, 2015).
Uji Flavonoid
Larutan Percobaan
Sebanyak ±500 mg sampel
ditambah 10 mL metanol P, lalu dipanaskan selama kurang lebih 5 menit. Disaring panas melalui kertas saring berlipat, diencerkan
dengan 10 mL air. Setelah dingin
ditambahkan 5 mL eter minyak tanah P, dikocok hati-hati, didiamkan, diambil lapisan methanol, diuapkan pada suhu 40OC dibawah tekanan. Sisa dilarutkan dalam 5 mL etil asetat P, disaring.
Cara Percobaan.
1. Diuapkan hingga kering 1 mL larutan percobaan, sisa dilarutkan dalam 1 mL sampai 2 mL etanol (95%) P, ditambahkan 500mg serbuk seng P dan 2 tetes asam klorida 2N, didiamkan selama 1 menit. Ditambahkan 10 mL asam klorida pekat P, jika dalam waktu 2 sampai 5 menit terjadi warna merah
intensif, menunjukkan adanya
flavonoid (glikosida-3-flavonol) 2. Diuapkan hingga kering 1 mL larutan
percobaan, sisa dilarutkan dalam 1 mL etanol (95%) P, ditambahkan 100 mg serbuk magnesium P dan ditambahkan 10 mL HCl pekat P, jika terjadi warna
merah jingga sampai merah ungu, menunjukkan adanya flavonoida. Jika
terjadi warna kuning jingga
menunjukkan adanya flavon, kalkon, dan auron (DepKes RI, 1979).
Penetapan Kadar Flavonoid Total
Penetapan Panjang Gelombang Maksimum Kuersetin
Sebanyak 5 mL larutan standar kuarsetin dalam etanol konsentrasi 10 ppm dimasukkan dalam labu ukur 50 mL ditambahkan 15 mL etanol 96%, lalu ditambahkan 1 mL AlCl3 10 %, 1 mL natrium asetat 1 M dan diencerkan dengan air suling sampai batas. Dikocok homogen lalu dibiarkan selama 30 menit, diukur absorbannya pada panjang gelombang
380-780 nm dengan menggunakan
spektrofotometer (Chang, et al. 2002).
Penentuan Waktu Inkubasi Optimum
Sebanyak 5 mL larutan standar kuersetin konsentrasi 10 ppm dimasukkan dalam labu ukur 50 mL ditambahkan 15 mL etanol 96%, lalu ditambahkan 1 mL AlCl3 10 %, 1 mL natrium asetat 1 M dan diencerkan dengan air suling sampai batas. Kemudian dihomogenkan dan diinkubasi pada suhu kamar. Serapan diukur pada panjang gelombang maksimum pada 5, 10, 15 20, 25, dan 30 menit sehingga didapat waktu optimum yang stabil (Chang, et al. 2002).
Pembuatan Kurva Kalibrasi Standar Kuersetin
Dibuat deret standar kuersetin 2,4,6,8 dan 10 ppm dari larutan 100 ppm, sebanyak 1,2,3,4,5 mL larutan standar 100 ppm dipipet ke dalam labu ukur 50 mL, kemudian ditambahkan 15 mL etanol 96%, lalu ditambahkan 1 mL AlCl3 10 %, 1 mL natrium asetat 1 M dan diencerkan dengan air suling sampai batas. Dikocok hingga homogen dan diinkubasi pada waktu
optimum pada suhu kamar. Diukur
absorbannya dengan spektrofotometer UV-Vis pada panjang gelombang maksimum (Chang, et al. 2002).
Pengukuran absorban diatas dibuat kurva antara konsentrasi larutan standar kuersetin dengan nilai absorban yang diperoleh dan akan dihasilkan persamaan regresi linier (y= bx + a). persamaan regresi ini untuk menghitung kadar ekstrak (ppm) dengan memasukkan absorban ekstrak sebagai nilai Y dan ke dalam persamaan.
Penentuan Kadar Flavonoid Total
Masing-masing ekstrak etanol daun binahong dan ekstrak etanol sediaan daun binahong yang diperoleh di pasaran dipipet 1 mL dari masing- masing ekstrak ke dalam labu ukur 50 mL, dicampur dengan 15 mL etanol 96%, ditambahkan 1 mL AlCl3 10 %, 1 mL natrium asetat 1M dan air suling sampai batas. Dikocok hingga homogen dan diinkubasi pada waktu optimum pada suhu
kamar. Diukur serapannya dengan
spektrofotometer UV-Vis pada panjang gelombang maksimum (Chang, et al. 2002). Absorban yang dihasilkan dimasukkan kedalam persamaan regresi dari kurva standar kuersetin. kemudian dihitung flavonoid total dengan menggunakan rumus: (Desmiyati, dkk. 2009)
% kadar = 𝑘𝑎𝑑𝑎𝑟 (𝑝𝑝𝑚)𝑥 𝑣𝑜𝑙𝑢𝑚𝑒 (𝑚𝐿)𝑥 𝑓𝑝 𝑥 10𝑔𝑟𝑎𝑚 𝑏𝑜𝑏𝑜𝑡 𝑠𝑎𝑚𝑝𝑒𝑙 −6 x 100 %
Uji Potensi Antioksidan
Penetapan Panjang Gelombang Maksimum DPPH
Penentuan panjang gelombang
maksimum dilakukan dengan cara:
Sebanyak 1 mL larutan DPPH 1 mM dimasukkan ke dalam labu ukur 10 mL yang seluruh bagian labu ukurnya telah ditutup dengan alumunium foil, lalu ditambahkan metanol sampai tanda batas (10
mL) dan dihomogenkan, kemudian
diinkubasi terlebih dahulu selama 30 menit. Setelah itu serapannya diukur pada panjang gelombang 480-550 nm (Mustikasari, dkk. 2012).
Penentuan Waktu Inkubasi Optimum
Sebanyak 0,6 mL larutan induk vitamin C (100 ppm) dimasukkan ke dalam labu ukur 10 mL yang seluruh bagian labu ukurnya telah ditutup dengan alumunium foil, lalu ditambahkan 1 mL larutan DPPH 1mM. Kemudian, ditambahkan metanol
sampai tanda batas (10 mL) dan
dihomogenkan. Serapan diukur pada
panjang gelombang maksimum tiap 10, 20, 30, 40, 50 dan 60 menit, serta ditentukan waktu optimum (waktu inkubasi yang
memberikan serapan cukup stabil)
(Mustikasari, dkk. 2012).
Pembuatan Deret Standar Larutan Vitamin C
Dibuat deret larutan Vitamin C dalam beberapa konsentrasi yaitu 2, 4, 6, 8,
dan 10 ppm. Dengan cara dipipet larutan induk vitamin C (100 ppm) sebanyak 0,2; 0,4; 0,6; 0,8; dan 1 mL pada masing-masing labu ukur 10 mL dan ditambahkan 1mL larutan DPPH 1mM pada masing-masing labu ukur, kemudian ditambahkan metanol sampai batas (10 mL), lalu dihomogenkan dan didiamkan selama waktu optimum pada suhu kamar. Serapan diukur pada panjang gelombang maksimum (Mustikasari, dkk. 2012).
Pembuatan Larutan Uji ( Serbuk Simplisia Daun Binahong dan sediaan Daun Binahong yang Beredar di Pasaran)
Masing-masing ekstrak daun
binahong dan ekstrak sediaan daun binahong yang diperoleh di pasaran dipipet setara ± 250 mg simplisia daun binahong dan sediaan daun binahong yang beredar di pasaran. Dimasukkan masing-masing sampel tersebut kedalam labu takar 50 mL, yang telah
dilapisi dengan alumunium foil dan
dilarutkan dalam metanol sampai tanda batas lalu dihomogenkan (5000 ppm).
Larutan uji 5000 ppm dibuat deret menjadi 1000, 1500, 2000, 2500 dan 3000 ppm, dengan cara dipipet 2, 3, 4, 5 dan 6 mL dari larutan uji 5000 ppm pada masing-masing labu ukur 10 mL, kemudian pada masing-masing labu ukur ditambahkan 1 mL larutan DPPH 1 mM yang seluruh bagian
labu ukurnya telah ditutup dengan
alumunium foil dan diencerkan dengan metanol sampai tanda batas (10 mL), lalu
dihomogenkan. Kemudian dibiarkan
ditempat gelap pada suhu kamar selama waktu inkubasi optimum (Mustikasari, dkk. 2012).
Pengujian Antioksidan Dengan Metode DPPH
Deret larutan uji, deret larutan control positif (Vitamin C) dan larutan blanko diukur serapannya pada panjang gelombang maksimum yang telah ditentukan dengan spektrofotometer. Nilai Persentase hambatan terhadap DPPH dihitung dengan rumus berikut:
% Hambatan = 𝑠𝑒𝑟𝑎𝑝𝑎𝑛 𝑏𝑙𝑎𝑛𝑘𝑜−𝑠𝑒𝑟𝑎𝑝𝑎𝑛 𝑠𝑎𝑚𝑝𝑒𝑙𝑠𝑒𝑟𝑎𝑝𝑎𝑛 𝑏𝑙𝑎𝑛𝑘𝑜 𝑥 100 % Nilai IC50 dengan konsentrasi
penghambatan tengah (50%) dengan
persamaan y = bx + a, dimana y = 50 dan x adalah konsentrasi larutan uji yang mampu menghambat 50 % larutan radikal bebasa 1,1- difenil-2-fikrilhidrazil (Mustikasari, dkk. 2012).
HASIL DAN PEMBAHASAN
Karakteristik Serbuk Simplisia Daun Binahong
Serbuk simplisia daun binahong yang diperoleh berwarna hijau pekat kecoklatan, mempunyai rasa sedikit asin, kelat dan lama-lama terasa pahit serta mempunyai bau yang menyengat dan khas. Rendemen simplisia daun binahong sebesar 5,675 %. Kadar air dari simplisia dan sediaan daun binahong di pasaran dapat dilihat pada Tabel 1 dan kadar abu sebesar 16,28%. Serbuk Simplisia dapat dilihat pada Gambar 1.
Gambar.1 Serbuk Simplisia Daun Binahong
Tabel 1. Kadar Air
Sampel Kadar air (%)
1 2 Rata-rata A 5,9 6,7 6,3 B 5,8 5,6 5,7 C 5,7 6,1 5,9 D 6,5 6,1 6,3 E 5,1 5,3 5,2 F 4,9 5 4,95 Keterangan :
Sampel A,B,C,D dan E : Sediaan daun
binahong yang terdapat di pasaran.
Sampel F : Daun
binahong
Ekstrak Cair Daun Binahong dan Sediaan Kapsul daun Binahong yang Beredar di Pasaran
Gambar 2. Ekstrak cair etanol 70%
daun binahong dan sediaan daun binahong yang beredar di pasaran (sediaan daun binahong yang ada di
pasaran: sampel a,b, c, d dan e ; sampel daun binahong : sampel f)
Ekstrak cair yang diperoleh dari masing masing sampel yaitu sebanyak 50 mL.Ekstrak cair etanol 70% (daun binahong dan sediaan daun binahong yang beredar di
pasaran) yang diperoleh kemudian
digunakan dalam tahap uji selanjutnya yaitu uji fitokimia, penetapan kadar flavonoid total dan potensi antioksidan daridaun binahong dan sediaan daun binahong di pasaran.
Hasil Uji Fitokimia
Tujuan dari uji fitokimia ini sebagai uji pendahuluan untuk mengetahui kandungan kimia yang ada di dalam suatu sampel,
khususnya metabolit sekunder atau
senyawa- senyawa yang terkandung dalam serbuk simplisia daun binahong dan sediaan daun binahong yang beredar di pasaran sebelum dilakukan ekstraksi, serta untuk
mengetahui senyawa- senyawa yang
terkandung dalam ekstrak etanol 70% daun binahong serta sediaan daun binahong yang terdapat di pasaran. Dari hasil uji dapat diketahui baik serbuk simplisia maupun ekstrak cair daun binahong dan sediaan daun binahong di pasaran mengandung flavonoid, alkaloid, saponin dan tanin.
Hasil Penetapan Kadar Flavonoid Total
Kadar flavonoid total pada simplisia daun binahong dan sediaan daun binahong yang beredar di pasaran yang diperoleh dihitung dengan menggunakan persamaan kurva kalibrasi standar kuersetin yaitu y = 0,0826x + 0.0367. Kandungan flavonoid total dari setiap sampel dapat dilihat pada Tabel 2.
Tabel 2. Kadar Flavonoid Total
Sampel Rata-Rata Kadar
Flavonoid (%) serbuk simplisia A 5,888 ± 0,129 B 7,327 ± 0,128 C 5,943 ± 0,112 D 6,066 ± 0,048 E 13,019 ± 0,207 F 21,180 ± 0,175 Keterangan :
Sampel A,B,C,D dan E : Sediaan daun binahong yang terdapat di pasaran
Berdasarkan metode analisis ini, flavonoid total yang terukur merupakan sumbangan dari golongan flavon dan flavonol yang terdapat pada ekstrak karena hanya kedua golongan flavonoid ini yang
dapat membentuk kompleks stabil dengan AlCl3 pada gugus keto C4 dan C3 atau C5
pada gugus hidroksil yang dimiliki
(Markham, 1988). Reaksi dari Flavonoid dan AlCl3 dapat dilihat pada Gambar 3.
Gambar 3. Reaksi antara flavonoid dengan AlCl3 (Sumber : Markham, 1988)
Berdasarkan Tabel 2 diatas dapat terlihat bahwa terdapat perbedaan kadar flavonoid dari masing-masing sampel. Diperkirakan hal tersebut dapat dikarenakan proses pembuatan sediaan yang berbeda dari setiap sampel dan lama penyimpanan sediaanpun dapat berpengaruh. Selain itu, perbedaan kadar flavonoid pada setiap sampel dapat dipengaruhi oleh faktor lingkungan seperti kondisi lingkungan tempat tumbuh, suhu, sinar ultraviolet, hara, ketersediaan air dan kadar CO2 pada atmosfer (Rohaeti, E, dkk. 2011).
Berdasarkan hasil tersebut dapat terlihat pula bahwa simplisia daun binahong yaitu sampel F mempunyai kandungan flavonoid
total yang lebih tinggi dibandingkan dengan sediaan daun binahong yang beredar di pasaran. Jika sediaan daun binahong di pasaran di urutkan sampel E mempunyai kadar flavonoid total yang paling tinggi dibandingkan sediaan di pasaran lainnya. Hal tersebut dapat dilihat dari warna serbuk sediaan kapsul daun binahong. Dimana sampel E mempunyai warna yang lebih pekat dibandingkan sampel yang lain, hal tersebut menunjukkan kemungkinan adanya keterkaitan antara kadar flavonoid dengan warna serbuk simplisia. Gambar dari serbuk simplisia daun binahong dan sediaan daun binahong dapat di lihat pada Gambar 4.
Sampel A Sampel B Sampel C
Sampel D Sampel E Sampel F
Gambar 4. Serbuk simplisia daun binahong (sampel F) dan serbuk sediaan kapsul daun
Hasil Penetapan Potensi Antioksidan
Penetapan potensi antioksidan ini dilakukan dengan cara menetapkan nilai IC50 atau melihat potensi antioksidan simplisia daun binahong dan sediaan daun binahong yang beredar di pasaran yang mampu menghambat 50% radikal bebas, dimana radikal yang digunakan pada penelitian ini adalah DPPH (1,1-difenil-2-fikrilhidrazil).
Standar yang digunakan disini yaitu vitamin C karena vitamin C mempunyai potensi antioksidan yang tinggi, dimana hasil penelitian sebelumnya menyatakan bahwa
vitamin C berpotensi aktif sebagai
antioksidan yaitu sebesar 3,87 ppm
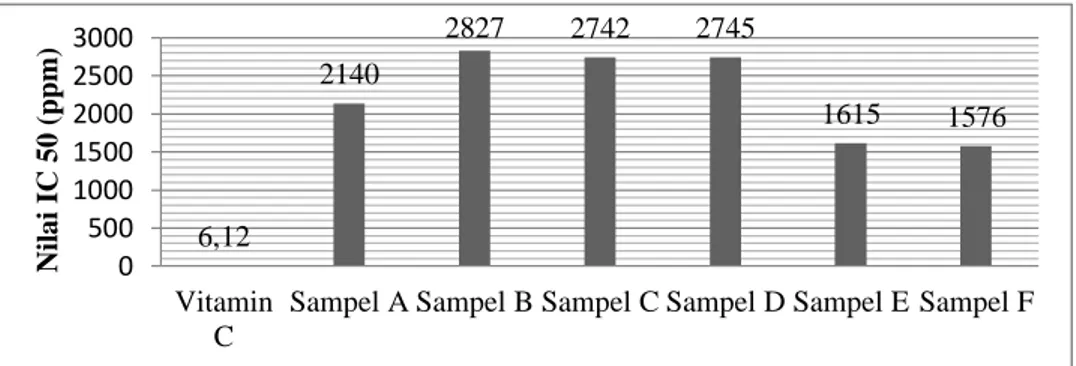
(Mustikasari, 2012). Hasil penetapan potensi antioksidan pada setiap sampel dapat dilihat pada Gambar 5.
Gambar 5. Potensi antioksidan Vitamin C, simplisa daun binahong dan sediaan daun binahong
yang ada di pasaran. Uji Potensi antioksidan didasarkan
pada penangkapan radikal bebas (DPPH)
oleh senyawa antioksidan melalui
mekanisme donasi atom hydrogen sehingga akan dihasilkan DPPH tereduksi atau DPPH non radikal (DPPH-H). Parameter penentuan potensi antioksidan dapat dilihat dari nilai IC50. Harga IC50 digunakan untuk
menyatakan potensi atau aktivitas
antioksidan suatu senyawa dengan metode peredaman radikal bebas DPPH (Chow, et
al. 2003). semakin kecil nilai IC50 suatu senyawa yaitu kurang dari 50 ppm berarti senyawa tersebut sangat aktif sebagai antioksidan atau dengan kata lain senyawa tersebut mempunyai potensi yang besar sebagai antioksidan .
Sampel yang digunakan disini yaitu dalam bentuk simplisia yaitu berupa simplisia daun binahong dan sediaan daun
binahong yang beredar di pasaran.
Berdasarkan Gambar 5 jika diurutkan dapat terlihat bahwa potensi antioksidan yang paling tinggi yaitu sampel F ( simplisia daun
binahong) dibandingkan sediaan daun
binahong di pasaran, kemudian diikuti oleh sempel E, A,D,C dan B. Sampel F dan E berbading lurus dengan kadar flavonoid yang didapat dimana kadar flavonoid yang
tinggi dari sampel F dan E memiliki potensi antioksidan yang cukup baik dibandingkan sediaan daun binahong yang beredar di pasaran (sampel A, B, C dan D). Sedangkan pada sampel A, D, C dan B tidak berbanding lurus terhadap kadar flavonoid yang didapat. Seperti sampel A yang memiliki kadar flavonoid lebih kecil dibandingkan sampel B tetapi nilai IC50 pada sampel A lebih baik dibandingkan sampel B. Hal tersebut dapat dikarenakan tidak semua senyawa flavonoid bereaksi dengan AlCl3, kemungkinan adanya senyawa polifenol lain didalam daun binahong dan sediaan daun binahong di pasaran seperti tanin dan flavonoid jenis lain yang dapat berpengaruh terhadap IC50 suatu tumbuhan yang tidak dapat bereaksi dengan AlCl3 (Markham, 1988 dan Maulidzy, 2016). Selain itu, dapat dikarenakan sumber daun binahong pada setiap sediaan kapsul daun binahong di pasaran berasal dari tempat berbeda, karena
tempat tumbuh suatu tanaman akan
mempengaruhi jumlah kandungan metabolit
sekunder termasuk senyawa flavonoid
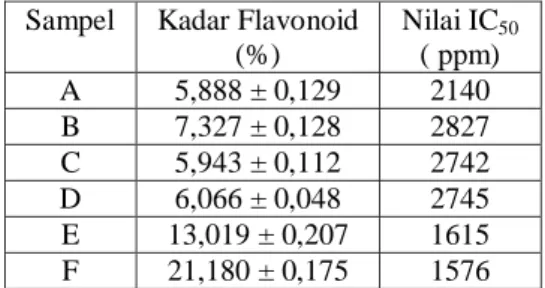
(Rohaeti, 2011) Perbandingan antara potensi antioksidan dan kandungan flavonoid dapat dilihat pada Tabel 3.
6,12 2140 2827 2742 2745 1615 1576 0 500 1000 1500 2000 2500 3000 Vitamin C
Sampel A Sampel B Sampel C Sampel D Sampel E Sampel F
Nil ai IC 50 (p p m )
Tabel 3. Pebandingan Kadar Flavonoid dan Nilai IC50 serbuk simplisia daun
Binahong dan Sediaan Daun Binahong di Pasaran
Sampel Kadar Flavonoid
(%) Nilai IC50 ( ppm) A 5,888 ± 0,129 2140 B 7,327 ± 0,128 2827 C 5,943 ± 0,112 2742 D 6,066 ± 0,048 2745 E 13,019 ± 0,207 1615 F 21,180 ± 0,175 1576
Standar antioksidan yang
digunakan yaitu vitamin C. Vitamin C
merupakan antioksidan yang sering
dikonsumsi oleh masyarakat secara luas.
Hasil penelitian menunjukkan bahwa
vitamin C berpotensi aktif sebagai
antioksidan dengan IC50 sebesar 6,12 ppm dan berdasarkan hasil penentuan potensi antioksidan menunjukkan bahwa baik daun binahong maupun sediaan daun binahong yang beredar di pasaran tidak mempunyai potensi sebagai antioksidan karena nilai IC50 yang diperoleh lebih dari 1000 ppm (Chow,
et al. 2003). Hal tersebut berbanding terbalik
dengan penelitian sebelumnya bahwa
ekstrak etanol daun binahong aktif sebagai
antioksidan atau berpotensi sebagai
antioksidan, dimana nilai IC50 yang diperoleh sebesar 75,26 ppm (Mustikasari, 2012) Hal tersebut dapat dikarenakan perbedaan bentuk sediaan yang digunakan dimana pada penelitian sebelumnya tersebut menggunakan ekstrak kering, sedangkan, pada penelitian ini menggunakan simplisia. Penggunaan simplisia ini kurang efektif pada penetapan potensi antioksidan, karena jumlah simplisia yang digunakan tidak sebanding dengan ekstrak kering atau kental yang digunakan pada penelitian sebelumnya.
SIMPULAN DAN SARAN Kesimpulan
Dari hasil penelitian ini dapat ditarik kesimpulan bahwa:
1. Serbuk simplisia daun binahong
memiliki kadar flavonoid sebesar 21,1801% dan sediaan daun binahong yang beredar di pasaran memiliki kadar
flavonoid antara 5,888% sampai
13,0194%.
2. Serbuk simplisia daun binahong dan sediaan daun binahong yang beredar di pasaran tidak aktif sebagai antioksidan dengan nilai IC50 lebih dari 1000 ppm.
Saran
1. Perlu dilakukan penelitian lebih lanjut untuk mengetahui potensi antioksidan sediaan daun binahong yang beredar di pasaran dan kadar flavonoid sediaan daun binahong yang beredar di pasaran yang dibuat dalam bentuk ekstrak kering dan ekstrak kental.
2. Perlu dilakukan optimasi waktu
maserasi terhadap ekstraksi daun binahong.
DAFTAR PUSTAKA
Chang C, M. Yang , H. Wen dan J. Chern. 2002. Estimation of totalf content in propolis by two complementary colorimetric methods. Journal of
Food and Drug Analysis. 10 (3):
178-182
Chow,S.T., WW Chau, YC Chung. 2003. Antioxidant activity and safety of 50% etanolic red bean ekstraks (Phaceolus raditus L. Var Aurea).
Journal of Food Sciene. 68 (1) :
21-25
DepKes RI. 1979. Materia Medika
Indonesia, Jilid III. Direktorat
Jenderal Pengawasan Obat Dan Makanan. Jakarta. Halaman 171
DepKes RI. 1980. Materia Medika
Indonesia, Jilid IV. Direktorat
Jenderal Pengawasan Obat Dan Makanan. Jakarta. Halaman 166-170
DepKes RI. 1995. Farmakope Indonesia
Edisi IV. Direktorat Jendral Pengawasan Obat dan Makanan. Jakarta. Halaman 7
DepKes RI. 2000. Parameter Standar
Umum Tumbuhan Obat. Direktorat
Jendral Pengawasan Obat dan Makanan. Jakarta. Halaman 10-17 Desmiyati, Y., Ratnawati J dan Andini P.
2009. Penentuan Jumlah Flavonoid Total Ekstrak Etanol Daun Buah Merah (Pandanus conoideus Lamk.) Secara Kolorimetri Komplementer.
Jurnal Farmasi Universitas Jendral Ahmad Yani. Bandung.
Dipresentasikan Pada Seminar
Nasional POKJANAS TOI XXXVI 13& 14 mei 2009, Universitas Sanata Dharma, Yogyakarta. Harborne J.B.1987. Metode Fitokimia.
Penerjemah Kosasih Padmawinata dan Iwang Sudiro. ITB. Bandung.
Terjemahan dari Phytocemycal
Methods. Halaman 69-71
Markham K.R. 1988. Cara Mengidentifikasi
Flavonoid. ITB. Bandung. Penerjemah Kosasih Padmawinata. Terjemahan dari Techniques of
flavonoid identification. Halaman
3-10
Maulidzy, A.Z dan Adisti D. 2016
Perbandingan Aktivitas
Antioksidan dan Kadar Tanin Ekstrak Pegagan dengan Produk
Jadi Pegagan. Universitas
Indonesia. Jakarta. eJKI. Vol. 4(1): 15-20
Mustikasari, V., Sutanto dan S. Wardatun.
2012. Potensi ekstrak daun
binahong (Anredera cordifolia
(Ten.) Steenis) sebagai antioksidan. Program Studi Farmasi FMIPA
Universitas Pakuan. Bogor.
Kumpulan Jurnal Farmasi.
Halaman 8-14
Rohaeti, E., R. Heryanto, M.Raffi, A.
Wahyuningrum, dan L.K.
Darusman.2011. Prediksi Kadar
Flavonoid Total Tempuyung
(Sonchus arvensis L.)
Menggunakan Kombinasi
Spektroskopi IR Dengan Regresi Kuadrat Terkecil Parsial. Fakultas MIPA, IPB. Bogor. Jurnal Kimia. Vol. 5 (2): 101-108
Sastrawan, Idza N., M. Sangi dan Vanda K. 2013. Skrining Fitokimia dan Uji aktivitas Antioksidan Ekstrak Biji
Adas (Foeniculum vulgare)
Menggunakan Metode DPPH.
Program Studi Kimia FMIPA
Universitas Sam Ratulangi.
Manado. Jurnal Ilmiah Sains Vol. 13 No. 2: 110-115
Suryanto, E. dan F. Wehantouw.2009. Aktivitas Penangkap Radikal Bebas Dari Ekstrak Fenolik Daun Sukun (Artocarpus altilis F.). Fakultas MIPA Universitas Sam Ratulingi. Manado. Chem Prog. Vol. 2 (1): 1-7
Umar, A., Dwi K., dan Diah T.M. 2012. Pengaruh pemberian ekstrak daun binahong (Anredera cordifolia (Ten) Steenis) terhadap
kesembuhan luka infeksi
Staphylococcus aureus pada
mencit. Analisis Kesehatan
Poltekkes Kemenkes. Surabaya.
Analisis Kesehatan Sains. Vol. 1
(2): 68-75
Widya S., M.R.J Runtuwena dan Gayatri C. 2013. Kandungan Flavonoid dan
Kapasitas Antioksidan Total Ekstrak Etanol Daun Binahong
(Anredera cordifolia (Ten)
Steenis). Program Studi Farmasi FMIPA UNSRAT. Manado. Jurnal
Ilmiah Farmasi. Vol. 02 (01):
18-22
Winarsi, H. 2007. Antioksidan Alami dan
Radikal Bebas. Kanisius. Yogyakarta.