SINTESIS DAN KARAKTERISASI HIDROGEL CRF BERBASIS
AKRILAMIDA DAN CROSSLINKER N,N’-METILENBISAKRILAMIDA
DENGAN PENAMBAHAN EKSTRAK SDT
SKRIPSI
diajukan untuk memenuhi sebagian dari syarat memperoleh gelar Sarjana Sains Progam Studi Kimia
Oleh
TRIA ADHIMU KURNIA NIM 0902038
PROGRAM STUDI KIMIA JURUSAN PENDIDIKAN KIMIA
FAKULTAS PENDIDIKAN MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS PENDIDIKAN INDONESIA
SINTESIS DAN KARAKTERISASI HIDROGEL CRF BERBASIS
AKRILAMIDA DAN CROSSLINKER N,N’-METILENBISAKRILAMIDA
DENGAN PENAMBAHAN EKSTRAK SDT
Oleh
Tria Adhimu Kurnia
Sebuah skripsi yang diajukan untuk memenuhi salah satu syarat memperoleh gelar Sarjana Sains pada Fakultas Pendidikan Matematika dan Ilmu Pengetahuan Alam
© Tria Adimu Kurnia Universitas Pendidikan Indonesia
Januari 2014
Hak Cipta dilindungi undang-undang.
TRIA ADHIMU KURNIA
SINTESIS DAN KARAKTERISASI HIDROGEL CRF BERBASIS
AKRILAMIDA DAN CROSSLINKER N,N’-METILENBISAKRILAMIDA
DENGAN PENAMBAHAN EKSTRAK SDT
Disetujui dan disahkan oleh pembimbing:
Pembimbing I
Dr. Hendrawan, M.Si. NIP. 196309111989011001
Pembimbing II
Fitri Khoerunnisa, Ph.D. NIP. 197806282001122001
Mengetahui,
Ketua Jurusan Pendidikan Kimia FPMIPA UPI
ABSTRAK
Telah disintesis hidrogel controlled release fertilizer (CRF) berbahan dasar akrilamida (AAm) dan crosslinker N,N’-Metilenbisakrilamida (MBA) dengan penambahan ekstrak SDT. Penelitian ini bertujuan untuk mensintesis hidrogel CRF dan mengetahui karakteristik serta kinerjanya. Penyiapan hidrogel CRF dilakukan melalui penyisipan nutrien (Zink nitrat) ke dalam hidrogel yang disintesis pada kondisi optimum. Morfologi struktur dari hidrogel CRF diidentifikasi dengan menggunakan Fourier Transform Infrared Spectra (FTIR) spektroskopi dan metode X-Ray Diffraction (XRD). Kinerja hidrogel CRF ditentukan melalui pengukuran swelling ratio, water retention, dan release behavior. Hasil karakterisasi menunjukkan bahwa penyisipan nutrien meningkatkan kristalinitas hidrogel dan hasil FTIR menunjukkan dalam hidrogel CRF terdapat puncak serapan gugus fungsi –OH/-NH, C=O, C-O, dan –NO. Swelling ratio (%SR) dan water retention (%WR) dari hidrogel CRF yang disintesis adalah 60,63% dan
9,62% secara berturut-turut. Release behavior yang disisipkan pada hidrogel bergantung pada jumlah nutrien yang terabsorpsi pada hidrogel, dengan nilai optimum yang terjadi pada penyisipan nutrien 4,987 ppm per 0,3313 gram hidrogel. Hasil uji kinerja ini menunjukkan bahwa hidrogel CRF yang disintesis berpeluang untuk diaplikasikan sebagai agen controlled release nutrient dalam bidang pertanian.
ABSTRACT
We have successfully been synthesized the hydrogel based on Acrylamide (AAM) with addition of SDT extract and the cross-linker of N,N’-methylenebisacrylamide (MBA) for controlled release fertilizer (CRF) material. The aim of study was to synthesis the CRF hydrogels and to determine their characteristics and performance. Preparation of CRF hydrogel was determined through the insertion of nutrient (Zink nitrate) into hydrogel synthesized at optimum condition. The morphological structure of CRF hydrogel was identified by Fourier Transform Infrared Spectra (FTIR) spectroscopy and X-ray diffraction (XRD) method. Performance of CRF hydrogel was determined by measured swelling ratio (%SR), water retention (%WR), and release behavior. The characterization results indicated that insertion of nutrient increased the crystallinity of the hydrogel and the result of FTIR showed in CRF hydrogel existed absorption peak of functional group –
OH/-NH, C=O, C-O, and –NO . The synthesized CRF hydrogel has the swelling ratio (% SR) and water retention (WR%) of the synthesized hydrogels were 60,63% and 9,62%, respectively. The release behavior of nutrient was influenced by the amount of nutrients absorbed in the hydrogel with inserted nutrient/hydrogel = 4.987 ppm / 0.3313 gram. The performance study indicated that the CRF hydrogels was applicable to be used as CRF agent in agriculture practices.
DAFTAR ISI
PERNYATAAN ... i
ABSTRAK ... ii
KATA PENGANTAR ... iv
UCAPAN TERIMA KASIH ... v
DAFTAR ISI ... vii
DAFTAR TABEL ... x
DAFTAR GAMBAR ... xi
DAFTAR LAMPIRAN ... xiii
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Rumusan Masalah ... 3
1.3 Tujuan Penelitian ... 3
1.4 Manfaat Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Hidrogel ... 5
2.2 Reaksi Pembentukan Hidrogel ... 6
2.3 Poliakrilamida ... 7
2.4 Polimerisasi Akrilamida ... 8
2.4.1. Tahap Inisiasi ... 8
2.4.2. Tahap Propagasi ... 9
2.4.3. Reaksi Terminasi ... 10
2.7 Kinerja Hidrogel ... 13
2.7.1. Swelling Ratio ... 13
2.7.2. Water Retention ... 14
2.7.3. Release Behavior ... 15
2.8 Hidrogel CRF ... 16
2.9 Nutrien ... 16
2.9.1.Makronutrien ... 16
2.9.2.Mikronutrien ... 18
BAB III METODE PENELITIAN ... 20
3.1Lokasi dan Waktu Penelitian ... 20
3.2Alat-Alat Penelitian ... 20
3.3Bahan-Bahan Penelitian ... 20
3.4Prosedur Penelitian ... 21
3.4.1. Tahap Preparasi ... 24
3.4.1.1 Pembuatan Larutan Asam Klorida 5% ... 24
3.4.1.2 Pembuatan Larutan NaOH 10-4 M ... 24
3.4.1.3 Pembuatan Larutan Akrilamida 1,4 M ... 24
3.4.1.4 Pembuatan Larutan MBA 0,13 M ... 24
3.4.1.5 Pembuatan Larutan Kalium Persulfat 1,4M ... 24
3.4.1.6 Pembuatan Larutan Sodium Metabisulfit 0,07 M .... 24
3.4.1.7 Tahap Pembuatan Nutrien 0,25 M ... 25
3.4.1.8 Tahap Pembuatan Ekstrak SDT ... 25
3.4.2. Tahap Sintesis ... 25
3.4.2.1 Optimasi Waktu Ekstraksi SDT ... 25
3.4.2.2 Sintesis Hidrogel ... 26
3.4.3. Sintesis Hidrogel CRF ... 26
3.4.3.1 Penyisipan Nutrien ke dalam Hidrogel ... 26
3.4.3.2 Tahap Karakterisasi Struktur Morfologi Hidrogel ... 26
3.4.3.2.2. X-Ray Difraction (XRD) ... 27
3.4.3.3 Uji Kinerja Hidrogel ... 28
3.4.3.3.1 Swelling Ratio ... 28
3.4.3.3.2 Water Retention ... 28
3.4.3.3.3 Release Behavior ... 28
BAB IV PEMBAHASAN ... 30
4.1Tahap Preparasi dan Ekstraksi SDT ... 30
4.1.1. Penyiapan Simplisia ... 30
4.1.2. Optimasi Pelarut ... 31
4.2Sintesis Hidrogel ... 32
4.2.1. Optimasi Waktu Ekstraksi dengan HCl 5% ... 32
4.2.1.1 Uji Swelling Ratio ... 33
4.2.1.2 Uji Water Retention ... 35
4.2.1.3 Karakteristik FTIR Hidrogel ... 37
4.3Sintesis Hidrogel CRF (Controlled Release Fertilizer) ... 37
4.3.1. Sintesis Hidrogel CRF ... 37
4.3.2. Karakterisasi Hidrogel CRF... 38
4.3.2.1 Analisis FTIR ... 38
4.3.2.2 Analisis X-Ray Difraction (XRD) ... 39
4.3.3. Uji Kinerja Hidrogel CRF ... 40
4.3.3.1 Uji Swelling Ratio ... 40
4.3.3.2 Uji Water Retention ... 43
4.3.3.3 Release Behavior ... 44
BAB V KESIMPULAN DAN SARAN ... 47
5.1Kesimpulan ... 47
5.2Saran... 47
DAFTAR PUSTAKA ... 48
DAFTAR TABEL
Tabel 2.1 Polimer Alami dan Polimer/Monomer Sintetik yang Digunakan
dalam Pembuatan Hidrogel ... 5
Tabel 2.2 Sifat-Sifat Poliakrilamida ... 8
Tabel 2.3 Nutrisi Esensial untuk Pertumbuhan Tanaman ... 16
Tabel 2.4 Makronutrien Primer dan Sekunder, Gejala Umum Defisiansi,
Kemungkinan Penyebab, serta Metode untuk Memperbaiki ... 17
Tabel 2.5 Mikronutrien, Gejala Umum Defisiensi, Kemungkinan Penyebab,
serta Metode untuk Memperbaiki ... 18
Tabel 3.1 Optimasi Waktu Ekstraksi SDT ... 26
Tabel 4.1 Parameter Difraksi Sinar-X untuk Hidrogel dan Hidrogel-
Nutrien... 40
DAFTAR GAMBAR
Gambar 2.1 Struktur Molekul Akrilamida... 7
Gambar 2.2 Struktur Molekul Poliakrilamida ... 8
Gambar 2.3 Tahap Inisiasi ... 9
Gambar 2.4 Tahap Propagasi ... 9
Gambar 2.5 Tahap Disporposionasi ... 10
Gambar 2.6 Tahap Kombinasi ... 10
Gambar 2.7 Jenis Tumbuhan SDT ... 11
Gambar 2.8 Struktur N,N’-metilenbisakrilamida (MBA) ... 13
Gambar 2.9 Reaksi Crosslinking antara PAAm dan MBA ... 13
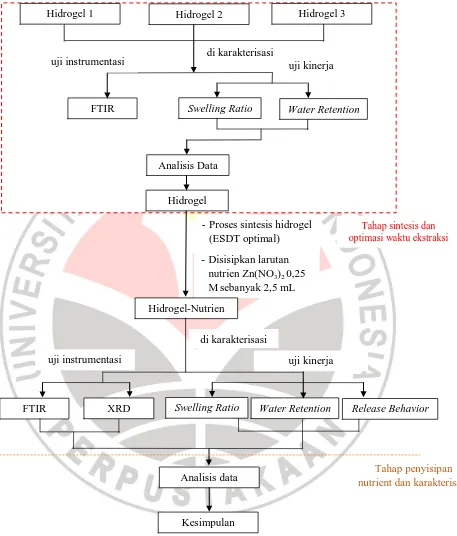
Gambar 3.1 Diagram Alir Penelitian ... 21
Gambar 4.1 Spektrum FTIR SSDT ... 30
Gambar 4.2 Hidrogel ESDT A ... 32
Gambar 4.3 Hidrogel dalam kondisi basah (a), dan Hidrogel setelah Pengeringan dalam oven (b) ... 33
Gambar 4.4 Swelling Ratio Hidrogel ... 34
Gambar 4.5 Water Retention Hidrogel per Menit ... 36
Gambar 4.6 Water Retention Hidrogel per Hari ... 36
Gambar 4.7 Spektra FTIR Hidrogel ... 37
Gambar 4.8 Spektrum FTIR Hidrogel dan Hidrogel-Nutrien ... 38
Gambar 4.10 Swelling Ratio Hidrogel-Nutrien dan Hidrogel per Menit .... 41
Gambar 4.11 Swelling Ratio Hidrogel-Nutrien per Hari ... 41
Gambar 4.12 (a) Perbandingan Massa Swelling Hidrogel dengan Hidrogel-
Nutrien per Menit dan (b) Perbandingan Massa Swelling
Hidrogel per Menit dengan Hidrogel-Nutrien per Hari ... 43
Gambar 4.13 Water Retentio pada Hidrogel dan Hidrogel-Nutrien... 44
DAFTAR LAMPIRAN
Lampiran 1 Data Perhitungan ... 51
Lampiran 2 Tabel Swelling Ratio Tahap Optimasi Waktu Ekstraksi SDT .. 53
Lampiran 3 Tabel Swelling Ratio Hidrogel tanpa SDT per Menit ... 54
Lampiran 4 Tabel Swelling Ratio Hidrogel tanpa SDT per Hari ... 55
Lampiran 5 Tabel Water Retention Tahap Optimasi Waktu Ekstraksi SDT 56 Lampiran 6 Tabel Swelling Ratio Hidrogel-Nutrien per Menit ... 57
Lampiran 7 Tabel Swelling Ratio Hidrogel-Nutrien per Hari ... 58
Lampiran 8 Tabel Water Retention Hidrogel-Nutrien ... 59
Lampiran 9 Spektrum FTIR Akrilamida ... 60
Lampiran 10 Spektum FTIR N,N’-Metilenbisakrilamida ... 61
Lampiran 11 Spektrum FTIR Simplisia SDT ... 62
Lampiran 12 Spektum FTIR Ekstrak SDT 0 Hari ... 63
Lampiran 13 Spektrum FTIR Ekstrak SDT 1 Hari ... 64
Lampiran 14 Spektrum FTIR Ekstrak SDT 7 Hari ... 65
Lampiran 15 Spektrum FTIR Hidrogel-Nutrien ... 66
Lampiran 16 Difraktogram Hidrogel dan Hidrogel-Nutrien ... 67
BAB 1
PENDAHULUAN
1.1 Latar Belakang Masalah
Indonesia merupakan salah satu negara agraris yang memiliki sumber daya
alam yang melimpah dan masih bertumpu pada pertanian. SAKERNAS (2006)
menyatakan bahwa penduduk Indonesia yang bekerja dalam bidang pertanian
mencapai 42.039.250 orang dari 95.177.102 orang (44,2%) penduduk Indonesia
yang bekerja. Ada beberapa hal yang mendasari mengapa pembangunan pertanian
di Indonesia mempunyai peranan penting, antara lain: potensi sumber daya alam
yang besar dan beragam, pangsa terhadap pendapatan nasional (ekspor) yang
cukup besar, dan besarnya penduduk Indonesia yang menggantungkan hidupnya
pada sektor ini, serta perannya dalam penyediaan pangan masyarakat dan menjadi
basis pertumbuhan di pedesaan.
Produktivitas pertanian Indonesia sampai saat ini masih dihadapkan
dengan berbagai masalah, diantaranya; (1) adanya pembaharuan agraria (konversi
lahan pertanian menjadi lahan non pertanian) yang menyebabkan lahan pertanian
menjadi semakin sempit, (2) pencemaran lingkungan akibat inefisiensi penggunaan
pupuk untuk pertumbuhan tanaman, dimana hanya sekitar 20 - 70 % dari pupuk
yang digunakan akan hilang ke lingkungan. Kehilangan ini disebabkan karena
adanya leaching, dekomposisi, dan volatilisasi komponen pupuk di tanah (Shaviv
dan Mikkelsen, 1993), dan (3) kenaikan harga pupuk yang mengakibatkan
meningkatnya biaya produksi.
Hidrogel merupakan salah satu alternatif material yang dapat digunakan
untuk mengatasi berbagai masalah pertanian seperti dijelaskan di atas karena
penggunaan hidrogel dapat meningkatkan efisiensi proses pertanian terutama
dalam meminimalkan pengaruh negatif terhadap lingkungan yang disebabkan oleh
penggunaan pupuk secara berlebih. Penggunaan hidrogel dalam sektor pertanian
telah mendapatkan banyak perhatian dari berbagai peneliti khususnya dalam
2
Menurut Wang et al dalam Putri (2013), CRF merupakan salah satu
metode untuk mengurangi tingkat kehilangan pupuk dari tanah akibat pencucian
oleh air hujan atau air irigasi, mempertahankan persediaan air atau mineral untuk
waktu yang cukup lama hingga pemulihan lahan kering, meningkatkan efisiensi
pupuk, mengurangi potensi efek negatif dari kelebihan dosis, dan mengurangi
tingkat toksisitas
Hidrogel dapat dijadikan salah satu agen CRF karena material hidrogel
tersusun atas struktur ikatan silang tiga dimensi yang dibentuk oleh polimer
hidrofilik, yang bersifat tidak larut dalam air, dapat mengembang dalam air
(swelling), dan dapat mempertahankan bentuk aslinya. Dengan menggunakan
hidrogel CRF dapat meningkatkan efisiensi pemupukan karena pelepasan air dan
nutrien dapat diperlambat atau bahkan dapat dikontrol, sehingga tanaman dapat
menyerap nutrien dan air lebih banyak tanpa terbuang percuma (Putri, 2013). Pada
beberapa tahun belakangan ini penelitian dan pengembangan hidrogel dari bahan
alam untuk pertanian telah menjadi pusat perhatian ilmuan. Bahan polimer alam
memiliki banyak keunggulan dibanding bahan sintetis dimana bahan alam bersifat
biodegradable, ketersediaannya melimpah, bernilai ekonomis, dan berkontribusi
positif pada konservasi alam (Chotimah, 2013).
Terdapat beberapa alternatif bahan alam yang merupakan jenis tumbuhan
tingkat rendah dengan kandungan polimer yang tinggi, yang berpotensi digunakan
sebagai komponen hidrogel. Dalam penelitian ini peneliti mencoba
mengeksplorasi tumbuhan SDT (agar-agar) yang kelimpahannya cukup besar di
Indonesia sebagai salah satu bahan dasar hidrogel. Komponen terbesar SDT ialah
polisakarida yang memiliki struktur tiga dimensi, dapat mengembang, menyusut,
dan membentuk gel (Chotimah, 2013). Selain itu, senyawa metabolit sekunder
pada SDT (alkaloid, saponin, tanin, steroid, dan glikosida) dapat berkontribusi
dalam pembentukan hidrogel (Firdaus, dkk., 2009).
Erizal dkk (2007) telah berhasil mensintesis hidrogel berbahan dasar polimer
alami (alginat) yang dicampurkan dengan Akrilamida (AAm) dengan crosslinking
3
khusus yang sulit diaplikasikan di laboratorium secara umum. Oleh karena itu
pada penelitian ini akan disintesis hidrogel menggunakan bahan dasar AAm dan
polimer alam dari ekstrak SDT dengan teknik crosslinking secara kimiawi.
Diharapkan metoda sintesis ini dapat dijadikan alternatif dalam pembuatan
hidrogel berbahan dasar AAm.
Berdasarkan latar belakang di atas, dalam penelitian ini akan disintesis dan
dikarakterisasi hidrogel CRF berbahan dasar AAm dan crosslinker MBA dengan
penambahan ekstrak SDT.
1.2 Rumusan Masalah
Berdasarkan uraian latar belakang yang dikemukakan di atas, maka
rumusan masalah penelitian ini adalah:
1. Bagaimana preparasi hidrogel CRF berbahan dasar AAm dan
crosslinker MBA dengan penambahan ekstrak SDT?
2. Bagaimana karakterisasi struktur dan morfologi hidrogel CRF
berbahan dasar AAm dan crosslinker MBA dengan penambahan
ekstrak SDT?
3. Bagaimana kinerja hidrogel CRF berbahan dasar AAm dan
crosslinker MBA dengan penambahan ekstrak SDT?
1.3 Tujuan Penelitian
Tujuan dari penelitian ini adalah:
1. Mengetahui preparasi hidrogel CRF berbahan dasar AAm dan
crosslinker MBA dengan penambahan ekstrak SDT.
2. Mengetahui karakterisasi struktur dan morfologi hidrogel CRF
berbahan dasar AAm dan crosslinker MBA dengan penambahan
ekstrak SDT.
3. Mengetahui kinerja hidrogel CRF berbahan dasar AAm dan
4
1.4 Manfaat Penelitian
Hasil dari penelitian ini diharapkan dapat memberikan manfaat sebagai:
1. Metode alternatif untuk sintesis hidrogel CRF secara kimiawi
berbahan dasar AAm dengan penambahan ekstrak SDT.
2. Referensi mengenai hidrogel CRF berbasis AAm dengan penambahan
20
BAB III
METODE PENELITIAN
3.1 Lokasi dan Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Riset Jurusan Pendidikan Kimia
FPMIPA UPI. Untuk keperluan analisis FTIR dilakukan di Laboratorium Kimia
Analitik Jurusan Pendidikan Kimia FPMIPA UPI, analisis AAS dilakukan di
TEKMIRA, dan analisis XRD dilakukan di Laboratorium Pusat Survei Geologi.
Waktu penelitian di mulai pada bulan Maret 2013 sampai dengan Januari 2014.
3.2 Alat-Alat Penelitian
Preparasi dan sintesis hidrogel CRF menggunakan beberapa alat sebagai
berikut: gelas kimia (50 mL, 100 mL, dan 250 mL), gelas ukur (10 mL dan 50
mL), labu ukur (100 mL dan 250 mL), kaca arloji, neraca analitik, botol semprot,
kertas saring, spatula, batang pengaduk, oven, plastik wraps, alumunium foil,
stopwatch, pipet tetes, blender. Instrumentasi yang digunakan untuk keperluan
karakterisasi adalah FTIR (Shimadzu), AAS (Verkin Kelmer), dan XRD (X’Pert
PRO).
3.3 Bahan- Bahan Penelitian
Bahan yang digunakan adalah simplisia SDT, monomer akrilamida, N’-N
metilenbis akrilamida (MBA), kalium persulfat (KPS), sodium metabisulfit
21
3.4 Prosedur Penelitian
Tumbuhan SDT AAm MBA KPS
- Dicuci - Dikeringkan - Diblender
SDT
-Ditimbang -Dilarutkan dalam
larutan HCl 5% -Diaduk -Didiamkan -Disaring -Ditimbang -Ditambahkan aquades sebanyak 40mL Larutan AAm -Ditimbang -Ditambahkan aquades sebanyak 40mL Larutan MBA -Ditimbang -Ditambahkan aquades sebanyak40mL Larutan KPS SMBS -Ditimbang -Ditambahkan aquades sebanyak 40mL mL Larutan SMBS -Ditimbang
-Dilarutkan dalam larutan NaOH 10-4M
-Diaduk -Didiamkan -Disaring
-Ditimbang -Dilarutkan dalam
aquades -Diaduk -Didiamkan -Disaring
Residu Residu Residu
Ekstrak SDT (ESDT A) Ekstrak SDT (ESDT B) Ekstrak SDT (ESDT C)
- Ditambahkan larutan
akrilamida, , KPS, SMBS, dan MBA dengan perbandingan volume masing-masing (1:0,5:0,5:0,5)
- Diaduk sampai homogen pada suhu 50oC
Hidrogel
ESDT-X
Tahap optimasi pelarut
Tahap Preparasi
Zn(NO3)2
22
-Diambil sebanyak 10 mL
- Ditambahkan larutan akrilamida 10 mL, KPS 5 mL, dan SMBS 5 mL - Diaduk sampai
homogen pada suhu 50oC
Campuran ESDT-AAm (1) Campuran ESDT-AAm (2) Campuran ESDT-AAm (3) ESDT-X ESDT 1
-Diambil sebanyak 10 mL
- Ditambahkan larutan akrilamida 10, KPS 5 mL, dan SMBS 5 mL Diaduk sampai homogen pada suhu 50oC
-Diambil sebanyak 10 mL
- Ditambahkan larutan akrilamida 10 mL, KPS 5 mL, dan SMBS 5 mL Diaduk sampai homogen pada suhu 50oC
-Ditambahkan larutan MBA sebanyak 5 mL
-Diaduk sampai homogen pada suhu 50oC selama 12 menit
-Didiamkan di atas hot plate pada suhu 50oC selama 2 menit -Didiamkan pada suhu
ruang selama 15 menit -Dioven pada suhu 58oC
selama 24 jam -Dicuci dengan aquades -Dioven pada suhu 58oC
selama 20 jam
-Ditambahkan larutan MBA sebanyak 5 mL
-Diaduk sampai homogen pada suhu 50oC selama 12 menit
-Didiamkan di atas hot plate pada suhu 50oC selama 2 menit -Didiamkan pada suhu
ruang selama 15 menit -Dioven pada suhu 58oC
selama 24 jam -Dicuci dengan aquades -Dioven pada suhu 58oC
selama 20 jam
-Ditambahkan larutan MBA sebanyak 5 mL
-Diaduk sampai homogen pada suhu 50oC selama 12 menit
-Didiamkan di atas hot plate pada suhu 50oC selama 2 menit -Didiamkan pada suhu
ruang selama 15 menit -Dioven pada suhu 58oC
selama 24 jam -Dicuci dengan aquades -Dioven pada suhu 58oC
selama 20 jam
Hidrogel 1 Hidrogel 2 Hidrogel 3
Variasi waktu maserasi
0 hari (30 menit)
ESDT 2 ESDT 3
23
Hidrogel 1 Hidrogel 2 Hidrogel 3
FTIR Swelling Ratio Water Retention
Analisis Data
Hidrogel
-Disisipkan larutan nutrien Zn(NO3)2 0,25
Msebanyak 2,5 mL
Hidrogel-Nutrien
FTIR Swelling Ratio Water Retention Release Behavior
Analisis data
Kesimpulan
uji instrumentasi uji kinerja
Tahap penyisipan nutrient dan karakterisasi
XRD
di karakterisasi di karakterisasi
uji kinerja uji instrumentasi
Gambar 3.1 Diagram Alir Penelitian
Tahap sintesis dan optimasi waktu ekstraksi
24
3.4.1 Tahap Preparasi
3.4.1.1. Pembuatan Larutan Asam Klorida 5%
Larutan asam klorida 37% dipipet sebanyak 33,8 mL, kemudian
dimasukan ke dalam labu ukur 250 mL, lalu ditambahkan aquades sampai volume
250 mL dan dihomogenkan.
3.4.1.2. Pembuatan Larutan NaOH 10-4 M
NaOH ditimbang sebanyak 0,0004 gram, kemudian dimasukkan ke
dalam labu ukur 1000 mL, lalu ditambahkan aquades sampai volume 1000 mL
dan dihomogenkan.
3.4.1.3. Pembuatan Larutan Akrilamida 1,4 M
Akrilamida ditimbang sebanyak 4,002 gram, kemudian dimasukkan ke
dalam gelas kimia 100 mL, lalu ditambahkan aquades sebanyak 40 mL dan
dihomogenkan.
3.4.1.4. Pembuatan Larutan MBA 0,13 M
MBA ditimbang sebanyak 0,8002 gram, kemudian dimasukkan ke dalam
gelas kimia 100 mL, lalu ditambahkan aquades sebanyak 40 mL dan
dihomogenkan.
3.4.1.5. Pembuatan Larutan Kalium Persulfat (KPS) 1,4 M
KPS ditimbang sebanyak 2,013 gram, kemudian dimasukkan ke dalam
gelas kimia 50 mL, lalu ditambahkan aquades sebanyak 5 mL dan dihomogenkan.
3.4.1.6. Pembuatan Larutan Sodium Metabisulfit (SMBS) 0,07 M
SMBS ditimbang sebanyak 0,5604 gram, kemudian dimasukkan ke
dalam gelas kimia 100 mL, lalu ditambahkan aquades sebanyak 40 mL dan
25
3.4.1.7. Tahap Pembuatan Nutrien 0,25 M
Zink nitrat (Zn(NO3)2.4H2O) ditimbang sebanyak 6,5349 gram.
Kemudian dilarutkan ke dalam aquades 50 mL, dihomogenkan dan ditambahkan
kembali aquades hingga volume 100 mL.
3.4.1.8. Tahap Pembuatan Ektrak SDT
Simplisia SDT dikeringkan di udara terbuka selama 6 jam. Simplisia
yang telah kering kemudian dihaluskan menggunakan blender. Pembuatan ekstrak
SDT dilakukan dengan cara simplisia SDT yang telah dihaluskan, ditimbang
sebanyak 20 gram lalu dilarutkan ke dalam tiga jenis pelarut yang berbeda yaitu
larutan HCl 5%, larutan NaOH 10-4 M, dan aquades masing-masing sebanyak 100
mL. Kemudian diaduk menggunakan batang pengaduk. Ekstrak yang didapat
kemudian disaring menggunakan corong kaca dan kertas saring, filtrat SDT
dengan HCl 5%, NaOH 10-4 M , dan aquades secara berturut-turut dibebut ESDT
A, ESDT B, dan ESDT C. Selanjutnya ESDT digunakan dalam pembuatan
hidrogel. Ditambahkan AAm, KPS, SMBS, dan MBA kepada masing-masing
ESDT dengan perbandingan volume ESDT:AAm:KPS:SMBS:MBA
(1:1:0,5:0,5:0,5). Dari hasil sintesis akan didapat ESDT optimal (ESDT-X) yang
ditunjukkan dengan terbentuknya hidrogel.
3.4.2 Tahap Sintesis
3.4.2.1. Optimasi Waktu Ekstraksi SDT
Ekstrak SDT hasil optimasi pelarut (ESDT-X) diambil dengan jumlah
yang sama pada tiap waktu ekstraksi (0, 1, dan 7 hari) dengan mencampurkan
pereaksi dalam jumlah yang sama (Tabel 3.1). Hidrogel yang terbentuk kemudian
di uji kinerja dan instrumentasi. Uji kinerja hidrogel meliputi swelling ratio dan
water retention, sedangkan uji instrumentasi dengan analisis FTIR. Dari hasil uji
akan didapatkan waktu optimum ekstraksi SDT yang ditunjukkan dengan hasil uji
26
Tabel 3.1 Optimasi waktu ekstraksi SDT
3.4.2.2. Sintesis Hidrogel
Campurkan larutan ekstrak SDT kondisi optimal, akrilamida, larutan
KPS dan SMBS dalam gelas kimia 250 mL, kemudian diaduk selagi dipanaskan
pada suhu 50oC. Kemudian ditambahkan larutan MBA. Diaduk selagi dipanaskan
kembali dengan suhu yang sama selama 12 menit hingga homogen. Hidrogel yang
terbentuk dikeringkan dengan menggunakan oven selama 24 jam pada suhu
58oC. Kemudian hidrogel dicuci menggunakan aquades dan dikeringkan kembali
menggunakan oven selama 20 jam pada suhu 58oC.
3.4.3 Sintesis Hidrogel CRF (Controlled Release Fertilizer)
3.4.3.1 Penyisispan Nutrien ke dalam Hidrogel
Hidrogel hasil sintesis dalam kondisi optimum disisipkan nutrisi yang
dalam bentuk larutan nutrien. Metode yang digunakan yaitu larutan nutrien
disisipkan ke dalam hidrogel pada saat proses sintesis. Adapun mikronutrien yang
disisipkan yaitu Zink Nitrat 0,25 M. Selanjutnya hidrogel yang ditambahkan
nutrien akan di karakterisasi dan serta di uji kinerjanya melalui pengukuran FTIR,
XRD, uji swelling ratio, water retention, dan release behavior.
3.4.3.2 Tahap Karakterisasi Struktur Morfologi Hidrogel
3.4.3.2.1 Fourier Transform Infrared (FTIR) Spectroscopy
Karakterisasi FTIR ini dilakukan untuk mengetahui interaksi kimia
(gugus fungsi) dalam pembentukan hidrogel. Spesifikasi alat FTIR yang
digunakan adalah SHIMADZU FTIR-8400, jenis sampel yang dikarakterisasi Waktu
ekstraksi SDT (hari)
ESDT Akrilamida MBA KPS SMBS
0 10 mL 10 mL 5 mL 5 mL 5 mL
1 10 mL 10 mL 5 mL 5 mL 5 mL
27
dengan FTIR yaitu SDT, Akrilamida, MBA, hidrogel dengan kondisi waktu
optimasi berbeda (0, 1, dan 7 hari). Sampel dihaluskan kemudian dipadatkan
bentuk pelet KBr. Sampel KBr kemudian dianalisa dengan FTIR spectrometer.
Spektrum direkam dalam daerah bilangan gelombang dari 4000 cm-1 sampai 600
cm-1. Spektrum yang diperoleh kemudian dibandingkan satu sama lain untuk
melihat interaksi kimia dan meramalkan mekanisme reaksi yang terjadi dalam
pembentukan hidrogel.
3.4.3.2.2 X-Ray Difraction (XRD) (Cu ke α) (X-Pert PRO)
Pengujian XRD ditujukan untuk menentukan kristalinitas hidrogel
digunakan instrumentasi XRD dimana energi yang digunakan adalah
50kV/300mA dan sumber radiasi (Cu ke α). Sebelum pengukuran, hidrogel
terlebih dahulu dikeringkan dan kemudian dihaluskan. Setelah itu, sampel
hidrogel ditempatkan pada sampel holder kemudian dianalisa XRD dan diperoleh
difraktogram dari sampel. Jarak inter layer dan kristalinitas sampel dapat
ditentukan dengan menganalisa menggunakan persamaan Bragg dan Scherrer.
Persamaan Bragg dapat menentukan jarak inter layer, sehinga dengan
menggunakan persamaan Scherrer dapat menentukan nilai kristalinitas.
Persamaan Bragg:
n λ = 2 d sin θ………(3.1)
Dimana d adalah jarak inter layer, λ adalah panjang gelombang, n adalah orde
difraksi, dan θ adalah sudut difraksi.
Persamaan Scherrer:
………(3.2)
Dimana L adalah nilai kristalinitas, K adalah faktor bentuk dari kristal/tetapan
28
3.4.3.3 Uji Kinerja Hidrogel
3.4.3.3.1 Swelling Ratio
Untuk mempelajari swelling hidrogel, digunakan metode swelling ratio
dari sampel hidrogel dapat ditentukan melalui gravimetri. Swelling rasio
diperlukan untuk mengetahui tingkat elastisitas hidrogel. Hidrogel kering
ditimbang (Wd) lalu direndam dalam 25 mL aquades dalam gelas kimia 100 mL.
Setelah beberapa saat, hidrogel diangkat dan permukaannya dikeringkan dengan
menggunakan kertas hisap. Hidrogel kemudian ditimbang kembali berdasarkan
rentang waktu yang telah ditentukan (tiap 2 menit selama 10 menit, kemudian 5
menit selama 50 menit, 10 menit selama 30 menit, 30 menit selama 180 menit dan
setiap satu hari selama 3 hari) setelah waktu pengangkatan hidrogel (Ws). Swelling
Rasio pada hidrogel dipelajari dengan menggunakan persamaan 2.1.
3.4.3.3.2 Water Retention (Retensi Air)
Faktor water retention dalam hidrogel berfungsi untuk mempertahankan
kelembaban dan kandungan nutrisi dalam tanah pertanian. Untuk mempelajari
water retention tanah yang mengandung hidrogel, sampel hidrogel kering dibenamkan di dalam 40 g tanah kering yang ditempatkan dalam cangkir (A).
Sejumlah 40 g tanah kering lain tanpa hidrogel ditempatkan dalam cangkir (B),
kemudian setiap cangkir ditimbang (W). Setelah itu, air suling sebanyak 25mL
ditambahkan ke dalam kedua cangkir dan ditimbang kembali (Wo). Cangkir
tersebut disimpan pada kondisi suhu kamar yang sama dan ditimbang setiap hari
(Wt) sampai berat tanah kembali seperti sebelum ditambahkan air suling. Water
retention (%WR) dari hidrogel kemudian dihitung dengan Persamaan 2.2.
3.4.3.3.3 Release Behavior
Profil release nutrien dalam hidrogel dapat ditentukan dari pengukuran
absorpsi dan desorpsi nutrien pada dan dari hidrogel dengan menggunakan
bantuan instrumentasi AAS (Atomic Absorption Spectroscopy). Pengukuran
dengan AAS untuk mengetahui perubahan konsentrasi pada hidrogel sebelum dan
setelah pelepasan nutrisi dengan cara mengukur larutan standar terlebih dahulu
29
(sumbu Y) dan konsentrasi (sumbu X). Kurva standar ini digunakan untuk
menentukan konsentrasi sampel yang terukur dengan cara hidrogel kering
direndam ke dalam larutan nutrien zink nitrat dengan konsentrasi 1, 2, 3, 4, dan 5
ppm selama 1 jam kemudian hidrogel yang telah dicoating nutrien dibenamkan ke
dalam 50 mL aquades selama 1 jam. Konsentrasi nutrien yang terdesorbsi dari
hidrogel ditentukan dengan mengukur konsentrasi dengan metode AAS pada
panjang gelombang 766.5 nm, energi 64 %, dan intensitas waktu 0,7 detik.
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan hasil penelitian yang telah dilakukan didapatkan beberapa
kesimpulan sebagai berikut :
1. Hidrogel CRF bernutrien dapat disintesis dari bahan dasar AAm dan
crosslinker MBA dengan penambahan ekstrak SDT dan larutan nutrien
Zn(NO3)2.
2. Hidrogel CRF bernutrien memiliki kristalinitas yang tinggi, gugus fungsi
dominan adalah –OH/-NH, C=O, C-O, dan –NO, dengan interaksi ESDT dan
AAm terjadi pada gugus -OH/-NH.
3. Hidrogel CRF bernutrien memiliki kapasitas %SR sebesar 60,63%, dan
%WR sebesar 9,62%.
4. Release behavior tergantung pada jumlah nutrien yang terabsorpsi pada
hidrogel, dengan nilai optimum yang terjadi pada penyisipan nutrien 4,987
ppm per 0,3313 gram hidrogel.
5.2 Saran
Dari penelitian yang telah dilakukan terdapat beberapa kekurangan yang
dapat diperbaiki dalam penelitian selanjutnya, diantaranya :
1. Sebaiknya digunakan larutan buffer pada saat proses maserasi agar pH tidak
berubah ketika perendaman serbuk simplisia SDT dengan waktu yang lama.
2. Dilakukan variasi jumlah SDT yang digunakan ketika proses sintesis untuk
mengetahui jumlah optimum SDT yang digunakan.
3. Dilakukan pengambilan instrumen SEM untuk mengetahui ukuran pori pada
hidrogel.
4. Dilakukan penelitian fundamental pada penelitian yang sudah di uji dengan
DAFTAR PUSTAKA
Anah, L., Astrini, N., Suharto, Nurhikmah, A. & Haryono, A. (2010). “Studi Awal Sintesa Carboxy Methyl Cellulose-Graft-Poly(Acrylic Acid)/Monmorilonit Superabsorben Polimer Hidrogel Komposit Melalui Proses Kopolimerisasi
Cangkok”. Berita Selulosa. 45, (1), 1-8.
Anonim. (2013). Pedoman Penulisan Karya Tulis Ilmiah. UPI.
Bachtiar, A. F, Tjahjaningsih, W., & Sianita, N. (2012). “Effect of Algae Brown (Sargassum sp.) Extract Against Bacterial Growth of Escherichia coli.
Journal of Marine and Science. 1, (1), 53-60.
Buyanov, A. L., Gofman, I. V., Revel’skaya, L. G., Khripunov, A.K., & Tkachenko, A. A. (2009). “Anisotropic Swelling And Mechanical Behavior of Composite Bacterial Cellulose–Poly(Acrylamide or Acrylamide–Sodium Acrylate) Hydrogels”. Journal of The Mechanical Behavior of Biomedical Materials. 102-111.
Chapman, R.J.& Hall .(1987).Introduction to Polymers. ISBN 0-412-22170-5.
Cho, E.C., Kim, J., Fernandez-Nieves, A. & Weitz, D.A. (2008). “Highly Responsive Hydrogel Scaffolds Formed by Three-Dimensional Organization
of Microgel Nanoparticles”. Nano Letters. 8, (1), 168-172.
Chotimah, N. (2013). Sintesis, Karakterisasi, dan Uji Kinerja Biohidrogel
Berbahan Dasar EGN-PVA dengan Crosslinker Glutaraldehida. Skripsi
Sarjana pada FPMIPA Universitas Pendidikan Indonesia Bandung: tidak diterbitkan.
Departemen Kesehatan RI. (1979). Farmakope Indonesia Edisi III. Jakarta.
D’Souza, L., Devi, P., Shridhar, D. & Naik, C.G. (2008). “Use of Fourier Transform Infrared (FTIR) Spectroscopy to Study Cadmium-Induced Change
in Padina Tetrastromatica (Hauck)”. Analytical Chemistry Insight. 3,
135-143.
Erizal. (2010). “Synthesis and Characterization of Crosslinked Polyacrilamide (PAAM)-Carrageenan Hydrogel Superabsorbent Prepared by Gamma
Radiation”. Indo. J. Chem. 10, (1), 12-19.
Erizal, Tita P., & Dewi S.P. (2007). “Sintesis Hidrogel Poliakrilamida (PAAM) -Ko-Alginat dengan Iradiasi Sinar Gamma dan Karakterisasinya”. Jurnal Sains Materi Indonesia. 13-20.
49
Flory, P.J. (1969). Principles of Polymer Chemistry. Seventh Edition. Ithaca :
Cornell University Press.
Ganji, F. G. & Vasheghani-Farahani, E. (2009). “Hydrogel in Controlled Drug
Delivery System”. Iranian Polymer Journal. 18, (1), 63-88.
Handayani, P.A. (2010). “Polimerisasi Akrilamid dengan Metode Mixedsolvent Precipitation dalam Pelarut Etanol-Air”. 8, (1).
Jones, C., & Jacobsen, J. (2001). Plant Nutrition and Soil Fertility. Dalam
Nutrient Management [online], Vol 2, (1), 11 halaman. Tersedia
http://landresources.montana.edu/nm/modules/mt44492.pdf [18 November 2013]
Juliana, V. (2010). Isolasi dan Karakterisasi Senyawa Turunan Terpenoid dari
Fraksi N-Heksan Momordica charantia L. Skripsi Program Studi Kimia
Jurusan Pendidikan Kimia UPI Bandung : tidak diterbitkan.
Kirk, G.W., & Othmer, D.F. (1978). Encyclopedia of chemical Technology. Third
Edition. vol 1. pp 298 – 311. 312 – 330. New York: John Wiley and Sons.
Mashuri, Sujud, A., & Karo, A. (2001). “Studi Sinergi Crosslink Agent dan Coupling Agent Terhadap Peningkatan Kinerja Sifat Mekanik Komposit
Polietilena Massa Jenis Tinggi (HDPE)-Tembaga (Cu)”. Jurnal Sains Materi Indonesia. 2, (2), 7-11.
Muthoharoh, S. P. (2012). Sintesis Polimer Superabsorben dari Hidrogel Kitosan
Terikat Silang. Skripsi Sarjana pada FMIPA Universitas Indonesia Depok:
tidak diterbitkan
Nurkomarasari, R. (2012). Pengaruh Crosslinker N,N’-Metilenbisakrilamida (MBA)Terhadap Kinerja Kopolimer Superabsorbent Selulosa Bakterial Nata De Soya-Asam Akrilat Yang Disintesis Menggunakan Radiasi Microwave.
Skripsi Sarjana pada FPMIPA Universitas Pendidikan Indonesia Bandung: tidak diterbitkan.
Odian, G. (1970). Principle of Polymerization. New York : Mc. Graw Hill Book
Company.
Purnawijaya, Y. (2013). Preparasi Uji Swelling Ratio Hidrogel Berbahan Dasar
Polivinil Alcohol, Bioflokulan TAD, dan Kitosan. Skripsi Sarjana pada
FPMIPA Universitas Pendidikan Indonesia Bandung: tidak diterbitkan.
Putri, A.D. (2013). Sintesis, Karakterisasi, dan Uji Kinerja Biohidrogel Berbahan
Dasar DYT-PVA dengan Crosslinker Glutaraldialdehid. Skripsi Sarjana pada
FPMIPA Universitas Pendidikan Indonesia Bandung: tidak diterbitkan.
50
Rasyid, A. (2010). “Ekstraksi Natrium Alginat dari Alga Coklat”. Oseanologi dan Limnologi. 36, (3), 393-400.
SAKERNAS. (2006). Sumber Daya Alam Indonesia. Jakarta.
Sandler, S.R. & Karo, W. (1992). “Polymer Syntheses”. Academic Press. Inc.
1, 420–445.
Saputra, D.R., Ridlo, A., & Widowati, I. (2012). “Kajian Rumput Laut Sargassum duplicatum J. G. Agardh sebagai Penghasil Bioetanol dengan Proses Hidrolisis Asam dan Fermentasi”. Journal Of Marine Research.1, (2),
145-151.
Septiana, A. T. & Asnani, A. (2012). “Kajian Sifat Fisikokimia Ekstrak Rumput
Laut Coklat Sargassum Duplicatum Menggunakan Berbagai Pelarut dan
Metode Ekstraksi”. Agrointek. 6, (1).
Shaviv, A., & Mikkelsen, R.L. (1993). “Controlled-release fertilizers to increase
efficiency of nutrient use and minimize environmental degradation review”..
Fertilizer Research. 35, 1–12.
Syed K. H. Gulrez, Saphwan Al-Assaf & Glyn O Phillips (2011). Hydrogels:
Methods of Preparation, Characterisation and Applications, Progress in
Molecular and Environmental Bioengineering - From Analysis and Modeling
to Technology Applications, Prof. Angelo Carpi (Ed.), ISBN:
978-953-307-268-5, InTech, Available from:
http://www.intechopen.com/books/progress-
in-molecular-andenvironmental-bioengineering-from-analysis-and-modeling-to-technology56applications/hydrogels-methods-of-preparation
characterisation-andapplications.
Wang, W. & Wang, A. (2010). “Preparation, Swelling and Water-retention
Properties of Crosslinked Superabsorbent Hydrogels Based on Guar Gum”.
Advanced Materials Research . 96, 177-182.
Zohuriaan-Mehr, M. & Kabiri, K. (2008). “Superabsorbent Polymer Material: A