TUGAS MAKALAH
KIMIA FISIKA
KRISTAL
KELOMPOK: 4
KELAS : 3M
Disusun oleh :
FEBRITA RAMADHANI (1304015181) HIDAYATUS SOLIHAH (1304015223) IRVAN JAYA KELANA (1304015245) ISMAN NATAWIJAYA (1304015246) TRYAN AGUS PRIATNA (1304015524)
DOSEN PEMBIMBING
FAHJAR PRISISKA, M.Farm.,Apt
FAKULTAS FARMASI DAN SAINS
UNIVERSITAS MUHAMMADIYAH PROF DR HAMKA
JAKARTA
BAB I PENDAHULUAN A. LATAR BELAKANG
Fisika zat padat adalah ilmu yang mempelajari secara spesifik mengenai kristal dan elektron di dalam kristal. Pengetahuan tentang kristal mulai ditekuni pada awal abad ke 19 yang di ikuti dengan ditemukannya difraksi sinar-X. Dengan menggunakan difraksi X dan dilandasi oleh landasan teoritis yang memadai serta ditemukannya perhitungan yang sederhana dan perkiraan yang tepat dapat mempelajari struktur kristal.
Istilah "kristal" memiliki makna yang sudah ditentukan dalam ilmu material dan fisika zat padat, dalam kehidupan sehari-hari "kristal" merujuk pada benda padat yang menunjukkan bentukgeometri tertentu, dan kerap kali sedap di mata. Berbagai bentuk kristal tersebut dapat ditemukandi alam. Bentuk-bentuk kristal ini bergantung pada jenis ikatan molekuler antara atom-atom untukmenentukan strukturnya, dan juga keadaan terciptanya kristal tersebut. Bunga salju, intan, dangaram dapur adalah contoh-contoh kristal. Proses terbentuknya kristal secara sederhana bahwa dalam keadaaan cair, atom-atomtidak memiliki susunan yang teratur (selalu mudah bergerak) dan mempunyai temperature yangrelatip tinggi serta atom-atomnya memiliki energi yang cukup banyak sehingga mudah bergerakdan tidak ada pengaturan letak atom relatip terhadap atom lainnya.
B. TUJUAN
1. Mengetahui dan memahami apa itu padatan kristal dan padatan amorf 2. Mengetahui dan memahami klasifikasi kristal
BAB II
TINJAUAN PUSTAKA
Kristal adalah suatu padatan yang atom, molekul, atau ion penyusunnya terkemas secara teratur dan polanya berulang melebar secara tiga dimensi. Secara umum, zat cair membentuk kristal ketika mengalami proses pemadatan. Pada kondisi ideal, hasilnya bisa berupa kristal tunggal, yang semua atom-atom dalam padatannya “terpasang” pada kisi atau struktur kristal yang sama, tapi, secara umum, kebanyakan kristal terbentuk secara simultan sehingga menghasilkan padatan polikristalin. Misalnya, kebanyakan logam yang kita temui sehari-hari merupakan polikristal. Struktur kristal mana yang akan terbentuk dari suatu cairan tergantung pada kimiacairannya sendiri, kondisi ketika terjadi pemadatan, dan tekanan ambien. Kristal terbentuk karena proses kristalisasi. Pengertian kristalisasi sendiri yaitu proses pembentukan kristal yang terjadi pada saat pembekuan, perubahan dari fasa cair ke fasa padat.Kristal dapat terbentuk dari proses pengendapan. Endapan adalah zat yang memisahkan diri sebagai suatu fase padat keluar dari larutan dan terbentuklah kristal. Ukuran kristal yang terbentuk selama pengendapan tergantung pada dua faktor penting, yaitu laju pembentukan inti dan laju pertumbuhan kristal. Laju pembentukan inti dapat dinyatakan dengan jumlah inti yang terbentuk dalam satuan waktu. Jika laju pembentukan inti tinggi, banyak sekali kristal yang akan terbentuk tetapi dengan ukuran yang kecil. Sedangkan jika laju pertumbuhan kristal tinggi, maka akan didapatkan kristal dengan ukuran yang tinggi (Vogel, 1979).
BAB III PEMBAHASAN
Padatan digolongkan dalam dua golongan, padatan kristalin yang partikel penyusunnya tersusun teratur, dan padatan amorf yang partikel penyusunnya tidak memiliki keteraturan yang sempurna. Studi bahan kristalin mempunyai sejarah yang jauh lebih panjang karena kristal lebih mudah dipelajari daripada bahan amorf. Awalnya teknik ini hanya dapat digunakan untuk struktur yang sangat sederhana seperi garam (NaCl). Terdapat berbagai cara untuk mengklasifikasikan padatan, yang meliputi berbagai bahan. Namun, klasifikasi yang paling sederhana adalah membaginya menjadi dua golongan: padatan kristalin yang partikelnya tersusun teratur dan padatan amorf yang keteraturannya kecil atau tidak ada sama sekali.
Kristal
Diklasifikasikan berdasarkan cara penyusunan partikelnya Kristal juga dapat diklasifikasikan dengan jenis partikel yang menyusunnya atau dengan interaksi yang menggabungkan partikelnya.
a. Kristal Logam
terjadi interaksi antara atom/ion dengan elektron bebas di sekitarnya sehingga dapat membuat logam mempertahankan strukturnya bila diberikan suatu gaya yang kuat.
b. Kristal Ionik
Kristal ionik semacam natrium khlorida (NaCl) dibentuk oleh gaya tarik antara ion bermuatan positif dan negatif. Kristal ionik biasanya memiliki titik leleh tinggi dan hantaran listrik yang rendah. Namun, dalam larutan atau dalam lelehannya, kristal ionik terdisosiasi menjadi ion-ion yang memiliki hantaran listrik. Biasanya diasumsikan bahwa terbentuk ikatan antara kation dan anion. Dalam kristal ion natrium khlorida, ion natrium dan khlorida diikat oleh ikatan ion. Berlawanan dengan ikatan kovalen, ikatan ion tidak memiliki arah khusus, dan akibatnya, ion natrium akan berinteraksi dengan semua ion khlorida dalam kristal, walaupun intensitas interaksi beragam. Demikian juga, ion khlorida akan berinteraksi dengan semua ion natrium dalam kristal. Susunan ion dalam kristal ion yang paling stabil adalah susunan dengan jumlah kontak antara partikel bermuatan berlawanan terbesar, atau dengan kata lain, bilangan koordinasinya terbesar. Namun, ukuran kation berbeda dengan ukuran anion, dan akibatnya, ada kecenderungan anion yang lebih besar akan tersusun terjejal, dan kation yang lebih kecil akan berada di celah antar anion.
c. Kristal Molekular
d. Kristal Kovalen
Banyak kristal memiliki struktur mirip molekul-raksasa atau mirip polimer. Dalam kristal seperti ini semua atom penyusunnya (tidak harus satu jenis) secara berulang saling terikat dengan ikatan kovelen sedemikian sehingga gugusan yang dihasilkan nampak dengan mata telanjang. Intan adalah contoh khas jenis kristal seperti ini, dan kekerasannya berasal dari jaringan kuat yang terbentuk oleh ikatan kovalen orbital atom karbon hibrida sp3.
e. Kristal Cair
Kristal memiliki titik leleh yang tetap, dengan kata lain, kristal akan mempertahankan temperatur dari awal hingga akhir proses pelelehan. Sebaliknya, titik leleh zat amorf berada di nilai temperatur yang lebar, dan temperatur selama proses pelelehan akan bervariasi. Terdapat beberapa padatan yang berubah menjadi fasa cairan buram pada temperatur tetap tertentu yang disebut temperatur transisi sebelum zat tersebut akhirnya meleleh. Fasa cair ini memiliki sifat khas cairan seperti fluiditas dan tegangan permukaan. Namun, dalam fasa cair, molekul-molekul pada derajat tertentu mempertahankan susunan teratur dan sifat optik cairan ini agak dekat dengan sifat optik kristal. Material seperti ini disebut dengan kristal cair. Molekul yang dapat menjadi kristal cair memiliki fitur struktur umum, yakni molekul-molekul ini memiliki satuan struktural planar semacam cincin benzen.
Bahan Kristalin
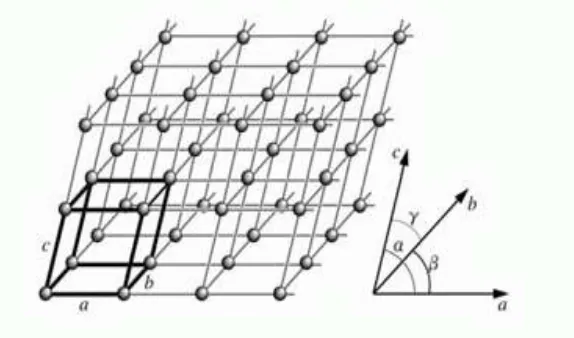
Gambar 8.1Definisi sel satuan.
Sel satuan digambarkan dengan garis tebal. Jarak antar dua titik sepanjang ketigasumbu didefiniskan sebagai a, b dan c. Sudut yang dibuat antar dua sumbu
didefinisikan sebagai α, β dan γ.
Kristalografi adalah studi ilmiah kristal dan pembentukannya.Kristal tunggal juga disebut sebagai monokristalin, yaitu suatu padatan kristal yang mempunyai kisi kristal yang susunannya teratur secara kontinyu dan kisi-kisi kristal yang membentuk bingkai tersebut tidak rusak atau tetap struktur-nya (Liu Z. and Stavrinadis, A, 2008). Menurut Milligan (1979), kristal tunggal adalah suatu padatan yang atom-atom dalam molekul-molekulnya diatur dalam keterulangan dimana sebagian padatan kristal tersusun dari jutaan kristal tunggal yang disebut grain.
Dalam proses pembentukan struktur kristal tersebut, dalam ilmu kristalografi dijelaskan dengan dua jalan yaitu hcp (hexagonal close-packed) dimana kristal terbentuk dengan urutan atom ABABAB dan seterusnya serta urutan pembentukan kristal lainnya adalah ccp (cubic close-packed) dimana urutan atom pembentuknya adalah ABCABC dan seterusnya (Hammond, 2009).
kristalnya terdapat tujuh yang ditampilkan pada tabel 1. Keempatbelas kisi tersebut memiliki perbedaan dalam bentuk dan ukuran unit sel. Perbedaan tersebut dilambangkan dengan huruf a, b, c dan sudut diantara huruf tersebut dilambangkan dengan α, β, γ, dimana α adalah sudut diantara b dan c, β adalah sudut diantara a dan c, dan γ adalah sudut diantara a dan b (Hammond, 2009).
Tabel 1. Sistem Kristal
Suatu senyawa kristal dapat mengandung pelarut kristalisasi dalam jumlah stoikiometris. Pelarut kristalisasi nonstoikiomertis misalnya inklusi dan clathrates, melibatkan molejul-molekul pelarut yang terjerat dalam kisi kristal. Pelarut kristal yang terkandung dalam jumlah stoikiometris dalam kristal disebut solvat, suatu kompels molekular yang telah bergabung dengan molekul-molekul pelarut yang mengkristalisasi ke dalam tempat-tempat spesifik dalam ksi kristal tersebut.
Padatan Amorf
Fitur padatan amorf dapat dianggap intermediate antara padatan dan cairan. Baru-baru ini perhatian telah difokuskan pada bahan buatan seperti fiber optik dan silikon amorf (tabel 8.1)
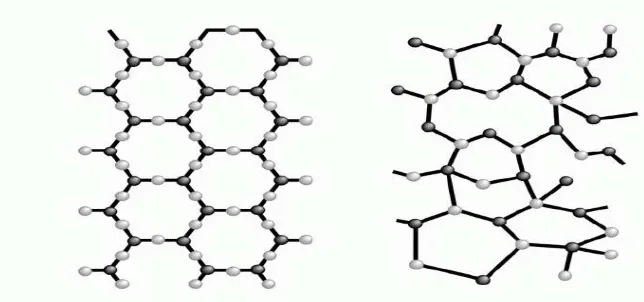
Gambar 8.3 Padatan kristalin dan amorf
Terdapat perbedaan besar dalam keteraturan partikel penyusunnya.
Beberapa ilmuwan bertahan dengan pendapat bahwa padatan amorf dapat dianggap wujud keempat materi.
Contoh padatan amorf fungsional
Amorf Penggunaan material
Gelas kuarsa Serat optik
Gelas khalkogenida Membran selenium untuk mesin fotokopi
Silikon amorf Sel surya
Polimer Polistirene
Karbon amorf karbon hitam (adsorben)
Silika gel gel (adsorben)
Padatan amorf mempunyai atom-atom molekul yang tersusun dalam keadaan tidak teratur seperti dalam wujud cairan. Bentuk amorf biasanya mempunyai energi termodinamis yang lebih tinggi daripada kristal, sehingga kelarutan dan laju disolusinya lebih besar, dan dapat dianggap sebagai cairan yang membeku terlambat dengan viskositas yang besar. Berbeda dengan kristal, sebab bentuk amorf cenderung mengalir jika diberikan tekanan cukup selama beberapa waktu dan tidak mempunyai titik lebur tertentu, titik lebur berupa suatu interval temperatur.
ATOMIC PACKING FACTORS (APF)
Bidang kristal adalah bidang-bidang atom dalam suatu kisi kristal. Arah ^ (tegak lurus) bidang kristal disebut sebagai arah kristal.
Suatu kristal tentunya memiliki bidang-bidang atom yang mempenga-ruhi sifat dan perilaku bahan. Baik bidang, maupun arah bidang dinyatakan dalam 3 angka yang disebut sebagai indeks miller .
Bidang kisi yang paling mudah digambarkan adalah bidang-bidang yang membatasi sel satuan di samping bidang lainnya. h, k, l, tersebut adalah bilang-bilangan bulat seperti 0, 1, 2, 3, dan seterusnya yang dapat ditentukan dengan cara sebagai berikut :
1. Tentukan panjang perpotongan bidang kristal terhadap ketiga sumbu kristal misalnya x1, y1 , z1. x1, y1 dan z1 dinyatakan dalam kelipatan
besaran- besaran sel satuan a, b, dan c. Contoh : x1 = p1 a y1 = p2 b z1 = p3 c.
2. Ketiga nilai p1 , p2 dan p3 dapat dikalikan/dibagi dengan faktor yang
Coordination numbers atau diterjemahkan sebagai bilangan koordinasi (BK) adalah suatu bilangan yang menunjukkan berapa jumlah atom-atom tetangga terdekat (atom-atom yang bersentuhan).
1. Kovalensi .
Jumlah ikatan kovalen di sekitar suatu atom tergantung pada jumlah elektron valensinya
Contoh :
Kebalikannya : 1,1/2, dan 3/2
Indeks Miller h, k, l dapat dikalikan Receprocal dengan bilangan yang memberikan bilangan bulat terkecil yaitu dengan 2. Sehingga bidangnya menjadi 213 ; Jadi bilangan tersebut (2, 1, 3)
BAB IV PENUTUP Kesimpulan
Padatan digolongkan dalam dua golongan, padatan kristalin yang partikel penyusunnya tersusun teratur, dan padatan amorf yang partikel penyusunnya tidak
memiliki keteraturan yang sempurna.Kristal di
DAFTAR PUSTAKA
Sinko, Patrick.J. Farmasi fisika dan ilmu Farmasetika Martin. Alih bahasa, Joshita Djajadisastra, Amalia H. Hadinata. Jakarta : EGC, 2011( diakses pada tanggal 13 september 2014)
http://www.chem-is-try.org/materi_kimia/kimia_dasar/padatan1/padatan-kristalin-dan-amorf
( diakses pada tanggal 13 september 2014)
http://id.wikipedia.org/wiki/Kristal ( diakses pada tanggal 13 september 2014)