BAB II
TINJAUAN PUSTAKA
II.1. STROKE PERDARAHAN INTRASEREBRAL II.1.1. Definisi
Stroke adalah suatu episode dari disfungsi neurologis yang
disebabkan oleh iskemia atau hemoragik, berlangsung selama > 24 jam
atau meninggal, tetapi tidak memiliki bukti yang cukup untuk
diklasifikasikan (Sacco dkk, 2013).
Stroke perdarahan intraserebral adalah tanda klinik disfungsi
neurologis yang berkembang cepat akibat perdarahan dalam parenkim
otak yang tidak disebabkan oleh trauma (Sacco dkk, 2013).
II.1.2. Epidemiologi
Insiden stroke bervariasi di berbagai negara di Eropa, diperkirakan
terdapat 100 – 200 kasus stroke baru per 10.000 penduduk per tahun
(Hacke dkk, 2003). Di Amerika diperkirakan terdapat lebih dari 700.000
insiden stroke per tahun, yang menyebabkan lebih dari 160.000 kematian
per tahun, dengan 4,8 juta penderita stroke yang bertahan hidup
(Goldstein dkk, 2006).
Meskipun dapat mengenai semua usia, insiden stroke meningkat
dengan bertambahnya usia dan terjadi lebih banyak pada wanita usia
64 tahun adalah 1,25; pada umur 65 – 74 tahun adalah 1,50; 75 – 84
tahun adalah 1,07; dan pada umur >85 tahun adalah 0,76 (Lloyd dkk,
2009).
Dari survei ASNA di 28 RS seluruh Indonesia, diperoleh gambaran
bahwa penderita laki-laki lebih banyak dari pada perempuan dan profil
usia 45 tahun yaitu 11,8%, usia 45 – 64 tahun berjumlah 54,2% dan diatas
usia 65 tahun sekitar 33,5%. Data-data lain dari ASNA Stroke
Collaborative Study diperoleh angka kematian sebesar 24,5% (Misbach dkk, 2011).
Insiden stroke perdarahan intraserebral di belahan bumi Barat
selama era CT umumnya berkisar dari 10 sampai 30 kasus per 100.000
orang. Tingkat insiden perdarahan intraserebral lebih tinggi di Asia Timur,
di mana perdarahan intraserebral tersebut memiliki persentase yang lebih
besar dari semua stroke dibandingkan pada populasi Barat (Flaherty dkk,
2010).
Insiden perdarahan intraserebral menurun antara 1950-an dan
1980-an. Studi sebelumnya mendapatkan bahwa ada kecenderungan
penurunan kejadian perdarahan intraserebral di Oxfordshire, Inggris
antara tahun 1981 dan 2006. Kejadian perdarahan intraserebral juga
menurun selama tahun 1990-an di beberapa kota di Cina. Namun,
penurunan yang serupa belum terlihat dalam penelitian lain. Stabilisasi
setidaknya sebagian disebabkan oleh deteksi dan klasifikasi yang tepat
dari perdarahan kecil dengan neuroimaging modern (Flaherty dkk, 2010). Risiko perdarahan intraserebral tampaknya sedikit lebih besar pada
pria dibandingkan pada wanita. Di Amerika Serikat kulit hitam dan
Hispanik memiliki insidensi jauh lebih tinggi dibandingkan kulit putih. Di
antara orang kulit hitam dan Hispanik, risiko perdarahan intraserebral
paling sering pada orang muda dan setengah baya. Lokasi dominan
perdarahan intraserebral dalam otak juga bervariasi dalam populasi yang
berbeda. Di Amerika Serikat, Eropa, dan Australia, perdarahan yang
berasal dari periventrikular, nukleus kaudatus, kapsula interna, putamen,
globus pallidus, atau talamus adalah yang paling umum, diikuti oleh
perdarahan lobar pada gray matter atau white matter subkortikal. Sedangkan dalam sebuah studi berbasis populasi yang besar di Jepang,
perdarahan lobar hanya terjadi 15% dari keseluruhan perdarahan
intraserebral (Flaherty dkk, 2010).
II.1.3. Faktor Risiko
Faktor-faktor risiko untuk terjadinya stroke dapat diklasifikasikan
sebagai berikut : (Sjahrir, 2003)
1. Non modifiable risk factors
a. Usia
b. Jenis kelamin
2. Modifiable risk factors
a. Behavioral risk factors
1. Merokok
2. Unhealthy diet : lemak, garam berlebihan, asam urat, kolesterol, low fruit diet
3. Alkoholik
4. Obat-obatan : narkoba (kokain), antikoagulansia, anti platelet,
obat kontrasepsi
b. Physiological risk factors
1. Penyakit hipertensi
2. Penyakit jantung
3. Diabetes mellitus
4. Infeksi / lues, arthritis, traumatik, AIDS, lupus 5. Gangguan ginjal
6. Kegemukan (obesitas)
7. Polisitemia, viskositas darah meninggi dan penyakit perdarahan
8. Kelainan anatomi pembuluh darah
9. Dan lain-lain
II.1.4. Klasifikasi
Dikenal bermacam-macam klasifikasi stroke berdasarkan atas
patologi anatomi (lesi), stadium dan lokasi (sistem pembuluh darah)
I. Berdasarkan patologi anatomi dan penyebabnya :
1. Stroke iskemik
a. Transient Ischemic Attack (TIA) b. Trombosis serebri
c. Emboli serebri
2. Stroke hemoragik
a. Perdarahan intraserebral
b. Perdarahan subaraknoid
II. Berdasarkan stadium :
1. TIA
2. Stroke in evolution
3. Completed stroke
III. Berdasarkan lokasi (sistem pembuluh darah) :
1. Tipe karotis
2. Tipe vertebrobasiler
II.1.5. Patofisiologi
Perdarahan intrakranial meliputi perdarahan di parenkim otak dan
perdarahan subaraknoid. Insiden perdarahan intrakranial kurang lebih
20% adalah stroke hemoragik, dimana masing-masing 10% adalah
perdarahan subaraknoid dan perdarahan intraserebral (Caplan, 2000).
Perdarahan intraserebral biasanya timbul karena pecahnya
sering terjadi di daerah subkortikal, serebelum, dan batang otak.
Hipertensi kronik menyebabkan pembuluh arteriol berdiameter 100 – 400
mikrometer mengalami perubahan patologi pada dinding pembuluh darah
tersebut berupa lipohialinosis, nekrosis fibrinoid serta timbulnya aneurisma
tipe Bouchard. Pada kebanyakan penderita, peningkatan tekanan darah yang tiba-tiba menyebabkan rupturnya penetrating arteri yang kecil. Keluarnya darah dari pembuluh darah kecil membuat efek penekanan
pada arteriol dan pembuluh kapiler yang akhirnya membuat pembuluh ini
pecah juga. Hal ini mengakibatkan volume perdarahan semakin besar
(Caplan, 2000).
Elemen-elemen vasoaktif darah yang keluar serta kaskade iskemik
akibat menurunnya tekanan perfusi, menyebabkan neuron-neuron di
daerah yang terkena darah dan sekitarnya lebih tertekan lagi. Gejala
neurologik timbul karena ekstravasasi darah ke jaringan otak yang
menyebabkan nekrosis (Caplan, 2000).
Perdarahan intraserebral sekunder (sekitar 12 sampai 22% dari
seluruh kejadian perdarahan intraserebral) disebabkan oleh penyebab lain
selain pecahnya pembuluh darah kecil, misalnya, aneurisma, malformasi
arteri-vena, transformasi hemoragik stroke iskemik, dan neoplasma
II.1.6. Penanganan
Stroke perdarahan dikaitkan dengan tingkat kematian yang tinggi
dan morbiditas yang berat. Pengobatan pilihan masih kontroversial,
mengingat bahwa data dari beberapa uji klinis belum memberikan bukti
yang meyakinkan untuk mendukung efektivitas surgical clot removal. Oleh karena itu, penanganan dilakukan terutama terhadap edema serebri
sebagai target potensial untuk terapi intervensi pada penderita stroke
hemoragik (Thiex dkk, 2007).
Beberapa hal yang berperan besar untuk menjaga agar TIK tidak
meninggi pada stroke, antara lain (Misbach, 2011) :
1. Mengatur posisi kepala lebih tinggi 15 – 300
2. Mengusahakan tekanan darah yang optimal.
dengan tujuan
memperbaiki venous return.
Tekanan darah yang sangat tinggi dapat menyebabkan edema
serebral, sebaliknya tekanan darah terlalu rendah akan
mengakibatkan iskemia otak dan akhirnya juga akan menyebabkan
edema dan peninggian TIK.
3. Mengatasi kejang, menghilangkan rasa cemas, mengatasi rasa
nyeri dan menjaga suhu tubuh normal < 37,50
Kejang, gelisah, nyeri dan demam akan menyebabkan
ketidakseimbangan antara suplai dan kebutuhan akan substrat
metabolisme. Di satu sisi terjadi peningkatan metabolisme serebral,
terjadi kerusakan jaringan otak dan edema. Hal ini pada akhirnya
akan mengakibatkan peninggian TIK.
4. Koreksi kelainan metabolik dan elektrolit.
Hiponatremia akan menyebabkan penurunan osmolalitas plasma
sehingga akan terjadi edema sitotoksik sedangkan hipernatremia
akan menyebabkan lisisnya sel-sel neuron.
5. Mengatasi hipoksia.
Kekurangan oksigen akan menyebabkan terjadinya metabolisme
anaerob, sehingga akan terjadi metabolisme tidak lengkap yang
menghasilkan asam laktat sebagai sisa metabolisme. Peninggian
asam laktat di otak akan menyebabkan terjadinya asidosis laktat
dan selanjutnya menyebabkan edema otak dan peninggian TIK.
6. Menghindari beberapa hal yang menyebabkan peninggian tekanan
abdominal seperti batuk, mengedan dan penyedotan lendir
pernafasan yang berlebihan.
7. Pemberian larutan manitol 20 – 25% dengan dosis 0,75 – 1 mg /
kgBB bolus, diikuti 0,25 – 0,5 mg / kgBB setiap 3 – 5 jam
tergantung pada respon klinis. Komplikasi penggunaan manitol
adalah hipotensi, hipokalemia, gangguan fungsi ginjal karena
hiperosmolaritas, gangguan jantung kongestif dan hemolisis.
Terdapat beberapa pedoman untuk mengendalikan pembengkakan
sederhana, seperti obat penenang, ventilasi, dan posisi kepala yang
ditinggikan, gagal untuk mengontrol pembengkakan otak, perawatan
medis lebih lanjut dapat diterapkan, termasuk inotropik, salin hipertonik,
manitol, dan hipotermia. Perfusi otak dan tekanan intrakranial merupakan
target terapi dalam mencegah hipoperfusi otak yang berpotensi
mengancam nyawa. Pedoman baru-baru ini merekomendasikan target
tekanan intrakranial adalah kurang dari 25 mmHg dan CPP lebih besar
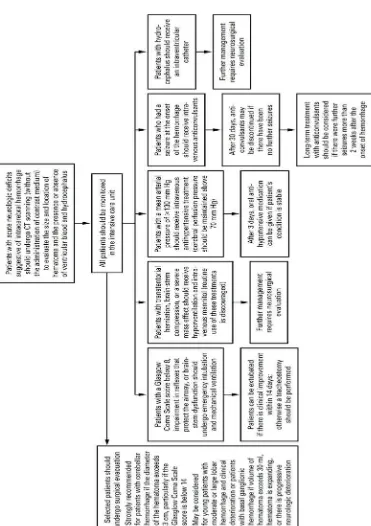
Gambar 1. Algoritma penanganan perdarahan intraserebral
Dikutip dari : Qureshi, A.I., Tuhrim, S., Broderick, J.P., Batjer, H.H., Hondo, H.,
Hanley, D.F. 2001. Spontaneous intracerebral hemorrhage. N Engl J Med.
II.1.7. Terapi Osmotik
Efek terapi osmotik terhadap TIK diduga dengan menyebabkan
penyusutan otak setelah pergeseran air keluar dari substansi otak.
Berbagai zat yang digunakan sebagai terapi osmotik, antara lain urea,
gliserol, sorbitol, manitol, dan salin hipertonik (White dkk, 2006).
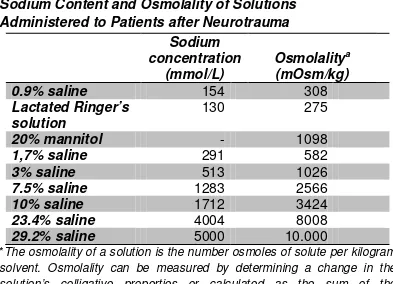
Sodium Content and Osmolality of Solutions
Administered to Patients after Neurotrauma
Sodium
*The osmolality of a solution is the number osmoles of solute per kilogram solvent. Osmolality can be measured by determining a change in the solution’s colligative properties or calculated as the sum of the concentration of the solutes present in the solution.
Tabel 1. Kandungan natrium dan osmolalitas cairan infus
Dikutip dari : White, H., Cook, D., Venkatesh, B. 2006. The use of hypertonic
Meskipun efektif, urea tidak lagi digunakan karena memiliki
berbagai efek samping termasuk mual, muntah, diare, hemoglobinuria,
koagulopati, dan rebound hipertensi intrakranial. Gliserol dan sorbitol dapat menurunkan TIK akan tetapi dapat menyebabkan hiperglikemia
yang signifikan. Manitol cukup efektif dan aman serta direkomendasikan
oleh Brain Trauma Foundation dan European Brain Injury Consortium
sebagai terapi osmotik pilihan (White dkk, 2006).
II.2. MANITOL II.2.1. Farmakologi
Manitol adalah polialkohol nonmetabolik C-6 dengan berat molekul
182, dan merupakan agen diuretik tertua serta paling banyak digunakan
sebagai osmotik. Selain menjadi agen hiperosmotik, manitol juga telah
terbukti sebagai scavenger efektif radikal hidroksil bebas dalam berbagai sistem biologis termasuk ekstraselular (Better dkk, 1997).
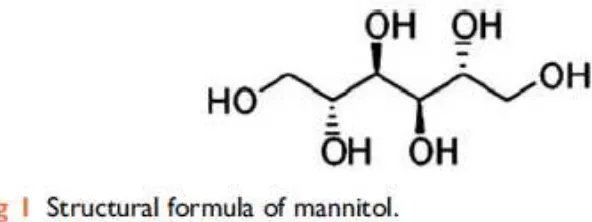
Gambar 2. Struktur manitol
Dikutip dari : Shawkat, H., Westwood, M., Mortimer, A. 2012. Mannitol : a review
Manitol memiliki struktur kimia 1,2,3,4,5,6-hexanehexol (C6H8 (OH)6) dan merupakan poliol (alkohol gula) yang banyak digunakan dalam
industri makanan dan farmasi. Manitol adalah zat alami yang ditemukan
dalam ganggang laut, jamur segar, dan dalam eksudat dari pohon. Serta
merupakan isomer dari sorbitol, yang biasanya disintesis oleh hidrogenasi
glukosa. Manitol juga tersedia secara komersial dalam berbagai bubuk
kristal putih dan bentuk granular, yang semuanya larut dalam air. Infus
manitol bersifat asam (pH 6.3) dan dapat mengkristal jika disimpan pada
suhu kamar, tetapi dapat dibuat larut lagi dengan pemanasan (Shawkat
dkk, 2012).
Manitol hipertonik intravena (iv) merupakan agen farmakologis
pertama yang digunakan untuk profilaksis terhadap GGA, diperkenalkan
oleh Homer Smith pada tahun 1940 untuk memperkirakan laju filtrasi
glomerulus (GFR) pada manusia dan anjing. Smith mencatat efek diuretik
osmotik manitol tersebut. Hal ini diikuti oleh Selkurt tahun 1945 yang
menunjukkan bahwa manitol memperbaiki GGA iskemik pada anjing.
Sejak saat itu, profilaksis manitol terhadap GGA pada manusia digunakan
secara luas tetapi tidak secara universal (Better dkk, 1997).
II.2.2. Farmakokinetik
Manitol harus diberikan secara parenteral karena pemberian secara
oral tidak diserap. Manitol didistribusikan hampir seluruhnya dalam cairan
hasilnya, hanya 7% hingga 10% yang dimetabolisme, mungkin di hati,
sedangkan sisanya secara bebas disaring oleh glomerulus dan
diekskresikan utuh dalam urin. Sekitar 7 persen diserap kembali oleh
tubulus ginjal. Dengan fungsi ginjal normal, setelah dosis tunggal manitol
intravena, half life manitol dalam sirkulasi plasma adalah sekitar 15 menit. Dari dosis yang diberikan, 90% ditemukan dalam urin setelah 24 jam.
Namun, pada insufisiensi ginjal yang berat maka tingkat ekskresi manitol
sangat berkurang sehingga manitol dalam tubuh dapat meningkatkan
tonisitas ekstraselular menyebabkan pergeseran air keluar dari sel,
memperbanyak cairan ekstraselular dan menyebabkan terjadinya
hiponatremia serta osmolalitas serum yang meningkat. Oleh karena itu,
manitol harus digunakan dengan hati-hati pada kondisi insufisiensi ginjal
(Nissenson dkk, 1979).
Karena berat molekulnya yang rendah (182), manitol secara bebas
disaring melalui tubulus ginjal. Namun, karena tidak diserap, terus menjadi
osmotik aktif dalam tubulus, hal inilah yang menyebabkan aksinya sebagai
diuretik osmotik. Manitol juga menyebabkan pelepasan prostaglandin
ginjal yang menyebabkan vasodilatasi ginjal dan peningkatan aliran urin
tubular yang dipercaya untuk melindungi terhadap cedera ginjal dengan
mengurangi obstruksi tubular. Hal ini juga bertindak sebagai scavenger
radikal bebas dan mengurangi efek berbahaya dari radikal bebas selama
II.2.3. Farmakodinamik
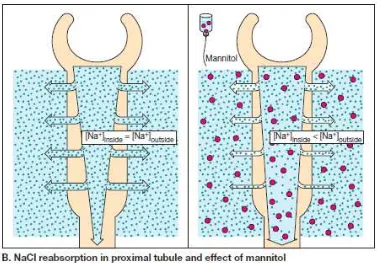
Diuretik osmotik terutama bekerja pada tubulus proksimal dan pars
desendens lengkung Henle. Melalui efek osmotik, diuretik juga
menghambat efek ADH pada collecting tubule. Manitol mencegah
penyerapan normal air dengan kekuatan osmotik, sehingga volume urin
meningkat. Peningkatan laju aliran urin mengurangi waktu kontak antara
cairan dan epitel tubular, sehingga mengurangi Na+ serta reabsorpsi air
(Tavakkoli, 2011).
Gambar 3. Efek manitol pada tubulus proksimal renal
Dikutip dari : Lullmann, H., Ziegler, A., Mohr, K., Bieger, D. 2000. Color atlas of
II.2.4. Dosis
Manitol biasanya diberikan dalam larutan 20% dalam dosis bolus,
dibandingkan sebagai infus kontinyu. Tekanan intrakranial akan menurun
dalam 5 – 10 menit. Efek maksimum terjadi dalam waktu sekitar 60 menit
dan total efek dapat berlangsung 3 – 4 jam. Pemberian bolus
meminimalkan hemokonsentrasi dan memperpanjang efek. Bolus 0,25 –
0,5 g / kg (diberikan selama 10 – 20 menit) dapat digunakan dan diulang
tergantung pada respon. Dosis 0,25 g / kg tampaknya seefektif dosis 1 g /
kg dalam mengurangi TIK tetapi tidak memiliki lama efek yang sama
(Reilly, 1997).
II.2.5. Efek Fisiologis
Selain penggunaannya dalam industri makanan dan farmasi,
manitol juga banyak digunakan dalam praktek medis untuk berbagai
indikasi (Tabel 2), terutama karena sifat osmotiknya. Untuk penggunaan
klinis, manitol diberikan sebagai cairan steril 10% dan 20% dalam 500 mL
Indikasi manitol
Menurunkan peningkatan tekanan intrakranial
Menjaga fungsi ginjal perioperasi pada pasien rencana operasi jantung
dan pasien jaundice
Diuresis dan mengurangi resiko gagal ginjal akut setelah transplantasi
ginjal
Menjaga fungsi ginjal pada rhabdomyolysis akibat trauma dan compartment syndrome
Persiapan kolon sebelum operasi kolorektal, kolonoskopi,dan
enema barium
Meningkatkan ekskresi zat toksik pada urin
Tabel 2. Kegunaan medis manitol
Dikutip dari : Shawkat, H., Westwood, M., Mortimer, A.2012. Mannitol : a review
of its clinical uses. Contin Educ Anaesth Crit Care Pain. 12:82-85.
II.2.5.1. Efek Penurunan TIK
Edema serebral terlibat dalam berbagai macam penyakit saraf
seperti iskemia otak, perdarahan otak, trauma otak dan tumor otak atau
abses otak. Edema serebral yang parah harus dikelola segera untuk
mencegah herniasi otak (Zeng dkk, 2010).
Osmoterapi telah digunakan sejak awal abad 20 untuk mengobati
TIK yang meningkat. Dasar fisiologis dan konsep osmoterapi pertama kali
diterbitkan pada 1919. Infus intravena manitol dianggap sebagai 'standar
emas' untuk penanganan TIK yang meningkat (Harutjunyan dkk, 2005).
Pemantauan terus menerus TIK menunjukkan bahwa edema otak
dapat menyebabkan peningkatan TIK, yang membutuhkan perawatan.
Kortikosteroid, meskipun sering digunakan untuk mengobati edema otak,
tidak meningkatkan kelangsungan hidup setelah stroke. Diuretik osmotik,
terutama manitol, adalah salah satu agen yang banyak digunakan dalam
penanganan edema serebral. Manitol diperkirakan menurunkan TIK
dengan cara mengurangi kadar air keseluruhan dan volume cairan
serebrospinal serta dengan mengurangi volume darah melalui
vasokonstriksi. Manitol juga dapat meningkatkan perfusi otak dengan
mengurangi viskositas (Bereczki dkk, 2000).
Situasi di mana penurunan tekanan intrakranial yang sangat cepat
diperlukan merupakan indikasi untuk terapi dengan agen osmotik seperti
manitol. Infus larutan hipertonik manitol dapat dengan cepat mengurangi
cairan otak dengan menciptakan gradien osmotik antara otak dan plasma.
Ketika manitol (1 g / kg) diberikan selama 10 sampai 15 menit (misalnya,
250 mL larutan 20% pada orang dewasa), penurunan tekanan intrakranial
dari 30 sampai 60% dapat diharapkan dalam 2 sampai 4 jam. Manitol
tampaknya meningkatkan sirkulasi dengan mengurangi tekanan
intrakranial serta dengan menciptakan efek langsung pada perfusi
serebral dalam mikrosirkulasi. Selain itu, manitol bertindak sebagai
scavenger radikal bebas. Karena manitol secara bertahap berdifusi dari kompartemen vaskular ke dalam sistem saraf pusat, tindakan ini dapat
II.2.5.2. Efek Proteksi Ginjal
Manitol telah digunakan sebagai agen pelindung ginjal pada
penderita berisiko tinggi terkena gagal ginjal, seperti yang menjalani
operasi jantung dan pembuluh darah, transplantasi ginjal, dan pada
penderita jaundice dan rhabdomyolysis. Namun, studi-studi
menunjukkan bahwa meskipun manitol meningkatkan output urin, hal tersebut tidak mengurangi risiko terjadinya GGA (Shawkat dkk, 2012).
II.2.5.3. Efek Pada Sirkulasi Darah
Manitol dapat menginduksi peningkatan cardiac output dan tekanan pengisian, serta peningkatan sementara tekanan arterial dan tekanan
perfusi serebral. Cardiac output dapat meningkat hingga 30% sehingga menyebabkan aliran darah otak juga meningkat. Beberapa studi
menunjukkan bahwa manitol sangat mempengaruhi resistensi vaskular
sistemik karena efek reologinya. Hal ini juga meningkatkan transportasi
oksigen sistemik maupun serebral (Castillo dkk, 2009).
II.2.5.4. Efek Mikrosirkulasi
Manitol merupakan scavenger radikal bebas dan memiliki efek mikrosirkulasi yang kuat dengan cara meningkatkan aliran darah kapiler.
Efek ini bersifat sementara dan berdasarkan kenaikan volaemia kapiler,
urea dan gliserol, yang tidak lagi digunakan secara klinis (Castillo dkk,
2009).
II.2.6. Efek Samping
Manitol memiliki banyak efek samping, antara lain ekspansi volume
awal (meningkatkan risiko gagal jantung), hipovolemia dan hipotensi,
asidosis metabolik, dan ketidakseimbangan elektrolit, termasuk
hipernatremia dan hipokalemia (Shawkat dkk, 2012).
Efek samping manitol
Gangguan keseimbangan cairan dan elektrolit Asidosis metabolik
Gagal jantung Kongesti paru Hipovolemia Hipotensi Tromboplebitis
Nekrosis kulit pada lokasi ekstravasasi Reaksi alergi, termasuk anafilaksis Peningkatan rebound TIK
Tabel 3. Efek samping manitol
Dikutip dari : Shawkat, H., Westwood, M., Mortimer, A. 2012. Mannitol : a review
of its clinical uses. Contin Educ Anaesth Crit Care Pain. 12:82-85.
Dalam dosis besar, juga dapat menyebabkan gagal ginjal karena
dapat mengakibatkan osmolalitas serum sangat tinggi (>320 mOsm / liter)
dan komplikasi neurologis berikutnya. Efek samping yang dapat terjadi
akibat pemberian manitol dapat dilihat dalam Tabel 3 (Shawkat dkk,
2012).
II.3. PENGARUH MANITOL TERHADAP FUNGSI GINJAL
Komplikasi yang paling umum dari terapi manitol adalah
ketidakseimbangan cairan dan elektrolit, edema kardiopulmoner, dan
rebound edema serebral. Manitol juga dapat menyebabkan gagal ginjal dalam dosis terapi, dan reaksi hipersensitivitas juga dapat terjadi.
Mekanisme patogenesa manitol terkait cedera ginjal akut melibatkan
dehidrasi, tubuloglomerular feedback, cedera osmotik dan vasokonstriksi (Bereczki dkk, 2000).
Penggunaan manitol di bawah dosis 200 g / hari jarang
menyebabkan terjadinya GGA. Pada dosis rendah manitol memberikan
efek vasodilator ginjal, sedangkan pada dosis tinggi menyebabkan
vasokonstriktor ginjal yang dapat mempengaruhi terjadinya GGA (Better
dkk, 1997). Gagal ginjal akut tersebut biasanya berupa oliguria dengan
ekskresi sodium fraksi rendah. Mekanisme terjadinya gagal ginjal diduga
karena efek tubuloglomerular feedback akibat keluarnya air dan garam setelah penggunaan dosis tinggi manitol (Schwartz, 1997). Selain itu,
diuresis manitol juga dapat meningkatkan penggunaan energi di ginjal
menyebabkan lebih mudahnya terjadi GGA. Akan tetapi, komplikasi
tersebut jarang terjadi dan umumnya terjadi akibat penggunaan dosis
tinggi manitol 400 hingga 900 g / hari (Better dkk, 1997).
Nefrotoksisitas manitol
1. Terjadi setelah dosis tinggi manitol (>200 g/hari)
2. Resembles vasomotor ARF
3. Pulih setelah dilakukan hemodialisis
4. Umumnya berhubungan dengan dekompresi peningkatan tekanan intrakranial atau intraokular
Data are from Gadallah et al, Am J Med Sci 309:219-222, 1995 (case report and review; N=10). Used with permission.
Tabel 4. Nefrotoksisitas manitol
Dikutip dari : Visweswaran, P., Massin, E.K., Dubose, T.D. 1997.
Mannitol-Induced Acute Renal Failure. J Am Soc Nephrol. 8:1028-1033.
Pada gambar 4 dapat dilihat skema klasifikasi untuk GGA. Sistem
klasifikasi termasuk kriteria terpisah untuk kreatinin dan output urin. Seorang penderita dapat memenuhi kriteria perubahan kreatinin serum
Gambar 4. Kriteria gagal ginjal akut
Dikutip dari : Bellomo, R., Ronco, C., Kellum, J.A., Mehta, R.L., Palevsky, P.,
ADQI workgroup. 2004. Acute renal failure – definition, outcome measures,
animal models, fluid therapy and information technology needs: the Second
International Consensus Conference of the Acute Dialysis Quality Initiative
(ADQI) Group. Critical Care. 8:R204-R212.
Penderita dengan gangguan ginjal, usia tua dan menggunakan
agen nefrotoksik merupakan faktor risiko untuk terjadinya GGA akibat
manitol. Jadi penderita harus diskrining untuk fungsi ginjal sebelum
dipertimbangkan menggunakan manitol (Tsai dkk, 2010).
Ketika merawat penderita dengan dosis tinggi manitol, penting
untuk memantau secara rutin konsentrasi serum natrium, kalium, kalsium,
osmolal gap serum melebihi 55 mOsmol / kg H2
[Mannitol] = Osmolal gap X 182 / 10
O atau jika konsentrasi
serum manitol melebihi 1000 mg / L, maka manitol harus dihentikan.
Konsentrasi serum manitol dapat diperkirakan dengan menggunakan
rumus:
(182 merupakan berat molekul manitol)
Dosis tinggi terapi manitol harus digunakan dengan teliti,
khususnya dalam menghadapi insufisiensi ginjal. Pencegahan GGA akibat
manitol dapat dilakukan dengan menghindari dosis yang besar dan terapi
terus–menerus pada penderita berisiko. Namun, ketika toksisitas manitol
terjadi dapat ditangani dengan menghentikan manitol dan dengan
mengembalikan volume cairan ekstraselular. Pemulihan dapat terjadi
secara spontan. Jika diuresis tidak terjadi, hemodialisis mungkin
II.4. KERANGKA TEORI
Stroke Perdarahan Intraserebral
Peningkatan Tekanan Intrakranial
Manajemen Tekanan Intrakranial
Manitol 20%
Mortazavi dkk, 2012: Penanganan peningkatan TIK merupakan hal yang penting dan selalu menjadi permasalahan utama di fasilitas rawat neuro intensif. Manitol telah menjadi salah satu pilihan utama dalam penanganan peningkatan TIK yang cepat.
Dziedzic dkk, 2003: Terjadi peningkatan sementara kadar ureum dan kreatinin serum pada 51 penderita stroke hemoragik yang diterapi dengan manitol menurut pedoman American Heart Association.
Perez dkk, 2002: Melaporkan 4 kasus yang mengalami gagal ginjal akut (3 anuria, 1 nonoliguria) setelah menerima manitol 1,172±439 g (rata-rata±SD) selama jangka waktu 58±28 jam dengan tingkat infus adalah 0,25±0,02 g/kg/jam. Terjadinya gagal ginjal akut terdeteksi 48±22 jam setelah infus.
Du dkk, 1996: Melaporkan 14 kasus GGA yang diinduksi manitol dengan serum Na+, HCO3- menurun,
K+ dan BUN serta osmolal gap meningkat secara
signifikan.
Dorman dkk, 1990: Melaporkan 8 kasus GGA diinduksi manitol. Oliguria terjadi dalam waktu 3,5+1,1 (rata-rata+SD) hari setelah menerima dosis manitol harian 189+64g dan total 626+270g, selama >3,5+1,5 hari. Puncak serum kreatinin 5,7+2,7 mg/dL. Puncak osmolal gap 74+39 mOsm/kgH2O. Dijumpai sel epitel
tubular mengandung vakuola dalam sedimen urin. Thiex dkk, 2007: Terdapat beberapa pedoman untuk mengendalikan pembengkakan otak dan peningkatan TIK. Perfusi otak dan TIK merupakan target terapi dalam mencegah hipoperfusi otak yang mengancam nyawa. Rekomendasi target TIK < 25 mmHg dan CPP > 60–70 mmHg.
Harutjunyan dkk, 2005: Manitol dianggap sebagai 'standar emas' untuk pengobatan peningkatan TIK.
Bereckzi dkk, 2000: Manitol menurunkan TIK dengan cara mengurangi kadar air keseluruhan, volume CSS, volume darah dan meningkatkan perfusi otak dengan mengurangi viskositas.
Broderick dkk, 1999: Peningkatan TIK dianggap penyebab utama kematian pada PIS.
Brouwers dkk, 2012: PIS menyebabkan terbentuknya edema di sekeliling hematoma (perihematomal edema) setelah beberapa jam onset PIS dan semakin lama semakin berkembang.
Brouwers dkk, 2012: Peningkatan TIK berhubungan dengan outcome yang buruk. Penderita PIS dengan gejala klinik dan gambaran radiologis peningkatan TIK harus dilakukan tindakan preventif untuk menurunkan TIK.
II.5. KERANGKA KONSEP
Stroke Perdarahan Intraserebral
Dengan Peningkatan TIK
Manitol 20%
Fungsi Ginjal
Hari 0 dan Hari 3
Kreatinin Serum
Ureum Serum
Osmolalitas Serum
Output
Urin