BAB II
TINJAUAN PUSTAKA
2.1. Teori Umum Adsorpsi
Kemampuan benda padat yang berpori untuk mengadsopsi volume gas
dalam ukuran yang besar telah ditemukan pada abad ke-18 ditemukan oleh
eksperimen yang dilakukan oleh Scheele dan Fontana [3]. Tetapi aplikasi
pemisahan dan pemurnian dari prosess industri dalam ukuran besar baru
dipraktekkan dalam beberapa tahun belakangan ini. Praktek adsorpsi mengunakan
karbon aktif atau silica gel serta zeolite sintetis sebagai adsorbent telah dipakai
secara luas pada akhir tahun 1950.
2.1.1. Jenis – Jenis Adsorpsi
Berdasarkan Interaksi molekular antara permukaan adsorben dengan adsorbat,
adsorpsi dibagi menjadi 2 yaitu :
2.1.1.1. Adsorpsi Fisika
Adsorpsi Fisika terjadi karena adanya gaya Van der Waals. Pada adsorpsi fisika,
gaya tarik menarik antara molekul fluida dengan molekul pada permukaan
padatan (Intermolekuler) lebih kecil dari pada gaya tarik menarik antar molekul
fluida tersebut sehingga gaya tarik menarik antara adsorbat dengan permukaan
adsorben relatif lemah pada adsorpsi fisika, adsorbat tidak terikat kuat dengan
permukaan adsorben sehingga adsorbat dapat bergerak dari suatu bagian
permukaan ke permukaan lainnya dan pada permukaan yang ditinggalkan oleh
permukaan padatan dengan molekul fluida biasanya cepat tercapai dan bersifat
reversibel. Adsorpsi fisika memiliki kegunaan dalam hal penentuan luas
permukaan dan ukuran pori.
2.1.1.2. Adsorpsi Kimia
Adsorpsi kimia terjadi karena adanya ikatan kimia yang terbentuk antara molekul
adsorbat dengan permukaan adsorben. Ikatan kimia dapat berupa ikatan
kovalen/ion. Ikatan yang terbentuk kuat sehingga spesi aslinya tidak
dapatditentukan. Karena kuatnya ikatan kimia yang terbentuk maka adsorbat tidak
mudah terdesorpsi. Adsorpsi kimia diawali dengan adsorpsi fisik dimana adsorbat
mendekat kepermukaan adsorben melalui gaya Van der Waals/ Ikatan Hidrogen
kemudian melekat pada permukaan dengan membentuk ikatan kimia yang biasa
merupakan ikatan kovalen .[4]
2.1.2. Faktor – Faktor yang Mempengaruhi Daya Adsorpsi
Adapun faktor- faktor yang mempengaruhi daya adsorpsi yaitu :
2.1.2.1. Jenis Adsorbat
• Ukuran molekul adsorbat, Ukuran molekul adsorbat yang sesuai
merupakan hal yang penting agar proses adsorpsi dapat terjadi, karena
molekul-molekul yang dapat diadsorpsi adalah molekul-molekul yang
diameternya lebih kecil atau sama dengan diameter pori adsorben.
• Kepolaran zat, Adsorpsi lebih kuat terjadi pada molekul yang lebih polar
dibandingkan dengan molekul yang kurang polar pada kondisi diameter
molekul-molekul yang kurang polar yang telah lebih dahulu teradsorpsi .
Pada kondisi dengan diameter yang sama, maka molekul polar lebih
dahulu diadsorpsi.
2.1.2.2. Suhu
Molekul-molekul adsorbat menempel pada permukaan adsorben terjadi
pembebasan sejumlah energi sehingga adsorpsi digolongkan bersifat eksoterm.
Bila suhu rendah maka kemampuan adsorpsi meningkat sehingga adsorbat
bertambah.
2.1.2.3. Tekanan Adsorbat
Bila tekanan adsorbat pada adsorpsi fisika meningkat maka jumlah molekul
adsorbat akan bertambah namun pada adsorpsi kimia jumlah molekul adsorbat
akan berkurang bila tekanan adsorbat meningkat.
2.1.2.4. Karakteristik Adsorben
Ukuran pori dan luas permukaan adsorben merupakan karakteristik penting
adsorben. Ukuran pori berhubungan dengan luas permukaan, semakin kecil
ukuran pori adsorben maka luas permukaan semakin tinggi. Sehingga jumlah
molekul yang teradsorpsi akan bertambah. Selain itu kemurnian adsorben juga
merupakan karakterisasi yang utama dimana pada fungsinya adsorben yang lebih
murni yang lebih diinginkan karena kemampuan adsorpsi yang baik.
• Temperatur, Oleh karena proses adsorpsi adalah proses yang eksotermis,
maka adsorpsi akan berkurang pada temperatur lebih tinggi. Jika terdapat
reaksi antara kontaminan yang teradsorpsi dan permukaan adsorben antara
2 atau lebih kontaminan kimia tersebut maka laju reaksinya akan
meningkat pada temperatur yang lebih tinggi.
• Kelembapan, Uap air mudah diadsorpsi oleh jenis adsorben polar sehingga
kelembapan yang tinggi dapat mempengaruhi dan mengurangi
kemampuan adsorben tersebut untuk mengadsorpsi kontaminan.
• Laju Alir Pengambilan Sampel, Jika terlalu tinggi laju alir dapat
mengurangi efisiensi adsorpsi
• Adanya Kontaminan Lain, Adanya kontaminan lain dapat mengurangi
efisiensi adsorpsi karena adanya kompetisi antar kontaminan tersebut pada
bagian adsorpsi. Reaksi antar senyawaan juga mungkin terjadi, sehingga
diperoleh hasil konsentrasi yang lebih rendah yang seharusnya.
• Adsorpsi Zat Terlarut oleh Zat Padat, Penyerapan zat dari larutan, mirip
dengan penyerapan gas oleh zat padat. Penyerapan bersifat selektif yang
diserap hanya zat terlarut oleh pelarut. Bila didalam suatu larutan terdapat
2 buah zat ataupun lebih maka zat yang satu akan diserap lebih kuat
dibanding zat yang lain. Zat yang dapat menurunkan tegangan permukaan
maka lebih kuat diserap. Makin kompleks zat terlarut makin kuat diserap
oleh adsorben. Makin tinggi temperatur, maka makin kecil daya serap.
Namun pengaruh temperatur tidak sebesar pada adsorpsi gas. [5]
Isoterm adsorpsi adalah hubungan kesetimbangan antara konsentrasi dalam fase
fluida dan konsentrasi di dalam partikel adsorben pada suhu tertentu. Ada
beberapa isoterm adsorpsi yang diketahui seperti model isoterm Langmuir,
Freundlich dan juga model isoterm Brunauer, Emmet, dan Teller (BET).
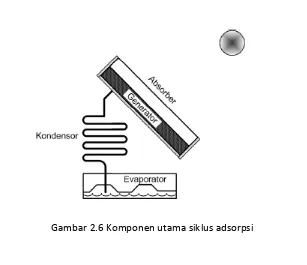
2.2. Sistem Pendinginan Adorbsi
Gambar 2.1 Siklus Dasar Refrigerasi Adsorpsi[6]
Pada kondisi awal sistem berada pada tekanan dan temperatur rendah, adsorben
memiliki konsentrasi refrigeran yang tinggi dan vessel lain terdapat refrigeran
dalam bentuk gas (gambar a). Vessel yang terdapat adsorben dipanaskan yang
adsorbat yang ada di dalam adsorben berkurang atau menguap. Proses
berkurangnya kandungan adsorbat pada adsorben pada kasus ini disebut desorpsi.
Refrigeran yang terdesorpsi kemudian terkondensasi sebagai cairan di dalam labu
kedua dengan dikeluarkannya panas ke lingkungan dimana tekanan dan
temperatur sistem masih tinggi (gambar b). Pemanasan pada labu pertama
dihentikan, lalu pada botol labu yang pertama terjadi perpindahan panas ke
lingkungan sehingga tekanan sistem menjadi rendah. Tekanan sistem yang rendah
menyebabkan adsorbat cair pada botol labu yang kedua menguap dan terserap ke
botol pertama yang berisi adsorben. Proses terserapnya adsorbat ke adsorben pada
kasus ini disebut adsorpsi. Proses adsorpsi menghasilkan efek pendinginan yang
terjadi pada botol labu kedua, dimana pada tekanan rendah panas dari lingkungan
diserap untuk menguap adsorbat (d) sampai sistem kembali ke kondisi awal.
Siklus mesin pendingin adsorpsi dapat digambarkan pada diagram Clayperon
Gambar 2.2 Diagram Clayperon pada Sistem Pendingin Siklus Adsorpsi[2]
Prosess pemanasan (prosess 1-2) dan prosess desorbsi (prosess 2-3) adalah
stengah dari prosess keseluruhan dan prosess pendinginan (prosess 3-4) dan
prosess adsorbs (prosess 4-1) adalah prosess yag terjadi pada saat terjadinya siklus
Adsorpsi. Pada prosess pemanasan, adsorben menerima panas dari matahari dan
meningkatkan panas pada adsorbent dan adsorbat adalah prosess pemanasan
isoteric pada konsentrasi adsorbat = xmax. Ketika tekanan pada adsorben mencapai
tekanan pada kondensor, uap adsorbat akan berpindah ke kondensor dan
mengalami prosess kondensasi, maka konsentrasi dari adsorbat akan turun hingga
minimumnya xmin
2.3.Adsorben
. Pada akhir dari prosess desorbsi, siklus ini akan dilanjutkan
dengan pendinginan kolektor, prosess pendinginan isoteric (prosess 3-4).
Kemudian adsorbat yang telah berbentuk cair akan turun hingga evaporator,
dimana dia akan mengalami prosess penguapan dengan menggunakan panas
lingkungannya yaitu air. Pada akhirnya air akan mengalami pendinginan dan
menjadi es sebahagian atau seluruhnya, setelah itu adsorbent akan mengadsorpsi
uap adsorbent yang mengalir dari evaporator pada tekanan evaporator, ditandai
dengan prosess 4-1 [2].
Adsorben merupakan bahan yang sangat berpori dan adsorpsi berlangsung
terutama pada dinding-dinding pori atau pada letak-letak tertentu di dalam
partikelnya. Karena pori-porinya biasa kecil maka luas permukaan dalam
mencapai beberapa orde besaran lebih besar dari permukaan luar dan bisa sampai
sedemikian kuat sehingga memungkinkan pemisahan komponen itu secara
menyeluruh dari fluida tanpa terlalu banyak adsorpsi terhadap komponen lain.
2.3.1. Jenis – jenis Adsorben
2.3.1.1. Adsorben Tidak Berpori (Non-Porous Sorbent)
Adsorben tidak berpori dapat diperoleh dengan cara presipitasi deposit kristalin
seperti BaSO4 atau penghalusan padatan kristal. Luas permukaan spesifiknya
kecil tidak lebih dari 10 m2 /g dan umumnya antara 0,1 s/d 1 m2/g. Adsorben yang
tidak berpori seperti filter karet (rubber filters) dan karbon hitam bergrafit
(graphitized Carbon Black) adalah jenis adsorben tidak berpori yang telah
mengalami perlakuan khusus sehingga luas permukaannya dapat mencapai
ratusan m2
2.3.1.2. Adsorben Berpori( Porous Sorbents) /g.
Luas permukaan spesifik dsorben berpori berkisar antara 100 s/d 1000 m2
2.3.2. Kriteria Adsorben untuk Menjadi Adsorben Komersil
/g.
Biasanya digunakan sebagai penyangga katalis, dehidrator, dan penyeleksi
komponen. Adsorben ini umumnya benbentuk granular. Klasifikasi pori menurut
International Union of Pure and Applied Chemistry (IUPAC) adalah : • Pori-pori
berdiameter kecil (Mikropores d < 2 nm ) • Pori-pori berdiameter sedang (
Mikropores 2 < d <50 nm) • Pori-pori berdiameter besar ( Makropores d > 50 nm
)
Kriteria yang harus dipenuhi suatu adsorben untuk menjadi adsorben komersial
1. Memiliki permukaan yang besar/unit massanya sehingga
kapasitas adsorpsinya akan semakin besar pula
2. Secara alamiah dapat berinteraksi dengan adsorbat pasangan
3. Ketahanan struktur fisik yang tinggi
4. Mudah diperoleh, harga tidak mahal, tidak korosif dan tidak
beracun
5. Tidak ada perubahan volume yang berarti selama proses adsorpsi
Mudah dan ekonomis untuk diregenerasi.
Beberapa jenis adsorben berpori yang telah digunakan secara komersial antara
lain karbon aktif, zeolit, silika gel, alumina aktif. Seperti pada gambar di bawah
ini :
2.4. Karbon Aktif Sebagai Adsorben
Karbon aktif secara komersial diketahui pertama kali karena penggunaannya
sebagai topeng uap pada perang dunia I. Namun, pada abad ke-15 sudah diketahui
bahwa karbon hasil dekompresiasi kayu dapat menyingkirkan bahan berwarna
dari pada abad ke-17. Penerapan secara komersil arang kayu digunakan dalam
sebuah pabrik gula di Inggris. Karbon aktif merupakan adsorben terbaik dalam
sistem adsorpsi. Ini dikarenakan arang aktif memiliki luas permukaan yang besar
dan daya adsorpsi yang tinggi sehingga pemanfaatannya dapat optimal. Karbon
aktif yang baik harus memiliki luas permukaan yang besar sehingga daya
adsorpsinya juga besar. Luas permukaan karbon aktif umumnya berkisar antara
300–3000 m2/g dan ini terkait dengan struktur pori pada karbon aktif tersebut.
Karbon aktif adalah material berpori dengan kandungan karbon 87%-97% dan
sisanya berupa hidrogen, oksigen, sulfur, dan material lain. Karbon aktif
merupakan karbon yang telah diaktivasi sehingga terjadi pengembangan struktur
pori yang bergantung pada metode aktivasi yang digunakan. Struktur pori
menyebabkan ukuran molekul teradsorpsi terbatas, sedangkan bila ukuran partikel
tidak masalah, kuantitas bahan yang diserap dibatasi oleh luas permukaan karbon
aktif. Perbedaan antara arang dan arang aktif adalah pada bagian permukaannya.
Bagian permukaan arang masih ditutupi oleh deposit hidrokarbon yang
menghalangi keaktifannya, sementara bagian permukaan arang aktif relatif bebas
dari deposit dan permukaannya lebih luas serta pori–pori yang terbuka sehingga
dapat melakukan penyerapan. Kemampuan adsorpsi arang aktif tidak hanya
arang aktif, karakteristik permukan dan keberadaan grup fungsional pada
permukaan pori.
Pada saat pemilihan karbon aktif yang dipakai untuk aplikasi, ada beberapa
spesifikasi yang perlu diperhatikan :
1. Kekerasan karbon aktif
Penggunaaan karbon aktif sebagai penyaringan air, maka kekerasan karbon aktif,
atau kuatnya karbon aktif terhadap abrasi sangat berpengaruh pada hasil
penyaringan.
2. Densitas karbon aktif
Densitas karbon aktif yang paling bagus adalah yang paling rendah, dimana
dengan semakin kecil nilai densitas karbon aktif tersebut maka semakin banyak
dan semakin rapat karbon aktif yang dipakai untuk memenuhi satu wadah
dibandingkan dengan karbon aktif yang memiliki densitas yang tinggi.
3. Kadar iodine
Kadar iodine adalah suatu nilai yang sangat penting dilihat pada saat pemilihan
untuk aplikasi adsorbsi, kadar iodine menunjukan seberapa besar pori-pori
berukuran mikro yang terdapat dalam karbon aktif tersebut, atau total permukaan
dalam karbon aktif. Untuk aplikasi adsorbsi ini penulis menggunakan karbon aktif
Gambar 2.4 Karbon Aktif
2.5.Metanol Sebagai Adsorbat
Untuk terjadinya suatu proses pendinginan diperlukan suatu bahan yang
mudah menguap ataupun berubah dari gas menjadi cair atau sebaliknya. Adapun
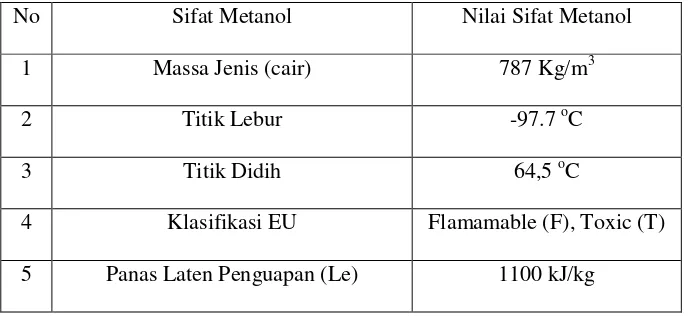
sifat metanol dapat dilihat seperti tabel berikut ini
Tabel 2.1. Sifat Metanol [7]
No Sifat Metanol Nilai Sifat Metanol
1 Massa Jenis (cair) 787 Kg/m3
2 Titik Lebur -97.7 oC
3 Titik Didih 64,5 oC
4 Klasifikasi EU Flamamable (F), Toxic (T)
Metanol merupakan bent
metanol berbentuk cairan yang ringan, mudah menguap, tidak berwarna, mudah
terbakar, dan beracun dengan bau yang khas (berbau lebih ringan daripada
Metanol digunakan sebagai bahan pendingin anti beku, pelarut, bahan bakar dan
sebagai bahan additif bagi etanol industri. Metanol diproduksi secara alami oleh
metabolisme
(dalam jumlah kecil) di udara. Setelah beberapa hari, uap metanol tersebut
aka
2.6. Studi Literatur Jurnal Internasional
Sistem pendinginan dengan menggunakan konsep siklus adsorpsi ini telah
menarik minat para peneliti dan mengalami peningkatan sejak tahun 1990an
karena sistem ini murah, ramah lingkingan dan mudah digunakan sebagai sistem
pendingin, pembuatan es, pengawetan makanan dan penyimpanan vaksin.[2]
Sistem ini bergantung pada suatu material solid yang berongga yang dapat
mengadsorpsi dan mendesorbsi uap dari refrigerant pada kondisi tertentu. Siklus
adsorbs ini mebutuhkan suatu lapisan adsorbent yang diletakan didalam kolektor
surya untuk mendesorbsi refrigerant dalam siang hari dan melakukan adsorpsi
pada refrigerant pada malam hari sehingga evaporator dapat menjadi dinggin dan
dapat menghasilkan es.
Pada siklus adsorpsi ini, medium yang digunakan sebagai pengadsorpsi
(adsorbent) dapat dibagi menjadi dua bagian utama, yaitu adsorpsi fisik (physical
adsorption) dan adsorpsi kimia (chemical adsorption). Adsorpsi fisik disebabkan
oleh gaya Van de Walls antara molekul adsorben dan adsorbat. Karena memiliki
porositas yang tinggi, adsorben ini dapat menyerap adsorbat dan menempatkannya
dalam celah - celahnya. Sementara adsorpsi kimia disebabkan oleh reaksi kimia
antara adsorben dan adsorbat. Transfer elektron, pembentukan dan pemutusan
ikatan kimia selalu terjadi pada adsorpsi kimia . Adsorbent fisik yang umum
digunakan pada pendingin adsorpsi adalah karbon aktif (activated carbon), karbon
aktif fiber (activated carbon fiber), silica gel, dan zeloit. Khusus untuk adsorben
karbon aktif dibuat dari material yang banyak mengandung karbon antara lain dari
Sebagai langkah awal telah dilakukan studi literatur hasil - hasil penelitian tentang
mesin pendingin siklus adsorpsi khusunya yang menggunakan pasangan karbon
aktif dan metanol telah dipublikasikan secara international. Sistem mesin
pendingin siklus adsorpsi terdiri dari kolektor yang sekaligus bertindak sebagai
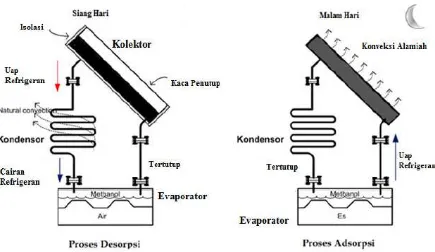
generator, kondensor, dan evaporator. Komponen dari siklus ini dapat dilihat pada
gambar 1 dan gambar 2 yang menjelaskan prinsip kerja proses desorpsi dan
adsorpsi. Di dalam kolektor ini dimuat karbon aktif yang massa optimumnya
menurut adalah sebesar 20 – 26 kg/m2. Kolektor ini harus tertutup, tidak tembus
udara luar dan memiliki pipa penghubung yang menjadi laluan refrigeran masuk
dan keluar dari generator. Karbon aktif akan menyerap uap refrigeran, uap ini
akan menempati celah - celah kosong di antara karbon aktif dengan fasa hampir
cair. Karbon aktif yang mengandung metanol ini jika dipanaskan dengan
menggunakan sinar matahari, maka temperatur dan tekanannya akan naik. Kondisi
ini akan membuat uap refrigeran pada suhu dan tekanan tinggi akan terlepas dari
adsorben dimana prosesnya disebut adsorpsi. Uap refrigeran ini akan mengaliri
kondensor dan karena pendinginan uap akan berubah menjadi cair dan
terakumalasi di evaporator. Proses ini akan berlangsung selama adanya energi
panas dan sinar matahari. Pada malam hari atau jika adsorber ditutup, temperatur
dan tekanan generator akan turun. Pada kondisi ini karbon aktif siap untuk
menyerap metanol kembali. Kondisi ini akan membuat metanol yang ada di
evaporator menguap dan diserap oleh karbon aktif dan proses ini disebut adsorpsi.
Gambar 2.7 Prinsip kerja mesin pendingin siklus adsorpsi
Proses evaporasi metanol ini akan menyerap kalor dari air sebesar kalor
menjadi es. Pada hari berikutnya proses akan berulang kembali. Dengan
menggunakan siklus adsorpsi, penelitian yang menggunakan pasangan karbon
aktif dan metanol sebagai refrigeran yang digerakkan oleh energi matahari telah
banyak dilakukan dan dilaporkan dalam beberapa jurnal ilmiah. Pons dan
Guillminot [8] merupakan pelopor penelitian di bidang ini, mereka melakukan
perancangan dan pengujian mesin pembuat es yang digerakkan tenaga matahari.
Kolektor yang digunakan adalah tipe plat datar dengan luas bidang penyerapan 6
m2 yang mengandung 130 kg karbon aktif dan metanol sebagai refrigeran
sebanyak 18 kg. Pada kondisi sinar matahari yang baik dan lokasi pengujian ada
di daerah Orsay, Francis, mereka mengklaim dapat menghasilkan 30 – 35 kg es
per hari. Li dkk[9] melakukan pengujian performansi dan analisis mesin pembuat
es dengan menggunakan solar kolektor tipe dua plat datar dengan metanol sebagai
refrigeran. Pengujian dilakukan di laboratorium dan sinar matahari disimulasikan
dengan menggunakan lampu quartz. Dengan total radiasi dan lampu sebesar 28 -
30 MJ dapat dihasilkan 7 – 10 kg es. Khattab [10], melakukan penelitian di cairo
(300 latitute), juga menggunakan pasangan karbon aktif (produk lokal) dan
metanol dan melakukan modifikasi pada kolektor. Hasil yang didapatkan adalah
6,9 kg es/m2 pada musim dingin dan 9,4 kg es/m2 pada musim panas. Li dkk
melakukan pengembangan mesin pembuat es tanpa menggunakan katup.
Kolektornya adalah tipe plat datar dengan luas 1 m2 dan mengandung 19 karbon
aktif yang diproduksi di China. Dengan kapasitas penyinaran sebesar 18 – 22
2.7 Kalor (Q)
Kalor adalah energi yang berpindah yang mengakibatkan perubahan temperatur
[12]. Pada abad ke-19 berkembang teori bahwa kalor merupakan fluida ringan
yang dapat mengalir dari suhu tinggi ke suhu rendah, jika suatu benda
mengandung banyak kalor, maka suhu benda itu tinggi (panas). Sebaliknya, jika
benda itu mengandung sedikit kalor, maka dikatakan benda itu bersuhu rendah
(dingin). Kuantitas energi kalor (Q) dihitung dalam satuan joules (J). Laju aliran
kalor dihitung dalam satuan joule per detik (J/s) atau watt (W). Laju aliran energi
ini juga disebut daya, yaitu laju dalam melakukan usaha.
2.7.1 Kalor Laten
Suatu bahan biasanya mengalami perubahan temperatur bila terjadi perpindahan
kalor antara bahan dengan lingkungannya. Pada suatu situasi tertentu, aliran kalor
ini tidak merubah temperaturnya. Hal ini terjadi bila bahan mengalami perubahan
fasa. Misalnya padat menjadi cair, cair menjadi uap dan perubahan struktur kristal
(zat padat) [12]. Energi yang diperlukan disebut kalor transformasi. Kalor yang
diperlukan untuk merubah fasa dari bahan bermassa m adalah:
QL= Le
= Kapasitas kalor spesifik laten (J/kg)
2.7.2 Kalor Sensibel
Tingkat panas atau intensitas panas dapat diukur ketika panas tersebut merubah
termometer. Ketika perubahan temperatur didapatkan, maka dapat diketahui
bahwa intensitas panas telah berubah dan disebut sebagai kalor sensible. Dengan
kata lain, kalor sensibel adalah kalor yang diberikan atau yang dilepaskan oleh
suatu jenis fluida sehingga temperaturnya naik atau turun tanpa menyebabkan
perubahan fasa fluida tersebut [12].
Qs
dimana:
= m Cp ΔT...(2.2.)
Qs
Cp = Kapasitas kalor spesifik sensibel (J/kg.K)
= Kalor sensible (J)
ΔT = Beda temperatur (K)
2.7.3 Perpindahan Kalor
Panas hanya akan berpindah jika ada perbedaan temperatur, yaitu dari sistem yang
bertemperatur tinggi ke sistem bertemperatur rendah. Perbedaan temperatur ini
mutlak diperlukan sebagai syarat terjadinya perpindahan panas. Selama ada
perbedaan temperatur antara dua sistem maka akan terjadi perpindahan panas.
Mekanisme perpindahan panas yang terjadi dapat dikategorikan atas 3 jenis yaitu:
konduksi, konveksi dan radiasi.
1. Konduksi
Konduksi adalah proses perpindahan panas yang mengalir melalui suatu bahan
padat dari daerah yang bersuhu lebih tinggi ke daerah yang bersuhu lebih rendah
di dalam suatu medium (padat, cair atau gas). Peristiwa ini menyangkut
pemikiran telah menghasilkan laju aliran kalor untuk konduksi. Kepadatan aliran
(flux) energi perpindahan kalor secara konduksi disebuah batangan padat,
sebanding dengan beda suhu dan luas penampang serta berbanding terbalik
dengan panjangnya [13].
Pengamatan dibuktikan dengan serentetan percobaan sederhana. Fourter telah
memberikan sebuah model matematika untuk proses ini. Dalam hal satu dimensi,
model matematikanya yaitu :
�= −�.�.��
��...(2.3.)
dimana :
q = Laju perpindahan panas (W)
A = Luas penampang dimana panas mengalir (m2
��
�� = Gradien suhu pada penampang, atau laju perubahan suhu T
)
terhadap jarak dalam arah aliran panas x (K)
k = Konduktivitas termal bahan (W/m.K)
Daya hantar termal merupakan suatu karakteristik dari bahan dan perbandingan
K/l disebut hantaran (konduktivitas) yang ditentukan oleh struktur molekul bahan.
Semakin rapat dan tersusun rapinya molekul-molekul yang umumnya terdapat
pada logam akan memindahkan energi yang semakin cepatdibandingkan dengan
susunan yang acak dan jarang yang pada umumnya terdapat terdapat pada bahan
bukan logam.
Bahan yang mempunyai konduktifitas termal yang tinggi dinamakan konduktor,
sedangkan bahan yang konduktifitas termal rendah disebut isolator. Nilai angka
konduktifitas termal menunjukan beberapa cepat kalor mengalir dalam bahan
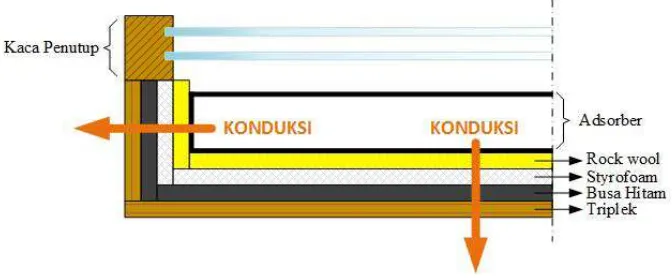
Gambar 2.8. Perpindahan panas pada kolektor surya
Peristiwa perpindahan konduksi pada mesin pendingin tenaga surya terjadi pada
sisi-sisi kolektor yang diisolasi oleh rockwool, styrofoam,busa hitam dan kayu.
Energi panas hilang (Qloss) dan berpindah dari ruang dalam kolektor menuju
temperatur yang lebih dingin (temperatur lingkungan).
2. Konveksi
Perpindahan kalor konveksi bergantung pada konduksi antara permukaan
benda padat dengan fluida terdekat yang bergerak. Persamaan laju perpindahan
panas secara konveksi secara umum:
�= ℎ�(∆�)...(2.4.)
dimana:
q = Laju perpindahan panas konveksi (W)
h = koefisien pindahan panas konveksi (W/m2
A = luas penampang (m
K)
2
ΔT = perubahan suhu (K)
)
- Konveksi Alami (Natural Convection)
Konveksi jenis ini terjadi karena proses pemanasan yang menyebabkan fluida
konveksi bebas terjadi karena gaya buoyancy (apung) yang dialaminya apabila
kerapatan fluida di dekat permukaan perpindahan kalor berkurang sebagai akibat
proses pemanasan.[14] Bilangan Grashof merupakan perbandingan antara gaya
buoyancy terhadap gaya viskositas fluida.
��� = ��(��−�∞)��
3
�2 ...(2.5)
dimana:
g adalah percepatan gravitasi (m/s2); � adalah koefisien ekspansi volume, 1/K
(�=1� untuk gas ideal); Ts adalah temperatur permukaan (oC); �∞ adalah
temperatur fluida yang bergerak di sekitar permukaan (oC); Lc adalah karateristik
panjang dari bentuk geometri (m); � adalah viskositas kinematik (m2
Tabel 2.2. Korelasi empiris bilangan Nusselt rata-rata yang terjadi pada
permukaan proses konveksi bebas[14].
Dari nilai Grashof dan Prandtl dapat dihitung nilai Rayleigh dengan rumus 2.6
untuk plat datar dan 2.7 untuk fin :
��� =��(��−�∞)�
3
�2 �� ……….(2.6)
��� =
��(��−�∞)(���)3
�2 ��……….(2.7)
Dimana As adalah luas seluruh perukaan fin, dan p adalah total perimeter atau
3. Radiasi
Radiasi adalah proses perpindahan panas tanpa melalui media. Bila energi radiasi
mengenai permukaan suatu bahan, maka sebagian akan dipantulkan (refleksi) ,
sebagian lagi akan diserap (absorbsi) dan sebagian lagi akan diteruskan
(transmisi). Kebanyakan benda padat tidak bisa mentransmisikan radiasi thermal
sehingga penerapan transmisivitas dianggap nol [14].
Energi yang diradiasikan dari suatu permukaan ditentukan dalam bentuk daya
pancar (emissive power) yang secara termodinamika dapat dibuktikan bahwa daya
pancar tersebut sebanding dengan pangkat empat dari temperatur absolutnya.
Untuk radiator ideal, biasanya berupa benda hitam (black body).
Persamaan untuk mencari perpindahan panas radiasi adalah sebagai berikut:
���� = ���(��4− ����4 )...(2.6.)
dimana :
qrad = laju perpindahan panas radiasi (W)
ε = emisivitas bahan
A = luas permukaan (m2
Penggunaan energi surya meliputi pengaturan kedudukan permukaan pengumpul
(kolektor) pada berbagai sudut dengan bidang horizontal. Sementara pengukuran
radiasi pada permukaan horizontal di banyak tempat sudah
matahari yang disebut fotosfer memancarkan suatu spektrum radiasi yang
kontiniu.
1. Luas permukaan benda yang bertemperatur, yang akan menentukan besar
kecil jumlah pancaran yang akan dapat dilepaskan.
2. Sifat permukaan yang berhubungan dengan kemudahan memancarkan atau
menyerap panas.
3. Kedudukan masing-masing permukaan satu terhadap yang lain akan
menentukan besar fraksi pancaran yang dapat diterima oleh permukaan
lain.
2.8 Computational Fluid Dynamics (CFD)
Computational Fluid Dynamics (CFD) adalah suatu cabang dari mekanika fluida
yang menggunakan metode numerik untuk menyelesaikan dan menganalisa
elemen-elemen yang akan disimulasikan. Pada proses ini, komputer diminta untuk
menyelesaikan perhitungan-perhitungan numerik dengan cepat dan akurat. Prinsip
kerja pada CFD adalah model yang akan kita simulasikan berisi fluida akan dibagi
menjadi beberapa bagian atau elemen. Elemen-elemen yang terbagi tersebut
merupakan sebuah kontrol perhitungan yang akan dilakukan oleh software
selanjutnya elemen diberi batasan domain dan boundry condition. Prinsip ini lah
yang banyak digunakan pada proses perhitungan dengan menggunakan bantuan
komputasi.
2.8.1 Penggunaan CFD
CFD dalam aplikasinya dipergunakan diberbagai bidang antara lain :
1. Pada bidang teknik
b. Mendesain aerodinamis kendaraan agar menghemat konsumsi
bahan bakar.
c. Mendesain performa pembakaran pada piston kendaraan.
2. Pada bidang olahraga
a. Menghitung kekuatan dan kecepatan pada tiap cara tendangan pada
sepakbola.
b. Menganalisa aerodinamis pada sepatu bola.
3. Pada bidang kedokteran.
a. Menganalisa peredaran udara pada pasien yang mengalami penyakit sinusitis
2.8.2 Manfaat CFD
Terdapat tiga hal yang menjadi alasan kuat menggunakan CFD, yakni :
1. Insight-Pemahaman mendalam
Ketika melakukan desain pada sebuah sistem atau alat yang sulit untukdibuat
prototype-nya atau sulit untuk dilakukan pengujian, analisis CFD memungkinkan
untuk menyelinap masuk secara virtual ke dalam alat/sistem yang akan dirancang
tersebut.
2. Foresight-Prediksi menyeluruh
CFD adalah alat untuk memperidiksi apa yang akan terjadi pada alat/sistem, dan
CFD dapat mengubah-ubah kondisi batas (variasi kondisi batas)
Foresight yang diperoleh dari CFD sangat membantu untuk mendesain lebih cepat
dan hemat uang. Analisis/simulasi CFD akan memperpendek waktu riset dan
desain sehingga juga akan mempercepat produk untuk sampai pasaran.
2.8.3 Metode Diskritisasi CFD
Secara matematis CFD mengganti persamaan-persamaan diferensial parsial dari
kontinuitas, momentum dan energi dengan persamaan-persamaan aljabar
linear.CFD merupakan pendekatan dari persoalan yang asalnya kontinum
(memiliki jumlah sel tak terhingga) menjadi model yang diskrit (jumlah sel
terhingga). Perhitungan/komputasi aljabar untuk memecahkan
persamaan-persamaan diferensial parsial ini ada beberapa metode (metode diskritisasi),
diantaranya adalah sebagai berikut :
1. Finite Volume Method (FVM)
Metode ini adalah pendekatan yang umum digunakan dalam CFD, persamaan
yang mengatur diselesaikan melalui volume kontrol diskrit. Metode volume
terbatas menyusun kembali persamaan diferensial parsial yang mengatur
(biasanya persamaan Navier-Stokes) dalam bentuk konservatif, dan kemudian
discretize persamaan baru.
2. Finite Element Method (FEM)
Digunakan dalam analisis struktural dari padatan, tetapi juga berlaku untuk cairan.
Namun, formulasi FEM membutuhkan perawatan khusus untuk memastikan
solusi konservatif. Perumusan FEM telah diadaptasi untuk digunakan dengan
dirumuskan untuk menjadi konservatif, jauh lebih stabil dibandingkan dengan
pendekatan volume terbatas.
3. Finite Difference Method (FDM)
Memiliki sejarah penting dan sederhana untuk program. Hal ini hanya digunakan
dalam beberapa kode khusus. Modern Kode beda hingga menggunakan sebuah
batas tertanam untuk menangani geometri yang kompleks, membuat kodekode
yang sangat efisien dan akurat. Cara lain untuk menangani geometri termasuk
penggunaan tumpang tindih grid, dimana solusinya adalah interpolated di jaringan
masing-masing.
Metode diskritisasi yang dipilih umumnya menentukan kestabilan dari program
numerik/CFD yang dibuat atau program software yang ada. Oleh karenanya,
diperlukan kehati-hatian dalam cara mendiskritkan model khususnya cara
mengatasi bagian yang kosong atau diskontinu.
2.8.4 Heat Conduction Equation
Untuk mengetahui temperatur pada medium (padat, cair, gas dan
combinasi fasa) karena distribusi temperatur terhadap perubahan posisi pada
keadaan steady dan terhadap waktu pada keadaan transient adalah tujuan utama
dari analisa konduksi. Setelah distribusi temperatur diketahui, maka heat flux pada
setiap titik didalam maupun dipermukaan medium tersebut dapat diketahui dengan
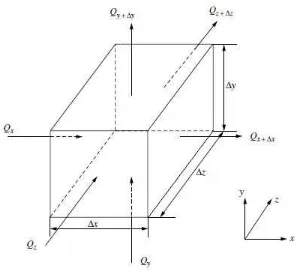
Gambar 2.9 Diagram Heat Conduction pada sistem
Ekspansi Taylor dari gambar diatas dapat ditulis :
��+�� = ��+ ���
�� ∆� … … … 2.7�)
��+�� = �� + ���
�� ∆� … … … 2.7�)
��+�� = �� +���
�� ∆�… … … 2.7�)
Inlet energy pada sistem tersebut adalah �∆�∆�∆�, dan energi yang tersimpan
dalam sistem adalah , dan energi yang tersimpan dalam sistem adalah
�∆�∆�∆��� ��
�� … … … 2.8)
Maka dari kesetimbangan energi didapat
Energi Inlet + Energi yang terbentuk = Energi yang tersimpan + Energi yang
Maka,
�∆�∆�∆�+ ��+�� +��=
�∆�∆�∆��� ��
�� + ��+�� + ��+�� + ��+��. 2.9)
Substitusi persamaan 1a,1b,1c pada persamaan 3, didapat
− ���� ∆� −� ����� ∆� − ���� ∆�� + �∆�∆�∆� = �∆�∆�∆��� ��
�� … . .2.10)
Total perpindahan panas Q pada setiap sumbu adalah :
�� = ∆�∆��� = −��∆�∆���
Substitusi persamaan 2.11a, 2.11b, 2.11c, pada persamaan 2.10 dan dibagi dengan
volume ∆�∆�∆� didapat :
Persamaan 6 merupakan konduksi panas transient dari sebuah sistem yang
diam diekspresikan dalam koordinat kartesian, Konduktifitas thermal , k, dari
persamaan diatas adalah vector, dan dapat ditulis dalam bentuk skalar jadi :
� =�
��� ��� ���
��� ��� ���
��� ��� ����
… … 2.13)
Persamaan 2.8 dan 2.13 digunakan untuk menyelesaikan permasalahan
konduksi panas dalam kondisi material anisotropicdengan sebuah variasi arah
dalam konduktifitas thermalnya. Pada beberapa material, persamaan konduksi
�2�
��� adalah diffusi thermal, merupakan parameter yang
penting dalam analisa konduktifitas panas transient. Untuk kondisi steady maka
rumus 8 dapat dipersingkat menjadi
�2�
Untuk kondisi 1 dimensi, maka rumus 9) dapat dipersingkat lagi menjadi
�
�� ��
��
���= 0 … … 2.16)
2.8.5 Energy Equation
ANSYS Fluent menyelesaikan persamaan energi dengan rumus :
�
��(��) + ∇.��⃑ (��+�)�= ∇.�����∇� − � ℎ� ��⃑� + ��̿���.�⃑��+�ℎ. . .2.17)
Dimana ���� adalah effektivitas konduktif (k+��, dimana �� adalah konduktivitas
thermal turbulent, didevinisikan tergantung model turbulensi yang dipakai), dan �⃗�
adalah flux diffuse dari species j. Sebelah kanan persamaan diatas menyatakan
transfer energi melalui konduksi, diffusi material, dan viscous dissipation. �ℎ
termasuk dalam reaksi kimia, dan panas volumetric yang ditentukan pengguna.
Dari rumus diatas :
� = ℎ −�
�+
�2
Dimana entalpi sensibel dari h untuk gas ideal adalah :
ℎ= � ��ℎ�… … … .2.19)
�
dan untuk incompressible flows adalah :
ℎ =� ��ℎ� +�
� �
… … … .2.20)
dimana �� adalah fraksi massa dari species j dan
ℎ� = � �����… … … . .2.21) �
����
���� yang dipakai dalam menghitung sensible energi dikalkulasikan tergantung
pada solver dan models yang digunakan. Untuk pressure-based solver ���� adalah
298.15 K diluar dari PDF model yang dimana ���� adalah ditentukan dengan
input parameter dari pengguna. Untuk density-based solver ���� adalah 0 K
terkecuali ketika modeling species transport dengan reaksi dimana ����
![Gambar 2.1 Siklus Dasar Refrigerasi Adsorpsi[6]](https://thumb-ap.123doks.com/thumbv2/123dok/3578813.1450909/5.595.137.500.255.609/gambar-siklus-dasar-refrigerasi-adsorpsi.webp)
![Gambar 2.3 Jenis-jenis adsorben[7]](https://thumb-ap.123doks.com/thumbv2/123dok/3578813.1450909/9.595.197.430.398.624/gambar-jenis-jenis-adsorben.webp)