BAB 2
TINJAUAN PUSTAKA 2.1. Ranti Hitam (Solanum blumei Nees ex Blume)
Genus Solanum (famili Solanaceae) adalah suatu kelompok tanaman yang sangat besar terdiri dari sekitar 1400 spesies, yang tersebar di seluruh daerah beriklim tropis dan dunia. Mereka kaya glikosida steroid dalam bentuk glycoalkaloids (Shabana et al., 2013). Salah satu tanaman yang satu genus dan satu famili dengan Solanum nigrum L adalah ranti hitam (Solanum blumei Nees ex Blume). Tanamanini banyak ditemukan di daerah Dairi dan Karo, khususnya desa Kuta Nangka, Kecamatan tanah Pinem, Kabupaten Dairi, berada 800 m di atas permukaan laut dan disebut dengan tanaman ranti hitam. Ranti hitam tumbuh baik di daerah beriklim tropis dan banyak dijumpai di daerah pegunungan, hutan- hutan, dan bekas-bekas pembakaran. Selain telah sering digunakan oleh masyarakat sebagai sayur (daunnya), buah tanaman ini juga digunakan sebagai obat tradisional (etnomedikal), antara lain sebagai obat sakit pinggang, telinga berair, demam, sakit perut, anti peradangan dan lain-lain.
Tanaman ranti hitam ini termasuk ke dalam golongan semak, tumbuh menjalar dan memiliki akar tunggang dengan warna putih kecoklatan. Batang kecil, berbentuk bulat, lunak, dan berwarna kehitaman. Berdaun tunggal, bulat melebar, dan tersebar dengan panjang 7-9 cm ; lebar 4-6 cm. Pangkal dan ujung daun meruncing dengan tepi rata dan tidak bergelombang. Pertulangan daun menyirip. Daun mempunyai tangkai dengan panjang ± 3,5 cm dan berwarna hijau. Bunga berupa bunga majemuk dengan mahkota kecil, bangun bintang, berwarna ungu, benang sari berwarna kuning dengan jumlah 5 buah. Tangkai bunga berwarna hitam. Buah berbentuk bulat, berwarna hitam mengkilat sejak masih muda dan jika sudah tua diameter buahnya kira-kira 0,7 cm. Biji berbentuk bulat pipih, kecil-kecil, dan berwarna kuning (Gambar 2.1). Tanaman yang memiliki nama daerah Leuh mbiring
Biologi-LIPI pada bulan Maret 2013. Gambar tanaman ranti hitamdan bagian-bagian tanaman yang diperoleh dari daerah Kuta Nangka, Kecamatan Tanah Pinem, Kabupaten Dairi, disajikan pada Gambar 2.1.
Gambar 2.1. Tanaman Ranti Hitam (Solanum blumei Nees ex Blume) dan Bagiannya 2.1.1. Nama Umum
Nama umum dari tanaman yang diteliti adalah : Karo : Leweh mbiring
Dairi : Leuh mbiring Indonesia : Ranti hitam Sunda : Leunca
Inggris : Black nightshade Melayu : Ranti
Filipina : Kama-kamatisan
Cina : Long Kui (Anonim, 2013). 2.1.2. Sistematikan Tumbuhan
Sistematika tumbuhan ranti hitam adalah :
Super Divisi : Spermatophyta (menghasilkan biji) Divisi :Magnoliophyta (Tumbuhan berbunga Kelas : Magnoliopsida (berkeping dua/dikotil) Sub kelas : Asteridae
Ordo : Solanales
Genus : Solanum
Spesies : Solanum blumei Nees ex Blume
(Hasil determinasi “Herbarium Bogoriense” bidang Botani Pusat Penelitian Biologi -LIPI Bogor, ranti hitam tersebut adalah Solanum blumei Nees.ex Blume, termasuk famili Solanaceae (Maret, 2013).
2.1.3. Kandungan Kimia Ranti dan Aktivitas Biologisnya
Publikasi atau penelitian terhadap tanaman ranti hitam, baik uji fitokimia metabolit sekundernya maupun uji bioaktivitasnya belum ada ditemukan. Hasil uji fitokimia metabolit sekunder pada tanaman ranti hitam yang dilakukan oleh penulis (Simorangkir dkk, 2013), ekstrak n-heksana dan etilasetat dari daun dan buah ranti hitam banyak mengandung senyawa kimia steroid dan sedikit alkaloid yang terdapat pada ekstrak n-heksana. Senyawa flavonoid hanya terdapat pada ekstrak etilasetat dan ekstrak etanol dari bagian daun dan buahnya, sedangkan senyawa fenol dan saponin hanya terdapat pada ekstrak etanol dari bagian daun, buah dan alkaloid terdapat pada ekstrak etanol buah dan daun. Senyawa kuinon sama sekali tidak terdapat dalam semua ekstrak, sedangkan senyawa tanin lebih banyak diperoleh di dalam ekstrak etanol bagian daun dan buahnya. Tanaman ranti hitam yang telah sering digunakan oleh masyarakat sebagai obat tradisional mempunyai potensi untuk dikembangkan sebagai obat atau bahan baku obat. Tanaman obat umumnya mengandung senyawa bioaktif dalam bentuk metabolit sekunder seperti alkaloid, flavonoid, steroid, triterpenoid, tannin dan lain-lain (Cordell, 2000) yang dapat diekstraksi dengan berbagai pelarut berdasarkan tingkat kepolarannya.
payudara (Prima dan Raditya, 2012). Tanaman Solanum nigrum complex juga telah banyak digunakan secara tradisional sebagai analgetik, antispasmodic, antiseptic, antidysentri, emollient, diuretic, tonic, soporific, laxative, anticancer,antiulcer dan gangguan neuro-vegetatif sistem (Akhtar & Muhammad, 1989). Khasiat obat tanaman Solanum nigrum complex ini disebabkan oleh kandungan alkaloidnya. Glikoalkaloid dan Aglikon Glikoalkaloid pada kelima taxa tanaman Sola num nigrum Complex adalah α-Solamargin, solanin, α-solasodnin) dan aglyconnya (Solasodina dan Solanidine) (Mohy-Ud-Din et al.,2010). Gambar Struktur alkaloid disajikan pada Gambar2.2.
α-Solanin Solasonin Solamargin
Aglikon Solanidin Tigogenin
Gambar 2.2. Struktur Kimia Glikoalkaloid α-Solanin, Solasonin, α-Solamargin, α -Chaconin dan Aglikon (Solasodin, Diosgenin, Solanidin dan Tigogenin) (Prima dan Raditya, 2012).
Komponen alkaloid total Solanum nigrum L mempunyai efek antikanker, tumor dan ekstrak daunnya menghambat Ascitic sarcoma 180 pada tikus. Solanine mempunyai efek antimitosis (menghambat pembelahan sel) sehingga perkembangan sel kanker dapat dihambat. Kandungan metabolit sekunder seperti solasodine pada Solanum nigrum L mempunyai efek menghilangkan sakit (analgetik), menurunkan panas, antiradang dan antishok. Solamargine dan solasonine mempunyai efek antibakteri, sedangkan solanine sebagai antimitosis. Senyawa-senyawa ini bisa mengatasi gangguan kenker, yakni kanker payudara, leher rahim, lambung dan saluran pernafasan (Kabayan, 2009).
Hasil penelitian pendahuluan penulis (Simorangkir dkk, 2013), pada ekstrak etanol buah Solanum blumei Nees.ex Blume terdapat alkaloid, flavonoid, fenol, sedikit saponin dan tanin, dan rendemen tertinggi terdapat pada ekstrak etanol bagian daun dan buah dibandingkan dengan ekstrak n-heksana dan etilasetat.
2.2 Uji Bioaktivitas Bahan Alam
2.2.1 Metode Uji Antioksidan DPPH (1,1-Diphenyl-2-Picrylhydrazyl)
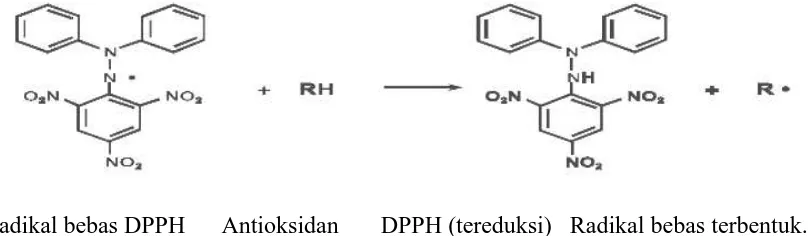
Pada tahun 1922, ditemukan senyawa berwarna ungu radikal bebas stabil DPPH, yang sekarang digunakan sebagai reagen kolorimetri. Metode peredaman radikal bebas adalah sebuah metode yang sederhana yang dapat digunakan untuk menguji kemampuan antioksidan yang terkandung dalam makanan. Metode peredaman radikal bebas dapat digunakan untuk sampel yang padat dan juga dalam bentuk larutan (Molyneux, 2004). Uji antioksidan dapat dilakukan dengan metode peredaman DPPH. Prinsip metode Peredaman Radikal Bebas (DPPH) adalah kemampuan sampel uji dalam meredam proses oksidasi DPPH sebagai radikal bebas dalam larutan metanol (sehingga terjadi perubahan warna DPPH dari ungu menjadi kuning) dengan nilai IC50 (konsentrasi sampel uji yang mampu meredam radikal bebas 50%) digunakan sebagai parameter untuk menentukan aktivitas antioksidan sampel uji (Molyneux, 2004).
Radikal bebas DPPH Antioksidan DPPH (tereduksi) Radikal bebas terbentuk.
Gambar 2.3 .Reaksi Antara DPPH dengan Atom H yang Berasal dari Antioksidan (Molyneux, 2004).
Senyawa yang berperan sebagai antioksidan dengan cara memberikan atom hidrogennya akan mereduksi DPPH sehingga terjadi perubahan warna DPPH dari ungu menjadi kuning (Molyneux, 2004). Penapisan (screening) obat antikanker biasanya didahului dengan penapisan akvitas antioksidan dari suatu senyawa. Hirota,
Atas dasar fungsinya, antioksidan dapat dibedakan menjadi lima bagian yaitu :
1. Antioksidan Primer : Antioksidan yang berfungsi mencegah terbentuknya radikal bebas baru karena dapat merubah radikal bebas yang ada menjadi molekul yang berkurang dampak negatifnya, yaitu sebelum sempat bereaksi. Antioksidan primer yang ada dalam tubuh yang sangat terkenal adalah enzim superoksida dismutase.
2. Antioksidan Sekunder : Antioksidan sekunder merupakan senyawa yang berfungsi menangkap radikal bebas serta mencegah terjadinya reaksi berantai sehingga tidak terjadi kerusakan yang lebih besar. Contoh antioksidan sekunder adalah vitamin E, vitamin C dan beta karoten yang dapat diperoleh dari buah-buahan.
3. Antioksidan Tersier : merupakan senyawa yang dapat memperbaiki sel-sel jaringan yang rusak karena serangan radikal bebas. Biasanya yang termasuk kelompok ini adalah enzim misalnya metionin sulfoksida reduktase yang dapat memperbaiki DNA dalam inti sel. Enzim tersebut bermanfaat untuk perbaikan DNA pada penderita Kanker.
4. Chelator atau Sequestrants : Senyawa Chelator atau Sequestrants dapat mengikat logam sehingga logam tersebut tidak dapat mengkatalisis reaksi oksidasi dan kerusakan dapat dicegah. Misalnya asam sitrat dan asam amino.
5. Oxygen Scavanger : antioksidan yang mampu mengikat oksigen sehingga tidak mendukung reaksi oksidasi, misalnya vitamin C (Kumalaningsih, 2006).
2.2.2. Uji Toksisitas Brine Shrimp Lethality Test (BSLT)
Metode BSLT adalah metode yang sederhana dan mudah dilakukan untuk menguji senyawa bioaktif dari bahan alam dengan menggunakan larva udang Artemia
sitotoksik atau anti tumor (Meyer, et al., 1982). Penggunaan larva udang Artemia salina Leach untuk uji aktivitas biologis sudah dilakukan sejak tahun 1956 dan sejak saat itu metode ini banyak digunakan untuk studi lingkungan, toksisitas dan penapisan senyawa bioaktif di dalam ekstrak tanaman. Uji aktivitas dengan menggunakan larva udang Artemia salina Leach memiliki spektrum aktivitas farmakologi, mudah dilakukan, sederhana, cepat dan tidak memerlukan biaya besar dengan tingkat kepercayaan 95%. Cara yang dilakukan menggunakan sejumlah larva udang yang ditetaskan, kemudian ke dalam wadah yang berisi larva udang dimasukkan ekstrak tanaman yang diuji, kemudian dihitung mortalistasnya. Dalam metode BSLT, toksisitas senyawa antitumor dinyatakan dengan nilai Lethal concentration 50 (LC50), yaitu konsentrasi senyawa yang memberikan tingkat mortalitas sebanyak 50%. Senyawa aktif akan memberikan mortalitas tinggi. Semakin kecil nilai LC50 maka semakin besar toksisitasnya. Suatu sampel dikatakan sangat toksik terhadap larva udang Artemia salina Leach apabila mempunyai LC50 < 30 µg/mL, toksik apabila LC50 30 – 1000 µg/mL dan tidak toksik apabila mempunyai LC50 > 1000 µg/mL (Steven dan Molyneux, 1993). Uji BSLT dapat digunakan untuk uji bahan sebagai penenang, toksisitas, insektisida dan uji awal untuk senyawa sitotoksik atau antikanker (Meyer, etal., 1982).
2.2.3. Uji Anti Kanker
Untuk menentukan suatu bahan alami atau sintetis yang dapat digunakan sebagai anti kanker, terdapat beberapa istilah yang harus diperhatikan, berdasarkan efek biologi dari suatu senyawa terhadap sel yang dicobakan yaitu sitotoksik, anti tumor, dan anti kanker (Suffness dan Pezzuto, 1991; Bulan, 2002).
Sitotoksik adalah toksik terhadap sel dalam jaringan. Sifat ini dapat dibedakan menjadi sitostatik dan sitosidal. Sitotoksik yaitu menghentikan pertumbuhan sel yang
sama. Maka dari kedua sistem tersebut dapat disimpulkan bahwa in vitro dan in vivo
bersifat saling melengkapi.
Sejak tahun 1955–1975 lembaga kanker nasional Amerika (NCI, National Cancer Institute) menggunakan lini sel L1210 untuk penapisan awal zat anti kanker, zat – zat yang aktif terhadap lini sel L1210, kemudian di uji secara in vivo pada tikus yang diinokulasi dengan tumor. Program penapisan yang dilakukan NCI berhasil menguji aktivitas 40.000 senyawa. Senyawa yang menunjukkan aktivitas terhadap lini sel L1210 diuji lebih lanjut terhadap suatu panel uji sel tumor tikus sebelum dilakukan uji klinik. Selanjutnya NCI menggunakan suatu desain dalam penapisan awal untuk mendeteksi aktivitas suatu zat antitumor berdasarkan model seleksi dari beberapa tumor padat pada tikus. Hasil seleksi yang dilakukan menghasilkan sel P388 digunakan sebagai uji penapisan awal, karena sel ini sangat sensitif terhadap bermacam golongan senyawa dan banyak sekali senyawa–senyawa yang menunjukkan aktivitas terhadap sel P388. Setelah diketahui bahwa suatu zat aktif pada penapisan awal maka diuji lebih lanjut terhadap sel kanker yang lebih spesifik yaitu suatu panel uji sel tumor tikus baik secara in vitro maupun secara in vivo dan selanjutnya di uji lagi dengan sel xenograft tumor manusia. Sel tumor tikus yang biasa digunakan untuk panel uji tersebut adala lini sel L1210, sel Melanoma B16, sel tumor payudara CDFI, sel kanker paru–paru, dan sel tumor usus. Sedangkan sel xenograft tumor manusia digunakan sel tumor usus besar CX-1, sel tumor paru–paru LX-1, sel tumor payudara MX-1 (Suffnes dan Pezzuto, 1991).
Selain IC50 untuk menentukan sifat sitotoksik suatu zat digunakan juga ukuran lain yaitu Lethal Dosis 50 (LD50) yaitu dosis yang efektif untuk menghambat pertumbuhan sel sebesar 50%. Setelah lolos dari uji penapisan awal selanjutnya dilakukan uji toksikologi pra klinis dan farmakologis melalui pengujian secara in vivo
dengan beberapa sistem tumor hewan yang dapat ditransplantasikan dan telah ditentukan sifat – sifatnya pada hewan percobaan. Kriteria yang ditetapkan pada hewan percobaan adalah berdasarkan nilai LD50 (mg/Kg) yaitu dosis yang dapat menyebabkan kematian hewan percobaan sebesar 50%. Senyawa yang memberikan harapan yaitu senyawa yang tidak mempunyai toksisitas berlebihan dilanjutkan ke uji coba klinik fase I yaitu penelitian jaringan tempat efek toksik dan farmakologinya pada pasien kanker stadium lanjut. Konsentrasi awal yang dianggap aman untuk digunakan pada manusia adalah konsentrasi dengan nilai LD10 pada hewan percobaan. Seterusnya dilakukan uji coba klinik fase II untuk menentukan jenis tumor tempat zat ini bermanfaat dan selanjutnya dilakukan uji coba klinik fase III untuk membandingkan zat tersebut dengan terapi standar terbaik. Untuk zat yang telah dinyatakan memenuhi standar tersebut diberi izin oleh Food and Drug Administration
(FDA) untuk digunakan sebagai obat. Obat anti kanker yg ideal akan membasmi sel kanker tanpa merugikan jaringan normal (Salmon dan Sartorelli, 1998).
2.3. Kanker
Kanker adalah suatu pertumbuhan sel atau tumor, hasil dari pembelahan sel yang tidak normal dan tidak terkendali. Pada setiap pembelahan sel selalu diawali oleh pembelahan inti sel. Menurut teori dogma sentral, pada proses pembelahan inti sel terjadi proses replikasi (biosintesis molekul DNA) dan proses transkripsi (Watson,
et. al, 1988).
2.3.1. Replikasi DNA
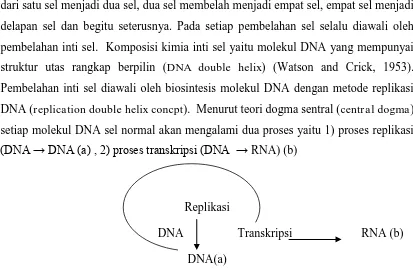
dari satu sel menjadi dua sel, dua sel membelah menjadi empat sel, empat sel menjadi delapan sel dan begitu seterusnya. Pada setiap pembelahan sel selalu diawali oleh pembelahan inti sel. Komposisi kimia inti sel yaitu molekul DNA yang mempunyai struktur utas rangkap berpilin (DNA double helix) (Watson and Crick, 1953). Pembelahan inti sel diawali oleh biosintesis molekul DNA dengan metode replikasi DNA (replication double helix concpt). Menurut teori dogma sentral (central dogma) setiap molekul DNA sel normal akan mengalami dua proses yaitu 1) proses replikasi
(DNA → DNA (a) , β) proses transkripsi (DNA → RNA) (b)
Replikasi
DNA Transkripsi RNA (b)
DNA(a)
Gambar 2.4. Teori Dogma Sentral (Watson, et.al., 1988)
Replikasi molekul DNA (duplikasi DNA) adalah pembuatan copi DNA baru dimana DNA awal akan berfungsi sebagai patron atau cetakan (template) dalam mensintesis
rantaiDNAbaru. Proses replikasi membutuhkan unsur-unsur berikut :
a. dNTP–dNTP yang meliputi: dATP; dGTP; dCTP dan dTTP.
b. Enzim unwindase yaitu enzim yang berfungsi untuk membuka rantai DNA utas
rangkap berbentuk heliks (double strands) menjadi utas tunggal (single strand).
Tahap Replikasi (biosintesis) DNA terdiri dari :
a. Tahap inisiasi adalah tahap terbukanya rantai DNA utas rangkap bentuk heliks oleh enzim unwindase, sehingga memungkinkan enzim DNA polimerase mengawali sintesis DNA baru.
b. Tahap pemanjangan (phase elonggation) yaitu proses pemanjangan rantai DNA baru dengan dibawanya dNTP yang sesuai merupakan basa-basa komplementer pada DNA cetakan oleh enzim DNA polimerase.
c. Tahap pengakhiran (phase termination) yaitu fase berakhirnya aktivitas enzim DNA polimerase untuk membawa dNTP-dNTP yang sesuai, karena DNA baru telah terbentuk dengan sempurna mengikuti pola basa yang terdapat pada DNA template.
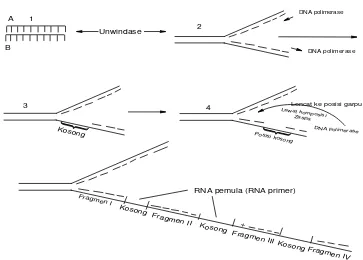
Gambar 2.5. Replikasi DNA Metode Semikonservatif (Watson et al., 1988). 2.3.2. Replikasi DNA dengan Metode Okazaki Fragmentasi (Teori
Terbentuknya Kanker)
Gambar 2.6. Replikasi DNA Dengan Metode Okazaki Fragmentasi (Teori . Terbentuknya Kanker)
A
B 1
Unwindase
DNA polimerase
DNA polimerase
2
Kosong 3
Posisi koson g Lewat komposisi
Zaspa
DNA polimerase
4
+
Fragmen I
Fragmen II
Fragmen III
Fragmen IV Kosong
Kosong
Kosong RNA pemula (RNA primer)
Pada saat utas rangkap DNA terbuka dari pilinannya dengan adanya enzim unwindase, satu utas DNA direplikasi dalam bentuk segmen panjang yang utuh untuk setiap garpu. Utas DNA template yang baru terbentuk ini bertambah panjang kearah garpu bersamaan dengan bertambah panjangnya pilinan yang terbuka pada DNA induk. Utas lain direplikasi dalam bentuk potongan-potongan pendek yang dikenal dengan nama fragmen okazaki (okazaki pieces) sesuai dengan nama orang yang menemukannya. Bila fragmen okazaki ini mengalami replikasi akan terbentuk beberapa pasangan DNA yang pendek, lalu disertai dengan pembelahan sel sehingga terbentuk beberapa jumlah sel. Kejadian seperti ini mengakibatkan terganggunya program genetik sel yang mengakibatkan pembelahan sel yang tidak terkendali sehingga terjadi keganasan. Faktor-faktor penyebab terjadinya proses seperti ini dinamakan faktor karsinogenik atau onkogenik(oncos = tumor) (Okazaki dan Ogawa, 1980). Panjang fragmen ini biasanya 40 s/d 290 nukleotida, rata-rata 135 nukleotida. Panjang RNA pemula pada posisi kosong 8 sampai dengan 20 nukleotida, umumnya 9 nukleotida (Gambar 2.6). Untuk melepaskan RNA pemula dari segmen DNA dihidrolisis oleh enzim hidrolase yang spesifik hibrida RNA-DNA. Hasil akhir dari proses replikasi DNA dengan metode okazaki fragmentasi yaitu 1) untuk rantai A sebagai template akan terbentuk DNA yang utuh dan 2) rantai B sebagi tamplate akan diperoleh segmen-segmen DNA yang didalam pembelahan sel akan terbentuk sel-sel baru dalam jumlah tidak menentu (Okazaki dan Ogawa, 1980; Soultanas dan Wigley, 2001).
dapat tumbuh dan berkembang pada jaringan lain (tempat baru). Kanker merupakan suatu penyakit dimana individu dari sel yang telah mengalami mutasi secara irreversibel pada DNA-nya mulai menyebar dan menyerang jaringan di sekitarnya sehingga pertumbuhannya tidak terkendali (Alberts, et al., 1994 ; Bulan, 2002). Umumnya sel kanker mempunyai sifat pertumbuhan yang berlebihan, gangguan diferensiasi dari sel dan jaringan, bersifat invasif terhadap jaringan di sekitarnya (metastatis) yaitu menyebar ke jaringan lain dan menyebabkan pertumbuhan baru, dan perubahan metabolisme kearah pembentukan makromolekul dari nukleosida dan asam amino serta peningkatan katabolisme karbohidrat untuk energi sel (Watson et al., 1988).
Organ tubuh yang berpotensi terkena kanker antara lain, paru-paru, payudara, sistem reproduksi seperti uterus, serviks, ovarium pada wanita dan prostat pada laki-laki, usus besar (kolon dan rektum), lambung, kulit, vasofaring, kelenjar getah bening, hati, otak, darah dam rongga mulut (Bishop and Harold, 1991). Kanker diklasifikasikan sesuai dengan jaringan atau tipe sel darimana ia timbul. Kanker yang timbul pada sel–sel epitelial (sel–sel permukaan) dinamakan karsinoma (carcinoma), misalnya kanker payudara, kanker kulit, dan kanker lambung. Kanker yang timbul pada jaringan konektif (penyambung) atau sel–sel otot disebut sarkoma, misalnya fibrosarkoma (kanker jaringan ikat) dan kanker yang tidak memenuhi salah satu dari dua kategori di atas adalah termasuk dalam berbagai jenis leukimia yaitu kanker yang berasal dari sel–sel hemopoietic (sel darah) dan kanker yang berasal dari sistem syaraf (Alberts et al., 1994 ; Bulan, 2002)
interaksi antara faktor lingkungan dan lingkungan kerja (Occupational) yang disebut dengan zat karsinogenik yang dapat dibagi sebagai berikut :
1. Karsinogenik kimia seperti nikotin, tar dari rokok, zat radioaktif, zat pengawet, penyedap, pewarna makanan, nitrosamine, asbes, arsen, batubara, merkuri, alkohol, dan lain-lain.
2. Karsinogenik fisika seperti sinar-x, ultraviolet, laser, radiasi atom dan lain-lain. 3. Karsinogenik biologi seperti infeksi virus (papiloma, herves) yang merupakan
salah satu faktor resiko kanker serviks, jamur misalnya jamur Aspergillus flavus
penyebab kanker hati (Ames, 1979)..
2.3.3. Hubungan Telomerase dengan Tumor
Kromosom eukariot berbentuk rantai lurus. Ujung kromosom mempunyai struktur yang spesifik yang dikenal dengan nama telomer. Bentuk telomer semua kromosom eukariot umumnya tersusun dari nukleotida-nukleotida pendek dan letaknya pada
ujung γ’ kromosom DNA. Sebagai contoh telomer sel sperma manusia dan sel telur
terdiri dari 1000 s/d 1700 copi dari TTAGGG. Telomer kromosom ini berfungsi untuk mencegah degradasi DNA atau penggabungan antar DNA. Pengikatan telomer ini pada ujung DNA dilakukan oleh RNA primase yang dikenal dengan telomerase. Telomerase tidak sama dengan DNA polimerase yang pertama sekali ditemukan oleh Elizabeth Blackburn dan Carol Greider dari university California (1985) menunjukkan bahwa telomerase bertanggung jawab dalam pembelahan sel somatik. Telah ditemukan bahwa untuk setiap siklus pembelahan sel, DNA akan mengalami pemendekan sebesar 50 nukleotida pada posisi ujung telomer. Oleh karena itu setiap siklus pembelahan sel, telomer-telomer ini makin lama makin pendek sehingga sel menjadi tidak stabil dan lama kelamaan akan mati. Penomena seperti ini telah
ditemukan para ilmuan yang dikenal dengan “Telomere Theory of Aging Interstingly Cancer Cells of Pear Immortal because They Continue to Reproduce Indetimitely”.
Corporation of Neulo Park California bahwa semua tumor terjadi diakibatkan oleh aktivitas telomerase.
T T A G G G T T A G G G ← Gugus telomer pada DNA polimerase
5’---
γ’ ---
A A U C C C A A U C C C → Gugus telomer pada RNA
Gambar 2.7. Gugus Telomer pada DNA Polimerase dan RNA
Sama halnya dengan telomer lain, telomer manusia merupakan ribonukleotida protein. Jumlah nukleotida telomer RNA manusia 962 nukleotida. RNA ini merupakan cetakan untuk sintesis DNA telomerase yang aktif untuk mensintesis telomer-telomer. Urutan nukleotida telomerase RNA berkisar 46 s/d 56 nukleotida yang urutannya AAUCCC dimana basa T pada telomerase DNA digantikan oleh basa U pada telomerase RNA. Telomer-telomer merupakan kelipatan nukleotida heksamer TTAGGG yang jumlahnya antara 1000-1700 nukleotida dan terletak pada ujung γ’ kromosom DNA yang terbanyak basanya adalah basa G. RNA primase adalah suatu enzim yang lebih dikenal dengan enzim telomerase yang membentuk segmen-segmen okazaki ( Feng et al., 1995).
Enzim Telomerase
Telomerase adalah suatu ribonuklease. Telomerase pada manusia merupakan enzim yang sangat komplek baik struktur maupun aktivitas kerjanya. Esensial struktural komponennya adalah :
1. Gugus katalitik protein ini disebut TERT, yang berfungsi sebagai transkriptase balik (reverse transkriptase) yaitu suatu enzim yang mengkatalis transkripsi RNA menjadi DNA.
3. Additional interacting protein meliputi : TRF, TRT, dan lain sebagainya. Telomerase mempunyai berbagai tingkat aktivitas yang mampu mengendalikan pembelahan sel sehingga telomerase disebut agent pembelahan sel. Telomerase biasanya memperpendek siklus sel secara normal. Apabila telomerase menjadi lebih pendek (telomerase menjadi tidak aktif) mengakibatkan kromosom tidak stabil, pembelahan sel akan berhenti lalu sel akan mati (apoptosis). Secara alami proses pemendekan telomerase merupakan kunci biologis didalam pengaturan pembelahan sel. Hasil riset akhir-akhir ini menunjukkan bahwa telomerase merupakan pemicu terbentuknya sel kanker. Telah diketahui bahwa aktivitas telomerase dijumpai pada sel kanker ovarium wanita, tetapi tidak ditemukan pada sel non malignat pasien kanker yang sama. Ini menunjukkan bahwa ada hubungan langsung antara aktivitas telomerase dalam pembentukan kanker payudara (breast cancer). Sebanyak 85-90% pembentukan kanker sangat dipengaruhi oleh aktivitas telomerase (Greider and Blackburn, 1996; Perkel, 2002).
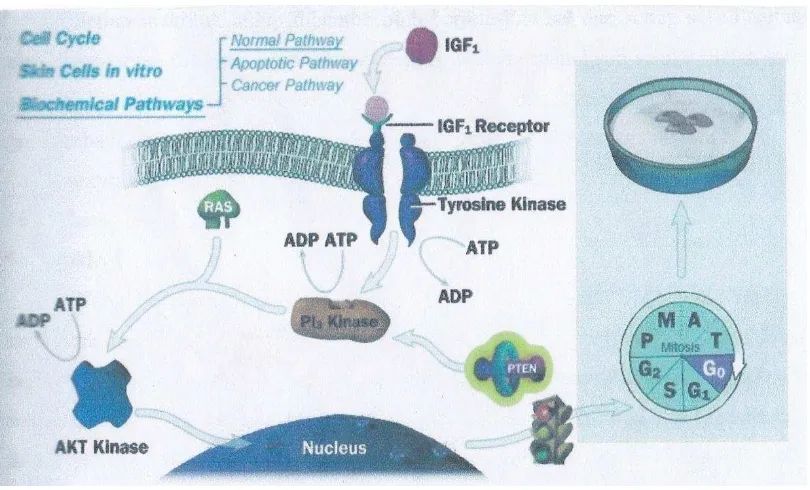
2.3.4. Mekanisme Pembentukan Kanker
Kanker adalah suatu pertumbuhan sel atau tumor hasil dari pembelahan sel yang tidak normal dan tidak terkendali. Pada dasarnya pembelahan sel dibedakan menjadi 2 macam yaitu pembelahan sel secara langsung dan secara tidak langsung. Pembelahan sel secara langsung jika proses pembelahan tidak didahului dengan pembentukan gelondong pembelahan dan penampakan kromosom yang disebut dengan amitosis. Pembelahan secara tidak langsung jika proses pembelahan didahului dengan pembentukan gelondong pembelahan dan penampakan kromosom. Pembelahan secara tidak langsung ini meliputi pembelahan mitosis dan pembelahan meiosis.
Kinase-RAS akan mengaktifkan Kinase dengan bantuan ATP selanjutnya akan memberi sinyal kepada Nukleus untuk memulai melakukan pembelahan sel sesuai kebutuhannya.
Gambar 2.8. Mekanisme Terbentuknya Sel Kanker
Setelah keperluan sel yang dibutuhkan tercukupi maka PTEN akan merebut ATP yang akan digunakan PI3 Kinase sehingga kompleksnya dengan RAS tidak berlangsung dan sinyal selanjutnya akan terhenti maka pembelahan sel berikutnya akan terhenti juga.
Proses terbentuknya sel kanker diawali terganggunya PTEN oleh faktor inflamasi maupun paparan benda asing mengakibatkan PI3 Kinase akan mengikat ATP secara tidak terkendali sehingga respon untuk pembelahan sel juga tidak terkendali yang menghasilkan sel yang tidak dewasa dan tidak memiliki hubungan antar sel sehingga sel tidak memiliki fungsi bologis sebagaimana mestinya yang disebut sel kanker.
terlibat di dalam pembelahan sel (perkembangbiakan sel) adalah inti sel. Inti sel terdiri dari 3 komponen yaitu : a. Deoxyribonucleic Acid (DNA), b. Ribonucleic Acid (RNA) dan c. Nukleoprotein (Protein Inti).
Yang berperan penting dalam pembelahan sel adalah DNA yang mampu menurunkan sifat baka (kekal) setiap makhluk hidup, sehingga DNA dikenal dengan unsur genetika. Komposisi DNA secara umum dibagi 2 bagian yaitu intron dan exon. Intron atau faktor pengendali pada pembelahan sel dan terdiri dari nukleotida dalam jumlah tertentu dan berbeda untuk setiap spesies, sedangkan exon adalah urutan nukleotida dalam jumlah tertentu yang berfungsi untuk mensintesis komponen sel di dalam perkembangannya.
Penggambaran struktur DNA berdasarkan pernyataan di atas sebagai berikut :
Intron - - - - - - - - - - - Ekson
R P O X Y Z
DNA
Pembelahan mitosis berfungsi menggandakan pertumbuhan (termasuk mengganti sel rusak atau mati), sedangkan pembelahan meiosis bertujuan untuk membentuk sel-sel perkembangbiakan (gamet). Secara normal, pembelahan mitosis menghasilkan dua bahan nukleus anak (sel anak) dengan perangkat kromosom yang identik. Sel yang normal dalam tubuh akan tumbuh dan mati secara terkendali. Di samping itu, dapat juga terjadi penyimpangan yaitu sekelompok sel yang tumbuh dan membelah secara abnormal membentuk tumor (benjolan). Beberapa tumor bersifat jinak, artinya sampai tahap tertentu pertumbuhannnya berhenti. Sebaliknya ada tumor ganas atau kanker, yang sel-selnya terus menerus tumbuh dan membelah sehingga mendesak dan merusak jaringan yang ada di sekitarnya dan menyebar ke jaringan lain (metastatis) yang menyebabkan pertumbuhan baru dan terjadi perubahan metabolisme ke arah pembentukan makromolekul dari nukleosida serta asam amino juga peningkatan katabolisme karbohidrat untuk energi sel (Watson et al., 1988).
Sel kanker mempunyai sistem enzim yang berbeda yaitu jumlah macam enzim sel kanker lebih sedikit dibanding sel normal, misalnya sel kanker tidak mempunyai enzim asparagin sintetase. Enzim-enzim untuk pertumbuhan pada sel kanker lebih besar dibandingkan sel normal. Sel normal tumbuh hanya satu lapis setelah sampai dinding tempat media (dinding petri jika di dalam cawan petri), akan terhenti pertumbuhannya, sedangkan sel kanker akan tumbuh terus dan terbentuk lapisan-lapisan yang tidak teratur (Mulyadi, 1997). Faktor-faktor penyebab kanker (karsinogen) dapat berupa senyawa kimia, faktor fisika seperti radiasi sinar X atau UV, virus atau disebut virus onkogenik serta ketidakseimbangan hormonal (Bulan, 2002). .
2.3.5. Leukimia (Kanker Darah)
tidak berfungsi. Sel-sel tersebut berinfiltrasi secara progresif ke dalam jaringan tubuh terutama ke dalam sumsum tulang belakang. Hal ini akan mengakibatkan fungsi sumsum tulang belakang untuk membentuk sel darah merah (eritrosit), sel darah putih normal dan keping darah (platelets) menjadi terganggu. Sel darah merah berfungsi membawa oksigen dan karbon dioksida, keping darah (trombosit) berfungsi membantu penggumpalan darah ketika terluka dan sel darah putih (leukosit) membantu tubuh melawan infeksi dari penyakit.
Ada 4 macam leukimia yaitu 1) Leukimia limfositik akut (LLA), 2) Leukimia mielositik akut (LMA), 3) Leukimia limfositik kronis (LLK) dan 4) Leukimia mielositik kronis (LMK). Leukemia mielositik melibatkan granulosit, sedangkan leukemia limfositik melibatkan limfosit yaitu sel T dan sel B.
Leukimia Akut
Leukimia akut, penyakit leukimia yang kondisinya akan semakin memburuk secara cepat. Leukimia akut menunjukkan gejala klinik suhu badan naik, ada tanda– tanda infeksi, pendarahan karena trombositopenia, pucat, lesu, karena anemia dan nyeri pada tulang. Pemeriksaan laboratorium menunjukkan kesamaan, kecuali jenis sel leukemianya, yaitu kadar haemoglobin turun, jumlah leukosit naik, jumlah eritrosit turun, ditemukan banyak sel muda (immature), jumlah trombosit turun dan waktu pendarahan lama. Ada dua jenis leukimia akut yaitu leukimia mielositik akut (LMA) dan leukimia limfositik akut (LLA).
bisa menyebabkan meningitis, anemia, gagal hati, gagal ginjal dan kerusakan organ lainnya (Medi, 2010)..
Gejala pertama biasanya terjadi karena sumsum tulang gagal menghasilkan sel darah yang normal dalam jumlah yang memadai, ditandai dengan lemah, sesak nafas, infeksi, pendarahan dan demam. Gejala lainnya adalah sakit kepala, muntah, gelisah dan nyeri tulang dan sendi. Penyakit LMA terutama menyerang orang dewasa. Tanpa pengobatan, jangka waktu bertahan hidup penderita dalam batas tiga bulan. Tujuan pengobatan adalah menghancurkan semua sel leukemik sehingga penyakit bisa dikendalikan. LMA hanya memberikan respon terhadap obat tertentu dan pengobatan sering kali membuat penderita lebih sakit sebelum mereka membaik. Penderita menjadi lebih sakit karena pengobatan menekan aktivitas sumsum tulang, sehingga jumlah sel darah putih semakin sedikit (terutama granulosit) dan hal ini menyebabkan penderita mudah mengalami infeksi (Medi, 2010). Pada kemoterapi awal biasanya diberikan sitarabin (selama7 hari) dan daunorubisin (selama 3 hari). Kadang diberikan obat tambahan (misalnya tioguanin atau vinkristin) dan prednison. Dengan kemoterapi yang intensif harapan hidup pasien LMA lebih dari satu tahun dan beberapa pasien ada yang bertahan sampai tiga tahun dan sekitar 20% kemungkinan dapat sembuh. Obat tunggal yang paling aktif bagi pasien LMA adalah sitarabin, tetapi lebih baik bila digunakan kombinasi dengan obat lain. Kombinasi
yang baik yaitu sitarabin dengan tioguanin atau sitarabin dengan daunorubisin.
sel-sel yang menghasilkan sel darah yang normal. Sel kanker ini kemudian dilepaskan ke dalam aliran darah dan berpindah ke hati, limpa, kelenjar getah bening, otak, ginjal dan organ reproduksi, dimana mereka melanjutkan pertumbuhannya dan membelah diri. Sel kanker bisa mengiritasi selaput otak, menyebabkan meningitis dan bisa menyebabkan anemia, gagal hati, gagal ginjal dan kerusakan organ lainnya. Penderita LLA mengalami anemia, pendarahan dan mudah terkena infeksi. Dengan proses kemoterapi yang intensif harapan hidup pasien LLA antara tiga sampai lima tahun dan lebih dari 50% peluang untuk dapat sembuh. Beberapa pusat medis menggunakan proses kemoterapi dengan kombinasi obat yaitu vinkristin dan prednison (Medi, 2010). Penderita LLA mengalami anemia, perdarahan dan mudah terkena infeksi. Dengan kemoterapi yang intensif harapan hidup pasien LLA antara tiga sampai lima tahun dan lebih dari 50% dapat sembuh. Beberapa pusat medis menggunakan kemoterapi kombinasi obat yaitu vinkristin dan prednison (Medi, 2010).
Leukimia Kronis
setelah tiga sampai empat tahun setelah diagnosis dan penyakit ini berubah menjadi leukimia akut. Proses penghambatan dapat dilakukan menggunakan proses kemoterapi menggunakan busulfan.
LLK merupakan penyakit yang timbul akibat akumulasi sel limfosit dalam sumsum tulang, darah, kelenjar getah bening, limfa dan hati sehingga sel pembentuk darah lainnya di dalam sumsum tulang berkurang. Penyakit LLK ini sering timbul pada pasien yang berusia lanjut (usia 45 tahun ke atas) dan sangat jarang terjadi pada pasien sebelum umur 45 tahun. Tetapi LLK meliputi kortikosteroid atau kemoterapi obat alkilasi. Obat alkilasi akan menurunkan jumlah limfosit pada kebanyakan pasien penderita penyakit ini dan yang biasa digunakan adalah klorambusil dan mempunyai efek samping yang sangat kecil (Medi, 2010).
2.3.6. Lini Sel L1210
Salah satu yang digunakan untuk menguji sifat anti kanker suatu zat adalah sel L1210, di samping sel yang lainnya seperti sel hela (sel kanker yang berasal dari kanker leher rahim manusia), sel P388, sel KB (nasopharynx carcinoma), sel sarkoma 180 A, sel V 79, sel walker 256 dan lain – lain (Bulan, 2002).
1975 lembaga kanker nasional Amerika ( NCI, National Cancer Institute)
menggunakan lini sel L1210 untuk penapisan awal zat anti kanker, zat – zat yang aktif terhadap lini sel L1210, kemudian di uji secara in vivo pada tikus yang diinokulasi dengan tumor. Program penapisan yang dilakukan NCI berhasil menguji aktivitas 40.000 senyawa. Senyawa yang menunjukkan aktivitas terhadap lini sel L1210 diuji lebih lanjut terhadap suatu panel uji sel tumor tikus sebelum dilakukan uji klinik.
2.3.7. Aktivitas Biologis Penghambatan Sel Kanker
Kanker adalah suatu pertumbuhan sel atau tumor, hasil dari pembelahan sel yang tidak normal dan tidak terkendali. Setiap pembelahan sel selalu diawali oleh pembelahan inti sel. Menurut teori dogma sentral, pada proses pembelahan inti sel terjadi proses replikasi (biosintesis molekul DNA) dan proses transkripsi (Watson,
et.al,1988). Aktivitas biologis penghambatan sel kanker dapat dilakukan dengan mekanisme penghambatan sintesa DNA (Replikasi DNA ). Replikasi DNA dapat terjadi dengan adanya sintesis rantai nukleotida baru dimana rantai nukleotida lama berfungsi sebagai cetakan DNA baru. Proses replikasi meliputi yaitu : 1) Denaturasi molekul DNA utas rangkap → utas tunggal (enzim unwindase), 2) Sintesis DNA baru dgn DNA template (dNTP, enzim DNA polimeras), 3) Pembentukan DNA rangkap (enzim ligase) secara konservatif, semi konservatif dan 4) Untuk sel kanker diperlukan enzim telomerase yg memotong rantai DNA awal menjadi fragmen dimana urutan nukleotidanya sudah memenuhi unsur gen.
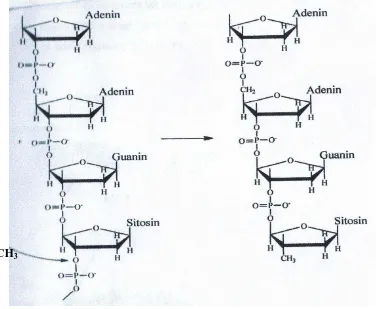
no 3 dari DNA, maka sintesa DNA pada sel kanker akan terhambat karena tidak terjadi perpanjangan rantai DNA (Gambar 2.9). Akibat masuknya metil pada deoksiribosa, maka perpanjangan DNA berikutnya akan terhambat karena posfat tidak dapat berikatan lagi pada atom C nomor 3 sehingga sintesa DNA akan terhenti (Munchberg et al., 2007).
-CH3
Gambar 2.9. Reaksi Penghambatan Rantai DNA Yang Mengandung Adenin, Guanin dan Sitosin (Munchberg et al., 2007).
2.3.7. 1. Menginhibisi Telomerase
sel. Aktivitas tolemerase menyebabkan sel kanker tidak mati (immortal). Banyak peneliti mengemukakan hipotesis bahwa senyawa-senyawa kimia yang menghambat aktivitas kerja tolemerase adalah obat yang ampuh sebagi anti kanker. Untuk menghambat kerja tolomerase dapat dilakukan dengan beberapa cara antara lain : 1) Membuang (memotong=silencing) gene yang mengkode pembentukan enzim tolomerase, 2) Menginhibisi sub unit katalitik protein TERT, 3) Interferensi dengan faktor protein esensial TRF and TRF2 dan 4) Interferensi dengan aksi RNA tamplate T.R.
Oleh karena itu banyak laboratorium diseluruh dunia berusaha untuk mendapatkan inhibitor enzim tolomerase untuk tujuan ilmu lebih-lebih untuk mendapatkan hadiah nobel, popularitas didalam blokingnya kromosomal DNA (telomerase Strands). Komplek enzim telomerase hanya mempunyai aktivitas untuk mensintesis telomer-telomer dalam bentuk rantai tunggal (single Strands). Analisis kristalografi sinar X maupun NMR menunjukkan bahwa bagian yang kaya G dari utas tunggal telomerase secara alami cendrung terikat pada utas tunggal sendiri. Struktur sperti ini dapat mengakibatkan satu atau dua rantai telomer yang kemudian akan berkembang menjadi 4 (empat) telomer yang terpisah satu dengan yang lain. Biokimiawan sekarang berusaha untuk mendapatkan agent kimia yang mampu menginhibisi aktivitas enzim telomerase pada posisi yang kaya dengan G dengan cara berikatan dengan ujung yang kaya G tersebut, membentuk suatu struktur komplek yang kuat (Pindur et al., 1993).
2. 3.7.2. Beberapa Senyawa Anti Kanker
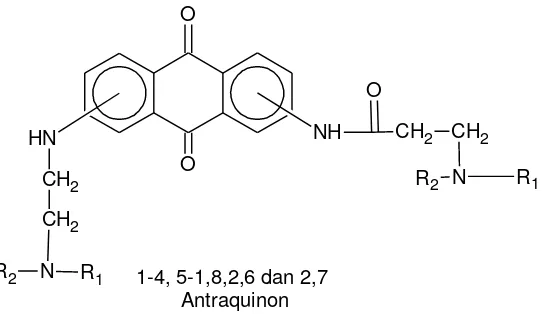
NH
Gambar 2.10. Struktur Antraquinon (Pindur et al., 1993).
N
Gambar 2.11. Struktur Akrimida (Pindur et al., 1993).
N
O O O
H O
O OH H
OH
OH
O
CH3
OH
NH2
H3CO
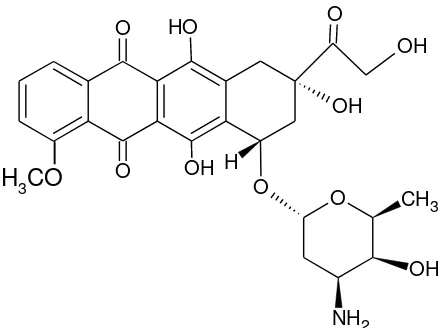
Gambar 2.13. Struktur Doxorubicin (Pindur et al., 1993)
2.3.7.3. Obat Anti Kanker
Pencarian obat antikanker baru memainkan peranan penting, tidak hanya oleh perusahaan obat tetapi juga oleh banyak organisasi pemerintah. Tingkat kematian akibat kanker cendrung meningkat diperkirakan dari 9 juta kematian pada tahun 2015 meningkat menjadi 11,4 juta pada tahun 2030. Oleh karena itu obat-obat kanker baru yang lebih efektif sangat diperlukan (Saiz-Urra et al., 2009). Jenis pengobatan kanker salah satunya dengan memberikan obat-obat pembunuh sel kanker/sitostatika (kemoterapi). Tujuan utama kemoterapi kanker adalah merusak secara selektif sel tumor yang berbahaya tanpa mengganggu sel normal.
Antitumor yaitu efektif terhadap suatu model sistem tumor secara in vivo. Antikanker yaitu efektif dalam suatu percobaan terhadap suatu penyakit pada manusia. Sedangkan untuk menetapkan suatu senyawa bersifat antikanker dilakukan beberapa tahap penelitian yaitu uji sifat farmakologi dan aktivitas terhadap berbagai sel (penapisan awal) adalah untuk menentukan toksisitas suatu senyawa. Uji toksikologi pra klinis dan farmakologi pada hewan percobaan untuk menentukan sifat antitumor suatu senyawa, dan uji coba klinik pada manusia untuk menetapkan suatu senyawa sebagai obat antikanker.
Penentuan sifat toksisitas suatu senyawa dilakukan uji sifat farmakologi dan aktivitasnya terhadap berbagai sel secara in vitro atau in vivo. Sel–sel yang digunakan antara lain sel P388 (sel limfositis yang berasal dari kanker pada tikus), lini sel L1210 (sel yang diisolasi dari limfa tikus), sel hela (sel yang berasal dari kanker leher rahim manusia), sel KB (nasopharynx carsinoma), sel sarcoma 180 A, sel walker 256 (Itokawa dan Takeya, 1993 ; Bulan, 2002). Bagaimanapun juga, berbagai macam lini sel leukimia lebih sering digunakan untuk mengelusi mekanisme apoptosis. Hal ini terjadi karena obat-obatan antikanker maupun reagen sitotoksik lebih efektif terhadap kanker leukimia daripada penyakit kanker lainnya. Contoh lini sel leukimia lainnya yang sering digunakan adalah lini sel promyelocytic HL-60 serta lini sel Jurkat T (Zhang et al., 2008).
Menurut penelitian yang dilakukan oleh Eagle dan Foley (1958), sel kanker yang dibiakkan dalam kultur jaringan secara in vitro dapat digunakan sebagai alat penapisan awal untuk mendeteksi sifat antitumor suatu zat. Toplin pada tahun 1959 menyusun prosedur kultur jaringan untuk program penapisan zat antikanker secara besar–besaran dan dengan prosedur tersebut telah berhasil menguji aktivitas senyawa antitumor sebanyak 17.000 jenis senyawa hasil fermentasi. Sel yang digunakan dalam kultur jaringan tersebut adalah sel hela.
Hasil pengujian yang diperoleh dibandingkan dengan pengujian secara in vivo
aktivitas antitumor pada kultur jaringan dengan aktivitas pada tikus yang diinokulasi dengan tumor. Namun ada beberapa kekecualian yaitu ada zat yang sangat aktif pada kultur jaringan tetapi tidak aktif pada tikus percobaan dan sebaliknya ada zat yang aktif pada tikus percobaan tetapi tidak aktif pada kultur jaringan dengan tingkat konsentrasi yang sama. Maka dari kedua sistem tersebut dapat disimpulkan bahwa in vitro dan in vivo bersifat saling melengkapi.
Sejak tahun 1955–1975 lembaga kanker nasional Amerika ( NCI, National Cancer Institute) menggunakan lini sel L1210 untuk penapisan awal zat anti kanker, zat – zat yang aktif terhadap lini sel L1210, kemudian di uji secara in vivo pada tikus yang diinokulasi dengan tumor. Program penapisan yang dilakukan NCI berhasil menguji aktivitas 40.000 senyawa. Senyawa yang menunjukkan aktivitas terhadap lini sel L1210 diuji lebih lanjut terhadap suatu panel uji sel tumor tikus sebelum dilakukan uji klinik. Selanjutnya NCI menggunakan suatu desain dalam penapisan awal untuk mendeteksi aktivitas suatu zat antitumor berdasarkan model seleksi dari beberapa tumor padat pada tikus.
Penentuan dapat atau tidaknya suatu zat dikembangkan sebagai obat anti kanker didasarkan pada sifat toksisitasnya. NCI telah menetapkan kriteria aktivitas berdasarkan nilai inhibisy Concentration 50 (IC50) yaitu konsentrasi yang dibutuhkan untuk menghambat pertumbuhan sel sebesar 50%. Suatu zat disebut bersifat sitotoksik bila aktivitas terhadap sel uji mempunyai nilai IC50 < 20 µ g/ml untuk suatu ekstrak, dan nilai IC50 < 4 µg/mL untuk senyawa murni (Suffnes dan Pezzuto, 1991).
Selain IC50 untuk menentukan sifat sitotoksik suatu zat digunakan juga ukuran lain yaitu Lethal Dosis 50 (LD50) yaitu dosis yang efektif untuk menghambat pertumbuhan sel sebesar 50%. Setelah lolos dari uji penapisan awal selanjutnya dilakukan uji toksikologi pra klinis dan farmakologis melalui pengujian secara in vivo
dengan beberapa sistem tumor hewan yang dapat ditransplantasikan dan telah ditentukan sifatnya pada hewan percobaan. Kriteria yang ditetapkan pada hewan percobaan adalah berdasarkan nilai LD50 (mg/Kg) yaitu dosis yang dapat menyebabkan kematian hewan percobaan sebesar 50%. Senyawa yang memberikan harapan yaitu senyawa yang tidak mempunyai toksisitas berlebihan dilanjutkan ke uji coba klinik fase I yaitu penelitian jaringan tempat efek toksik dan farmakologinya pada pasien kanker stadium lanjut. Konsentrasi awal yang dianggap aman untuk digunakan pada manusia adalah konsentrasi dengan nilai LD10 pada hewan percobaan. Seterusnya dilakukan uji coba klinik fase II untuk menentukan jenis tumor tempat zat ini bermanfaat dan selanjutnya dilakukan uji coba klinik fase III untuk membandingkan zat tersebut dengan terapi standar terbaik. Untuk zat yang telah dinyatakan memenuhi standar tersebut diberi izin oleh Food and Drug Administration
(FDA) untuk digunakan sebagai obat. Obat anti kanker yang ideal akan membasmi sel kanker tanpa merugikan jaringan normal (Salmon dan Sartorelli, 1998).
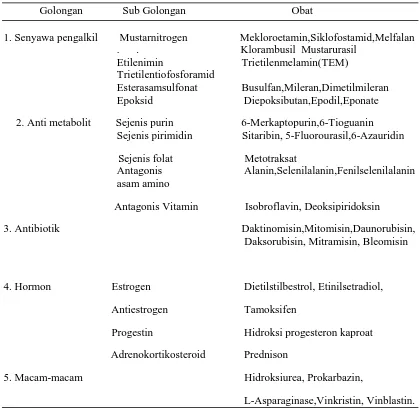
Kelompok obat CCS ini adalah vinkristin, vinblastin, sitarabin, fluorourasil, azositidin, bleomisin, merkaptopurin, tioguanin, hidroksiurea dan metotreksat. Kelompok obat CCNS adalah mekloroetamin, siklofosfamid, melfalan, busulfan, tiotepa, karmustin, lomustin, semustin, mitomisin, daktomisin, deoksorubisin dan daunorobisin. Obat antikanker dapat digolongkan menjadi beberapa jenis, seperti yang disajikan pada Tabel 2.1.
Tabel 2. 1 Obat Antikanker dan Penggolongannya
Golongan Sub Golongan Obat
1. Senyawa pengalkil Mustarnitrogen Mekloroetamin,Siklofostamid,Melfalan . . Klorambusil Mustarurasil Etilenimin Trietilenmelamin(TEM) Trietilentiofosforamid Esterasamsulfonat Busulfan,Mileran,Dimetilmileran
Epoksid Diepoksibutan,Epodil,Eponate
2. Anti metabolit Sejenis purin 6-Merkaptopurin,6-Tioguanin Sejenis pirimidin Sitaribin, 5-Fluorourasil,6-Azauridin
Sejenis folat Metotraksat Antagonis Alanin,Selenilalanin,Fenilselenilalanin asam amino
Antagonis Vitamin Isobroflavin, Deoksipiridoksin
3. Antibiotik Daktinomisin,Mitomisin,Daunorubisin,
Daksorubisin, Mitramisin, Bleomisin
4. Hormon Estrogen Dietilstilbestrol, Etinilsetradiol,
Antiestrogen Tamoksifen
Progestin Hidroksi progesteron kaproat
Adrenokortikosteroid Prednison
5. Macam-macam Hidroksiurea, Prokarbazin,
L-Asparaginase,Vinkristin, Vinblastin.
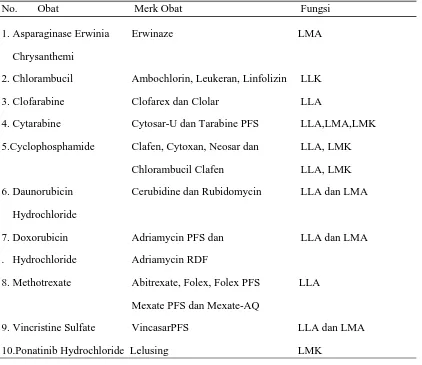
Beberapa merk obat antikanker yang sudah dijual di pasaran secara komersil beserta fungsinya disajikan pada Tabel 2.2.
Tabel 2.2. Beberapa Obat Antikanker yang Dijual Secara Komersil
No. Obat Merk Obat Fungsi
1. Asparaginase Erwinia Erwinaze LMA
Chrysanthemi
2. Chlorambucil Ambochlorin, Leukeran, Linfolizin LLK
3. Clofarabine Clofarex dan Clolar LLA
4. Cytarabine Cytosar-U dan Tarabine PFS LLA,LMA,LMK
5.Cyclophosphamide Clafen, Cytoxan, Neosar dan LLA, LMK
Chlorambucil Clafen LLA, LMK
6. Daunorubicin Cerubidine dan Rubidomycin LLA dan LMA
Hydrochloride
7. Doxorubicin Adriamycin PFS dan LLA dan LMA
. Hydrochloride Adriamycin RDF
8. Methotrexate Abitrexate, Folex, Folex PFS LLA
Mexate PFS dan Mexate-AQ
9. Vincristine Sulfate VincasarPFS LLA dan LMA
10.Ponatinib Hydrochloride Lelusing LMK
Sumber (NCI, 2008)
2.3.7. 3. Mekanisme Reaksi Beberapa Senyawa Anti Kanker
harus dikombinasikan agar kinerjanya dapat maksimal. Sebagai contoh obat untuk leukimia akut yang digunakan selama ini adalah kombinasi dari 6-Merkaptopurin, Metotraksat, Prednison dan L-Asparaginase. Fungsi masing-masing obat adalah sebagai berikut :
a. 6-Merkaptopurin
6-Merkaptopurin merupakan analog basah adenin dan hiposantin. Bila difosporilasi dengan 5-fosfo-α-D-ribosilposfat menghasilkan 6-Merkaptopurin ribosit yang merupakan inhibitor perubahan IMP (Inosinmonoposfat) menjadi AMP (Adenosinmonoposfat).
b. Metotraksat
Metotraksat analog asam folat merupakan inhibitor (penghambat) enzim dihidrofolat reduktase sehingga reaksi pembentukan koenzim aktif asam tetrahidrofolat (THF) dari asam folat tidak dapat berlangsung (Gambar 2.14). Koenzim tetrahidrofolat (THF) berfungsi sebagai pembawa sementara gugus 1-karbon (metilen CH2) (Gambar 2.15) dalam reaksi enzimatik biosintesis asam deoksitimidilat dari asam deoksiuridilat. Asam deoksitimidilat merupakan suatu nukleotida unit pembangun DNA. Penghambatan enzim dihidrofolat reduktase ini oleh obat-obatan tertentu akan menghambat replikasi DNA pada sel kanker sehingga dapat digunakan dalam penyembuhan beberapa kanker.
Gambar 2.16.
N5,N10-Metilentetrahidro folat
Gambar 2.17. Peranan N5,N10-metilentetrehidrofolat Sebagai Pemberi Gugus Metil di dalam Pembentukan Asam Timidilat Secara Enzimatik. Deoksitimilat merupakan Unit Pembangun DNA. (Lehninger, 1988).
Enzim dihidrofolat reduktase ini sangat peka terhadap senyawa-senyawa analog asam folat (antimetabolit) sehingga digunakan pada kemoterapi untuk sel kanker. Fungsi folat terutama di dalam sintesis prekursor asam nukleat dimana analog-analog senyawa tersebut akan menghambat sintesis DNA sel-sel kanker.
c. L-Asparaginase
Aspargin merupakan asam amino esensial bagi sel kanker, dengan adanya enzim L-asparaginase maka aspargin akan diubah menjadi asam aspartat. Adanya ion amonium , matrik essensialnya tidak terpenuhi sehingga sel kanker akan mati.
C
Gambar 2.18. Reaksi Dalam Bentuk Asam Amino
d. Prednison
Prednison merupakan senyawa anti inflamasi (peradangan) menghambat sintesis DNA/RNA limfosit.
Mekanisme kerja prednison belum begitu jelas tetapi aktivitas penyembuhan leukimia dihubungkan dengan penghambatan sintesis DNA dan RNA limfosit. Prednison adalah suatu ortikosteroid golongan glukokortikoid yang berfungsi untuk menghambat pengambilan glukosa oleh sel-sel kanker sehingga membatasi energi yang sangat dibutuhkan untuk biosintesis asam nukleat dan beberapa kasus sintesis DNA dan RNA mungkin langsung dipengaruhi (Montgomery et al., 1993). Prednison suatu senyawa hasil sintesis yang mempunyai aktivitas antikanker yang lebih tinggi dari efek antikanker metotraksat yaitu dengan cara menghambat sintesis DNA maupun RNA limfosit (Montgomery et al., 1993).
e. Mustard Nitrogrn
R
Tabel 2.3. Gangguan Fungsi DNA dan Senyawa/Obat Terapi Kanker (Pindur et al., 1993)
No Gangguan Fungsi DNA Senyawa/Obat Terapi Kanker
Memutus rantai DNA Bleomisin, Prokarbasin, Radiasi sinar gamma,
neokarsinostatin, mitomisin
2 Mengikat silang DNA Senyawa-senyawa pengalkil, mitomisin,
cis-platinum (II) diaminklorida.
3 Menghilangkan pilinan berganda DNA m-AMSA (4-(9-akridilamino)-meta sulfono-m-amisidin)
(tahap uji coba klinis), Bahan penginterkolasi, cis-platinum (II) diaminklorida, Elliptisin (uji coba klinis).
4 Menghambat DNA polimerase Aphidikholin (uji coba klinis), Arabinosil sitosin.
5 Menghambat sintesis DNA pada sembarang tempat
Arabinosil sitosin, 5-azasitidin (uji coba klinis), Daunorubisin, Vinblastin, Vinkristin. 6 Menghentikan sintesis 45 S RNA Aktinomisin D, Daunorubisin, Adriamisin,
Mithramisin, Mustard nitrogen, Kloroetil sikloheksil (nitroso urea) (CCNU), Elliptisin (ujicoba klinis).
7 Membentuk ikatan silang antara DNA dan Protein
Adriamisin
8 Menghambat pemprosesan 45 S RNA CCNU, Biskloromitrosourea (BCNU), Dihidro 5- azasitidin (ujicoba),
5- floxourasil, 5- florourasil deoksiribosida (5 FUdR).
9 Menghambat sintesis hn RNA Aktinomisin D, Mustard nitrogen
10 Menghambat poliadenilisasi m RNA 3- deoksiadenosin
11 Pemutusan rantai m RNA BCNU
12 Menghambat sintesis t RNA Formisin (tidak digunakan untuk manusia), 5- azisitidin (uji coba klinis).
13 Menghambat sintesis t RNA mitokondria Etidium bromida (bukan untuk manusia).
14 Degradasi Poliribosom BCNU, D-galaktosamin
15 Menghambat pembentukan ribosom Aktinomisin D
16 Menghambat sintesis rantai peptida Sikloheksamida (bukan untuk manusia), Auquidin (ujicobaklinis),
Emitin (tidak dipakai untuk kanker)
Beberapa Ekstrak Bahan Alam Yang Memiliki Aktivitas Antikanker
1. Bruceosida merupakan senyawa alkaloid yang telah diesktraksi dari buah makasar (Bruea javnica L. Merr.) aktif menghambat leukimia 388 dengan cara menghambat sintesis DNA pada sel kanker (Yu, 1995).
2. Vinblastin (VLB) merupakan senyawa alkaloid yang diisolasi dari daun tapak dara (Catharantus roseus L. ) efektif menghambat berbagai jenis kanker seperti pada sel kanker L1210; P1534; AKR; EAC; S180 dan tumor payudara, sedangkan alkaloid Vincristin mempunyai efek antikanker lebih tinggi dari Vinblastin. Selain efektif terhadap kanker di atas, Vincristin telah diuji sangat efektif menghambat sel kanker ridgeway oesteosarcoma; lymfosarcoma dan X5563 meyloma (Ziyin
and Zelin., 1994 dan Yuan et al.,1999). Ekstrak alkohol dari tumbuhan tapak dara ini dapat menghambat perkembangan sarkoma 180 (S180), daya tingkat keberhasilan 97,5% (Ziyin and Zelin, 1994; Siaw, 1998).
3. Ekstrak etanol dari tumbuhan bawang hutan (Scorodocarpus borneensis Becc) merupakan senyawa bioaktif yang secara signifikan dapat menghambat pertumbuhan sel kanker leukimia L1210 (Kartika dkk, 2014).
4. Senyawa indol dan sulforafan hasil ekstraksi tanaman Brokoli (Brassica oleraceae
var italica juga sangat berpotensi untuk mencegah pertumbuhan kanker (Yuan
et.al., 1999).
2..3.7.4. Uji Antikanker (Sitotoksik) Terhadap Sel Leukimia L1210
organ lainnya dan dapat menyebabkan kematian dalam kurun waktu 8-11 hari, merupakan sel tumor yang tumbuh cepat dengan persentase sel cukup tinggi dan memiliki tingkat pertumbuhan 100% (Bauguess, et.al., 1981). Sel leukimia L1210 diperoleh dari The Institute of Physical and Chemical Research Japan (RIKEN). Sel leukimia L1210 tersebut kemudian disuspensikan ke dalam formula media RPMI-1640 dan mengandung larutan calf bovine serum. Ekstrak kasar dari suatu bahan alam yang dapat diuji secara langsung dalam biakan sel leukimia L1210. Jika hasilnya positif menghambat pertumbuhan sel leukimia L1210, maka dapat dikatakan ekstrak tersebut aktif sebagai inhibitor. Sebagai ukuran aktivitas sitotoksik, ditentukan IC50 dari ekstrak kasar tersebut. Aktivitas kristal (isolat murni) dikatakan aktif sebagai antikanker bila nilai IC50 < 4 µg/mL dan IC50<20 µg/mL untuk suatu ekstrak (Suffines dan Pezzuto, 1991).
Metode Uji Aktivitas Sitotoksik Terhadap Sel Leukimia L1210
Pembuatan media RPMI-1640 seberat 10,4 g yang mengandung L-glutamin dilarutkan dalam 1 L air steril (A). Kemudian 1,3 g NaHCO3 dilarutkan dalam 50 ml air steril (larutan B). Sebanyak 25 ml larutan B ditambahkan ke dalam 475 ml larutan A, maka diperoleh 500 ml media (C). Untuk keperluan uji, 15 ml calf bovine serum
ditambahkan ke dalam 85 ml larutan C. Semua pekerjaan dilakukan di ruang steril. Sel leukimia L1210 disuspensikan ke dalam media yang telah mengandung calf bovine
serum sehingga jumlah sel sekitar 2 x 105 sel/mL. Sel leukimia L1210 yang digunakan dalam penelitian ini diperoleh dari The Isntitute of Physical and Chemical Research Jepang.
metanol) yang telah ditambahkan 990 µL suspensi sel. Percobaan dilakukan duplo, selanjutnya suspensi sel yang telah diisi zat uji diinkubasi selama 48 jam pada suhu 37°C dalam inkubator 5% CO2. Perhitungan sel dilakukan menggunakan
haemocytometer Neubauer improved. Untuk membedakan antara sel hidup dengan sel mati maka sebelum dilakukan penghitungan, 90 µL suspensi dimasukkan ke dalam sero cluster plate (96 sumuran) dan ditambah 10µ L larutan 1% tryphan blue
dan dihomogenkan. Sebanyak 10µ L larutan dialirkan ke dalam haemocytometer Neubauer improved. Setelah itu jumlah sel yang masih hidup dihitung di bawah mikroskop. Sel hidup terlihat sebagai bulatan bening dengan bintik biru inti sel di tengah bulatan, sedangkan sel mati terlihat sebagai bercak biru pekat yang bentuknya tidak teratur. Persentase penghambatan zat uji terhadap pertumbuhan sel leukimia L1210 dihitung sebagai berikut:
%inhibisi=(1–A/B)x100%
A: jumlahsel hidup dalam media yang mengandung zat uji. B: jumlahsel hidup dalam media yang tidak mengandung zat uji (kontrol).
Tabel 2.4. Tabel Probit
2.4 Metode Pemisahan dan Pemurnian
Prinsip dari metode pemisahan adalah perbedaan sifat fisik dan kimia dari senyawa-senyawa dalam campuran yaitu kecendrungan dari molekul untuk melarut dalam cairan (kelarutan), kecenderungan molekul untuk menguap (keatsirian), kecenderungan molekul untuk melekat pada permukaan serbuk halus (adsorpsi, penyerapan) .
2.4.1 Ekstraksi
bertingkat umunya diawali dengan pelarut yang kurang polar, dilanjutkan dengan pelarut yang lebih polar. Tingkat polaritas pelarut ditentukan dari nilai konstanta dielektrik pelarut.
2.4.2 Kromatografi
Kromatografi merupakan salah satu metode pemisahan zat terlarut oleh suatu proses migrasi diferensial dinamis dalam sistem yang terdiri dari dua fase atau lebih. Salah satu diantara fase tersebut bergerak secara berkesinambungan dalam arah tertentu dan di dalamnya zat-zat menunjukkan perbedaan mobilitas disebabkan oleh adsorbsi, partisi, kelarutan, tekanan uap, ukuran molekul atau kerapatan muatan ion. Secara umum teknik kromatografi didasarkan pada distribusi zat terlarut diantara dua fase, yaitu fase diam dan fase gerak. Fase gerak membawa zat terlarut melaui media, hingga terpisah dari zat terlarut lainnya, yang terelusi lebih awal atau lebih akhir. Umumnya zat terlarut dibawa melalui media pemisah oleh aliran suatu pelarut berbentuk cairan atau gas yang disebut eluen. Fase diam dapat bertindak sebagai penyerap, atau dapat bertindak melarutkan zat sehingga terjadi partisi antara fase diam dan fase gerak. (Gritter et al.,1991)
Berbagai jenis kromatografi yang umum digunakan antara lain Kromatografi Lapis Tipis (KLT), Kromatografi Kolom, Kromatografi Cair Kenerja Tinggi dan Kromatografi Gas-Spektroskopi Massa (KG-SM).
KLT merupakan salah satu metode pemisahan secara fisikokimia yang digunakan
secara luas untuk pemisahan dan identifikasi senyawa obat. Proses pemisahan terjadi akibat perbedaan distribusi komponen campuran di dalam
daya lekatnya, dimana zat ini digunakan sebagai adsorben universal untuk kromatografi senyawa netral, asam dan basa. Campuran yang akan dipisah, berupa larutan ditotolkan berupa bercak atau pita. Setelah itu pelat atau lapisan ditaruh di dalam bejana tertutup yang berisi larutan pengembang yang cocok (fase gerak). Pemisahan terjadi selama perambatan fase gerak, selanjutnya senyawa yang tidak berwarna harus dideteksi. Fase gerak adalah medium angkut yang terdiri atas satu atau beberapa pelarut dan bergerak di dalam fase diam karena adanya daya kapiler. Pemakian campuran pelarut dengan tingkat polaritas berbeda dapat memberikan daya pemisahan yang baik karena daya kembangnya dapat disesuaikan dengan semua jenis senyawa. Pada KLT, pemilihan fase gerak berdasarkan deret eluotropik, yaitu deret yang disusun menurut kemampuan elusi naik sebanding dengan kenaikan polaritas. KLT dapat digunakan pertama untuk mengetahui secara kualitatif, kuantitatif, atau perparatif dan kedua untuk menjajaki sistem pelarut dan sistem penyangga yang akan digunakan pada kromatografi kolom (Gritter, et al., 1991)
2.5. Metode Penentuan Struktur Kimia
Untuk menentukan struktur kimia suatu senyawa dapat digunakan metode Spektrometri. Spektrometri adalah pengukuran serapan atau emisi radiasi elektromagnetik pada panjang gelombang tertentu yang monokromatis dari suatu zat, baik dalam bentuk molekul atau atom. Spektrum biasanya diperoleh dengan melewatkan cahaya yang panjang gelombang tertentu melalui larutan encer suatu senyawa dalam pelarut yang sesuai dan tidak mengganggu penyerapan, misalnya air dan etanol (Silverstein et al.,2005). Untuk menentukan struktur kimia suatu senyawa dapat digunakan metode Spektroskopi UV-Vis, Spektrofotometri Fourier Transform-Infrared (FT-IR), Nuclear Magnetic Resonance (NMR) atau Spektrometri Resonansi Magnetik Inti (RMI) dan Mass Spectra atau Spektrometri Massa.
2.5.1 Spektrofotometri UV-Vis
Pengukuran serapan dapat dilakukan pada daerah ultraviolet (panjang gelombang 190-380 nm) atau daerah cahaya tampak (panjang gelombang 380-780 nm). Semua molekul dapat mengabsorbsi radiasi dalam daerah UV-Vis karena mengandung elektron yang dapat diekstasi ke tingkat energi yang lebih tinggi. Senyawa yang mengandung ikatan sigma (seperti pada ikatan tunggal C-C) akan tereksitasi pada panjang gelombang sangat pendek di bawah 150 nm berada di luar daerah ukur spektrofotometer, sehingga tidak akan menimbulkan serapan. Senyawa
yang memiliki elektron phi (π) (mempunyai ikatan rangkap), dan mempunyai
2.5.2 Spektrofotometri Infra Red (IR)
Daerah radiasi spektrofotometri IR berada pada bilangan gelombang 12800 – 10 cm-1 (Khopkar, 1990). Spektrofotometer Fourier-transform,adalah spektrofotometri yang dalam instrumennya tidak dipisahkan radiasinya, tetapi hampir semua panjang gelombang mencapai detektor secara bersamaan yang disebut Fourier-transform, yang digunakan untuk mengubah hasil spektrum IR menjadi khas. Pengganti monokromator adalah interferometer yang dapat memisahkan radiasi menjadi dua bagian dan menghubungkannya kembali sehingga variasi intensitas yang keluar dapat diukur sekali. Beberapa keuntungan spektrofotometer Fourier-transform
dibandingkan dengan spektrofotometer dispersive adalah menghasilkan spektrum yang lebih cepat, resolusi yang lebih baik, dapat mengukur sampel dalam jumlah yang sangat sedikit (Silverstein, et. al., 2005).
2.5.3. Spektrometri Massa
dihasilkan disertai integrasi semua puncak dan spektrum masing-masing komponen. Spektrum ini dapat memberikan informasi mengenai berat molekul, fragmentasi molekul, rumus molekul dan kemungkinan struktur molekulnya.
2.5. 4 Spektrometri Nuclear Magnetic Resonance (NMR)
Spektrometri Nuclear Magnetic Resonance (NMR) atau resonansi magnetik inti (RMI) merupakan metode yang dapat digunakan dalam mempelajari struktur molekul. Prinsip dari spektrometri RMI adalah adsorpsi radiasi elektromagnetik dengan frekuensi radio oleh inti atom. Pada kekuatan magnet konstan, untuk berbagai inti atom dan berbagai isotop dapat diamati adanya frekuensi resonansi yang berbeda. Spektrum dapat diperoleh dari senyawa yang intinya mempunyai momen magnet tidak sama dengan nol. Inti-inti atom tersebut antara lain proton (1H), inti flour (19F), isotop nitogen dan lain-lain. Inti karbon (12C) yang sangat penting dalam kimia organik tidak memiliki momen magnet sehingga studi RMI dengan karbon hanya terbatas pada isotop 13C. Pemecahan ini diakibatkan peristiwa penggabungan spin-spin (spin-spin coupling), yaitu merupakan hasil interaksi magnet dari satu inti dengan inti yang lain. Pelarut yang biasa digunakan adalah deutrokloroform (CDCl3), karbon tetraklorida (CCl4) dan deuterium oksida (D2O) (Silverstein, et al., 2005). Jenis-jenis spektrometer RMI yang memberikan informasi yang berguna dalam penentuan struktur kimia molekul organik adalah 1) RMI 1 dimensi, terdiri dari RMI proton (1H) , RMI karbon (13C), DEPT (Distortionless Enhancement by P olarization Transfer) dan 2) RMI 2 dimensi, terdiri dari COSY (Correlation Spectroscopy), HMQC (Hetero Multiple Quantum Coherence) dan HMBC (Hetero Multiple Bond Connectivity).
absorpsi yang dikenal dengan resonansi magnet. Tidak semua proton menyerap energi pada kekuatan medan magnet yang sama, karena proton-proton dilindungi dari medan magnet oleh elektron yang mengelilinginya. Makin besar densitas elektron yang mengelilingi proton maka makin besar medan magnet yang dihasilkan. Densitas elektron dipengaruhi olah ada atau tidaknya atom yang mempunyai elektronegatifitas tinggi.
Spektrum RMI karbon dan DEPT memberikan informasi jenis dan jumlah atom karbon primer (CH3), sekunder (CH2), tertier (CH) dan kuarterner (C) yang diukur berdasarkan sudut pengukuran RMI karbon. Hasil penelitian DEPT pada sudut 135° menunjukkan bahwa sinyal karbon CH3 dan CH mengarah ke atas, sedangkan CH2 mengarah ke bawah. Untuk mengetahui perbedaan CH3 dan CH dilakukan pengukuran pada sudut 90° (Siverstein et al., 2005).
Pergeseran kimia (Chemical shift, δH, δC) adalah parameter yang digunakan pada RMI proton dan RMI karbon yang mempunyai karakteristik untuk posisi proton dan
karbon di dalam struktur kimia. Pergeseran kimia untuk proton (δH) berkisar antara 0
-10 ppm dan pergeseran kimia untuk karbon (δC) berkisar antara 0 – 200 ppm. Spektrum RMI 2 dimensi HMQC (Hetero Multiple Quantum Connectivity)