52
HIDROLISIS ENZIMATIK SELULOSA DARI AMPAS SAGU MENGGUNAKAN CAMPURAN
SELULASE DARI Trichoderma reesei DAN Aspergillus niger
Rika Julfana Sutarno1*, Titin Anita Zaharah1, Nora Idiawati1 1
Program Studi Kimia, Fakultas MIPA, Universitas Tanjungpura, Jl. Prof. Dr. H. Hadari Nawawi
*email : [email protected] ABSTRAK
Hidrolisis enzimatik selulosa dari ampas sagu menggunakan campuran selulase dari Trichoderma reesei dan Aspergillus niger telah dilakukan. Penelitian ini bertujuan untuk mengkaji pengaruh perbandingan campuran enzim, pH, dan waktu hidrolisis untuk menghasilkan konsentrasi glukosa secara maksimal. Hidrolisis dilakukan menggunakan ekstrak selulase kasar dari Trichoderma reesei dan Aspergillus niger dengan perbandingan campuran 1:0, 0:1, 1:1, 2:1, dan 1:2 pada variasi pH 4, 5, dan 6 dengan waktu hidrolisis selama 2, 4, 6, dan 8 jam. Hasilnya menunjukkan bahwa campuran selulase dari Trichoderma reesei dan Aspergillus niger dapat memperbaiki komposisi dari kompleks enzim selulase sehingga proses hidrolisis menghasilkan konsentrasi glukosa yang lebih tinggi dibandingkan hidrolisis yang menggunakan enzim tunggal saja. Pada penelitian ini hidrolisis selulosa dari ampas sagu menggunakan campuran selulase Trichoderma reesei dan Aspergillus niger 2:1 pada pH 5 dengan waktu hidrolisis 8 jam menghasilkan konsentrasi glukosa paling banyak, yaitu sebesar 30,884 mg/L.
Kata kunci: Sagu, A.niger, T.reesei, hidrolisis
PENDAHULUAN
Ampas sagu merupakan limbah dari empulur sagu yang telah diambil patinya. Kandungan pati sagu sebesar 18,5% dan sisanya 81,5% merupakan ampas sagu yang memiliki kandungan selulosa sebesar 20% dan lignin 21% (Kiat, 2006). Kandungan selulosa pada ampas sagu dapat dimanfaatkan untuk memproduksi glukosa melalui hidrolisis menggunakan enzim selulase.
Enzim selulase adalah campuran beberapa enzim yaitu endoglukanase, eksoglukanase dan β-glukosidase. Fungi berfilamen seperti
Tricoderma dan Aspergillus adalah penghasil selulasesecara komersial (Ul-Haq, et al., 2005).
Hidrolisis enzimatis memiliki beberapa keuntungan dibandingkan hidrolisis asam. Pada hidrolisis enzimatis tidak terjadi degradasi gula hasil hidrolisis, dapat berlangsung pada suhu rendah, dan memberikan hasil yang tinggi (Taherzadeh dan Karimi, 2007).
Aspergillus niger (A.niger) merupakan salah satu jamur yang lazim digunakan untuk menghidrolisis selulosa. Mikroorganisme ini menghasilkan β-glukosidase tinggi akan tetapi
endo-β-1,4-glukanase dan ekso-β-1,4
glukanasenya rendah (Juhasz, et al., 2003).
Trichoderma reesei (T.reesei)
menghasilkan endoglukanase dan
eksoglukanase sampai 80% tetapi
β-glukosidasenya lebih rendah sehingga produk utama hidrolisisnya bukan glukosa melainkan selobiosa (Ahmed dan Vermette, 2008) yang
merupakan inhibitor kuat terhadap
eksoglukanase. Oleh karena itu perlu adanya penambahan β-glukosidase dari luar untuk mempercepat konversi selobiosa menjadi glukosa sehingga efek inhibisinya dapat
dihilangkan, yaitu dengan cara
mengkombinasikan enzim selulase dari T.ressei
dan A.niger.
Penelitian hidrolisis selulosa secara enzimatik telah banyak dilakukan menggunakan enzim yang dihasilkan dari 1 jenis jamur namun konsentrasi glukosa yang dihasilkan masih belum cukup tinggi (Anwar, dkk., 2010). Hidrolisis menggunakan campuran dari 2 jenis jamur telah dilakukan sebelumnya oleh Juhasz et al (2003) yang meneliti produksi β-glukosidase dari limbah kertas menggunakan campuran kultur dari
T.ressei RUT C30 dan A.niger BKMF 1305. Tahun 2005, Ul-Haq et al melakukan penelitian terhadap campuran kultur dari A.niger dan
T.viride pada substrat kapas. Hasil kedua penelitian tersebut menunjukkan bahwa kultur campuran dari 2 jenis jamur tersebut dapat
meningkatkan aktifitas enzim selulase
dibandingkan dengan monokultur.
Sanjaya dan Adrianti (2010) serta Anwar dkk (2010) meneliti hidrolisis jerami padi menggunakan campuran selulase kasar dari
T.reesei dan A.niger. Anwar dkk (2010) melaporkan bahwa campuran selulase kasar dari
T.reesei dan A.niger 2 kali lebih efektif dalam menghidrolisis jerami padi menjadi glukosa dibandingkan dengan enzim selulase A.niger. komersial dari Fluka Biochemika. Berdasarkan penelitian tersebut maka dilakukan hidrolisis
53
campuran selulase kasar dari T.reesei dan
A.niger dengan mengkaji pengaruh perbandingan campuran enzim selulase dari
T.ressei dan A.niger, pH, dan waktu pada proses hidrolisis untuk menghasilkan glukosa secara maksimal.
METODOLOGI PENELITIAN
Bahan
Bahan-bahan yang digunakan yaitu agar-agar, akuades, alkohol 70%, alumunium foil, amonium sulfat ((NH4)2SO4), ampas sagu, asam klorida (HCl), glukosa (C6H12O6), kalium dihidrogen fosfat (KH2PO4), kalsium klorida monohidrat (CaCl2.H2O), kentang, kertas saring whatman no.1, magnesium sulfat heptahidrat (MgSO4.7H2O), natrium hidroksida (NaOH), natrium sitrat (Na3C6H5O7), tween-80, urea (CO(NH2)2), dan wrapping plastic.
Mikroorganisme yang digunakan yaitu
A.niger dan T.reesei yang diperoleh dari Institut Pertanian Bogor.
Peralatan
Peralatan yang digunakan yaitu autoclave, bulb, centrifuge, hotplate, kuvet, laminar, neraca analitis, oven, peralatan gelas, pH-universal, pipet ukur, rak tabung reaksi, spatula, spektrofotometer UV-Vis, tabung reaksi, dan termometer.
Cara Kerja
Preparasi Sampel
Ampas sagu diperoleh dari daerah Sungai Ambawang, Kabupaten Kubu Raya. Ampas sagu diperas dan dikeringkan pada suhu 1050C selama 6 jam. Setelah kering ampas sagu dihaluskan dan diayak dengan ukuran 40 mesh.
Delignifikasi Sampel
Sebanyak 60 gr ampas sagu ditambahkan larutan NaOH 1% dan diaduk menggunakan
shaker selama 2 jam pada kecepatan 150 rpm. Campuran tersebut didiamkan selama 24 jam, kemudian disaring dan dibilas dengan akuades sampai pH 7. Residu berupa ampas sagu dikeringkan pada suhu 1050C selama 6 jam (Sukadarti, dkk., 2010).
Perbanyakan A.niger dan T.reesei
Pembiakkan T.reesei menggunakan media PDA (Potato Dextrose Agar). Media PDA dituangkan pada cawan petri steril. Ditambahkan satu ose biakkan T.reesei dan diinkubasi pada suhu ruang selama 1 minggu. Hal yang sama dilakukan untuk biakkan A.niger.
Pembuatan Larutan Nutrisi
Dilarutkan urea (3 g/L), (NH4)2SO4 (10g/L), KH2PO4 (3 g/L), MgSO4.7H2O (0,5 g/L), CaCl.H2O (0,5 g/L) dengan akuades (Singhania,
et al., 2006). Diukur pH awal dan diatur hingga pH 5 untuk A.niger (Harfinda, 2011) maupun
T.reesei (Sukadarti, dkk., 2010).
Produksi Enzim Selulase
Sebanyak 5 g ampas sagu ditambahkan 25 mL larutan nutrisi. Campuran (media) tersebut ditutup dan disterilisasi. Masing-masing bibit
A.niger dan T.reesei diinokulasikan pada media secara terpisah. Inkubasi T.reesei dilakukan selama 6 hari dan A.niger selama 8 hari pada suhu ruang (Anwar, dkk., 2010).
Ekstraksi Enzim
Enzim dipanen menggunakan 100 mL larutan 0,1% tween 80, diaduk pada 150 rpm selama 120 menit pada suhu ruang, kemudian disentrifugasi pada 3000 rpm selama 10 menit. Supernatan yang diperoleh digunakan sebagai ekstrak enzim kasar (Szendefy, et al., 2006).
Uji Aktivitas Enzim dengan Metode Fenol-Sulfat
Sebanyak 1 ml buffer Na-sitrat 0,05 M pH 4,8 dan kertas saring whatman no 1. ukuran 1x6 cm dimasukkan ke dalam tabung reaksi, dipanaskan pada suhu 50oC selama beberapa saat. Masing-masing 0,5 ml enzim kasar dari
A.niger dan T.reesei dimasukkan ke dalam tabung reaksi, diinkubasi pada suhu 50oC selama 1 jam, kemudian kertas saring diambil dari tabung reaksi (Adney dan Baker, 1996). Selanjutnya ditambahkan 0,5 ml larutan fenol 5% dan 2,5 ml H2SO4 pekat kemudian diaduk menggunakan vortex. Dilakukan pengenceran dengan penambahan buffer Na-sitrat dan diukur absorbansinya (Dubois, et al., 1956). Aktivitas enzim selulase dihitung dengan persamaan (Kamila, 2003) :
Aktivitas enzim selulase (U/mL)
Keterangan :
G = glukosa yang dihasilkan Fp = faktor pengenceran t = waktu inkubasi
Hidrolisis Sampel
Enzim selulase kasar dari T.ressei dan
A.niger dicampur berdasarkan perbandingan yg ditentukan (1:0, 0:1, 1:1, 2:1, 1:2). Campuran enzim dimasukkan ke dalam Erlenmeyer berisi 5 gr ampas sagu dan ditambahkan aquades hingga volumenya 150 mL, lalu diaduk pada 160
54
rpm beberapa saat, kemudian dipanaskan hingga suhu 40°C pada pH 4, 5, 6 selama 2, 4, 6, 8 jam (Sanjaya dan Adrianti, 2010). Pengaturan pH dilakukan dengan penambahan 0,1 M NaOH dan 0,1 M HCl.
Uji Kandungan Gula Pereduksi dengan Metode Samogyi-Nelson (AOAC, 1990)
Pengujian kandungan gula pereduksi dilakukan dengan metode Somogyi-Nelson AOAC, 1990.
HASIL DAN PEMBAHASAN
Delignifikasi Sampel
Preparasi mekanik atau kimiawi pada substrat diperlukan untuk mempermudah kontak antara enzim dengan substrat (Sun, 2002). Menurut Resita (2006) pengecilan ukuran sampel diduga menyebabkan terputusnya rantai polimer yang panjang menjadi rantai polimer yang lebih
pendek dan meningkatkan daerah amorf
sehingga menurunkan derajat kristalinitas. Delignifikasi dilakukan dengan NaOH karena larutan ini dapat merusak struktur lignin pada bagian kristalin dan amorf serta memisahkan sebagian hemiselulosa (Gunam dan Antara, 1999). Menurut Hespell (1998) ekstraksi hemiselulosa dapat menggunakan pelarut seperti NaOH, NH4OH dan KOH. Di antara ketiga pelarut tersebut yang paling baik digunakan adalah NaOH. Hemiselulosa memiliki struktur amorf sehingga penggunaan NaOH
dapat menghilangkan lignin sekaligus
mengekstraksi hemiselulosa.
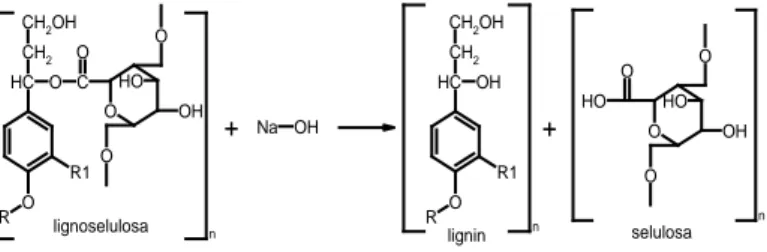
Gambar 1. Pemutusan ikatan antara lignin dan selulosa oleh NaOH (Fengel dan Wegener, 1995)
Mekanisme delignifikasi oleh larutan NaOH dapat dilihat pada Gambar 1. NaOHakan masuk dan memutuskan ikatan dari struktur dasar lignin dan berikatan dengan lignin membentuk natrium fenolat. Garam fenolat ini bersifat polar sehingga mudah larut dalam pelarut polar. Lignin yang terlarut ditandai dengan warna hitam pada larutan yang disebut lindi hitam (black liquor).
Lindi hitam tersebut menunjukkan lapisan lignin telah terpisah dari selulosa. Kondisi ini akan meningkatkan produktivitas mikroorganisme dalam memproduksi selulase dan efektivitas hidrolisis menjadi lebih tinggi.
Produksi Enzim Selulase
Tahap produksi enzim merupakan tahap dimana enzim selulase dihasilkan melalui proses fermentasi ampas sagu sebagai akibat dari metabolisme jamur A.niger dan T.reesei. Enzim selulase merupakan enzim ekstraseluler yang diproduksi di dalam sel dan dikeluarkan dari sel untuk mencerna selulosa.
Pada proses fermentasi dilakukan
pemberian larutan nutrisi untuk melengkapi nutrisi yang dapat merangsang pertumbuhan jamur. Nutrisi ini berupa karbon, nitrogen, hidrogen dan mineral seperti fosfor, sulfur, kalsium, kalium dan magnesium. Sumber karbon yang digunakan berupa selulosa yang berasal dari ampas sagu. Karbon berfungsi sebagai unsur utama dalam pembentukan sel. Nitrogen berfungsi dalam pembentukan asam amino, DNA, RNA dan ATP. Hidrogen dan oksigen berfungsi dalam proses pembentukan sel. Fosfor
berfungsi sebagai kofaktor enzim dan
pembentukan asam nukleat. Sulfur, kalium, dan kalsium berfungsi sebagai kofaktor enzim. Magnesium berfungsi untuk menjaga kestabilan ribosom, membran sel dan asam nukleat, sebagai kofaktor enzim, dan sebagai komponen dari klorofil (Gandjar, 2006).
Enzim selulase diekstraksi menggunakan 100 ml larutan tween 80 0,1% (Szendefy, et al., 2006). Tween 80 (polioksi etilen sorbitan mono-oleat) merupakan surfaktan non ionik. Sifatnya sebagai surfaktan dapat menurunkan tegangan permukaan antara air dan spora karena spora dari A.niger dan T.reesei tidak larut dalam air. (Jayashree dan Vasudevan, 2009). Tween 80 dapat meningkatkan permeabilitas dinding sel atau kemampuan keluar masuknya air dan larutan melalui dinding sel sehingga proses keluarnya enzim dari dinding sel menjadi lebih mudah. Selain itu penggunaan tween 80 tidak mempengaruhi pH dari ekstrak enzim kasar karena bersifat non ionik.
Pengaruh Perbandingan Campuran Enzim Terhadap Konsentrasi Glukosa
Glukosa yang dihasilkan melalui proses hidrolisis merupakan hasil kerja sinergis sekelompok enzim selulolitik. Sistem enzim selulolitik terdiri dari tiga kelompok utama yaitu
endoglukanase, eksoglukanase, dan
β-glukosidase (Howard, et al., 2003). Kerja sinergis
O O OH O H O C H CH2 CH2OH O C O R1 O R n + Na OH C H CH2 CH2OH R1 O R OH n + lignin lignoselulosa O O OH O H O O O H n selulosa
55
dari kompleks enzim selulase dapat dilihat pada Gambar 2.
Gambar 2. Skema hidrolisis enzimatik selulosa (Lynd, et al., 2002).
Enzim endoglukanase menghidrolisis secara acak pada bagian amorf serat selulosa sehingga menghasilkan oligosakarida dengan panjang berbeda-beda dan terbentuknya unjung rantai baru selulosa (Howard, et al., 2003). Enzim eksoglukanase bekerja terhadap ujung-ujung rantai polisakarida tersebut dan menghasilkan
selobiosa yang merupakan disakarida.
Selanjutnya enzim β-glukosidase memecah selobiosa menjadi 2 molekul glukosa yang merupakan produk utama hidrolisis selulosa (Lynd, et al., 2002).
Grafik pada Gambar 3 menunjukkan campuran 2:1 dari ekstrak enzim kasar T.reesei
dan A.niger pada pH 4, 5, dan 6 dengan waktu hidrolisis 8 jam menghasilkan konsentrasi glukosa yang lebih tinggi dibandingkan dengan hidrolisis menggunakan campuran enzim kasar
lainnya. Hidrolisis secara enzimatis
menggunakan campuran enzim dari T.reesei dan
A.niger pada substrat jerami padi juga menghasilkan konsentrasi glukosa paling tinggi
pada campuran 2:1 (Anwar, dkk., 2010; Sanjaya dan Adrianti, 2010).
Gambar 3. Grafik pengaruh perbandingan campuran enzim terhadap konsentrasi glukosa menggunakan campuran selulase T.reesei dan
A.niger 1:0, 0:1, 1:1, 2:1, 1:2 pada pH 4, 5 dan 6.
Pengaruh pH Terhadap Konsentrasi Glukosa
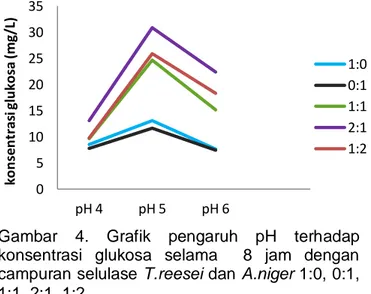
Grafik pada Gambar 4 menunjukkan hidrolisis enzimatik selulosa dari ampas sagu menggunakan campuran selulase dari T.reesei
dan A.niger pada campuran 1:0, 0:1, 1:1, 2:1, 1:2 selama 8 jam menghasilkan konsentrasi glukosa optimum pada pH 5.
Gambar 4. Grafik pengaruh pH terhadap konsentrasi glukosa selama 8 jam dengan campuran selulase T.reesei dan A.niger 1:0, 0:1, 1:1, 2:1, 1:2.
Konsentrasi glukosa yang lebih rendah pada pH 4 dan menurun pada pH 6 dikarenakan enzim selulase yang bekerja pada pH selain pH optimum akan mengalami perubahan struktur atau muatan asam amino yang merupakan sisi aktif yang berfungsi dalam pengikatan substrat. Hal ini mengakibatkan terganggunya interaksi antara sisi aktif enzim selulase dengan substrat selulosa sehingga konsentrasi glukosa yang dihasilkan menjadi lebih rendah. Penelitian Anwar dkk (2010) terhadap hidrolisis jerami padi menggunakan campuran enzim selulase dari
0 5 10 15 20 25 30 35 1:0 0:1 1:1 2:1 1:2 k o n se n tra si gl u ko sa m g/L pH 4 pH 5 pH 6 0 5 10 15 20 25 30 35 pH 4 pH 5 pH 6 ko n se n tra si gl u ko sa (m g/L ) 1:0 0:1 1:1 2:1 1:2
56 T.reesei dan A.niger juga meningkat dari pH 4 sampai pH 5,5 dan mengalami penurunan pada pH 6.
Pengaruh Waktu Hidrolisis Terhadap
Konsentrasi Glukosa
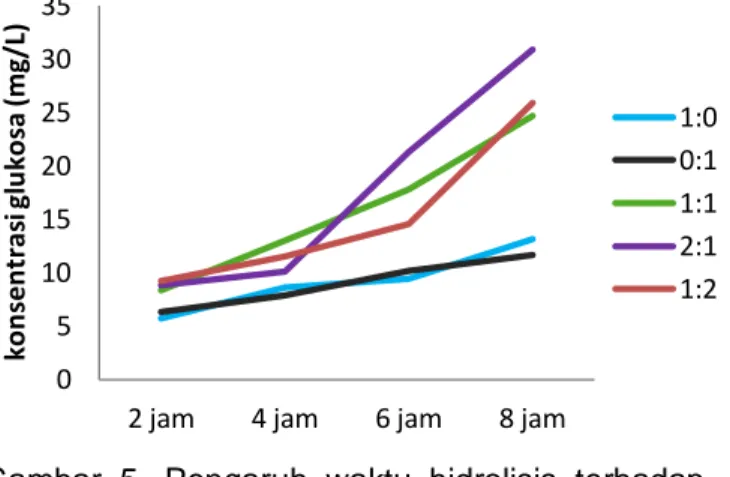
Profil pengaruh waktu hidrolis terhadap konsentrasi glukosa disajikan oleh Grafik pada Gambar 5.
Gambar 5. Pengaruh waktu hidrolisis terhadap konsentrasi glukosa pada pH 5 dengan campuran selulase T.reesei dan A.niger 1:0, 0:1, 1:1, 2:1, 1:2.
Hidrolisis enzimatik selulosa dari ampas sagu menggunakan campuran selulase dari
T.reesei dan A.niger 1:0, 0:1, 1:1, 2:1, 1:2 pada pH 5 menghasilkan konsentrasi glukosa paling tinggi pada waktu hidrolisis 8 jam. Hasil ini tidak jauh berbeda dengan penelitian Sanjaya dan Adrianti (2010) terhadap hidrolisis jerami padi menggunakan campuran selulase dari T.reesei dan A.niger yang menghasilkan konsentrasi glukosa tertinggi pada waktu hidrolisis 7 jam.
Interaksi antara enzim dengan substrat yang semakin lama menyebabkan semakin banyak glukosa yang terbentuk. Akan tetapi pada waktu hidrolisis tertentu konsentrasi glukosa akan mengalami penurunan. Penurunan ini disebabkan oleh adanya akumulasi produk yang telah terbentuk sebelumnya dan meyebabkan penghambatan bagi enzim selulase. Inhibitor enzim selulase berupa produk dari hidrolisis selulosa yaitu glukosa dan selobiosa. Selobiosa menghambat enzim eksoglukanase sedangkan glukosa menghambat enzim β-glukosidase (Ambriyanto, 2010).
SIMPULAN
Berdasarkan penelitian yang telah dilakukan dapat disimpulkan bahwa hidrolisis
selulosa dari ampas sagu menggunakan
campuran selulase dari T.reesei dan A.niger
pada penelitian ini menghasilkan konsentrasi glukosa terbanyak dengan kondisi pH 5, waktu hidrolisis 8 jam, dan campuran enzim 2:1, yaitu sebesar 30,884 mg/L.
DAFTAR PUSTAKA
Adney, B. And Baker J., 1996, Measurement of Cellulose Activities, CO: National Renewable Energy Laboratory, report.nf NREL/TP-501-42628.
Ahmed, A. dan P. Vermette, 2008, Culture-based Strategies to Enhance Cellulase Enzyme Production from Trichoderma reesei RUT-C30 in Bioreactor Culture Conditions, Biochemical Engineering Journal 40, 399–407.
Ambriyanto, K. S., 2010, Isolasi dan Karakterisasi Bakteri Aerob Pendegradasi Selulosa dari Serasah Daun Rumput Gajah (Pennisetum purpureum schaum), Institut Teknologi Sepuluh Nopember (Skripsi).
Anwar, N., A. Widjaja, dan S. Winardi, 2010, Peningkatan Unjuk Kerja Hidrolisis Enzimatik Jerami Padi Menggunakan
Campuran Selulase Kasar dari
Trichoderma ressei dan Aspergillus niger, Institut Teknologi Sepuluh November,
Makara, Sains, 14(2): 113-116.
AOAC. 1990. Official Methods of Analisis. Association of Official Analitycal, Penerbit UGM, Yogyakarta.
Badan Penelitian dan Pengembangan Pertanian,
2010, Warta Penelitian dan
Pengembangan Tanaman Industri, 16(2): 1-35, ISSN 0853-8204.
Dubois, M., Gilles, K.A., Hamilton, J.K., Rebers, P.A., and Smith F., 1956, Colorimetric Method for Determination of Sugars and Related Substances”, 28(3): 350-356. Fengel, D., dan Wegener G., 1995. Kayu: Kimia,
Ultra Struktur dan Reaksi-Reaksi, Gajah Mada Press. Yogyakarta.
Ganjar, I., 2006, Mikrobiologi Dasar dan Terapan, Yayasan Obor Indonesia, Jakarta.
Gunam, I.B.W., dan Antara, N.S., 1999, Study on Sodium Hydroxide Treatment Of Corn Stalk to Increase Its Cellulose Saccharification Enzymatically by Using Culture Filtrate of Trichoderma reesei. Gitayana, Agric. Technol. J, 5 (1): 34-38 Harfinda, E.M., 2011, Pengaruh Kadar Air, pH,
dan Waktu Fermentasi Tehadap Produksi Enzim Selulase oleh Aspergillus niger 0 5 10 15 20 25 30 35
2 jam 4 jam 6 jam 8 jam
ko n sen tr a si g lu ko sa (mg /L ) 1:0 0:1 1:1 2:1 1:2
57
Pada Ampas Sagu, Universitas
Tanjungpura (Skripsi).
Hespell, B., 1998, Extraction and
Characterization of Hemicellulose from Corn Fiber Produced by Corn Wet-Milling Processes, J. Agric. and Food Chem, 46 : 2615-2619.
Howard, R.L.; E. Abotsi; J.E.L. van Rensburg; and S. Howard, 2003, Lignocellulose Biotechnology: Issues of Bioconversion
and Enzyme Production, Afr. J.
Biotechnol, 2(12): 602−619.
Jayashree, R. dan Vasudevan N., 2009, Effect Of Tween 80 and Moisture Regimes on
Endosulfan Degradation by
Pseudomonas Aeruginosa, Applied
Ecology and Environmental Research,
7(10): 35-44
Juhasz, T.; K. Kozma; Z. Szengyel; and K.
Reczey, 2003, Production of
β-Glucosidase in Mixed Culture of
Aspergillus niger BKMF 1305 and
Trichoderma reesei RUT C30, Food Technol, J. Biotechnol. 41 (1) 49–53
Kamila, L., 2003, Pencirian Selulotik Isolat Khamir Rhodotorula sp. dari Tanah Hutan
Taman Nasional Gunung Halimun,
Jurusan Kimia, IPB (Skripsi)
Kiat, I.J., 2006, Preparation and Characterization of Carboxymetyl Sago Waste and its Hydrogel, Universiti Putra Malaysia, (Tesis).
Lynd, L.R., P.J. Weimer, W.H. van Zyl WH and I. S. Pretorius, 2002, Microbial Cellulose
Utilization: Fundamentals and
Biotechnology. Microbiol. Mol. Biol. Rev. 66(3):506-577.
Resita, E.T., 2006, Produksi Selo-Oligosakarida dari Fraksi Selulosa Tongkol Jagung Oleh Selulase Trichoderma Viride, Institut Pertanian Bogor (Skripsi).
Sanjaya, W. dan S. Adrianti, 2010, Optimasi Hidrolisis Enzimatik Jerami Padi Menjadi Glukosa Untuk Bahan Baku Biofuel Menggunakan Selulase dari Trichoderma ressei dan Aspergillus niger, Institut Teknologi Sepuluh November, (Skripsi). Singhania, R.R., Sukumaran, R.K., Pillai, A.,
Prema, P., Szakacs, G., and Pandey, A., 2006, Solid State Fermentation of Lignocellulosic Substrat for Cellulase Production by Trichoderma reesei NRRL 11460, Indian J. Biotechnol, 5: 332-336. Sukadarti, S.; S.D. Kholisoh; Heri Prasetyo; W.P.
Santoso; Tri Mursini, 2010, Produksi Gula Reduksi Dari Sabut Kelapa Menggunakan Jamur Trichoderma reesei, Prosiding
Seminar Nasional Teknik Kimia, ISSN 1693-4393.
Sun, Y., 2002, Enzymatic Hydrolisis of Rye Straw
and Bermudagras for Ethanol
Production”, Departement of Biological and Agricultural Enginering, Nort Carolina State University, North Carolina, (Disertasi).
Szendefy, J., Szakacs, G., and Christopher, L.,
2006, Potensial of Solid State
Fermentation Enzymes of Aspergillus oryzae in Biobleaching of Paper Pulp,
Enzyme and Microbial Technology Jr., 39: 1354-1360.
Taherzadeh, M.J. dan Karimi, K., Acid-based Hydrolysis Processes for Ethanol from Lignocellulosic Materials: a review, 2007,
Bioresources 2(3), pp. 472-499.
Ul-Haq, I., Javed, M. M., Khan, T. S., and Siddiq, Z., 2005, Cotton Saccharifying Activity of Cellulases Produced by Co-culture of
Aspergillus Niger and Trichoderma Viride,
Research Journal of Agriculture and Biological Sciences, 1(3): 241-245.