1
BAB I PENDAHULUAN A. Latar Belakang
Tanaman buah merah (Pandanus Conoideus Lam) adalah tanaman khas atau endemik yang tumbuh di pulau Papua. Minyak buah merah (MBM) dianggap sebagai minyak fungsional karena selain dapat dikonsumsi sebagai diet juga dapat digunakan sebagai agen pencegah berbagai penyakit, diantaranya sebagai antikanker (Munim et al., 2006). Buah merah mengandung asam oleat dan linoleat serta betakaroten dan tokoferol dalam jumlah tinggi (Budi & Paimin, 2004). Selain itu, MBM juga mengandung vitamin dan mineral esensial yang cukup lengkap.
Autentikasi MBM menjadi sangat penting karena harga MBM yang terbilang mahal. Harga jual MBM di pasaran berkisar antara Rp 300.000,- sampai dengan Rp 1.000.000,- per liter (Yuhono dan Pribadi, 2007). Oleh karena itu, minyak ini sangat berpotensi untuk dipalsukan dengan minyak lain yang harganya lebih murah seperti minyak jagung, minyak kedelai, kelapa sawit, minyak wijen, dan minyak nabati lainnya untuk memperoleh keuntungan yang lebih tinggi. Penentuan keaslian suatu minyak merupakan isu yang menarik tidak hanya bagi produsen minyak tetapi juga bagi konsumen karena terkait dengan kesehatan konsumen, dan dalam banyak hal terkait dengan larangan oleh agama tertentu seperti pemalsuan dengan lemak babi (Rohman dan Che Man, 2008).
Beberapa metode fisika-kimia telah dikembangkan untuk analisis minyak antara lain: electronic nose, differential scanning calorimetry (DSC), kromatografi, metode-metode spektroskopik, dan metode kimia basah (Che Man et al., 2010). Akan tetapi, metode-metode ini seringkali memerlukan waktu yang lama, menggunakan banyak pelarut, dan kurang efektif. Oleh karena itu, dibutuhkan metode yang mampu mendeteksi adanya pemalsuan minyak secara cepat, sederhana, dan terpercaya.
Spektroskopi Inframerah Fourier Transform (FTIR) dikenal sebagai teknik sidik jari (finger print) karena tidak ada 2 senyawa yang memiliki jumlah puncak atau intensitas absorbansi yang sama. Spektroskopi FTIR merupakan teknik analisis yang peka, reliabel, membutuhkan sampel yang sedikit, dan operasionalisasinya mudah. Digabungkan dengan kemajuan komputer dan perangkat lunak ―kemometrika‖, spektroskopi FTIR dapat memberikan informasi kualitatif dan kuantitatif. Spektroskopi FTIR yang dikombinasikan dengan kemometrika telah digunakan untuk mendeteksi adanya virgin coconut oil (VCO) dalam campuran biner dengan minyak zaitun dan minyak sawit (Rohman et al., 2010), lemak babi dalam minyak ikan (Rohman and Che Man, 2009), minyak sawit dalam VCO (Rohman dan Che Man, 2009), minyak jagung dan minyak bunga matahari dalam VCO (Rohman dan Che Man, 2011), serta minyak wijen dalam minyak buah merah (Martsasi et al., 2012). Namun, melalui studi literatur belum ada yang menjelaskan penggunaan spektroskopi FTIR untuk autentikasi MBM dalam campuran dengan minyak jagung dan kedelai. Dalam penelitian ini,
kombinasi spektroskopi FTIR dan kemometrika digunakan untuk autentikasi minyak merah dalam campuran dengan minyak jagung dan kedelai.
B. Rumusan Masalah
Minyak buah merah (MBM) tergolong minyak yang baru di pasaran. Minyak ini memiliki harga hingga 10-15 kali lebih mahal dibanding minyak nabati pada umumnya. Akibatnya, banyak produsen yang melakukan pemalsuan MBM dengan menambahkan minyak yang lebih murah sebagai campuran untuk memperoleh MBM oplosan. Berdasarkan latar belakang permasalahan diatas, permasalahan yang diangkat dalam penelitian ini adalah sebagai berikut:
1. Apakah spektroskopi FTIR dihubungkan dengan kemometrika dapat digunakan untuk autentikasi minyak buah merah dalam campuran dengan minyak jagung dan minyak kedelai?
2. Bagaimana optimasi spektrofotometri FTIR dan kalibrasi multivariat untuk menghasilkan model yang sesuai untuk autentikasi minyak buah merah dalam campuran dengan minyak jagung dan minyak kedelai?
C. Pentingnya Penelitian Dilakukan
Sebagai salah satu minyak fungsional yang berkhasiat untuk mencegah penyakit, autentikasi MBM dengan minyak lain yang harganya lebih rendah merupakan suatu keniscayaan. Deteksi adanya minyak pemalsu dengan metode-metode standar seperti kromatografi dirasakan terlalu lama dan membutuhkan preparasi sampel yang cukup rumit. Oleh karena itu dibutuhkan metode instrumen
yang cepat, reliabel, serta reprodusibel. Kombinasi metode spektroskopi inframerah (FTIR) dengan kemometrika diharapkan mampu menganalisis adanya campuran pemalsu dalam minyak buah merah secara cepat dan terpercaya. Hal ini dilakukan untuk melindungi konsumen karena terkait dengan kesehatan konsumen.
Hasil penelitian ini dapat dimanfaatkan oleh industri minyak dan lemak maupun pemerintah untuk menganalisis keaslian suatu minyak. Hasil penelitian ini juga dapat dimanfaatkan sebagai bahan acuan dalam analisis yang sama oleh peneliti lain.
D. Tujuan Penelitian
Tujuan penelitian ini adalah diperolehnya metode analisis yang cepat dan akurat untuk mendeteksi adanya minyak kedelai dan minyak jagung dalam MBM. Secara khusus, tujuan penelitian ini adalah:
1. Mengembangkan metode spektroskopi FTIR yang dikombinasikan dengan kemometrika untuk autentikasi MBM dalam campuran dengan minyak jagung dan minyak kedelai.
2. Melakukan optimasi spektroskopi FTIR dan kalibrasi multivariat untuk menghasilkan model yang sesuai untuk autentikasi MBM dalam campuran dengan minyak jagung dan minyak kedelai.
E. Tinjauan Pustaka 1. Minyak dan Lemak
Asam lemak merupakan suatu asam karboksilat berantai tinggi, semakin panjang rantai C penyusunnya, semakin tinggi titik didihnya dan semakin sukar larut dalam pelarut polar. Asam lemak tidak lain adalah asam alkanoat atau asam karboksilat berderajat tinggi (rantai C lebih dari 6). Asam lemak bersama dengan gliserol merupakan senyawa penyusun utama minyak nabati dan merupakan bahan baku untuk semua lemak pada makhluk hidup. Secara alami, asam lemak bisa terikat sebagai gliserida maupun berada dalam bentuk bebas karena lemak yang terhidrolisis (Fessenden dan Fessenden, 1999).
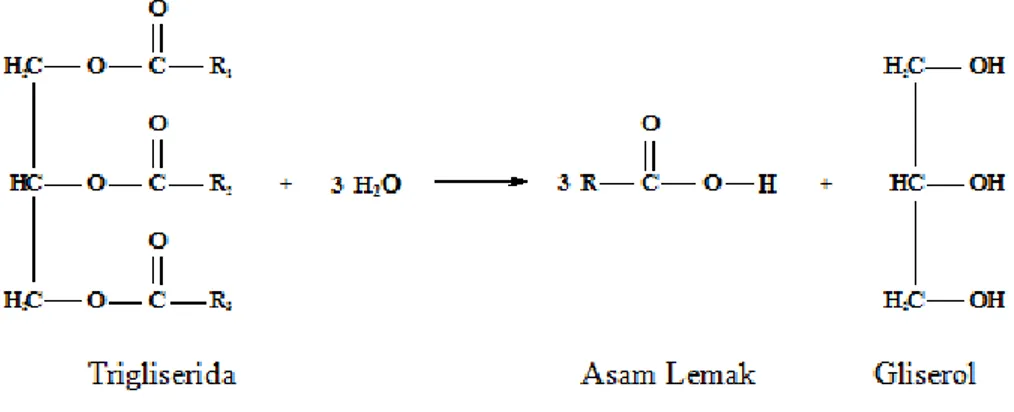
Komponen minyak umumnya terdiri atas trigliserida yang memiliki asam lemak jenuh dan asam-asam lemak tak jenuh, dengan satu atau lebih ikatan rangkap di antara atom-atom karbonnya. Trigliserida merupakan senyawa hasil kondensasi molekul gliserol dengan tiga molekul asam lemak. Reaksi hidrolisis trigliserida dapat dilihat dalam persamaan berikut:
Menurut rantainya, asam lemak dibagi menjadi tiga yaitu: asam lemak rantai pendek (Short Chain Fatty Acids/SCFA), asam lemak rantai sedang (Medium Chain Fatty Acids/MCFA), dan asam lemak rantai panjang (Long Chain Fatty Acids/LCFA). SCFA merupakan asam lemak dengan atom C kurang dari 8 dan terdapat dalam jumlah yang sedikit di alam, contohnya pada lemak susu. MCFA yaitu asam lemak dengan atom C8-C12. Sekitar 92 % asam lemak yang
terkandung dalam minyak kelapa adalah asam lemak golongan rantai karbon sedang (MCFA) yang terdiri dari 12 atom karbon jenuh. LCFA adalah asam lemak dengan atom C lebih dari 12. Jenis asam lemak yang terdapat dalam minyak nabati terdiri dari 18 atau lebih atom karbon, dan sebagian besar adalah golongan asam lemak rantai panjang (LCFA) yang umumnya mempunyai ikatan ganda (St-Onge dan Jones, 2002).
Berdasarkan ada tidaknya ikatan rangkap pada atom C, LCFA dapat dibedakan menjadi asam lemak jenuh (Saturated Fatty Acids/SFA) dan asam lemak tak jenuh (Unsaturated Fatty Acids/UFA) yang terdiri dari asam lemak tak jenuh tunggal (Monounsaturated Fatty Acids/MUFA) dan asam lemak tak jenuh poliena (Polyunsaturated Fatty Acids/PUFA). MUFA adalah asam lemak yang mempunyai satu ikatan rangkap, contohnya asam oleat. PUFA adalah asam lemak yang memiliki dua sampai enam ikatan rangkap, contohnya asam linoleat dan asam linolenat (Wuryastuti, 1991).
2. Buah Merah (Pandanus conoideus Lam.)
Buah merah (Pandanus conoideus Lam) termasuk tanaman endemik yang tumbuh liar di wilayah Maluku dan Papua (Bourke, 2005). P. conoideus Lam termasuk tanaman keluarga pandan-pandanan (pandanus), pohon menyerupai pandan, tinggi tanaman mencapai 16 m dengan tinggi batang bebas cabang setinggi 5-8 m yang diperkokoh akar-akar tunjang pada batang sebelah bawah.
Gambar 2. Buah merah (Wijaya dan Pohan, 2009).
Buah merah berbentuk lonjong dengan kuncup tertutup buah, panjang buah mencapai 96-102 cm, diameter 15-20 cm, dan bobot 7-8 kg. Saat matang buahnya berwarna merah maroon terang, meskipun ada jenis buah tanaman ini yang berwarna coklat dan coklat-kekuningan (Budi dan Paimin, 2004). Secara umum, habitat asal tanaman ini adalah hutan sekunder dengan kondisi tanah lembab. Tanaman buah merah ditemukan tumbuh di daerah dengan ketinggian 0-2300 meter diatas permukaan laut (dpl). Adapun klasifikasi tanaman buah merah menurut Brands (2000) dan Heyne (1987) adalah sebagai berikut :
Regnum : Plantae
Divisio : Spermatophyta Sub divisio : Angiospermae Classis : Liliopsida Subclassis : Aridae Ordo : Pandanales Familia : Pandanaceae Subfamilia : Pandanoidaeae Genus : Pandanus
Species : Pandanus conoideus Lamk.
Secara empiris buah merah telah digunakan untuk pengobatan berbagai macam penyakit antara lain kanker, liver, diabetes, dan HIV-AIDS. Menurut Budi (2001), buah merah mengandung komponen gizi yang bermanfaat dalam kadar tinggi, diantaranya betakaroten, tokoferol, asam oleat, asam linoleat, dan asam linolenat. Rohman et al. (2010) melaporkan bahwa ekstrak etil asetat dan fraksi-fraksinya mempunyai aktivitas antioksidan melalui penangkapan radikal bebas DPPH dan daya reduksi terhadap ion besi (III). Salah satu fraksinya bahkan menunjukkan aktivitas antioksidan yang lebih tinggi dibanding tokoferol. Etil asetat merupakan pelarut yang bersifat semi-polar, sehingga zat aktif yang terdapat dalam minyak dapat terekstrak oleh etil asetat.
Berdasar penelitian yang dilakukan oleh I Made Budi (2005), buah merah dapat berfungsi seperti obat antiretrovirus yang amat dibutuhkan penderita HIV/AIDS. Kandungan vitamin E (tokoferol) dan betakaroten yang sangat tinggi
diyakini mampu memperbaiki keadaan pasien AIDS karena kedua kandungan ini berfungsi sebagai antioksidan dan dapat meningkatkan sistem kekebalan tubuh.
Tabel I. Kandungan senyawa aktif dalam minyak buah merah (Budi dan Paimin, 2004). Senyawa Aktif Kandungan
Total karotenoid 12.000 ppm Total tokoferol 11.000 ppm β-karoten 700 ppm α-tokoferol 500 ppm Asam oleat 58 % Asam linoleat 8,8 % Asam linolenat 7,8 % Asam dekanoat 2,0 %
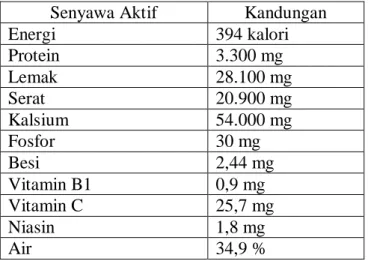
Tabel II. Komposisi zat gizi per 100 gram buah merah (Budi dan Paimin, 2004). Senyawa Aktif Kandungan
Energi 394 kalori Protein 3.300 mg Lemak 28.100 mg Serat 20.900 mg Kalsium 54.000 mg Fosfor 30 mg Besi 2,44 mg Vitamin B1 0,9 mg Vitamin C 25,7 mg Niasin 1,8 mg Air 34,9 %
Penelitian terkait dengan antikanker buah merah telah dilakukan oleh Meiyanto et al. (2005), yang mana ekstrak MBM memiliki potensi sitotoksik terhadap sel miolema, sel kanker leher rahim (HeLa) dan sel kanker payudara (T47D) dengan IC50 berturut-turut sebesar 5637 ppm, 1355 ppm, dan 914 ppm.
Penelitian lebih lanjut dilakukan oleh Munim et al. (2006) yang menunjukkan bahwa pemberian sari buah merah pada dosis 0,21 mL / 200 g BB mampu menghambat pertumbuhan kanker pada paru-paru tikus hasil induksi 7,12-
dimetilbenz(a)antrasen (DMBA). Sedangkan menurut Moeljopawiro et al. (2007), sari buah merah mempunyai kemampuan menghambat proliferasi sel kanker payudara, rahim, dan usus besar.
Tokoferol yang terkandung dalam buah merah merupakan antioksidan yang diduga mampu memperbaiki kerja pankreas sehingga sekresi insulin oleh sel β pulau langerhans dapat meningkat (Budi, 2005). Penelitian yang dilakukan oleh Febriyanti et al. menunjukkan bahwa pemberian ekstrak buah merah dapat menurunkan kadar glukosa darah secara signifikan. Pemberian ekstrak buah merah dengan dosis 0,13 dan 0,54 ml/ekor/hari/O mampu menurunkan kadar glukosa darah dan pemberian ekstrak buah merah dosis 0,13 dan 0,54 ml/ekor/hari/O selama 14 hari tidak bersifat toksik (Febriyanti et al., 2010).
Buah merah juga dapat menunjukkan aktivitas hepatoprotektif melawan kerusakan hati yang diinduksi oleh CCl4. Penelitian yang dilakukan oleh Maulita
menunjukkan bahwa pemberian ekstrak buah merah secara signifikan mampu menurunkan kadar SGPT dan SGOT. Berdasarkan pemeriksaan histopatologi, pemberian ekstrak buah merah mampu menghambat kerusakan dan mengurangi degenerasi dan nekrosis sel hati (Maulita, 2010). Buah merah memiliki kemampuan hepatoprotektif yang lebih baik dibandingkan dengan obat standar dalam mencegah terjadinya kerusakan sel hati yang ditunjukkan dengan tingkat aktivitas SGOT dan SGPT dan persentase kerusakan sel hati yang lebih rendah (Nugraha et al., 2008).
3. Minyak Kedelai
Minyak kedelai adalah minyak yang diperoleh dari ekstraksi biji kedelai (Glycine max L) dengan metode maserasi. Pelarut yang banyak digunakan dalam proses ekstraksi adalah etanol, heksana, etilen diklorida, aseton, isopropanol, dan metanol (Koswara, 2007). Isa (1996) telah mengekstraksi minyak dari biji kedelai dengan variasi pelarut (n-heksan, petroleum eter, kloroform, campuran petroleum eter dengan kloroform) dan diperoleh kadar minyak yang paling tinggi yaitu 18,83-20,36% menggunakan campuran petroleum eter dengan kloroform. Hasil analisis komponen penyusun minyak kedelai dengan kromatografi gas menunjukkan bahwa komponen dominan yang menyusun minyak kedelai adalah asam linoleat, asam oleat, asam palmitat, asam linolenat, dan asam stearat.
Asam lemak dalam minyak kedelai sebagian besar terdiri dari asam lemak essensial yang dibutuhkan oleh tubuh. Minyak kedelai yang sudah dimurnikan dapat digunakan sebagai minyak goreng serta untuk segala keperluan pangan seperti margarin. Hampir 90% produksi minyak kedelai digunakan di bidang pangan dalam bentuk telah dihidrogenasi, karena minyak kedelai mengandung lebih kurang 85% asam lemak tak jenuh (Ketaren, 1986). Kandungan asam lemak tak jenuh yang tinggi pada minyak kedelai dapat mencegah timbulnya atherosclerosis atau penyumbatan pembuluh darah (Rismunandar, 1978). Minyak kedelai juga digunakan untuk pembuatan lilin, sabun, semir, insektisida, pernis, dan cat.
Menurut Ketaren (1986), kadar minyak dalam kedelai relatif lebih rendah dibandingkan dengan jenis kacang-kacangan lainnya. Perbedaan kadar minyak dan komposisi asam lemak dalam kedelai sangat bergantung pada varietas dan keadaan iklim tempat tumbuh. Komposisi asam lemak yang terkandung dalam minyak kedelai disajikan dalam tabel III.
Tabel III. Komposisi asam lemak dalam minyak kedelai (Herschdoefer, 1986).
No. Asam Lemak Jumlah Karbon Kadar (%)
1. Asam miristat C14:0 < 0,5 2. Asam palmitat C16:0 7,0-12 3. Asam palmitoleat C16:1 0,0-0,5 4. Asam stearate C18:0 2,0-5,5 5. Asam oleat C18:1 19-30 6. Asam linoleat C18:2 48-58 7. Asam linolenat C18:3 < 4-10 8. Asam arakidonat C20:0 < 1,0 9. Asam gadoleat C20:1 < 1,0 10. Asam behenat C22:0 < 0,5
Menurut Bailey (1951), berat jenis minyak kedelai yang diukur pada temperatur 25oC adalah sebesar 0,916-0,922 dengan indeks bias sebesar 1,471-1,475. Angka penyabunan minyak kedelai berkisar antara 189-195 dengan kandungan asam lemak bebas sebesar 1,5%; bilangan asam sebesar 0,2-0,6; dan bilangan iod sebesar 189-195 (Allan dan Hamilton, 1983).
4. Minyak Jagung
Minyak jagung merupakan salah satu minyak nabati yang diperoleh dari biji jagung (Zee mays L) dan telah mengalami proses pemurnian dengan atau tanpa penambahan bahan tambahan yang diizinkan. Minyak jagung diperoleh dengan cara mengekstrak bagian lembaga. Sistem ekstraksi yang digunakan
biasanya sistem pres (pressing) atau kombinasi sistem pres dan pelarut menguap (pressing and solvent extraction). Lemak jagung terutama terdapat dalam lembaga dengan kadar lemak sekitar 30 %. Kadar lemak biji jagung secara keseluruhan yaitu 4,2-5 %. Minyak jagung berwarna merah gelap dan setelah dimurnikan akan berwarna kuning keemasan (Ketaren, 1986).
Presentase trigliserida pada minyak jagung sekitar 98,6%, sedangkan sisanya adalah bahan non lemak seperti zat warna atau pigmen dan abu. Minyak jagung merupakan minyak yang stabil (tahan terhadap ketengikan) karena adanya tokoferol yang larut dalam minyak. Minyak jagung dapat digunakan sebagai bahan dalam industri, misalnya obat-obatan, bahan kimia, insektisida, dan bahan pangan seperti salad, mentega putih, dan lainnya. Dalam produk farmasi, minyak jagung digunakan untuk sediaan injeksi seperti injeksi tamoxifen (Hayashi dan McMahon, 2002).
Minyak jagung mempunyai nilai gizi yang tinggi yaitu sekitar 25.000 kilokalori/gram. Dalam minyak jagung terdapat banyak asam lemak esensial yang dibutuhkan pada pertumbuhan sel. Minyak jagung lebih disukai konsumen karena selain harganya yang murah juga mengandung sitosterol yang dapat mencegah terjadinya atheroschlerosis melalui pembentukkan kompleks antara sitosterol dan Ca2+ dalam darah (Ketaren, 1986).
Salah satu mutu minyak jagung adalah terkait dengan bilangan iodium yang dikandungnya. Bilangan iod menunjukkan besarnya tingkat ketidakjenuhan suatu minyak atau lemak. Asam lemak tidak jenuh yang terkandung pada minyak
jagung sangat tinggi yaitu sekitar 86%. Mutu minyak juga dipengaruhi oleh kadar asam lemak bebas, karena jika kadar asam lemak bebasnya tinggi, maka akan timbul bau tengik. Adapun faktor-faktor yang dapat menyebabkan naiknya asam lemak bebas dalam minyak antara lain adalah kadar air yang terkandung dan enzim-enzim seperti peroksidase dan lipase yang terdapat dalam minyak tersebut. Data fisika dan kimia minyak jagung tersaji dalam tabel IV.
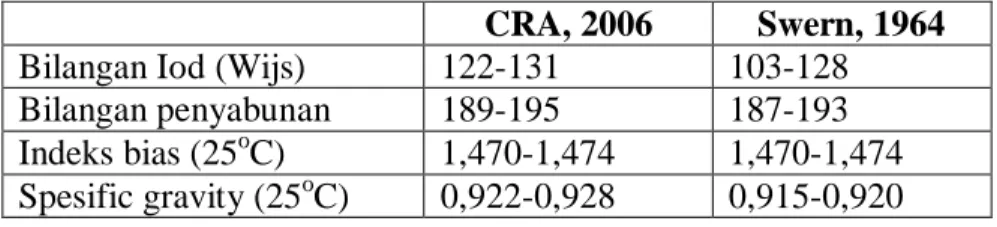
Tabel IV. Data fisika dan kimia minyak jagung (Sumber: Corn Refines Association, 2006 dan
Swern, 1964).
CRA, 2006 Swern, 1964
Bilangan Iod (Wijs) 122-131 103-128 Bilangan penyabunan 189-195 187-193 Indeks bias (25oC) 1,470-1,474 1,470-1,474 Spesific gravity (25oC) 0,922-0,928 0,915-0,920
Tabel V. Profil asam lemak minyak jagung (Sumber: Corn Refines Association, 2006). Profil asam lemak gram/100 gram minyak % berat
Asam linoleat 54-60 34-62
Asam palmitat 11-13 8-12
Asam stearate 2-3 2-5
Asam oleat 25-31 19-49
Asam lemak yang menyusun minyak jagung terdiri dari asam lemak jenuh dan asam lemak tak jenuh. Kandungan asam lemak jenuh pada minyak jagung relatif rendah, yaitu asam palmitat 8-12% dan asam stearat 2-5%. Sebaliknya, kandungan asam lemak tidak jenuhnya cukup tinggi, terutama asam linoleat yang mencapai 34-62%.
5. Spektroskopi Inframerah Fourier Transform (FTIR)
Metode spektrofotometri mengukur jumlah radiasi elektromagnetik yang diserap oleh larutan sampel. Spektroskopi inframerah merupakan salah satu jenis spektroskopi vibrasional. Bila radiasi IR dilewatkan melalui suatu cuplikan, maka molekul akan menyerap energi sehingga terjadi perubahan tingkat vibrasi/rotasi, tetapi hanya transisi vibrasi/rotasi yang dapat menyebabkan perubahan momen dipol yang aktif mengabsorpsi sinar IR (Hendayana et al. 1994). Disamping itu, frekuensi sinar yang datang harus sama dengan salah satu frekuensi vibrasi/rotasi molekulnya.
Secara umum spektra serapan inframerah dapat dibagi menjadi tiga daerah kerja, yaitu daerah inframerah (IR) jauh (400 – 50 cm-1), daerah IR tengah (4000 - 400 cm-1), dan daerah IR dekat (14000 – 4000 cm-1). Daerah yang paling penting untuk analisis minyak adalah inframerah tengah karena mampu memberikan berbagai macam jenis ikatan molekul (gugus fungsional) yang terdapat dalam minyak (Reid et al., 2006). Selain itu, spektroskopi IR juga dapat digunakan untuk analisis kuantitatif karena intensitas (absorbansi) dalam spektra IR berbanding lurus dengan gugus fungsional yang bersesuaian sebagaimana ditunjukkan dalam hukum Lambert-Beer (Guillen dan Cabo, 1997).
Sebagaimana jenis absorpsi energi yang lain, pada spektroskopi IR, molekul dieksitasikan ke tingkat energi yang lebih tinggi ketika molekul-molekul ini menyerap radiasi IR. Absorpsi radiasi inframerah, sebagaimana proses absorpsi yang lain, merupakan suatu proses kuantisasi yang berarti bahwa
hanya frekuensi (energi) tertentu dari radiasi IR yang dapat diserap oleh suatu molekul. Absorpsi radiasi IR bersesuaian dengan perubahan energi yang berkisar antara 2-10 kkal/mol. Radiasi pada kisaran energi ini bersesuaian dengan kisaran frekuensi vibrasi regangan dan ulur suatu ikatan dalam kebanyakan ikatan kovalen molekul. Dalam proses absorpsi, frekuensi-frekuensi radiasi inframerah yang bersesuaian dengan frekuensi vibrasi molekul akan diserap dan akan meningkatkan amplitudo gerakan-gerakan vibrasional ikatan dalam molekul. (Pavia et al., 2009).
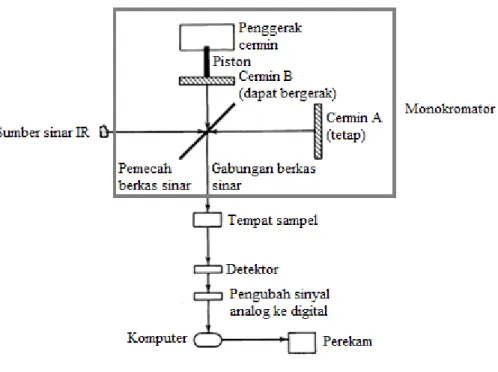
Saat ini dengan perkembangan transformasi Fourier, spektroskopi FTIR digunakan secara luas dalam bidang farmasi, makanan, lingkungan dan sebagainya (Che Man et al., 2010). Spektroskopi FTIR memiliki beberapa keuntungan di antaranya non-destruktif, dapat menganalisis multikomponen secara cepat, tidak perlu penyiapan contoh yang ekstensif, dan gangguan dapat diminimumkan selama penentuan suatu senyawa (Rohman dan Che Man, 2008). Spektroskopi IR juga dikenal sebagai teknik sidik jari (finger print), yang berarti bahwa tidak ada 2 senyawa/sampel yang mempunyai jumlah puncak atau intensitas absorbansi yang sama (Guillen dan Cabo, 1997). Skema instrumentasi spektrofotometer FTIR disajikan pada Gambar 3.
Gambar 3. Skema instrumentasi spektrofotometer FTIR (Silverstein dan Webster, 1998). Bagian pokok dari spektrofotometer inframerah adalah sumber cahaya, detektor dan monokromator. Cahaya dari sumber dilewatkan melalui cuplikan, dipecah menjadi frekuensi-frekuensi individunya dalam monokromator dan intensitas relatif dari frekuensi individu diukur oleh detektor. Pada spektrofotometer FTIR, monokromator digantikan dengan interferometer. Interferometer ini mengatur intensitas sumber sinar inframerah dengan mengubah posisi cermin pemantul yang memantulkan sinar dari sumber sinar ke sampel. Jadi, keberadaan interferometer membuat spektrofotometer mampu mengukur semua frekuensi optik secara serempak dengan mengatur intensitas dari semua frekuensi tunggal sebelum sinyal mencapai detektor. Hasil scanning interferometer yang berupa interferogram (pengaluran antara intensitas dan posisi cermin) ini tidak dapat diinterpretasikan dalam bentuk aslinya. Proses matematika transformasi Fourier akan mengubah interferogram menjadi spektra antara
intensitas dan frekuensi (George & McIntyre 1987). Kebanyakan prisma yang digunakan terbuat dari materi seperti KBr dan NaCl yang tidak menyerap radiasi inframerah (Harvey 2000). Kelemahan NaCl adalah sifatnya yang higroskopis sehingga cermin-cermin harus dilindungi dari kondensasi uap.
Perajahan (plotting) antara frekuensi atau bilangan gelombang dengan intensitas sinar yang ditransmisikan perlu dilakukan karena detektor merekam rasio intensitas 2 berkas sinar. Dalam beberapa bagian spektra, transmitan yang dihasilkan hampir 100 % yang berarti bahwa sampel hampir transparan terhadap frekuensi radiasi (tidak menyerap pada frekuensi tersebut). Seringkali, spektra senyawa diperoleh dengan melarutkannya dalam pelarut tertentu sehingga diperlukan pelarut murni sebagai referen dalam suatu sel sampel yang identik. Instrumen secara otomatis akan mengurangi sektrum sampel dengan spektra pelarut (Pavia et al., 2009).
6. Kemometrika
Kemometrika didefinisikan sebagai cabang ilmu pengetahuan yang mengaplikasikan ilmu statistika dan matematika untuk mengolah data kimia (dalam spektroskopi, data tersebut adalah spektra IR). Salah satu aplikasi kemometrika adalah aplikasi analisis multivariat, yang mana beberapa variabel (spektra dalam banyak bilangan gelombang) diukur untuk suatu sampel yang dituju (Miller and Miller, 2000). Kemometrika di dalam analisis secara spektrofotometri inframerah terdiri atas tiga aspek berikut: (1) pra-pengolahan
data spektra, (2) membangun model kalibrasi untuk analisis kuantitatif, (3) transfer model (Dea, 2012).
Salah satu analisis kemometrik yang terpenting adalah membentuk model kalibrasi melalui metode pengenalan pola untuk mengidentifikasi kemiripan dan pola utama data. Selanjutnya, model ini digunakan untuk memprediksi sampel yang tidak diketahui (Maharani, 2007). Analisis multivariat yang sering digunakan adalah principal component analysis (PCA), sementara kalibrasi mutivariat yang sering digunakan adalah regresi kuadrat terkecil sebagian (partial least square atau PLS) dan regresi komponen utama (principal component regression atau PCR).
a. Principal Component Analysis (PCA)
PCA merupakan salah satu metode multivariat yang dapat digunakan untuk menyederhanakan data dengan mengurangi sejumlah variabel ke jumlah variabel ortogonal yang lebih kecil. PCA berfungsi sebagai teknik pengurangan jumlah data ketika muncul korelasi antar data. Ketika variabel tidak saling berhubungan maka teknik ini tidak berguna (Miller dan Miller, 2000).
Secara umum, tujuan penggunaan PCA untuk analisis multivariat dapat dibagi menjadi dua. Pertama, PCA melibatkan pemutaran dan pengubahan data asli, n. Transformasi ini dilakukan sedemikian rupa sehingga sumbu baru terletak di sepanjang arah varian maksimum data dengan batasan bahwa sumbu-sumbu tersebut ortogonal, dengan kata lain variabel yang baru tidak berkorelasi. Hal ini biasanya terjadi pada kasus ketika jumlah variabel baru, p, yang diperlukan untuk
menggambarkan sebagian besar varian data sampel kurang dari n. Jadi, PCA menghasilkan metode dan teknik untuk mengurangi dimensi dari parameter ruang. Kedua, PCA dapat menampakkan variabel-variabel tersebut, atau kombinasi variabel, yang menentukan beberapa struktur yang melekat dalam data yang dapat ditafsirkan dalam terminologi kimia atau fisika-kimia (Adams, 2004).
Ide yang mendasari PCA adalah dengan menemukan komponen utama Z1, Z2,. . . , Zn yang merupakan kombinasi linear dari variabel asli yang menggambarkan masing-masing bahan percobaan, X1,X2,...,Xn, misalkan:
Z1 = a11X1 + + a12X2 a13X3 + · · · a1nXn
Z2 = a21X1 + + a22X2 a23X3 + · · · a2nXn
Koefisien, a11, a12, dll dipilih sedemikian rupa sehingga variabel-variabel baru, tidak seperti variabel awal, tidak berkorelasi satu sama lain. Membuat serangkain variabel baru dengan cara ini nampaknya tidak bernilai, karena akan diperoleh n variabel baru yang menggantikan n variabel asal, dan karenanya tidak ada reduksi atau pengurangan terhadap banyaknya data. Meskipun demikian, komponen utama dipilih sehingga Principal component pertama (PC1), Z1, memiliki variasi paling besar dari serangkaian data. PC2, Z2, memiliki variasi terbesar kedua terhadap serangkaian data, dan seterusnya. Nilai Z1 yang memiliki variasi paling besar memungkinkan digunakan untuk mengurangi jumlah data yang ditangani, yaitu dengan bekerja pada satu dimensi Z1 daripada dalam banyak dimensi X1,X2,..Xn. Principal components diperoleh dari matriks kovarian (gabungan dari dua variasi) (Miller and Miller, 2000).
Variabel laten yang paling tepat untuk menggambarkan jarak relatif antara obyek, diberikan dalam suatu arahan dengan varian maksimum. Arahan ini disebut komponen utama pertama (PC1). PC1 adalah kombinasi linear dengan varian maksimal; pada dasarnya mencari dimensi sepanjang mana pengamatan terpisah atau menyebar secara maksimal. Komponen utama kedua (PC2) adalah kombinasi linear dengan varian maksimal dalam arah ortogonal terhadap komponen utama pertama, dan sebagainya. Secara umum, komponen utama menentukan dimensi yang berbeda dari yang didefinisikan oleh fungsi diskriminan atau varian resmi (Rencher, 2002).
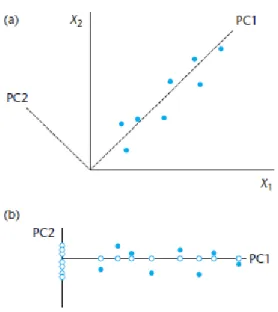
Gambar 4 menunjukkan bahwa PCA setara dengan rotasi sumbu asli sedemikian rupa sehingga PC1 berada dalam arah variasi maksimum, dengan sudut antar sumbu tidak berubah, PC2 ke arah variasi terbesar berikutnya, dan sebagainya. Dengan lebih dari 2 variabel, tidak mungkin untuk menggambarkan metode ini secara grafik, akan tetapi sekali terfikir bahwa PCA merupakan suatu pemutaran sumbu sedemikian rupa sehingga PC1 berada pada variasi maksimum, maka PC2 merupakan pemutaran pada arah yang memberikan variasi maksimum selanjutnya, dan seterusnya. Sebagai hasilnya, data dapat digambarkan dalam hanya 2 dimensi sebagai ganti dari sejumlah n data asal (Miller dan Miller, 2000).
Gambar 4. (a) Diagram yang menggambarkan dua komponen utama, PC1 dan PC2, untuk dua variabel X1 dan X2. (b) Titik-titik yang menunjuk pada sumbu-sumbu komponen utama.
● menunjukkan titik-titik data, sementara ○ merupakan proyeksinya ke dalam sumbu.
b. Partial Least Square (PLS )
Metode regresi kuadrat terkecil parsial atau sering disebut partial least square (PLS) digunakan untuk memperkirakan serangkaian variabel tidak bebas (respons) dari variabel bebas (prediktor) yang jumlahnya sangat banyak, memiliki struktur sistematik linear, dengan atau tanpa data yang hilang, dan memiliki kolinearitas yang tinggi. Dalam PLS, variabel yang menunjukkan korelasi yang tinggi dengan respon variabel diberikan bobot ekstra karena akan lebih efektif dalam prediksi. Dalam hal ini kombinasi linear variabel prediktor dipilih yang berkorelasi tinggi dengan variabel respon dan yang menjelaskan variasi dalam variabel prediktor (Miller dan Miller, 2000).
Menurut Maharani (2007), metode ini membentuk model dari variabel yang ada untuk merangkai respon dengan menggunakan regresi kuadrat terkecil
dalam bentuk matriks. Metode PLS mengkombinasikan analisis komponen utama dan regresi ganda. Tujuannya adalah untuk memprediksi suatu gugus peubah respon (Y) berdasarkan gugus peubah prediktor (X). Dalam PLS, regresi dihitung dengan algoritma kuadrat terkecil yang menghubungkan antara 2 matriks, data spektra pada matriks X dan nilai referens pada matriks Y. PLS sering digunakan dalam spektroskopi FTIR untuk mengekstraks informasi dari spektra yang kompleks yang mengandung puncak-puncak yang tumpang-tindih, adanya penganggu serta adanya derau (noise) dari instrumen yang digunakan untuk mengumpulkan data (Syahariza et al., 2005).
Dalam PLS dibutuhkan perhitungan kesalahan dalam perkiraan konsentrasi (predicted concentration) dan kesalahan spektra. Model seperti PCR mengasumsikan bahwa konsentrasi bebas dari kesalahan. Akan tetapi, PLS tidak memerlukan asumsi-asumsi yang ketat terhadap sebaran dari peubah, sisaan dan parameter, sehingga metode ini sering disebut dengan metode lunak. PLS dapat memprediksi sampel yang tidak diketahui dengan ketepatan lebih baik dibandingkan dengan teknik kalibrasi multivariat lainnya (Brereton, 2003).
c. Principal Component Regression (PCR)
PCR adalah sebuah alternatif untuk regresi linear ganda (multiple linear regression) dan dapat digunakan dalam analisis sinyal seperti dalam kalibrasi. Prinsip dasar analisis komponen utama adalah mengurangi jumlah variabel prediksi dengan mencari komponen utama yang merupakan kombinasi linear dari variabel asli. Metode regresi komponen utama (PCR) ditetapkan bila dalam
pembentukan model, pendugaan variabel bebas yang digunakan banyak dan terdapat hubungan yang erat antar variabel bebasnya. PCR merupakan analisis faktor yang mana hanya spektra yang tidak memberikan ko-linearitas yang digunakan dalam kalibrasi (Che Man et al., 2010). PCR merupakan teknik yang berguna ketika variabel prediksi memiliki korelasi yang sangat tinggi.
Komponen-komponen utama dipilih sedemikian rupa sehingga komponen utama pertama memiliki variasi yang terbesar dalam serangkaian data, sedangkan komponen utama kedua tegak lurus terhadap komponen utama pertama dan memiliki variasi terbesar berikutnya. Pemikiran dasar metode analisis ini adalah mendeskripsikan variasi serangkaian data multivariatif dengan serangkaian data baru yang mana variabel-variabel baru tidak berkolerasi satu sama lain. Variabel-variabel baru adalah kombinasi linear dari Variabel-variabel asal. Variabel baru diturunkan dalam arah menurun sehingga beberapa komponen pertama mengandung sebanyak mungkin variasi data asal.
F. Landasan Teori
Minyak buah merah (Pandanus conoidius Lam) merupakan salah satu minyak fungsional, yang mana selain dapat dikonsumsi sebagai diet juga dapat digunakan sebagai agen pencegah berbagai penyakit. Sebagai salah satu minyak yang harganya mahal di pasaran dibandingkan dengan minyak yang lain, minyak buah merah dapat dipalsukan dengan minyak lain yang harganya lebih murah seperti minyak jagung dan minyak kedelai. Pemalsuan minyak yang berharga tinggi dengan minyak yang berharga rendah telah berlangsung sejak lama dengan
tujuan untuk memperoleh keutungan yang tinggi (Rohman dan Che Man, 2008), yang dilakukan baik dengan sengaja maupun dengan tidak sengaja. Oleh karena itu, diperlukan suatu metode yang mampu mendeteksi adanya pemalsu minyak secara cepat dan reliabel untuk penjaminan kualitas dan keamanan bagi konsumen minyak buah merah.
Deteksi adanya minyak pemalsu dengan metode-metode standar seperti dengan melihat profil asam lemak atau triasilgliserol memerlukan waktu lama dan berbahaya bagi kesehatan manusia karena melibatkan berbagai macam pelarut organik. Oleh karena itu, saat ini dikembangkan berbagai metode instrumen yang cepat, reliabel, serta reprodusibel. Spektroskopi inframerah (FTIR) merupakan salah satu teknik yang menjanjikan karena kemampuanya sebagai teknik sidik jari. Selain itu, analisis minyak dengan spektroskopi FTIR juga dipertimbangkan sebagai salah satu analisis kimia ramah lingkungan (green chemistry), karena teknik ini tidak menggunakan reagen atau pelarut organik yang berbahaya bagi kesehatan manusia.
Spektroskopi FTIR juga merupakan teknik analisis yang peka, reliabel, dan operasionalisasinya mudah. Dihubungkan dengan kemometrika analisis multivariat, spektroskopi FTIR dapat memberikan informasi kualitatif dan kuantitatif (Guillen dan Cabo, 1997). Analisis multivariat yang sering digunakan adalah principal component analysis (PCA) sementara kalibrasi mutivariat yang sering digunakan adalah regresi kuadrat terkecil sebagian (partial least square atau PLS) dan regresi komponen utama (principal component regression atau PCR). Karena alasan ini, maka dalam penelitian ini akan digunakan kombinasi
keduanya (spektroskopi FTIR dan kemometrika) untuk mendeteksi dan mengkuantifikasi adanya pemalsuan pada minyak buah merah.
G. Hipotesis
1. Spektroskopi FTIR dan kemometrika dapat digunakan untuk melakukan optimasi dan menghasilkan model yang sesuai untuk autentikasi minyak buah merah dalam campuran dengan minyak jagung dan minyak kedelai.
2. Spektroskopi FTIR dihubungkan dengan kemometrika dapat digunakan untuk autentikasi minyak buah merah dalam campuran dengan minyak jagung dan minyak kedelai.