SINTESIS ASETIL EUGENOL
DARI EUGENOL DAN ANHIDRIDA ASAM ASETAT DENGAN KATALIS KALIUM HIDROKSIDA
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm.)
Program Studi Farmasi
Oleh:
Albertus Eka Yudistira Sarwono NIM : 078114118
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
ii
SINTESIS ASETIL EUGENOL
DARI EUGENOL DAN ANHIDRIDA ASAM ASETAT DENGAN KATALIS KALIUM HIDROKSIDA
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm.)
Program Studi Farmasi
Oleh:
Albertus Eka Yudistira Sarwono NIM : 078114118
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iii
Persetujuan Pembimbing
SINTESIS ASETIL EUGENOL
DARI EUGENOL DAN ANHIDRIDA ASAM ASETAT DENGAN KATALIS KALIUM HIDROKSIDA
Skripsi yang diajukan oleh: Albertus Eka Yudistira Sarwono
NIM : 078114118
telah disetujui oleh:
Pembimbing
v
There must be no barriers to freedom of inquiry ... There is
no place for dogma in science. The scientist is free, and
must be free to ask any question, to doubt any assertion, to
seek for any evidence, to correct any errors. ... We know
that the only way to avoid error is to detect it and that the
only way to detect it is to be free to inquire. And we know
that as long as men are free to ask what they must, free to
say what they think, free to think what they will, freedom
can never be lost, and science can never regress."
J. Robert Oppenheimer
vi
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan di bawah ini, saya mahasiswa Universitas Sanata Dharma:
Nama : Albertus Eka Yudistira Sarwono Nomor Mahasiswa : 078114118
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul: SINTESIS ASETIL EUGENOL DARI EUGENOL DAN ANHIDRIDA ASAM ASETAT DENGAN KATALIS KALIUM HIDROKSIDA beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan kepada Perpustakaan Universitas Sanata Dharma hak untuk menyimpan, mengalihkan dalam bentuk media lain,
mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas, dan mempublikasikannya di internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalti kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini yang saya buat dengan sebenarnya. Dibuat di Yogyakarta
Pada tanggal: 18 Januari 2011
Yang menyatakan,
vii PRAKATA
Puji dan syukur Penulis panjatkan kepada Tuhan Yang Maha Esa atas berkat dan rahmat-Nya, sehingga Penulis dapat menyelesaikan skripsi yang berjudul SINTESIS ASETIL EUGENOL DARI EUGENOL DAN ANHIDRIDA ASAM ASETAT DENGAN KATALIS KALIUM HIDROKSIDA. Skripsi ini disusun guna memenuhi salah satu syarat memperoleh gelar Sarjana Farmasi (S.Farm.) di Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
Selama perkuliahan, penelitian, dan penyusunan skripsi, Penulis telah banyak mendapatkan bantuan, sarana, dukungan, bimbingan, saran, dan kritik dari berbagai pihak. Oleh karena itu, Penulis ingin mengucapkan terima kasih yang sebesar-besarnya kepada:
1. Ipang Djunarko, M.Sc., Apt., selaku Dekan Fakultas Farmasi Universitas Sanata Dharma Yogyakarta
2. Jeffry Julianus, M.Si., selaku dosen pembimbing atas bantuan, kesabaran, perhatian, dan semangat selama penyusunan proposal hingga selesainya skripsi ini
3. Dra. M. M. Yetty Tjandrawati, M.Si. dan Lucia Wiwid Wijayanti, M.Si. selaku dosen penguji atas segala masukkan dan bimbingannya
viii
5. Helen yang selalu mendukung Penulis menyelesaikan penelitian dan penyusunan skripsi ini
6. Florentinus Dika Octa Riswanto selaku partner skripsiku atas segala bantuan, dukungan, motivasi, dan semangat dari awal penelitian sampai penyusunan skripsi ini
7. Sahabat-sahabatku: Yoga, Manda, Wicak, Dika, Wawan “Jinguk”, Daniel, Dani, Heru, Toro, Benny, Lala, Lia, Yunita, Dita, Maya, Olive, Devi, Felix, Anton atas kebersamaan, bantuan, serta dukungan selama ini
8. Teman-teman FST 2007 yang telah memberikan saran, dukungan, dan semangat bagi Penulis untuk menyelesaikan skripsi ini
9. Mas Parlan, Mas Bimo, Mas Kunto dan segenap laboran lain atas segala bantuannya selama ini
10.Tim UKF basket Farmasi dan Tim UKF basket FST (esp. Roy dan Teo) atas waktu-waktu yang berkesan di lapangan
11.Keluarga besar konggregasi Serikat Yesus dan Oblat Maria Immakulata atas segala pendidikan dan pengalaman yang diberikan
Penulis menyadari penelitian ini masih belum sempurna mengingat keterbatasan pengetahuan dan kemampuan Penulis. Oleh karena itu, Penulis sangat mengharapkan adanya kritik dan saran yang dapat berguna bagi kemajuan ilmu pengetahuan.
ix
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang saya tulis ini tidak memuat karya atau bagian karya orang lain, kecuali yang telah disebutkan dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Apabila di kemudian hari ditemukan indikasi plagiarisme dalam naskah ini, maka saya bersedia menanggung segala sanksi sesuai peraturan perundang-undangan yang berlaku.
Yogyakarta, 18 Januari 2011 Penulis
x DAFTAR ISI
HALAMAN JUDUL ... ii
HALAMAN PERSETUJUAN PEMBIMBING ... iii
HALAMAN PENGESAHAN ... iv
HALAMAN PERSEMBAHAN ... v
PERNYATAAN PERSETUJUAN PUBLIKASI ... vi
PRAKATA ... vii
PERNYATAAN KEASLIAN KARYA ... ix
DAFTAR ISI ... x
DAFTAR TABEL ... xiv
DAFTAR GAMBAR ... xv
DAFTAR LAMPIRAN ... xvi
INTISARI ... xvii
ABSTRACT ... xviii
BAB I PENGANTAR ... 1
A. Latar Belakang ... 1
xii
E. Tata Cara Penelitian ... 16
xiii
6. Spektroskopi Nuclear Magnetic Resonance (1H-NMR) ... 32
D. Perhitungan Rendemen ... 36
BAB V KESIMPULAN DAN SARAN ... 37
A. Kesimpulan ... 37
B. Saran ... 37
DAFTAR PUSTAKA ... 38
LAMPIRAN ... 41
xiv
DAFTAR TABEL
Tabel I. Perbandingan karakteristik organoleptis eugenol, asetil eugenol, dan senyawa hasil sintesis ... 25 Tabel II. Nilai Rf kromatogram KLT ... 26
Tabel III. Perbandingan gugus eugenol, asetil eugenol, dan senyawa hasil
xv
DAFTAR GAMBAR
Gambar 1. Eugenol ... 5
Gambar 2. Asetil eugenol ... 6
Gambar 3. Anhidrida asam asetat ... 7
Gambar 4. Reaksi esterifikasi ... 8
Gambar 5. Reaksi pembentukan asetil eugenol ... 13
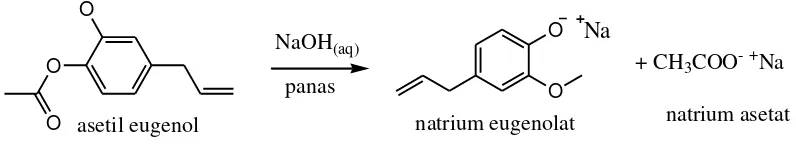
Gambar 6. Reaksi pembentukan garam eugenolat ... 21
Gambar 8. Mekanisme reaksi sintesis asetil eugenol ... 23
Gambar 7. Hidrolisis asetil eugenol ... 24
Gambar 9. Kromatogram dari KLT ... 26
Gambar 10. Kromatogram dari KG senyawa hasil sintesis ... 28
Gambar 11. Spektra MS puncak 1 dengan waktu retensi 10,158 menit ... 29
Gambar 12. Spektra MS puncak 2 dengan waktu retensi 13,239 menit ... 29
Gambar 13. Usulan pola fragmentasi spektra MS asetil eugenol ... 30
Gambar 14. Spektra IR senyawa hasil sintesis ... 31
Gambar 15. Penomoran tipe proton asetil eugenol ... 32
Gambar 16. Penomoran tipe proton eugenol... 33
xvi
DAFTAR LAMPIRAN
Lampiran 1. Perhitungan rendemen asetil eugenol ... 42
Lampiran 2. Foto penelitian ... 43
A. Rangkaian alat sintesis ... 43
B. Senyawa hasil sintesis ... 43
Lampiran 3. Kromatogram Kromatografi Gas Senyawa Hasil Sintesis…... 44
Lampiran 4. Spektra Massa Senyawa Hasil Sintesis ... 45
A. Puncak 1 ... 45
B. Puncak 2 ... 46
Lampiran 5. Spektra Infra Merah Senyawa Hasil Sintesis ... 47
Lampiran 6. Spektra Infra Merah Senyawa Tunggal ... 48
A.Eugenol ... 48
B.Asetil Eugenol ... 48
Lampiran 7. Spektra 1H-NMR Senyawa Hasil Sintesis ... 49
xvii
SINTESIS ASETIL EUGENOL
DARI EUGENOL DAN ANHIDRIDA ASAM ASETAT DENGAN KATALIS KALIUM HIDROKSIDA
INTISARI
Eugenol merupakan senyawa yang diketahui berkhasiat sebagai senyawa antiinflamasi. Meskipun demikian, selektifitas mekanisme antiinflamasi eugenol terhadap jalur siklooksigenase 2 (COX-2) rendah, sehingga perlu dilakukan modifikasi terhadap strukturnya. Salah satu modifikasi yang dapat dilakukan adalah dengan asetilasi pada eugenol. Substitusi asetil pada OH fenolik eugenol dapat membentuk senyawa asetil eugenol (4-alil-2-metoksifenil asetat). Adanya gugus asetil ini diharapkan dapat memberikan selektifitas lebih baik, didasari asumsi bahwa molekul Non-Steroidal Anti-Inflamatory Drugs (NSAID) selektif
COX-2 cenderung lebih besar daripada molekul yang tidak selektif.
Sintesis asetil eugenol dilakukan dengan mereaksikan eugenol 0,0323 mol dengan kalium hidroksida 0,0321 mol dan dipanaskan pada 70-80° C selama 30 menit. Kemudian ditambahkan anhidrida asam asetat 0,0969 mol dalam suhu 70-80° C dan direaksikan selama 3 jam. Senyawa hasil sintesis diisolasi, dimurnikan dengan proses ekstraksi menggunakan pelarut kloroform dan dicuci dengan natrium hidroksida 5%. Hasil sintesis dianalisis dengan uji pendahuluan organoleptis, kromatografi lapis tipis, dan kromatografi gas, serta elusidasi struktur yang meliputi spektroskopi massa, spektroskopi 1H-Nuclear Magnetic Resonance, dan spektrofotometri inframerah.
Senyawa hasil sintesis berupa cairan coklat kehitaman. Berdasarkan elusidasi struktur disimpulkan bahwa senyawa hasil sintesis berupa campuran molekul target asetil eugenol (rumus molekul C12H14O3, berat molekul 206 g/mol)
dan starting material eugenol. Rendemen kasar asetil eugenol yang diperoleh sebesar 78,54%.
xviii
SYNTHESIS OF ACETYL EUGENOL
FROM EUGENOL AND ACETIC ACID ANHYDRIDE WITH POTASSIUM HYDROXIDE AS CATALYST
ABSTRACT
Eugenol is a compound that has been known as an anti-inflammatory agent. However, the selectivity of anti-inflammatory mechanisms of eugenol on cyclooxygenase 2 path (COX-2) is low, so that modification to the structure is necessary. One modification that can be done is acetylation. Acetyl substitution on
eugenol’s OH phenolic forms acetyl eugenol (4-allyl-2-methoxyphenyl
acetate). Substitution of this acetyl group is expected to give better selectivity, based on assumption that the molecules of Non-Steroidal Anti-Inflammatory Drugs (NSAIDs) COX-2 selective tend to be larger than the molecules that are not selective.
Synthesis of acetyl eugenol performed by reacting 0.0323 mol eugenol with 0.0321 mol potassium hydroxide and heated at 70-80° C for 30 minutes. Then 0.0969 mol of acetic acid anhydride added in same temperature and reacted for 3 hours. Synthesized compound then isolated and purified by chloroform extraction, washed with 5% sodium hydroxide, then analyzed with preliminary organoleptic test, thin layer chromatography and gas chromatography, as well as structure elucidation, including mass spectroscopy, spectroscopy 1 H-Nuclear Magnetic Resonance, and infrared spectrophotometry.
The synthesized compound was blackish brown liquid. Based on the structure elucidation, synthesized compound was a mixture of target molecule acetyl eugenol (molecular formula C12H14O3, molecular weight 206 g / mol) and
starting material eugenol. Crude rendement of acetyl eugenol obtained was 78,54%.
1 BAB I PENGANTAR
A. Latar Belakang
Angka morbiditas peristiwa inflamasi cukup tinggi di masyarakat. Gejala ini umumnya ditangani dengan pemberian obat antiinflamasi pada penderita. Untuk menghindari efek samping obat golongan steroid, biasanya diberikan obat-obat antiinflamasi golongan Non-Steroid Anti-Inflammatory Drugs (NSAID).
Namun, kebanyakan obat golongan NSAID bersifat non selektif jalur COX (siklooksigenase), sehingga dapat berinteraksi dengan COX-1 maupun COX-2. Penghambatan pada COX-1 akan mengakibatkan efek merugikan terutama pada saluran gastrointestinal pasien. Oleh karena itu, penelitian untuk penemuan senyawa antiinflamasi baru yang selektif COX-2 menjadi penting.
2
Pada penelitian ini dilakukan asetilasi pada gugus –OH fenolik eugenol. Penambahan gugus meruah ini dilakukan dengan mereaksikan eugenol dengan anhidrida asam asetat berdasarkan reaksi esterifikasi pada gugus –OH fenoliknya. Dalam reaksi ini, eugenol berperan sebagai nukleofil dan anhidrida asam asetat berperan sebagai elektrofil. Hasil dari reaksi ini adalah senyawa asetil eugenol yang memiliki struktur lebih besar daripada eugenol. Senyawa asetil eugenol telah diketahui memiliki pengaruh terhadap biosintesis prostaglandin (Srivastara and Maholtra, 1991).
Sintesis dilakukan dengan menggunakan katalis basa kalium hidroksida. Proses esterifikasi dengan katalis basa dinilai dapat menurunkan kemungkinan terjadinya reaksi reversibel seperti pada penggunaan katalis asam. Katalis basa ini dapat menambah nukleofilisitas gugus fenolik eugenol dengan mengubah eugenol menjadi ion eugenolat. Bertambahnya nukleofilisitas menyebabkan ion eugenolat dapat bereaksi lebih cepat dengan atom C karbonil anhidrida asam asetat sehingga rendemen optimum dapat diperoleh.
1. Permasalahan
a. Apakah asetil eugenol dapat disintesis dari eugenol dan anhidrida asam asetat dengan katalis kalium hidroksida?
3
2. Keaslian Penelitian
Penelitian tentang sintesis asetil eugenol pernah dilakukan oleh Manoppo (2010) pada Isolasi Eugenol dari Bunga Cengkeh dan Sintesis Eugenil
Asetat dengan natrium asetat sebagai katalis, oleh Carrasco et al. (2008) pada Eugenol and Its Synthetic Analogues Inhibit Cell Growth of Human Cancer Cells
(Part I) dengan katalis piridin, dan oleh Bulan (2004) pada Reaksi Asetilasi Eugenol dan Oksidasi Metil Iso Eugenol dengan katalis asam sulfat. Sintesis asetil eugenol dari eugenol dan anhidrida asam asetat dengan katalis kalium hidroksida sejauh pengamatan peneliti belum pernah dilakukan.
3. Manfaat Penelitian
a. Manfaat Teoritis. Penelitian ini diharapkan dapat memperkaya ilmu pengetahuan pada jalur-jalur modifikasi senyawa eugenol.
4
B. Tujuan Penelitian Penelitian ini bertujuan untuk:
1. Mengetahui apakah asetil eugenol dapat disintesis dari eugenol dan anhidrida asam asetat dengan katalis kalium hidroksida.
5 BAB II
PENELAAHAN PUSTAKA
A. Eugenol
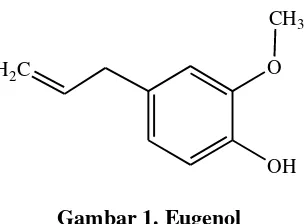
Eugenol diperoleh dari minyak cengkeh, berbentuk cairan tidak berwarna atau kuning pucat, memiliki bau cengkeh kuat, menusuk, rasa pedas, dan tidak memutar bidang polarisasi. Bila terpapar udara warna eugenol menjadi gelap dan mengental. Kelarutan eugenol adalah 1 bagian volume terlarut dalam 2 bagian volume etanol 70% (Budavari, 2001).
OH O H2C
CH3
Gambar 1. Eugenol
6
B. Asetil Eugenol
Asetil eugenol merupakan senyawa derivat eugenol, senyawa atsiri dalam minyak tumbuhan cengkeh (Syzygium aromatikum L.). Asetil eugenol
berwarna kuning sampai kuning kecoklatan, berbau pedas aromatik cengkeh (Sigma-Aldrich, 2010). Asetil eugenol atau eugenil asetat memiliki nama kimia 4-alil-2-metoksifenil asetat serta rumus kimia C12H14O3 dengan berat molekul
206,241 gram/mol (R&DChemicals, 2006). Hasil penelitian Srivastava and Maholtra (1991) terhadap asetil eugenol menunjukkan adanya aktivitas antiinflamasi pada asetil eugenol. Karena itu, asetil eugenol memiliki potensi penggunaan sebagai agen antiinflamasi baru.
Pada penelitian sintesis asetil eugenol Bulan (2004) digunakan katalis asam sulfat dan dihasilkan area 69:31 untuk asetil eugenol:eugenol pada kromatografi gas. Manoppo (2010) melakukan sintesis dengan metode refluks menggunakan katalis natrium asetat anhidrida dan menghasilkan rendemen 63,54%. Pada penelitian Carrasco et al. (2008) digunakan katalis piridin.
O
7
dan sebuah hidroksil dan antaraksi kedua gugus ini menyebabkan kereaktifan kimia asam karboksilat (Tarigan, 2009).
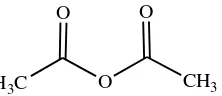
Anhidrida asam karboksilat, RCO-O-COR biasanya hanya disebut anhidrida. Senyawa ini dapat disintesis dari dua molekul asam karboksilat dengan penghilangan air (Suggs, 2002). Karena kereaktifitasannya tinggi, turunan asam karboksilat ini sangat berguna dalam sintesis senyawa organik yang lain (Fessenden and Fessenden, 1986).
Anhidrida asam asetat digunakan dalam proses asetilasi karena lebih reaktif dibandingkan asam karboksilat. Hal ini disebabkan karena ion karboksilat pada anhidrida asam asetat merupakan leaving group yang lebih baik
dibandingkan gugus –OH pada asam karboksilatnya. Elektrofilisitas C karbonil pada anhidrida asam asetat juga lebih besar daripada elektrofilisitas C karbonil asam asetat, sehingga molekul anhidrida asam asetat menjadi lebih reaktif (Supardjan, 2004).
H3C O CH3
O O
8
D. Reaksi Esterifikasi Eugenol
Suatu ester asam karboksilat ialah suatu senyawa yang mengandung gugus -CO2-R dengan R dapat berbentuk alkil maupun aril. Suatu ester dapat
terbentuk dengan reaksi langsung antara suatu asam karboksilat dan suatu alkohol, suatu reaksi yang disebut esterifikasi (Fessenden and Fessenden, 1986).
Reaksi esterifikasi secara umum dapat dijelaskan sebagai berikut: R-COOH + R’-OH R-COOR’ + H2O
(suatu asam karboksilat) (suatu alkohol) (suatu ester)
Gambar 4. Reaksi esterifikasi
Esterifikasi suatu fenol, termasuk eugenol, dapat terjadi dengan suatu asam karboksilat atau dengan derivat asam karboksilat yang lebih reaktif seperti anhidrida asam asetat. Esterifikasi dengan asam karboksilat umumnya memiliki rendemen yang kecil sehingga seringkali digunakan derivat yang lebih reaktif (Fessenden and Fessenden, 1986).
Kalium hidroksida (KOH) merupakan suatu basa kuat dan sangat reaktif terhadap senyawa asam (ChemicalLand21, 2010). Katalis basa pada substitusi nukleofilik asil akan merubah nukleofil OH menjadi O- yang lebih kuat atau basanya (-OH) dapat bertindak sebagai reagen nukleofilik kuat (Sykes, 1985).
E. Analisis Senyawa Hasil Sintesis 1. Kromatografi Lapis Tipis (KLT)
9
yang dilapisi dengan fase diam. Senyawa yang akan dianalisis ditotolkan pada dasar lempengan yang dilapisi fase diam dan dielusi dengan fase gerak yang akan bergerak naik oleh karena gaya kapilaritas (Bresnick, 1996).
Jika fase diam bersifat polar maka senyawa yang bersifat polar akan melekat lebih kuat pada lempeng daripada senyawa non polar akibat interaksi tarik-menarik dipol-dipol. Senyawa non polar kurang melekat pada fase diam polar sehingga terelusi lebih cepat (Bresnick, 1996).
Identifikasi adalah suatu proses mendapatkan identitas dari senyawa yang dianalisis. Identifikasi dari komponen yang dianalisis memiliki prinsip bahwa setiap komponen memiliki kondisi dan karakteristik pada kromatogram yang disebut sebagai harga Rf. Karakteristik tersebut dapat berupa variasi dari
harga Rf, ketajaman fluoresensi warna, dan lain-lain. Variasi harga Rf dapat
dibandingkan antara senyawa yang dicari dengan senyawa standarnya dalam kromatogram yang sama (Gasparic and Churacek, 1978).
KLT dapat digunakan untuk menguji kemurnian secara kualitatif dari campuran suatu senyawa (Gasparic and Churacek, 1978). Senyawa dikatakan murni apabila memberikan peak tunggal pada KLT dengan berbagai fase gerak (Setyowati, 2007).
2. Kromatografi Gas (KG)
10
analisa kualitatif (penentuan sifat-sifat dari suatu komponen atau campuran suatu komponen) serta analisa kuantitatif (penentuan jumlah dari suatu komponen atau komponen-komponen dalam suatu campuran) (Sastrohamidjojo, 2001).
Data kromatografi gas biasanya terdiri dari waktu retensi atau waktu tambat berbagai komponen campuran. Waktu retensi diukur mulai dari titik penyuntikan sampai titik maksimum puncak dan sangat khas untuk senyawa tertentu pada kondisi tertentu (Gritter, Bobbit, and Scharting, 1991).
Detektor pada kromatografi gas adalah suatu sensor elektronik yang mengubah sinyal gas pembawa dan komponen-komponen di dalamnya menjadi sinyal elektronik. Sinyal elektronik detektor akan sangat berguna untuk analisis kualitatif maupun kuantitatif terhadap komponen-komponen yang terpisah di antara fase diam dan fase gerak (Rohman, 2009).
3. Spektrofotometri Infra Merah (Infra Red)
11
maka spektrofotometri infra merah merupakan peralatan pokok dalam identifikasi kimia organik (Fessenden and Fessenden, 1986).
Banyaknya energi yang diabsorbsi oleh suatu ikatan bergantung pada perubahan dalam momen ikatan seperti vibrasi atom-atom yang saling berikatan. Lebih besar perubahan dalam momen ikatan mengakibatkan absorbsi sejumlah energi menjadi lebih besar pula. Jenis perubahan momen tersebut antara lain uluran (stretch) dan tekukan (bend) (Fessenden and Fessenden, 1986).
Spektrum inframerah pada dasarnya merupakan gambaran dari pita absorbsi yang spesifik dari gugus fungsional yang mengalami vibrasi karena pemberian energi dari luar. Interaksi antara gugus dengan atom yang mengelilinginya dapat menandai spektrum itu dalam setiap senyawa. Untuk analisa kualitatif, ada atau tidaknya absorbsi pada frekuensi tertentu merupakan penanda ada tidaknya gugus fungsional tertentu dalam molekul (Fessenden and Fessenden, 1986).
4. Spektroskopi Resonansi Magnetik Inti Proton (1H-NMR)
Resonansi magnetik inti diakibatkan oleh penyerapan radisai elektromagnetik di daerah frekuensi radio oleh proton dalam suatu medan magnet (Silverstein and Webster, 1998). Bila sejumlah proton ditempatkan dalam medan magnet, beberapa proton akan terletak searah sedangkan beberapa yang lain terletak berlawanan arah terhadap medan magnet yang digunakan. Proton yang terletak searah dengan medan magnet dianggap lebih stabil. Dibutuhkan energi
12
berlawanan arah dengan medan magnet. Apabila inti yang berputar ini dikenai radiasi elektromagnetik pada frekuensi yang tepat (frekuensi radio), proton yang berenergi spin lebih rendah dapat menyerap energi dan akan “meloncat” ke keadaan spin berenergi lebih tinggi (Bresnick, 1996).
Medan magnet yang diderita oleh sebuah proton dipengaruhi oleh keadan spin dari proton-proton tetangganya. Proton-proton yang saling
mempengaruhi ini berada dalam lingkungan magnet dan molekul yang berlainan. Penyerapan energi yang berbeda – beda oleh proton akan menghasilkan spektrum dari berbagai proton (Sastrohamidjojo, 2001).
Nilai geseran kimia suatu proton dipengaruhi adanya ikatan phi yang
memperkuat medan magnetik yang dialami proton, sehingga proton menjadi tidak terperisai dan geseran kimianya jatuh pada daerah downfield (Fessenden and
Fessenden, 1986).
5. Spektroskopi Massa (Mass Spectroscopy)
Kromatografi gas dan spektrofotometri massa merupakan teknik dengan kompatibilitas tinggi. Pada kedua teknik tersebut, sampel berada pada fase uap dan kedua berhubungan dengan kesamaan jumlah sampel (biasanya kurang dari 1 ng) (Hites, 1997).
Metode yang paling sering digunakan dalam spektroskopi massa untuk menghasilkan ion dari sampel yang akan dianalisis yaitu electron impact–mass
spectroscopy (EI-MS). Pada metode EI-MS, molekul-molekul dalam fase gas
13
1 elektron dari molekul dan menghasilkan ion molekul yang merupakan suatu radikal kation (M.+). Ion molekul dapat mengalami fragmentasi lebih lanjut menjadi fragmen ion-ion yang lebih kecil (Silverstein and Webster, 1998).
Setelah ion-ion terbentuk, akan terjadi fragmentasi kembali dan penataan ulang yang sangat cepat. Partikel yang berumur panjang akan dapat terdeteksi oleh pengumpul ion, sedangkan partikel berumur pendek mungkin tidak mencapai pengumpul ion (Fessenden and Fessenden, 1986).
F. Landasan Teori
Esterifikasi merupakan reaksi yang terjadi antara alkohol dan asam karboksilat yang akan membentuk senyawa ester. Eugenol akan beperan sebagai alkohol yang bersifat nukleofil dan menyerang C karbonil anhidrida asam asetat sebagai turunan asam karboksilat yang bersifat elektrofil. Reaksi ini akan menghasilkan suatu senyawa ester yaitu asetil eugenol. Dengan menggunakan katalis basa, nukleofil lemah eugenol akan diubah menjadi nukleofil yang lebih kuat sehingga reaksi esterifikasi akan semakin cepat dan memberikan rendemen yang banyak.
14
G. Hipotesis
1. Asetil eugenol dapat disintesis dari eugenol dan anhidrida asam asetat dengan katalis kalium hidroksida.
15 BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini termasuk penelitian non eksperimental deskriptif. Tidak dilakukan perlakuan terhadap obyek uji dan variasi pada varibel penelitian, hanya dilakukan pemaparan terhadap fenomena yang terjadi.
B. Variabel Penelitian
1. Variabel bebas berupa jumlah mol dari eugenol dan anhidrida asam asetat. 2. Variabel terikat berupa rendemen senyawa hasil sintesis.
C. Definisi Operasional
1. Starting material adalah senyawa yang digunakan sebagai bahan awal yang akan bereaksi membentuk produk hasil reaksi. Starting material yang
digunakan pada penelitian ini adalah eugenol dan anhidrida asam asetat. 2. Molekul target adalah senyawa yang menjadi target proses sintesis dan
diharapkan terbentuk dari reaksi antar starting material. Molekul target pada
penelitian ini adalah asetil eugenol.
16
D. Bahan dan Alat Penelitian 1. Bahan
Eugenol (p.a., Sigma), anhidrida asam asetat (p.a., Merck), aquadest,
kloroform (teknis, Brataco), etil asetat (p.a., Merck), toluena (p.a., Merck), kalium
hidroksida (p.a., Merck), natrium hidroksida (p.a., Merck), es batu, dan lempeng
silika gel GF254 (Merck).
2. Alat
Erlenmeyer bertutup, statif dan klem, hot plate magnetic stirer
(Heidolph MR 2002), termometer, corong kaca, corong pisah, gelas arloji, gelas
pengaduk, penangas air (Memmert Water Bath, WB 7-45), timbangan elektrik
(Mextler PM 100), seperangkat alat kromatografi lapis tipis, stopwatch,
spektrofotometer IR (IR Shimadzu Prestige-21), spektrometer 1H-NMR (1H-NMR JEOL-MY60), kromatografi gas-spektrometer massa (Shimadzu QP 2010S), lampu UV (Desaga, Germany), mikropipet (Socorex), beaker glass, baskom, dan
alat gelas lainnya.
E. Tata Cara Penelitian
1. Sintesis asetil eugenol dari eugenol dan anhidrat asam asetat dengan katalis kalium hidroksida
17
selama 30 menit. Anhidrida asam asetat 9,2 ml (0,0969 mol) ditambahkan dalam campuran dan diaduk dengan kecepatan 450 rpm dan dipanaskan pada suhu 70-80° C selama 3 jam. Senyawa hasil sintesis diestraksi dengan kloroform dua kali masing-masing 20 ml. Fase kloroform diambil. Simpan dalam lemari pendingin
sampai suhu fase kloroform kurang dari 10˚C.
2. Pemurnian asetil eugenol hasil sintesis
Fase kloroform dicuci dengan larutan natrium hidroksida 5% bersuhu kurang dari 10o C dalam corong pisah, dengan perbandingan volume fase kloroform : larutan natrium hidroksida 5% 1:2. Fase kloroform diambil dan didiamkan dalam wadah tertutup sampai mencapai temperatur ruangan. Fase kloroform kemudian diletakkan pada cawan petri dan dipanaskan pada penangas air suhu 120o C sampai semua kloroform menguap.
3. Analisis senyawa hasil sintesis a. Uji Organoleptis
Senyawa hasil sintesis diamati warna, bau, dan bentuknya, serta diperbandingkan dengan warna, bau, dan bentuk eugenol sebagai starting material
dan asetil eugenol sebagai molekul target.
b. Kromatografi Lapis Tipis
Larutan pembanding (starting material) dan senyawa hasil sintesis
ditotolkan sebanyak 3µL pada lempeng KLT dengan fase diam silika gel GF254
18
cm. Bercak diamati di bawah sinar UV pada panjang gelombang 254 nm dan dihitung harga Rf-nya.
c. Kromatografi Gas-Spektroskopi Massa
Senyawa hasil sintesis dilarutkan dalam kloroform kemudian dilakukan pemeriksaan dengan alat kromatografi gas-spektroskopi massa dengan kondisi: alat pengionan Electron Impact (EI) 70 eV, suhu injector 310° C, jenis kolom
Restek RXi-5MS (30m) suhu kolom 100° C, gas pembawa helium, tekanan 22,0 kPa, kecepatan alir fase gerak 80,1 ml/menit.
d. Spektrofotometri Infra Merah
Senyawa hasil sintesis diteteskan pada plat NaCl dengan pipet Pastuer. Sebuah plat NaCl lain diletakkan untuk menutupi tetesan tersebut, kedua plat ditekan. Absorbsi background dihilangkan pada instrument, lalu plat diletakkan
pada holder instrumen. Digunakan sumber cahaya Air Cooled Ceramic, detektor
DLATGS, resolusi 0,5, 1, 2, 4, 8, 16 cm-1, rasio S/N 40.000:1. Dilakukan
scanning pada senyawa hasil sintesis sehingga diperoleh spektra Infra Merah.
e. Spektroskopi Proton Nuclear Magnetic Resonance (1H-NMR)
Sejumlah senyawa hasil sintesis dilarutkan dengan CDCl3 pada tabung
NMR dan ditambahkan beberapa tetes tetrametilsilan (TMS). Tabung NMR dimasukkan dalam instrumen. Digunakan amplitude 1-8, sweep width 600 Hz, gelombang magnetik 60 MHz. Dilakukan scanning senyawa hasil sintesis
19
F. Analisis Hasil 1. Uji pendahuluan
Dilakukan uji pendahuluan pada senyawa hasil sintesis yang meliputi uji organoleptis, kromatografi lapis tipis, dan kromatografi gas.
2. Elusidasi struktur senyawa hasil sintesis
Dilakukan elusidasi struktur senyawa hasil sintesis yang meliputi uji Spektroskopi Massa, Spektrofotometri Infra Merah, dan Spektoskopi Proton
Nuclear Magnetic Resonance (1H-NMR).
3. Perhitungan rendemen
Perhitungan rendemen didasarkan pada rumus berikut:
20 BAB IV
HASIL DAN PEMBAHASAN
A. Sintesis Asetil Eugenol
Sintesis asetil eugenol dari eugenol dan anhidrida asam asetat didasarkan pada reaksi substitusi nukleofilik asil. Pada sintesis ini, gugus –OH fenolik pada eugenol akan berperan sebagai nukleofil dan menyerang elektrofil pada atom C karbonil molekul anhidrida asam asetat. Adanya penyerangan oleh nukleofil ini menyebabkan terjadinya substitusi atom H pada gugus -OH fenolik eugenol dengan gugus asetil dari anhidrida asam asetat dan membentuk asetil eugenol.
Gugus -OH fenolik pada eugenol memiliki kemampuan sebagai nukleofil dengan adanya pasangan elektron bebas pada atom O. Pasangan elektron bebas ini memunculkan kecenderungan gugus tersebut untuk bereaksi dengan atom yang bermuatan positif atau elektrofil. Sifat nukleofil gugus -OH fenolik eugenol ini dapat diperkuat dengan adanya reaksi dengan basa, yang mampu mengambil proton dari gugus tersebut. Hilangnya proton menyebabkan gugus tersebut semakin reaktif menjadi nukleofil lebih kuat. Fungsi basa ini dilakukan oleh basa kuat kalium hidroksida (KOH), yang diasumsikan dapat bereksi sempurna dengan
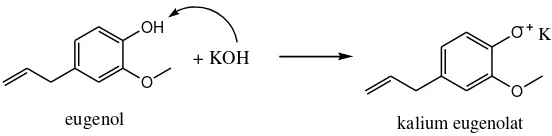
–OH fenolik eugenol sebagai asam lemah, membentuk garam kalium eugenolat.
21
Gambar 6. Reaksi pembentukan garam kalium eugenolat
Anhidrida asam asetat merupakan agen pengasilasi kuat yang memiliki dua atom C karbonil yang bersifat sebagai elektrofil. Elektrofilisitas ini bersumber dari model resonansinya yang dapat menyebabkan atom C karbonil bermuatan positif. Atom C karbonil pada molekul anhidrida asam asetat merupakan gugus yang lebih reaktif daripada C karbonil asam asetat sebab ion karboksil pada anhidrida asam asetat merupakan gugus pergi yang lebih baik daripada –OH pada asam karboksilatnya. Hal ini menyebabkan kecenderungan gugus asetat untuk lepas pada reaksi dengan nukleofil akan lebih besar.
Perancangan dan pemilihan kedua starting material, yaitu eugenol dan
anhidrida asam asetat masing-masing sebagai nukleofil kuat dan elektrofil kuat dilakukan agar reaksi berjalan dengan cepat dan rendemen hasil reaksi tinggi.
Perancangan molekul pada reaksi memerlukan urutan pencampuran
starting material yang tepat. Oleh karena itu, pertama-tama dilakukan
22
Pencampuran tidak dilakukan sekaligus pada eugenol, anhidrida asam asetat, dan katalis kalium hidroksida untuk mencegah terbentuknya garam kalium asetat, bukan garam kalium eugenolat yang diinginkan. Reaksi antara anhidrida asam asetat dan kalium hidroksida lebih kuat dari reaksi antara kalium hidroksida dan eugenol sebab parsial positif pada C karbonil anhidrida asam asetat lebih kuat daripada parsial positif proton pada –OH fenolik eugenol. Hal ini mengakibatkan katalis akan bereaksi dengan anhidrida asam asetat dan memutus ikatan ester pada molekul ahidrida tersebut, menghasilkan kalium asetat dan asam asetat.
Garam kalium eugenolat selanjutnya direaksikan dengan anhidrida asam asetat pada reaksi substitusi asil. Jumlah mol anhidrida asam asetat yang digunakan adalah tiga kali mol eugenol agar dapat terbentuk rendemen optimum asetil eugenol, sebab eugenol menjadi pereaksi pembatas dalam sintesis.
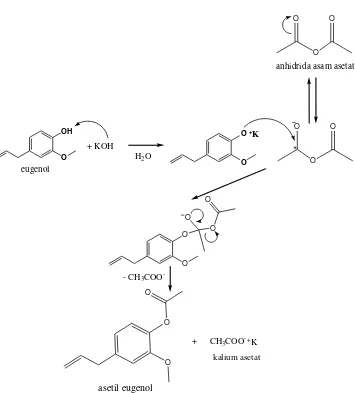
23
Gambar 7. Mekanisme reaksi sintesis asetil eugenol
Setelah reaksi, dilakukan proses isolasi terhadap senyawa hasil sintesis dengan ekstraksi menggunakan pelarut kloroform. Ektraksi ini diperlukan untuk memisahkan senyawa hasil sintesis dari senyawa hasil reaksi samping. Penggunaan kloroform untuk proses ini dikarenakan senyawa hasil sintesis bersifat nonpolar.
24
target asetil eugenol dengan starting material eugenol yang belum bereaksi
namun ikut terektraksi karena kedua molekul tersebut larut dalam kloroform. Ektraksi ini dilakukan dengan mencuci fase kloroform menggunakan larutan natrium hidroksida 5% dengan kondisi fase kloroform dan larutan natrium hidroksida bersuhu kurang dari 10° C (Ntamila and Hassanali, 1976). Pengaturan suhu dan penggunaan konsentrasi rendah natrium hidroksida ini diperlukan untuk menjamin tidak terjadinya reaksi hidrolisis molekul asetil eugenol hasil sintesis kembali menjadi eugenol, yang dalam suasana basa berupa garam eugenolat.
O
Gambar 8. Hidrolisis asetil eugenol
25
B. Uji Pendahuluan 1. Uji Organoleptis
Uji ini dilakukan dengan membandingkan warna, bau, dan bentuk senyawa hasil sintesis dengan eugenol sebagai starting material dan asetil eugenol
dari. Data hasil uji organoleptis dapat dilihat di tabel I.
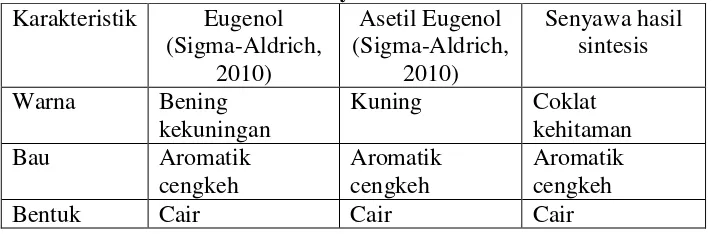
Tabel I. Perbandingan karakteristik organoleptis eugenol, asetil eugenol, dan senyawa hasil sintesis
Dari tabel tersebut dapat ditarik kesimpulan sementara bahwa reaksi telah terjadi ditandai adanya perbedaan karakter warna senyawa hasil sintesis dari
starting material eugenol. Namun, karakteristik organoleptis senyawa tersebut tidak sama dengan karakteristik asetil eugenol pada Sigma-Aldrich(2010), maka belum bisa ditunjukkan bahwa molekul target asetil eugenol terbentuk pada proses sintesis.
2. Kromatografi Lapis Tipis (KLT)
Uji ini dilakukan sebagai uji kemurnian awal senyawa hasil sintesis. Uji ini dilakukan dengan mengelusi totolan senyawa hasil sintesis dan pembanding
starting material eugenol pada plat KLT silica gel GF254 dengan fase gerak
26
cm, dan kemudian diamati bercak pengembangannya pada sinar UV 254 nm. Eugenol dan asetil eugenol memiliki kromofor yang akan menimbulkan pemadaman (quenching) pada floresensi plat sehingga dapat diamati bercaknya.
Kromatogram senyawa hasil sintesis ditunjukkan pada gambar 9.
Gambar 9. Kromatogram dari KLT
Dari hasil elusi dapat dilihat bahwa terdapat perbedaan Rf antara
senyawa hasil sintesis dengan eugenol sebagai starting material, ditandai adanya
perbedaan jarak titik terjauh kedua bercak. Nilai Rf kedua bercak adalah sebagai
berikut:
Tabel II. Nilai Rf kromatogram KLT
Senyawa Rf
Eugenol 0,375
27
Pada plat hasil elusi dan nilai Rf kedua bercak, dapat dilihat bahwa
senyawa hasil sintesis cenderung lebih non polar daripada eugenol sehingga bercaknya memiliki Rf yang lebih besar daripada bercak eugenol. Hal ini
menunjukkan terbentuknya senyawa baru pada reaksi. Nilai Rf senyawa hasil
sintesis yang lebih besar daripada eugenol menunjukkan kesesuaian dengan polaritas teoritis asetil eugenol, yang lebih non polar daripada eugenol, sebab adanya gugus asetil pada asetil eugenol. Namun, kemurnian senyawa hasil sintesis belum dapat ditentukan sebab perbedaan Rf yang muncul sangat kecil dan masih
terdapat bagian kedua bercak yang berjarak sama dari titik penotolan.
3. Kromatografi Gas (KG)
Uji kromatografi gas dilakukan untuk mengetahui kandungan senyawa hasil sintesis sekaligus sebagai indikator kemurnian hasil sintesis.
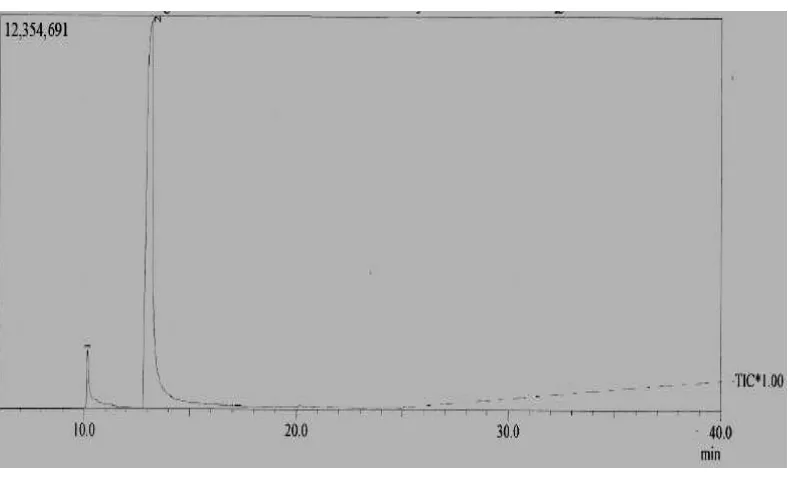
Dari kromatogram pada gambar 10, dapat dilihat bahwa terdapat dua puncak, yang menandakan adanya dua jenis senyawa yang berbeda interaksinya dengan fase diam, ditandai perbedaan waktu retensi. Dua puncak tersebut masing- masing berada pada waktu retensi 10,158 menit (puncak 1) dan 13,239 menit (puncak 2), dengan area masing-masing 2,06% dan 97,94%. Dengan hasil demikian, dapat disimpulkan bahwa senyawa hasil sintesis belum murni.
28
Gambar 10. Kromatogram dari KG senyawa hasil sintesis
C. Elusidasi Struktur 1. Spektroskopi Massa (Mass Spectroscopy– MS)
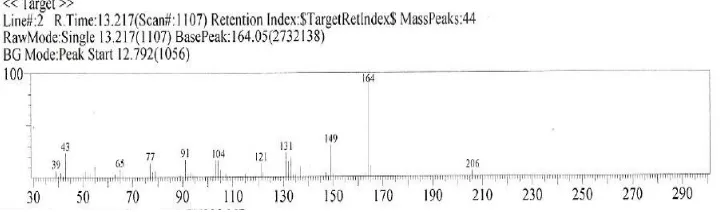
Spektroskopi massa berfungsi untuk menunjukkan massa molekular dan pola fragmentasi ion dari senyawa yang diuji. Dalam uji ini akan diidentifikasi dua puncak yang muncul dalam proses kromatografi gas.
29
Gambar 11. Spektra MS puncak 1 dengan waktu retensi 10,158 menit
Puncak 2 menunjukkan massa ion molekul dengan nilai m/z 206. Nilai ini sesuai dengan bobot molekul asetil eugenol yaitu 206 gram/mol. Fragmen ion paling stabil memiliki nilai m/z 164 yaitu eugenol, yang merupakan pemecahan dari ikatan ester pada asetil eugenol. Selain itu, terdapat fragmen ion lain yang bernilai m/z 43 yang merupakan fragmen dari gugus asetil pada asetil eugenol. Oleh karena itu, dapat disimpulkan berdasarkan spektroskopi massa bahwa puncak 2 merupakan asetil eugenol.
30
Berikut adalah usulan pola fragmentasi asetil eugenol:
O
Gambar 13. Usulan pola fragmentasi spektra MS asetil eugenol
2. Spektrofotometri Infra Merah (Infra Red– IR)
31
Gambar 14. Spektra IR senyawa hasil sintesis
Pada profil spektra IR senyawa hasil sintesis, didapatkan pita-pita representatif yang menunjukkan beberapa gugus fungsi, yaitu pita A pada 3471 cm-1(gugus –OH fenolik), pita B pada 1766 cm-1(gugus C=O ester), pita C pada 1605 cm-1(gugus C=C alil), pita D pada 1512 cm-1(gugus C-C aromatis), dan pita E pada 1196 cm-1(gugus C-O).
Adanya kelima gugus fungsi ini mengindikasikan ketidakmurnian senyawa hasil sintesis. Sebab, secara teoritis gugus OH fenolik hanya dimiliki molekul starting material eugenol dan gugus C=O ester hanya dimiliki molekul
asetil eugenol.
32
Tabel III. Gugus fungsi senyawa hasil sintesis pada spektra IR
Bilangan gelombang
Gugus fungsi Senyawa hasil sintesis
Dari tabel tersebut dapat disimpulkan bahwa senyawa hasil sintesis tersebut belum murni, sebab pita serapan –OH fenolik dan C=O ester yang masing-masing merupakan ciri serapan eugenol dan asetil eugenol muncul keduanya. Sehingga dari spektra IR yang diperoleh, diperkirakan senyawa hasil sintesis merupakan campuran antara eugenol dan asetil eugenol, sehingga gugus-gugus yang terdapat di kedua senyawa tersebut tetap muncul secara tumpang tindih pada spektra senyawa hasil sintesis.
3. Spektroskopi Nuclear Magnetic Resonance (1H-NMR)
Analisis 1H-NMR dilakukan untuk mengidentifikasi tipe proton dan jumlah proton pada senyawa hasil sintesis. Tipe proton pada asetil eugenol (Gambar 15) yang diuraikan dibawah ini, diurutkan berdasarkan posisi puncak yang ditimbulkan pada spektra 1H-NMR.
H3C
33
Karena campuran tersebut diduga mengandung eugenol, maka tipe proton ditambahkan dengan proton pada –OH fenolik yang dimiliki oleh eugenol.
O
Gambar 16. Penomoran tipe proton eugenol
Dari kedua gambar tersebut, dapat disimpulkan bahwa secara teoritis dapat teridentifikasi 9 tipe proton berbeda dari asetil eugenol dan eugenol.
Hasil spektra 1H-NMR senyawa hasil sintesis adalah sebagai berikut:
Gambar 17. Spektra 1H-NMR senyawa hasil sintesis
Analisis puncak pada 1H-NMR dilakukan dari puncak dengan geseran
kimia (δ) terkecil sampai terbesar. Puncak singlet G berintegral 3 di δ 2,2 ppm
34
sp3, sehingga cenderung lebih memiliki nilai δ relatif kecil dibandingkan proton
yang terikat pada C sp2 dan sp. Resonansi pada karbonil hanya memiliki efek induksi kecil pada tipe proton ini karena adanya O yang dapat mendonorkan elektron ke C karbonil parsial positif. Oleh karena itu, proton ini cenderung terperisai dan menimbulkan puncak paling atas (upfield) dibandingkan semua tipe
proton yang lain akan tetapi nilai δ pada proton tipe 1 tidak lebih kecil daripada 2 sebab adanya efek induksi karbonil tersebut.
Puncak doublet F berintegral 2 di δ 3,5 ppm dihasilkan oleh dua buah proton tipe 2. Proton ini terikat pada C sp3 yang mengikat gugus etena dan cincin benzen. Adanya ikatan ini menyebabkan adanya pengaruh induktif gugus etena dan cincin benzen yang bersifat menarik elektron, sehingga proton tipe 2 memiliki nilai δ yang relatif lebih besar daripada proton alkana tak terinduksi. Efek
kenaikan δ pada proton tipe 2 lebih besar daripada tipe 1 sehingga puncaknya
terletak lebih ke bawah (downfield) daripada proton tipe 1.
Puncak singlet E berintegral 3 di δ 3,8 ppm dihasilkan oleh tiga buah proton tipe 3. Proton ini terikat pada C sp3 yang mengikat substituen O rantai
benzena. Ikatan dengan O yang merupakan substituen benzena mengakibatkan efek anisotropik besar dan nilai δ menjadi lebih besar, sebab proton menjadi kurang terperisai dengan adanya elektronegatifitas atom O.
Puncak doublet D berintegral 2 di δ 5,1 ppm dihasilkan oleh proton tipe 4 dan 9. Proton tipe 4 ini terikat secara langsung dengan C yang memiliki ikatan
phi sehingga terkena efek anisotropik yang kuat. Tipe proton 9 merupakan proton
35
menyebabkan efek anisotropik yang dialaminya juga cukup kuat. Puncak D diduga merupakan campuran dua buah puncak dari tipe proton yang berlainan (puncak tipe 4 dan puncak tipe 9) di tandai dengan pola splitting puncak yang
lebar dan kurang wajar.
Puncak C multiplet berintegral 1 di δ 5,9 ppm dihasilkan oleh proton tipe 5. Proton tipe 5 merupakan proton yang terikat pada C sp2, namun efek
anisotropik pada tipe ini hanya diemban 1 proton saja, sehingga efeknya lebih besar daripada proton tipe 4. Maka, nilai δ proton ini jatuh ke bawah secara relatif terhadap tipe 4.
Puncak B multiplet berintegral 2 dihasilkan di nilai δ 6,9 dihasilkan oleh proton tipe 6 dan 7. Proton tipe 6 dan 7 adalah proton yang terikat pada cincin benzen, sehingga mengalami efek anisotropik yang sangat besar dan hampir sama. Oleh karena itu, puncak yang dimunculkan dua tipe proton dapat terlihat sebagai puncak tunggal yang berintegral bukan satu.
Puncak A doublet berintegral 1 pada δ 7,2 ppm dihasilkan oleh proton tipe 8. Proton ini merupakan proton yang terikat pada C sp2 pada cincin benzen,
36
Dari spektra 1H-NMR yang diperoleh dan hasil analisisnya, dapat diperkirakan bahwa senyawa hasil sintesis merupakan campuran antara eugenol dan asetil eugenol. Hal ini ditandai dengan munculnya puncak-puncak yang mencerminkan tipe proton kedua senyawa tersebut di spektra senyawa hasil sintesis, yaitu puncak G yang menunjukkan tipe proton 1 pada gugus asetil senyawa asetil eugenol, dan puncak D yang menunjukkan tipe proton 9 pada gugus –OH fenolik senyawa eugenol. Namun, secara keseluruhan, spektra 1 H-NMR mirip dengan deskripsi 1H-NMR asetil eugenol pada Carrasco et al. (2008)
dan Manoppo (2010). Selain itu, terdapat perbedaan yang jelas antara spektra 1 H-NMR senyawa hasil sintesis dengan spektra 1H-NMR eugenol (lampiran 8) di nilai δ 2,2 ppm yang merupakan nilai geseran kimia untuk puncak proton tipe 1. Eugenol yang tidak memiliki proton tipe ini terlihat kosong pada nilai geseran kimia tersebut.
D. Perhitungan Rendemen
37 BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
1. Asetil eugenol dapat disintesis dari eugenol dan anhidrida asam asetat dengan katalis kalium hidroksida.
2. Rendemen kasar asetil eugenol hasil sintesis eugenol dan anhidrida asam asetat dengan katalis kalium hidroksida adalah 78,54 %.
3. Senyawa hasil sintesis merupakan campuran antara molekul target asetil eugenol dengan area puncak 97,94% dan starting material eugenol dengan
area puncak sebesar 2,06% pada kromatografi gas.
B. Saran
1. Perlu dioptimasi nilai pada variabel waktu dan suhu reaksi proses sintesis asetil eugenol sehingga dapat ditentukan nilai variabel optimum yang menghasilkan rendemen lebih tinggi.
38
DAFTAR PUSTAKA
Bresnick, 1996, High-Yield Organic Chemistry, diterjemahkan oleh Hadian
Kotong, Penerbit Hipokrates, Jakarta, 101-107.
Budavari, S., 2001, Merck Index: An Encyclopedia of Chemicals, Drugs, and Biological 13th ed., Merck & Co., Inc., USA, 239.
Bulan, R., 2004, Reaksi Asetilasi Eugenol dan Oksidasi Metil Iso Eugenol,
Laporan Penelitian, Program Studi Teknik Kimia Fakultas Matematika
dan Ilmu Pengetahuan Alam Universitas Sumatera Utara, Medan.
Carrasco, H., Espinoza, L., Cardile, V., Gallardo, C., Carrasco, W., Lombardo, L.,
et al., 2008, Eugenol and its synthetic analogues inhibit cell growth of human cancer cells (Part I), http://www.scielo.br/scielo.php?pid=S0103-50532008000300024&script=sci_arttext, diakses pada tanggal 13 Januari 2011.
ChemicalLand21, 2010, Potassium Hydroxide (Caustic Soda),
http://www.chemicalland21.com/industrialchem/inorganic/KOH.htm, diakses tanggal 25 November 2010.
Fessenden, R., and Fessenden, J., 1986, Organic Chemistry, diterjemahkan oleh
Aloysius Hadyana Pudjaatmaka, Edisi ketiga, Jilid I, Penerbit Erlangga, Jakarta, 456.
Fessenden, R., and Fessenden, J., 1986, Organic Chemistry, diterjemahkan oleh
Aloysius Hadyana Pudjaatmaka, Edisi ketiga, Jilid II, Penerbit Erlangga, Jakarta, 82-84, 109-111.
Food and Agriculture Organization of the United Nations, 2010, Eugenol Infra Red Spectrum, http://www.fao.org/ag/agn/jecfa-flav/img/img/1529.gif, diakses tanggal 31 Januari 2011.
Food and Agriculture Organization of the United Nations, 2010, Eugenyl Acetate Infra Red Spectrum,
http://www.fao.org/ag/agn/jecfa-flav/img/img/1531.gif, diakses tanggal 5 Januari 2011.
39
Gritter, J.R., Bobbit, J. M., and Scharting, A. E., 1991, Introduction of Chromatography, diterjemahkan oleh Kosasih Padmawinata, Edisi II,
Penerbit ITB, Bandung, 109-112.
Hites, R.A., 1997, Gas Chromatography Mass Spectrometry, Handbook of Instrumental Techniques for Analitycal Chemistry, Prentice Hall, New
Jersey, 609-626.
Lahlou, S., Interaminense, L.F., Magalhães, P.J., Leal-Cardoso, J.H., and Duarte, J.P., 2004, Cardiovascular effects of eugenol, a phenolic compound present in many plant essential oils, in normotensive rats, J Cardiovasc Pharmacol., 43(2), 250-257.
Manoppo, Y., 2010, Isolasi Eugenol dari Bunga Cengkeh dan Sintesis Eugenil Asetat, http://molucasablog.blogspot.com/2010/06/isolasi-eugenol-dari-bunga-cengkeh-dan.html, diakses pada tanggal 13 Januari 2011.
Ntamila, M., dan Hassanali, A., 1976, Isolation of Oil of Clove Oil and Separation of Eugenol and Acetyl Eugenol, An instructive experiment for beginning chemitryunder graduates, 53(4), 263.
Öztürk, A., and Özbek, H., 2005, Caryophyllata Essential Oil: An Animal Model of Anti-inflammatory Activity, Department of Pharmacology, Van
Turkey, 159-162.
Rohman, A., 2009, Kromatografi untuk Analisis Obat, Graha Ilmu, Yogyakarta,
181.
R&DChemicals, 2006, Sygmyum aromatikum, http://www.rdchemicals.com
/chemicals.php?mode=details&mol_id=7485, diakses tanggal 24 April 2010.
Sastrohamidjojo, H., 2001, Kromatografi, Liberty, Yogyakarta, 163-164.
Satrohamidjojo, H., 2008, The Prospect of Indonesian Essential Oil Industry,
http://chemistry.uii.ac.id/Prof%20Jon/Prospek_Atsiri_di_Indonesia.pdf, diakses tanggal 26 April 2009.
Setyowati, E.P., Jenie, U.A., dkk, 2007, Isolasi Senyawa Sitotoksik Spon Kaliapsis, Majalah Farmasi Indonesia, 185.
Sigma-Aldrich, 2010, Eugenol Natural ≥98%,
40
Sigma-Aldrich, 2010, Eugenyl Acetate,
http://www.sigmaaldrich.com/catalog/ProductDetail.do?lang=en&N4= W246905|ALDRICH&N5=SEARCH_CONCAT_PNO|BRAND_KEY& F=SPEC, diakses tanggal 5 Januari 2011.
Silverstein, R.M., and Webster, F.X., 1998, Spectrometric Identification of Organic Compound, John Wiley & Sons Inc., New York, 2.
Srivastava, K.C., andMalhotra N., 1991, Acetyl Eugenol, a Component of Oil of Cloves (Syzygium aromatikum L.) Inhibits Aggregation and Alters Arachidonic Acid Metabolism in Human Blood Platelets, NCBI, 42(1),
73-81.
Suggs, J., 2002, Organic Chemistry, Barron’s Education Series, New York, 205.
Supardjan, A.M, 2004, Sintesis Diasetil Heksagamavunon-1 dengan Katalis Basa,
Pharmacon, 5(2), 48-55.
Sykes, P., 1985, A Guide Book to Mechanism in Organic Chemistry,
diterjemahkan oleh Hartono, A.J., Sugiharjo, C.J., Broto, S.K.L., dan Sukartini, Edisi 6, Penerbit Gramedia, Jakarta, 268-269.
Tarigan, H.Y.S., 2009, Sintesis 4-Alil-2-Metoksi Fenil Laurat melalui Reaksi Transesterifikasi antara 4-Alil-2-Metoksi Fenil Asetat dengan Metil Laurat, Skripsi, Universitas Sumatra Utara, Medan, 9-13.
University of Birmingham, 2010, Eugenol Proton NMR Spectrum,
41
42
Lampiran 1. Perhitungan Rendemen Asetil Eugenol
O
Perhitungan massa teoritis asetil eugenol Kerapatan eugenol = 1,06 g/ml
Massa eugenol = 5,0 ml x 1,06 g/ml
Massa teoritis asetil eugenol = mol asetil eugenol x BM asetil eugenol = 0,0323 mol x 206 g/mol
= 6,654 gram Perhitungan massa asetil eugenol hasil sintesis Massa senyawa hasil sintesis = 5,336 gram Presentase asetil eugenol (KG) = 97,94 %
43
Lampiran 2. Foto Penelitian A. Rangkaian alat sintesis
44
45
46
47
48
Lampiran 6. Spektra Infra Merah Senyawa Tunggal A. Eugenol
(Food and Agriculture Organization of The United Nations, 2010a)
B. Asetil Eugenol
49
50
Lampiran 8. Spektra 1H-NMR Eugenol
51
BIOGRAFI PENULIS
Penulis skripsi dengan judul “Sintesis Asetil Eugenol dari Eugenol dan Anhdrida Asam Asetat dengan Katalis Kalium Hidroksida” ini memiliki nama lengkap Albertus Eka Yudistira Sarwono dengan
nama panggilan “Yudi”. Penulis lahir tanggal 9
Maret 1989 di Murray, Kentucky sebagai putra pertama dari tiga bersaudara, pasangan Slamet S. Sarwono dan Yasinta Tamalo.
i