BAB I. PENDAHULUAN
I.1 Latar belakang
Krom ( Cr ) merupakan salah satu unsur yang keberadaannya di lingkungan perlu dikendalikan mengingat sifatnya yang dapat mempengaruhi terhadap kesehatan manusia serta makhluk hidup lainnya. Sifat yang dimiliki krom adalah unik bergantung pada spesinya. Dilaporkan bahwa Cr (III) bermanfaat dalam proses metabolisme glukosa, lemak dan protein pada makhluk hidup. Akan tetapi Cr(VI) merupakan oksidator kuat dan bersifat sangat toksik serta karsinogenik(1).
Akhir-akhir ini dengan semakin meningkatnya kesadaran masyarakat terhadap masalah lingkungan, kadar logam krom dalam tekstil dan produk tekstil (TPT) pun dibatasi. Keberadaan krom dalam TPT diperkirakan berasal dari bahan kimia dan zat warna yang digunakan dalam proses pencelupan. Dalam Ökotex Standard 100, yaitu suatu persyaratan kriteria ekolabel tekstil dan produk tekstil dari negara Jerman telah menetapkan bahwa kandungan krom total dalam TPT untuk bayi tidak boleh melebihi 1 mg/Kg, dan TPT untuk keperluan lainnya maksimum 2 mg/Kg, sedangkan kadar Cr(VI) dibatasi maksimum 0,5 mg/kg(5). Dalam Ökotex Standard 200 yaitu standar lainnya yang mengatur ketentuan metode analisis yang harus digunakan untuk pengujian kriteria ekolabel TPT, telah ditetapkan bahwa penentuan kadar logam dalam TPT termasuk logam Cr harus dilakukan dengan cara mengekstraksi contoh tekstil menggunakan larutan keringat asam buatan dan penentuannya secara spektrometri serapan atom(6). Namun demikian metode tersebut tidak dijelaskan secara rinci.
Oleh karena kandungan Cr (VI) dalam TPT diperkirakan dalam jumlah renik, maka dalam analisisnya perlu melalui proses pemisahan dan prakonsentrasi terlebih dahulu agar dapat dilakukan penentuannya secara spektrometri serapan atom. Dengan maksud untuk mempermudah serta mempersingkat waktu pengerjaan analisis, pada penelitian ini dilakukan proses pemisahan dan prakonsentrasi Cr (VI) dalam contoh tekstil dengan cara kopresipitasi menggunakan zat pengkompleks APDC dan nikel sebagai pembawa (carrier). Terhadap endapan kompleks yang terjadi dilakukan proses penyaringan dan pelarutan kembali menggunakan asam nitrat pekat. Penentuan kadar krom dalam contoh uji dilakukan secara spektrometri serapan atom tungku karbon (SSATK).
I.2 Tujuan Penelitian
Tujuan penelitian ini adalah mengembangkan metode analisis Cr (VI) dalam contoh tekstil dengan cara prakonsentrasi menggunakan kombinasi amonium pirolidin ditiokarbamat (APDC) dan Ni serta penentuannya secara spektrometri serapan atom tungku karbon (SSATK).
BAB II. TINJAUAN PUSTAKA
II.1 Logam krom ( Cr ) dalam tekstil
Secara alamiah krom dapat ditemukan dalam batuan, tanah, debu vulkanik, binatang dan tumbuhan. Krom di lingkungan umumnya dalam bentuk Cr (0), Cr (III) dan Cr(VI). Keberadaan krom di lingkungan sebagian besar berasal dari limbah industri seperti industri baja, elektroplating, industri yang melakukan proses tanning, industri kimia, pencelupan tekstil dan lain-lain. Tingkat oksidasi krom yang penting adalah +3 dan +6. Kedua spesi krom tersebut mempunyai sifat dan dampak yang berbeda terhadap kesehatan manusia. Cr (III) dalam jumlah besar dapat mempengaruhi berbagai reaksi enzimatis dan dapat bereaksi dengan zat organik, namun demikian dilaporkan bahwa krom (III) dalam jumlah kecil diperlukan oleh makhluk hidup dalam proses metabolisme glukosa, lemak dan protein. Cr(VI) yang bersifat sebagai oksidator kuat dapat merusak jaringan sel dan bersifat toksik dan karsinogenik(1). Environtmental Protection Agency (EPA) telah menetapkan bahwa kadar krom total dalam air minum adalah 2,5 µg/L. Dilaporkan pula dalam www.osha.gov bahwa kontak kulit dengan senyawa Cr(VI) tertentu dapat menyebabkan penyakit kulit dan pada beberapa orang yang sensitif dapat menyebabkan reaksi alergik. Penelitian terhadap binatang diketahui Cr(VI) dapat meningkatkan resiko kanker paru-paru.
Adanya logam krom dalam tekstil kemungkinan berasal dari bahan kimia yang digunakan dalam proses tekstil maupun sebagai zat pengotor (impurities) yang terkandung dalam bahan kimia tersebut. Senyawa krom di industri tekstil terutama digunakan dalam proses pencelupan yang menggunakan zat warna direk dan zat warna mordan. Dalam proses pencelupan kain dengan zat warna direk, krom dalam bentuk senyawa dikromat digunakan untuk fiksasi zat warna tersebut pada serat kain, sedangkan dalam pencelupan dengan zat warna mordan krom digunakan dalam bentuk garam Cr(III). Salah satu contoh zat warna direk adalah Congo Red ( C.I. Direct red 28), sedangkan contoh zat warna mordan adalah Eriochrome Black T ( C.I Mordant Black 11 ) masing-masing memiliki rumus molekul seperti pada Gambar II.1. Zat warna direk adalah zat warna azo yang mengandung gugus sulfonat, namun demikian afinitasnya terhadap serat selulosa kecil dibanding dengan zat warna asam atau basa. Hasil pencelupan kain katun dengan zat warna direk memiliki ketahanan terhadap pencucian yang kurang baik, sehingga dalam prakteknya memerlukan perlakuan setelah proses pencelupan menggunakan garam elektrolit yang disebut dengan proses
fiksasi. Garam yang biasa digunakan adalah tembaga sulfat atau senyawa dikromat. Pada proses fiksasi atom oksigen pada gugus OH dalam zat warna akan membentuk kompleks dengan logam yang berasal dari garam elektrolit, menyebabkan ukuran molekul zat warna menjadi lebih besar dan kurang larut dalam air, sehingga tahan luntur terhadap pencucian menjadi meningkat(2-3).
Congo Red Eriochrome Black T ( C.I. Direct red 28) ( C.I Mordant Black 11 )
Gambar II.1 Struktur zat warna direk dan mordan
Di samping berasal dari bahan kimia yang digunakan dalam proses tekstil, keberadaan krom dalam tekstil juga dapat berasal dari pengotor zat warna. Zat warna tekstil yang digunakan memiliki kualitas teknis sehingga terdapatnya pengotor dalam zat warna termasuk logam-logam berat sangat dimungkinkan. Hal ini ditegaskan sebagaimana yang tercantum dalam kriteria ekolabel Uni-Eropa yang mempersyaratkan penggunaan zat warna yang memiliki kadar pengotor logam-logam berat dalam jumlah tertentu. Dalam ekolabel tersebut ditetapkan kadar Cr dalam zat warna yang digunakan dalam proses tekstil maksimum 100 ppm(4).
II.2 Prakonsentrasi krom
Berbagai teknik dapat digunakan dalam penentuan logam krom renik dalam air. Analisis instrumental secara langsung biasanya sulit dilakukan dikarenakan adanya kemungkinan gangguan matriks contoh yang dapat mempengaruhi hasil analisis serta konsentrasi krom dalam contoh yang sangat rendah mendekati atau bahkan jauh di bawah limit deteksi alat/instrumen yang digunakan. Untuk mengatasi masalah tersebut, proses pemisahan dan prakonsentrasi perlu dilakukan. Teknik prakonsentrasi dapat dilakukan dengan beberapa cara seperti ekstraksi pelarut, pertukaran ion, ekstraksi fasa padat dan kopresipitasi.
Proses spesiasi dan prakonsentrasi Cr (VI) dapat dilakukan dengan menggunakan zat pengompleks amonium pirolidinditiokarbamat (APDC), kemudian diekstraksi dengan menggunakan pelarut metil isobutil keton (MIBK). Penentuan Cr(VI) dilakukan langsung dari ekstrak secara spektrometri serapan atom tungku karbon (SAATK), sedangkan Cr (III) ditentukan dari selisih antara kadar krom total dan Cr (VI). Kondisi reaksi pembentukan kompleks antara Cr(VI) dan APDC diketahui optimum pada pH 3,5. Limit deteksi untuk Cr (III) dan Cr (VI) adalah 0,3 µg/L(7).
Spesi Cr (III) dapat diprakonsentrasi menggunakan teknik pertukaran ion. Kelebihan dari teknik ini adalah kolom resin yang dipakai dapat digunakan berulang-ulang, sedangkan kekurangannya adalah sering terjadi masalah ketika proses desorpsi lambat sehingga diperlukan modifikasi secara kimia terhadap resin tersebut. Resin penukar ion yang secara luas digunakan adalah amberlit XAD, karena resin tersebut mempunyai sifat adsorpsi dan kemurnian yang baik. Resin amberlit XAD-16 dalam penelitian spesiasi beberapa logam berat termasuk di dalamnya Cr (III) diperoleh hasil recovery Cr (III) mencapai ≥ 95 % dengan limit deteksi 0,008 µg/mL(8).
Prakonsentrasi Cr (III) juga dapat dilakukan dengan cara kopresipitasi yakni didasarkan pada pembentukan senyawa kompleks yang dapat mengendap. Sebagai kopresipitan biasanya digunakan senyawa hidroksida unsur tanah jarang seperti galium, indium, scandium, terbium. Telah dilaporkan bahwa terbium mempunyai kemampuan sebagai kopresipitan yang baik untuk analisis Cr (III), Cu(II) dan Pb(II)(9). Percobaan yang dilakukannya adalah dengan cara mencampurkan contoh analit dengan larutan terbium hidroksida dalam gelas kimia pada beberapa variasi pH. Endapan yang terjadi dipisahkan dan dilarutkan dengan asam nitrat 0,85 M. Larutan hasil prakonsentrasi kemudian ditentukan secara spektrometri serapan atom tungku karbon. Diperoleh hasil bahwa recovery Cr(III) mencapai hampir 100 % pada pH 8,4 – 10,8 dan limit deteksinya diketahui sebesar 0,3 µg/L. Dilaporkan pula bahwa adanya terbium hingga 7 g/L dalam contoh uji tidak mengganggu dalam penentuan analit. Peneliti lainnyatelah berhasil melakukan percobaan kopresipitasi Cr (III) dalam contoh air alam menggunakan kopresipitan kombinasi kompleks Pd/8-quinolinol/asam tannic dan penentuannya secara spektrometri serapan atom tungku karbon(10). Ditemukan bahwa kondisi kopresipitasi optimum terjadi pada pH 5,1 - 5,3. Limit deteksi untuk Cr(III) adalah 20 ng/L untuk 300 mL contoh air yang digunakan.
Teknik prakonsentrasi lainnya adalah ekstraksi fasa padat. Pada umumnya teknik ini didasarkan pada sifat adsorpsi analit pada kolom adsorben seperti C18 ,
alumina aktif, selulosa Cellex T, dan politetrafluoroetilen (PTFE). Dengan teknik ekstraksi fasa padat telah berhasil dilakukan prakonsentrasi Cr(VI) menggunakan kolom politetrafluoroetilen (PTFE)(11). Pertama-tama contoh analit dicampurkan dengan larutan APDC pada berbagai variasi pH, kemudian khelat Cr-PDC dilewatkan ke dalam kolom PTFE. Proses elusi dilakukan dengan menggunakan pelarut MIBK dan eluat secara langsung dialirkan masuk ke dalam sistem nyala spektrometer serapan atom. Dilaporkan bahwa kurva kalibrasi linear terjadi pada rentang konsentrasi 1 – 40 µg/L dan limit deteksinya adalah 0,8 µg/L. Standar deviasi relatif 3,2 % pada konsentrasi 20 µg/L.
Zat pengkompleks amonium pirolidin ditiokarbamat (APDC) yang mempunyai rumus kimia C5H9NS2. NH3 telah dikenal secara luas sebagai zat pengkomplek yang
dapat digunakan dalam analisis logam berat renik seperti Pb, Ni, Cu, Sn, Co, Cd, Mn, Zn dan Cr . Dilaporkan bahwa Cr(VI) dalam air dapat bereaksi cepat dengan APDC menjadi Cr(III) dan segera membentuk komplek Cr-PDC pada kondisi pH asam dan temperatur kamar. Sedangkan Cr(III) dengan APDC pada kondisi yang sama bereaksi lambat, hal ini disebabkan karena Cr(III) dalam air berada dalam keadaan terhidrasi sangat kuat sehingga sulit membentuk kompleks dengan APDC. Dengan demikian APDC dapat digunakan dalam spesiasi logam Cr(VI) dan Cr(III) dalam air. Lebih jauh telah diketahui bahwa APDC memiliki sifat lebih stabil pada pH rendah dibandingkan dengan natrium dietilditiokarbamat (DDTC). Pada pH rendah DDTC mudah terdekomposisi. Hasil karakterisasi menggunakan kromatografi lapis tipis, difraksi sinar-X, spektroskopi IR dan spektrometri massa yang dilakukan menunjukkan bahwa hasil reaksi Cr(VI) dengan APDC pada pH asam adalah dua bentuk kompleks yakni Cr(PDC)3 dan Cr(PDC)2(OPDC) sebagai produk utamanya(12).
II.3. Spektrometri serapan atom tungku karbon (SSATK)(13)
Pada prinsipnya mekanisme spektrometri serapan atom tungku karbon sama dengan pada spektrometri serapan atom nyala, yang membedakan adalah proses pengatoman terjadi pada tabung karbon yang terpanasi oleh arus listrik secara terprogram. Sumber sinar dengan intensitas Io dipancarkan mengarah ke lorong tabung
karbon yang mengandung uap atom analit dalam keadaan dasar (ground state). Intensitas sinar akan berkurang dikarenakan sebagian terabsorpsi oleh atom-atom
analit ( I ). Jumlah sinar yang terserap ditentukan dengan cara membandingkan I terhadap Io. Absorban merupakan karakteristik sinar yang terabsorpsi dinyatakan
secara matematika sebagai A = log ( Io/I ). Hubungan absorban dengan konsentrasi
analit mengikuti hukum Beer’s. A = a b c Dimana a = koefisien absorpsi
b = panjang sel absorpsi yang terlewati cahaya c = konsentrasi analit.
Pada spektrometri serapan atom tungku karbon sinyal yang teramati bergantung pada massa, bukan pada konsentrasi. Sehingga sensitivitasnya dinyatakan dengan “ karaktristik massa” ( mo ). Karakteristik massa analog dengan karakteristik konsentrasi
pada spektrometri serapan atom nyala, yakni massa analit dalam pikogram yang diperlukan untuk menghasilkan sinyal tinggi puncak sebesar 0,0044 absorban atau sinyal luas puncak sebesar 0,0044 absorban.detik (A-s ).
Volume sampel ( µL ) x Konsentrasi sampel ( µg/L ) x 0,0044 A-s mo = ---
Luas puncak ( A-s )
Sistem tungku karbon pada spektrometri serapan atom dibangun oleh tiga
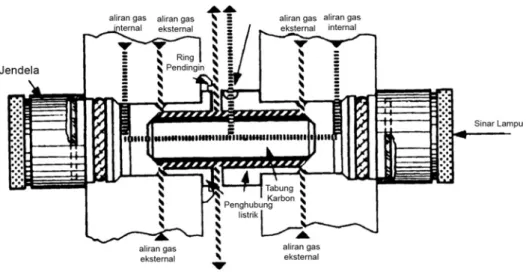
komponen utama yaitu unit pengatoman (atomizer), sumber daya listrik ( power supply ) dan unit pemograman. Unit pengatoman sebagaimana tampak pada
Gambar II.2 pada dasarnya terdiri atas tabung karbon, penghubung listrik ( electrical contact ), sistem pendingin dan pengaturan aliran gas inert. Tabung karbon merupakan elemen pemanas dimana terjadi proses pengatoman analit logam. Kedua ujung tabung karbon ditutup dengan jendela kwarsa. Lorong tabung karbon tersebut diarahkan lurus terhadap sinar datang. Ketika tabung karbon mengalami pemanasan, gas inert argon mengalir di sekelilingnya. Fungsi dari aliran gas argon adalah untuk mencegah terjadinya proses oksidasi terhadap tabung karbon ketika terjadi proses pemanasan. Aliran gas argon terbagi dua yakni aliran gas argon eksternal dan internal. Aliran gas
argon eksternal melindungi tabung karbon bagian luar, sedangkan aliran gas argon internal mengalir ke lorong tabung karbon dan alirannya dapat diatur. Pada saat proses pengatoman analit berlangsung, aliran gas argon internal ini dihentikan agar waktu tinggal uap atom analit logam dalam tabung karbon menjadi maksimal. Penghubung arus listrik berfungsi mengalirkan arus listrik di sepanjang tabung karbon, sehingga tabung karbon menjadi panas menyala, sedangkan suatu sistem pendingin digunakan untuk mendinginkan penghubung arus listrik tersebut.
Gambar II.2 Tungku karbon longitudinal
Sumber daya listrik dan pemograman melakukan fungsi pengaturan terhadap daya listrik, temperatur, aliran gas inert dan spektrometer, sehingga proses pemanasan sampel sesuai dengan yang diinginkan.
Beberapa mikro liter contoh disuntikkan melalui lubang kecil yang terdapat di bagian tengah atas tabung karbon. Pengaliran arus listrik secara terprogram terhadap tabung karbon menyebabkan contoh analit logam terpanasi dan akhirnya terjadi proses pengatoman. Uap atom logam kemudian akan mengabsorpsi sebagian intensitas sinar yang datang dari sumber sinar dan spektrometer mencatat absorban yang dihasilkan.
II.3.1 Tahapan program pemanasan pada tungku karbon
Larutan contoh yang telah disuntikkan ke dalam sistem tungku karbon akan mengalami beberapa tahap proses pemanasan secara terprogram selama berada di dalam tungku karbon. Tahap-tahap proses pemanasan yang terjadi meliputi proses
pengeringan, pirolisis, pengatoman, dan terakhir tahap pembersihan tungku karbon. Contoh tahap-tahap proses pemanasan tungku karbon dapat dilihat pada Gambar II.3.
2500 2000 º C 1500 1000 500 0 Atomisasi Pirolisis Pengeringan Waktu
Gambar II.3 Contoh tahap-tahap proses pemanasan tungku karbon Tahap proses pengeringan umumnya dilakukan pada temperatur 100 – 120 ºC selama kurang dari satu menit. Untuk mencapai temperatur tersebut, proses pemanasan berlangsung secara bertahap ( ramp ), sehingga percikan contoh dapat dicegah. Selama proses pengeringan, gas argon internal dialirkan secara maksimal sebesar 250 – 300 mL/menit agar uap pelarut contoh terdorong keluar dari tabung karbon.
Tahap pirolisis atau kadang-kadang disebut sebagai proses pengabuan bertujuan untuk menguapkan komponen matriks organik dan anorganik yang terkandung dalam contoh. Temperatur yang dipilih untuk proses pirolisis bergantung pada sifat matriks dan analit, biasanya temperatur dinaikkan setinggi mungkin namun tetap masih di bawah temperatur menguapnya analit. Pada tahap ini gas argon internal tetap mengalir seperti pada proses pengeringan dengan maksud agar uap matriks terdorong ke luar dari tabung karbon.
Tahap pengatoman bertujuan untuk pembentukan uap atom analit. Temperatur pengatoman berbeda untuk setiap analit logam. Temperatur tabung karbon dinaikkan dengan cepat. Perlu diperhatikan bahwa temperatur pengatoman jangan
terlampau tinggi, karena hal ini dapat mempersingkat waktu tinggal uap atom analit dalam tabung karbon dan menurunkan sensitivitas. Di samping itu penggunaan temperatur pengatoman yang terlampau tinggi dapat memperpendek umur tabung karbon.
Tahap pembersihan dimaksudkan untuk menghilangkan residu contoh yang kemungkinan tertinggal dalam tabung karbon. Temperatur yang digunakan pada tahap ini biasanya lebih tinggi dari temperatur tahap pengatoman. Proses pembersihan tidak boleh terlampau lama karena dapat memperpendek umur tabung karbon.
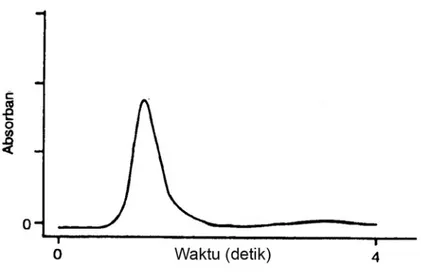
II.3.2 Profil signal pada tungku karbon
Dalam spektrometri serapan atom nyala, signal absorpsi keadaannya steady sehingga absorban yang teramati konstan selama proses penyedotan larutan contoh ke dalam nyala berlangsung. Akan tetapi tidak demikian halnya dalam spektrometri serapan atom tungku karbon, pembentukan atom analit berlangsung pertama-tama meningkat kemudian menurun, sehingga signal yang terjadi berbentuk puncak yang merefleksikan populasi atom analit terhadap waktu proses pengatoman seperti pada Gambar II.4. Luas puncak sebanding dengan jumlah atom analit dalam larutan contoh yang disuntikkan ke dalam tungku.
BAB III. METODOLOGI PENELITIAN
III.1 Peralatan
Peralatan yang digunakan dalam penelitian ini adalah sebagai berikut : - Spektrometer serapan atom ( Perkin-Elmer tipe Aanalyst 100 )
- Tungku karbon ( Perkin-Elmer HGA-800 ) - pH meter ( Schott-Handylab 1 )
- Pengaduk magnet ( Magnetic stirrer )
- Filter membran selulosa asetat ( WhatmanΦ 47 mm, pori 0,45 µm ) - Alat filtrasi dan pompa vakum ( Millipore )
- Alat pemurnian aquades Nanopure ( USF-Elga ) - Pemanas listrik ( Hot plate )
- Alat gelas ( labu ukur, beaker glass, pipet dan lain-lain) - Pipet mikro volume 20-200 µL, 100-1000 µL
III.2 Bahan-bahan
Bahan-bahan kimia yang digunakan dalam penelitian ini berkualitas pro analisis (pa) produk Merck dan Sigma-Aldrich sebagai berikut :
- Amonium pirolidinditiokarbamat (APDC) - Kalium dikromat ( K2Cr2O7 )
- Kromium triklorida ( CrCl3 .6H2O )
- Magnesium nitrat ( Mg(NO3)2 . 6H2O )
- Nikel nitrat ( (Ni(NO3)2.6H2O )
- Kalium hidrogenftalat
- L-Histidin monoklorida monohidrat ( C6H9O2N3.HCl.H2O )
- Natrium dihidrogen fosfat dihidrat ( NaH2PO4.2H2O ).
- Natrium klorida ( NaCl ) - Natrium hidroksida ( NaOH ) - Asam klorida ( HCl )
- Aquades
III.3 Lokasi penelitian
Penelitian ini dilakukan di Laboratorium Penelitian Lingkungan Balai Besar Tekstil Departemen Perindustrian, Jl. Ahmad Yani Bandung No. 390 Bandung.
III.4 Diagram alir penelitian
III.4.1 Penentuan kondisi percobaan
- 100 mL larutan Cr(VI) 50 µg/L - pH larutan divariasikan 2 – 8 - ditambah 1 mL larutan APDC 3 g/L - disaring
pH Larutan
- 100 mL larutan Cr(VI) 50 µg/L - pH larutan optimum ( pH 4 )
- larutan APDC 3 g/L divariasikan 2 – 6 mL
Jumlah volume larutan APDC
- 100 mL variasi konsentrasi larutan Cr(VI) 5 - 40 µg/L
- pH 4
- ditambah 5 mL larutan APDC 3 g/L - 0,3 mL larutan Ni 1 g/L
- 100 mL larutan Cr(VI) 50 µg/L - pH 4
- ditambah 5 mL larutan APDC 3 g/L - volume larutan Ni 1 g/L divariasikan
0,1 – 0,8 mL Variasi konsentrasi larutan Cr(VI) Jumlah volume larutan Ni
III.4.2 Prakonsentrasi dan penentuan Cr(VI) dalam contoh tekstil
Sampel kain
- Diekstraksi dengan 100 mL larutan keringat buatan pH 5,5
Ekstrak
- Pada kondisi optimum direaksikan dengan larutan APDC 3 g/L dan Ni 1g/L.
- Filtrasi endapan dengan filter selulosa asetat 0,45 µm
Filtrat yang mengandung endapan
- Dilarutkan dengan 2 mL HNO3 pekat panas
dan diencerkan dengan aquades hingga volume 10 mL
Larutan
- Penentuan Cr secara spektrometri serapan tungku karbon
III.5 Pembuatan larutan
- Larutan induk Cr(VI) 1000 mg/L
0,283 gram K2Cr2O7 dilarutkan dengan aquades di dalam labu ukur 100 mL.
- Larutan induk Cr(III) 1000 mg/L
0,5125 gram CrCl3. 6H2O dilarutkan dengan aquades di dalam labu ukur 100 mL.
- Larutan Mg(NO3)2 0,5 g/L
0,058 gram Mg(NO3)2 .6H2O dilarutkan dengan aquades di dalam labu ukur 100 mL.
- Larutan Ni 1 g/L
0,4953 gram Ni(NO3)2.6H2O dilarutkan dengan aquades dalam labu ukur 100 mL.
0,3 gram APDC dilarutkan dengan aquades dalam labu ukur 100 mL. Larutan ini dibuat pada saat ketika hendak digunakan ( larutan segar ).
- Larutan bufer ftalat pH 4
1,0209 gram kalium hidrogen ftalat dilarutkan dengan 50 mL aquades, kemudian pH larutan ditepatkan hingga pH 4 dengan menggunakan larutan HCl 0,1M dan diencerkan dengan aquades hingga tanda batas labu ukur 100 mL.
- Larutan keringat buatan pH 5,5(14)
Ke dalam labu ukur 1 liter dimasukkan masing-masing 0,5 gram L-histidin monoklorida monohidrat (C6H9O2N3.HCl.H2O), 5 gram NaCl dan 2,2 gram
Na-dihidrogen ortofosfat dihidrat (NaH2PO4.2H2O) kemudian dilarutkan dengan
aquades. Larutan ditepatkan pHnya hingga 5,5 menggunakan larutan NaOH 0,1 M dan diencerkan dengan aquades hingga tanda batas labu ukur.
III.6 Prosedur percobaan
III.6.1 Penentuan kondisi percobaan
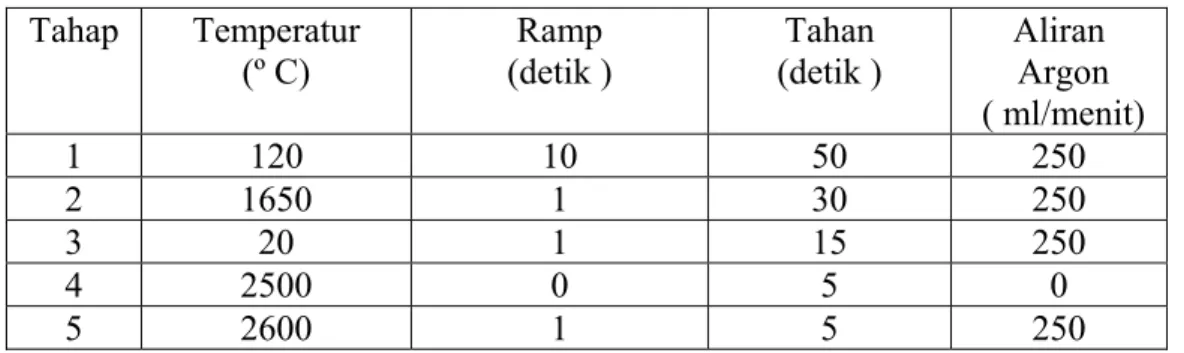
Variabel kondisi percobaan prakonsentrasi Cr(VI) yang ditentukan meliputi pH optimum larutan, jumlah pemakaian larutan APDC, jumlah pemakaian larutan Ni, dan rentang konsentrasi larutan Cr(VI). Penentuan Cr dalam larutan dilakukan secara spektrometri serapan tungku karbon dengan kondisi operasional seperti tertera pada Tabel III.1
Tabel III.1 Kondisi operasi tungku karbon Tahap Temperatur
(º C) (detik ) Ramp (detik ) Tahan Argon Aliran ( ml/menit) 1 120 10 50 250 2 1650 1 30 250 3 20 1 15 250 4 2500 0 5 0 5 2600 1 5 250
III.6.1.1 Penentuan pH optimum
Ke dalam beberapa gelas piala dimasukkan masing-masing 100 mL larutan Cr(VI) 50 µg/L dan dilakukan pengaturan variasi pH larutan 1 – 8 dengan penambahan larutan HCl 0,1 M atau larutan NaOH 0,1 M. Kemudian ke dalam masing-masing
gelas piala tersebut dimasukkan 1 mL larutan APDC ( 3 g/L) dan dilakukan proses pengadukan diatas pengaduk magnet (magnetic stirrer) selama 5 menit. Larutan selanjutnya disaring dengan menggunakan filter selulosa asetat 0,45 µm dengan kecepatan 25 mL/menit. Filter selulosa asetat yang telah digunakan dipindahkan ke dalam gelas piala dan ditambahkan 2 mL HNO3 pekat kemudian dibiarkan hingga
filter larut. Larutan dipindahkan ke dalam labu ukur 100 mL kemudian ditambahkan 1 mL Mg(NO3)2 ( 0,5 g/L ) dan diencerkan dengan aquades hingga tanda batas labu
ukur. Larutan diukur absorbansinya menggunakan spektrometer serapan atom tungku karbon.
III.6.1.2 Penentuan jumlah larutan APDC yang ditambahkan
Ke dalam beberapa gelas piala dimasukkan masing-masing 100 mL larutan Cr(VI) 50 µg/L, 5 mL larutan bufer pH 4, dan sejumlah variasi volum ( 2 – 6 mL ) larutan APDC ( 3 g/L) kemudian diaduk dengan menggunakan pengaduk magnet selama 5 menit. Larutan selanjutnya disaring menggunakan filter selulosa asetat 0,45 µm dengan kecepatan 25 mL/menit. Filter selulosa asetat yang telah digunakan dipindahkan ke dalam gelas piala dan ditambahkan 2 mL HNO3 pekat kemudian
dibiarkan hingga filter larut. Larutan dipindahkan ke dalam labu ukur 100 mL kemudian ditambahkan 1 mL Mg(NO3)2 ( 0,5 g/L ) dan diencerkan dengan aquades
hingga tanda batas labu ukur. Larutan diukur absorbansinya menggunakan spektrometer serapan atom tungku karbon.
III.6.1.3 Penentuan jumlah larutan Ni yang ditambahkan
Ke dalam beberapa gelas piala dimasukkan masing-masing 100 mL larutan Cr(VI) 50 µg/L, 5 mL larutan bufer pH 4, 5 mL larutan APDC ( 3 g/L ) dan sejumlah variasi volume 0,1– 0,6 mL larutan Ni ( 1 g/L) kemudian diaduk dengan menggunakan pengaduk magnet selama 5 menit. Larutan selanjutnya disaring menggunakan filter selulosa asetat 0,45 µm dengan kecepatan 25 mL/menit. Filter selulosa asetat yang telah digunakan dipindahkan ke dalam gelas piala dan ditambahkan 2 mL HNO3 pekat kemudian dipanaskan hingga filter larut. Larutan
dipindahkan ke dalam labu ukur 100 mL kemudian ditambahkan 1 mL Mg(NO3)2 ( 0,5
g/L ) dan diencerkan dengan aquades hingga tanda batas labu ukur. Larutan diukur absorbansinya menggunakan spektrometer serapan atom tungku karbon.
III.6.1.4 Pengaruh konsentrasi larutan Cr (VI)
Dipipet larutan standar Cr (VI) 1 mg/L sebanyak 0,5; 1,0; 1,5; 2,0; 3,0; 4,0 dan 5,0 mL dan masing-masing dimasukkan ke dalam labu ukur 100 mL, kemudian diencerkan dengan aquades hingga tanda batas labu ukur. Larutan standar dengan variasi konsentrasi tersebut dipindahkan ke dalam gelas kimia dan ditambahkan berturut-turut 5 mL larutan bufer ftalat pH 4, 5 mL APDC ( 3 g/L) dan 0,3 mL larutan Ni (1 g/L), kemudian dikocok dengan pengaduk magnet selama 5 menit dan disaring menggunakan kertas saring selulosa asetat 0,45 µm. Filter selulosa asetat yang telah digunakan dipindahkan ke dalam gelas piala dan ditambahkan 2 mL HNO3 pekat
kemudian dipanaskan hingga filter larut. Larutan dipindahkan ke dalam labu ukur 100 mL kemudian ditambahkan 1 mL Mg(NO3)2 ( 0,5 g/L ) dan diencerkan dengan
aquades hingga tanda batas labu ukur. Larutan diukur absorbansinya menggunakan spektrometer serapan atom tungku karbon.
III.6.2 Prakonsentrasi
III.6.2.1 Pengaruh Cr (III) dalam larutan
Dipipet 100 mL larutan tandar Cr(VI) 5 µg/L, 100 mL Cr (III) 5 µg/L serta campuran Cr (VI) 10 µg/L dan Cr(III) 10 µg/L masing-masing sebanyak 50 mL dan dimasukkan ke dalam gelas piala 250 mL. Ke dalam masing-masing larutan ditambahkan berturut-turut 5 mL larutan buffer pH 4, 5 mL larutan APDC ( 3 g/L) dan 0,3 mL Ni (1 g/L), kemudian larutan diaduk dengan pengaduk magnet selama 5 menit dan disaring dengan filter selulosa asetat 0,45 µm dengan kecepatan 25 ml/menit. Filter selulosa asetat yang telah digunakan dipindahkan ke dalam gelas piala dan ditambahkan 2 mL HNO3 pekat kemudian dipanaskan hingga filter larut. Larutan
dipindahkan ke dalam labu ukur 10 mL kemudian ditambahkan 1 mL Mg(NO3)2
( 0,5 g/L ) dan diencerkan dengan aquades hingga tanda batas labu ukur. Larutan diukur absorbansinya menggunakan spektrometer serapan atom tungku karbon.
III.6.2.2 Pengaruh matriks ekstrak tekstil
Pertama-tama ekstrak kain dipersiapkan dengan cara merendam sambil sesekali mengaduk setiap 2 gram contoh kain dengn 100 mL larutan bufer ptalat pH 4 selama 30 menit. Sebanyak 0,5 mL larutan Cr(VI) 1 mg/L dimasukkan ke dalam labu ukur 100 mL dan diencerkan dengan ekstrak kain hingga tanda batas labu ukur. Larutan selanjutnya dipindahkan ke dalam gelas kimia 250 mL dan ditambahkan berturut-turut
5 mL larutan APDC (3 g/L), dan 0,3 ml larutan Ni (1 g/L). Kemudian dilakukan proses pengadukan menggunakan pengaduk magnet selama 5 menit dan penyaringan dengan filter selulosa asetat 0,45 µm. Filter selulosa asetat yang telah digunakan dipindahkan ke dalam gelas piala dan ditambahkan 2 mL HNO3 pekat kemudian dipanaskan hingga
filter larut. Larutan dipindahkan ke dalam labu ukur 10 mL kemudian ditambahkan 1 mL Mg(NO3)2 ( 0,5 g/L ) dan diencerkan dengan aquades hingga tanda batas labu
ukur. Larutan diukur absorbansinya menggunakan spektrometer serapan atom tungku karbon.
III.6.3 Aplikasi metode parakonsentrasi terhadap contoh tekstil III.6.3.1 Persiapan contoh kain
Contoh kain/tekstil yang digunakan dalam penelitian ini adalah contoh kain komersial yang diambil dari Laboratorium Pengujian Tekstil Balai Besar Tekstil dan kain hasil pencelupan sendiri.
Kain yang dicelup adalah kain katun 100 % dengan tahapan proses pencelupan sebagai berikut :
- Proses Pencelupan
Contoh kain katun dicelup dengan vlot 1 : 20. Kain katun dicelup dengan larutan celup dengan komposisi zat warna direct yellow RL dan direct red BNLE 3 %, zat pembasah 1 ml/L, natrium karbonat 1 g/L, dan NaCl 10 g/L. Proses pencelupan dilakukan pada temperatur 95 ºC selama 60 menit, kemudian dilakukan proses pencucian dan pembilasan dengan menggunakan air kran.
- Proses Penyabunan
Kain yang telah dicelup kemudian dicuci dengan larutan sabun teepol 2 ml/L pada temperatur 80 ºC selama 10 menit, kemudian dilakukan proses pembilasan dengan menggunakan air kran.
- Proses Fiksasi
Kain yang telah mengalami proses pencucian kemudian difiksasi dngan menggunakan larutan K2Cr2O7 2 g/L pada temperatur 70 ºC selama 20 menit,
kemudian diperas dan dikeringkan.
III.6.3.2 Penentuan Cr(VI) dalam contoh kain
2 gram contoh kain/tekstil diekstraksi dengan 100 mL larutan keringat buatan pH 5,5 selama 30 menit. pH ekstrak kain kemudian diatur hingga pH 4 dengan larutan
HCl 0,1 M serta ditambahkan berturut-turut 5 mL larutan APDC (3 g/L) dan 0,3 mL larutan Ni (1 g/L). Kemudian larutan diaduk dengan pengaduk magnet selama 5 menit dan disaring dengan filter selulosa asetat dengan kecepatan 25 mL/menit. Filter selulosa asetat yang telah digunakan dimasukkan ke dalam gelas piala dan ditambahkan 2 mL HNO3 pekat, kemudian dipanaskan hingga filter sellulosa asetat
larut. Larutan dipindahkan ke dalam labu ukur 10 mL, ditambah1 mL Mg(NO3)2
( 5 g/L ) dan diencerkan dengan aquades hingga tanda batas labu ukur. Absorban larutan ditentukan menggunakan spektrometri serapan atom tungku karbon.
III.6.3.3 Penentuan limit deteksi
Ke dalam masing-masing gelas piala dimasukkan 100 mL aquades, 100 mL larutan tandar Cr(VI) 2 ppb dan 5 ppb. Kemudian berturut-turut ditambahkan 5 mL larutan buffer pH 4, 5 mL larutan APDC ( 3 g/L) dan 0,3 mL Ni (1 g/L). Campuran larutan diaduk dengan pengaduk magnet selama 5 menit dan disaring dengan filter selulosa asetat dengan kecepatan 25 mL/menit. Filter selulosa asetat yang telah digunakan dimasukkan ke dalam gelas piala dan ditambahkan 2 mL HNO3 pekat,
kemudian dipanaskan hingga filter sellulosa asetat larut. Larutan selanjutnya dipindahkan ke dalam labu ukur 10 mL, ditambah 1 mL Mg(NO3)2 ( 5 g/L ) dan
diencerkan dengan aquades hingga tanda batas labu ukur. Absorban larutan ditentukan menggunakan spektrometri serapan atom tungku karbon.
BAB IV. HASIL DAN PEMBAHASAN
IV.1 Pengaruh pH larutan terhadap pembentukan Cr-PDC
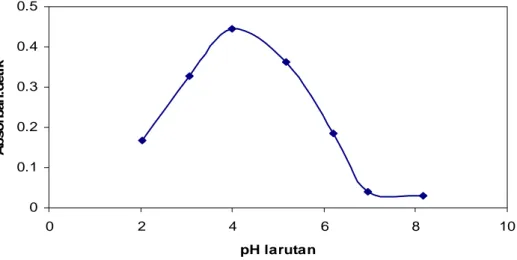
pH merupakan faktor yang penting dalam pembentukan senyawa kompleks, oleh karena itu perlu dilakukan percobaan penentuan pH optimum pembentukan kompleks Cr-PDC. Percobaan yang dilakukan dimulai dari pH 2 sampai dengan pH 8 dan memberikan hasil sebagaimana terlihat pada Gambar IV.1. Dari bentuk kurva yang diperoleh menunjukkan bahwa mulai pH 2 hingga pH 4 nilai luas puncak (absorban.detik) meningkat, kemudian pada pH 5 dan seterusnya nilai absorban yang teramati terus menurun hampir mendekati nol. Dengan demikian pH 4 dapat ditetapkan sebagai pH optimum pembentukan komplek Cr-PDC dan digunakan dalam percobaan berikutnya. 0 0.1 0.2 0.3 0.4 0.5 0 2 4 6 8 pH larutan A b so rb an .d et ik 10
Gambar IV.1 Pengaruh pH larutan terhadap pembentukan kompleks Cr-PDC
IV.2 Pengaruh jumlah larutan pengkompleks APDC
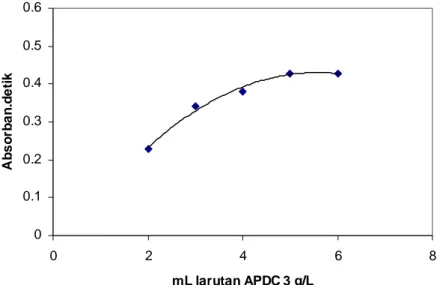
Agar dapat diketahui pengaruh jumlah larutan APDC yang diperlukan untuk mengikat krom dalam 100 mL larutan Cr(VI) 50 ppb, maka percobaan yang dilakukan adalah dengan cara menvariasikan penambahan volume larutan APDC ke dalam larutan tersebut. Hasil percobaan penambahan larutan APDC ( 3 g/L ) sebanyak 2 – 6 mL pada pH 4 yang merupakan pH optimum pembentukan kompleks Cr-PDC dapat dilihat pada Gambar IV.2. Pada penambahan larutan APDC sebanyak 2 mL hingga 5 mL terlihat nilai luas puncak absorban yang meningkat, akan tetapi pada penambahan larutan APDC sebanyak 6 mL nilai luas puncak absorban cenderung tetap. Penambahan larutan APDC lebih dari 5 mL tidak efisien untuk mengkhelat Cr yang
terkandung dalam larutan. Dengan demikian dalam percobaan selanjutnya penambahan larutan APDC ditetapkan sebanyak 5 mL.
0 0.1 0.2 0.3 0.4 0.5 0.6 0 2 4 6 mL larutan APDC 3 g/L A b so rb an .d et ik 8
Gambar IV.2 Pengaruh jumlah larutan APDC terhadap pembentukan kompleks Cr-PDC
Kemudian untuk mengetahui retensi kompleks Cr-PDC terhadap filter selulosa asetat dapat diamati dari persentase perolehan kembali ( recovery ) Cr yang dihasilkan. Percobaan dilakukan dengan cara mereaksikan 100 mL larutan Cr(VI) 50 µg/L dengan 5 mL larutan APDC pada pH 4 . Absorban larutan akhir diukur dan dialurkan ke dalam persamaan kurva kalibrasi pada Lampiran C.
Percobaan dengan pengulangan sebanyak empat kali, menghasilkan data sebagaimana tertera pada Tabel IV.1. Perolehan kembali yang dihasilkan berkisar 77 – 80 %, dengan rata-rata 79 ± 2 %. Untuk tujuan analisis kuantitatif hasil tersebut kurang memuaskan. Hal ini memperlihatkan bahwa interaksi antara kompleks Cr-PDC dengan filter selulosa kurang kuat sehingga ada sebagian kompleks Cr-PDC yang lolos melewati filter tersebut.
Tabel IV.1 Hasil percobaan retensi kompleks Cr-PDC terhadap filter selulosa asetat Konsentrasi Cr(VI) awal
(µg/L) Konsentrasi ditemukan (µg/L) Perolehan kembali (%)
50 38,90 78
50 38,66 77
50 39,92 80
50 39,84 80
IV.3 Pengaruh jumlah Ni yang ditambahkan
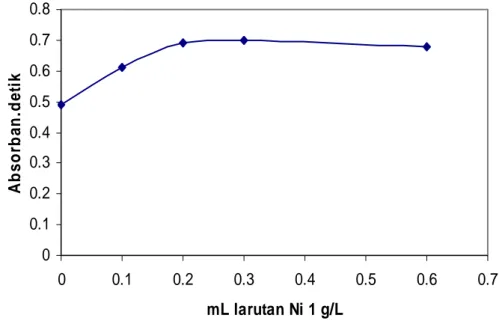
Penambahan Ni ke dalam larutan dimaksudkan untuk membantu meningkatkan retensi kompleks Cr-PDC terhadap filter selulosa asetat, sehingga absorban atau perolehan kembali dari metode prakonsentrasi yang dikembangkan ini menjadi dapat meningkat pula. Dari pengamatan secara visual, penambahan larutan Ni ke dalam larutan kompleks Cr-PDC menyebabkan terjadinya kekeruhan pada larutan. Kecenderungannya adalah semakin besar jumlah volume penambahan larutan Ni, kekeruhan pada larutan semakin meningkat pula. Hasil percobaan penambahan larutan Ni ke dalam larutan kompleks Cr-PDC dapat dilihat sebagaimana tertera pada Gambar IV.3. Penambahan larutan Ni ( 3 g/L ) sebanyak 0,1 – 0,3 mL memperlihatkan peningkatan signal luas puncak (absorban.detik) dari 0,49 hingga 0,70, akan tetapi luas puncak yang dihasilkan cenderung tetap pada penambahan larutan Ni berikutnya. Penambahan Ni sebagai carrier diduga menyebabkan terbentuknya senyawa Ni-Cr, sehingga dapat meningkatkan sensitivitas penentuan secara SSATK. Dengan demikian dapat ditetapkan bahwa penambahan larutan Ni ( 3g/L) yang efisien untuk percobaan berikutnya adalah sebanyak 0,3 mL.
0 0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0 0.1 0.2 0.3 0.4 0.5 0.6 0.7 mL larutan Ni 1 g/L A b so rb a n .d et ik
IV.4 Pengaruh konsentrasi larutan Cr(VI)
Untuk mengetahui hubungan antara jumlah Cr(VI) dalam larutan terhadap % perolehan kembali dengan cara prakonsentrasi sesuai prosedur, percobaan dilakukan dengan cara memvariasikan konsentrasi larutan Cr(VI) 5 – 40 µg/L pada kondisi percobaan yang telah diperoleh sebelumnya. Sebagaimana hasil percobaan yang tertera pada Tabel IV.2, perolehan kembali yang cukup baik terjadi pada konsentrasi larutan Cr(VI) di bawah 15 µg/L. Pada konsentrasi Cr(VI) diatas 15 µg/L perolehan kembali Cr(VI) menurun dikarenakan proses kopresipitasi ditentukan oleh jumlah APDC dan Ni yang ditambahkan . Pada kondisi ini zat pengompleks APDC yang ditambahkan ke dalam larutan seluruhnya telah berikatan dengan hanya sebagian Cr(VI) saja dan menyisakan sebagian lagi yang tidak terkopresipitasikan.
Tabel IV.2 Pengaruh konsentrasi larutan terhadap % perolehan kembali Konsentrasi Cr(VI) Awal (µg/L) Konsentrasi Cr(VI) ditemukan (µg/L) Perolehan kembali ( % ) 5 4,61 92 10 8,27 93 15 16,07 107 20 11,92 60 30 18,13 61 40 16,93 42
IV.5 Pengaruh Cr(III) terhadap perolehan kembali Cr(VI)
Di dalam literatur telah dilaporkan bahwa spesi Cr(III) dan Cr(VI) memiliki sifat berbeda ketika direaksikan dengan APDC pada pH rendah dan temperatur kamar. Untuk membuktikan hal tersebut, suatu percobaan telah dilakukan dengan cara mencampurkan kedua spesi Cr(III) dan Cr(VI), selanjutnya larutan campuran Cr diuji menggunakan metode yang dikembangkan pada kondisi percobaan optimum yang telah diperoleh sebelumnya. Hasil percobaan dapat dilihat pada Tabel IV.3. Terbukti bahwa spesi Cr(III) tidak mengganggu terhadap perolehan Cr(VI). Pada kondisi percobaan Cr(III) sukar membentuk komplek dengan APDC dikarenakan Cr(III) berada dalam bentuk terhidrasi yang sangat kuat, sedangkan Cr(VI) akan tereduksi oleh APDC menjadi Cr(III) dan segera membentuk kompleks dengan APDC(1) .
Tabel IV.3 Pengaruh Cr(III) terhadap % perolehan kembali Cr(VI) No. Sampel Konsonsentrasi
Awal (µg/L) Konsentrasi ditemukan (µg/L) Perolehan kembali ( % ) 1 Cr(III) 5 0,46 9 2 Cr(VI) 5 4,75 95 3 Campuran Cr (VI) dan Cr(III) Cr(III) = 5 Cr(VI) = 5 4,80 96
IV.6 Pengaruh matriks contoh kain
Ketika contoh tekstil diekstraksi menggunakan larutan keringat asam kemungkinannya tidak hanya logam-logam saja yang terektraksi melainkan juga zat-zat lainnya akan ikut terekstraksi, sehingga menghasilkan suatu matriks tertentu yang perlu dipertimbangkan pengaruhnya terhadap hasil prakonsentrasi. Matriks tersebut terbentuk disamping oleh zat yang digunakan dalam pembuatan larutan keringat, juga oleh zat-zat pembantu tekstil yang terkandung dalam contoh tekstil. Untuk mengetahui pengaruh matriks larutan ekstrak tekstil terhadap prakonsentrasi Cr(VI), pada percobaan ini pengaruh matrik larutan ekstrak kain tekstil diuji dengan cara menambahkan (spike) sejumlah larutan Cr(VI) ke dalam larutan hasil ekstraksi kain tekstil dengan larutan keringat asam. Hasil percobaan disajikan pada Tabel IV.4. Dari hasil percobaan dengan tiga kali ulangan diperoleh perolehan kembali sebesar 95 ± 1%, hal ini menunjukkan bahwa matrik larutan ekstrak kain relatif tidak mempengaruhi terhadap hasil perolehan kembali Cr(VI).
Tabel IV.4 Pengaruh matriks ekstrak kain terhadap % perolehan kembali Cr(VI) Konsentrasi Cr(VI) (µg/L) Spike Cr(VI) (µg/L) Faktor Prakonsentrasi ( P ) teoritis ditemukan Perolehan kembali (%) 5 10 50 47,12 94 5 10 50 48,12 96 5 10 50 47,50 95 Rata-rata 95 ± 1
IV.7 Kinerja analitik IV.7.1 Kebolehulangan
Kebolehulangan ( presisi ) dapat diartikan sebagai kedekatan antara nilai-nilai yang dihasilkan dari suatu pengukuran yang dilakukan menggunakan cara yang persis sama. Umumnya kebolehulangan ditentukan dengan melakukan pengukuran dengan beberapa kali ulangan. Kebolehulangan antara lain dapat dinyatakan dengan koefisien variansi (KV) . Koefisiensi variansi merupakan persentasi standar deviasi atau standar deviasi dikalikan dengan 100 %.
Hasil penentuan koefisien variansi dari pengukuran spike larutan standar Cr(VI) 5 ug/L dalam ekstrak kain yang dijadikan sebagai matriks larutan menggunakan metode yang dikembangkan dengan pengulangan n = 3, memberikan hasil perolehan kembali dengan KV sebesar 1,1 %. Hasil perhitungan % KV dapat dilihat pada Lampiran F.
IV.7.2 Kurva kalibrasi
Dalam analisis kuantitatif secara spektrometri, untuk mengetahui kadar atau konsentrasi analit dalam contoh dilakukan dengan cara mengalurkan sinyal analitik yang terukur oleh instrumen ke dalam kurva kalibrasi. Kurva kalibrasi menyatakan hubungan antara respon sinyal yang dihasilkan terhadap sederet larutan analit yang telah diketahui konsentrasinya. Bentuk kurva kalibrasi yang umum digunakan dalam analisis adalah kurva linear. Hubungan linearitas antara variabel kurva kalibrasi dinyatakan dengan koefisien korelasi r, dimana nilai r berada dalam rentang -1 ≤ r ≤ 1. Suatu kurva kalibrasi linear positif sempurna jika r = 1. Namun demikian dalam praktek, nilai r yang ditemukan biasanya mendekati 1.
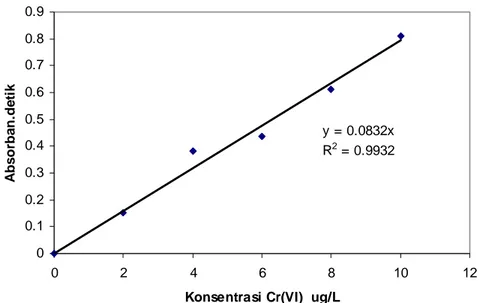
Untuk mengetahui apakah terjadi hubungan yang linear antara konsentrasi dengan respon sinyal (absorban.detik) yang dihasilkan, maka terhadap sejumlah variasi konsentrasi Cr(VI) 2 – 10 ug/L yang mengalami perlakukan sama sesuai dengan metode yang dikembangkan dilakukan pengukuran secara SSATK. Dari data hasil penentuan pada Lampiran G kemudian dibuat kurva kalibrasinya. Kurva kalibrasi terbukti cukup linear dengan nilai r = 0,9932 seperti tampak pada Gambar IV.4.
y = 0.0832x R2 = 0.9932 0 0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 0 2 4 6 8 10 12
Konsentrasi Cr(VI) ug/L
A b so rb a n .d eti k
Gambar IV.4 Kurva kalibrasi
IV.7.3 Limit deteksi
Limit deteksi didefinisikan sebagai konsentrasi terkecil analit yang memberikan sinyal terkecil dan dapat dibedakan dari sinyal blanko. Untuk mengetahui limit deteksi metode percobaan yang dikembangkan, maka dilakukan pengukuran dalam larutan blanko dan larutan standar Cr (VI) hasil prakonsentrasi dengan beberapa kali ulangan. Pada percobaan ini penentuan limit deteksi dilakukan dengan cara mengukur absorban larutan blanko dan larutan standar Cr(VI) 5 µg/L dengan ulangan n = 10 . Data penentuan limit deteksi dapat dilihat pada Tabel 6. Hasil perhitungan yang didasarkan pada 3 kali deviasi standar sinyal blanko diperoleh limit deteksi sebesar 3,48 µg/L.
IV.8 Penentuan Cr(VI) dalam contoh kain
Kondisi optimum yang diperoleh dari metode percobaan diaplikasikan untuk penentuan kadar Cr(VI) dalam contoh kain. Kain tekstil yang dijadikan contoh dalam percobaan ini adalah kain hasil pencelupan dan contoh kain komersial yang diperoleh dari Laboratorium Pengujian Balai Besar Tekstil. Pencelupan dilakukan dengan menggunakan dua jenis zat warna direk yang berbeda dengan proses fiksasi menggunakan K2Cr2O7 . Kedua jenis contoh kain yang disiapkan kemudian diekstraksi
diprakonsentrasi pada kondisi optimum percobaan menjadi 10 mL dan dilakukan penentuan kadar Cr(VI) secara spektrometri serapan atom tungku karbon. Hasil penentuan kadar Cr(VI) dalam contoh kain dapat dilihat pada Tabel 6. Kedua contoh kain hasil pencelupan masing-masing mengandung Cr(VI) sebesar 2,65 mg/kg kain dan 2,70 mg/kg kain, sedangkan contoh kain komersial diketahui tidak mengandung Cr(VI).
BAB V. KESIMPULAN DAN SARAN
V.1 Kesimpulan
Kompleksasi Cr (VI) menggunakan zat pengkomplek APDC dan Ni dapat digunakan untuk tujuan prakonsentrasi Cr(VI) dalam larutan. Dengan kondisi pembentukan kompleks Cr(VI) optimum pH 4, penggunaan pereaksi 5 mL larutan APDC (3g/L) dan 0,3 mL larutan Ni (1 g/L), prosedur ini cocok untuk larutan Cr(VI) dengan konsentrasi ≤ 15 µg/L. Matriks larutan ekstrak kain tekstil ternyata tidak mengganggu proses prakonsentrasi. Dengan menggunakan faktor prakonsentrasi 10, dihasilkan perolehan kembali (recovery) sebesar 95±1% dengan kebolehulangan (% KV) 1,1 %. Perhitungan yang didasarkan pada 3 x deviasi standar larutan blanko diperoleh limit deteksi sebesar 3,48 µg/L. Aplikasi metode ini dalam pengujian kadar Cr(VI) dalam 2 contoh kain hasil pencelupan sendiri menunjukkan kedua contoh kain tersebut mengandung Cr(VI) masing-masing 2,65 dan 2,70 mg/kg kain, sedangkan dalam 2 contoh kain komersial tidak terdeteksi mengandung Cr(VI).
V.2 Saran
Karena dalam penelitian ini ditemui kesulitan-kesulitan yang dapat mengganggu terhadap hasil analisis, disarankan untuk dilakukan penelitian lebih lanjut prakonsentrasi Cr(VI) menggunakan zat pengkompleks APDC dan Ni serta penentuannya secara spektrometri serapan atom tungku karbon yang dilengkapi dengan autosampler dan background Zeeman atau yang lainnya.
DAFTAR PUSTAKA
1. Chwastowska, J., Skawara, W., Sterlinska, E., Pszonicki, L. (2005), Speciation of chromium in mineral water and salinas by solid-phase extraction and graphite furnace atomic absorption spectrometry, Talanta, 66, 1345-1349.
2. Shore, J. (1990), Colorant and Auxiliaries, Society of Dyers and Colourists, Vol.1, Manchester, England, 177, 196 – 228.
3. Trotman, E.H. (1970), Dyeing and Chemical Technology of Textile Fibre, 4th Edition, Griffin & Co Ltd, 405 – 443.
4. The Commission of The European Communities (2002), Establishing the ecological criteria for the award of community eco-label to textile product and amending decision 1999/178/EC, Official Journal of European Communities, L 133, 29 – 41.
5. Ökotex Standard 100, General and special condition, International Association for Research and Testing in the Field of Textile Ecology, Zurich, 2000.
6. Ökotex Standard 200, Testing Procedures, Edition 01, Zurich, 2003.
7. Subramanian, K.S. (1988), Determination of chromium (III) and chromium(VI) by ammonium pyrrolidinecarbodithioate-methyl isobuthyl ketone furnace atomic absorption spectrometry, J. Anal. Chem, 60, 11 – 15.
8. Tokalioglu, E., Kartal, S., Elci, L. (2000), Speciation and determination of heavy metals in lake waters by atomic absorption spectrometry after sorption on amberlite XAD-16 resin, Analytical Science, 16, 1169-1174.
9. Minami, T., Sohrin, Y., Ueda, J. (2005), Determination of chromium, copper and Lead in river water by graphite furnace atomic absorption spectrometry after coprecipitation with terbium hydroxide, Analytical Science, 21, 1519-1521.
10.Zhang, Q., Minami, H., Inoue, S., Atsuya, I. (1999), Preconcentration by coprecipitation of chromium in natural waters with Pd/8-quinolinol/tannic acid complex and its direct determination by solid sampling atomic absorption spectrometry, Analitical Chimica Acta, 401, 277-282.
11.Anthemidis, A.N., Zachariadis, G.A., Kougoulis, J.S., Stratis, J.A. (2002), Flame atomic absorption spectrometric determination of chromium(VI) by on-line preconcentration system using a PTFE packed coloumn, Talanta, 57, 15-22.
12.Wang, J.S., Chiu, K.H. (2004), Simultaneous extraction of Cr(III) and Cr(VI) with a dithiocarbamate reagent followed by HPLC separation for chromium speciation, Analytical Science, 20, 841-846.
13.Beaty, R.D., Kerber, J.D. (1993), Concept instrumentation and techniques in atomic absorption spectrometry, The Perkin-Elmer Corporation, USA.
14.ISO 105-EO4-1994, Colour Fastness to perspiration.
15.Zhang, Q., Minami, H., Inoue, S., Atsuya, I. (2001), Preconcentration by coprecipitation of arsenic and tin in natural water with a Ni-pyrrolidyne dithiocarbamate complex and their direct determination by solid sampling atomic absorption spectrometry, Fresenius J. Anal. Chem, 370, 860-864.
16.Anthemidis, A.N., Zachariadis, G.A., Kougoulis, J.S., Stratis, J.A. (2002), On-line preconcentration and determination of copper, lead and chromium(VI) using anloaded polyurethane foam packed column by flame atomic absorption spectrometry in natural waters and biological samples, Talanta, 58, 831-840.
17.Dong,X., Nakaguchi, Y., Hiraki, K. (1998), Determination of chromium, iron, manganese and lead in human hair by graphite furnace atomic absorption spectrometry, Analytical Science, 14, 785-789.
18.Hiraide, M., Hori, J. (1999), Enrichment of metal-APDC complexes on admicelle-coated alumina for water analysis, Analytical Science, 15, 1055-1058.
19.Krishna, P.G., Gladis, J.M., Rambabu, U., Rao, T.P., Naidu, G.R.K. (2004), Talanta, 63, 541-546.
20.Soylak, M., Erdo, N.D., Elci, L. (2004), Membrane filtration of iron(III), copper(II) and lead(II) ions as 1-(2-pyridilazo) 2-naphtol (PAN) for their preconcentration and atomic absorption determination, J. Chinese Chemical Society, 51, 703-706.
Lampiran A.
Data hasil percobaan pengaruh pH larutan terhadap pembentukan kompleks Cr-PDC Absorban.detik
No. pH Larutan Cr(VI)
1 2 Rata-rata 1 1,02 0,016 0,024 0,020 2 2,03 0,173 0,161 0,167 3 3,07 0,325 0,331 0,328 4 3,99 0,440 0,451 0,446 5 5,17 0,354 0,373 0,363 6 6,20 0,184 0,184 0,185 7 6,95 0,042 0,037 0,040 8 8,17 0,028 0,030 0,029
Lampiran B
Data hasil percobaan pengaruh jumlah larutan APDC yang ditambahkan Absorban.detik
No. Jumlah larutan APDC (3 g/L)
( mL ) 1 2 Rata-rata 1 2 0,206 - 0,206 2 3 0,331 0,352 0,342 3 4 0,431 0.431 0,431 4 5 0,426 0,432 0,429 5 6 0,433 0,423 0,428
Lampiran C
Data pembuatan kurva kalibrasi Cr(VI) No. Konsentrasi standar Cr(VI)
(ppb) Absorban.detik Keterangan 1 10 0,196 2 20 0,236 3 30 0,392 4 40 0,483 Y=0,0127X r = 0,9626
Data hasil percobaan retensi kompleks Cr-PDC terhadap filter selulosa asetat Cr ditemukan Konsentrasi Cr awal ( µg/L) Absorban.detik Konsentrasi ( µg/L) Perolehan kembali ( % ) 50 0,494 38,90 78 50 0,491 38,66 77 50 0,506 39,92 80 50 0,507 39,84 80 Rata-rata 79 SD 2 Perhitungan :
- % Perolehan kembali = ( Kons. Cr ditemukan ÷ Kons. Cr awal ) x 100 % = ( 38,90 ppb ÷ 50 ppb ) x 100 %
= 78 %
- Standar deviasi (SD) = √∑ (Xi – Xrata-rata )2/( n-1)
= √{(78-79)2 + (77-79)2 + (80-79)2 + (80-79)2}/ 3 = 2 (pembulatan)
Lampiran D
Data hasil percobaan pengaruh jumlah larutan Ni yang ditambahkan kedalam 100 mL larutan Cr(VI) 50 µg/L
No. Penambahan larutan Ni (II) 1 g/L ( mL ) Absorban.detik 1 0 0,494 2 0,1 0,609 3 0,2 0,694 4 0,3 0,705 5 0,6 0,677
Lampiran E
Data kurva kalibrasi larutan standar Cr(VI) No. Konsentrasi standar Cr(VI)
(ppb) Absorban.detik Keterangan 1 5 0,139 2 10 0,301 3 15 0,470 4 20 0,591 Y=0,03012X r = 0,9974
Data hasil percobaan pengaruh konsentrasi larutan Cr(VI) Cr ditemukan No. Konsentrasi larutan Cr(VI) ( µg/L) Absorban.detik Konsentrasi ( µg/L) Perolehan kembali ( % ) 1 5 0,139 4,61 92 2 10 0,279 9,26 93 3 15 0,484 16,07 107 4 20 0,359 11,91 60 5 30 0,555 18,34 61 6 40 0,510 16,93 42
Lampiran F
Data kurva kalibrasi larutan standar Cr(VI) No. Konsentrasi standar Cr(VI)
(ppb) Absorban.detik Keterangan 1 1 0,001 2 5 0,028 3 10 0,105 4 15 0,142 Y=0,0096X r = 0,9461
Data hasil percobaan pengaruh matriks contoh kain Konsentrasi Cr(VI) (µg/L) Faktor Prakonsentrasi ( P ) Kons. Cr(VI) teoritis (µg/L) Konsentrasi Cr(VI) ditemukan (µg/L) Perolehan kembali ( % ) 5 10 50 47,12 94 5 10 50 48,12 96 5 10 50 47,50 95 Rata-rata 95 SD 1 Perhitungan % KV : % KV = (SD ÷ Hasil rata-rata) x 100 % = ( 1 ÷ 95 ) x 100 % = 1,1 %
Lampiran G
Data penentuan limit deteksi Absorban.detik No. Blanko (AB) Std Cr(VI) 5 µg/L Keterangan 1 0,073 0,109 2 0,068 0,113 3 0,067 0,114 4 0,061 5 0,059 6 0,058 7 0,059 8 0,058 9 0,056 10 0,054 Rata-rata 0,061 0,112 Perhitungan
LD = {[(AB)rata-rata+ 3 SD(AB)]/(AStd)} x [Std]
0,061 + 3(0,0057)
LD = X 5 µg/L = 3,48 µg/L 0,112
Lampiran H
Data pembuatan kurva kalibrasi Cr(VI) Absorban.detik No. Konsentrasi standar Cr(VI)
(ppb) 1 2 Rata-rata Keterangan 1 2 0,124 0,177 0,151 2 4 0,334 0,433 0,383 3 6 0,457 0,420 0,438 4 8 0,605 0,617 0,611 5 10 0,803 0,820 0,811 Y= 0,0832X r = 0,9932
Data hasil percobaan prakonsentrasi Cr(VI) dari contoh kain Absorban.detik Contoh kain 1 2 Rata-rata Konsentrasi Cr(VI) (ppb) Kadar Cr(VI) dalam kain (mg/kg kain) Poliester komersial 0,000 0,000 0,000 ttd ttd T/C komersial 0,002 -0,005 -0,002 ttd ttd Kain katun celup/kuning ( pengenceran 10 X ) 0,432 0,458 0,445 5,35 2,65
Kain katun celup/biru ( pengenceran 10 X)
SURAT PELIMPAHAN HAK CIPTA
Yang bertanda tangan di bawah ini : Nama : Tatang Wahyudi
NIM : 20504005
Menyatakan bahwa penulis tesis dengan judul : Prakonsentrasi Krom (VI) dari matriks tekstil dan penentuannya secara spektrometri serapan atom tungku karbon Dibawah bimbingan : Dr. Muhammad Bachri Amran
Adalah benar-benar tesis tersebut hasil karya tulis berdasarkan data hasil eksperimen/perhitungan/permodelan penulis selama melakukan penelitian Pasca Sarjana di Program Studi Kimia ITB.
Dengan ini penulis menyerahkan/melimpahkan Hak Cipta dari karya tulis tesis tersebut kepada Program Studi Kimia ITB.
Bandung, September 2007
Tatang Wahyudi NIM. 20504005