PERBANDINGAN AKTIVITAS ANTIBAKTERI EKSTRAK
ETANOL BIJI DENGAN BATANG PEPAYA (Carica
papaya L.) TERHADAP Staphylococcus
epidermidis DAN Shigella sonnei
NASKAH PUBLIKASI
Oleh:
DESTY RIRIN ROMAWATI
K100110031
FAKULTAS FARMASI
UNIVERSITAS MUHAMMADIYAH SURAKARTA
SURAKARTA
PERBANDINGAN AKTIVITAS ANTIBAKTERI EKSTRAK ETANOL BIJI DENGAN BATANG PEPAYA (Carica papaya L.) TERHADAP
Staphylococcus epidermidis DAN Shigella sonnei
COMPARISON OF ANTIBACTERIAL ACTIVITY OF ETHANOLIC EXTRACT OF Papaya (Carica papaya L.) SEEDS WITH STEM
AGAINST Staphylococcus epidermidis AND Shigella sonnei Desty Ririn Romawati* dan Ratna Yuliani
Fakultas Farmasi, Universitas Muhammadiyah Surakarta, Jl A Yani Tromol Pos I, Pabelan Kartasura Surakarta 57102
*E-mail: destyririn_r@yahoo.co.id ABSTRAK
Pepaya (Carica papaya L.) adalah tanaman yang mempunyai berbagai khasiat, misalnya sebagai antibakteri. Tujuan penelitian ini untuk membandingkan aktivitas antibakteri ekstrak etanol biji dan batang pepaya terhadap Staphylococcuss epidermidis dan Shigella sonnei dan mengetahui golongan senyawa yang mempunyai aktivitas antibakteri. Biji dan batang pepaya diekstraksi dengan cara maserasi menggunakan etanol 70%. Metode uji antibakteri yang digunakan adalah difusi disk Kirby Bauer. Hasil aktivitas antibakteri diamati dengan mengukur diameter zona hambat. Diameter zona hambat dianalisis menggunakan analisis statistik Independent-Sample T Test. Analisis kandungan senyawa menggunakan Kromatografi Lapis Tipis (KLT). Bioautografi dilakukan untuk mengetahui golongan senyawa yang mempunyai aktivitas antibakteri. Hasil penelitian menunjukkan tidak adanya perbedaan yang signifikan antara aktivitas antibakteri ekstrak etanol biji dengan batang pepaya dalam menghambat Shigella sonnei dan Staphylococcus epidermidis. Ekstrak etanol biji dan batang pepaya dengan konsentrasi 1.250-10.000 µg menghasilkan diameter zona hambat 6,00-8,33 mm dan 6,33-7,17 mm terhadap Shigella sonnei dan 6,33-7,55 mm dan 6,00-7,33 mm terhadap Staphylococcus epidermidis. Hasil KLT menunjukkan bahwa ekstrak etanol biji pepaya mengandung steroid, alkaloid, dan tanin, sedangkan ekstrak etanol batang pepaya mengandung triterpen dan tanin. Hasil bioautografi tidak dapat diidentifikasi adanya senyawa yang bertanggungjawab sebagai antibakteri terhadap Staphylococcus epidermidis dan Shigella sonnei.
Kata kunci: Carica papaya L., antibakteri, Staphylococcuss epidermidis, Shigella sonnei.
ABSTRACT
Papaya (Carica papaya L.) is a fruit plants that have benefits. According to previous research seeds and stems of papaya has antibacterial activity against Gram negative and Gram positive bacteria. The purpose of this study were to compare the antibacterial activity of ethanolic extract of papaya seeds and stems against Staphylococcuss epidermidis and Shigella sonnei and determine classes of compounds that have antibacterial activity. Papaya seeds and stems were extracted by maceration using 70% ethanol. Antibacterial test method used was Kirby Bauer disk diffusion. The results of antibacterial activity was observed by measuring diameter of inhibition zone. The diameter of inhibition zone were analyzed using statistical analysis of the Independent-Sample T Test. Analysis of compounds was conducted using Thin Layer Chromatography (TLC). Bioautography was done to determine the class of compounds that have antibacterial activity. The results showed no significant difference between antibacterial activity of ethanolic extract of papaya seeds with stems in inhibiting Shigella sonnei and Staphylococcus
epidermidis. Ethanolic extract of papaya seeds and stems with concentration 1.250-10.000 µg result
diameter of inhibition zone 6,00-8,33 mm and 6,33-7,17 mm against Shigella sonnei and 6,33-7,55 mm dan 6,00-7,33 mm against Staphylococcus epidermidis. TLC results showed that ethanolic extract of papaya seeds contain steroids, alkaloids, and tannins, while the ethanolic extract of papaya stems contain triterpenes and tannins. Bioautography results could not determine compounds that has antibacterial activity against Staphylococcus epidermidis and Shigella sonnei.
PENDAHULUAN
Infeksi adalah masuk dan berkembang biaknya suatu mikroorganisme di dalam jaringan tubuh (Hartati, 2012). Infeksi merupakan penyakit yang dapat ditularkan dari satu orang ke orang atau dari hewan ke manusia. Infeksi disebabkan oleh berbagai mikroorganisme yaitu bakteri, virus, riketsia, jamur dan protozoa. Contoh bakteri yang dapat menyebabkan penyakit infeksi adalah Staphylococcus epidermidis dan Shigella sonnei (Jawetz et al., 2001).
Staphylococcus epidermidis dapat menyebabkan infeksi kulit ringan yang disertai pembentukan abses (Syahrurahman et al., 1994), penyakit jerawat dan puru (Volk dan Wheeler, 1984). Shigella sonnei adalah bakteri patogen usus yang menyebabkan disentri (Syahrurahman et al., 1994).
Menurut Orhue dan Momoh (2013) infeksi yang disebabkan oleh mikroorganisme patogen menjadi penyebab kematian terutama di negara-negara berkembang. Hal ini menjadi alasan untuk mencari sumber baru antibakteri yang lebih efektif, terjangkau, dan mudah didapat (Adekunle dan Adekunle, 2009). Antimikroba yang berasal dari tumbuhan berpotensi memiliki efek terapeutik dan efektif untuk pengobatan penyakit menular (Joshi dan Edington, 1990 dalam Joshi et al., 2009). Salah satu tanaman yang berkhasiat sebagai antibakteri adalah pepaya (Sukadana et al., 2008). Pepaya (Carica papaya L.) dapat digunakan untuk pengobatan berbagai macam penyakit, misalnya konstipasi, antivirus, antijamur, dan antibakteri (Aravin et al., 2013). Hasil dari beberapa penelitian menunjukkan bahwa tanaman pepaya dapat digunakan sebagai bahan alternatif untuk terapi antibakteri (Adriana et al., 2007 dalam Orhue dan Momoh, 2013).
Biji pepaya mengandung senyawa triterpenoid (Sukadana et al., 2008), alkaloid, flavonoid, saponin, dan tanin yang berkhasiat sebagai antibakteri (Okoye, 2011). Menurut penelitian yang telah dilakukan Orhue dan Momoh (2013) ekstrak etanol biji pepaya dengan konsentrasi hambat minimum (KHM) sebesar 28,0 mg/mL memiliki aktivitas antibakteri terhadap Staphylococcus aureus, Escherichia coli, dan Pseudomonas aeruginosa. Ekstrak metanol biji pepaya mempunyai aktivitas antibakteri terhadap Shigella flexneri, Staphylococcus aureus, dan Escherichia coli dengan diameter zona hambat masing-masing sebesar 10,67 mm, 12,67 mm, dan 12,67 mm dan dengan konsentrasi 8 µg/mL (Ocloo, 2012).
Hasil penelitian yang telah dilakukan oleh Rahman et al. (2011) menyatakan bahwa ekstrak etanol batang pepaya dengan konsentrasi 10 mg/mL memiliki aktivitas
antibakteri terhadap Salmonella typhi dengan diameter zona hambat sebesar 14,00 mm. Ekstrak etanol biji pepaya dengan konsentrasi 10 mg/mL memiliki kemampuan menghambat Streptococcus pyogenes (bakteri Gram positif) dan Escherichia coli (bakteri Gram negatif) dengan diameter zona hambat berturut-turut sebesar 9 mm dan 8,5 mm (Martiasih et al., tanpa tahun). Berdasarkan kedua hasil penelitian tersebut dapat disimpulkan bahwa dengan konsentrasi yang sama ekstrak etanol batang pepaya memiliki aktivitas antibakteri yang lebih baik dibandingkan dengan ekstrak etanol biji pepaya.
METODE PENELITIAN Alat
Alat yang digunakan dalam penelitian yaitu oven (Memmert), autoklaf (My Life), seperangkat alat maserasi, rotary evaporator (Heidolph), waterbath (Memmert), alat gelas, cawan petri, ose steril, bunsen, mikropipet, blue tips, yellow tips, pipet ukur, alat timbang (Precisa dan Ohaus), LAF (Astari Niagara International), mikroskop (Olympus), inkubator (Memmert), shaker inkubator (New Brunswick Scientific), vorteks (Thermolyne), bejana elusi, lampu UV 254 nm, dan UV 366 nm.
Bahan
Bahan yang digunakan dalam penelitian ini antara lain: biji dan batang pepaya yang diperoleh dari perkebunan pepaya dari Dusun Ringinsari, Desa Randusari, Kecamatan Teras, Kabupaten Boyolai, Jawa Tengah, etanol 70%, Staphylococcus epidermidis dan Shigella sonnei dari Balai Laboratorium Kesehatan Yogyakarta, cat Gram A, cat Gram B, cat Gram C dan cat Gram D, akuades, formalin 1%, etanol, akuades, media Mueller Hinton (MH), media Brain Heart Infusion, media Kligler Iron Agar (KIA), media Lysine Iron Agar (LIA), media Motility Indol Ornithine (MIO), silika gel GF 254, kloroform, metanol, etil asetat, uap amonia, pereaksi semprot Dragendorff, FeCl3,
Liebermann-Burchard (LB), dan KOH etanolik. Jalannya Penelitian
Ekstraksi biji dan batang
Ekstraksi dilakukan dengan cara maserasi. Serbuk biji dan batang pepaya kering masing-masing seberat 312,00 gram dan 455,81 gram direndam dalam etanol 70% masing-masing sebesar 3,2 liter dan 2,8 liter. Masing-masing bahan dimasukkan dalam wadah yang berbeda, dibasahi etanol 70% sedikit demi sedikit kemudian direndam dalam etanol 70%, didiamkan selama 3-5 hari dan dilakukan pengadukan beberapa kali
sehari. Setelah itu dilakukan penyaringan. Maserat dikumpulkan dan dievaporasi dengan rotary evaporator hingga didapatkan ekstrak etanol biji dan batang pepaya cair. Ekstrak yang diperoleh diuapkan di atas waterbath untuk mendapatkan ekstrak yang kental.
Identifikasi Bakteri a. Pewarnaan bakteri
Pewarnaan bakteri menggunakan pengecatan Gram. b. Uji Biokimia Staphylococcus epidermidis
Bakteri yang diambil dari biakan ditusukkan pada agar garam manitol (Manitol Salt Agar = MSA), kemudian diinkubasi pada suhu 37ºC selama 24 jam. c. Uji Biokimia Shigella sonnei
Bakteri diambil dari biakan kemudian ditusukkan pada media KIA, LIA, dan MIO secara tegak lurus mengenai bidang miring maupun bidang tegak, kemudian diinkubasi pada suhu 37ºC selama 24 jam.
d. Uji aktivitas antibakteri
Uji aktivitas antibakteri dilakukan dengan metode disk. Media MH diinokulasi bakteri Staphylococcus epidermidis dan Shigella sonnei dengan konsentrasi 1,5x108 CFU/mL sebanyak 300 µL. Masing-masing disk diisi kontrol negatif dan 4 seri konsentrasi ekstrak biji dan batang yaitu 50%, 25%, 12,5%, dan 6,25% dengan volume masing-masing 20 µL sehingga masing-masing disk berturut-turut mengandung 10.000 µg, 5.000 µg, 2.500 µg,dan 1.250 µg ekstrak. Kemudian disk diletakkan pada media MH yang sudah diinokulasi bakteri. Inkubasi dilakukan pada 37o C selama 24 jam. Diameter zona hambat yang terjadi diamati. Kontrol positif yang digunakan untuk Staphylococcus epidermidis adalah sefalotin 30 µg, sedangkan Shigella sonnei streptomisin 10 µg. Kontrol negatif yang digunakan adalah etanol 70%.
e. Uji kromatografi lapis tipis
Identifikasi senyawa dalam ekstrak etanol biji dan batang pepaya dilakukan dengan metode KLT. Fase diam yang digunakan silika gel GF254, dan fase gerak
yang digunakan untuk batang adalah metanol:kloroform (7:3), sedangkan untuk biji setelah dilakukan optimasi didapatkan hasil yang paling baik menggunakan etil asetat: metanol: air (100:12:18).
Ekstrak etanol biji dan batang pepaya sebanyak 750 mg dilarutkan dalam etanol 1,5 mL, kemudian ditotolkan 10 µL ekstrak pada lempeng silika gel dan
dielusi. Hasil elusi dilihat di bawah sinar tampak, UV dengan panjang gelombang 254 nm dan 366 nm.
f. Bioautografi
Analisis bioautografi dilakukan untuk mendeteksi bercak yang menunjukkan adanya senyawa aktif yang memiliki aktivitas antibakteri. Lempeng yang telah ditotoli ekstrak dan dielusi dengan fase gerak diletakkan pada permukaan media MH yang telah diinokulasi dengan bakteri dalam cawan petri. Setelah 20 menit, lempeng KLT diambil kemudian cawan petri diinkubasi pada suhu 37°C selama 24 jam. Letak senyawa aktif yang memiliki aktivitas antibakteri akan tampak sebagai zona atau area jernih dengan latar belakang keruh.
HASIL DAN PEMBAHASAN Ekstraksi
Ekstraksi biji dan batang pepaya dilakukan dengan cara maserasi menggunakan pelarut etanol 70%. Ekstrak yang digunakan untuk uji aktivitas antibakteri adalah ekstrak kental. Setelah dilakukan remaserasi 3x dari 455,81 gram batang pepaya kering didapatkan ekstrak kental sebesar 105,40 gram, sedangkan dari 312,00 gram kering biji pepaya didapatkan ekstrak kental sebesar 91,80 gram. Rendemen yang diperoleh sebesar 23,12 % untuk ekstrak etanol batang pepaya dan 29,42 % untuk ekstrak etanol biji pepaya.
Identifikasi Bakteri a. Pewarnaan Bakteri
Staphylococcus adalah sel berbentuk kluster yang tersusun dalam kelompok yang tidak teratur seperti anggur dan merupakan Gram positif (Jawetz et al., 2001). Gram positif berwarna ungu disebabkan karena bakteri Gram positif mengikat cat Gram A (crystal violet) (Capuccino & Sherman, 2013). Berdasarkan hasil pengecatan Gram Staphylococcus epidermidis termasuk bakteri Gram positif yang berwarna ungu dengan susunan sel bergerombol, bulat dan tidak teratur. Hasil pengecatan Gram pada Staphylococcus epidermidis sesuai dengan teori.
Shigella sonnei merupakan bakteri Gram negatif yang berbentuk batang (Jawetz et al., 2001). Warna merah pada bakteri Gram negatif disebabkan karena bakteri mengikat cat gram D (safranin) (Capuccino & Sherman, 2013). Berdasarkan hasil pengecatan Gram Shigella sonnei berwarna merah dan berbentuk batang
dengan susunan sel bergerombol. Hasil pengecatan Gram pada Shigella sonnei sesuai dengan teori.
Perbedaan warna pada bakteri disebabkan karena perbedaan struktur dinding sel. Dinding sel bakteri Gram positif lebih banyak mengandung peptidoglikon, sedangkan dinding sel bakteri Gram negatif lebih tipis. Kandungan lipid dinding sel bakteri Gram negatif lebih banyak dibandingkan bakteri Gram positif (Syahrurahman et al., 1994). Lipopolisakarida merupakan ciri khas yang dimiliki oleh bakteri Gram negatif (Elliott et al., 2013).
b. Uji Biokimiawi Staphylococcus epidermidis
Identifikasi Staphylococcus epidermidis menggunakan agar garam manitol (Manitol Salt Agar = MSA) untuk mendeteksi kemampuan bakteri dalam memfermentasi manitol. Staphylococcus yang memfermentasi manitol menunjukkan warna kuning disekitar petumbuhannya, dan Staphylococcus yang tidak memfermentasi manitol tidak menunjukkan perubahan warna (Cappuccino dan Sherman, 2013). Staphylococcus epidermidis tidak memfermentasi manitol (Syahrurahman et al., 1994). Hasil menunjukkan tidak terjadi perubahan warna pada media, hal ini menunjukkan bahwa Staphylococcus epidermidis tidak memfermentasi manitol. Hasil uji biokimia Staphylococcus epidermidis menggunakan MSA sesuai dengan teori.
c. Uji Biokimiawi Shigella sonnei
Identifikasi Shigella sonnei menggunakan media KIA, LIA, dan MIO. Media KIA digunakan untuk mengetahui kemampuan bakteri memfermentasi karbohidrat, menghasilkan H2S (Mikoleit, 2010), dan menghasilkan gas (WHO,
2003). Shigella sonnei memfermentasi laktosa (Radji, 2011), tidak menghasilkan H2S dan sedikit atau tidak menghasilkan gas (WHO, 2003). Hasil identifikasi
menggunakan media KIA menunjukkan Shigella sonnei memfermentasi glukosa ditandai dengan warna merah (basa) pada bagian miring dan warna kuning (asam) pada bagian tegak. Shigella sonnei tidak menghasilkan warna hitam dan menghasilkan gelembung. Hal ini menunjukkan bahwa Shigella sonnei tidak menghasilkan H2S dan memproduksi gas. Hasil uji biokimia Shigella sonnei
menggunakan KIA sesuai dengan teori.
Uji biokimia menggunakan media LIA untuk mengetahui kemampuan bakteri mendekarboksilasi lisin, mendeaminasi lisin dan membentuk H2S. Shigella
Hasil uji Shigella sonnei pada bagian tegak berwarna kuning menunjukkan Shigella sonnei tidak mendekarboksilasi lisin dan media miring berwarna ungu menunjukkan Shigella sonnei tidak mendeaminasi lisin. Shigella sonnei tidak menghasilkan warna hitam dan gelembung. Hal ini menunjukkan Shigella sonnei tidak menghasilkan H2S
dan gas. Hasil uji biokimia Shigella sonnei menggunakan LIA sesuai dengan teori. Shigella sonnei menunjukkan hasil negatif pada uji motilitas (Syahrurahman et al., 1994). Shigella sonnei positif mendekarboksilasi ornitin yang ditandai warna ungu pada media MIO bagian atas dan tidak produksi indol yang ditandai dengan tidak adanya cincin merah (Mikoleit, 2010). Hasil uji menggunakan media MIO menunjukkan media berwarna ungu pada bagian atas. Hal ini menunjukkan bahwa Shigella sonnei positif mendekarboksilasi ornitin. Shigella sonnei tidak ada pergerakan (nonmotil) yang ditandai dengan hanya keruh pada sekitar tusukan, tidak pada seluruh media. Setelah ditambahkan pereaksi Kovac’s tidak terbentuk cincin berwarna merah. Hal ini menunjukkan bahwa Shigella sonnei tidak produksi indol. Hasil uji biokimia Shigella sonnei menggunakan MIO sesuai dengan teori.
Uji Aktivitas Antibakteri
Uji ini bertujuan untuk membandingkan aktivitas antibakteri ekstrak etanol biji dengan batang pepaya terhadap Staphylococcus epidermidis dan Shigella sonnei. Uji ini dilakukan dengan menggunakan metode diffusion disc Kirby Bauer menggunakan paper disc. Parameter yang digunakan dalam penelitian ini adalah dengan mengukur zona hambat yang terbentuk disekitar disk yang berisi ekstrak etanol biji dan batang pepaya.
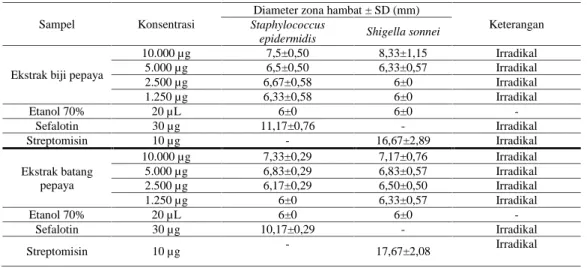
Media yang digunakan untuk uji ini adalah media MH dalam petri. Seri konsentrasi yang digunakan yaitu 10.000 µg, 5.000 µg, 2.500 µg, dan 1.250 µg. Kontrol negatif yang digunakan pada uji ini adalah disk kosong yang diberi etanol 70% dan kontrol positifnya disk antibiotik. Staphylococcus epidermidis menggunakan antibiotik sepalotin 30 µg sedangkan untuk Shigella sonnei menggunakan antibiotik streptomisin 10 µg. Hasil uji aktivitas antibakteri ekstrak etanol batang dan biji pepaya terhadap Staphylococcus epidermidis dan Shigella sonnei dapat dilihat pada Tabel 1.
Zona hambat yang terbentuk adalah irradikal karena masih ditemukannya pertumbuhan bakteri disekitar disk. Biasanya semakin besar konsentrasi ekstrak semakin besar zona hambat yang terbentuk. Pada Staphylococcus epidermidis dan Shigella sonnei, ekstrak batang pepaya menunjukkan hasil semakin besar konsentrasi ekstrak semakin besar zona hambat yang terbentuk. Hal ini kemungkinan karena kandungan senyawa terakumulasi lebih banyak di konsentrasi yang lebih besar.
Menurut Martiasih et al. (tanpa tahun) cit Lorian (1980) konsentrasi mempengaruhi kecepatan difusi zat berkhasiat, makin besar konsentrasi ekstrak maka makin cepat difusi, akibatnya makin besar daya antibakteri dan makin luas diameter zona hambat yang terbentuk.
Tabel 1. Hasil uji aktivitas antibakteri ekstrak etanol batang dan biji pepaya terhadap Staphylococcus epidermidis dan
Shigella sonnei
Sampel Konsentrasi
Diameter zona hambat ± SD (mm)
Keterangan
Staphylococcus
epidermidis Shigella sonnei
Ekstrak biji pepaya
10.000 µg 7,5±0,50 8,33±1,15 Irradikal 5.000 µg 6,5±0,50 6,33±0,57 Irradikal 2.500 µg 6,67±0,58 6±0 Irradikal 1.250 µg 6,33±0,58 6±0 Irradikal Etanol 70% 20 µL 6±0 6±0 -Sefalotin 30 µg 11,17±0,76 - Irradikal Streptomisin 10 µg - 16,67±2,89 Irradikal Ekstrak batang pepaya 10.000 µg 7,33±0,29 7,17±0,76 Irradikal 5.000 µg 6,83±0,29 6,83±0,57 Irradikal 2.500 µg 6,17±0,29 6,50±0,50 Irradikal 1.250 µg 6±0 6,33±0,57 Irradikal Etanol 70% 20 µL 6±0 6±0 -Sefalotin 30 µg 10,17±0,29 - Irradikal Streptomisin 10 µg - 17,67±2,08 Irradikal
Berdasarkan Tabel 1, konsentrasi 10.000 µg ekstrak etanol biji pepaya dengan ekstrak etanol batang pepaya memiliki perbedaan yang tidak signifikan dalam menghambat Staphylococcus epidermidis. Hal ini ditunjukkan oleh hasil uji T sebesar 0,643 sehingga dinyatakan memiliki perbedaan yang tidak signifikan karena lebih besar dari 0,05. Pada konsentrasi 5.000 µg ekstrak etanol biji pepaya dengan ekstrak etanol batang memiliki perbedaan yang tidak signifikan dalam menghambat Staphylococcus epidermidis. Hal ini ditunjukkan oleh hasil uji T lebih besar dari 0,05, yaitu 0,374. Pada konsentrasi 2.500 µg ekstrak etanol biji pepaya dengan ekstrak etanol batang pepaya memiliki perbedaan yang tidak signifikan dalam menghambat Staphylococcus epidermidis. Hal ini ditunjukkan oleh hasil uji T lebih besar dari 0,05, yaitu 0,251. Pada konsentrasi 1.250 µg ekstrak etanol biji pepaya dan ekstrak etanol batang pepaya memiliki aktivitas yang sama dalam menghambat Staphylococcus epidermidis. Hal ini ditunjukkan oleh hasil uji T lebih besar dari 0,05, yaitu 0,374. Dari hasil penelitian ekstrak etanol biji pepaya dengan ekstrak etanol batang pepaya memiliki perbedaan yang tidak signifikan dalam menghambat Staphylococcus epidermidis.
Hasil uji pada konsentrasi 10.000 µg ekstrak etanol biji pepaya dengan batang pepaya memiliki perbedaan yang tidak signifikan dalam menghambat Shigella sonnei. Hal ini ditunjukkan oleh hasil uji T lebih besar dari 0,05, yaitu 0,218. Pada konsentrasi 5.000 µg ekstrak etanol biji pepaya dengan batang pepaya memiliki perbedaan yang
tidak signifikan dalam menghambat Shigella sonnei. Hal ini ditunjukkan oleh hasil uji T lebih besar dari 0,05, yaitu 0,349. Pada konsentrasi 2.500 µg ekstrak etanol biji pepaya dengan batang pepaya memiliki perbedaan yang tidak signifikan dalam menghambat Shigella sonnei. Hal ini ditunjukkan oleh hasil uji T lebih besar dari 0,05, yaitu 0,158. Pada konsentrasi 1.250 µg ekstrak etanol biji pepaya dan ekstrak etanol batang pepaya tidak memiliki perbedaan yang signifikan dalam menghambat Shigella sonnei. Hal ini ditunjukkan oleh hasil uji T lebih besar dari 0,05, yaitu 0,374. Dari hasil penelitian ekstrak etanol biji pepaya dengan ekstrak etanol batang pepaya memiliki perbedaan yang tidak signifikan dalam menghambat Shigella sonnei.
Hasil penelitian Oladimeji et al. (2007) menunjukkan bahwa ekstrak metanol batang pepaya dengan konsentrasi 15 mg/mL memiliki aktivitas antibakteri terhadap Escherichia coli dengan diameter zona hambat sebesar 11,50 mm. Hasil penelitian Okoye (2011) menunjukkan bahwa ekstrak metanol biji pepaya dengan konsentrasi 8x10-3mg/mL memiliki aktivitas antibakteri terhadap Escherichia coli dengan diameter zona hambat sebesar 12,67 mm. Dari hasil kedua penelitian tersebut menunjukkan bahwa ekstrak metanol biji pepaya dengan konsentrasi 8x10-3 mg/mL dapat menghasilkan zona hambat yang lebih besar dibandingkan dengan ekstrak metanol batang pepaya dengan konsentrasi 15 mg/mL dalam menghambat Escherichia coli. Berdasarkan hasil uji T dan perhitungan SD hasil penelitian tidak sesuai dengan penelitian sebelumnya, yaitu ekstrak etanol batang pepaya dengan ekstrak etanol biji pepaya tidak menunjukkan hasil berbeda signifikan dalam menghambat Shigella sonnei (Gram negatif) dan Staphylococcus epidermidis (Gram positif). Perbedaan hasil penelitian dengan hasil penelitian sebelumnya kemungkinan karena perbedaan variasi umur biji dan batang pepaya yang digunakan. Menurut Martiasih et al. (tanpa tahun) tiap umur biji pepaya memiliki kemampuan yang berbeda dalam menghambat pertumbuhan bakteri.
Hasil penelitian menunjukkan bahwa ekstrak etanol biji pepaya lebih cenderung memiliki aktivitas antibakteri dalam menghambat Staphylococcus epidermidis dibandingkan Shigella sonnei. Hasil penelitian ini tidak sama dengan penelitian Sukadana et al. (2008) yaitu ekstrak biji pepaya memiliki kemampuan menghambat Escherichia coli lebih besar dibandingkan Staphylococcus aureus dan Martiasih (2014) menunjukkan bahwa ekstrak biji pepaya lebih efektif menghambat Escherichia coli dibandingkan Streptococcus pyogenes. Ekstrak etanol batang pepaya pepaya lebih cenderung memiliki aktivitas antibakteri dalam menghambat Shigella
sonnei dibandingkan Staphylococcus epidermidis. Hasil penelitian ini tidak sama dengan penelitian Rahman et al. (2011), yaitu ekstrak etanol batang pepaya lebih efektif terhadap Staphylococcus aureus dibandingkan Escherichia coli.
Perbedaan tersebut disebabkan oleh beberapa faktor, yaitu karena resistensi bakteri terhadap substansi bioaktif, perbedaan bakteri yang digunakan menyebabkan perbedaan sensitivitas bakteri terhadap substansi bioaktif. Perbedaan tempat tumbuh tanaman, tanaman yang digunakan dalam penelitian ini berasal dari Boyolali, Jawa Tengah sedangkan penelitian Sukadana et al. (2008) berasal dari NTT, Martiasih et al. (2014) dari Bantul dan Rahman et al. (2011) dari Pakistan. Difusi zat aktif pada medium yang berlangsung lambat, pada penelitian ini menggunakan metode difusi disk, sedangkan penelitian Martiasih et al. (2014) dan Rahman et al. (2011) menggunakan metode difusi sumuran sehingga difusi zat aktif lebih cepat.
Analisis Kromatografi Lapis Tipis
Analisis kromatografi lapis tipis digunakan untuk mengetahui kandungan senyawa yang terdapat dalam ekstrak etanol batang dan biji pepaya. Konsentrasi yang digunakan untuk uji KLT sebesar 50%. Fase diam yang digunakan silika Gel GF254.
Berdasarkan hasil optimasi fase gerak didapatkan hasil bahwa fase gerak etil asetat: metanol: air (100:12:18) merupakan fase gerak terbaik untuk ekstrak etanol biji pepaya, sedangkan ekstrak etanol batang pepaya menggunakan fase gerak metanol:kloroform (7:3).
Berdasarkan Wagner dan Bladt (1996) hasil KLT dinyatakan mengandung antrakinon jika dengan menggunakan pereaksi semprot KOH etanolik kemudian diamati di sinar tampak menunjukkan warna merah. Pereaksi LB dapat digunakan untuk mendeteksi steroid menunjukkan warna biru atau hijau (Farnsworth, 1966). Dragendorff untuk mendeteksi adanya alkaloid yang ditandai warna merah jingga latar belakang kuning kelabu, coklat/jingga coklat (Wagner dan Bladt, 1996). Uap ammonia untuk mendeteksi adanya flavonoid yang ditandai dengan warna kuning (Kumalasari & Sulistyani (2011) cit Robinson (1995)). FeCl3 untuk mendeteksi tanin yang ditandai
dengan warna biru, biru hitam, hijau, dan hitam pada sinar tampak (Farnsworth, 1966). Hasil uji ekstrak etanol batang pepaya menggunakan pereaksi KOH etanolik berwarna hijau. Hal ini mengindikasikan bahwa ekstrak etanol batang pepaya tidak mengandung antrakinon karena tidak ditemukan adanya warna merah. Hasil uji ekstrak etanol batang pepaya menggunakan pereaksi LB menunjukkan adanya spot warna merah. Hal ini menunjukan ekstrak etanol batang pepaya mengandung triterpen pada Rf
0,42. Hasil uji ekstrak etanol batang pepaya menggunakan Dragendorff menunjukkan adanya spot warna hijau. Hal ini tidak menunjukkan adanya alkaloid. Hasil uji ekstrak etanol batang pepaya menggunakan uap amonia menunjukkan adanya spot warna hijau bukan warna kuning. Hal ini menunjukkan tidak ada senyawa flavonoid. Hasil uji ekstrak etanol batang pepaya menggunakan FeCl3menunjukkan adanya senyawa tanin
karena adanya spot warna hijau pada Rf 0,5.
Tabel 2. Hasil analisis KLT ekstrak etanol batang pepaya menggunakan fase gerak kloroform:metanol (3:7) dan fase diam silika gel GF254
No Rf
Sebelum disemprot Setelah disemprot
Senyawa Sinar tampak UV 254 nm UV 366 nm KOH etanolik sinar tampak LB UV 366 Nm Dragen-dorff Sinar tampak Uap amonia Sinar tampak FeCl3 Sinar tampak 1. 0,42 H P FH - M - - - Triterpen 2. 0,50 H P FH - - - - H Tanin Keterangan H = Hijau P = Pemadaman FH = Fluoresensi hijau M = Merah
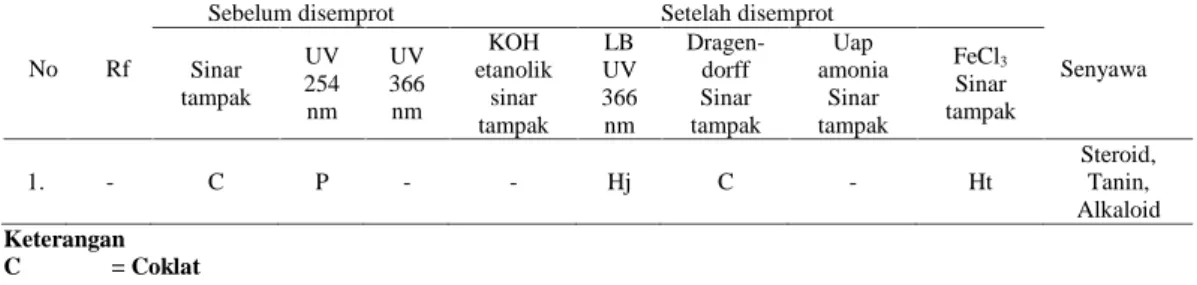
Hasil uji ekstrak etanol biji pepaya menggunakan pereaksi KOH etanolik berwarna coklat. Hal ini mengindikasikan bahwa ekstrak etanol batang pepaya tidak mengandung antrakinon karena tidak ditemukan adanya warna merah. Hasil uji ekstrak etanol biji pepaya menggunakan LB menunjukkan adanya warna hijau pada Rf 0,17. Hal ini menunjukkan ekstrak etanol biji pepaya mengandung steroid. Hasil uji ekstrak etanol biji pepaya menggunakan Dragendorff menunjukkan adanya warna coklat pada Rf 0,25. Hal ini menunjukkan adanya alkaloid. Hasil uji ekstrak etanol biji pepaya menggunakan uap amonia menunjukkan adanya warna coklat, hal ini menunjukkan tidak ada senyawa flavonoid. Hasil uji ekstrak etanol biji pepaya menggunakan FeCl3
menunjukkan adanya senyawa tanin karena adanya warna hitam pada Rf 0,23.
Tabel 3. Hasil analisis KLT ekstrak etanol biji pepaya menggunakan fase gerak etil asetat: metanol: air (100:12:18) dan fase diam silika gel GF254
No Rf
Sebelum disemprot Setelah disemprot
Senyawa Sinar tampak UV 254 nm UV 366 nm KOH etanolik sinar tampak LB UV 366 nm Dragen-dorff Sinar tampak Uap amonia Sinar tampak FeCl3 Sinar tampak 1. - C P - - Hj C - Ht Steroid, Tanin, Alkaloid Keterangan C = Coklat Hj = Hijau Ht = Hitam P = Pemadaman
Ekstrak etanol batang pepaya yang diambil dari daerah Akwa Iborn State mengandung metabolit sekunder alkaloid, saponin, tanin, glikosida jantung, dan flavonoid (Oladimeji et al., 2011). Batang pepaya yang diambil dari daerah Osisioma Ngwa LGA, Abia State mengandung alkaloid, saponin, tanin, dan steroid (Stephen et al., 2013). Hasil penelitian menunjukkan ekstrak etanol batang pepaya mengandung tanin. Hasil penelitian ini tidak sesuai dengan penelitian sebelumnya karena senyawa yang terdapat dalam ekstrak etanol batang pepaya belum memisah secara maksimal dan perbedaan tempat tumbuh pepaya. Hal ini menunjukkan bahwa faktor-faktor lingkungan seperti iklim, cahaya matahari, suhu udara, lingkungan atmosfer (CO2, O2 dan
kelembaban), lingkungan perakaran (sifat kimia dan fisika tanah), dan ketersediaan air di dalam tanah memiliki pengaruh terhadap hasil metabolisme sekunder tanaman (Mahatriny et al. (tanpa tahun) cit Nitisapto dan Siradz (2005)).
Biji pepaya yang berasal dari Anambra, Nigeria mengandung flavonoid, tanin, saponin, fenol, dan steroid (Okoye, 2011). Biji pepaya yang berasal dari Kupang, Nusa Tenggara Tengah mengandung triterpeneoid (Sukadana et al., 2008). Hasil penelitian menunjukkan ekstrak etanol biji pepaya mengandung steroid, alkaloid, dan tanin. Hal ini tidak sesuai dengan penelitian sebelumnya karena senyawa yang terdapat dalam ekstrak etanol biji pepaya belum memisah secara maksimal, dan perbedaan tempat tumbuh pepaya mempengaruhi hasil metabolisme sekunder tanaman (Mahatriny et al. (tanpa tahun) cit Nitisapto dan Siradz (2005)).
Uji Bioautografi
Bioautografi adalah metode spesifik untuk mendeteksi bercak yang berada pada lempeng hasil KLT yang mempunyai aktivitas sebagai antibakteri (Dwidjoseputro, 1989). Bioautografi yang dilakukan pada uji ini menggunakan metode bioautografi kontak.
Hasil bioautografi dinyatakan mempunyai aktivitas antibakteri jika terdapat zona jernih. Hasil penelitian Setiawan (2009) menunjukkan bahwa senyawa yang mempunyai aktivitas sebagai antibakteri dalam ekstrak etanol batang pepaya adalah saponin. Uji menggunakan ekstrak etanol batang dan biji pepaya terhadap Staphylococcus epidermidis dan Shigella sonnei tidak menunjukkan adanya zona jernih. Senyawa yang bertanggungjawab sebagai antibakteri terhadap Staphylococcus epidermidis dan Shigella sonnei belum diketahui. Hasil penelitian tidak sesuai dengan penelitian sebelumnya. Hal ini dapat dikarenakan senyawa belum memisah secara
maksimal, lempeng KLT yang tidak menempel secara sempurna dan adanya gelembung udara saat menempelkan lempeng KLT.
KESIMPULAN
1. Aktivitas antibakteri ekstrak etanol biji dengan batang pepaya mempunyai perbedaan yang tidak signifikan terhadap Staphylococcus epidermidis dan Shigella sonnei. Ekstrak etanol biji dan batang pepaya dengan konsentrasi 1.250-10.000 µg menghasilkan diameter zona hambat 6,00-8,33 mm dan 6,33-7,17 mm terhadap Shigella sonnei dan 6,33-7,55 mm dan 6,00-7,33 mm terhadap Staphylococcus epidermidis.
2. Senyawa dalam ekstrak etanol batang dan biji pepaya yang bertanggungjawab sebagai antibakteri terhadap Staphylococcus epidermidis dan Shigella sonnei belum diketahui.
SARAN
1. Perlu dilakukan fraksinasi untuk mengetahui kelompok senyawa yang berperan sebagai antibakteri.
2. Perlu dilakukan uji menggunakan spesies bakteri yang berbeda.
DAFTAR PUSTAKA
Adekunle, A. S. & Adekunle, O. C., 2009, Preliminary Assessment of Antimicrobial Properties of Aqueous Extract of Plants Against Infectious Diseases, Biology and Medicine, 1 (3), 20-24
Adriana, B., Almodovar, A. N. M., Pereiral, C. T., & Mariangela, T. A., 2007, Antimicrobial Efficacy of Curcuma Zedoaria Extracts as Assessed by Linear Regression Compared with Commercial Mounthrinses, Brazilian Journal of Microbiology, 38, 440-445
Aravind, G., Bhowmik, D., Duraivel, S., & Harish, G., 2013, Traditional and Medicinal Uses of Carica papaya, Journal of Medicinal Plants Studies, 1 (1), 7-15
Cappuccino, J. G. & Sherman, N., 2013, Manual Laboratorium Mikrobiologi, editor Miftahurrahmah, N., diterjemahkan oleh Manurung, J. & Vidhayanti, H., 74, 104, Jakarta, Penerbit Buku Kedokteran EGC
Dwidjoseputro, 1989, Dasar-dasar Mikrobiologi, cetakan ke-10, 24, Jakarta, Penerbit Djembatan
Elliott, T., Worthington, T., Osman, H., & Gill, M., 2013, Mikrobiologi Kedokteran dan Infeksi, editor Puspadewi, N., Suyono, J., & Djayasaputra, L., diterjemahkan oleh Pendit, B. U., 1, 26-27, Jakarta, Penerbit Buku Kedokteran EGC
Farnsworth, N.R., 1966, Review Article Biological and Phytochemical Screening of Plants, Journal Of Pharmaceutical Sciences, 55(3): 225-268
Hartati, A. S., 2012, Dasar-dasar Mikrobiologi Kesehatan, 139, Yogyakarta, Nuha Medika
Jawetz, E., Melnick, J. L., & Adelberg, E. A., 2001, Mikrobiologi Kedokteran, diterjemahkan oleh Mudihardi, E., Kuntaman, W. B. E., Mertaniasih, M. N., Harsono, S., & Alimsardjono, L., Edisi 22, 79, 317-318, 322, 362, Jakarta, Penerbit Salemba Medika
Joshi, B., Lekhak, S., & Sharma, A., 2009, Antibacterial Property of Different Medicinal Plants: Ocimum sanctum, Cinnamomum zeylanicum, Xanthoxylum armatum and Origanum majorana, Kathmandu University Journal of Science, 5 (1), 143-150
Kumalasari, E., & Sulistyani, N., 2011, cit Robinson, 1995, Aktivitas Antifungi Ekstrak Etanol Batang Binahong (Anredera cordifolia (Tenore) Steen.) terhadap Candida albicans serta Skrining Fitokimia, Jurnal Ilmiah Kefarmasian, 1 (2), 51-62
Mahatriny, N. N., Payani, N. P. S., Oka, I. B. M., & Astuti, K. W., tanpa tahun, Skrining Fitokimia Ekstrak Etanol Daun Pepaya (Carica papaya L.) yang Diperoleh dari Daerah Ubud, Kabupaten Gianyar, Bali, Jurnal Penelitian, 8-13
Martiasih, M., Sidharta, B. R., & Atmodjo, P. K., tanpa tahun, Aktivitas Antibakteri Ekstrak Biji Pepaya (Carica papaya L.) terhadap Escherichia coli dan Streptococcus pyogenes, Jurnal Penelitian, 1-12
Mikoleit, M. L., 2010, Laboratory Protocol: Biochemical Identification of Salmonella and Shigella Using an Abbreviated Panel of Tests, 19-45, USA, World Health Organization
Nirosha, N. & Mangalanayaki, R., 2013, Antibacterial Activity of Leaves and Stem Extract of Carica papaya L., International Journal of Advances in Pharmacy, Biology and Chemistry, 2 (3), 473-476
Ocloo, A., Nwokolo, N. C., & Dayie, N. T. K. D., 2012, Phytochemical Characterization and Comparative Efficacies of Crude Extracts of Carica Papaya, International Journal of Drug Research and Technology, 2 (5), 399-406
Okoye, E. I., 2011, Preliminary Phytochemical Analysis and Antimicrobial Activity of Seeds of Carica Papaya, Journal of Basic Physical Research, 2 (1), 66-69
Oladimeji, O. H., Nia, R., Ndukwe, K., & Attith, E., 2007, In Vitro Biological Activities of Carica Papaya, Research Journal of Medicinal Plant, 1 (3), 92-99
Orhue P. O. & Momoh, 2013, Antibacterial Activity of Different Solvent Extracts of Carica papaya Fruit Parts on Some Gram Positive and Gram Negative Organisms, International Journal of Herbs and Pharmacological Research, 2 (4), 42-47
Radji, M., 2011, Buku Ajar Mikrobiologi Panduan Mahasiswa Farmasi dan Kedokteran, 103, Jakarta, Penerbit Buku Kedokteran EGC
Rahman, S., Imran, M., Muhammad, N., Hassan, N., Chisthi, A. K., Khan, A. F., et al., 2011, Antibacterial Screening of Leaves and Stem of Carica papaya, Journal of Medicinal Plants Research, 5 (20), 5167-5171
Setyawan, W., 2009, Aktivitas Antibakteri Ekstrak Etanol Batang Pepaya (Carica papaya L) terhadap Staphylococcus aureus dan Escherichia coli Multiresisten Antibiotik, Skripsi, Fakultas Farmasi Universitas Muhammadiyah Surakarta Stephen, C., Ukpabi, C., Esihe, T., & Brown, N., 2013, Chemical Composition of
Carica papaya L. Stem, American Open Food Science Journal, 1 (1), 1-5 Sukadana, I. M., Santi, S. R., & Juliarti, J. K., 2007, Aktivitas Antibakteri Senyawa
Golongan Triterpenoiddari Biji Pepaya (Carica papaya L.), Jurnal Kimia, 2 (1), 15-18
Syahrurahman, A., Chatim, A., Sardjito, R., Karuniawati, A., Santoso, A. U. S., Bela, B., et al., 1994, Mikrobiologi Kedokteran, Edisi Revisi, 15, 103, 111, 165-166, Jakarta, Binarupa Aksara
Volk, W. A. & Wheeler, M., 1984, Mikrobiologi Dasar, editor Soenartono Adisoemarto, diterjemahkan oleh Markham, 22, 104, 155., Jakarta, Erlangga Wagner, H. & Bladt, S., 1996, Plant Drug Analysis: A Thin Layer Chromatography
Atlas, Second edition, Germany, Springer
WHO, 2003, Manual for the Laboratory Identification and Antimicrobial Susceptibility Testing of Bacterial Pathogens of Public Health Importance in the Developing Wor, 121-129, USA, World Health Organization