BAB II
TINJAUAN PUSTAKA
2.1Uraian Tumbuhan
Uraian tumbuhan meliputi daerah tumbuh, morfologi tumbuhan, nama
daerah, nama asing, sistematika tumbuhan, kandungan kimia dan kegunaan dari
tumbuhan.
2.1.1Daerah tumbuh
Tanaman padi adalah tumbuhan yang tergolong tanaman air dan dapat
tumbuh di tanah yang terus-menerus digenangi air, baik penggenangan itu terjadi
secara alami seperti tanah rawa-rawa, maupun yang disengaja seperti tanah sawah.
Tanaman ini juga dapat tumbuh di daratan atau tanah kering yang curah hujannya
dapat mencukupi kebutuhan air tanaman. Padi yang tumbuh di tanah yang
digenangi air disebut padi sawah, sedangkan yang tumbuh di tanah darat/kering
disebut padi ladang (Siregar, 1981).
2.1.2Morfologi tumbuhan
Habitus: Semak, semusim, tinggi lebih kurang 1,5 m. Batang: Tegak,
lunak, beruas, berongga, kasar, hijau. Daun: Tunggal, lanset, tersebar, ujung
runcing, tepi rata, berpelepah, panjang lebih kurang 25 cm, lebar 3-5 cm,
pertulangan sejajar, hijau. Bunga: Majemuk, bentuk malai, menggantung, panjang
lebih kurang 20 cm, benang sari enam, tangkai putik dua, kepala putik berbulu,
putih. Buah: Batu, bulat telur, kuning tua. Biji: Keras, bulat telur, merah. Akar:
2.1.3Nama daerah
Sumatera: Pade (Aceh), Page (Batak), Batang padi (Minangkabau), Pari
(Lampung), Banih (Melayu). Jawa: Pare (Sunda), Pari (Jawa), Padi (Madura).
Bali: Padi. Nusa Tenggara: Pare (Sumba), Woya (Flores), Ale (Timor). Sulawesi:
Pale (Gorontalo), Pae (Toraja), Ase (Makasar), Ase (Bugis). Maluku: Alakutu
(Ambon), Pinge (Halmahera) (Hutapea, dkk., 1994).
2.1.4Nama asing
Riz (Perancis), Arroz (Spanyol), Riso (Italia), Reis (Jerman), Rice
(Inggris) (Pillai, 2004).
2.1.5Sistematika tumbuhan
Divisi : Spermatophyta
Sub divisi : Angiospermae
Kelas : Monocotyledoneae
Bangsa : Poales
Suku : Gramineae
Marga : Oryza
Jenis : Oryza sativa L. (Hutapea, dkk., 1994).
Varietas : Oryza sativa L. var Kuku Balam Merah
(Sumber: Balai Pengkajian Teknologi Pertanian Sumatera Utara)
2.1.6Kandungan kimia
Beras merah mengandung makronutrien berupa karbohidrat, protein, dan
lemak. Kadar karbohidrat memiliki komposisi terbesar, protein dan lemak
menempati posisi kedua dan ketiga. Karbohidrat utama dalam beras adalah pati
antara 85-90% dari berat kering beras. Protein beras terdiri dari 5% fraksi
albumin, 10% globulin, 5% prolamin, dan 80% glutein. Kandungan lemak
berkisar antara 0,3-0,6% pada beras kering giling dan 2,4-3,9% pada beras pecah
kulit (Indrasari dan Adnyana, 2007).
Selain itu beras merah mengandung vitamin dan mineral (Barber dan
Barber, 1980), trisin dan betasitosterol (Chung, et al., 2005), asam fenolat dan
quinolin alkaloid (Chung dan Shin, 2007), antosianin, tokoferol dan tokotrienol
(Yawadio, et al., 2007) dan proantosianidin (Oki, et al., 2002).
2.1.7Kegunaan
Beras merah memiliki manfaat potensial dalam kesehatan seperti
mencegah sakit kepala, penyakit jantung, penyakit Alzheimer, menurunkan
tekanan darah (Kayahara, et al., 2000), mencegah diabetes (Yawadio, et al.,
2007), mengurangi stres oksidatif dan mencegah masalah kardiovaskuler (Ling, et
al., 2001) serta mencegah kanker (Hudson, et al., 2000).
2.2Ekstraksi
Ekstraksi adalah suatu proses pemisahan kandungan senyawa kimia dari
jaringan tumbuhan maupun hewan. Sebelum ekstraksi dilakukan biasanya
bahan-bahan dikeringkan terlebih dahulu kemudian dihaluskan pada derajat kehalusan
tertentu (Harborne, 1987).
Menurut Depkes (2000), beberapa metode ekstraksi yang sering digunakan
A. Cara dingin
1. Maserasi
Maserasi adalah proses penyarian simplisia dengan cara perendaman
menggunakan pelarut dengan sesekali pengadukan pada temperatur kamar.
Maserasi yang dilakukan pengadukan secara terus-menerus disebut maserasi
kinetik sedangkan yang dilakukan pengulangan panambahan pelarut setelah
dilakukan penyaringan terhadap maserat pertama dan seterusnya disebut
remaserasi.
2. Perkolasi
Perkolasi adalah proses penyarian simplisia dengan pelarut yang selalu
baru sampai terjadi penyarian sempurna yang umumnya dilakukan pada
temperatur kamar. Proses perkolasi terdiri dari tahap pelembaban bahan, tahap
perendaman antara, tahap perkolasi sebenarnya (penetesan/penampungan ekstrak)
terus - menerus sampai diperoleh perkolat yang jumlahnya 1-5 kali bahan.
B. Cara panas
1. Refluks
Refluks adalah proses penyarian simplisia dengan menggunakan alat pada
temperatur titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang
relatif konstan dengan adanya pendingin balik.
2. Digesti
Digesti adalah proses penyarian dengan pengadukan kontinu pada
temperatur lebih tinggi daripada temperatur ruangan, yaitu secara umum
3. Sokletasi
Sokletasi adalah proses penyarian dengan menggunakan pelarut yang
selalu baru, dilakukan dengan menggunakan alat soklet sehingga menjadi
ekstraksi kontinu dengan pelarut relatif konstan dengan adanya pendingin balik.
4. Infudasi
Infudasi adalah proses penyarian dengan menggunakan pelarut air pada
temperatur 90°C selama 15 menit.
5. Dekoktasi
Dekoktasi adalah proses penyarian dengan menggunakan pelarut air pada
temperatur 90°C selama 30 menit.
2.3 Radikal Bebas
Radikal bebas adalah spesies kimia yang memiliki satu atau lebih elektron
yang tidak berpasangan pada orbital terluarnya, sehingga dapat menyerang
senyawa-senyawa lain seperti DNA, membran lipid, dan protein. Radikal ini akan
merebut elektron dari molekul lain yang ada disekitarnya untuk menstabilkan diri,
sehingga spesies kimia ini sering dihubungkan dengan terjadinya kerusakan sel,
kerusakan jaringan, dan proses penuaan (Halliwell dan Gutteridge, 1999).
Radikal bebas sangat reaktif dan dengan mudah menjurus ke reaksi yang
tidak terkontrol, menghasilkan ikatan silang (cross-link) pada DNA, protein,
lipida, atau kerusakan oksidatif pada gugus fungsional yang penting pada
biomolekul ini. Perubahan ini akan menyebabkan proses penuaan. Radikal bebas
juga terlibat dan berperan dalam patologi dari berbagai penyakit degeneratif,
2.4 Antioksidan
Antioksidan adalah senyawa yang mempunyai struktur molekul yang
dapat memberikan elektronnya kepada molekul radikal bebas dan dapat memutus
reaksi berantai dari radikal bebas (Kumalaningsih, 2006). Antioksidan atau
reduktor berfungsi untuk mencegah terjadinya oksidasi atau menetralkan senyawa
yang telah teroksidasi dengan cara menyumbangkan hidrogen dan atau elektron
(Silalahi, 2006).
Menurut Kumalaningsih (2006), antioksidan dikelompokkan menjadi 3
jenis yakni:
1. Antioksidan primer
Antioksidan primer berfungsi untuk mencegah pembentukan senyawa
radikal baru karena dapat mengubah radikal bebas yang ada menjadi molekul
yang berkurang dampak negatifnya, sebelum radikal bebas ini sempat bereaksi.
Contohnya adalah enzim superoksida dismutase (SOD) yang berfungsi sebagai
pelindung hancurnya sel-sel dalam tubuh karena radikal bebas.
2. Antioksidan sekunder
Antioksidan sekunder merupakan senyawa yang berfungsi menangkal
senyawa radikal bebas serta mencegah terjadinya reaksi berantai. Contohnya
adalah vitamin E, vitamin C dan betakaroten yang dapat diperoleh dari
buah-buahan.
3. Antioksidan tersier
Antioksidan tersier merupakan senyawa yang memperbaiki kerusakan
sel-sel dan jaringan yang disebabkan oleh radikal bebas. Contohnya enzim metionin
Antioksidan digunakan untuk melindungi komponen makanan yang
bersifat tidak jenuh (mempunyai ikatan rangkap), terutama lemak dan minyak.
Mekanisme kerja antioksidan secara umum adalah menghambat oksidasi lemak.
Tahapannya menurut Almatsier (2004) adalah:
I. Inisiasi
RH + initiator → R• + H
II. Propagasi
R• + O2→ ROO•
ROO•+ RH → ROOH + R•
III. Terminasi
R• + R• → RR
ROO• + R• → ROOR
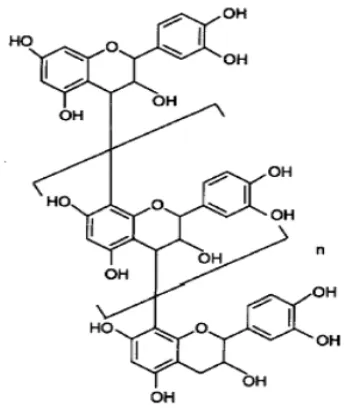
2.4.1 Proantosianidin
Proantosianidin merupakan senyawa golongan tanin terkondensasi,
polimer dari 2 sampai 50 unit flavonoid yang dihubungkan oleh rantai karbon
sehingga tidak mudah terhidrolisis. Tanin jenis ini dapat terhidrolisis membentuk
antosianidin. Tanin terkondensasi ada dua jenis yaitu prosianidin dan
prodelfinidin. Proantosianidin banyak ditemukan dalam bentuk prosianidin.
Prosianidin terdiri dari epikatekin dan katekin sedangkan prodelfinidin terdiri dari
epigalokatekin dan galokatekin. Senyawa-senyawa ini memiliki aktivitas
antioksidan yang tinggi (Handaya, 2008). Rumus bangun proantosianidin dapat
Gambar 2.1 Rumus bangun proantosianidin
2.4.2 Antosianin
Antosianin merupakan pigmen yang tersebar luas pada tanaman,
berbentuk struktur aromatik tunggal (sianidin) dan berfungsi sebagai antioksidan
(Metaliri, 2007). Kemampuan antioksidatif antosianin timbul dari reaktifitasnya
yang tinggi sebagai pendonor hidrogen atau elektron. Antosianin juga memiliki
kemampuan radikal turunan polifenol untuk menstabilkan dan mendelokalisasi
elektron tidak berpasangan serta memiliki kemampuan untuk mengkhelat ion
logam (Ariviani, 2010).
Pigmen antosianin dapat rusak dengan perlakuan panas pada suhu 60OC
selama 30-60 menit dimana proses tersebut mengakibatkan antosianin kehilangan
warna (Isnaini, 2010). Suhu pasteurisasi yang tinggi yaitu 75OC, 85OC, 95OC
selama 12 menit dapat merusak senyawa antosianin dan menurunkan
bioaktivitasnya (Gupita dan Rahayuni, 2012). Rumus bangun antosianin dapat
Gambar 2.2 Rumus bangun antosianin
2.4.3 Vitamin C
Vitamin C atau asam askorbat mempunyai berat molekul 176,13 dengan
rumus bangun C6H8O6 dan titik lebur lebih kurang 190°C. Asam askorbat
mengandung tidak kurang dari 99,0% dan tidak lebih dari 100,5% C6H8O6.
Pemerian: hablur atau serbuk putih atau agak kuning, oleh pengaruh cahaya
lambat laun menjadi gelap, dalam keadaan kering stabil di udara, dalam larutan
cepat teroksidasi. Kelarutan: mudah larut dalam air, agak sukar larut dalam etanol,
tidak larut dalam kloroform, dalam eter dan dalam benzena. Penyimpanan dalam
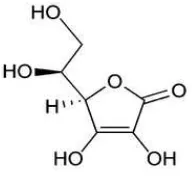
wadah tertutup rapat, tidak tembus cahaya (Depkes1, 1995). Rumus bangun
vitamin C dapat dilihat pada Gambar 2.3 berikut ini.
Gambar 2.3 Rumus bangun vitamin C
Vitamin C berperan dalam pencegahan penyakit jantung koroner dan
mencegah kanker. Vitamin ini juga dapat meningkatkan sistem kekebalan tubuh
terhadap infeksi virus dan bakteri serta berperan dalam regenerasi vitamin E
Pada semua percobaan baik untuk menggunakan standar atau kontrol
positif di samping sampel utama yang sedang dipelajari. Sesuai standar yang
secara luas digunakan adalah asam askorbat (vitamin C) (Molyneux, 2004).
2.5 Spektrofotometri UV-Visibel
Prinsip kerja spektrofotometer UV-Vis adalah dimana sinar/cahaya
dilewatkan melewati sebuah wadah (kuvet) yang berisi larutan, dimana akan
menghasilkan spektrum. Alat ini menggunakan hukum Lambert Beer sebagai
acuan (Ewing, 1975).
Panjang gelombang untuk sinar ultraviolet antara 200-400 nm sedangkan
panjang gelombang untuk sinar tampak/visibel antara 400-750 nm. Sinar
ultraviolet dan sinar tampak memberikan energi yang cukup untuk terjadinya
transisi elektronik. Keadaan energi yang paling rendah disebut dengan keadaan
dasar (ground state). Jika suatu molekul dikenai suatu radiasi elektromagnetik
pada frekuensi yang sesuai, energi molekul tersebut akan ditingkatkan ke level
yang lebih tinggi dan terjadi peristiwa penyerapan (absorbsi) energi oleh molekul.
Transisi-transisi elektronik akan meningkatkan energi molekuler dari keadaan
dasar ke satu atau lebih tingkat energi tereksitasi (Gandjar dan Rohman, 2007).
Spektrofotometri serapan adalah pengukuran serapan radiasi
elektromagnetik yang diserap zat pada panjang gelombang tertentu dan mendekati
monokromatik. Spektrofotometer pada dasarnya terdiri atas sumber sinar
monokromator, tempat sel untuk zat yang diperiksa, detektor, penguat arus dan
alat ukur atau pencatat (Depkes, 1979).
2.6 Metode DPPH (1,1-Diphenyl-2-Picrylhydrazyl)
Pada tahun 1922, ditemukan senyawa berwarna ungu radikal bebas stabil
DPPH yang sekarang digunakan sebagai reagen kolorimetri. DPPH sangat
berguna dalam berbagai penyelidikan seperti inhibisi atau radikal polimerisasi
kimia, penentuan sifat antioksidan amina, fenol atau senyawa alami (vitamin,
ekstrak tumbuh-tumbuhan, obat-obatan). DPPH berwarna sangat ungu seperti
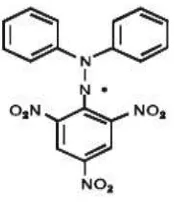
KMnO4 dan bentuk tereduksinya berwarna oranye-kuning (Ionita, 2005). Rumus
bangun DPPH dapat dilihat pada Gambar 2.4 berikut ini.
Gambar 2.4 Rumus bangun DPPH
Metode DPPH adalah sebuah metode yang sederhana yang dapat
digunakan untuk menguji kemampuan antioksidan yang terkandung dalam
makanan. Metode DPPH dapat digunakan untuk sampel dalam bentuk larutan.
Prinsipnya dimana elektron ganjil pada molekul DPPH memberikan serapan
maksimum pada panjang gelombang 516 nm yang berwarna ungu. Warna ini akan
berubah dari ungu menjadi kuning lemah apabila elektron ganjil tersebut
berpasangan dengan atom hidrogen yang disumbangkan senyawa antioksidan.
Perubahan warna ini berdasarkan reaksi kesetimbangan kimia (Prakash, 2001).
Parameter yang dipakai untuk menunjukan aktivitas antioksidan adalah
harga konsentrasi efisien atau efficient concentration (EC50) atan Inhibitory
menyebabkan 50% DPPH kehilangan karakter radikal atau konsentrasi suatu zat
antioksidan yang memberikan persen peredaman sebesar 50%. Zat yang
mempunyai aktivitas antioksidan tinggi, akan mempunyai harga EC50 atau IC50
yang rendah (Molyneux, 2004).
2.6.1 Pelarut
Metode ini dapat bekerja dengan baik dengan metanol atau etanol, karena
tidak ada di antara keduanya yang menganggu reaksi tersebut. Penggunaan pelarut
lain, seperti ekstrak dalam air atau aseton, memberikan hasil yang lebih rendah
(Molyneux, 2004).
2.6.2 Pengukuran absorbansi-panjang gelombang
Panjang gelombang maksimum (λmaks) yang digunakan dalam pengukuran
sampel uji sangat bervariasi. Menurut beberapa literatur panjang gelombang
maksimum untuk DPPH antara lain 515-520 nm. Nilai absorbansi yang mutlak
tidak penting, karena panjang gelombang dapat diatur untuk memberikan
absorbansi maksimum sesuai dengan alat yang digunakan (Molyneux, 2004).
2.6.3 Waktu pengukuran
Waktu pengukuran menurut literatur yang direkomendasikan adalah
selama 60 menit, tetapi dalam beberapa penelitian waktu yang digunakan sangat
bervariasi yaitu 5 menit, 10 menit, 20 menit, 30 menit dan 60 menit. Waktu reaksi
yang tepat adalah ketika reaksi sudah mencapai kesetimbangan. Kecepatan reaksi
dipengaruhi oleh sifat dari aktivitas antioksidan yang terdapat di dalam sampel
(Molyneux, 2004; Prakash, 2001; Rosidah, et al., 2008).
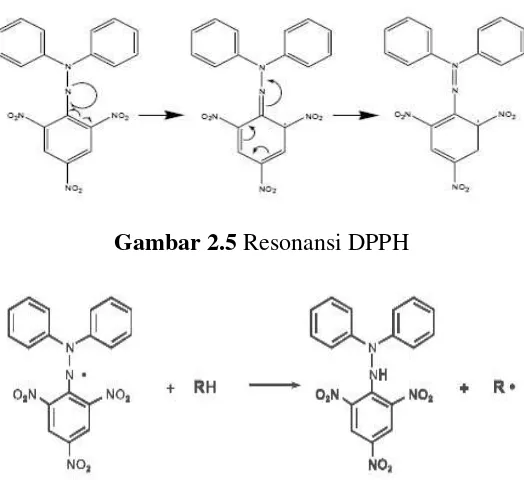
Resonansi DPPH dan reaksi antara DPPH dengan atom H yang berasal
Gambar 2.5 Resonansi DPPH