11 Gambar 8 memperlihatkan bahwa perubahan energi pita meningkat seiring dengan meningkatnya ukuran kristal dan menurun seiring dengan meningkatnya ukuran partikel. Artinya ukuran kristal yang besar memiliki energi pita yang besar dengan ukuran partikelnya lebih kecil dan sebaliknya.
Simpulan
Hasil sintesis nonostruktur ZnO dengan metode hidrotermal terhadap waktu 3 jam, 6 jam dan 12 jam telah didapatkan ukuran-ukuran partikel cenderung menurun yaitu 249 nm, 147 nm dan 107 nm dengan ukuran kristalnya juga meningkat seiring dengan perubahan ukuran partikel yaitu 44,32 nm, 50,65 nm, dan 54,37 nm dengan sebaran butiran partikelnya cenderung merata dan homogeny dengan masing-masing besarnya nilai energi pita adalah 3,18 eV, 3,21 eV dan 3,24 eV.
3
EKSTRAKSI, MODIFIKASI DAN KARAKTERISASI
KLOROFIL
Pendahuluan
Klorofil merupakan pigmen alam yang umumnya terdapat pada kelompok tumbuhan hijau yang terletak pada daun. Klorofil memiliki peranan sangat penting dalam proses fotosintesis. Cahaya matahari yang mengenai daun akan di serap oleh pigmen ini untuk mengubah gas karbon dioksida dan air menjadi glukosa dan oksigen. Secara khusus proses fotosintesis ini dapat digambarkan dengan reaksi sebagai berikut:
6 CO2 + H2O C6H12O6 + 6 O2
Penyerapan cahaya oleh klorofil ini disebabkan adanya peranan utama dari struktur porfirin yang mengikat ion magnesium (Mg2+), yang merupakan struktur utama klorofil. Saat menyerap cahaya, klorofil akan mentransferkan energinya untuk mengeksitasi elektron menuju ke pusat reaksi. Semakin lama tahapan eksitasi singlet klorofil, semakin besar konversi energi elektronik dari tingkat dasar ke tingkatan tereksitasi triplet dapat terjadi (Schaber et al. 1984).
Begitu kompleksnya reaksi fisika dan kimia dalam proses fotosintesis ini, telah menginspirasi manusia untuk membuat fotosintesis buatan yang dikenal sebagai artifisial fotosintesis. Dalam proses fotosintesis alami, elektron akan diubah menjadi energi kimia sebagai sumber makanan. Sedangkan dalam artifisialnya, elektron akan diubah menjadi energi listrik untuk menjadi arus listrik.
12
Untuk berbagai aplikasi, klorofil dianggap kurang efektif karena keberadaanya yang mudah terdegradasi. Menurunnya unsur Mg saat terdegradasi ini dapat disebabkan oleh reaksi langsung terhadap sifat asam (Budiyanto et al. 2008) dan panas (Erge et al. 2008).
Daun Katuk yang umumnya dimanfaatkan oleh masyarakat sebagai tanaman obat, akan dikembangkan lebih lanjaut dengan memanfaatkan kandungan klorofilnya untuk aplikasi lain. Dalam bagian penelitian ini akan dikaji tingkat stabilitas klorofil dari daun Katuk dengan mengganti unsur Mg nya dengan Zn2+ dan Cu2+, sebagaimana telah dilakukan oleh peneliti sebelumnya ( Kupper et al. 1996; Nurdin (2009); Nurhayati and Suendo. 2011; Zvezdanovic et al. 2012). Hasil subtitusi selanjutnya akan dimanfaatkan sebagai fotosensitiser atau fotoaktif yang berfungsi sebagai pemanen cahaya dalam sel surya hibrid nanopartikel ZnO bulk heterojunktion.
Tujuan
Melakukan ekstraksi dan modifikasi klorofil dengan ion Zn dan Cu serta menguji foto stabilitasnya.
Metode Isolasi dan Modifikasi Klorofil
Ekstraksi
Klorofil diperoleh dari daun Katuk yang telah diekstraksi dengan menggunakan pelarut organik etanol 96%. Pertama-tama daun Katuk dibilas terlebih dahulu dengan menggunakan akuades sampai bersih, kemudian ditiriskan sampai airnya benar-benar mengering. Selanjutnya menimbang daun Katuk sebanyak 100 gram dan dihancurkan dengan menggunakan mortar hingga permukaan daun Katuk benar-benar memar seluruhnya. Hasil tumbukan daun Katuk dimasukkan ke dalam 500 ml etanol 96% dan didiamkan selama 24 jam, setelah itu dilakukan penyaringan dengan menggunakan corong Bruncher. Penyaringan pertama dengan menggunakan kertas saring biasa. Residu dicuci dengan 500 ml atanol 96% dan disaring menggunakan kertas saring Whatman ukuran 40 mess. Penyaringan dilakukan dengan menggunakan pompa vakum. Filtrat diambil sebagai ekstrak kasar klorofil (Nurdin, 2009). Hasil penyaringan kemudian ditambahkan dengan MgCO3 sebanyak 1 ml. Kemudian disimpan semalam ke dalam freezer (-20oC), setelah itu dilakukan uji spektroskopi abasorbansi dan flouresensi dengan menggunakan spektrofotometer UV-Vis dan spektroflouresens (Ocean optics, Departemen Fisika, IPB). Semua proses dilakukan dalam ruang gelap. Pengukuran absorbansi dilakukan dengan sumber lampu Halogen.
Pengukuran flouresensi atau emisi dilakukan dengan menembakkan sinar laser (405 ±10 nm) ke sampel dengan posisi tegak lurus (90o), selanjutnya sinar tersebut akan diteruskan oleh fiber optik dan diterima oleh spektroflourometer dan diteruskan oleh konektor menuju PC. Di dalam PC, spektrum diolah ke dalam
13 bentuk gambar dan data yang ditampilkan oleh monitor. Lebih jelasnya proses pengukuran flouresensi ini dapat dilihat pada Gambar 9.
Gambar 9. Skema pengukuran flouresensi dye klorofil
Subtitusi logam inti klorofil
Penggantian logam inti pada klorofil (Mg) dengan unsur Zn dan Cu, pertama-tama dilakukan pendegradasian terlebih dahulu yaitu dengan menambahkan larutan klorofil dengan HCl 1M tetes demi tetes hingga pH 4 sambil diaduk menggunakan pengadu dengan kecepatan putaran 400 rpm (Nurdin. 2009). Hasil pendegradasian ini disebut feofitin. Feofitin ini kemudian disimpan dalam inkubator selama 24 jam pada suhu 40oC (Zvezdanovic et al. 2012). Setelah itu dilakukan penambahan ion Zn2+ atau Cu2+ dengan melarutkan 0,1 g/ml Zinc Acetat dihidrat ke dalam etanol atau 0,1 g/ml Cuprum chloride (Kupper et al. 1996) dan diaduk selama 30 menit sampai terjadi perubahan warna. Semua proses dilakukan dalam ruang gelap. Setelah reaksi dilakukan, campuran dimasukkan ke dalam freezer (-20oC) dan didiamkan selama semalam setelah itu dilakukan uji spektroskopi absorbansi, kemudian semua larutan (klorofil, Zn-feofitin dan Cu-Zn-feofitin) dikeringkan dengan menggunakan pengering (freezdryer, PAU laboratorium mikrobiologi IPB).
Fotostabilitas
Uji stabilitas ini dilakukan melalui pengukuran spektroskopi absorbansi, dimana larutan klorofil dan klorofil kompleks didegradasi menggunakan lampu halogen yang berintensitas 34 W/m2. Penyinaran dilakukan selama 5 jam dan pengambilan data absorbansi dilakukan setiap 30 menit.
Laser Sampel Spektroflourometer (Fl) (Ocen Optics) Monitor PC Fiber optik Konektor
14
Hasil dan Pembahasan
Sifat optik klorofil ekstrak daun Katuk menggunakan etanol 96% menghasilkan dua daerah serapan utama yaitu 436,53 nm (soret band) dan 664,00 nm (Q-band). Serapan pada daerah soret band lebih tinggi dari pada daerah Q-band. Ini menunjukkan bahwa pada klorofil tahapan eksitasi elektronnya ada dua dari keadaan ground state (So), yaitu singlet pertama (S1) yang terjadi pada daerah merah dan singlet kedua (S2) yang terjadi pada daerah biru.
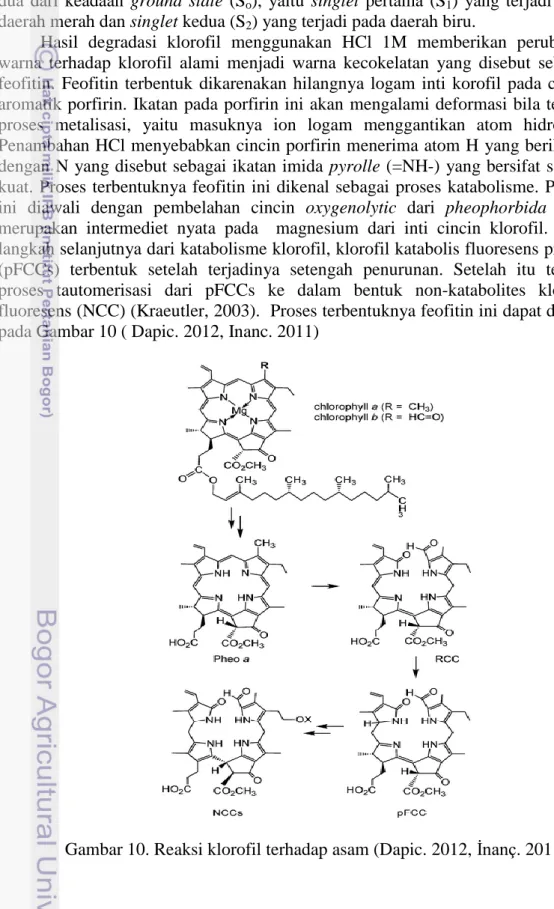
Hasil degradasi klorofil menggunakan HCl 1M memberikan perubahan warna terhadap klorofil alami menjadi warna kecokelatan yang disebut sebagai feofitin. Feofitin terbentuk dikarenakan hilangnya logam inti korofil pada cincin aromatik porfirin. Ikatan pada porfirin ini akan mengalami deformasi bila terjadi proses metalisasi, yaitu masuknya ion logam menggantikan atom hidrogen. Penambahan HCl menyebabkan cincin porfirin menerima atom H yang berikatan dengan N yang disebut sebagai ikatan imida pyrolle (=NH-) yang bersifat sangat kuat. Proses terbentuknya feofitin ini dikenal sebagai proses katabolisme. Proses ini diawali dengan pembelahan cincin oxygenolytic dari pheophorbida yang merupakan intermediet nyata pada magnesium dari inti cincin klorofil. Pada langkah selanjutnya dari katabolisme klorofil, klorofil katabolis fluoresens primer (pFCCs) terbentuk setelah terjadinya setengah penurunan. Setelah itu terjadi proses tautomerisasi dari pFCCs ke dalam bentuk non-katabolites klorofil fluoresens (NCC) (Kraeutler, 2003). Proses terbentuknya feofitin ini dapat dilihat pada Gambar 10 ( Dapic. 2012, Inanc. 2011)
15 Hasil karakterisasi optik feofitin menunjukkan daerah serapan utama untuk soret band adalah 421,50 nm dan 657,28 nm untuk Q-band. Feofitin kemudian dimetalisasi dengan ion logam Zn2+ dan Cu2+, dan menunjukkan adanya perubahan warna dan daerah serapan. Feofitin yang tersubtitusi dengan ion Zn2+ mengalami perubahan warna menjadi hijau muda dengan daerah puncak serapannya 428,82 nm untuk daerah soret band dan 658,41 nm untuk daerah Q-band. Sedangkan untuk yang termodifikasi ion Cu2+, memberikan perubahan warna pada feofitin menjadi hijau tua dengan daerah puncak serapan 408,44 nm untuk daerah soret band dan 646,00 nm untuk daerah Q-band. Hasil karakterisasi optik ini dapat dilihat pada Gambar 11.
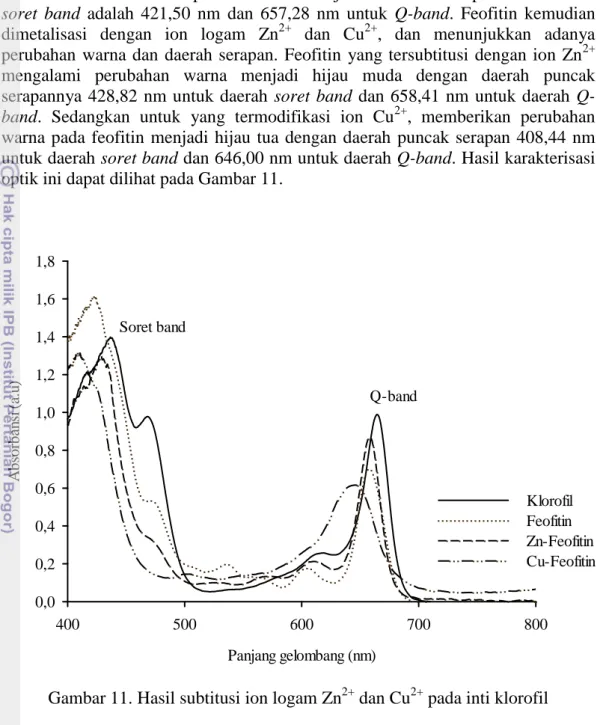
soret band Q-band Panjang gelombang (nm) 400 500 600 700 800 A b so rb an si ( a.u ) 0,0 0,2 0,4 0,6 0,8 1,0 1,2 1,4 1,6 1,8 Klorofil Feofitin Zn-Feofitin Cu-Feofitin Soret band Q-band
Gambar 11. Hasil subtitusi ion logam Zn2+ dan Cu2+ pada inti klorofil Berdasarkan pengamatan pola spektrum pada Gambar 11 tampak bahwa penggantian unsur logam pada inti klorofil, menyebabkan terjadinya pergeseran baik daerah Soret band maupun Q-band yang bergeser ke daerah biru. Hasil ini berbeda dengan hasil penelitian sebelumnya oleh Nurhayati et al (2009), dimana daerah soret band bergeser ke arah merah dengan pelarut metanol. Namun, dari hasil penelitian yang dilakukan Zvedanovic et al (2012), juga melakukan subtitusi pada klorofil dengan unsur Zn2+ dan Cu2+ menggunakan pelarut etanol 96% dan didapatkan pergeseran ke daerah biru, baik daerah soret band maupun Q-band. Dari hasil tersebut menunjukkan bahwa pelarut yang digunakan juga berpengaruh pada daerah serapan.
Pergeseran pada daerah Soret band dan Q-band maksimum ke panjang gelombang yang lebih rendah atau energi yang lebih besar dari klorofil. Ini
16
mengindikasikan bahwa energi gap antara HOMO (Highest Occupied Molecular Orbital) dan LUMO (Lowest Unoccupied Molecular Orbital) pada Zn-feofitin dan Cu-feofitin lebih besar dari klorofil. Perbedaan besarnya nilai energi ini, tentu saja akan berpengaruh pada tahapan tingkat eksitasi elektroniknya. Energi yang besar akan memberikan tahapan eksitasi yang lebih lama pada daerah singlet dan memberikan peluang untuk tereksitasi pada daerah triplet. Kelebihan energi pada daerah triplet, akan menyebabkan peluang terjadinya transfer energi ke molekul oksigen yang bersifat merusak (Fiedor et al. 2002; Agostiano et al. 2003).
Pada Gambar 11 pula, dapat dilihat khususnya daerah Q-band, telah terjadi penurunan tingkat absorbansi. Penurunan nilai absorbansi ini mengindikasikan besarnya kosentrasi pada masing-masing dye, sehingga pada Gambar 11 dapat dilihat bahwa hasil subtitusi logam Zn dan Cu lebih rendah dari klorofil. Untuk klorofil yang tersubtitusi Cu memiliki daerah serapan yang lebih luas dari pada yang tersubtitusi Zn. Akan tetapi secara keseluruhan, klorofil yang tersubtitusi dengan ion logam, menyebabkan pelebaran pada daerah serapan klorofil. Pelebaran daerah serapan ini kemungkinan disebabkan oleh struktur baru yang terbentuk akibat proses metalisasi sehingga mengakibatkan perubahan energi pada level HOMO dan LUMO.
Pada daerah Q- band yang menyatakan absorbansi maksimum dari dye, dan daerah flouresensi yang menyatakan tempat terjadinya emisi. Hubungan antara spektrum absorbansi dan emisi terhadap panjang gelombang yang dikonversi ke dalam bentuk energi (eV) memberikan gambaran yang dikenal sebagai pergeseran Stokes. Pergeseran ini disebabkan oleh perbedaan antara struktur relaksasi pada keadaan ground dan keadaan eksitasi, sebagaimana pada Gambar 12.
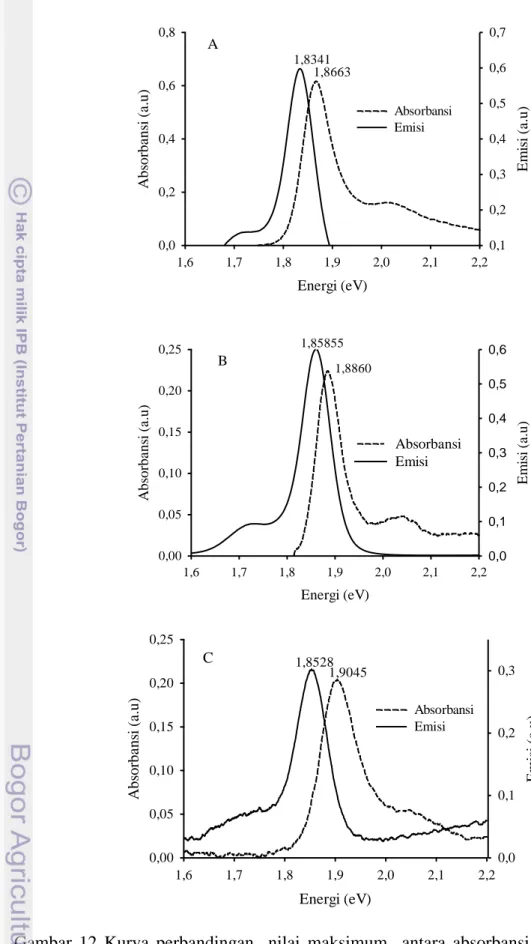
Pada Gambar 12 tampak bahwa pergeseran Stokes antara absorbansi maksimum dan emisi maksimum yaitu 0,032 eV untuk korofil, 0,028 eV untuk Zn-feofitin dan 0,053 eV untuk Cu-feofitin. Hasil ini memperlihatkan bahwa pergeseran Stokes dari Cu-feofitin lebih besar dari pada klorofil dan Zn-feofitin. Ini menunjukkan bahwa waktu yang dibutuhkan Cu-feofitin dalam relaksasi lebih lama, sedangkan untuk Zn-feofitin lebih singkat dari klorofil. Hasil ini berbeda dengan eksperimen sebelumnya yang dilakukan oleh Nurhayati et all (2011), yang lebih mengkhususkan pada klorofil a, dimana Zn-feofitin membutuhkan waktu yang lebih lama dalam relaksasi yaitu dua kali dari klorofil a. Dalam kajian yang lain, telah dijelaskan bahwa pergeseran Stokes juga dipengaruhi oleh pelarut yang digunakan (Agmon. 1990).
17 Energi (eV) 1,6 1,7 1,8 1,9 2,0 2,1 2,2 A bs orba ns i (a .u) 0,0 0,2 0,4 0,6 0,8 E m is i (a .u) 0,1 0,2 0,3 0,4 0,5 0,6 0,7 Absorbansi Emisi 1,8341 1,8663 A Energi (eV) 1,6 1,7 1,8 1,9 2,0 2,1 2,2 A bs orba ns i (a .u) 0,00 0,05 0,10 0,15 0,20 0,25 E m is i (a .u) 0,0 0,1 0,2 0,3 0,4 0,5 0,6 Absorbansi Emisi 1,8860 1,85855 B Energi (eV) 1,6 1,7 1,8 1,9 2,0 2,1 2,2 A bs orba ns i (a .u) 0,00 0,05 0,10 0,15 0,20 0,25 E m is i (a .u) 0,0 0,1 0,2 0,3 Absorbansi Emisi 1,8528 1,9045 C
Gambar 12 Kurva perbandingan nilai maksimum antara absorbansi dan emisi dari dye alam dalam etanol 96%. Klorofil (A), Zn-feofitin (B) dan Cu-feofitin (C)
18
Analisis fotostabilitasklorofil
Pengujian klorofil hasil ekstrak dan yang telah disubtitusi dengan ion logam Zn2+ dan Cu2+ dengan penyinaran lampu halogen dengan intensitas 34 W/m2. Dari hasil pengamatan yang diperoleh, klorofil yang terdegradasi mengalami pemudaran warna menjadi hijau kelabu (Zvezdanovic et al. 2008) yang disertai dengan penurunan puncak absorbansi (proses hipokromik) pada daerah Q-band (Erge et al. 2008). Selain penyinaran, pendegradasian warna klorofil juga disebabkan oleh pengaruh asam yang menyebabkan proses pembentukan produk degradasi seperti pelepasan inti logam klorofil sehingga lebih cepat dalam pembentukan proses feofitinase (Gross. 1991; Jeffrey et al. 1997; Gaur et al.2006; Budiyanti et al. 2008). Pada proses ini terjadi reaksi oksidasi pada ikatan metin antara C4 dan C5 yang menyebabkan terjadinya tetrapirol linier, sehingga C5 membentuk gugusformil (HCO-) yang kelebihan atom O, sedangkan C4 membentuk gugus laktam (Matile et al.1999).
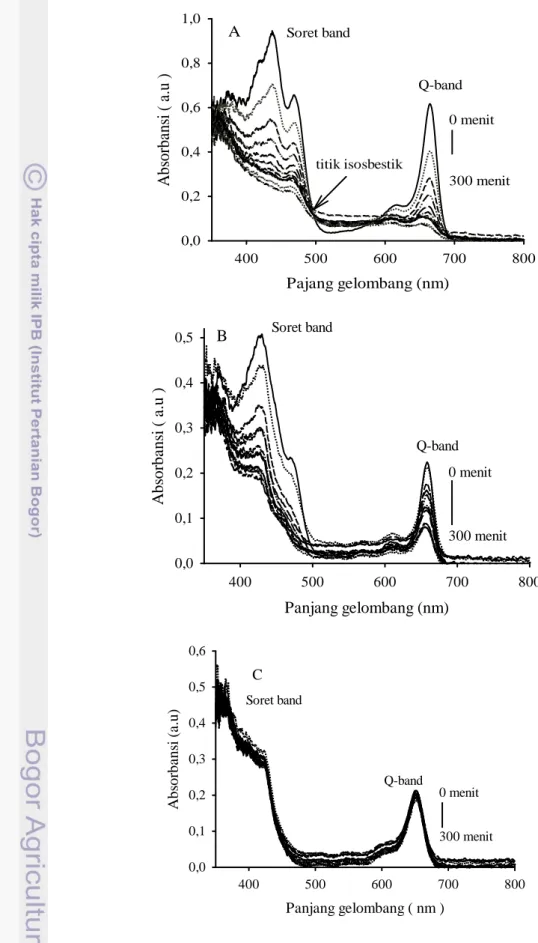
Gambar 13(A) dapat dilihat bahwa klorofil setelah dilakukan penyinaran mengalami kenaikan pada daerah panjang gelombang sekitar 500-600 nm dan akhirnya membentuk suatu kurva yang terikat secara bersama. Ini menunjukkan bahwa telah terjadi reaksi kesetimbangan dan memiliki koefisien serapan pola yang sama pada molekul yang berbeda (isosbestik) (Endo et al. 1984; Christina et al. 2008). Sedangkan pada Gambar 13(B) hampir tidak terlihat terjadinya perubahan yang signifikan pada daerah isosbestik, Ini memperlihatkan bahwa klorofil yang tersubtitusi oleh ion Zn2+ (Zn-feofitin) cenderung lebih stabil dari klorofil, akan tetapi pada daerah Q-band terjadi penurunan puncak meskipun tidak begitu signifikan. Ini menunjukan bahwa pada Zn-feofitin masih terjadi proses feofitinase dan pada daerah 500-600 nm terdapat sedikit puncak-puncak kecil yang mengindikasikan terjadinya eksitasi terendah dari spesis singlet (Budiyanto et al. 2008). Untuk klorofil yang tersubtitusi oleh ion Cu2+ (Gambar 13(C)) terlihat spektrum absorbansinya pada daerah Q-band hampir tidak terjadi penurunan dan tidak terlihat terbentukya daerah isobestik, Ini menunjukkan bahwa molekul-molekul yang ada setelah penambahan ion Cu2+ cenderung tidak mengalami perubahan.
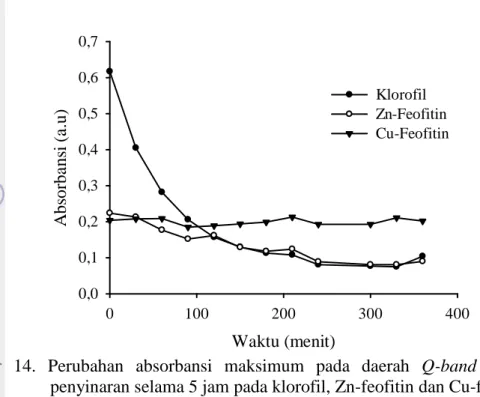
Perbedaan perubahan klorofil sebelum dan sesudah penambahan ion logam setelah penyinaran selama 5 jam dapat dilihat pada Gambar 14. Gambar 14 merupakan hasil plot antara nilai absorbansi maksimum pada daerah Q-band terhadap perubahan waktu.
Pada Gambar 14 tersebut memperlihatkan bahwa klorofil yang telah termodifikasi mengalami penurunan kosentrasi, yang ditandai dengan penurunan tingkat absorbansi. Klorofil tampak mengalami penurunan drastis sampai pada menit ke 90. Untuk klorofil termodifikasi dengan Zn (Zn-feofitin) sedikit mengalami penurunan juga pada menit ke 90. Sedangkan untuk klorofil yang termodifikasi dengan Cu (Cu-feofitin) hampir tidak terlihat mengalami penurunan absorbansi, yang mana nilai absorbansinya tetap menunjukkan pada nilai absorbansi kurang lebih 0,2 selama dilakukan penyinaran. Untuk klorofil dan Zn-feofitin stabil pada nilai absorbansi kurang lebih 0,1 selama penyinaran.
19 Pajang gelombang (nm) 400 500 600 700 800 A bs orba ns i ( a.u ) 0,0 0,2 0,4 0,6 0,8 1,0 A Q-band Soret band titik isosbestik 0 menit 300 menit Panjang gelombang (nm) 400 500 600 700 800 A bs or ba ns i ( a .u ) 0,0 0,1 0,2 0,3 0,4 0,5 Q-band Soret band B 0 menit 300 menit Panjang gelombang ( nm ) 400 500 600 700 800 A bs or ba ns i ( a .u ) 0,0 0,1 0,2 0,3 0,4 0,5 0,6 Q-band Soret band C 0 menit 300 menit
Gambar 13. Kurva absorbansi degradasi klorofil dan klorofil kompleks terhadap waktu: Klorofil (A), Zn-peofitin (B), Cu-peofitin (C).
20 Waktu (menit) 0 100 200 300 400 A bs orba ns i (a .u) 0,0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 Klorofil Zn-Feofitin Cu-Feofitin
Gambar 14. Perubahan absorbansi maksimum pada daerah Q-band setelah penyinaran selama 5 jam pada klorofil, Zn-feofitin dan Cu-feofitin Gambar 14 juga menunjukkan adanya nilai absorbansi yang sama khususnya untuk klorofil dan Zn-feofitin, yaitu pada menit ke 150. Ini menunjukkan bahwa klorofil dan Zn-feofitin telah mengalami perubahan struktur molekul menjadi bentuk yang baru, selama itu juga ditandai dengan adanya titik isobestik yang terbentuk, seperti yang dijelaskan pada Gambar 13.
Simpulan
Panambahan ion logam Zn2+ Cu2+ pada klorofil membentuk molekul baru yang dikenal sebagai Zn-feofitin dan Cu-feofitin menunjukkan tingkat kestabilan yang lebih baik, khusunya Cu-feofitin setelah diradiasi selama 5 jam dengan lampu halogen 34 W/m2+. Tingkat kestabilan ini memberikan tingkat relaksasi yang lebih lama antara absorbansi maksimum dan emisi maksimum yang terjadi pada daerah merah