BAB III
METODOLOGI PENELITIAN
3.1 LOKASI DAN WAKTU PENELITIAN
Penelitian ini dilaksanakan di Laboratorium Penelitian, Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara. Penelitian ini dilakukan selama lebih kurang 6 bulan.
3.2 BAHAN DAN PERALATAN
3.2.1 Bahan Penelitian
Pada penelitian ini bahan utama yang digunakan adalah:
1. Minyak Kelapa Sawit Mentah (Crude Palm Oil) diperoleh dari Pabrik Kelapa Sawit (PKS) Pagar Merbau PTPN II Persero, Tanjung Morawa, Medan, Indonesia.
2. Ampas Teh diperoleh dari pedagang Mie Aceh Pasar V, Kecamatan Medan Selayang, Padang bulan, Medan
3. Asam Posfat (H3PO4)
3.2.2 Peralatan Penelitian
3.2.2.1 Peralatan Pembuatan Karbon Aktif Peralatan utama yang digunakan:
1. Pengering Baki (Tray Drier) 2. Ball mill
3. Ayakan 50 mesh 4. Cawan
5. Reaktor Pirolisis 6. Kertas pH
7. Kertas Saring Whatman no. 1 8. Water bath
3.2.2.2 Peralatan untuk Proses Adsorpsi Peralatan utama yang digunakan:
1. Erlenmeyer 2. Beaker glass 3. Pipet tetes
4. Kertas saring Whatman no. 1 5. Gelas ukur
6. Corong gelas 7. Neraca digital 8. Termometer 9. Alumunium foil 10. Hot plate 11. Motor listrik 12. Impeller paddle 13. Pengunci impeller 14. Statif dan klem 15. Stopwatch
3.2.2.3 Uji dan Analisa 1. Alat HPLC 2. BET 3. Furnace.
3.3 VARIASI PENELITIAN
Tabel 3.1 Variasi Penelitian Kajian Kinetika pada Proses Adsorpsi α-tokoferol Waktu (menit) Rasio Karbon Aktif : Berat
CPO
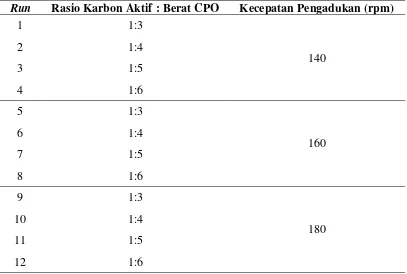
Tabel 3.2 Variasi Penelitian Kajian Isoterm pada Proses Adsorpsi α-tokoferol Run Rasio Karbon Aktif : Berat CPO Kecepatan Pengadukan (rpm)
1 1:3
3.4 PROSEDUR PENELITIAN
3.4.1 Prosedur Pembuatan Karbon Aktif
1. Ampas teh diambil dari pedagang mie aceh Pasar V Padang Bulan, Medan.
2. Ampas teh dikeringkan dengan menggunakan Tray Drier dengan suhu 40 o
3. Ampas teh dihaluskan dengan menggunakan ball mill. 4. Ampas teh diayak dengan menggunakan ayakan 50 mesh
5. Ampas teh direndam dalam larutan H3PO4 85% selama 24 jam. Perbandingan antara ampas teh : H3PO4 adalah 1:2.
6. Ampas teh yang telah diaktivasi selanjutnya dikeringkan di dalam oven pada suhu 110 C.
7. Ampas teh yang telah kering dikarbonisasi dengan menggunakan reaktor pirolisis pada suhu 500 C selama 15 menit
8. Karbon aktif hasil pirolisis dicuci dengan air bersuhu 85 C sampai pH netral.
9. Karbon aktif dikeringkan dalam oven pada suhu 110 C. 10. Karbon aktif dihaluskan dengan menggunakan mortar.
3.4.2 Prosedur Analisa Kadar Abu (SNI 06-3730-1995)
1. Cawan porselin dikeringkan di dalam furnace pada suhu 600 oC selama 30 menit.
2. Kemudian cawan didinginkan dalam desikator selama 30 menit lalu ditimbang berat kosongnya.
3. Ke dalam cawan tersebut dimasukkan sampel sebanyak 1 gram.
4. Cawan yang telah berisi sampel selanjutnya dimasukkan ke dalam furnace pada suhu 850 oC selama 4 jam sampai sampel menjadi abu. 5. Cawan diangkat dari dalam furnace dan didinginkan di dalam desikator
lalu ditimbang.
6. Kadar abu dihitung dengan Persamaan 3.1.
Kadar abu (%) = (A/B) x 100% (3.1) A = Berat abu (gram)
B = Berat sampel (gram)
3.4.3 Pengujian Kadar Zat Volatil (SNI 06-3730-1995)
2. Kemudian ditimbang dengan teliti sebanyak 1 gram sampel ke dalam cawan kosong tersebut
3. Cawan selanjutnya ditutup dan dimasukkan ke dalam furnace dengan suhu 950 oC selama 7 menit
4. Kadar zat volatil pada suhu 950 oC dapat dihitung dengan menggunakan Persamaan 3.2.
Kadar volatil = w -w1
w x 1 dimana:
w0 = Berat sampel awal (gram)
w1 = Berat sampel setelah pemanasan (gram)
3.4.4 Prosedur Kinetika Adsorpsi
1. Minyak kelapa sawit (crude palm oil) dan karbon aktif disiapkan dengan perbandingan (w/w) 1 : 6 di dalam beaker glass .
2. Campuran dipanaskan menggunakan hot plate pada suhu 40 oC dan dihomogenkan menggunakan motor listrik dengan kecepatan konstan 180 rpm.
3. Campuran diambil dengan interval waktu yang telah ditentukan hingga mencapai waktu setimbang.
4. Sampel disaring dengan kertas saring Whatman No.1.
5. Campuran yang telah selesai disaring, dimasukkan ke dalam botol plastik dan dianalisa dengan alat HPLC.
3.4.5 Prosedur Kajian Isoterm Adsorpsi
1. Minyak kelapa sawit (crude palm oil) dan karbon aktif disiapkan dengan perbandingan (w/w) 1 : 3 di dalam beaker glass .
2. Campuran dipanaskan menggunakan hot plate pada suhu 40 C dan dihomogenkan menggunakan motor listrik dengan kecepatan konstan 180 rpm selama 20 menit. Selama proses berlangsung beaker glass ditutup dengan menggunakan alumunium foil.
3. Setelah selesai, campuran disaring untuk memisahkan filtrat dan adsorbennya menggunakan kertas saring Whatman No. 1.
4. Filtrat dimasukkan ke dalam botol plastik dan dianalisa dengan alat HPLC.
5. Percobaan diulangi dengan variasi berat Karbon aktif : CPO yaitu untuk 1:4 ; 1:5 ; 1:6 dan kecepatan pengadukan adsorpsi yaitu 140 dan 160 rpm.
3.4.6 Analisa Sampel
1. Pengujian Kadar Abu dan Kadar Zat Volatil (Volatile matter) dilakukan di Laboratorium Pendidikan Teknologi Kimia Industri (PTKI), Medan. 2. Pengujian luas permukaan karbon aktif dilakukan di Laboratorium
Universitas Gajah Mada (UGM), Yogyakarta.
3. Konsentrasi α-tokoferol dalam CPO akan dianalisa sebelum dan sesudah proses adsorpsi dengan menggunakan instrumen spektrofotometer UV-VIS pada Laboratorium Pusat Penelitian Kelapa Sawit (PPKS), Medan.
3.4.7 Pengolahan Data
1. Penentuan % adsorpsi dan kapasitas adsorben.
2. Penentuan model isoterm yang sesuai dengan hasil penelitian pada masing-masing suhu adsorpsi.
BAB IV
HASIL DAN PEMBAHASAN
4.1 KARAKTERISTIK KARBON AKTIF DARI AMPAS TEH
Karakteristik karbon aktif dari ampas teh ditentukan oleh beberapa parameter diantaranya adalah kadar abu, kadar volatile matter, dan luas permukaan karbon aktif. Tabel 4.1 menampilkan karakteristik karbon aktif dari ampas teh.
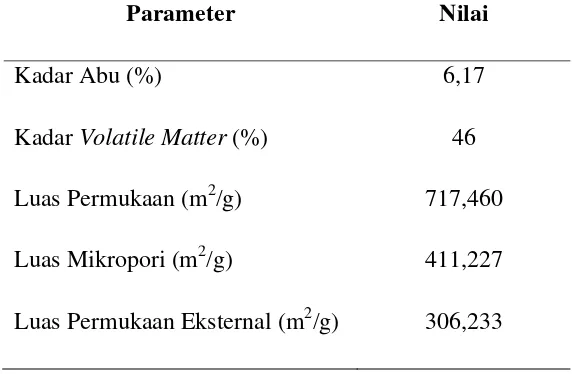
Tabel 4.1 Karakteristik Karbon Aktif dari Ampas Teh
Parameter Nilai
Kadar Abu (%) 6,17
Kadar Volatile Matter (%) 46
Luas Permukaan (m2/g) 717,460 Luas Mikropori (m2/g) 411,227 Luas Permukaan Eksternal (m2/g) 306,233
Penentuan kadar abu dan kadar volatile matter maing-masing dilakukan menggunakan metode SNI 06-3730-1995 dan metode SNI 06-3730-1995. Sedangkan untuk penentuan luas permukaan, luas mikropori, dan luas permukaan eksternal dilakukan dengan metode BET menggunakan alat Nova Station B buatan Quantachcrome.
Untuk parameter volatile matter, jumlah volatile matter yang terkandung dalam karbon aktif dari ampas teh adalah 46%. Kadar volatile matter menunjukkan besarnya kandungan senyawa yang mudah menguap yang terkandung dalam karbon aktif pada suhu 950 oC [35]. Semakin lama waktu perendaman dan semakin tinggi konsentrasi aktivator akan menyebabkan semakin tinggi pula kandungan volatile matter yang terdapat dalam karbon aktif [36]. Kadar volatile matter yang sesuai dengan Standar Nasional Indonesia adalah maksimal 25% [36]. Berdasarkan hal tersebut, maka kadar volatile matter pada karbon aktif dari ampas teh belum sesuai dengan Standar Nasional Indonesia. Hal ini dapat disebabkan oleh waktu perendaman yang terlalu lama dan konsentrasi aktivator yang digunakan terlalu tinggi sehingga menyebabkan tingginya kandungan zat volatile matter yang terdapat dalam karbon aktif dari ampas teh.
Dari Tabel 4.1 juga dapat dilihat bahwa karbon aktif dari ampas teh memiliki luas permukaan sebesar 717,460 m2/g dengan luas mikropori sebesar 411,227 m2/g, dan luas permukaan eksternal sebesar 306,233 m2/g. Luas permukaan karbon aktif umumnya berkisar antara 300-2.000 m2/g [37]. Berdasarkan hal ini dapat disimpulkan bahwa luas permukaan karbon aktif dari ampas teh telah berada dalam rentang nilai yang umum.
Berdasarkan parameter yang telah diuraikan diatas, maka karbon aktif dari ampas teh telah mendekati karakteristik dari karbon aktif standar, hal ini dapat dilihat dari kadar abu dan luas permukaan karbon aktif dari ampas teh yang telah sesuai dengan standar. Namun karbon aktif dari ampas teh masih memiliki kadar volatile matter yang tinggi sehingga perlu ditentukan proses aktivasi yang optimal agar kadar
volatile matter sesuai dengan standar.
4.2 PENGARUH KECEPATAN PENGADUKAN DAN RASIO KARBON AKTIF : CPO TERHADAP PERSENTASE ADSORPSI α-TOKOFEROL
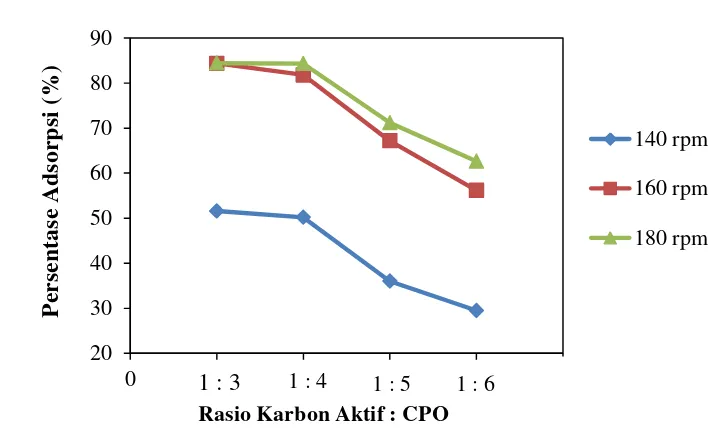
Gambar 4.1 Pengaruh Kecepatan Pengadukan dan Rasio Karbon Aktif : CPO Terhadap Persentase Adsorpsi α-Tokoferol
Dengan jumlah massa adsorben yang sama, dapat dilihat bahwa dengan bertambahnya jumlah CPO yang digunakan akan mengakibatkan penurunan pada persentase adsorpsi. Dari Gambar 4.1 dapat dilihat untuk ketiga kondisi kecepatan pengadukan, persentase adsorpsi terus menurun seiring dengan bertambahnya rasio antara karbon aktif : CPO. Hal ini menunjukkan bahwa kemampuan adsorben untuk menjerap α-tokoferol semakin berkurang seiring dengan bertambahnya jumlah CPO.
Sedangkan untuk pengaruh kecepatan pengadukan, dapat dilihat bahwa semakin cepat pengadukan maka persentase adsorpsi semakin meningkat. Laju adsorpsi dikendalikan oleh film dan difusi pori yang dipengaruhi oleh pengadukan. Kecepatan pengadukan yang rendah menyebabkan menebalnya lapisan film pelarut yang mengelilingi adsorben dan menjadikan lapisan film sebagai tahap pengendali laju adsorpsi, sedangkan apabila kecepatan pengadukan tinggi lapisan film akan menipis sehingga difusi pori menjadi tahap pengendali laju adsorpsi [40]. Dengan meningkatnya kecepatan pengadukan maka difusi pori α-tokoferol akan semakin mudah dan adsorbat yang dapat dijerap semakin besar, sehingga akan meningkatkan persentase adsorpsi α-tokoferol. Hal ini dapat dilihat dari nilai persentase adsorspi maksimum yang diperoleh untuk adsorpsi α-tokoferol yaitu pada rasio karbon aktif : CPO sebesar 1:3 dengan kecepatan pengadukan 180 rpm yaitu sebesar 84,42%.
Rasio Karbon Aktif : CPO
140 rpm
160 rpm
180 rpm
Namun pada kecepatan yang tinggi, untuk rasio karbon aktif : CPO yang rendah, pengaruh kecepatan pengadukan tidak begitu besar. Hal ini dapat dilihat pada rasio 1:3 untuk kecepatan pengadukan 160 rpm persentase adsorpsi sebesar 84,36% sedangakan untuk kecepatan pengadukan 180 rpm sebesar 84,42%.
4.3 PENGARUH KECEPATAN PENGADUKAN DAN RASIO KARBON AKTIF : CPO TERHADAP KAPASITAS ADSORPSI α-TOKOFEROL
Selain persentase adsorpsi, aspek yang ditinjau dalam proses adsorpsi α -tokoferol dengan karbon aktif dari ampas teh adalah jumlah adsorbat yang mampu dijerap oleh karbon aktif dari ampas teh. Pada penelitian ini dilihat bagaimana pengaruh kecepatan pengadukan dan rasio karbon aktif : CPO terhadap kapasitas adsorpsinya. Data hasil penelitian mengenai pengaruh kecepatan pengadukan dan rasio karbon aktif : CPO ditunjukkan pada Gambar 4.2.
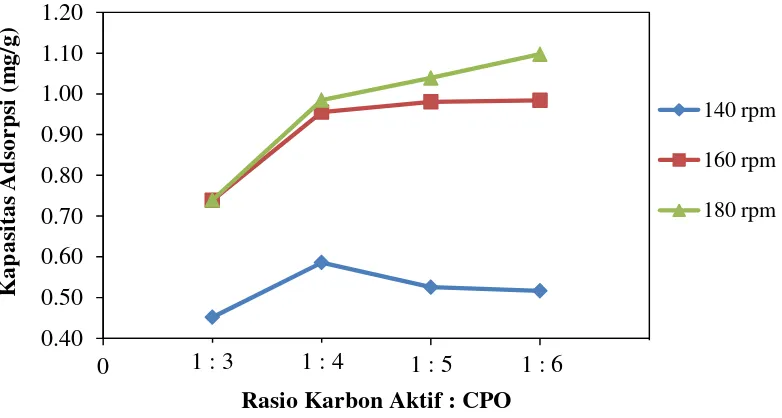
Gambar 4.2 Pengaruh Kecepatan Pengadukan dan Rasio Karbon Aktif : CPO Terhadap Kapasitas Adsorpsi α-Tokoferol
Dari Gambar 4.2 dapat dilihat bahwa terjadi peningkatan pada kapasitas adsorpsi seiring dengan semakin bertambahnya kecepatan pengadukan. Dapat dilihat pada percobaan dengan kondisi rasio karbon aktif : CPO sebesar 1:6, terjadi kenaikan pada kapasitas adsorpsi dari 0,5164 mg/gram untuk kecepatan 140 rpm, menjadi 0,9841 mg/gram untuk kecepatan 160 rpm kemudian bertambah lagi menjadi 1,0973
0.40
Rasio Karbon Aktif : CPO
140 rpm
160 rpm
180 rpm
mg/gram untuk kecepatan 180 rpm. Hal ini disebabkan oleh dengan semakin besarnya kecepatan pengadukan maka akan menyebabkan lapisan film pelarut yang mengelilingi adsorben semakin tipis [43] sehingga akan meningkatkan kapasitas adsorpsi. Namun untuk rasio karbon aktif : CPO yang rendah seperti pada keadaan 1:3, kenaikan kapasitas adsorpsi tidak begitu signifikan pada kecepatan 160 rpm dengan 180 rpm yaitu dari 0,7388 mg/gram menjadi 0,7394 mg/gram.
Sedangkan untuk pengaruh rasio antara karbon aktif : CPO, kapasitas adsorpsi akan semakin meningkat seiring dengan semakin besarnya rasio. Hal ini dapat dilihat pada percobaan dengan kecepatan 160 dan 180 rpm dimana kapasitas adsorpsi terus meningkat seiring dengan semakin besarnya rasio antara karbon aktif : CPO. Dengan jumlah massa karbon aktif dari ampas teh yang sama, penambahan massa CPO akan meningkatkan massa α-tokoferol yang terkandung didalamnya, sehingga akan menyebabkan semakin besar jumlah massa α-tokoferol yang dapat diadsorpsi. Berdasarkan hasil percobaan, kapasitas adsorpsi terbesar diperoleh pada keadaan rasio karbon aktif : CPO pada 1:6 dan kecepatan pengadukan 180 rpm dengan nilai sebesar 1,0973 mg/g.
4.4 KINETIKA ADSORPSI α-TOKOFEROL
Penetuan model kinetika dilakukan berdasarkan persamaan model kinetika orde satu dan orde dua semu yang ditunjukkan oleh Persamaan 2.5 dan 2.7. Pada penelitian ini, digunakan perbandingan karbon aktif : CPO (w/w) = 1:6 pada kecepatan pengadukan 180 rpm yang dianalisa pada interval waktu yang telah ditentukan hingga mencapai kesetimbangan.
Gambar 4.3 Kurva Penyerapan α-Tokoferol
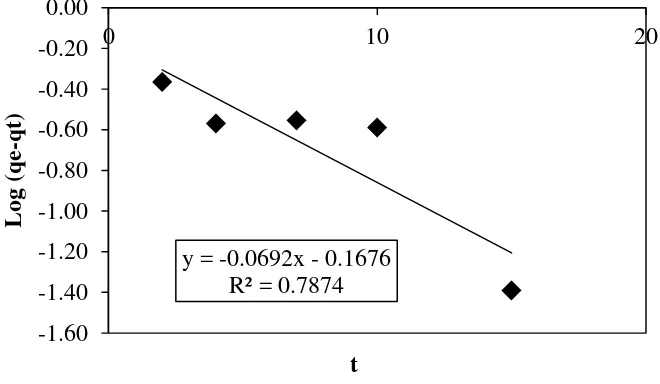
Data hasil penelitian yang diperoleh kemudian diolah untuk menentukan model kinetika yang sesuai pada proses adsorpsi α-tokoferol. Penentuan model kinetika dilakukan dengan menguji kesesuaian antara data hasil penelitian dengan Persamaan 2.5 dan Persamaan 2.7 yang telah dilinierisasi menjadi Persamaan 2.6 dan Persamaan 2.8 seperti yang ditunjukkan pada Subbab 2.7 sehingga diperoleh grafik hubungan antara t vs Log(qe-qt) untuk model kinetika orde satu semu dan t vs t/qt untuk model kinetika orde dua semu. Uji kesesuaian data penelitian dengan kedua model kinetika ditunjukkan pada gambar 4.2 dan 4.3
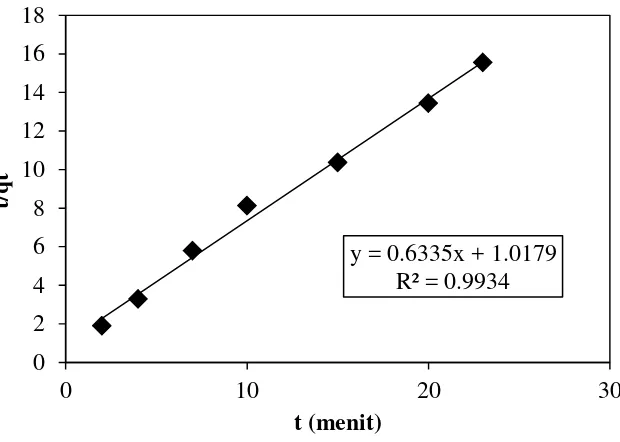
Gambar 4.5 Uji Kesesuaian Data Penelitian dengan Model Kinetika Orde Dua Semu Dari Gambar 4.2 dan 4.3 didapat persamaan dan nilai koefisien korelasi masing-masing model kinetika untuk dihitung konstantanya. Persamaan dan nilai koefisien korelasi masing-masing model kinetika disajikan pada Tabel 4.2
Tabel 4.2 Data Kinetika Adsorpsi α-tokoferol
Model Kinetika Persamaan R2 Konstanta
Orde Satu Semu
Lagergen y = -0,0692x - 0,1676 0,7874 k1 = 0,6798 Orde Dua Semu
Lagergen y = 0,6335x + 1,0179 0,9934 k2 = 0,0578
disimpulkan bahwa proses adsorpsi α-tokoferol dengan karbon aktif adalah model kinetika orde dua semu dengan nilai konstanta sebesar 0,0578. Model kinetika orde dua semu memberikan asumsi bahwa adsorpsi kimia merupakan tahap penentu kecepatan yang mengontrol proses adsorpsi tersebut [41, 42].
4.5 PENENTUAN MODEL ISOTERM ADSORPSI
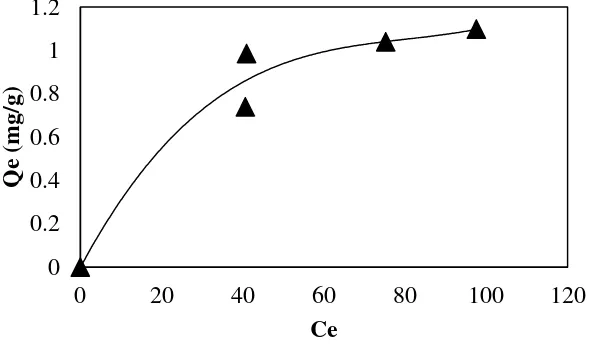
Pada penelitian ini, model isoterm adsorpsi didekati menggunakan persamaan isoterm Langmuir dan persamaan isoterm Freundlich. Hal ini bertujuan untuk mengetahui apakah proses adsorpsi α-tokoferol merupakan adsorpsi lapisan tunggal atau lapisan jamak [39]. Gambar 4.3 menyajikan hubungan antara konsentrasi keseimbangan dengan kapasitas adsorpsi ada keadaan isoterm.
Gambar 4.6 Keadaan Isoterm Adsorpsi α-Tokoferol
Data pada keadaan isoterm kemudian diolah untuk mendapatkan model isoterm adsorpsi yang sesuai. Uji kesesuaian dengan model isoterm Langmuir dilakukan mengikuti Persamaan 2.1 yang telah dilinierisasi menjadi Persamaan 2.2. sedangkan untuk model isoterm Freundlich dengan menggunakan Persamaan 2.3 yang telah dilinierisasi menjadi Persamaan 2.4
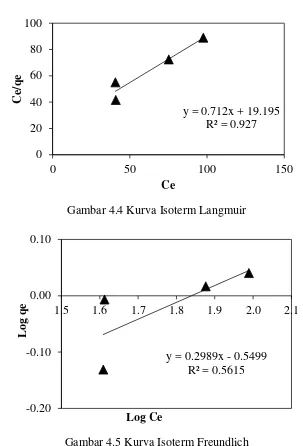
Uji kesesuaian data penelitian dengan model isoterm pada berbagai kecepatan ditunjukkan oleh Gambar 4.4 untuk model isoterm Langmuir dan Gambar 4.5 untuk model isoterm Freundlich
0 0.2 0.4 0.6 0.8 1 1.2
0 20 40 60 80 100 120
Qe (
m
g/g)
Gambar 4.4 Kurva Isoterm Langmuir
Gambar 4.5 Kurva Isoterm Freundlich
Dari persamaan linier yang diperoleh dilakukan perhitungan untuk memperoleh nilai dari konstanta masing-masing model adsorpsi. Parameter dari model isoterm Langmuir dan Freundlich yang ditentukan untuk proses penjerapan α -tokoferol disajikan dalam Tabel 4.3.
y = 0.712x + 19.195 R² = 0.927 0
20 40 60 80 100
0 50 100 150
Ce
/q
e
Ce
y = 0.2989x - 0.5499 R² = 0.5615
-0.20 -0.10 0.00 0.10
1.5 1.6 1.7 1.8 1.9 2.0 2.1
L
og q
e
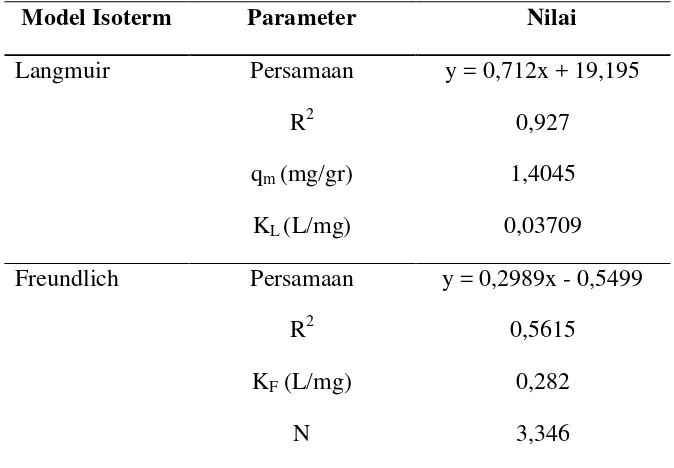
Tabel 4.3 Nilai Konstanta untuk Model Isoterm Langmuir dan Freundlich
Model Isoterm Parameter Nilai
Langmuir Persamaan
Persamaan isoterm Langmuir dan Freundlich merupakan persamaan isoterm yang paling sering digunakan dalam studi mengenai adsorpsi. Data hasil percobaan yang paling sesuai dengan persamaan digunakan untuk menentukan karakteristik dari kesetimbangan adsorpsi [39].
Penentuan model isoterm adsorpsi didasari oleh nilai R2 yang paling mendekati 1. Apabila nilai R2 semakin mendekati 1, menunjukkan bahwa semakin besar korelasi antara data percobaan dengan pemodelan isoterm tersebut. Berdasarkan data yang diperoleh pada Tabel 4.4, dapat dilihat bahwa pada percobaan adsorpsi α -tokoferol dengan karbon aktif dari ampas teh, model isoterm lebih condong kepada pemodelan Langmuir. Hal ini dapat dilihat dari nilai R2untuk model isoterm Langmuir yaitu sebesar 0,927, sedangkan untuk model Freundlich hanya diperoleh nilai R2 sebesar 0,5615.
Berdasarkan hasil percobaan, dapat diambil kesimpulan bahwa adsorpsi yang terjadi pada α-tokoferol memiliki energi adsorpsi yang sama untuk setiap situs aktif dari karbon aktif dari ampas teh. Adsorpsi yang terjadi pada karbon aktif dari ampas teh dengan α-tokoferol membentuk suatu sistem adsorpsi lapisan tunggal.
BAB V
KESIMPULAN DAN SARAN
5.1 KESIMPULAN
Kesimpulan yang dapat diambil dari penelitian yang telah dilakukan adalah: 1. Berdasarkan luas permukaan dan kadar abu, maka karakteristik karbon aktif
dari ampas teh telah sesuai dengan karakteristik karbon aktif secara umum 2. Persamaan model kinetika yang mewakili penjerapan α-tokoferol adalah
kinetika orde dua semu Lagergren dengan nilai R2 sebesar 0,9934.
3. Persamaan model isoterm yang mewakili penjerapan α-tokoferol adalah isoterm Langmuir dengan nilai R2 sebesar 0,927.
4. Kondisi operasi adsorpsi terbaik diperoleh pada kecepatan pengadukan 180 rpm.
5. Nilai persentase adsorpsi maksimum sebesar 84,42% diperoleh pada perbandingan karbon aktif : CPO (w/w) 1: 3 pada kecepatan pengadukan 180 rpm.
6. Nilai kapasitas adsorpsi maksimum sebesar 1,0973 mg/gram diperoleh pada perbandingan karbon aktif : CPO (w/w) 1: 6 pada kecepatan pengadukan 180 rpm.
5.2 SARAN
Saran yang dapat diberikan untuk penelitian selanjutnya adalah:
1. Melakukan variasi menggunakan pelarut yang sesuai untuk α-tokoferol sehingga mengurangi kompetisi antara α-tokoferol dengan komponen lain yang terkandung dalam CPO.
2. Menggunakan karbon aktif komersil untuk membandingkan kemampuan daya serap karbon aktif dari ampas teh dengan karbon aktif komersil tersebut dalam mengadsorpsi α-tokoferol dari CPO
3. Menggunakan larutan α-tokoferol murni untuk melihat kemampuan terbaik dari karbon aktif dari ampas teh dalam menjerap α-tokoferol.