BAB II
TINJAUAN PUSTAKA
2.1 Selada Romaine
2.1.1 Sistematika Tumbuhan
Menurut Pracaya (2002), sistematika tanaman selada romaine adalah sebagai berikut:
Kingdom : Plantae
Divisio : Spermatophyta Subdivisio : Angiospermae Class : Dicotyledonae Ordo : Asterales Famili : Compositae Genus : Lactuca
Species : Lactuca sativa L. Varietas : longifolia
2.1.2 Nama Lain
Selada romaine juga dikenal dengan berbagai nama lain. Di Indonesia selada ini dikenal dengan nama-nama berikut antara lain, selada kerucut, selada silindris, dan selada cos (Pracaya, 2002).
2.1.3 Morfologi Tumbuhan
tersusun bertumpang-tindih satu sama lain, tetapi tidak membentuk kepala (Rubatzky dan Yamaguchi, 1998).
2.1.4 Kegunaan dan Komposisi
Menurut Rubatzky dan Yamaguchi (1998), sebagai komponen sayuran salad utama, selada romaine memiliki kandungan air yang tinggi, sementara kandungan karbohidrat dan proteinnya rendah. Namun, karena volume yang dikonsumsi tiap tahunnya tinggi, selada dikenal kontribusi gizinya sebagai sumber mineral, vitamin A, vitamin C, dan serat. Selada tipe ini menghasilkan pro-vitamin A yang lebih banyak karena bagian daun hijaunya lebih besar ketimbang tipe lainnya.
2.2 Sistem Pertanian Organik dan Non-Organik
Pertanian yang mirip dengan kehidupan tumbuhan liar disebut pertanian organik karena kesuburan tanaman berasal dari bahan organik secara alamiah. Pengertian lain, pertanian organik adalah sistem pertanian (dalam hal bercocok tanam) yang tidak mempergunakan bahan kimia, tetapi menggunakan bahan organik. Bahan kimia tersebut dapat berupa pupuk, pestisida, hormon pertumbuhan, dan lain sebagainya (Pracaya, 2002).
Prinsip pertanian organik yaitu berteman akrab dengan lingkungan, tidak mencemarkan dan merusak lingkungan hidup. Cara yang ditempuh agar tujuan tersebut tercapai antara lain:
1) memupuk dengan kompos, pupuk kandang;
2) memupuk dengan pupuk hijau, seperti orok-orok, maupun batang, akar, dan daun kacang-kacangan, serta turi;
4) mempertahankan dan melestarikan habitat tanaman dengan pola tanam poilikultur (Pracaya, 2002).
Penggunaan bahan kimia terbesar untuk menyuburkan tanah dan memberantas hama serta penyakit. Dengan pertanian organik, kedua macam kegiatan tersebut dapat diatasi. Selain menggunakan pupuk kandang, tanaman yang termasuk famili Leguminosae, misalnya kacang-kacangan, mempunyai bintil akar yang dapat menambat nitrogen dari udara dan mengubahnya menjadi nitrogen yang dapat diserap oleh tanaman. Adapun pestisida yang digunakan untuk memberantas hama dan penyakit, dapat diganti dengan pestisida organik. Pestisida organik mudah dibuat, tidak mencemari udara, tidak berbahaya, tidak meracuni konsumen karena cepat terurai, dan tanamannya mudah diperoleh, serta dapat ditanam di kebun (Pracaya, 2002).
Pestisida organik terdiri dari pestisida botani (pestisida nabati) dan biopestisida. Pestisida botani berasal dari tumbuh-tumbuhan yang mana tumbuhan tersebut mengandung metabolit sekunder yang bersifat racun terhadap hama dan penyakit. Contoh tumbuhan yang merupakan pestisida botani antara lain bunga krisan yang mengandung zat piretrum dan piretrin, akar tuba yang mengandung rotenon, daun tembakau yang mengandung nikotin, serta daun mimba mengandung azadirachtin dan salanin. Semua tanaman tersebut bersifat insektisida (Novizan, 2002).
Sistem pertanian non-organik atau yang biasa disebut konvensional dalam pemeliharaannya menggunakan pupuk buatan pabrik, pestisida sintesis, perangsang tumbuh antibiotika, dan lain-lain yang meningkatkan produksi pangan. Dengan cara ini, produksi sangat meningkat, tetapi di sisi lain hadirnya produk-produk pabrik tersebut dapat mencemari lingkungan dan mengganggu kesehatan. Selain itu, sistem pertanian ini banyak tergantung pada bahan kimia yang harganya mahal. Ketergantungan ini dapat menyebabkan produksi merosot dan biaya produksi yang tinggi sehingga tidak sesuai dengan harga jual (Pracaya, 2002).
Menurut Pracaya (2002) dan Soenandar dan Tjachjono (2013), sistem pertanian organik mempunyai kelebihan dan kekurangan dibandingkan sistem pertanian non-organik. Kelebihan sistem pertanian organik, antara lain sebagai berikut:
1) tidak menggunakan pupuk maupun pestisida kimia sehingga tidak menimbulkan pencemaran lingkungan, baik pencemaran tanah, air, maupun udara, serta produknya tidak mengandung racun.
2) Tanaman organik mempunyai rasa yang lebih manis dibandingkan tanaman non-organik.
3) Produk tanaman organik lebih mahal.
4) Kandungan zat antioksidannya lebih banyak.
5) Kandungan vitamin C dan serat lebih banyak, khususnya pada sayuran dan buah.
6) seratus persen tidak mengandung residu yang beracun.
Kekurangan sistem pertanian organik, antara lain sebagai berikut:
penyakit. Apabila menggunakan pestisida alami, perlu dibuat sendiri karena pestisida ini belum ada di pasaran.
2) Frekuensi pemberian pestisida alami harus lebih sering karena pestisida alami cepat terurai.
3) Ukuran tanaman organik biasanya lebih kecil dibandingkan tanaman non-organik.
2.3 Mineral
Mineral berasal dari dalam tanah. Tanaman yang ditanam di atas tanah akan menyerap mineral yang dibutuhkan untuk pertumbuhan dan kemudian disimpan dalam akar, batang, daun, bunga, dan buah (Achadi, 2007). Pada umumnya mineral merupakan bagian dari tubuh dan memegang peranan penting dalam pemeliharaan fungsi tubuh, baik pada tingkat sel, jaringan, organ maupun fungsi tubuh secara keseluruhan (Almatsier, 2001). Mineral merupakan unsur esensial bagi fungsi normal sebagian enzim dan sangat penting dalam pengendalian komposisi cairan tubuh. Tubuh tidak mampu mensintesa mineral sehingga unsur-unsur ini harus disediakan lewat makanan (Budiyanto, 2001).
2.3.1 Kalsium
Kalsium merupakan mineral yang paling banyak terdapat di dalam tubuh, yaitu 1,5 – 2% dari berat badan orang dewasa. Dari jumlah ini, 99% berada di dalam jaringan keras, yaitu tulang dan gigi. Di dalam cairan ekstraseluler dan intraseluler kalsium memegang peranan penting dalam mengatur fungsi sel, seperti untuk transmisi saraf, kontraksi otot, penggumpalan darah dan menjaga permeabilitas membran sel. Kalsium mengatur pekerjaan hormon-hormon dan faktor pertumbuhan (Almatsier, 2009).
Konsumsi kalsium hendaknya tidak melebihi 2500 mg sehari karena kelebihan kalsium dapat menimbulkan gangguan ginjal. Di samping itu, dapat menyebabkan konstipasi. Kelebihan kalsium bisa terjadi bila menggunakan suplemen kalsium. Kekurangan kalsium pada masa pertumbuhan dapat menyebabkan gangguan pertumbuhan, seperti tulang kurang kuat, mudah bengkok dan rapuh. Pada orang dewasa kehilangan kalsium menyebabkan tulang menjadi rapuh dan mudah patah yang disebut osteoporosis (Almatsier, 2009).
Sumber utama kalsium adalah susu dan hasil susu, seperti keju, serelia, kacang-kacangan dan hasil kacang-kacangan, tahu dan tempe, dan sayuran hijau (Almatsier, 2009).
2.3.2 Kalium
dalam transmisi saraf dan relaksasi otot. Di dalam sel, kalium berfungsi sebagai katalisator dalam banyak reaksi biologik, terutama dalam metabolisme energi dan sintesis glikogen dan protein. Kalium berperan dalam pertumbuhan sel. Tekanan darah normal memerlukan perbandingan antara natrium dan kalium yang sesuai di dalam tubuh. Kebutuhan minimum akan kalium ditaksir sebanyak 2000 mg sehari (Almatsier, 2009).
Kelebihan kalium akut dapat menyebabkan gagal jantung yang berakibat kematian. Kelebihan kalium juga dapat terjadi bila ada gangguan fungsi ginjal. Kekurangan mineral ini menyebabkan lemah, lesu, kehilangan nafsu makan, kelumpuhan, mengigau, dan konstipasi. Jantung akan berdebar detaknya dan menurunkan kemampuannya untuk memompa darah (Almatsier, 2009).
Kalium terdapat di dalam semua makanan yang berasal dari tumbuh-tumbuhan dan hewan. Sumber utama adalah makanan segar, terutama buah, sayuran, dan kacang-kacangan (Almatsier, 2009).
2.3.3 Magnesium
merangsang kontraksi otot, sedangkan magnesium mengendorkan otot. Kalsium mendorong penggumpalan darah sedangkan magnesium mencegah. Kalsium menyebabkan ketegangan saraf, sedangkan magnesium melemaskan saraf. Magnesium juga mencegah kerusakan gigi dengan cara menahan kalsium di dalam email gigi (Almatsier, 2009).
Akibat kelebihan magnesium belum diketahui dengan pasti. Kelebihan magnesium biasanya terjadi pada penyakit gagal ginjal. Kekurangan magnesium berat menyebabkan kurang nafsu makan, gangguan dalam pertumbuhan, gugup, kejang, gangguan sistem saraf pusat, halusinasi, koma, dan gagal jantung (Almatsier, 2009).
Sumber utama magnesium adalah sayuran hijau, serelia tumbuk, biji-bijian dan kacang-kacangan. Daging, susu, dan hasilnya serta cokelat juga merupakan sumber magnesium yang baik (Almatsier, 2009).
2.3.4 Natrium
Natrium adalah kation utama dalam cairan ekstraselular. 35-40% natrium ada di dalam kerangka tubuh. Sebagai kation utama dalam cairan ekstraselular, natrium menjaga keseimbangan cairan dalam kompartemen tersebut. Secara normal tubuh dapat menjaga keseimbangan antara natrium di luar sel dan kalium di dalam sel. Natrium menjaga keseimbangan asam basa di dalam tubuh dengan mengimbangi zat-zat yang membentuk asam. Natrium berperan dalam transmisi saraf dan kontraksi otot. Natrium berperan pula dalam absorpsi glukosa dan sebagai alat angkut zat-zat gizi lain melalui membran, terutama melalui dinding usus sebagai pompa natrium. Taksiran kebutuhan sehari untuk orang dewasa adalah sebanyak 500 mg (Almatsier, 2009).
akut menyebabkan edema dan hipertensi. Kelebihan konsumsi natrium dapat menimbulkan hipertensi. Kekurangan natrium menyebabkan kejang, apatis, dan kehilangan nafsu makan. Bila kadar natrium darah turun, perlu diberikan natrium dan air untuk mengembalikan keseimbangan (Almatsier, 2009).
Sumber utama natrium adalah garam dapur atau NaCl, mono sodium glutamat, kecap dan makanan yang diawetkan dengan garam dapur. Sementara buah dan sayuran hanya mengandung sedikit natrium (Almatsier, 2009).
2.4 Spektrofotometri Serapan Atom
Peristiwa serapan atom pertama kali diamati oleh Fraunhofer, ketika menelaah garis-garis hitam pada spektrum matahari. Sedangkan yang memanfaatkan prinsip serapan atom itu sendiri pada bidang analisis adalah seorang Australia bernama Alan Walsh di tahun 1955 (Khopkar, 1985). Spektrofotometri serapan atom digunakan untuk analisis kuantitatif unsur-unsur logam dalam jumlah sekelumit (trace) dan sangat sekelumit (ultratrace). Cara ini cocok untuk analisis kelumit logam karena mempunyai kepekaan yang tinggi (batas deteksi kurang dari 1 ppm), pelaksanaannya relatif sederhana, dan interferensinya sedikit. Spektrofotometri serapan atom didasarkan pada penyerapan energi sinar oleh atom-atom netral, dan sinar yang diserap biasanya sinar tampak atau ultraviolet (Gandjar dan Rohman, 2008).
Metode Spektrofotometri serapan atom (SSA) mendasarkan pada prinsip absorpsi cahaya oleh atom. Atom-atom akan menyerap cahaya pada panjang gelombang tertentu, tergantung pada sifat unsurnya. Cahaya pada panjang gelombang tersebut mempunyai cukup energi untuk mengubah tingkat elektronik suatu atom yang mana transisi elektronik suatu atom bersifat spesifik. Dengan menyerap suatu energi, maka atom akan memperoleh energi sehingga suatu atom pada keadaan dasar dapat ditingkatkan energinya ke tingkat eksitasi (Gandjar dan Rohman, 2008).
2.4.1 Instrumentasi Spektrofotometri Serapan Atom
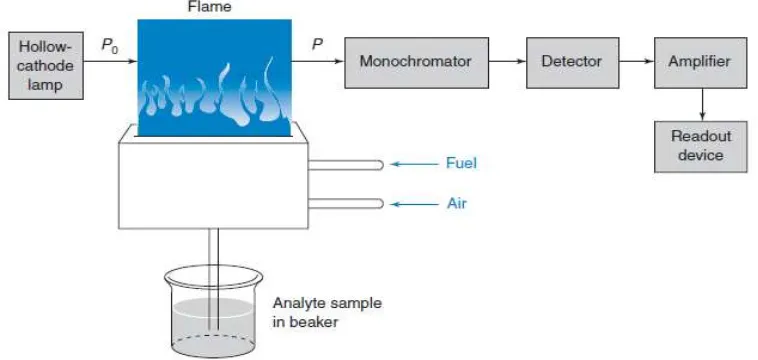
Instrumen spektrofotometer serapan atom dapat dilihat pada gambar berikut ini:
Gambar 2.1 Instrumen spektrofotometer serapan atom (Harris, 1982)
2.4.1.1 Sumber Sinar
2.4.1.2 Tempat Sampel
Dalam analisis dengan spektrofotometri serapan atom, sampel yang akan dianalisis harus diuraikan menjadi atom-atom netral yang masih dalam keadaan asas. Ada berbagai macam alat yang dapat digunakan untuk mengubah suatu sampel menjadi uap atom-atom yaitu: dengan nyala (flame) dan dengan tanpa nyala (flameless) (Gandjar dan Rohman, 2008).
a. Nyala (Flame)
Nyala digunakan untuk mengubah sampel yang berupa cairan menjadi bentuk uap atomnya dan untuk proses atomisasi. Suhu yang dapat dicapai oleh nyala tergantung pada gas yang digunakan, misalnya untuk gas asetilen-udara suhunya sebesar 2200oC. Sumber nyala yang paling banyak digunakan adalah campuran asetilen sebagai bahan pembakar dan udara sebagai pengoksidasi (Gandjar dan Rohman, 2008). Temperatur nyala dengan berbagai kombinasi bahan bakar dan oksidan dapat dilihat pada tabel berikut.
Tabel 2.1 Temperatur Nyala dengan berbagai kombinasi bahan bakar dan oksidan (Khopkar, 1985)
Bahan Bakar Oksidan Udara Oksidan Oksigen N2O
Hidrogen b. Tanpa Nyala (Flameless)
netral dan pada fraksi atom ini dilewatkan suatu sinar yang berasal dari lampu katoda berongga sehingga terjadilah proses penyerapan energi sinar yang memenuhi kaidah analisis kuantitatif (Gandjar dan Rohman, 2008).
2.4.1.3 Monokromator
Monokromator merupakan alat untuk memisahkan dan memilih panjang gelombang yang digunakan dalam analisis dari sekian banyak panjang gelombang yang dihasilkan lampu katoda berongga (Gandjar dan Rohman, 2008).
2.4.1.4 Detektor
Detektor digunakan untuk mengukur intensitas cahaya yang melalui tempat pengatoman (Gandjar dan Rohman, 2008).
2.4.1.5 Readout
Readout merupakan alat pencatat hasil. Hasil pembacaan dapat berupa angka atau berupa kurva dari suatu recorder yang menggambarkan absorbansi atau intensitas emisi (Gandjar dan Rohman, 2008).
2.4.2 Gangguan-gangguan pada Spektrofotometri Serapan Atom
Yang dimaksud dengan gangguan-gangguan (interference) pada spektrofotometri serapan atom adalah peristiwa-peristiwa yang menyebabkan pembacaan absorbansi unsur yang dianalisis menjadi lebih kecil atau lebih besar dari nilai yang sesuai dengan konsentrasinya dalam sampel (Gandjar dan Rohman, 2007).
Menurut Gandjar dan Rohman (2007), gangguan-gangguan yang dapat terjadi dalam spektrofotometri serapan atom adalah sebagai berikut:
A. Gangguan yang berasal dari matriks sampel yang mana dapat mempengaruhi banyaknya sampel yang mencapai nyala.
terjadi di dalam nyala.
C. Gangguan oleh absorbansi yang disebabkan bukan oleh absorbansi atom yang dianalisis; yakni absorbansi oleh molekul-molekul yang tidak terdisosiasi di dalam nyala. Adanya gangguan-gangguan di atas dapat diatasi dengan menggunakan cara-cara sebagai berikut:
a. Penggunaan nyala/suhu atomisasi yang lebih tinggi b. Penambahan senyawa penyangga
c. Pengekstrasian unsur yang dianalisis d. Pengekstrasian ion atau gugus pengganggu
D. Gangguan oleh penyerapan non-atomik. Gangguan jenis ini berarti terjadinya penyerapan cahaya dari sumber sinar yang bukan berasal dari atom-atom yang akan dianalisis.
2.5 Validasi Metode
Menurut Harmita (2004), validasi metode analisis adalah suatu tindakan penilaian terhadap parameter tertentu, berdasarkan percobaan laboratorium, untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya.
Beberapa parameter analisis yang harus dipertimbangkan dalam validasi metode analisis adalah sebagai berikut:
A. Kecermatan (Accuracy)
Kecermatan adalah ukuran yang menunjukkan derajat kedekatan hasil analisis dengan kadar analit sebenarnya. Kecermatan dinyatakan sebagai persen perolehan kembali (recovery) analit yang ditambahkan.
B. Keseksamaan (Precision)
hasil uji individual, diukur melalui penyebaran hasil dari rata-rata jika prosedur diterapkan secara berulang pada sampel-sampel yang diambil dari campuran yang homogen.
C. Selektivitas (Spesifisitas)
Selektivitas atau spesifisitas suatu metode adalah kemampuannya yang hanya mengukur zat tertentu secara cermat dan seksama dengan adanya komponen lain yang mungkin ada di dalam matriks sampel.
D. Linearitas dan Rentang
Linearitas adalah kemampuan metode analisis yang memberikan respon baik secara langsung maupun dengan bantuan transformasi matematik yang baik, proposional terhadap konsentrasi analit dalam sampel. Rentang metode adalah batas terendah dan batas tertinggi analit yang dapat ditetapkan secara cermat seksama dan dalam linearitas yang dapat diterima.
E. Batas Deteksi dan Batas Kuantitasi