BAB 2
TINJAUAN PUSTAKA
2.1 Sumber Air
Air yang keluar dari perut bumi pada umumnya merupakan air asin panas yang
disebut “Brine”. Air yang terproduksi ini banyak mengandung mineral - mineral yang dapat
menyebabkan kerak dan korosi. Terbentuknya kerak disebabkan adanya senyawa – senyawa
dalam air dengan jumlah yang melebihi kelarutannya pada keadaan kesetimbangan. Salah
satu senyawa tersebut antara lain adalah kalsium karbonat, yang memberikan konstribursi
terbesar dalam proses terjadinya kerak dan korosi. (Effendi,H.2003)
Adapun didaratan, proses presipitasi lebih banyak terjadi dibandingkan dengan
evaporasi, transpirasi dan sublimasi. Akibatnya, secara total terjadi aliran air dari atmosfer
menuju daratan dalam bentuk hujan dan salju. Di daratan, sebagian air membeku menjadi es
(puncak gunung yang tinggi), sebagian air masuk tanah (infiltrasi), dan sebagian lainnya
mengalir di permukaan membenrtuk sungai menuju laut kembali.
Air yang digunakan untuk keperluan sehari – hari bersifat tawar sehingga dikenal
dengan istilah air tawar. Akan tetapi, hanya 3% air yang ada di bumi ini berupa air tawar dan
dua pertiganya membeku di kutub dan puncak gunung yang tinggi. Sisanya merupakan air
tanah dan 0,3% adalah air permukaan (sungai, danau, dan rawa).Tidak semua air tawar dapat
langsung digunakan untuk kegiatan sehari – hari. Pemerintah telah menerapkan standar
Air yang diperlukan dalam dunia industri dapat diambil dari setiap titik dalam siklus
hidrologis, tergantung teknologi yang dimiliki dan biaya yang tersedia untuk pengambilan
dan untuk memperbaiki kualitasnya sehingga sesuai untuk penggunaannya.
Sumber – sumber air :
1. Air Hujan
2. Air Permukaan
3. Air Tanah
Ditinjau dari sudut kualitasnya, secara singkat diuraikan sebagai berikut :
2.1.1 Air Hujan
Dalam lintasan jatuhnya air hujan mengabsorpsi gas-gas dan uap-uap yang terdapat
di udara, terutama oksigen, nitrogen dan karbon dioksida, yang merupakan
komponen-komponen utama dari udara.
Air hujan mempunyai sifat agresif terutama terhadap pipa-pipa penyalur maupun
bak-bak penampungan air, sehingga hal ini akan mempercepat terjadinya korosi, dan air
hujan juga bersifat lunak, sehingga boros terhadap pemakaian sabun. Maka untuk
menjadikan air hujan sebagai air minum hendaknya pada waktu mulai turun dibiarkan dan
Air hujan yang jatuh ke bumi dan menjadi air permukaan memiliki kadar
bahan-bahan terlarut atau unsur hara yang sangat sedikit. Air hujan biasanya bersifat asam, dengan
nilai pH sekitar 4,2. Hal ini disebabkan air hujan melarutkan gas-gas yang terdapat di
atmosfer, misalnya gas karbon dioksida (CO2), sulfur (S), dan nitrogen oksida (NO2) yang
dapat membentuk asam lemah. Setelah jatuh ke permukaan bumi, air hujan mengalami
kontak dengan tanah dan melarutkan bahan-bahan yang terkandung di dalam tanah.
2.1.2 Air Permukaan
Air permukaan adalah air yang berada di sungai, danau, waduk, rawa, dan badan air
lain, yang tidak mengalami infiltrasi ke bawah tanah. Areal tanah yang mengalirkan air ke
suatu badan air disebut watersheds atau drainage basins.
Air permukaan yang mencakup : air sungai, air danau, air kolam dapat merupakan
kumpulan air hujan yang jatuh dan mengalir diatas permukaan tanah atau campuran antara
lain aliran permukaan dan air tanah ataupun air yang mengalir ke luar pada musim kemarau.
Air yang mengalir dari daratan menuju suatu badan air disebut limpasan permukaan
(surface run off), dan air yang mengalir di sungai menuju laut disebut aliran air sungai (river
run off). Sekitar 69% air yang masuk ke sungai berasal dari hujan, pencairan es/salju
(terutama untuk wilayah ugahari), dan sisanya berasal dari air tanah.
Secara alamiah, sungai, danau, kolam dapat tercemar pada daerah permukaan air
saja. Pada sungai yang besar dan arus air yang deras,sejumlah kecil bahaya pencemar akan
mengalami pengenceran sehingga tingkat pencemaran menjadi sangat rendah. Di Indonesia
air permukaan ini banyak digunakan sebagai sumber air minum tetapi harus diolah terlebih
2.1.3 Air Tanah
Air Tanah merupakan air yang berada di bawah permukaan tanah. Air tanah
ditemukan pada akifer. Pergerakan air tanah sangat lambat, kecepatan arus berkisar antara
10-10 – 10-3 m/detik dan dipengaruhi oleh porositas, permeabilitas dari lapisan tanah, dan
pengisian kembali air (recharge).
Air tanah umumnya mengandung garam terlarut. Jenis dan kadar
garam-garam terlarut yang tergantung dalam air tanah adalah tergantung pada kondisi tanah dalam
lintasan aliran air tanah. Umumnya kadar konstituen terlarut dalam air tanah adalah lebih
tinggi jika dibandingkan dengan kadarnya pada air permukaan, disebabkan oleh lebih
lamanya periode kontak antara air dan zat-zat yang dapat larut yang berada dalam lapisan
tanah.
Konsentrasi utama yang terdapat dalam air tanah adalah :
- Kation : Ca2+, Mg2+
- Anion : CO32- , HCO3-, Cl- dan NO3
-Konstituen-konstituen yang dapat dijumpai dalam kadar yang relative rendah atau sangat
rendah adalah : Fe2+, Mn2+, Al3+, F-.
Disamping itu, air tanah mengadsorpsi pula gas-gas hasil penguraian dan zat-zat
anorganik. Gas-gas tersebut dapat berupa CO2, H2S dan NH4. Air tanah yang mengalir
melalui daerah yang kaya akan zat organik yang sifatnya dapat terurai, dapat kehilangan
kandungan oksigen terlarutnya. Oksigen tersebut digunakan oleh mikroorganisme dalam
Diantara sumber-sumber air yang ditinjau tersebut, air permukaan dan air tanah
merupakan sumber-sumber air yang paling luas penggunaannya sebagai sumber air untuk
berbagai keperluan, keperluan industri maupun keperluan konsumsi domestik. Mata air juga
merupakan bagian dari air tanah. Mata air adalah air tanah yang keluar dengan sendirinya
kepermukaan tanah. Mata air ini hampir tidak terpengaruh oleh musim dan kualitasnya sama
dengan keadaan air pada bagian dalamnya.
Karakteristik utama yang membedakan air tanah dan air permukaan adalah
pergerakan yang sangat lambat dan waktu tinggal (residence time) yang sangat lama, dapat
mencapai puluhan bahkan ratusan tahun. Karena pergerakan yang sangat lambat dan waktu
tinggal yang lama tersebut, air tanah akan sulit untuk pulih kembali jika mengalami
pencemaran.
Air tanah banyak mengandung ion Kalsium (Ca) dan Magnesium (Mg) yang
menyebabkan air bersifat sadah. Air tanah ini juga membawa dan melarutkan berbagai
mineral apalagi karena sifatnya yang asam (CO2 terlarut). Air tersebut memiliki kemampuan
membentuk padatan kalsium karbonat. Bila keasaman hilang, air akan bersifat sadah
(sementara). Penggunaan air tanah cenderung membentuk kerak pada ketel. Walau tak
menimbulkan korosi, air tanah sering banyak mengandung besi dan mangan.
(Effendi,H.2003)
Daerah dibawah tanah yang terisi air disebut daerah saturasi (zone of saturation).
Pada daerah saturasi, setiap pori tanah dan batuan terisi oleh air, yang merupakan air tanah
saturasi/jenuh (unsaturated/vadose zone) yang masih mampu menyerap air.
(Effendi,H.2003)
Tabel 2.1 Karakteristik Fisika dan Kimia Tanah dengan Tekstur yang Berbeda
Tekstur Tanah
Kualitas air diatur oleh pemerintah dalam beberapa peraturan, yakni Peraturan
Pemerintah Republik Indonesia Nomor 20 Tahun 1990 tentang Pengendalian Pencemaran
Air, Peraturan Pemerintah Republik Indonesia Nomor 82 Tahun 2001 tentang Pengelolaan
Kualitas Air dan Pengendalian Pencemaran Air,Peraturan Menteri Kesehatan Republik
Indonesia nomor 416/Menkes/Per/IX/1990 tentang syarat-syarat dan Pengawasan Kualitas
Air, serta Keputusan Menteri Kesehatan Republik Indonesia Nomor
907/Menkes/Sk/VII/2002 tentang syarat-syarat dan Pengawasan Kualitas Air Minum.
Dalam Peraturan Pemerintah Republik Indonesia Nomor 20 Tahun 1990 tentang
Pengendalian Pencemaran Air, air menurut peruntukannya digolongkan menjadi empat
golongan, yakni A, B, C, dan D, golongan – golongan air tersebut dapat di uraikan sebagai
1. Golongan A
Air yang dapat digunakan sebagai air minum secara langsung tanpa pengolahan
terlebih dahulu.
2. Golongan B
Air yang dapat digunakan sebagai air baku air minum.
3. Golongan C
Air yang dapat digunakan untuk keperluan perikanan dan peternakan.
4. Golongan D
Air yang dapat digunakan untuk keperluan pertanian dan dapat dimanfaatkan untuk
usaha perkotaan, industri, pembangkit listrik tenaga air.
Menurut Peraturan Pemerintah Republik Indonesia Nomor 82 Tahun 2001 tentang
Pengelolaan Kualitas Air dan Pengendalian Pencemaran Air, Klassifikasi mutu air
ditetapkan menjadi 4 (empat) kelas. Berikut diuraikan kelas-kelas air tersebut :
1. Kelas Satu
Air yang peruntukannya dapat digunakan untuk air baku air minum, dan atau
2. Kelas Dua
Air yang peruntukannya dapat digunakan untuk prasarana/sarana rekreasi air,
pembudidayaan ikan air tawar, peternakan, air untuk mengairi pertanaman, dan atau
peruntukkan lain yang mempersyaratkan mutu air yang sama dengan kegunaan tersebut.
3. Kelas Tiga
Air yang peruntukannya dapat digunakan untuk pembudidayaan ikan air tawar,
peternakan, air untuk mengairi pertanaman, dan atau peruntukan lain yang mempersyaratkan
air yang sama dengan kegunaan tersebut.
4. Kelas Empat
Air yang peruntukannya dapat digunakan untuk mengairi pertanaman dan atau
peruntukan lain yang mempersyaratkan mutu air yang sama dengan kegunaan tersebut.
(Rahayu,I.2007)
2.3 Pencemaran Air
Pencemaran air adalah masuknya atau dimasukkannya mahluk hidup, zat, energi atau
komponen lain kedalam air atau berubahnya tatanan air oleh kegiatan manusia atau oleh
proses alam, sehingga kualitas air menurun sampai ke tingkat tertentu yang menyebabkan air
berkurang atau tidak dapat berfungsi lagi sesuai kegunaannya.
Air merupakan substrat yang paling parah akibat pencemaran. Berbagai jenis
a. Sumber domestik (rumah tangga), perkampungan, kota, pasar, jalan, dan sebagainya.
b. Sumber non-domestik seperti pabrik, pertanian, peternakan, perikanan serta
sumber-sumber lainnya.
Secara langsung ataupun tidak langsung pencemaran tersebut akan berpengaruh terhadap
kualitas air, baik untuk keperluan air minum, air industri ataupun keperluan lainnya.
Berbagai cara dan usaha telah banyak dilakukan agar pencemaran terhadap air dapat
dihindari, dikurangi atau minimal dapat dikendalikan. (Fardias,S.1992)
Dewasa ini air menjadi masalah yang perlu mendapat perhatian yang seksama dan
cermat. Untuk mendapatkan air yang baik, sesuai dengan standar tertentu, saat ini menjadi
barang yang mahal karena air sudah banyak tercemar oleh bermacam-macam limbah dari
hasil kegiatan manusia, baik limbah dari kegiatan rumah tangga, limbah dari kegiatan
industri dan kegiatan-kegiatan lainnya.
Walaupun penetapan standar air yang bersih tidak mudah, namun ada kesepakatan
bahwa air yang bersih tidak ditetapkan pada kemurnian air akan tetapi didasarkan pada
keadaan normalnya. Apabila terjadi penyimpangan dari keadaan normal maka hal itu berarti
air tersebut telah mengalami pencemaran. Air dari mata air di pegunungan, apabila lokasi
pengambilannya lain, akan menghasilkan keadaan normal yang lain pula.
(Wardhana,W.A.1995)
Masalah pencemaran serta efisiensi penggunaan sumber air, merupakan pokok
persoalan yang paling banyak dibahas. Hal ini mengingat keadaan perairan alami dibanyak
Negara yang cenderung semakin menyusut dan menurun. Baik kualitas maupun
dilanda krisis air seperti halnya krisis pangan, energi dan sebagainya. Bahkan untuk
beberapa Negara masalah kekurangan air sudah terjadi sejak lama.
Beberapa pokok-pokok yang ditekankan pada pengertian Pencemaran Air meliputi
dasar-dasar sebagai berikut :
1. Air pada suatu “badan air” dikatakan mengalami pencemaran, bila pembebasan
akan bahan-bahan buangan (kontaminan) sampai pada suatu tingkat/keadaan
tertentu dapat membahayakan fungsi air dari badan air tersebut.
2. Bahwa masing-masing fungsi air dalam badan-badan air memiliki suatu “standar
kualitas” yang perlu ditentukan terlebih dahulu sebagai batasan sebelum dapat
dilakukan suatu penilaian apakah suatu pencemaran pada suatu badan air itu terjadi
atau tidak. Jelasnya, masing-masing badan air sesuai dengan fungsinya mempunyai
standar kualitas sendiri-sendiri.
3. Masing-masing standar tersebut diatas masih perlu ditentukan pula secara lokal,
nasional, atau internasional. Dasar-dasar pertimbangan yang digunakan untuk
penentuan standar tersebut bermacam-macam, tergantung pada dominasi sasaran
yang akan dilindungi.
Karena air memiliki jaringan aliran yang luas (hydrological cycle), maka air yang
berada disuatu tempat baik mengalir maupun menetap (relatif) pada permukaan tanah
disebut “Badan Air”. Yang termasuk dalam klassifikasi badan air adalah sungai, waduk,
2.4 Teori Kesadahan
2.4.1 Pengertian Kesadahan
Kesadahan merupakan sifat air yang disebabkan oleh adanya ion-ion atau kation
logam valensi dua. Kation-kation penyebab utama dari kesadahan adalah Ca2+, Mg2+, Sr2+,
Fe2+ dan Mn2+, sedangkan anion-anionnya yang terdapat dalam air adalah HCO3-, SO42-, Cl-,
NO3-. (Sutrisno,C.T.1996)
Air sadah mengakibatkan konsumsi sabun lebih tinggi, karena adanya hubungan
kimiawi antara ion kesadahan dengan molekul sabun menyebabkan sifat detergen sabun
hilang. Kelebihan ion Ca2+ serta ion CO32- (salah satu ion alkaliniti) mengakibatkan
terbentuknya kerak pada dinding pipa yang disebabkan oleh endapan kalsium karbonat
CaCO3. Kerak ini akan mengurangi penampang basah pipa dan menyulitkan pemanasan air
dalam ketel. (Allaerts,G.1987)
Air sadah umumnya digambarkan sebagai reaksi air terhadap sabun untuk
menghasilkan busa atau kemampuan menimbulkan kerak pada pipa air panas, boiler, dan
peralatan logam lainnya.
Kesadahan air sangat penting sehubungan dengan berbagai penggunaan air, karena
kecenderungan membentuk kerak. Air yang kesadahannya amat rendah, dengan sedikit
sabun saja telah berbuih banyak, tetapi jika terdapat kesadahan air tinggi, dapat
menyebabkan pemborosan sabun. Kesadahan air harus optimum, karena apabila terlalu
tinggi akan menimbulkan kerak, dan apabila terlalu rendah menyebabkan korosi pada suhu
Kesadahan air bervariasi dari satu tempat dengan tempat lain. Umumnya, air
permukaan lebih sadah dari pada air tanah. Kesadahan air bergantung pada formasi geologi
alami dengan apa air tersebut mengalami kontak. Air yang sadah ditemukan di Negara
Inggris, Atlantik Selatan, Bagian Utara Pasifik, Lowa, India, Arizona, Meksiko adalah
Negara yang memiliki kesadahan air cukup tinggi. (Sawyer and Mc Carty.1998)
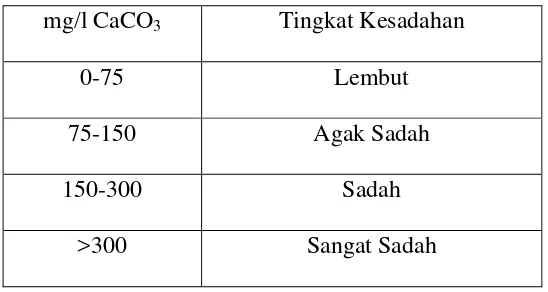
Tabel 2.4 Klassifikasi air dengan tingkat kesadahannya
mg/l CaCO3 Tingkat Kesadahan
0-75 Lembut
75-150 Agak Sadah
150-300 Sadah
>300 Sangat Sadah
Sumber : Fardias,S.1992
2.4.2 Penyebab Kesadahan
Kesadahan disebabkan kation logam divalent. Dengan kata lain kemampuan ion
untuk bereaksi dengan sabun untuk menimbulkan endapan dan tentunya dengan kehadiran
anion dalam air untuk membentuk kerak. Dalam prinsipnya kesadahan disebabkan kation
antara lain, Ca2+, Mg2+, Sr2+, Fe2+, dan Mn2+.
Kesadahan air juga disebabkan kontak dengan tanah dan formasi bebatuan. Air hujan
sebenarnya tidak memiliki kemampuan untuk melarutkan ion-ion penyusun kesadahan yang
banyak terikat di dalam tanah dan batuan kapur, meskipun memiliki kadar karbon dioksida
lebih banyak disebabkan oleh aktivitas bakteri didalam tanah, yang banyak mengeluarkan
karbon dioksida.
Keberadaan karbon dioksida membentuk kesetimbangan dengan asam karbonat.
Pada kondisi yang relatif asam, senyawa-senyawa karbonat yang terdapat di dalam tanah
dan batuan kapur yang sebelumnya tidak larut berubah menjadi senyawa bikarbonat yang
bersifat larut. Batuan kapur pada dasarnya tidak hanya mengandung karbonat, tetapi juga
mengandung sulfat, klorida dan silikat. Ion-ion ini juga ikut terlarut dalam air.
2.4.3 Klassifikasi Kesadahan
Klassifikasi kesadahan berdasarkan dua cara, yaitu berdasarkan ion logam dan
berdasarkan anion yang berasosiasi dengan ion logam. Berdasarkan ion logam, kesadahan
dibedakan menjadi kesadahan kalsium dan kesadahan magnesium.Berdasarkan anion yang
berasosiasi dengan ion logam, kesadahan dibedakan menjadi kesadahan karbonat dan
kesadahan non-karbonat.
2.4.3.1 Kesadahan Kalsium dan Magnesium
Kesadahan perairan dikelompokkan menjadi kesadahan kalsium dan kesadahan
magnesium karena pada perairan alami kesadahan banyak disebabkan oleh kation kalsium
dan magnesium. Kesadahan kalsium dan magnesium sering kali perlu diketahui untuk
menentukan jumlah kapur dan soda abu yang dibutuhkan dalam proses pelunakan
air(lime-soda ash softening). Jika nilai kesadahan kalsium diketahui maka kesadahan magnesium
dapat ditentukan melalui persamaan. ( Cole,G.A.1998 )
Pada penentuan nilai kesadahan baik kesadahan total, kesadahan kalsium maupun
kesadahan magnesium, keberadaan besi dan mangan dianggap sebagai pengganggu karena
dapat bereaksi dengan pereaksi yang digunakan. Oleh karena itu, kesadahan kalsium
dianggap lebih besar dari kadar ion kalsium, dan sebaliknya. Untuk mendapatkan kadar ion
kalsium dan ion magnesium dari nilai kesadahan, digunakan persamaan :
Kadar Ca2+ (mg/liter) = 0,4 x kesadahan kalsium
Kadar Mg2+ (mg/liter) = 0,243 x kesadahan magnesium
( Effendi,H.2003)
2.4.3.2 Kesadahan Karbonat dan Non-karbonat
Pada kesadahan karbonat, kalsium dan magnesium berasosiasi dengan ion CO32- dan
HCO3-. Pada kesadahan non-karbonat, kalsium dan magnesium berasosiasi dengan ion SO4
2-, Cl-, dan NO3-. Kesadahan karbonat sangat sensitif terhadap panas dan mengendap dengan
mudah pada suhu tinggi. Seperti reaksi berikut ini :
Ca(HCO3)2→ CaCO3 endapan + CO2 + H2O
Mg(HCO3)2 → Mg(OH)2 endapan + 2CO2
Oleh karena itu, kesadahan karbonat disebut juga kesadahan sementara. Kesadahan
non-karbonat disebut kesadahan permanen karena kalsium dan magnesium yang berikatan
dengan sulfat dan klorida tidak mengendap dan nilai kesadahan tidak berubah meskipun
Bagian dari total kesadahan yaitu ekuivalen dengan bikarbonat yang berperan serta
dalam kehadiran alkalinitas karbonat sesuai dengan kesadahan karbonat. Sejak alkalinitas
dan kesadahan ditentukan dalam CaCO3, kesadahan karbonat dapat dihitung berdasarkan :
Apabila alkalinitas total < kesadahan total : Maka kesadahan karbonat = alkalinitas total.
Apabila alkalinitas total ≥ kesadahan total : Maka kesadahan karbonat = kesadahan total.
Kesadahan non karbonat = kesadahan total – kesadahan karbonat.(Sawyer and Mc
Carty.1998)
Jika alkalinitas total melebihi kesadahan total maka sebagian dari anion penyusun
alkalinitas (bikarbonat dan karbonat) berasosiasi dengan kation valensi satu (monovalent),
misalnya kalium (K+) dan Natrium (Na+) yang tidak terdeteksi pada penentuan kesadahan.
Sebaliknya, jika kesadahan total melebihi alkalinitas total maka sebagian dari kation
penyusun kesadahan (kalsium dan magnesium) berikatan dengan sulfat (SO42-), klorida (Cl
-), silikat (SiO32-) atau nitrat (NO3-) yang tidak terdeteksi pada penentuan alkalinitas. Oleh
karena itu hubungan antara kesadahan dan alkalinitas tidak selalu positif atau semakin besar
kesadahan tidak selalu disertai dengan semakin tingginya alkalinitas dan sebaliknya. (
Effendi,H.2003)
2.5 Metode Penentuan Kesadahan
Kesadahan biasanya dinyatakan sebagai CaCO3. Beberapa metode telah digunakan
2.5.1 MetodeTotal
Metode ini menghitung kesadahan berdasarkan konsentrasi ion-ion divalen dalam air,
diantaranya Ca2+, Mg2+, dan Sr2+.
Perhitungan kesadahan berdasarkan kosentrasi ion-ion divalent tersebut
menggunakan persamaan :
Kesadahan(mg/l) sebagai CaCO3 = M2+ (mg/l) x
50
��.� �� �� �2+
Dimana M2+ = ion logam divalent
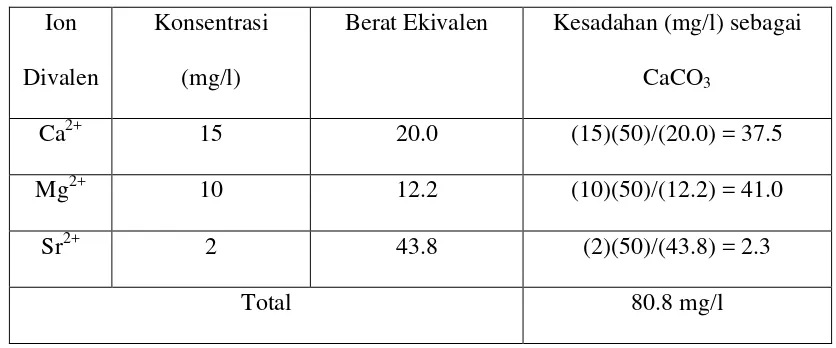
Contoh: Dari hasil analisa air diketahui kandungan ion-ionnya (mg/l) sebagai berikut: Hanya
kation divalent,Ca2+, Mg2+, dan Sr2+ yang diperhitungkan sebagai penyebab kesadahan,
maka kesadahan total berdasarkan konsentrasi dan berat ekivalen masing-masing ion
divalent kesadahan :
Tabel 2.5 Perhitungan Kesadahan Metode Total Ion
Divalen
Konsentrasi
(mg/l)
Berat Ekivalen Kesadahan (mg/l) sebagai
CaCO3
Ca2+ 15 20.0 (15)(50)/(20.0) = 37.5
Mg2+ 10 12.2 (10)(50)/(12.2) = 41.0
Sr2+ 2 43.8 (2)(50)/(43.8) = 2.3
Total 80.8 mg/l
2.5.2 Metode Titrasi EDTA
Titrasi kompleksometri meliputi reaksi pembentukan ion-ion kompleks ataupun
pembentukan molekul netral yang terdisosiasi dalam larutan. Persyaratan mendasar
terbentuknya kompleks demikian adalah tingkat kelarutannya tinggi. Titik akhir titrasi
ditetapkan dengan indicator logam ataupun secara potensiometer dan spektrofotometri.
(Khopkar,2003)
Metode ini menggunakan larutan EDTA (ethylenediamine tetra eacetic acid) sebagai
larutan standarnya. Untuk mengetahui titik akhir titrasi digunakan indikator logam. Diantara
indikator yang biasa digunakan adalah Eriochrome Black T (EBT). (Sawyer and Mc
Carty.1998)
Eriochrome Black T sebagai indicator akan membentuk senyawa kompleks
seluruhnya dengan EDTA yang ditambahkan, dengan kata lain kapan penambahan larutan
EDTA mulai berlebih yang ditunjukkan oleh perubahan warna larutan dari merah menjadi
biru. Reaksi ini berlangsung sempurna pada pH 8-10. Untuk mempertahankan larutan pada
pH tersebut ditambahkan larutan buffer salmiak.Ca2+ dan Mg2+ akan membentuk senyawa
kompleks warna merah anggur, dengan EBT.
M2++ EBT → (M EBT)kompleks merah anggur
Perubahan semakin jelas bila pH semakin tinggi, namun pH yang tinggi dapat
menyebabkan ion-ion kesadahan hilang dari larutan, karena terjadi pengendapan Mg(OH)2
dan CaCO3. Pada pH > 9, CaCO3 sudah mulai terbentuk.
2.6 Menghilangkan Kesadahan Air
Ada beberapa cara untuk menghilangkan kesadahan air. Dalam skala besar, misalnya
air untuk konsumsi masyarakat digunakan proses penghilangan kesadahan air dengan
penambahan soda. Dalam proses pengolahan air ditambahkan soda Ca(OH)2 dan abu soda
Na2CO3 sehingga kalsium akan mengendap sebagai CaCO3 dan magnesium sebagai
Mg(OH)2. Bila kesadahan hanya disebabkan oleh „kesadahan karbonat‟ maka cukup hanya
dengan menambahkan Ca(OH)2 untuk menghilangkannya.
Untuk menghilangkan kesadahan air yang disebabkan oleh ion magnesium agar
magnesium dapat mengendap dalam bentuk Mg(OH)2 harus dibuat pH air tinggi, yaitu
penambahan abu soda.
Cara lain untuk menghilangkan kesadahan air adalah secara pertukaran ion, dengan
cara melewatkan air ke dalam wadah penukar kation yaitu bahan resin yang sudah
mengandung senyawa kimia penukar kation, kemudian dilanjutkan dengan melewatkan air
kedalam wadah penukar anion, sehingga kation didalam air ditukar dengan ion hidrogen dan
anion ditukar dengan ion hidroksida dan menghasilkan air dalam keadaan murni. Beberapa
materi telah dikembangkan sebagai wadah penukar ion, termasuk diantaranya mineral
aluminium silikat atau zeolit. Zeolit yang sudah berhasil digunakan dalam pemurnian air