TESIS
POTENSI FLAVONOID EKSTRAK BIJI MAHONI
(
Swietenia mahagoni
Jacq) UNTUK MENURUNKAN
KONSENTRASI 8-OHdG PADA URIN TIKUS
WISTAR JANTAN YANG TERPAPAR ETANOL
AGUNG ARI CHANDRA WIBAWA
PROGRAM PASCASARJANA
UNIVERSITAS UDAYANA
TESIS
POTENSI FLAVONOID EKSTRAK BIJI MAHONI
(
Swietenia mahagoni
Jacq) UNTUK MENURUNKAN
KONSENTRASI 8-OHdG PADA URIN TIKUS
WISTAR JANTAN YANG TERPAPAR ETANOL
AGUNG ARI CHANDRA WIBAWA NIM. 1392061007
PROGRAM MAGISTER
PROGRAM STUDI KIMIA TERAPAN
PROGRAM PASCASARJANA
UNIVERSITAS UDAYANA
DENPASAR
POTENSI FLAVONOID EKSTRAK BIJI MAHONI
(
Swietenia mahagoni
Jacq) UNTUK MENURUNKAN
KONSENTRASI 8-OHdG PADA URIN TIKUS
WISTAR JANTAN YANG TERPAPAR ETANOL
Tesis untuk Memperoleh Gelar Magister
Pada Program Magister, Program Studi Kimia Terapan,
Program Pascasarjana Universitas Udayana
AGUNG ARI CHANDRA WIBAWA NIM. 1392061007
PROGRAM MAGISTER
PROGRAM STUDI KIMIA TERAPAN
PROGRAM PASCASARJANA
UNIVERSITAS UDAYANA
DENPASAR
Lembar Persetujuan Pembimbing
TESIS INI TELAH DISETUJUI
PADA TANGGAL 30 JULI 2016
Pembimbing I, Pembimbing II,
Prof. Dr. Drs. I Made Dira Swantara, M.Si Dr. Drs. Manuntun Manurung, M.S. NIP. 19540101 198603 1 001 NIP. 19610525 199009 1 001
Mengetahui
Ketua Program Studi Kimia Terapan Direktur
Program Pascasarjana Program Pascasarjana
Universitas Udayana, Universitas Udayana,
PENETAPAN PANITIA PENGUJI TESIS
Tesis Ini Telah Diuji pada
Tanggal 30 Juni 2016
Panitia Penguji Tesis Berdasarkan SK Rektor Universitas Udayana
No: 3070 / UN. 14.4 / HK / 2016
Tanggal: 30 Juni 2016
Ketua : Prof. Dr. Drs. I Made Dira Swantara, M.Si
Anggota :
SURAT PERNYATAAN BEBAS PLAGIAT
Saya yang bertanda tangan di bawah ini:
Nama : Agung Ari Chandra Wibawa
NIM : 1392061007
Program Studi : Kimia Terapan
Judul Tesis : Potensi Flavonoid Ekstrak Biji Mahoni (Switenia mahagoni Jacq) Untuk Menurunkan Konsentrasi 8-OHdG Pada Urin Tikus
Wistar Jantan yang Terpapar Etanol.
Dengan ini menyatakan bahwa karya ilmiah tesis ini bebas plagiat.Apabila di
kemudian hari terbukti plagiat dalam karya ilmiah ini, maka saya bersedia
menerima sanksi sesuai peraturan Mendiknas RI No. 17 Tahun 2010 dan
Peraturan Perundang-undangan yang berlaku.
Denpasar, Juni 2016
Yang membuat pernyataan,
UCAPAN TERIMA KASIH
Pertama-tama perkenankanlah penulis memanjatkan puji syukur ke
hadapan Ida Sang Hyang Widhi Wasa/ Tuhan Yang Maha Esa, karena hanya atas
asung kerta wara nugraha-Nya/ karunia-Nya, tesis ini dapat diselesaikan.
Pada kesempatan ini perkenankanlah penulis mengucapkan terima kasih
yang sebesar-besarnya kepada Prof. Dr. Drs. I Made Dira Swantara, M.Si,
pembimbing I yang dengan penuh perhatian telah memberikan dorongan,
semangat, bimbingan, dan saran selama penulis mengikuti program magister,
khususnya dalam penyelesaian tesis ini. Terima kasih sebesar-besarnya pula
penulis sampaikan kepada Dr. Drs. Manuntun Manurung, M.S., Pembimbing II
yang dengan penuh perhatian dan kesabaran telah memberikan bimbingan dan
saran kepada penulis.
Ucapan yang sama juga ditujukan kepada Rektor Universitas Udayana
Prof. dr. dr. Ketut Suastika, Sp.PD-KEMD untuk kesempatan dan fasilitas yang
diberikan kepada penulis untuk mengikuti dan menyelesaikan pendidikan
Program Magister di Universitas Udayana. Ucapan terima kasih ini juga ditujukan
kepada Direktur Program Pascasarjana Universitas Udayana Prof. Dr. dr. A.A.
Raka Sudewi, Sp.S(K) atas kesempatan yang diberikan kepada penulis untuk
menjadi mahasiswa Program Magister pada Program Pascasarjana Universitas
Udayana. Tidak lupa pula penulis ucapkan terima kasih pada seluruh penguji tesis
ini Dr. Dra. Ni Made Suaniti, M.Si., Prof. Dr. Ir. I Gede Mahardika, M.S., serta
Dr. Dra. Wiwik Susanah Rita, M.Si yang telah memberikan saran dan kritik yang
membangun demi kesempurnaan tesis ini.
Pada kesempatan ini penulis ingin mengucapkan terima kasih kepada
kedua orang tua Drs. Made Gunawan, M.Pd dan Dra. Ni Ketut Alit Suarti, M.Pd
yang mengasuh dan membesarkan penulis serta memberikan bantuan moral dan
finansial selama penelitian dan penyusanan tesis. Kakak kandung tercinta Agung
Gede Wikantara beserta keluarga besar dari ayah dan ibu yang sangat membantu
penulis dalam memberikan semangat dan bantuan kepada penulis selama
kesabaran, kritik, saran, dukungan dan kasih sayang kepada penulis yang tidak
ada henti-hentinya dari menyelesaikan program studi sarjana hingga magister.
Sahabat angkatan 2013 program Magister Kimia Terapan Udayana dan sahabat
Gede Sugita Artana yang telah memberikan semangat dan motivasi selama
penyusunan tesis ini
Semoga Ida Sang Hyang Widi Wasa/ Tuhan Yang Maha Esa selalu
melimpahkan rahmat dan karunia-Nya kepada semua pihak yang telah membantu
pelaksanaan dan penyelesaian tesis ini, serta kepada pihak-pihak yang tidak dapat
penulis sebutkan satu persatu.
Denpasar, Juni 2016
ABSTRAK
POTENSI FLAVONOID EKSTRAK BIJI MAHONI (Switenia mahogany
Jacq) UNTUK MENURUNKAN KONSENTRASI 8-OHdG PADA TIKUS WISTAR JANTAN YANG TERPAPAR ETANOL
Penelitian ini bertujuan untuk menentukan fraksi aktif senyawa flavonoid biji mahoni sebagai antioksidan dalam menurunkan konsentrasi 8-OHdG dalam urin tikus yang terpapar etanol. Biji mahoni dimaserasi dengan etanol 70% dan dipartisi secara berlanjut dengan n-heksana, etil asetat, dan n-butanol. Uji kadar total flavonoid pada fraksi dilakukan dengan metode spektrofotometri UV-Vis yang menunjukan fraksi n-butanol mengandung flavonoid terbanyak yaitu sebesar 41,734 mg/L. Pengukuran konsentrasi 8-OHdG dilakukan dengan ELISA pada
λ450 nm. Berdasarkan hasil analisis dengan ELISA, dosis 50,100,150,200 mg/kg
bb terbukti dapat menurunkan konsentrasi 8-OHdG selama 21 hari pada urin tikus yang terpapar etanol selama 30 hari. Konsentrasi 8-OHdG pada perlakuan fraksi n-butanol dosis 50, 100, 150, dan 200 mg/kg bb, diprediksi membutuhkan waktu selama 64, 66, 54, dan 32 hari agar konsentrasi 8-OHdG menjadi 0,3318 ng/mL.
ABSTRACT
POTENCIAL FLAVONOID MAHONI (Switenia mahogany Jacq) SEED EXTRACT TO DECREASE URINARY 8-OHdG CONCENTRATION IN
MALE RATS AFTER EXPOSED TO ETHANOL
This study aim for determine active fraction flavonoid compounds in mahoni seed as the antioxidant in decrease urinary concentration of 8-OHdG in rats after exposed to ethanol. Mahoni seed was macerated by ethanol 70% and then partitioned with n-hexane, ethyl acetate, and buthanol. Total flavonoid test was conducted using spectrophotometry UV-Vis method and showed that n-buthanol fraction has the highest level flavonoid is 41,73 mg/L. Measurement urinary 8-OHdG concentration has been carried out by ELISA on λ450 nm. Based on analysis result carried by ELISA, concentration of 8-OHdG with dose of 50, 100, 150, and 200 mg/kg bb was decreased during 21 days in male rats after exposed to ethanol. 8-OHdG concentration on dose fraction n-buthanol 50, 100, 150, and 200 mg/kg bb, predicted takes time 64, 66, 54, 31 days for 8-OHdG concentration becomes 0,3318 ng/mL.
RINGKASAN
Mengonsumsi etanol berlebihan akan mengakibatkan gangguan pada
organ hati. Metabolisme etanol terjadi di hati yang dapat meningkatkan radikal
bebas di dalam tubuh. Pada reaksi biotransformasi, etanol mengalami dua fase
yaitu fungsionalisme (fase I) dan konyugasi (Fase II). Khusus reaksi fase I, etanol
mengalami reaksi oksidasi menjadi asetaldehid oleh alkohol dehidrogenase
(ADH). Perubahan aldehid menjadi etanol ataupun sebaliknya dapat menghasilkan
radikal hidroksil (•OH) atau sebagai Radical Oxygen Species (ROS).
ROS dapat menyebabkan kerusakan pada senyawa-senyawa biomolekul
seperti karbohidrat, protein, lipid, dan DNA. Jika radikal bebas yang dihasilkan
melebihi antioksidan dalam tubuh dapat menyebabkan keadaan stres oksidatif.
Radikal hidroksil dapat mengoksidasi basa guanosin menjadi 8-OHdG, sehingga
dapat mengubah struktur DNA yang dapat mengakibatkan mutagenesis atau
karsinogenesis. Akibat yang dialami apabila terjadi mutagenesis dan
karsinogensesis adalah penuaan atau degeneratif dan penyakit kanker. Kadar
8-OHdG di dalam tubuh dapat diturunkan dengan mengonsumsi senyawa
antioksidan.
Senyawa antioksidan merupakan senyawa yang sangat berlimpah di alam.
Salah satu senyawa yang banyak mengandung antioksidan adalah senyawa
golongan flavonoid. Pada penelitian ini dilakukan uji kadar total flavonoid pada
fraksi aktif flavonoid biji mahoni untuk menurunkan konsentrasi 8-OHdG dalam
urin tikus setelah terpapar etanol. Biji mahoni dimaserasi dengan pelarut etanol
70% selama 2x24 jam dan dipartisi dengan pelarut heksana, etil asetat, dan
n-butanol secara berturut-turut. Masing-masing fraksi diuji fitokimia untuk
mengetahui ada atau tidaknya senyawa flavonoid yang terkandung dalam 3 fraksi.
Senyawa yang positif flavonoid dihitung kadar totalnya dengan metode
spektrofotometri UV-Vis dengan panjang gelombang 415 nm. Hasil pengujian
menunjukkan, fraksi n-butanol mengandung kadar total flavonoid terbanyak
mengadung kadar total flavonoid tertinggi diberikan pada hewan uji sebagai
antioksidan dalam menurunkan konsentrasi 8-OHdG selama 21 hari yang
sebelumnya telah dipapari etanol 20%.
Berdasarkan hasil uji analisis dengan metode ELISA pada sampel urin,
didapatkan hasil bahwa konsentrasi 8-OHdG pada hewan uji pada perlakuan dosis
50, 100, 150, dan 200 mg/kg bb mengalami penurunan kosentrasi 8-OHdG yang
dapat dilihat dengan membandingkan kelompok perlakuan dosis dengan
kelompok positif atau kelompok yang dikondisikan stres oksidatif. Tetapi selama
pemberian dosis fraksi n-butanol selama 21 hari, masih belum menurunkan
konsentrasi 8-OHdG pada hewan uji agar menjadi normal seperti saat awal.
Dengan menggunakan perhitungan dapat diprediksi pada hari keberapa
konsentrasi 8-OHdG hewan uji menjadi keadaan normal. Hasil perhitungan
memberikan prediksi untuk perlakuan dosis 200 mg/kg bb membutuhkan 32 hari,
150 mg/kg bb membutuhkan 54 hari, 100 mg/kg bb membutuhkan 66 hari dan 50
DAFTAR ISI
Halaman
SAMPUL DEPAN ... i
SAMPUL DALAM ... ii
PERSYARATAN GELAR ... iii
LEMBAR PERSETUJUAN PEMBIMBING ... iv
PENETAPAN PANITIA PENGUJI ... v
SURAT PERNYTAAN BEBAS PLAGIAT ... vi
UCAPAN TERIMAKASIH ... vii
1.3 Tujuan Penelitian ... 4
1.4 Manfaat Penelitian ... 5
BAB II TINJAUAN PUSTAKA ... 6
2.1 Biji Mahoni ... 6
2. 2 Flavonoid ... 8
2. 3 Hewan Uji ... 11
2. 4 Etanol ... 12
2.5 Radikal Bebas ... 13
2.5.2 Sifat-sifat radikal bebas ... 14
2.5.3 Tahap pembentukan radikal bebas ... 14
2.6 Stres oksidatif ... 16
2.7 Senyawa 8-OHdG ... 17
2.8 Isolasi komponen aktif tanaman ... 18
2.8.1 Ekstraksi ... 18
2.8.2 Pemisahan dan pemurnian... 18
2.8.2.1 Partisi ... 19
2.9 Karakterisasi ... 19
2.10.1 Uji fitokimia flavonoid ... 20
2.10.2 Spektrofotometer Ultra Violet... 20
2.10 Enzyme Linked Immunosorbent Assay... 20
BAB III KERANGKA BERPIKIR, KONSEP, DAN HIPOTESIS PENELITIAN ... 22
3.1 Kerangka Berpikir ... 22
3.2 Konsep Penelitian ... 24
3.3 Hipotesis Penelitian ... 25
BAB IV METODE PENELITIAN ... 26
4.1 Rancangan Penelitian... 26
4.2 Lokasi dan Waktu Penelitian ... 28
4.3 Penentuan Sumber Data ... 29
4.3.1 Populasi ... 29
4.3.2 Kriteria sampel ... 29
4.3.3 Penentuan jumlah ulangan sampel ... 29
4.4 Variabel Penelitian... 30
4.5 Bahan Penelitian ... 30
4.6 Instrumen Penelitian ... 30
4.7 Prosedur Penelitian ... 30
4.7.1 Preparasi sampel... 30
4.7.2 Ekstraksi ... 31
4.7.3 Partisi ... 31
4.7.4 Uji flavonoid ... 32
4.7.5 Uji kadar total flavonoid ... 32
4.7.6 Perlakuan hewan uji ... 32
4.7.7 Pengambilan urin hewan uji ... 33
4.7.8 Analisis 8-OHdG dalam urin tikus ... 33
4.8 Analisis Data ... 34
BAB V HASIL DAN PEMBAHASAN ... 35
5.1 Ekstraksi Senyawa Flavonoid Dalam Biji Mahoni ... 35
5.2 Pemisahan Ekstrak Kasar Etanol ... 35
5.3 Uji Fitokimia dan Uji Kadar Total Flavonoid ... 36
5,5,1 Pemberian etanol ... 40
5.5.2 Pemberian fraksi n-butanol biji mahoni ... 41
5.6 Analisis 8-OHdG dalam Urin Tikus Wistar ... 42
BAB VI SIMPULAN DAN SARAN ... 50
6.1 Simpulan ... 50
6.2 Saran ... 50
DAFTAR PUSTAKA ... 51
DAFTAR TABEL
Halaman
5.1 Berat Hasil Partisi ... 36 5.2 Uji Skrining Fitokimia Senyawa Golongan Flavonoid Pada Fraksi
DAFTAR GAMBAR
Halaman
2.1 Tanaman Mahoni ... 7
2.2 Struktur Dasar Flavonoid ... 9
2.3 Struktur Dasar Beberapa Golongan Flavonoid ... 10
2.4 Tikus Wistar ... 11
2.5 Metabolisme Etanol ... 13
2.5 Struktur 8-hidroksi-2’-deoksiguanosin ... 17
3.1 Kerangka Konsep Penelitian ... 24
4.1 Bagan Rancangan Penelitian ... 27
5.1 Kurva Standar 8-OHdG... 44
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Skema Proses Ekstraksi Senyawa Flavonoid dari Biji Mahoni ... 56
Lampiran 2. Skema Proses Partisi Senyawa flavonoid dari Ekstrak Biji Mahoni ... 57
Lampiran 3. Skema Perlakuan Hewan Uji Tikus Wistar Jantan ... 58
Lampiran 4, Perhitungan Pembuatan Larutan Etanol 19,80% ... 59
Lampiran 5. Perhitungan Kadar Total Flavonoid ... 60
Lampiran 6. Volume Pemberian Fraksi n-butanol ... 63
Lampiran 7. Perhitungan Nilai Konsentrasi 8-OHdG ... 65
BAB I PENDAHULUAN
1.1 Latar Belakang
Gaya hidup remaja yang telah digemari oleh masyarakat yaitu
mengonsumsi minuman beralkohol. Mengonsumsi etanol berlebihan akan
mengakibatkan gangguan pada organ hati yang disebut hepatitis. Angka kematian
akibat konsumsi minuman alkohol di Indonesia adalah sekitar 50 orang per hari
atau sekitar 18.000 per tahun (Conreng et al., 2014).
Metabolisme etanol terjadi di hati yang dapat meningkatkan radikal bebas
di dalam tubuh. Pada reaksi biotransformasi, etanol mengalami dua fase yaitu
fungsionalisme (fase I) dan konyugasi (Fase II). Khusus reaksi fase I, etanol
mengalami reaksi oksidasi menjadi asetaldehid oleh alkohol dehidrogenase
(ADH). Kekurangan ADH pada hati dapat digantikan oleh enzim Microsomal
Ethanol Oxidizing System (MEOS atau P4502E1). Perubahan aldehid menjadi
etanol ataupun sebaliknya dapat menghasilkan radikal hidroksil (•OH) atau
sebagai Radical oxygen species (ROS) maupun metabolit toksik lain seperti fatty
acid ethyl esters/FAEEs (Suaniti et al., 2013).
Radikal bebas adalah suatu senyawa atau molekul yang memiliki elektron
tidak berpasangan pada orbital luarnya, senyawa ini bersifat sangat reaktif, dengan
cara menyerang dan mengikat atau menarik elektron molekul yang berada di
sekitarnya. ROS dapat menyebabkan kerusakan pada senyawa-senyawa
2
dihasilkan melebihi antioksidan dalam tubuh dapat menyebabkan keadaan stres
oksidatif (Hardianty, 2011).
Stres oksidatif dalam tubuh dapat terdeteksi dari adanya
senyawa-senyawa penanda atau biomarkerstres oksidatif, salah satunya adalah 8-OHdG
(8-Hidroksi-2’-deoksiguanosin). Senyawa 8-OHdG merupakan senyawa yang mudah
larut dalam air sehingga dapat ditemukan pada cairan biologis, seperti serum
darah dan urin. Senyawa 8-OHdG terbentuk karena tidak adanya protein protektif
(histon) pada DNA mitokondria. Radikal hidroksil dapat mengoksidasi guanosin
menjadi 8-OHdG, sehingga dapat mengubah DNA dan mengakibatkan terjadinya
mutagenesis atau karsinogenesis. Akibat yang dialami apabila terjadi mutagenesis
dan karsinogensesis adalah penuaan atau degeneratif dan penyakit kanker
(Muctahdi, 2013). Kadar 8-OHdG di dalam tubuh dapat diturunkan dengan
mengonsumsi senyawa antioksidan.
Antioksidan adalah molekul yang dapat menetralkan radikal bebas
dengan cara menerima atau mendonorkan satu elektron untuk menghilangkan
elektron yang tidak berpasangan. Senyawa golongan flavonoid merupakan
senyawa yang bersifat antioksidan karena dapat mengubah radikal hidroksil
menjadi H2O2 dengan tahap terminasi, kemudian dengan bantuan katalase H2O2
diubah menjadi H2O. Flavonoid sangat penting dalam mempertahankan
keseimbangan antara oksidan dengan antioksidan di dalam tubuh. Menurut
Muchtadi (2013) flavonoid mempunyai aktivitas antioksidan yang paling
potensial, karena struktur kimianya yang mengandung o-difenol, suatu ikatan
3
bermanfaat dalam mencegah kerusakan sel akibat stres oksidatif. Pada penelitian
yang dilakukan Jawi et al. (2008) menyatakan hasil penelitian pada ekstrak ubi
jalar ungu yang mengandung senyawa golongan flavonoid dapat menurunkan
kadar malondialdehyde (MDA) pada mencit yang diberikan beban aktivitas fisik
maksimal.
Menurut Sumardika dan Jawi (2012), mekanisme kerja dari flavonoid
sebagai antioksidan bisa secara langsung maupun tidak langsung. Flavonoid
sebagai antioksidan secara langsung adalah dengan mendonorkan ion hidrogen
sehingga dapat menetralisir efek toksik dari radikal bebas, sedangkan flavonoid
sebagai antioksidan tidak langsung yaitu dengan meningkatkan ekspresi gen
antioksidan endogen.
Senyawa flavonoid pada tanaman di alam sangatlah berlimpah, salah satu
tanaman yang mengandung flavonoid yaitu tanaman mahoni (Swietenia mahagoni
Jacq), misalnya pada biji, kulit, dan batang (Sianturi, 2001). Menurut
Syamsuhidayat dan Hutapea (1991), biji mahoni dengan jenis Swietenia mahagoni
Jacq ternyata dapat digunakan untuk mengobati berbagai penyakit diantaranya
penyakit darah tinggi, kencing manis, rematik, dan biji mahoni juga berpotensi
untuk mengobati penyakit kanker (Ayuni dan Sukarta, 2013; Putri (2004).
Uji fitokimia biji mahoni yang telah dilakukan Rasyad et al., 2012
menyatakan bahwa biji mahoni (Swietenia mahagoni Jacq) mengandung
alkaloid, saponin, steroid, terpenoid, dan flavonoid. Sedangkan pada penelitian
Suryani et al. (2013) menyatakan kandungan fenol dalam ekstrak biji mahoni
4
356,24 ± 3,44 mg asam galat dan setara dengan 33,11 ± 8,83 mg katekin.Dengan
kadar fenol tersebut peneliti tertarik menguji aktivitas senyawa flavonoid pada biji
mahoni untuk menurunkan kadar 8-OHdG pada tikus yang terpapar etanol.
Menurut Ogino dan Wang (2007), ELISA merupakan metode yang sangat
popular digunakan dalam menganalisis 8-OHdG pada sampel biologis (darah atau
urin). Uji ini memiliki beberapa keunggulan seperti teknik pengerjaan yang relatif
sederhana, cepat, dan memiliki sensitivitas yang cukup tinggi.
1.2 Rumusan Masalah
Berdasarkan uraian latar belakang di atas, maka dapat dibuat rumusan
masalah sebagai berikut:
1. Apakah ekstrak biji mahoni mengandung senyawa flavonoid?
2. Apakah fraksi biji mahoni yang mengandung senyawa flavonoid dapat
menurunkan konsentrasi 8-OHdG pada tikus yang terpapar etanol?
3. Berapakah dosis optimal fraksi biji mahoni yang mampu menurunkan
konsentrasi 8-OHdG pada tikus yang terpapar etanol agar kembali
sehat?
1.3 Tujuan Penelitian
Adapun tujuan dalam penelitian ini, diantaranya:
1. Untuk mengetahui biji mahoni mengandung senyawa flavonoid.
2. Untuk mengetahui aktivitas fraksi biji mahoni yang mengandung
5
3. Untuk mengetahui dosis yang optimal fraksi biji mahoni yang mampu
menurunkan konsentrasi 8-OHdG pada tikus yang terpapar etanol agar
kembali sehat.
1.4 Manfaat Penelitian
Penelitian ini diharapkan dapat memaksimalkan potensi biji mahoni yang
BAB II
TINJAUAN PUSTAKA
2.1 Biji Mahoni
Tanaman mahoni (Swietenia mahagoni) merupakan salah satu tanaman
yang dianjurkan dalam pengembangan HTI (Hutan Tanaman Industri). Mahoni
dalam klasifikasinya termasuk famili Meliaceae. Mahoni dapat ditemukan tumbuh
liar di hutan jati dan tempat-tempat lain yang dekat dengan pantai atau ditanam
ditepi jalan sebagai pohon pelindung (Qodri et al., 2014), bentuk pohon dan biji
mahoni dapat dilihat pada Gambar 2.1.
Klasifikasi dari tanaman mahoni adalah (Plantamor, 2012):
Kingdom : Plantae (Tumbuhan)
Subkingdom : Tracheobionta (Tumbuhan berpembuluh)
Super Devisi : Spermatophyta (Menghasilkan Biji)
Devisi : Magnoliophyta (Tumbuhan berbunga)
Kelas : Magnoliopsida (berkeping dua/ dikotil)
Sub Kelas : Rosidae
Ordo : Sapindales
Famili : Meliaceae
Genus : Swietenia
7
A B
Gambar 2.1
Tanaman Mahoni (A) Pohon mahoni (B) Biji mahoni (Adminboro, 2014)
Pada tahun 70-an, mahoni banyak dicari orang sebagai obat. Orang-orang
mengonsumsi biji mahoni hanya dengan menelan bijinya setelah membuang
bagian yang pipih. Penelitian Genus Swietenia (mahoni) sekarang ini semakin
berkembang. Dadang dan Ohsawa (2000) melaporkan ekstrak biji Swietenia
mahagoni pada konsentrasi 5% dapat memberi penghambatan makan 100% larva
P. xylostella. Menurut Prijono (1998) ekstrak biji mahoni pada konsentrasi 0.25%
dapat menyebabkan kematian larva C. pavonana 10.4% (Siregar et al., 2006).
Kandungan kimia mahoni dipengaruhi oleh iklim dan cuaca serta habitat
masing-masing mahoni. Biji mahagoni afrika Khaya segenalensis yang diekstraksi
dengan etanol, dan dipartisi dengan etil asetat mengandung senyawa
tetranortriterpenoid. Ekstrak biji S. macrophylla mengandung triterpenoid yaitu
swietenin dan swietenolida tiglat, serta flavonoid dan tanin. Esktrak etanol dari
8
Biji mahoni memiliki efek farmakologis antipiretik, antijamur,
menurunkan tekanan darah tinggi (hipertensi), kencing manis (diabetes mellitus),
kurang nafsu makan, demam, masuk angin, dan rematik. Hasil penelitian yang
sering dipublikasi adalah ekstrak biji mahoni untuk menurunkan kadar glukosa
darah pada tikus Wistar. Kabar yang terbaru bahwa ekstrak biji mahoni termasuk
salah satu obat tradisional yang dapat menghambat pertumbuhan HIV AIDS
dalam laboratorium. Penelitian ekstrak mahoni sebagai antibiotik juga telah
dilaporkan, bahkan penelitinya menganjurkan agar diteliti lebih jauh, karena
potensial untuk digunakan sebagai antibiotik baru terutama untuk bakteri yang
resistan terhadap antibiotik yang ada (Rasyad, 2012).
2.2 Flavonoid
Flavonoid merupakan salah satu golongan fenol yang terbesar di alam.
Senyawa flavonoid ditemukan dalam tumbuhan tingkat tinggi, tetapi tidak dalam
mikroorganisme. Dalam tumbuhan flavonoid memiliki fungsi pengatur dalam
proses fotosintesis, kerja antimikroba, dan antivirus. Berbagai jenis senyawa,
kandungan dan aktivitas antioksidatif flavonoid sebagai salah satu kelompok
antioksidan alami yang terdapat pada sereal, sayur-sayuran biji-biji buah, telah
banyak dipublikasikan. Flavonoid berperan sebagai antioksidan dengan cara
mendonasikan atom hidrogennya atau melalui kemampuannya mengkelat logam,
berada dalam bentuk glukosida (mengandung rantai samping glukosa). Flavon,
flavonol, dan antosianidin adalah jenis yang banyak ditemukan di alam sehingga
9
disebabkan oleh berbagai tingkat hidroksilasi, alkoksilasi atau glikosilasi dari
struktur tersebut (Redha, 2010).
Umumnya flavonoid larut dalam pelarut polar seperti etanol, metanol,
aseton, dan air. Adanya gula yang terikat pada flavonoid cenderung menyebabkan
flavonoid lebih mudah larut dalam air (Markham, 1998). Flavonoid dapat
memberikan warna yang khas terhadap pereaksi pendeteksi flavonoid, seperti :
NaOH 10 %, asam sulfat pekat, bubuk magnesium-asam klorida pekat, dan
natrium amalgam-asam klorida pekat (Harborne, 1987).
Senyawa flavonoid tersusun atas 15 atom karbon pada inti dasarnya
dengan konfigurasi C6-C3-C6 yaitu dua cincin aromatik dan dihubungkan oleh
atom karbon yang dapat atau tidak dapat membentuk cincin ketiga (Indradewi,
2011). Struktur dasar flavonoid dapat dilihat pada Gambar 2.2.
A C
B
Gambar 2.2
Struktur dasar flavonoid (Robinson, 1991)
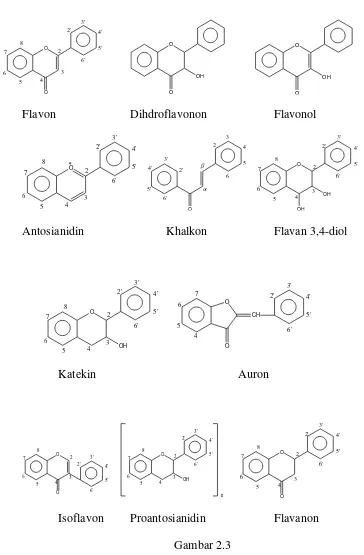
Berdasarkan struktur dasarnya maka dapat dikenal beberapa golongan
10
dihidroflavonol, flavonol, antosianidin, katekin, (flavan 3-ol), dan
proantosiainidin yang tertera pada Gambar 2.3.
Antosianidin Khalkon Flavan 3,4-diol
Isoflavon Proantosianidin Flavanon
Gambar 2.3
11
2.3 Hewan Uji
Hewan Uji yang digunakan dalam penelitian ini yaitu tikus putih berjenis
Rattus novergicus galur Wistar (Gambar 2.4) dikembangkan di Institut Wistar
pada tahun 1906 untuk digunakan dalam biologi dan penelitian medis.
Gambar 2.4
Tikus Wistar (Dokterternak, 2010)
Tikus putih atau dikenal tikus Wistar merupakan tikus yang paling sering
digunakan sebagai hewan uji dalam laboratorium. Keunggulan tikus putih
dibandingkan tikus lainnya yaitu penanganan dan pemeliharaannya yang mudah
karena tubuhya kecil, bersih, dan kemampuan reproduksi tinggi (Pribadi, 2008).
Selama bertahun-tahun, tikus telah digunakan dalam banyak eksperimen,
yang telah menambah pemahaman kita tentang genetika, penyakit, pengaruh
obat-obatan, dan topik lain dalam kesehatan dan kedokteran. Laboratorium tikus juga
terbukti berharga dalam studi psikologis belajar dan proses mental lainnya.
Pentingnya sejarah spesies ini untuk riset ilmiah tercermin dengan jumlah literatur
tentang itu, sekitar 50% lebih dari itu pada tikus. Konversi usia manusia ke tikus
12
(Umami, 2012). Konversi dosis pada manusia dengan berat badan 70 kg ke tikus
wistar dengan berat badan 200 gram adalah 0,018 (Indrapraja, 2009).
2.4 Etanol
Konsumsi etanol adalah merupakan bagian dari kehidupan masyarakat
yang dapat mengakibatkan masalah sosial. Etanol dapat mengubah respon
terhadap obat yang diberikan bersamaan. Hal ini terjadi karena adanya interaksi
antara etanol dan obat. Mekanisme interaksi farmakokinetik meliputi: absorbsi,
distribusi, metabolisme, dan ekskresi. Etanol yang dikonsumsi diabsorbsi di usus
halus sebesar 80%. Kecepatan absorbsi tergantung pada jumlah dan konsentrasi
etanol dalam minuman yang mengisi lambung dan usus. Etanol dalam lambung
yang kosong kadarnya dalam darah terdeteksi pada 30-90 menit setelah
mengkonsumsi (Gugule et al., 2013).
Distribusi etanol berjalan cepat, dalam jaringan mendekati kadar di dalam
darah. Volume distribusi dari etanol mendekati volume cairan tubuh total (0,5-0,7
L/kg). Sekitar 90-98% etanol yang diabsorbsi dalam tubuh akan mengalami
oksidasi. Metabolisme etanol terjadi di dalam hati. Etanol yang masuk ke dalam
tubuh akan cepat diabsorpsi dalam lambung dan usus halus. Etanol diabsorpsi
langsung secara difusi dan akan didistribusikan secara bebas dalam jaringan dan
cairan tubuh. Volume distribusi etanol berkisar antara 0,58-0,70 L/kg berat badan.
Kadar etanol dalam otak dicapai setelah absorpsi sempurna dalam darah.
Faktor-faktor yang mempengaruhi absorpsi etanol adalah volume, pengenceran,
kecepatan pencernaan, dan makanan yang ada di dalam lambung. Di dalam hati,
13
Alkohol
dehidrogenase Aldehid
dehidrogenase
Asetaldehid akan dioksidasi oleh aldehid dehidrogenase menjadi asam asetat atau
asetil ko-enzim A. Asam asetat yang dihasilkan dari oksidasi asetaldehid akan
masuk ke dalam siklus kreb, sehingga terbentuk karbon dioksida dan air.
Asetaldehid merupakan metabolit pertama dari etanol yang pada pasien alkoholis
terjadi proses metabolisme yang lambat sehingga mengakibatkan toksisitas
jaringan dan ketergantungan etanol (Wardjowinoto, 1998). Skema metabolisme
etanol dapat dilihat pada Gambar 2.5.
Gambar 2.5
Metabolisme Etanol (Wardjowinoto, 1998)
2.5 Radikal Bebas
Radikal bebas adalah suatu senyawa atau molekul yang mengandung satu
atau lebih elektron tidak berpasangan pada orbital luarnya. Molekul ini dapat
bereaksi dengan molekul lain yang akan menimbulkan reaksi rantai yang sangat
dekstruktif. Pengertian radikal bebas dan oksidan sering dianggap sama karena
keduanya memiliki kemiripan sifat, serta memiliki aktivitas yang sama dan
memberikan akibat yang hampir sama, meskipun melalui proses yang berbeda
(Hardianty, 2011).
2.5.1 Struktur radikal bebas
Atom terdiri atas inti (proton dan neutron) dan elektron. Jumlah proton
(bermuatan positif) dalam inti menentukan jumlah dari elektron (bermuatan
negatif) yang mengelilingi atom tersebut. Elektron mengelilingi suatu atom dalam
14
satu lapisan bahkan lebih. Jika satu lapisan penuh, elektron akan mengisi lapisan
kedua. Lapisan kedua akan penuh jika telah memiliki 8 elektron, dan begitu
seterusnya. Atom sering kali melengkapi lapisan luarnya dengan cara membagi
elektron-elektron bersama atom yang lain. Dengan membagi elektron, atom-atom
tersebut bergabung bersama dan mencapai kondisi stabilitas maksimum untuk
membentuk molekul. Oleh karena radikal bebas sangat reaktif, maka mempunyai
spesifitas kimia yang rendah, sehingga dapat bereaksi dengan berbagai
molekul lain, seperti protein, lemak, karbohidrat, dan DNA (Arief, 2012).
2.5.2 Sifat-sifat radikal bebas
Radikal bebas memiliki reaktifitas tinggi, karena adanya satu atau lebih
elektron tidak berpasangan pada orbital luarnya yang menyebabkan senyawa
tersebut sangat reaktif mencari pasangan dengan cara menyerang atau menarik
elektron molekul yang berada di sekitarnya. Hal ini mengakibatkan terbentuknya
senyawa radikal baru, dengan kata lain radikal bebas dapat mengubah suatu
molekul atau senyawa menjadi suatu radikal bebas baru, dan seterusnya sehingga
akan terjadi reaksi rantai. Sifat radikal bebas yang mirip dengan oksidan terletak
pada kecenderungannya untuk menarik elektron (Hardianty, 2011).
2.5.3 Tahap pembentukan radikal bebas
Tahap pembentukan Radikal Bebas terjadi melalui 3 tahap, yaitu;
1. Tahap Inisiasi, yaitu tahap pembentukan awal radikal bebas, dan menjadikan
senyawa yang non radikal menjadi radikal bebas. Contohnya:
15
2. Tahap propagasi, yaitu tahap pemanjangan rantai radikal, radikal bebas
diperluas sehingga membentuk beberapa radikal bebas yang baru.
Contohnya:
R2-H + R1• R2 • + R1-H
R3-H + R2 • R3 • + R2-H
Keterangan: R= rantai alkil
3. Tahap terminasi, yaitu tahap pembentukan non radikal dari radikal bebas,
bereaksinya senyawa radikal dengan radikal yang lain sehingga propagansinya
menjadi rendah. Contohnya:
R1 • + R1 • R1-R1
R2 • + R2 • R2-R2
R3 • + R3• R3-R3 (Hardianty, 2011).
Radikal bebas dapat terjadi melalui proses fisiologis normal dalam tubuh
atau karena pengaruh spesies eksogen. Spesies eksogen tersebut dapat berbentuk
senyawa yang muncul secara alami dalam biosfer (misalnya ozon, NO2, etanol,
atau tetradecanoyl phorbol acetate / TPA), senyawa kimia industri (seperti karbon
tetraklorida). Radikal yang sering muncul dalam proses biologis adalah
superoksida (O2-1) yang selanjutnya mengalami dismutasi menjadi hidrogen
peroksida (H2O2) atau mengalami protonasi menjadi radikal hidroperoksil.
Pembentukan hidrogen peroksida, menjadi sarana untuk mendeteksi adanya
proses yang melibatkan superoksida di dalam tubuh. Radikal superoksida dapat
ditemukan di semua sel yang mengalami metabolisme aerobik (Sholihah dan
16
Radikal bebas, yang sering disebut Reactive Oxygen Species, dapat
dibentuk melalui jalur enzimatis ataupun metabolik. Senyawa oksigen reaktif juga
dapat diproduksi oleh sel dalam kondisi stres ataupun tidak stres. Pada kondisi
tidak stres, terdapat keseimbangan antara proses pembentukan dan pemusnahan
senyawa oksigen reaktif. Sementara pada kondisi stres oksidatif, pembentukan
senyawa oksigen reaktif lebih tinggi dibandingkan dengan pemusnahannya yang
mengakibatkan sistem pertahanan tubuh terpacu untuk bekerja lebih keras untuk
memusnahkan senyawa oksigen reaktif. Salah satu sistem pertahanan tubuh itu
adalah sistem antioksidan enzimatis dan non enzimatis, yang bekerja menekan
senyawa oksigen reaktif yang berlebihan. Sebagai akibatnya adalah gangguan
metabolik yang mengakibatkan stres oksidatif (Hardianty, 2011).
2.6 Stres Oksidatif
Stres oksidatif adalah suatu keadaan tingkat Reactive oxygen species yang
toksik melebihi pertahanan antioksidan. Keadaan ini mengakibatkan kelebihan
radikal bebas, yang akan bereaksi dengan lemak, protein, asam nukleat seluler,
sehingga terjadi kerusakan lokal dan disfungsi organ tertentu (Arief, 2012).
Stres oksidatif pada susunan saraf pusat sangat mematikan, sebab otak
manusia terutama memakai metabolisme oksidatif. Meskipun berat otak hanya 2%
dari berat tubuh, otak menggunakan sekitar 50% dari seluruh oksigen tubuh.
Faktor stress oksidatif lain yang sangat berbahaya pada otak dengan adanya
kandungan PUFA (polyunsaturated fatty acid) yang tinggi, hampir 50% dari
struktur jaringan otak. Jaringan otak mengandung asam askorbat 100 kali lipat
17
peroksidase lebih rendah daripada jaringan lain yang juga meningkatkan risiko
terjadinya stres oksidatif. Radikal bebas merusak sel dan bereaksi dengan
makromolekuler sel melalui proses peroksidasi lipid, oksidasi DNA dan protein
(Siswonoto, 2008).
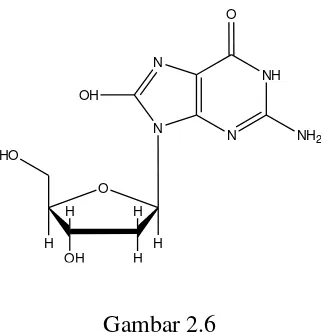
2.7 Senyawa 8-hidroksi-2’-deoksiguanosin (8-OHdG)
Senyawa 8-OHdG merupakan salah satu penanda stres oksidatif yang
merupakan hasil oksidasi basa guanin oleh ROS. 8-OHdG dapat dideteksi pada
sampel jaringan tubuh dan darah manusia. 8-OHdG dapat terdeteksi pada sampel
urin dikarenakan hasil dari nukleotida dan basa merupakan senyawa yang larut air
dan dieksresikan pada urin. Senyawa 8-OHdG dalam urin dijadikan biomarker
penting stres oksidatif dalam sel. Faktanya tingkat 8-OHdG dalam urin sering kali
digunakan dalam mengukur kerusakan oksidatif pada DNA. Struktur
8-Hidroksi-2’-deoksiguanosin dan struktur 2’-deoksiguanosin dapat dilihat pada Gambar 2.6
(Nakajima et al., 2012).
18
2.8 Isolasi Komponen Aktif Tanaman
Isolasi senyawa bioaktif yang berasal dari tumbuhan memegang peranan
yang sangat penting di dalam pencarian tumbuhan yang mempunyai aktivitas
biologi tertentu berkaitan dengan usaha untuk mengisolasi senyawa bioaktif.
Tahapan yang harus dilakukan adalah penyiapan sampel, ekstraksi, dan
pemisahan.
2.8.1 Ekstraksi
Ekstraksi adalah kegiatan penarikan senyawa kimia yang dapat larut
sehingga terpisah dari bahan yang tidak dapat larut dengan pelarut cair. Simplisia
yang diekstrak mengandung senyawa aktif yang dapat larut dan senyawa yang
tidak dapat larut. Senywa aktif yang terdapat dalam berbagai simplisia dapat
digolongkan ke dalam minyak atsiri, alkaloid, flavonoid dan lain-lain. Dengan
diketahuinya senyawa aktif yang terkandung dalam simplisia akan mempermudah
pemilihan pelarut dan cara ekstraksi yang tepat. Hasil yang diperoleh dari
ekstraksi disebut ekstrak. Ekstrak bisa dalam bentuk sediaan kering, kental, dan
cair (Raja, 2008).
2.8.2 Pemisahan dan pemurnian
Pemisahan dan pemurnian komponen atau senyawa kimia yang terdapat
dalam bahan tumbuhan umumnya dilakukan dengan teknik kromatografi. Teknik
kromatografi dipergunakan dalam pemisahan dan pemurnian suatu bahan alam.
Untuk pemisahan dan pemurnian umumnya menggunakan 2 jenis kromatografi
19
pemurnian, terlebih dahulu dilakukan pemisahan awal dengan menggunakan
metode partisi (Indradewi, 2011).
2.8.2.1 Partisi
Metode partisi bertujuan untuk memisahkan senyawa-senyawa kimia
dalam ekstrak kasar berdasarkan kepolarannya. Awalnya partisi dimulai dengan
pelarut non polar seperti n-heksan untuk menarik senyawa-senyawa non polar.
Selanjutnya digunakan pelarut semi polar seperti kloroform, etil asetat atau aseton
untuk menarik senyawa-senyawa semi polar. Terakhir digunakan pelarut polar
seperti metanol atau n-butanol untuk menarik senyawa polar.
Dalam metode partisi digunakan teknik yang umum digunakan yaitu
dengan corong pemisah dengan menggunakan dua pelarut yang tidak saling
tercampur. Untuk pemisahan senyawa yang berwarna, partisi dihentikan bila
ekstrak terakhir sudah tidak berwarna sedangkan untuk senyawa yang tidak
berwarna, dihentikan setelah 3 sampai 4 kali penggantian pelarut (Indradewi,
2011).
2.9 Karakterisasi
Karakterisasi suatu senyawa hasil isolasi dilakukan dengan cara kualitatif
dan kuantitatif. Dengan cara kualitatif, dilakukan dengan uji fitokimia untuk
mengetahui golongan senyawa dengan menggunakan pereaksi. Sedangkan dengan
uji kuantitatif, dilakukan dengan alat spektrofotometer UV-Visible untuk
mengukur nilai absrobansi dari sampel dan standar yang dapat digunakan untuk
20
2.9.1 Uji fitokimia flavonoid
Metode identifikasi ini dilakukan berdasarkan pada metode penapisan
fitokimia (phytochemical screening) terhadap golongan senyawa kimia tertentu
seperti flavonoid degan menggunakan pereaksi warna atau secara kualitatif
(Indradewi, 2011). Uji senyawa flavonoid dapat dilakukan dengan menggunakan
pereaksi pendeteksi senyawa flavonoid, antara lain pereaksi NaOH 10%, pereaksi
H2SO4, dan pereaksi Mg-HCl pekat.
2.9.2 Spektrofotometer ultraviolet
Spektrofotometri UV-Vis merupakan salah satu teknik analisis
spektroskopi yang memakai sumber radiasi eleltromagnetik ultraviolet dekat
(190-380) dan sinar tampak (380 - 780) dengan memakai instrumen spektrofotometer.
Radiasi ultraviolet diabsorpsi oleh molekul organik aromatik, molekul yang
mengandung elektron-terkonyugasi dan atau atom yang mengandung elektron,
menyebabkan transisi elektron di orbital terluarnya dari tingkat energi elektron
tingkat dasar ke tingkat energi elektron tereksitasi lebih tinggi. Besarnya serapan
radiasi tersebut sebanding dengan banyaknya molekul analit yang mengabsorpsi
sehingga dapat digunakan untuk analisis kuantitatif (Williams dan Fleming,
2008).
2.10 Enzyme Linked Immunosorbent Assay (ELISA)
Teknik ELISA pertama kali diperkenalkan pada tahun 1972 oleh Engval
dan Perlman. Teknik ini dapat digunakan untuk mendeteksi zat antibodi atau
21
melibatkan peran enzim konjugasi anti spesien imunoglobulin dan substrat
sebagai indikator dalam reaksi (Racmawati et al., 2004).
ELISA kit untuk penanda kerusakan DNA teroksidasi adalah
pengembangan immunoassay berdasarkan enzim kompetitif untuk mendeteksi dan
kuantisasi 8-OHdG dalam urin, serum, dan sel atau jaringan sampel DNA secara
cepat. Sejumlah sampel 8-OHdG ditentukan dengan membandingkan absorbansi
sampel dengan kurva standar. ELISA kit 8-OHdG memiliki batas deteksi antara
100 pg/mL hingga 20 ng/mL. Setiap kit terdapat reagen untuk analisis hingga 96
well termasuk kurva standar dan sampel (Cell Biolabs, Inc). Prinsipnya, sejumlah
sampel yang mengandung 8-OHdG atau standar pertama kali ditambahkan pada
8-OHdG/BSA konjugat yang sebelumnya telah ada dalam microplate. Kemudian
setelah dilakukan inkubasi awal, antibodi 8-OHdG monoklonal ditambahkan,
selanjutnya ditambahkan HRP sebagai antibodi kedua. Senyawa 8-OHdG yang
terdapat dalam sampel ditentukan dengan membandingkannya dengan kurva