BAB 3
BAHAN DAN METODE PENELITIAN
3.1 Alat-alat
Alat-alat yang digunakan dalam penelitian ini adalah :
- Labu leher tiga Pyrex
- Termometer 2100
- Kondensor bola Pyrex
C Fisons
- Buret (10 mL ± 0,05 mL) Pyrex
- Rotarievaporator Heidolph
- Hotplate stirrer Fisons
- Oven Fisons
- Botol Akuades - Magnetik Bar - Mortar dan Stamfer
- Corong Pisah Pyrex
- Tabung CaCl2
- Spektrofotometer FT-IR Shimadzu
Pyrex
- Tensiometer Cincin Du-Nuoy Kruss
- Alat Vakum Fisons
- Kertas Saring Biasa
- Neraca Analitis Mettler PM 480
- Alat shaker KL 2 Edmund Buhler
- Gelas Ukur 100 mL Pyrex
- Gelas Beaker 250 mL Pyrex
- Gelas Erlenmeyer 250 mL Pyrex
- Pipet Volumetri Pyrex
3.2 Bahan-bahan
- 2-propanol p.a. E.Merck
- Biji jarak
- Metanol p.a. E.Merck
- Benzena p.a. E.Merck
- n-Heksana p.a. E.Merck
- Asam sulfat 98% p.a. E.Merck
- Akuades
- Hidrogen peroksida 30% p.a. E.Merck
- Asam formiat 90% Fisons
- Natrium hidroksida(pellet) p.a. E.Merck
- Asam klorida 37 % p.a. E.Merck
- Barium klorida(s) p.a. E.Merck
- Phenolptalein p.a. E.Merck
- Natrium klorida(s) p.a. E.Merck
- Alkohol 95% teknis
- Pyridin Fisons
- Asam Asetat Anhidrida p.a. E.Merck - Kalium Hidroksida(pellet) p.a. E.Merck
- Asam Oksalat(s) p.a. E.Merck
- Natrium Karbonat(s) p.a. E.Merck
- Fenolftalein(s) p.a. E.Merck
- Larutan Wijs p.a. E.Merck
- Sikloheksana p.a. E.Merck
- Kalium Iodida p.a. E.Merck
- Amilum p.a. E.Merck
- Natrium Sulfat Anhidrous p.a. E.Merck
- Natrium Tiosulfat(s) p.a. E.Merck
- Iodium(s) p.a. E.Merck
3.3 Prosedur Penelitian
3.3.1 Pembuatan Reagen dan Standarisasi
3.3.1.1 Pembuatan Larutan HCl 0,5 N
Diukur sebanyak 10,45 ml larutan HCl(p) 37% lalu diencerkan dengan akuades dalam labu takar 250 ml sampai garis batas dan distandarisasi dengan menggunakan larutan Na2CO3 0,5 N.
3.3.1.2 Pembuatan Larutan HCl 0,1 N
Sebanyak 20 mL larutan HCl 0,5 N diencerkan dengan akuades dalam labu takar 100 mL.
3.3.1.3 Pembuatan Larutan Na2CO3 0,5 N
Sebanyak 6,623 gram Na2CO3 dilarutkan dengan akuades dalam labu takar 250 mL.
3.3.1.4 Pembuatan Larutan KOH-Alkohol 0,5 N
Ditimbang KOH sebanyak 7,0125 gram dan dilarutkan dengan alkohol dalam labu takar 250 ml sampai garis batas.
3.3.1.5 Pembuatan Larutan KOH 0,1 N
Ditimbang KOH sebanyak 1,4 gram dan dilarutkan dengan akuades dalam labu takar 250 mL sampai garis batas.
3.3.1.6 Pembuatan Larutan KOH 0,02 N
Diukur sebanyak 50 mL larutan KOH 0,1 N dan diencerkan dalam labu takar 250 mL dengan menggunakan akuades.
3.3.1.7 Pembuatan Larutan H2C2O4 0,1 N
Ditimbang 1,575 gram H2C2O4.2H2O dimasukkan ke dalam labu takar 250 mL dan diencerkan dengan akuades dalam labu takar 250 mL sampai garis batas.
3.3.1.8 Standarisasi Larutan KOH dengan Larutan H2C2O4 0,1 N
Dipipet sebanyak 5 mL larutan KOH 0,1 N lalu ditambahkan 3 tetes indikator phenolphthalein dan dititrasi dengan larutan H2C2O4 0,1 N sampai larutan berwarna merah lembayung, dicatat volume H2C2O4
3.3.1.11 Pembuatan Larutan KI 10%
yang dipakai.
3.3.1.9 Pembuatan Larutan Indikator PP
Ditimbang 1 gram fenolftalein dan diencerkan dengan alkohol dalam labu takar 100 mL .
3.3.1.10 Pembuatan Alkohol Netral
Sebanyak 200 mL alkohol 96%, ditanbahkan 4 tetes indikator fenolftalein dan ditetesi dengan larutan KOH 0,1 N hingga menjadi larutan merah muda.
Ditimbang 10 gram kristal KI dilarutkan dengan akuades dalam labu takar 100 mL sampai garis tanda.
3.3.1.12 Pembuatan Larutan Na2S2O3 0,1 N
Ditimbang 6,25 gram kristal Na2S2O3.5 H2O dilarutkan dengan akuades dan diencerkan dalam labu takar 250 mL sampai garis tanda Lalu distandarisasi dengan larutan K2Cr2O7 0,1 N.
3.3.1.13 Pembuatan larutan BaCl2 10 %
Ditimbang 10 gram kristal BaCl2.2H2O dan diencerkan dengan akuades dalam labu takar 100 mL.
3.3.1.14 Pembuatan Larutan Indikator Amilum
Ditimbang 1 gram serbuk amilum dan dilarutkan dengan 100 mL akuades dan dipanaskan di atas pemanas hingga mendidih dan disaring dalam keadaan panas.
3.3.1.15 Pembuatan Reagen Asetilasi
Sebanyak 25 mL asam asetat anhidrida dimasukkan ke dalam labu takar 100 mL dan diencerkan dengan piridin sampai garis batas.
3.3.2 Ekstraksi Minyak Jarak dari Biji Jarak (Ricinus communis Linn)
Biji jarak dipisahkan dari cangkang lalu dikeringkan dan dihaluskan. Serbuk biji jarak halus sebanyak 500 gram dimaserasi dengan 2-propanol selama ± 2 hari.
Ekstrak disaring dan filtrat ditambahkan Na2SO4 anhidrous kemudian disaring. Filtrat diuapkan melalui rotarievaporator untuk memperoleh minyak jarak.
3.3.3 Pembuatan Metil Ester Asam Lemak Campuran dari Minyak Jarak
Ke dalam labu alas bulat leher tiga dimasukkan sebanyak 100 mL minyak jarak, 50 mL metanol dan 100 mL benzena sambil diaduk dan didinginkan dan melalui corong penetes diteteskan sebanyak 2 mL H2SO4(p) secara perlahan-lahan, kemudian dirangkai alat refluks dan dilengkapi dengan tabung CaCl2, dan direfluks selama 5 jam. Kelebihan metanol dan pelarut diuapkan dengan alat rotarievaporator.
Residu yang diperoleh diekstraksi dengan 100 mL n-heksana dan dicuci dengan 25 mL akuades sebanyak 2 kali. Lapisan atas diambil lalu ditambahkan Na2SO4 anhidrous dan disaring. Filtratnya dirotarievaporasi sehingga diperoleh metil ester asam lemak campuran dari minyak jarak dan dikonfirmasikan strukturnya melalui analisis FT-IR, analisis bilangan iodin, bilangan hidroksi dan uji harga HLB.
3.3.4 Pembuatan 9,10,12-Trihidroksi Metil Stearat Campuran
Kedalam labu leher tiga dimasukkan 60 mL HCOOH 90% dan ditambah 30 mL H2O2 30% setetes demi setetes. Kemudian distirer pada suhu 40-45oC selama 1 jam. Kemudian ditambah 50 mL metil ester asam lemak campuran dari minyak jarak melalui corong penetes. Dipertahankan suhunya pada 40-45oC sambil diaduk.
Didiamkan selama 1 malam kemudian dirotarievaporasi. Residu yang diperoleh dilarutkan dengan 100 mL dietil eter. Lapisan eter dicuci dengan 25 mL akuades sebanyak dua kali. Hasil pencucian dikeringkan dengan Na2SO4 anhidrous kemudian disaring. Filtrat diuapkan melalui rotarievaporator untuk mendapatkan senyawa 9,10,12-trihidroksi metil stearat campuran dan dikonfirmasikan strukturnya melalui analisis FT-IR, analisis bilangan iodin, bilangan hidroksi dan uji harga HLB.
3.3.5 Pembuatan Sabun Natrium 9,10,12-Trihidroksi Stearat Campuran
Sebanyak 33,6 gram larutan 9,10,12-trihidroksi metil stearat dimasukkan ke dalam labu alas kemudian ditambah 5 gram NaOH dan 50 mL alkohol 95%. Direfluks campuran selama 1 jam pada suhu 78oC. Produk dituangkan ke dalam larutan NaCl jenuh dan diaduk selama 15 menit lalu disaring kemudian residu dibilas dengan alkohol 70% dan produk dikeringkan di dalam oven pada suhu 105oC. Hasilnya dikonfirmasikan strukturnya melalui spektrofotometer FT-IR, dilanjutkan karakterisasinya dengan menentukan alkalinitas bebas, tegangan permukaan, uji kekuatan dan stabilitas busa yang dibandingkan dengan sabun yang tidak memiliki gugus hidroksi (natrium stearat), dan sabun natrium asam lemak dari minyak jarak yang mengandung 1 gugus hidroksi.
3.3.6 Prosedur Analisis
3.3.6.1 Analisis Bilangan Iodin
Analisis ini dilakukan terhadap metil ester asam lemak dari minyak jarak dan 9,10,12- trihidroksi metil stearat campuran.
Ditimbang sampel sebanyak ± 0,5 gram ke dalam gelas erlenmeyer 250 mL yang bertutup lalu ditambahkan 20 mL sikloheksana kemudian dikocok/diguncang untuk memastikan sampel telah benar-benar larut. Ditambahkan 25 mL larutan Wijs ke dalamnya kemudian ditutup dan dikocok agar campuran telah benar-benar bercampur dan disimpan tabung tersebut dalam ruang gelap selama ± 30 menit.
Diambil bahan tersebut dari tempat penyimpanan dan ditambahkan 20 mL larutan KI 15%, dan 150 mL air suling. Dititrasi dengan larutan Na2S2O3
Bilangan Iodin =
Berat Sampel (gram)
Keterangan: B = Volume Blanko (mL) S = Volume Sampel (mL) N = Normalitas Na
0,1 N sampai warna kuning hampir hilang (kuning pucat). Ditambahkan 1-2 mL indikator pati ke dalamnya dan dititrasi kembali sampai warna biru hilang. Dilakukan hal yang sama terhadap larutan blanko dan dihitung dengan :
(B-S) x N x 12,69
2S2O3
3.3.6.2 Analisis Bilangan Hidroksi
Analisis ini dilakukan terhadap metil ester asam lemak dari minyak jarak dan 9,10,12- trihidroksi metil stearat campuran.
Ditimbang 1 gram sampel ke dalam labu dan ditambahkan 5 mL reagen asetilasi (asam asetat anhidrida dalam pyridin) dan direfluks pada suhu 95-100o
Bilangan OH = + A.V Berat sample (gram)
Dimana: T = Normalitas KOH-Etanol
Vo = Volume KOH-Etanol untuk titrasi blanko (mL) V = Volume KOH-Etanol untuk titrasi sampel (mL) AV = Bilangan asam dari ester
3.3.6.3 Analisis Bilangan Penyabunan
Analisis ini dilakukan terhadap metil ester asam lemak dari minyak jarak dan 9,10,12- trihidroksi metil stearat campuran.
Ditimbang 0,1 gram sampel dan dimasukkan ke dalam gelas Erlenmeyer.
Kemudian ditambahkan 25 mL larutan KOH-Alkohol 0,5 N dan direfluks selama 30 menit. Didinginkan dan ditambah 3 tetes indikator fenolftalein kemudian dititrasi dengan larutan HCl 0,5 N hingga warna merah lembayung hilang. Dicatat volume HCl 0,5 N yang dipakai dan dihitung bilangan penyabunan dengan rumus :
( V blanko – V titrasi). N
C selama 1 jam. Setelah selesai didinginkan dan ditambah 1 mL akuades, dan dipanaskan selama 10 menit. Setelah dingin ditambah 5 mL alkohol netral dan dipindahkan larutan ke dalam gelas erlenmeyer kemudian ditambahkan 2-3 tetes indikator fenolftalein selanjutnya dititrasi dengan larutan KOH-Etanol 0,5 N.
Dilakukan titrasi terhadap larutan blanko pada kondisi sama. Ditentukan bilangan asam terhadap sampel dan dihitung bilangan hidroksi.
56,1 x T x (Vo-V)
HCl
Bilangan Penyabunan =
Massa sampel (gram) . 56,1
3.3.6.4 Analisis Bilangan Asam
Analisis ini dilakukan terhadap metil ester asam lemak dari minyak jarak dan 9,10,12- trihidroksi metil stearat campuran.
Sebanyak 0,1 gram sampel dimasukkan ke dalam gelas erlenmeyer. Kemudian ditambah 10 mL larutan alkohol netral. Erlemeyer tersebut ditutup dengan plastik dan dipanaskan selama 30 menit sambil diaduk. Larutan tersebut didinginkan dan ditambahkan 3 tetes indikator fenolftalein dan dititrasi dengan larutan KOH 0,02 N sampai terbentuk warna merah lembayung. Dihitung volume KOH yang digunakan untuk menitrasi sampel dan dihitung bilangan asam dengan menggunakan rumus :
VKOH.NKOH Bilangan Asam =
Massa sampel (gram)
3.3.6.5 Uji HLB (Hydrophilic Lipophilic Balance)
Analisis ini dilakukan terhadap metil ester asam lemak dari minyak jarak dan 9,10,12-trihidroksi metil stearat campuran.Harga HLB dapat diperoleh dari bilangan asam dan bilangan penyabunan dari senyawa ester dengan menggunakan rumus :
HLB = 20 (1-S/A)
Dimana : S = Bilangan penyabunan senyawa ester A = Bilangan asam senyawa ester
3.3.6.6 Penentuan Tegangan Permukaan.
Analisis ini dilakukan sabun natrium asam lemak dari minyak jarak dan sabun natrium 9,10,12-trihidroksi stearat campuran.
Ke dalam labu takar, dilarutkan sabun dengan akuades dengan kadar (%) 0,02;
0,04; 0,06; 0,08; 0,09; 0,1; 0,12; 0,14; 0,15; 0,18 dan 0,2. Alat tensiometer dikalibrasi pada suhu 30
.56,1
oC, menggunakan akuades (tegangan permukaan = 72.75 dyne/cm, suhu 30oC). Kemudian diukur tegangan permukaan dari masing-masing larutan sabun.
Selanjutnya ditetapkan harga sebenarnya dengan menggunakan faktor koreksi.
Kemudian dimasukkan harga-harga tegangan permukaan tersebut ke dalam kurva tegangan permukaan Vs Konsentrasi larutan sabun. Melalui kurva akan diperoleh harga CMC dari larutan sabun.
3.3.6.7 Analisis Alkalinitas Bebas
Analisis ini dilakukan untuk sabun natrium stearat dan sabun natrium asam lemak dari minyak jarak dan sabun natrium 9,10,12-trihidroksi stearat campuran.
Sebanyak 5 gram sabun dilarutkan dalam 100 mL alkohol netral panas dan ditambahkan 20 ml larutan BaCl2 10%. Ditambah 4 tetes indikator fenolftalein.
Warna merah muda dari larutan menunjukkan adanya alkali bebas. Larutan dititrasi dengan HCl 0,1 N sampai warna merah muda hilang. Alkalinitas bebas dapat dihitung dengan :
% Alkalinitas bebas = (0,4 V) / W
Dimana: V = Volume dari HCl 0,1 N (mL) W = Berat Sampel (gram)
3.3.6.8 Uji Kekuatan dan Stabilitas Busa
Analisis ini dilakukan untuk sabun natrium stearat dan sabun natrium asam lemak dari minyak jarak dan sabun natrium 9,10,12-trihidroksi stearat campuran.
Sebanyak 50 ml larutan sabun 0,2%; 0,4%; 0,6%; 0,8% dan 1% dimasukkan ke dalam gelas ukur 100 mL lalu ditutup. Larutan dikocok selama 30 detik dengan menggunakan alat shaker. Volume busa dicatat setelah 30 detik (Vo) dan 3 menit (Vs). Stabilitas busa ditunjukkan sebagai perbandingan (rasio) dari volume busa pada 3 menit dan 30 detik.
3.4 Bagan Penelitian
3.4.1 Ekstraksi minyak jarak dari biji jarak (Ricinus communis Linn)
Dikeringkan Dihaluskan
Dimaserasi dengan 2-propanol selama ± 2 hari
Disaring
Dikeringkan dengan Na2SO4
Disaring
anhidrous
Dirotarievaporasi
Serbuk jarak
Filtrat Residu
Filtrat Residu
Minyak jarak
Biji Jarak
3.4.2 Pembuatan Metil Ester Asam Lemak Campuran dari Minyak Jarak
Dimasukkan ke dalam labu alas Ditambah 50 mL metanol Ditambah 100 mL benzena Diaduk dan diteteskan 2 mL
H2SO4(p)
Direfluks pada suhu 80o
Dirotarievaporasi pada suhu 80 C selama 5 jam
o
C
Diekstraksi dengan 100 mL n-Heksana
Dicuci dengan 25 mL akuades sebanyak 2 kali
Dikeringkan dengan Na2SO4 Disaring
anhidrous
Dirotarievaporasi
100 mL Minyak Jarak
Campuran
Residu Pelarut
Lapisan Atas Lapisan Bawah
Filtrat Residu
Metil Ester Asam Lemak Campuran
Pelarut
Analisa FT-IR Penentuan Bilangan Iodin
Penentuan Bilangan Hidroksi
Uji HLB
3.4.3 Pembuatan 9,10,12-Trihidroksi Metil Stearat Campuran
Dimasukkan ke dalam labu leher tiga
Ditambahkan 30 mL H2O2
Ditambah 2 mL H
30%
setetes demi setetes
2SO4
Diaduk pada suhu 40-45 (p)
o
C selama 1 jam dan ditambah 30 mL metil ester minyak jarak campuran melalui corong penetes
Diaduk pada suhu 40-45o
Didiamkan selama 1 malam C selama 1 jam
Dirotarievaporasi
Ditambah 100 mL dietil eter Dicuci dengan 25 mL akuades
Dikeringkan dengan Na2SO4 anhidrous dan disaring
Dirotarievaporasi
60 mL HCOOH 90%
Campuran
Residu HCOOH dan air
Analisa FT-IR
Penentuan Bilangan Iodin
Penentuan Bilangan Hidroksi
Uji HLB
Lapisan atas (eter) Lapisan Bawah
Filtrat Residu
Hasil
3.4.4 Pembuatan Sabun Natrium 9,10,12-Trihidroksi Stearat Campuran
Dimasukkan ke dalam labu alas Ditambah 5 gram NaOH dan 50 mL alkohol 96%
Direfluks sambil diaduk pada suhu 78o
C
Dimasukkan ke dalam larutan NaCl jenuh
Diaduk selama ± 15 menit Disaring
Dibilas dengan alkohol 70% dan dikeringkan di dalam oven pada suhu 105oC.
• Dilakukan perlakuan yang sama untuk pembuatan sabun natrium stearat dan sabun natrium dari minyak jarak
33,6 gram Trihidroksi Metil Stearat Campuran
Campuran
Hasil
Penentuan Alkalinitas
Bebas Penentuan
Tegangan Permukaan
Uji Kekuatan dan Stabilitas
Busa Produk
Residu (Padatan) Filtrat
Analisa FT-IR
3.4.5 Bagan Analisis
3.4.5.1 Analisis Bilangan Iodin
Dimasukkan ke dalam gelas erlenmeyer yang bertutup
Ditambah 20 mL sikloheksana dan diaduk sampai larut
Ditambah 25 mL larutan wijs, ditutup dan dikocok agar campuran benar- benar larut
Disimpan dalam ruang gelap selama
±30 menit
Ditambah 20 mL larutan KI 10% dan 150 mL air suling
Dititrasi dengan Na2S2O3
Ditambah1-2 mL indikator amilum 0,1 N sampai warna kuning pucat
Dititrasi kembali sampai warna biru hilang
Dicatat volume Na2S2O3 0,1 N
*Dilakukan terhadap senyawa metil ester asam lemak campuran dari minyak jarak dan senyawa 9,10,12-trihidroksi metil stearat campuran.
Sampel (± 0,5 gram)
Hasil
3.4.5.2 Analisis Bilangan Hidroksi
Dimasukkan ke dalam labu alas bulat Ditambah 5 mL reagen asetilasi (asetat anhidrida dalam pyridin)
Direfluks selama ± 1 jam pada suhu 95-1000
Diangkat dan didinginkan C
Ditambah 1 mL akuades Dipanaskan selama ± 10 menit Ditambah 5 mL alkohol netral
Dimasukkan kedalam gelas erlenmeyer Ditambah 3 tetes indikator fenolftalein Dititrasi dengan larutan KOH-alkohol 0,5 N
Dicatat volume KOH-alkohol 0,5 N
*Dilakukan terhadap senyawa metil ester asam lemak campuran dari minyak jarak dan senyawa 9,10,12-trihidroksi metil stearat campuran.
Hasil
Sampel ( ± 1 gram)
Campuran
Larutan merah muda
3.4.5.3 Analisis Bilangan Penyabunan
Dimasukkan ke dalam gelas erlenmeyer
Ditambah 25 mL KOH-alkohol 0,5N Direfluks selama 30 menit
Didinginkan
Ditambah 3 tetes indikator fenolftalein
Dititrasi dengan HCl 0,5 N
Dicatat volume HCl 0,5 N
*Dilakukan terhadap senyawa metil ester asam lemak campuran dari minyak jarak dan senyawa 9,10,12-trihidroksi metil stearat campuran.
Sampel (± 0,1 gram)
Larutan Merah Muda
Larutan Bening
Hasil
3.4.5.4 Analisis Bilangan Asam
Dimasukkan ke dalam gelas erlenmeyer
Ditambah 10 mL alkohol netral Dipanaskan selama 30 menit Didinginkan
Ditambah 3 tetes indikator fenolftalein
Dititrasi dengan KOH 0,02 N
Dicatat volume KOH 0,02 N
*Dilakukan terhadap senyawa metil ester asam lemak campuran dari minyak jarak dan senyawa 9,10,12-trihidroksi metil stearat campuran.
Sampel (± 0,1 gram)
Larutan Bening
Larutan Merah Muda
Hasil
3.4.5.5 Penentuan Tegangan Permukaan
Diencerkan dalam labu takar dengan konsentrasi (%) 0,02; 0,04; 0,06;
0,08; 0,09; 0,1; 0,12; 0,15; 0,18 dan 0,2 dengan menggunakan akuades Dikalibrasi alat tensiometer pada suhu 300
Diukur tegangan permukaan masing- masing
C
• Dilakukan perlakuan yang sama untuk sabun natrium stearat dan sabun natrium asam lemak dari minyak jarak
Sampel
Hasil
3.4.5.6 Analisis Alkalinitas Bebas
Dilarutkan dengan 100 mL alkohol netral panas
Ditambah 20 mL larutan BaCl2
Ditambah 3 tetes indikator fenolftalein
10%
Dititrasi dengan HCl 0,1 N
Dicatat volume HCl 0,1 N
• Dilakukan perlakuan yang sama untuk sabun natrium stearat dan sabun natrium asam lemak dari minyak jarak
Sampel (± 5 gram)
Larutan Merah Muda
Larutan Bening
Hasil
3.4.5.7 Uji Kekuatan dan Stabilitas Busa
Dibuat konsentrasi (%) 0,2; 0,4; 0,6;
0,8; 1 dan diencerkan dalam labu takar dengan menggunakan akuades Ditutup dengan plastik dan dikocok dengan menggunakan alat shaker Diukur volume busa yang dihasilkan masing-masing setelah 30 detik (Vo) dan 3 menit (Vs)
• Dilakukan perlakuan yang sama untuk sabun natrium stearat dan sabun natrium asam lemak dari minyak jarak
Sampel
Hasil
BAB 4
HASIL DAN PEMBAHASAN
4.1 Hasil
Minyak jarak yang digunakan dalam penelitian ini diperoleh secara ekstraksi maserasi menggunakan pelarut 2-propanol. Dari 500 gram biji jarak halus diperoleh minyak jarak sebanyak 245 gram (49%). Selanjutnya minyak jarak diinteresterifikasi dengan metanol menggunakan katalis asam H2SO4 dan pelarut Benzena sehingga dihasilkan metil ester asam lemak campuran dengan rendemen sebesar 89%.
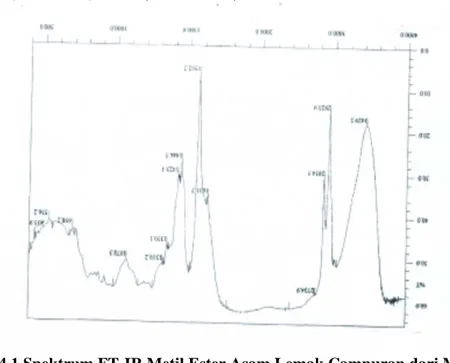
Metil risinoleat merupakan komposisi utama metil ester asam lemak campuran dari minyak jarak disamping metil ester asam lemak lainnya yakni metil oleat, linolenat, linoleat dan stearat dalam jumlah yang kecil. Senyawa metil ester asam lemak campuran ini dianalisis dengan menggunakan spektrofotometer FT-IR dan diperoleh spektrum yang memberikan puncak-puncak di daerah bilangan gelombang 3444,6 cm-1, 3000,8 cm-1, 2927,7 - 2854,5 cm-1, 1743 cm-1, 1651,0 cm-1, 1458,1 - 1438,8 cm-1, dan 1172,6 cm-1 (Gambar 4.1).
Gambar 4.1 Spektrum FT-IR Metil Ester Asam Lemak Campuran dari Minyak Jarak
Adapun analisis lain yang dilakukan yaitu analisis bilangan iodin, analisis bilangan hidroksi dan uji HLB (Hydrophylic Lipophylic Balance). Bilangan iodin untuk senyawa metil ester asam lemak campuran dari minyak jarak ialah sebesar 82,85 dan analisis bilangan hidroksi sebesar 221,51 serta nilai HLB untuk senyawa metil ester asam lemak campuran dari minyak jarak yang diperoleh sebesar 11,44.
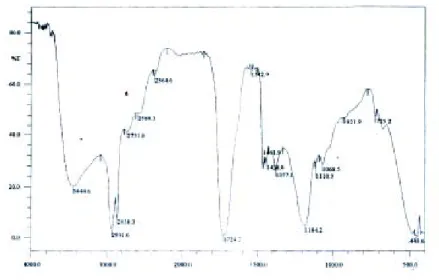
Epoksida ikatan rangkap pada atom C9 dan C10 dari senyawa metil risinoleat yang merupakan komposisi utama metil ester asam lemak dari minyak jarak, dengan cara mereaksikannya dengan campuran HCOOH 90% dan H2O2 30% dan diikuti dengan proses hidrolisis sehingga dihasilkan senyawa 9,10,12-trihidroksi metil stearat campuran dengan rendemen sebesar 83%. Asam formiat dan hidrogen hidroksida direaksikan akan membentuk senyawa perasid pada suhu 40-45oC yang selanjutnya diikuti penambahan metil ester asam lemak campuran dari minyak jarak, dan karena adanya air akan menyebabkan reaksi hidrolisis pada cincin epoksida. Dari hasil analisis senyawa 9,10,12-trihidroksi metil stearat dengan menggunakan spektrofotometer FT-IR diperoleh puncak-puncak serapan pada daerah bilangan gelombang 3444,6 cm-1, 2931,6 - 2858 cm-1, 1724,2 cm-1, 1461,9 - 1438,8 cm-1,1184,2 cm-1
Gambar 4.2 Spektrum FT-IR Senyawa 9,10,12-Trihidroksi Metil Stearat Campuran (Gambar 4.2).
Analisis lain yang dilakukan yaitu analisis bilangan iodin, analisis bilangan hidroksi dan penentuan HLB (Hydrophylic Lipophylic Balance). Bilangan iodin untuk
senyawa 9,10,12-trihidroksi metil stearat adalah sebesar 38,54 dan analisis bilangan hidroksi dari senyawa 9,10,12-trihidroksi metil stearat adalah sebesar 347,33 serta nilai HLB untuk senyawa 9,10,12-trihidroksi metil stearat ialah sebesar 15,18.
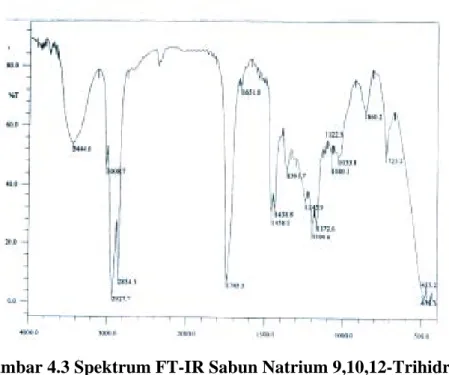
Reaksi penyabunan 9,10,12-trihidroksi metil stearat campuran dengan larutan basa kuat NaOH dan pelarut alkohol akan menghasilkan sabun natrium 9,10,12- trihidroksi stearat campuran sebagai komponen utama. Dari hasil analisis dengan menggunakan spektrofotometer FT-IR diperoleh puncak-puncak serapan pada daerah bilangan gelombang 3429,2 cm-1, 2923,9 – 2854,5 cm-1, 1446,5 – 1423,4 cm-1, 1631 cm-1
Gambar 4.3 Spektrum FT-IR Sabun Natrium 9,10,12-Trihidroksi Stearat Campuran
Analisis lain yang dilakukan untuk mengetahui karakteristik sabun natrium 9,10,12-trihidroksi stearat campuran yang diperoleh ialah penentuan alkalinitas bebas, uji tegangan permukaan dan uji kekuatan dan stabilitas busa. Analisis sabun ini juga didukung dengan melakukan uji yang sama terhadap sabun natrium asam lemak dari minyak jarak dan sabun natrium stearat. Alkalinitas bebas sabun natrium 9,10,12- trihidroksi campuran dari minyak jarak diperoleh sebesar 0,2%, alkalinitas bebas sabun natrium asam lemak dari minyak jarak adalah sebesar 0,28% dan alkalinitas sabun natrium stearat adalah sebesar 0,25%.
(Gambar 4.3).
Uji tegangan permukaan yang dilakukan dengan menggunakan tensiometer metode cincin Du-nuoy untuk sabun natrium 9,10,12-trihidroksi metil stearat campuran diperoleh sebesar 34,5 dyne/cm dengan titik konsentrasi misel kritis (CMC) ialah 0,1 %. Sabun natrium asam lemak dari minyak jarak yang diukur memiliki tegangan permukaan sebesar 36,68 dyne/cm dengan titik konsentrasi misel kritis (CMC) ialah 0,09%. Sabun natrium stearat sulit diukur tegangan permukaannya.
Data hasil uji kekuatan dan stabilitas busa yang diperoleh dapat dilihat pada tabel sebagai berikut:
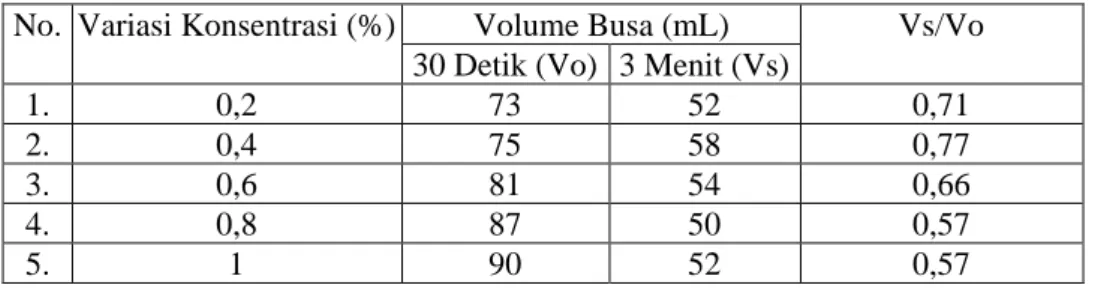
Tabel 4.1 Data Hasil Uji Kekuatan dan Stabilitas Busa Sabun Natrium 9,10,12-Trihidroksi Stearat Campuran dari Minyak Jarak
No. Variasi Konsentrasi (%) Volume Busa (mL) Vs/Vo 30 Detik (Vo) 3 Menit (Vs)
1. 0,2 73 52 0,71
2. 0,4 75 58 0,77
3. 0,6 81 54 0,66
4. 0,8 87 50 0,57
5. 1 90 52 0,57
Tabel 4.2 Data Hasil Uji Kekuatan dan Stabilitas Busa Sabun Natrium Asam Lemak dari Minyak Jarak
No. Variasi Konsentrasi (%) Volume Busa (mL) Vs/Vo
30 Detik (Vo) 3 Menit (Vs)
1. 0,2 70 35 0,5
2. 0,4 72 36 0,5
3. 0,6 75 35 0,46
4. 0,8 82 33 0,4
5. 1 86 34 0,39
Tabel 4.3 Data Hasil Uji Kekuatan dan Stabilitas Busa Sabun Natrium Stearat No. Variasi Konsentrasi (%) Volume Busa (mL) Vs/Vo
30 Detik (Vo) 3 Menit (Vs)
1. 0,2 65 53 0,81
2. 0,4 67 55 0,82
3. 0,6 70 61 0,87
4. 0,8 76 65 0,85
5. 1 77 69 0,89
Keterangan : Vo = Volume Busa pada saat 30 detik Vs = Volume Busa setelah 3 menit
Data hasil penentuan tegangan permukaan yang diperoleh dapat dilihat pada tabel sebagai berikut:
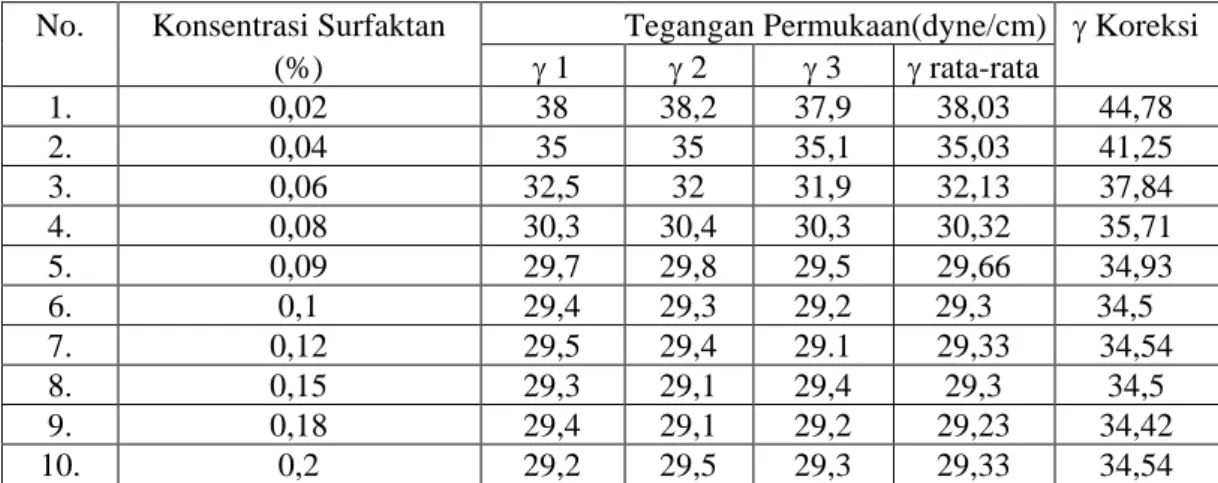
Tabel 4.4 Data Hasil Penentuan Tegangan Permukaan (γ) Sabun Natrium 9,10,12-Trihidroksi Stearat Campuran dari Minyak Jarak
No. Konsentrasi Surfaktan Tegangan Permukaan(dyne/cm) γ Koreksi
(%) γ 1 γ 2 γ 3 γ rata-rata
1. 0,02 38 38,2 37,9 38,03 44,78
2. 0,04 35 35 35,1 35,03 41,25
3. 0,06 32,5 32 31,9 32,13 37,84
4. 0,08 30,3 30,4 30,3 30,32 35,71
5. 0,09 29,7 29,8 29,5 29,66 34,93
6. 0,1 29,4 29,3 29,2 29,3 34,5
7. 0,12 29,5 29,4 29.1 29,33 34,54
8. 0,15 29,3 29,1 29,4 29,3 34,5
9. 0,18 29,4 29,1 29,2 29,23 34,42
10. 0,2 29,2 29,5 29,3 29,33 34,54
Faktor Koreksi : 1,1776
Tabel 4.5 Data Hasil Penentuan Tegangan Permukaan (γ) Sabun Natrium Asam Lemak dari Minyak Jarak
No. Konsentrasi Surfaktan Tegangan Permukaan (dyne/cm) γ.Koreksi
(%) γ 1 γ 2 γ 3 γ rata-rata
1. 0,02 40,1 40,3 40,4 40,26 47,4
2. 0,04 38,8 38,9 39,4 39,03 45,96
3. 0,06 35,4 35,6 35,7 35,56 41,87
4. 0,08 31,6 31,8 31,5 31,63 37,25
5. 0,09 31,2 31,1 31,2 31,15 36,68
6. 0,1 31,4 31,1 31 31,16 36,7
7. 0,12 31,5 31 30,9 31,13 36,66
8. 0,15 31,4 31,1 31 31,16 36,7 9. 0,18 31 31 31,4 31,13 36,66
10. 0,2 31,1 31,2 31,2 31,15 36,68
Faktor Koreksi : 1,1776
H3C (CH2)5 H C OH
CH2 CH CH (CH2)7 C O
OCH3
Metil risinoleat O
O C
O R2
C O
R1
O C O
R3
+ 3 CH3OH
OH
HO
OH +
R1 C O
OCH3
R2 C O
OCH3
R3 C O
OCH3 H+
Trigliserida Metanol Gliserol Metil Ester Asam Lemak Campuran
4.2 Pembahasan
Minyak jarak yang diperoleh dengan cara maserasi dengan menggunakan pelarut 2-propanol. Minyak jarak dimetanolisis secara refluks menggunakan katalis H2SO4 dan pelarut benzena pada suhu 80o
Metil risinoleat ialah komposisi terbesar (utama) yang terdapat dalam metil ester asam lemak campuran dari minyak jarak. Metil risinoleat merupakan ester dari asam lemak tidak jenuh yang memiliki gugus -OH pada atom C
C diharapkan membentuk metil ester asam lemak campuran dari minyak jarak dengan reaksi sebagai berikut :
12 sehingga ester dari asam lemak ini bersifat lebih polar dibandingkan asam lemak lainnya.
Spektrum FT-IR metil ester asam lemak campuran dari minyak jarak (Gambar 4.1) menunjukkan puncak serapan pada daerah bilangan gelombang 3444,6 cm-1 yang merupakan serapan khas untuk gugus hidroksil (-OH), pada bilangan gelombang 3008,7 cm-1 merupakan puncak serapan untuk CH sp2 dari gugus –CH=CH-, dan didukung dengan serapan pada bilangan gelombang 1651,0 cm-1 yang merupakan serapan khas dari ikatan C=C. Pada bilangan gelombang 1743,5 cm-1 merupakan serapan khas dari gugus karbonil (C=O) dari ester dan didukung dengan puncak vibrasi -C-O-C- pada daerah bilangan gelombang 1172,6 cm-1,sehingga dapat disimpulkan adanya gugus ester. Pada daerah bilangan gelombang 2927,7-2854,5cm-1
H C O
OH + H2O2 H C
O
O OH + H2O H+
H3C (CH2)5H C OH
CH2 CH CH (CH2)7C O
OCH3 + H C
O
OOH Hidrolisis
H3C (CH2)5H C OH
CH2 H
C H
C (CH2)7C O
OCH3
OH OH
H C O + OH
9,10,12-Trihidroksi Metil Stearat
menunjukkan adanya vibrasi stretching dari CH sp3 yang didukung vibrasi bending CH sp3 pada bilangan gelombang 1458,1-1438,8 cm-1.
Kemudian metil ester asam lemak campuran dari minyak jarak yang memiliki metil risinoleat sebagai komposisi utama diepoksidasi dengan campuran HCOOH 90% dan H2O2 30% dan dilanjutkan dengan hidrolisis dengan reaksi sebagai berikut :
Disamping senyawa 9,10,12-trihidroksi metil stearat yang terbentuk sesuai dengan adanya campuran asam lemak lain, juga dalam hal ini terbentuk hidroksi stearat dari senyawa metil oleat, linoleat dan linolenat dalam jumlah yang kecil.
Senyawa 9,10,12-trihidroksi metil stearat campuran yang diperoleh ini dianalisis dengan spektrofotometer FT-IR (gambar 4.2) menunjukkan puncak serapan pada daerah bilangan gelombang 3444,6 cm-1 yang merupakan serapan khas dari gugus hidroksi (OH). Pada daerah ini puncak serapan semakin melebar karena sebelum diepoksida hanya memiliki 1 gugus hidroksi dan setelah diepoksida yang dilanjutkan hidrolisis maka gugus hidroksi bertambah menjadi 3 buah. Pada bilangan gelombang 2931,6- 2838,3 cm-1 menunjukkan serapan khas dari vibrasi stretching CH sp3 dan pada daerah bilangan gelombang 1461,9-1438,8 cm-1 menunjukkan serapan khas dari vibrasi bending CH sp3. Pada bilangan gelombang 1724,2 cm-1 menunjukkan serapan khas gugus karbonil (C=O) dan bilangan gelombang 1184,2 cm-1menunjukkan serapan khas dari gugus C-O-C sehingga menunjukkan adanya gugus ester.
H3C (CH2)5 H C OH
CH2 H
C H
C (CH2)7C O
O- Na+ OH OH
Sabun Natrium 9,10,12-TrihidroksiStearat
Analisis bilangan iodin dari metil ester asam lemak campuran dari minyak jarak yaitu sebesar 82,85 dan 9,10,12-trihidroksi metil stearat yaitu sebesar 38,54 menunjukkan adanya penurunan jumlah ikatan rangkap maka ada terjadinya reaksi oksidasi terhadap ikatan rangkap pada senyawa metil risinoleat. Dan analisis bilangan hidroksi dari senyawa metil ester asam lemak campuran dari minyak jarak yaitu sebesar 221,51 dan senyawa 9,10,12-trihidroksi metil stearat yaitu sebesar 347,33 menunjukkan adanya kenaikan gugus hidroksi maka dapat dikatakan adanya terjadi reaksi epoksidasi yang diikuti reaksi hidrolisis pada senyawa metil risinoleat. Uji HLB yang dilakukan terhadap senyawa metil ester asam lemak campuran dari minyak jarak diperoleh sebesar 11,44 dan HLB dari senyawa 9,10,12-trihidroksi metil stearat diperoleh sebesar 15,18 menunjukkan adanya kenaikan nilai HLB maka senyawa 9,10,12-trihidroksi metil stearat campuran bersifat semakin hidrofil.
Selanjutnya senyawa 9,10,12-trihidroksi metil stearat campuran yang diperoleh disafonifikasi dengan menggunakan basa kuat yaitu NaOH dan diendapkan dengan menggunakan garam NaCl sehingga diperoleh sabun natrium 9,10,12- trihidroksi stearat sebagai komposisi utama yang kemungkinan sebesar 87,5 %, natrium oleat sebesar 5%, natrium linoleat sebesar 4%, natrium palmitat sebesar 1,5%, natrium stearat sebesar 0,5 % dan natrium linolenat sebesar 0,5%.
Sabun natrium 9,10,12-trihidroksi stearat campuran selanjutnya dianalisis dengan menggunakan spektrofotometer FT-IR (gambar 4.3) menunjukkan puncak serapan pada bilangan gelombang 3429 cm-1 yang merupakan serapan khas gugus hidroksil (OH). Pada bilangan gelombang 2923,9 – 2854,5 cm-1 menunjukkan serapan khas dari vibrasi stretching CH sp3 dan bilangan gelombang 1446,5 – 1423,4 cm-1 menunjukkan serapan khas dari vibrasi bending CH sp3. Pada bilangan gelombang 1631,7 cm-1 menunjukkan serapan khas gugus karbonil (C=O) untuk senyawa garam karboksilat.
CH C
H (CH2)7 CH2
HC OH (H2C)5
H3C C ONa
O
Sabun Natrium Asam Lemak dari Minyak Jarak
H3C (CH2)16 C O
ONa Sabun Natrium Stearat
Selanjutnya sabun natrium 9,10,12-trihidroksi stearat campuran dibandingkan dengan sabun natrium stearat dan sabun natrium asam lemak dari minyak jarak dalam analisis alkalinitas bebas, uji tegangan permukaan dan uji kekuatan dan stabilitas busa dimana struktur dari kedua jenis sabun ini adalah sebagai berikut :
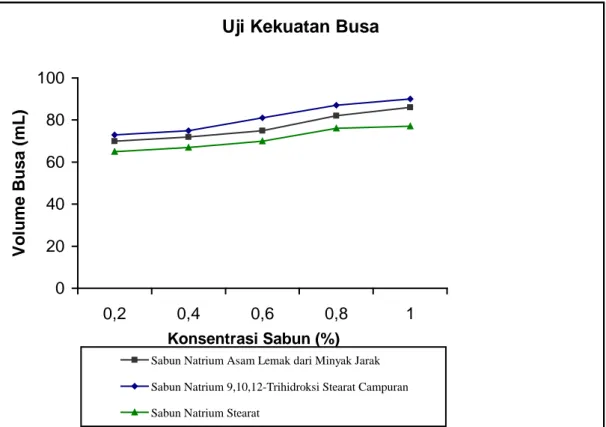
Pada uji kekuatan dan stabilitas busa, sabun dibuat menjadi 5 konsentrasi, kemudian dikocok dengan menggunakan alat shaker dan diukur volume busa yang diperoleh setelah 30 detik dan 3 menit, sehingga diperoleh hasil untuk sabun natrium 9,10,12-trihidroksi stearat campuran (tabel 4.1), sabun natrium asam lemak dari minyak jarak (tabel 4.2) dan sabun natrium stearat (tabel 4.3). Dari ketiga data, diperoleh hasil kekuatan busa dari sabun natrium 9,10,12-trihidroksi stearat campuran lebih besar dibandingkan sabun natrium asam lemak dari minyak jarak dan sabun natrium stearat (grafik 4.1). Hal ini mengambarkan bahwa adanya gugus hidroksil pada sabun natrium 9,10,12-trihidroksi stearat dapat meningkatkan kekuatan busa.
Pada uji stabilitas diperoleh hasil dimana sabun natrium stearat lebih baik stabilitasnya dibandingkan sabun natrium asam lemak dari minyak jarak dan sabun natrium 9,10,12-trihidroksi stearat campuran (grafik 4.2). Hal ini juga disebabkan kepolaran sabun natrium 9,10,12-trihidroksi stearat campuran ini lebih hidrofil sehingga stabilitas lebih rendah dibandingkan natrium stearat. Pada tabel hasil uji kekuatan dan stabilitas busa diperoleh data yang tidak teratur, hal ini dipengaruhi oleh stabilitas busa yang diperoleh.
Uji Kekuatan Busa
0 20 40 60 80 100
0,2 0,4 0,6 0,8 1
Konsentrasi Sabun (%)
Volume Busa (mL)
Sabun Natrium Asam Lemak dari Minyak Jarak Sabun Natrium 9,10,12-Trihidroksi Stearat Campuran Sabun Natrium Stearat
Grafik 4.1 Grafik Hasil Uji Kekuatan Busa
Uji Stabilitas Busa
0 0,2 0,4 0,6 0,8 1
0,2 0,4 0,6 0,8 1
Konsentrasi Sabun (%)
( Vs/Vo )
Sabun Natrium 9,10,12-Trihidroksi Stearat Campuran
Sabun Natrium Asam Lemak dari Minyak Jarak
Sabun Natrium Stearat
Grafik 4.2 Grafik Hasil Uji Stabilitas Busa
Pada analisis alkalinitas bebas sabun natrium 9,10,12-trihidroksi stearat campuran diperoleh kadar alkalinitas sebesar 0,2 %, sabun natrium asam lemak dari minyak jarak diperoleh sebesar 0,28 % dan sabun natrium stearat diperoleh sebesar 0,25 %.
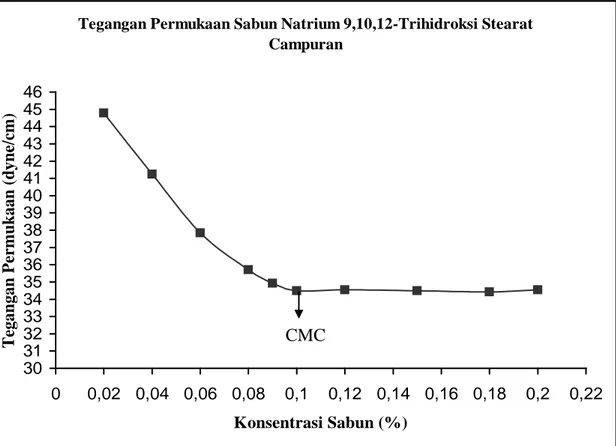
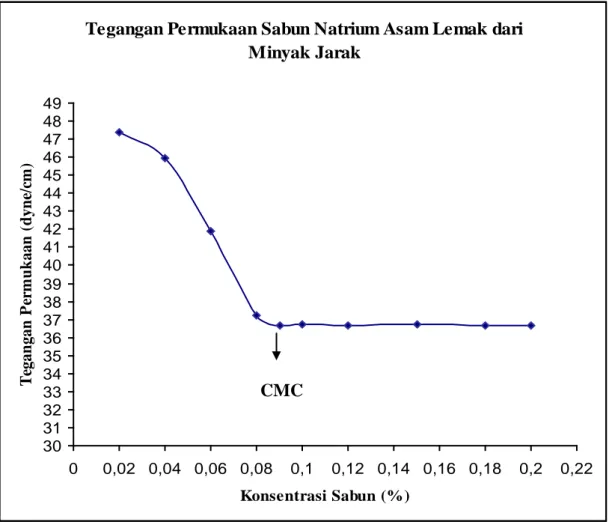
Pada hasil analisis penentuan tegangan permukaan untuk sabun natrium 9,10,12-trihidroksi stearat campuran (tabel 4.4) dan sabun natrium asam lemak dari minyak jarak (tabel 4.5) maka diperoleh hasil dimana titik CMC untuk sabun natrium 9,10,12-trihidroksi stearat campuran berada pada konsentrasi 0,1 % dan diperoleh tegangan permukaan sebesar 34,5 dyne/cm (grafik 4.3). Dan untuk sabun natrium asam lemak dari minyak jarak, titik CMC berada pada konsentrasi 0,09 % dan diperoleh tegangan permukaan sebesar 36,68 dyne/cm (grafik 4.4). Lebih rendahnya tegangan permukaan sabun natrium 9,10,12-trihidroksi stearat campuran dibandingkan sabun natrium asam lemak dari minyak jarak, maka makin mudah sabun tersebut untuk membasahi benda sehingga meningkatkan kemampuan untuk membersihkan kotoran.
Grafik 4.3 Grafik Hasil Penentuan Tegangan Permukaan CMC
Tegangan Permukaan Sabun Natrium 9,10,12-Trihidroksi Stearat Campuran
30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46
0 0,02 0,04 0,06 0,08 0,1 0,12 0,14 0,16 0,18 0,2 0,22 Konsentrasi Sabun (%)
Tegangan Permukaan (dyne/cm)
CMC
Grafik 4.4 Grafik Hasil Penentuan Tegangan Permukaan.
Tegangan Permukaan Sabun Natrium Asam Lemak dari Minyak Jarak
30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49
0 0,02 0,04 0,06 0,08 0,1 0,12 0,14 0,16 0,18 0,2 0,22 Konsentrasi Sabun (%)
Tegangan Permukaan (dyne/cm)
CMC
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Hal yang dapat disimpulkan dari penelitian ini adalah:
1. Sabun natrium 9,10,12-trihidroksi stearat yang berupa campuran dapat diturunkan dari minyak jarak melalui reaksi metanolisis, epoksidasi yang diikuti reaksi hidrolisis dengan HCOOH/H2O2
2. Hasil pemeriksaan spektrum FT-IR memberikan dukungan bahwa hasil metanolisis minyak jarak adalah metil ester asam lemak campuran, dan hasil epoksidasi yang dilanjutkan hidrolisis adalah senyawa 9,10,12-trihidroksi metil stearat campuran.
dan dilanjutkan safonifikasi dengan NaOH
3. Harga HLB yang ditentukan melalui metode titrasi diperoleh sebesar 11,44 untuk metil ester asam lemak campuran dari asam lemak dan harga HLB untuk senyawa 9,10,12-trihidroksi metil stearat campuran dari minyak jarak adalah sebesar 15,18.
4. Sifat-sifat dari sabun natrium 9,10,12-trihidroksi stearat campuran dari minyak jarak ialah :
- Titik konsentrasi misel kritis (CMC) berada pada konsentrasi 0,1 % - Tegangan Permukaan sebesar 34,5 dyne/cm
- Memiliki kekuatan busa lebih baik dibandingkan sabun natrium asam lemak campuran dari minyak jarak dan sabun natrium stearat
- Memiliki alkalinitas bebas sebesar 0,2%.
5.2 Saran
Diharapkan kepada peneliti berikutnya supaya lebih mengembangkan senyawa trihidroksi metil stearat untuk uji deterjen, biodegradasi dan uji sifatnya terhadap air sadah.