LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan di bawah ini, saya mahasiswa Universitas Sanata Dharma :
Nama : Danu Kusuma
Nomor mahasiswa : 028114047
Demi pengembangan ilmu pengetahuan, saya memberikan kepada perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul :
Uji Angka Lempeng Total (ALT) dalamJamu Gendong Beras Kencuryang Beredar di Tiga Pasar Tradisional di Kotamadya Yogyakarta
Beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan kepada perpustakaan Universitas Sanata Dharma hak untuk menyimpan, mengalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikannya secara terbatas, dan mempublikasikannya di Internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalti kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini saya buat dengan sebenarnya.
Yogyakarta, 11 Februari 2008 Yang menyatakan
UJI ANGKA LEMPENG TOTAL (ALT) DALAM JAMU GENDONG BERAS KENCUR YANG BEREDAR DI TIGA PASAR DI KOTAMADYA
YOGYAKARTA
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh: Danu Kusuma NIM : 028114047
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
iv
Bermimpilah tentang apa yang ingin kamu impikan, pergilah ke tempat-tempat kamu ingin pergi.
Jadilah seperti yang kamu inginkan,
karena kamu hanya memiliki satu kehidupan dan satu kesempatan untuk melakukan hal-hal yang ingin kamu lakukan.
Masa depan yang cerah berdasarkan pada masa lalu yang telah dilupakan. Kamu tidak dapat melangkah dengan baik dalam kehidupanmu
sampai kamu melupakan kegagalanmu dan rasa sakit hati. Doa memberikan kekuatan pada orang yang lemah,
membuat orang tidak percaya menjadi percaya dan memberikan keberanian
pada orang yang ketakutan Janganlah berputus asa. Tetapi kalau anda sampai berada dalam keadaan putus asa,
berjuanglah terus meskipun dalam keadaan putus asa.
P
P
e
e
r
r
s
s
e
e
m
m
b
b
a
a
h
h
a
a
n
n
k
k
e
e
p
p
a
a
d
d
a
a
M
M
a
a
m
m
a
a
,
,
P
P
a
a
p
p
a
a
,
,
A
A
j
j
e
e
n
n
g
g
d
d
a
a
n
n
“se
s
eorang” y
a
ng selalu me
n
ja
di
mo
t
iv
a
si
T
v PRAKATA
Puji syukur kepada Tuhan Yang Maha Kasih atas berkat dan kuasa-Nya, sehingga penulis dapat menyelesaikan skripsi yang berjudul : “Uji Angka Lempeng Total Jamu dalam Gendong Beras Kencur yang Beredar di Tiga Pasar Tradisional di Kotamadya Yogyakarta.” Skripsi ini disusun untuk memenuhi salah satu syarat memperoleh gelar Sarjana Farmasi (S.Farm) di Fakultas Farmasi Universitas Sanata Dharma.
Dalam menyelesaikan penelitian ini, penulis telah menerima banyak bantuan dari berbagai pihak, baik berupa bimbingan, saran, dukungan, dan kritikan. Penulis ingin menyampaikan ucapan terima kasih kepada:
1. Yustina Sri Hartini M.Si., Apt., selaku dosen pembimbing yang telah memberikan bimbingan, pengarahan, dan saran hingga terselesaikannya skripsi ini.
2. Rita Suhadi, M.Si., Apt., selaku Dekan Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
3. Bapak Yohanes Dwiatmaka, M.Si, selaku dosen penguji skripsi yang telah memberikan saran, kritik, dan bimbingan.
4. Ibu Maria Dwi Budi Jumpowati, S. Si, selaku dosen penguji skripsi yang telah memberikan saran, kritik, dan bimbingan.
vi
6. Mbak Has dan seluruh staf Laboratorium Mikrobiologi Balai Besar POM Yogyakarta atas bimbingan dan kerjasamanya.
7. Seluruh staf Laboratorium Farmasi Universitas Sanata Dharma atas bimbingan dan saran.
8. Teman-teman kelompok penelitian : Agustinus Daru, dan Theodorus Haryu, atas kerjasama, bantuan, dukungan, dan saran selama penelitian dan penyusunan skripsi ini.
9. Teman-teman, atas persahabatan, bantuan, dukungan, dan kerjasama selama penulis menempuh kuliah.
10. Semua pihak yang tidak dapat disebutkan satu persatu yang telah banyak membantu dalam penyelesaian penelitian ini.
Akhir kata, “tidak ada gading yang tak retak”, penulis menyadari bahwa
penelitian ini masih banyak kekurangannya. Oleh karena itu, penulis mengharapkan kritik dan saran yang membangun demi kesempurnaan skripsi ini dari para pembaca. Semoga skripsi ini bermanfaat bagi pembaca dan ilmu pengetahuan.
vii INTISARI
Jamu gendong merupakan salah satu jamu dalam bentuk cairan minum yang sangat digemari masyarakat. Departemen Kesehatan (Depkes) RI dalam Keputusan Menteri Kesehatan RI No : 55/Menkes/SK/I/2000 menyatakan bahwa obat tradisional harus memenuhi persyaratan mutu kefarmasian. Dengan persyaratan mutu tersebut dapat diharapkan adanya obat tradisional dengan dosis yang diketahui dan terulangkan, termasuk untuk keamanan dan kemanfaatannya. Salah satu parameter standar mutu bahan baku obat tradisional adalah uji Angka Lempeng Total, yang digunakan untuk menetapkan angka bakteri aerob mesofil dalam sediaan jamu gendong beras kencur.
Penelitian ini merupakan penelitian non eksperimental dengan rancangan penelitian deskriptif komparatif. Penelitian ini dilakukan untuk menghitung Angka Lempeng Total dalam jamu gendong beras kencur yang beredar di tiga pasar di wilayah kotamadya Yogyakarta, yaitu pasar Karangwaru, pasar Pingit, and pasar Kranggan.
Data yang diperoleh berupa data kuantitatif yang dianalisis dengan cara perhitungan Angka Lempeng Total. Angka Lempeng Total yang diperbolehkan berdasarkan Metode Analisis Pusat Pengujian Obat dan Makanan (PPOMN) Nomor 95/MIK/00 tidak lebih dari 104 koloni/mL. Dari data kuantitatif 5 sampel dan 3 kali replikasi yang dilakukan diperoleh jumlah koloni Sampel 1 = 14x104 koloni/mL; 82x104 koloni/mL; 74x104 koloni/mL, Sampel 2 = 13x103 koloni/mL; 14x105 koloni/mL; 14x103 koloni/mL, Sampel 3 = 13x106 koloni/mL; 66x106 koloni/mL; 89x106 koloni/mL, Sampel 4 = 64x103 koloni/mL; 33x103 koloni/mL; 99x103 koloni/mL, Sampel 5 = 50x106koloni/mL; 25x104koloni/mL; 42x105koloni/mL.
Dari data di atas dapat disimpulkan bahwa jamu gendong beras kencur yang beredar di 3 pasar di kotamadya Yogyakarta tidak memenuhi syarat yang ditentukan oleh Departemen Kesehatan RI.
viii ABSTRACT
Jamu gendong is one of jamu in a diluted form which is most delighted. For reaching the requirement of traditional medicine which can be use in the medical service, The Departement of Health of Indonesian require a traditional medicine to fulfill the pharmacy quality requirement by passing the clinical testing phase. By implementating this quality requirement, it is expected that a traditional medicine in a defined dosage can be reproduced by considering its safety an efficacy are available. One of the parameter of standard of the quality of raw material for traditional medicine is this Total Plate Count, which used to count aerobic mesophilic bacteria in Jamu Gendong Beras Kencur.
This research was non experimental with descriptive and comparative research design. This research purpose was to count the Total Plate Count of Jamu gendong beras kencur which were distributed in Three Traditional Markets in Yogyakarta. There arepasar Karangwaru,pasar Pingit, andpasar Kranggan.
The obtained data was quantitative which were analyzed by applying the computation of the Total Plate Count. The Total Plate Count allowed by the Method of Analysis Center Examination of Drug and Food No. 95/MIK/00 not greater 104 colony / mL. From quantitative data of 5 sample and 3 times replication which were implementated it was found that : the amount of colony of Sample 1 = 14x104colony / mL; 82x104 colony / mL; 74x104 colony / mL, Sample 2 = 13x103 colony / mL; 14x105 colony / mL; 14x103 colony / mL, Sample 3 = 13x106 colony / mL; 66x106 colony / mL; 89x106 colony / mL, Sample 4 = 64x103colony / mL; 33x103colony / mL; colony 99x103/ mL, and Sample 5 = 50x106colony / mL; 25x104colony / mL; 42x105colony / mL
Based on the findings above, it can be concluded that Jamu gendong beras kencur which were Distributed in Three Traditional Markets in Yogyakarta not fulfill the Indonesian Departement of health requirement.
ix
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang saya tulis ini tidak memuat karya atau bagian karya orang lain, kecuali yang telah disebutkan dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Yogyakarta, 20 Januari 2008 Penulis
x DAFTAR ISI
HALAMAN JUDUL... i
HALAMAN PERSETUJUAN PEMBIMBING... ii
HALAMAN PENGESAHAN... iii
HALAMAN PERSEMBAHAN... iv
PRAKATA... v
INTISARI... vii
ABSTRACT... viii
PERNYATAAN KEASLIAN KARYA... ix
DAFTAR ISI... x
DAFTAR GAMBAR... xiii
DAFTAR TABEL... xiv
DAFTAR LAMPIRAN... xv
BAB I. PENDAHULUAN... 1
A. Latar Belakang ... 1
1. Permasalahan... 3
2. Keaslian Penelitian... 3
3. Manfaat Penelitian ... 4
a. Manfaat Teoritis... 4
b. Manfaat praktis ... 4
xi
BAB II. PENELAAHAN PUSTAKA... 5
A. Obat Tradisional ... 5
B. Jamu Gendong ... 6
C. Pengeringan ... 9
D. Sterilisasi ... 10
E. Media ... 14
F. Penghitungan Angka Lempeng Total (ALT) ... 17
G. Landasan Teori... 21
H. Hipotesis... 22
BAB III. METODOLOGI PENELITIAN... 23
A. Jenis dan Rancangan Penelitian ... 23
B. Variabel Penelitian dan Definisi Operasional ... 23
C. Subjek dan Bahan Penelitian... 24
D. Alat Penelitian... 24
E. Tata Cara Penelitian ... 25
1. Pengambilan Sampel ... 25
2. Persiapan dan Homogenisasi Sampel... 25
3. Cara Pembuatan Media ... 25
4. Uji Angka Lempeng Total ... 26
5. Perhitungan koloni ... 27
xii
BAB III. HASIL DAN PEMBAHASAN... 30
A. Pengumpulan Sampel Jamu Gendong Beras Kencur... 30
B. Sterlisasi Alat ... 32
C. Sterilisasi Media... 33
D. Homogenisasi Sampel ... 34
E. Pengenceran ... 35
F. Uji ALT... 35
BAB IV. KESIMPULAN DAN SARAN... 48
A. Kesimpulan ... 48
B. Saran... 48
DAFTAR PUSTAKA... 49
LAMPIRAN... 52
xiii
DAFTAR GAMBAR
1. Gambar Media Plate Count Agar (PCA) ... 38
2. Gambar Blanko standar PCA dan Letheen broth (LB) ... 40
3. Gambar Blanko standar PCA ... 41
4. Gambar Blanko standar PCA dan Pepton Dilution Fluid (PDF) ... 41
xiv
DAFTAR TABEL
Tabel I. Hasil Perhitungan ALT pada Pengambilan Sampel Periode Pertama dari 5 Penjual setelah Pengamatan 24 jam, dan Setelah 48 jam... 42 Tabel II. Hasil Perhitungan ALT pada Pengambilan Sampel Periode kedua dari
5 Penjual setelah Pengamatan 24 jam, dan Setelah 48 jam... 43 Tabel III. Hasil Perhitungan ALT pada Pengambilan Sampel Periode Ketiga
dari 5 Penjual setelah Pengamatan 24 jam, dan Setelah 48 jam ... 44 Tabel IV. Perhitungan Angka Lempeng Total Jamu Gendong dari 5 Produsen
xv
DAFTAR LAMPIRAN
BAB I
PENDAHULUAN
A . Latar Belakang
Masyarakat di Indonesia lazim menggunakan obat tradisional atau yang disebut jamu, dengan memanfaatkan kekayaan alam di Indonesia. Obat tradisional
perlu dikembangkan dan dimanfaatkan. Pengembangan obat tradisional perlu dilakukan dengan tepat sehingga keamanan dan khasiatnya secara medik dapat
dipertanggungjawabkan.
Jamu sudah dikenal di Indonesia khususnya di Jawa sebagai perawatan kesehatan sehari-hari, maupun sebagai sarana pemulih kesehatan bila sembuh dari
sakit, dengan demikian penggunaan jamu sejak dahulu kala bermanfaat untuk preventif, promotif, kuratif, dan rehabilitatif. Penggunaan jamu telah berakar
sedemikian kuatnya dalam masyarakat Indonesia dari dahulu hingga sekarang, meskipun sejak seabad yang lalu pendidikan kedokteran dengan obat-obatan modern telah dikenal di Indonesia. Menurut World Health Organization (WHO),
kira-kira 80% dari penduduk dunia yang berjumlah 4 miliar penduduk percaya manfaat tumbuh-tumbuhan untuk kesehatan dan kebugaran tubuh, dan masyarakat
modern pun akhirnya juga memakai bahan-bahan alam segar untuk suplemen, makanan, minuman, dan sarana kecantikan dan penampilan bagi pria dan wanita. Pada umumnya khasiat dari jamu tidak dapat langsung dirasakan. Cara kerjanya
Jamu gendong merupakan salah satu jamu dalam bentuk cairan minum yang sangat digemari masyarakat. Jamu gendong dijual dalam botol dan
diletakkan dalam keranjang yang digendong di punggung belakang menggunakan kain. Dalam Peraturan Menteri Kesehatan Republik Indonesia Nomor
246/Menkes/Per/V/1990 tentang izin usaha industri obat tradisional dan
pendaftaran obat tradisional pasal 3 ayat 1 bahwa “Obat tradisional yang
diproduksi, diedarkan di wilayah indonesia maupun diekspor terlebih dahulu
harus didaftarkan sebagai persetujuan Menteri”, dan ayat 2 “Dikecualikan dari ketentuan ayat (1) adalah obat tradisional hasil produksi : industri obat tradisional
dalam bentuk gendong, pilis, tapel, parem, usaha jamu racikan dan usaha jamu gendong. Berdasarkan peraturan tersebut sediaan jamu gendong beras kencur belum terdaftar dalam persetujuan Menteri, ini berarti standarisasi obat tradisional
jamu gendong beras kencur belum dilakukan sehingga jaminan keamanan untuk sediaan tersebut belum ada, dan perlu dilakukan pengujian mutu bahan baku obat
tradisional.
Salah satu parameter standar mutu bahan baku obat tradisional adalah uji cemaran mikroba dengan uji Angka Lempeng Total. Dalam Keputusan Menteri
Kesehatan RI Nomor : 661/Menkes/SK/VII/1994 Tentang persyaratan Obat tradisional, jamu gendong yang termasuk dalam cairan obat dalam mengandung
Angka Lempeng Total tidak lebih dari 104(Anonim, 2000).
Angka Lempeng Total (ALT) merupakan metode penghitungan jumlah mikroba hidup yang paling sensitif untuk menentukan mikroba karena beberapa
mikroba dapat dihitung sekaligus, dapat digunakan untuk isolasi dan identifikasi mikroba karena koloni yang terbentuk mungkin berasal dari suatu mikroba yang
mempunyai penampakan pertumbuhan spesifik (Fardiaz, 1992).
1. Permasalahan
a. Berapakah jumlah Angka Lempeng Total (ALT) pada jamu gendong yang beredar di tiga pasar di Kotamadya Yogyakarta?
b. Apakah jumlah cemaran mikroba pada jamu gendong yang beredar di pasar di kotamadya Yogyakarta melebihi batas yang telah ditentukan,
yaitu 104koloni/ml?
2. Keaslian Penelitian
Pada tahun 2005 pernah dilakukan pengujian cemaran bakteri dan cemaran kapang/khamir pada produk jamu gendong di Daerah Istimewa Yogyakarta oleh
Sylvia Tunjung Pratiwi (2005). Penelitian tentang pemeriksaan Angka Lempeng Total dalam jamu gendong Beras Kencur yang beredar di tiga pasar pada tahun 2007, belum pernah dilakukan.
3. Manfaat Penelitian
Manfaat yang diharapkan dari penelitian ini, meliputi :
b. Manfaat praktis : dapat memberikan data tentang pemeriksaan Angka Lempeng Total dalam jamu gendong yang beredar di Kotamadya
Yogyakarta.
B. Tujuan Penelitian
1. Tujuan umum : memberikan evaluasi bahwa pada jamu gendong tidak boleh mengandung Angka Lempeng Total melebihi batas yang ditetapkan
Departemen Kesehatan RI.
2. Tujuan khusus : untuk memeriksa jumlah Angka Lempeng Total dalam
BAB II
PENELAAHAN PUSTAKA
A. Obat Tradisional
Kecenderungan masyarakat untuk back to nature dengan indikasi utama peningkatan kebutuhan produk-produk konsumsi untuk kesehatan dari bahan alam merupakan peluang besar bagi pengembangan tanaman obat dan obat tradisional
Indonesia.
Obat Tradisional atau lebih dikenal dengan nama jamu atau obat asli
Indonesia (OAIN) sudah dikenal sejak zaman nenek moyang kita dan tumbuh berkembang sejalan dengan perkembangan yang terjadi di negara kita. Oleh karena itu, jamu merupakan warisan nenek moyang yang perlu dikembangkan
utamanya untuk menunjang upaya meningkatkan kesehatan masyarakat baik digunakan untuk ujuan pencegahan (preventif), peningkatan (promotif), maupun
pengbatan kuratif. Obat tradisional juga digunakan daam usaha perawatan kecantikan dan kosmetik.
Menurut Undang-Undang Republik Indonesia No. 23 tahun 1992 tentang
kesehatan, obat tradisional adalah bahan atau ramuan bahan yang berupa bahan tumbuhan, bahan hewan, bahan mineral, sediaan sarian (galenik) atau campuran
dari bahan tersebut yang secara turun temurun telah digunakan untuk pengobatan berdasarkan pengalaman (Anonim, 1994a).
Obat tradisional Indonesia yang telah menjadi bagian integral dari
pelayanan kesehatan. Untuk itu harus sesuai dengan kaidah pelayanan kesehatan yaitu secara medis harus dapat dipertanggungjawabkan. Guna mencapai hal itu
perlu dilakukan pengujian ilmiah tentang khasiat, keamanan dan standar kualitasnya (Soegihardjo,2002).
Tidak seperti produk farmasi konvensional, yang biasanya dapat dibuat dari bahan sintetis dengan teknik dan prosedur pembuatan yang dapat diproduksi ulang, produk obat herbal dibuat dari bahan tumbuhan asal yang dapat
terkontaminasi dan terurai, serta memiliki komposisi dan sifat yang bervariasi. Selain itu, dalam pembuatan dan pengawasan mutu produk herbal, prosedur dan
teknik yang sering digunakan memiliki perbedaan mendasar dari yang digunakan pada produk farmasi konvensional. Pengawasan bahan awal, penyimpanan, dan pengolahan dianggap sangat penting karena sifat banyak produk obat herbal yang
sering kompleks dan variabel serta jumlah dan kuantitas kecil dari penetapan bahan aktif yang terdapat di dalamnya (Anonim, 2007).
B. Jamu Gendong
Jamu gendong merupakan salah satu ramuan tradisional yang banyak
dikonsumsi oleh masyarakat Indonesia, digunakan baik untuk memelihara kesehatan, meningkatkan kesehatan mempertahankan kesehatan, ataupun
botol-botol berisi racikan obat tradisional tersandang dengan selendang lusuh di punggungnya ( Kodim, 2000 ).
Usaha jamu gendong adalah usaha peracikan pencampuran pengolahan dan pengedaran obat tradisional dalam bentuk cairan, pilis, parem, tapel, tanpa
penandaan dan atau merk dagang serta dijajakan untuk langsung digunakan. Penjual jamu gendong menjajakan dari pintu ke pintu dengan membawa jamu perasan, pilis dan parem. Sering kali juga membawa jamu dari pabrik.
Perbedaan jamu gendong dan jamu bagolan adalah jamu gendong menjual barang jadi, sedangkan jamu bagolan menjual barang setengah jadi, yaitu berupa ramuan
yang sudah ditumbuk kemudian diracik dengan menambah air matang, disaring, dan hasilnya siap diminum. Dalam rumah tangga pekerjaan jamu gendong sering dilakukan oleh ibu rumah tangga dengan skala yang lebih kecil untuk keperluan
sendiri dengan ramuan yang lebih sederhana. Sebagai alat penumbuk digunakan pipisan dan gandhik, yaitu alat penumbuk yang dibuat dari batu, disamping
digunakan lumping dan alu. Bahan baku ramuan jamu terdiri dari bahan segar dan bahan kering atau simplisia, yang diperoleh dari pedagang simplisia pasar (craken). Hingga kini jamu digunakan oleh penduduk pedesaan maupun
perkotaan. Dalam rumah tangga ibu-ibu sering membuat ramuan dengan tujuan untuk memelihara kebugaran dan kecantikan baik berupa minuman maupun
bedak, pilis, atau param (Soegihardjo,2002).
Penggunaan jamu gendong biasanya berdasarkan kebiasaan turun-temurun secara umum, sudah diketahui manfaat jamu gendong, namun secara tertulis
gendong lebih banyak sebagai upaya promotif dan preventif kesehatan (Handayani & Suharmiati, 2001).
Beberapa hal yang perlu diperhatikan agar produk jamu gendong yang dihasilkan aman dikonsumsi oleh masyarakat adalah (Prabowo, 2001).
a. Bahan baku (simplisia) :
Bahan baku yang digunakan tidak boleh tercemar oleh cemaran fisik, mikroba dan senyawa kimia beracun (insektisida).
b. Air yang dipergunakan
Air yang sehat adalah yang tidak tercemar secara fisik, oleh organisme
merugikan, dan tidak tercemar senyawa beracun tidak berbau, tidak berwarna dan tidak keruh.
c. Alat yang digunakan
Agar jamu yang dihasilkan mempunyai keamanan, maka harus dibuat menggunakan peralatan yang bersih dan tidak mencemari jamu.
d. Kebersihan dan perilaku penjual
Perilaku merupakan pangkal terjadi kondisi bersih atau kotor. Bakteri yang umum terdapat dalam air adalah Pseudomonas, Micrococcus,
D. Pengeringan
Pengeringan bertujuan untuk mendapatkan simplisia yang tidak mudah
rusak sehingga dapat disimpan lebih lama. Penurunan mutu atau kerusakan simplisia dapat dihambat dengan pengurangan kadar air dengan tujuan untuk
penghentian reaksi enzimatik. Kandungan air dalam simplisia pada kadar tertentu dapat merupakan media pertumbuhan kapang dan mikroba lainnya. Dari hasil penelitian diketahui bahwa reaksi enzimatik tidak berlangsung bila kadar air
kurang dari 10% (Anonim, 1994b).
Pengeringan yang tepat meliputi dua masalah utama yaitu pengaturan suhu
dan pengaliran udara yang teratur. Cara pengeringan yang paling sederhana dilakukan adalah pengeringan di bawah sinar matahari. Simplisia yang dikeringkan dengan cara ini adalah yang berasal dari dari akar, rimpang, kulit, dan
biji-bijian. Keuntungan dari cara pengeringan ini adalah biaya yang murah, tetapi mempunyai kekurangan yaitu suhu dan kelembaban tidak dapat dikontrol, serta
waktu yang relatif lebih lama. Waktu pengeringan tergantung cuaca dan intensitas penyinaran, serta mudah terkontaminasi oleh mikroba dari luar, serta pengaruh sinar ultraviolet yang dapat merusak kandungan kimia dari simplisia.
Cara pengeringan yang lain adalah dengan menggunakan pengering mekanis (oven) yang menggunakan tambahan panas. Pengeringan dengan panas
buatan ini memberikan beberapa keuntungan yaitu : tidak tergantung cuaca, tidak memerlukan tampat yang luas, kondisi pengeringan dapat dikontrol sehingga pengeringan dapat rata pada tiap bagian dari simplisia. Pengeringan dengan alat
pengeringan ditentukan dengan tepat dan selama pengeringan dikontrol dangan baik (Anonim, 1994b).
D. Sterilisasi
Sterilisasi adalah suatu usaha untuk membebaskan alat-alat atau bahan-bahan dari segala bentuk kehidupan, terutama mikroba. Macam sterilisasi yang digunakan tergantung pada macam sifat dan bahan. Cara umum yang dipakai
untuk sterilisasi, yaitu : 1. Sterilisasi dengan panas
Penggunaan panas merupakan cara termudah untuk mensterilkan bahan, dengan syarat bahwa bahan tersebut tahan terhadap pemanasan. Suhu 121oC selama 15 menit digunakan untuk mematikan spora. Uap harus dipertahankan pada tekanan
15 lb/sq di atas tekanan atmosfer untuk memperoleh suhu 121oC (Jawetz dkk, 1996). Sterilisasi ini dibedakan menjadi 2, yaitu : sterilisasi panas lembab dan
sterilisasi panas kering (Hadioetomo, 1985).
Disebut sterilisasi panas lembab, bila digunakan bersama-sama dengan uap air dan sterilisasi panas kering, bila tanpa kelembaban. Panas lembab sangat efektif
meskipun pada suhu yang tidak begitu tinggi, karena ketika uap air berkondensasi pada bahan-bahan yang disterilkan, dilepaskan panas sebanyak 686 kalori per
gram uap air pada suhu 121oC. Panas ini mendenaturasikan atau mengkoagulasikan protein pada organisme hidup dan dengan demikian mematikannya. Sterilisasi basah biasanya dilakukan di dalam autoklav atau
bertekanan dengan suhu 121oC selama 15 menit. Sterilisasi basah dapat digunakan untuk mensterilkan bahan apa saja yang dapat ditembus oleh uap air dan tidak
rusak bila dipanaskan dengan suhu yang berkisar 110oC sampai 121oC. Bahan-bahan yang biasa disterilkan dengan cara ini antara lain medium biakan, air
suling, alat-alat gelas, biakan yang akan dibuang, medium tercemar dan bahan-bahan dari karet (Hadioetomo, 1985). Beberapa cara pemanasan basah dapat membunuh mikroba karena panas basah dapat menyebabkan denaturasi protein,
termasuk enzim-enzim di dalam sel (Fardiaz,1992).
Ada empat hal yang harus diingat bila melakukan sterilisasi basah: (1)
sterilisasi bergantung pada uap, karena itu udara harus dikosongkan betul-betul dari ruang sterilisator; (2) semua bagian bahan yang disterilkan harus terkena uap, karena itu tabung dan labu kosong harus diletakkan dalam posisi tidur agar udara
tidak terperangkap didasarnya; (3) bahan-bahan yang berpori atau yang berbentuk cair harus permeabel terhadap uap; (4) suhu sebagaimana yang terukur oleh
termometer harus mencapai 121oC dan dipertahankan setinggi itu selama 15 menit (Hadioetomo,1985)
Dibandingkan dengan panas lembab, panas kering kurang efisien dan
membutuhkan suhu lebih tinggi serta waktu yang lebih lama untuk sterilisasi. Karena bentuk kehidupan yang paling tahan panas, yaitu endospora bakteri,
berperilaku seakan-akan tidak mengandung kelembaban, maka panas kering harus mencapai suhu 166oC–175oC untuk dapat mematikannya. Sterilisasi panas kering dapat diterapkan pada apa saja yang tidak menjadi rusak, menyala, hangus, atau
ini antara lain pecah belah seperti pipet, tabung reaksi, cawan petri, bahan dari kaca, botol sampel, juga peralatan jarum suntik, dan bahan-bahan yang tidak
tembus uap seperti gliserin, minyak, vanilin, dan bahan-bahan berupa bubuk. Bahan-bahan yang harus disterilkan harus dilindungi dengan cara membungkus,
menyumbat, atau menaruhnya dalam suatu wadah tertutup untuk mencegah kontaminasi setelah dikeluarkan dari oven (Hadioetomo,1985).
2. Sterilisasi dengan penyaringan (filtrasi)
Sterilisasi ini digunakan untuk mensterilkan medium laboratorium dan larutan-larutan yang sangat peka terhadap panas atau relatif tidak tahan terhadap
pemanasan. Dengan cara ini larutan atau suspensi dibebaskan dari semua mikroba hidup dengan cara melakukannya lewat saringan dengan ukuran pori yang sedemikian kecil (0,45 atau 0,22 mikron) sehingga bakteri dan sel-sel yang lebih
besar tertahan di atasnya, sedangkan filtratnya ditampung di dalam wadah yang steril(Hadioetomo, 1985).
3. Sterilisasi dengan bahan kimia
Pelaksanaanya dilakukan dengan menggunakan gas atau cairan pembunuh mikroba yang secara khusus diterapkan untuk bahan yang tidak tahan pemanasan,
sediaan atau barang yang jika dipanaskan sekali atau berulang kali sedikit banyak akan mengalami perubahan. Sterilisasi secara kimia dapat menggunakan etilen
oksida, asam perasetat, dan formaldehide (Hadioetomo, 1985).
Pada konsentrasi yang biasa dipakai (70 % larutan dalam air) alkohol bekerja sebagai denaturan protein
b. Fenol. Fenol dan banyak senyawa fenol merupakan zat anti mikroba yang kuat. Pada konsentrasi yang biasa digunakan (larutan dalam air 1-2%),
fenol dan derivatnya menyebabkan denaturasi protein.
c. Ion logam berat. Air raksa, tembaga, dan perak dalam bentuk garam bersifat denaturan protein pada konsentrasi tinggi. Ion-ion ini biasanya
digunakan pada konsentrasi yang sangat rendah, ion-ion bekerja dengan bergabung pada gugus sulfhidril.
d. Unsur pengoksida. Unsur pengoksida kuat menyebabkan sel-sel tidak aktif karena gugus sulfhidril bebas dioksidasi.
e. Unsur pengalkil. Sejumlah unsur bereaksi dengan senyawa dalam sel
untuk menggantikan atom hidrogen labil dengan gugus alkil. Dua unsur jenis ini yang biasa digunakan untuk tujuan disinfeksi ialah formaldehida
dan etilen oksida.
f. Detergen. Permukaan antara selaput mengandung lipid pada sel bakteri dan perbenihan cair yang mengelilinginya menarik suatu golongan
senyawa aktif permukaan tertentu, yaitu senyawa yang sekaligus memiliki gugus yang dapat larut dalam lemak dan larut dalam air (Jawetz dkk,
1996).
4. Sterilisasi dengan radiasi
Sinar matahari yang dipancarkan langsung pada sel vegetatif mikroba
terhadap sinar matahari. Aktivitas bakterisida dari sinar matahari disebabkan oleh sinar ultraviolet dari spektrum sinar. Sinar ultraviolet yang dipancarkan dari
lampu uap merkuri sering digunakan untuk menyinari ruangan sehingga mengurangi kontaminasi mikroba di udara. Radiasi ultraviolet menyebabkan
kesalahan dalam replikasi DNA dan mempunyai aktivitas mutagenik pada sel-sel hidup. (Fardiaz,1992)
E. Media
Untuk menumbuhkan suatu mikroba, diperlukan suatu substrat makanan
yang biasa disebut media, yang mengandung unsur-unsur makanan yang diperlukan oleh mikroba tersebut. Unsur-unsur makanan itu dapat berupa garam-garam anorganik seperti protein, asam amino, dan vitamin-vitamin yang
diperlukan untuk pertumbuhan.
Agar mikroba dapat tumbuh dan berkembang dengan baik di dalam media
diperlukan persyaratan tertentu, yaitu :
1. Bahwa didalam media harus terkandung semua unsur hara yang diperlukan untuk pertumbuhan dan perkembang biakan mikroba.
2. Bahwa media harus mempunyai tekanan osmosa, tekanan permukaan, dan pH yang sesuai dengan kebutuhan mikroba.
3. Bahwa media harus dalam keadaan steril, artinya sebelum ditanami mikroba yang dimaksud, tidak ditumbuhi oleh mikroba lain yang tidak diharapkan.
Beberapa media diramu oleh ahli mikrobiologi untuk menjaring dan membedakan mikroba. Kelompok media biakan ini disebut media selektif dan
diferensial. Media selektif adalah media biakan yang mengandung paling sedikit 1 bahan yang menghambat perkembangbiakan mikrobayang tidak diinginkan, dan
membolehkan perkembangbiakan mikroba tertentu yang ingin diisolasi. Bahan yang digunakan untuk menghambat pertumbuhan mikroba adalah antibiotik seperi streptomycin, dan penicillin, bahan kimiawi seperti Na-azide atau zat warna
kristal violet dan malakit hijau.
Media diferensial diramu agar dapat membedakan kelompok mikroba
tertentu dapat tumbuh pada media biakan. Media diferensial biasanya mengandung bahan kimia yang dapat digunakan oleh kelompok mikroba tertentu. Bila berbagai kelompok mikroba tumbuh pada media diferensial, maka dapat
dibedakan kelompok mikroba berdasarkan perubahan pada media biakan atau koloninya.
Konsistensi medium bermacam macam. Medium cair seperti kaldu nutrien dapat digunakan untuk pembiakan organisme dalam jumlah besar, penelahaan fermentasi, dan uji lain. Medium padat digunakan untuk mengamati morofologi
koloni dan mengisolasi biakan murni. Bahan pemadat yang paling umum digunakan adalah agar-agar, walaupun bisa digunakan gelatin dan silika gel.
Media yang mengandung zat zat kimia tertentu yang dapat menghambat pertumbuhan satu kelompok bakteri atau lebih tanpa menghambat pertumbuhan
organisme yang diinginkan disebut media selektif contohnya Saboroud’s glucose agar. Media yang mengandung zat-zat kimia tertentu yang memungkinkan
pengamat membedakan berbagai tipe bakteri, contohnya eosin methylene blue agardisebut media differensial(Hadioetomo,1985).
Media umum adalah media yang dapat digunakan untuk menumbuhkan
dan mendeteksi sebagian besar organisme aerob maupun fakultatif anaerob. Media diperkaya adalah media yang dapat menumbuhkan suatu mikroba dengan
baik karena mengandung bahan tambahan tertentu. Media khusus adalah media yang dibuat dengan bahan tambahan khusus yang bertujuan untuk mengisolasi mikroba patogen tertentu tapi tidak ditemukan pada media umum atau pada media
diperkaya(Murray,1999).
Media biakan yang digunakan untuk menumbuhkan bakteri terdapat dalam
bentuk padat, semi padat, dan cair. Media padat diperoleh dengan menambahkan agar, dan agar berasal dari ganggang merah. Agar digunakan sebagai bahan pemadat karena tidak diuraikan oleh mikrooganisme, dan membeku pada suhu
45oC. Kandungan agar sebagai bahan pemadat dalam media adalah 1,5 sampai 2% (Bibiana, 1994).
a. Plate Count Agar
Plate Count Agar digunakan untuk penghitungan jumlah mikroba dalam susu, juga digunakan untuk penghitungan jumlah mikroba dalam air,
pankreatik kasein,ekstrak ragi dan glukosa yang penting untuk pertumbuhan dari mikroba yang ditumbuhkan(Atlas,1997)
b. Pepton water
Medium ini digunakan dalam uji indol. Untuk memperoleh satu
liter media dibuat dengan cara melarutkan 15 gram bahan dalam satu liter aquadest lalu dimasukkan dalam tabung reaksi. Sterilisasi dengan autoklaf selama. 15 menit dengan suhu 121○C (Atlas,1997).
F. Penghitungan Angka Lempeng Total (ALT)
Analisa kuantitatif, mikroba-mikroba tidak dapat dihitung secara tepat dengan pemeriksan mikroskopik kecuali bila sekurang-kurangnya ada 100 juta (108)sel untuk setiap ml.Air dalam alam jarang mengandung lebih dari 105 sel
untuk tiap ml. karena metode yang digunakan adalah perhitungan pada lempeng perbenihan. Sejumlah tertentu air yang akan diperiksa diencerkan secara
berturut-turut, kemudian 1 ml dari tiap larutan tersebut ditanamkan pada pada lempeng agar-agar nutrien dan koloni-koloni yang kemudian tumbuh dihitung. Karena hanya sel-sel yang hanya sanggup membentuk koloni saja yang dihitung maka
metode ini dikenal pula sebagai “perhitungan sel hidup”.
Untuk menentukan jumlah bakteri dapat digunakan beberapa cara, antara lain :
Menghitung langsung secara mikroskop. Pada cara ini dihitung jumlah bakteri dalam satuan isi yang sangat kecil. Untuk ini digunakan kaca obyek
khusus yang bergaris(Petroff-Hauser) berbentuk bujur sangkar. Jumlah cairan yang terdapat antara kaca obyek dan kaca penutup mempunyai
volume tertentu, sehingga satuan isi yang terdapat dalam bujur sangkar juga tertentu.
Pembesaran yang digunakan untuk melihat bakteri membatasi
volume cairan yang diperiksa. Hanya cairan yang mengandung jumlah bakteri yang tinggi yang dapat menggunakan cara ini. Selain menghitung
secara langsung dengan mata, dapat pula digunakan alat penghitung elektronik coulters counter. Dengan alat ini dihitung semua benda yang memiliki ukuran diameter 30µm, sehingga cairan yang akan dihitung
jumlah bakterinya haruslah benar-benar hanya mengandung bakteri (Lay,1994).
Pada penghitungan dengan metode ini hasil pengenceran dari bahan tidak ditanam dalam cawan berisi media, tetapi diteteskan dalam ruang penghitung, yaitu kaca obyek khusus yang selanjutnya dilihat di
bawah mikroskop terhadap sel mikroba yang terdapat dalam kolom-kolom penghitung. Misalnya didapatkan jumlah yang terhitung 12 sel, maka
penghitungan jumlah sel adalah : 12 x 25 x 50 x 103= 1,5 x 107sel/ml di mana 12 = jumlah sel yang terhitung, 25 = jumlah kotak pada ruang penghitung yang dipergunakan untuk menghitung, 50 = volume tiap-tiap
mempunyai keuntungan yaitu semua sel bakteri yang hidup maupun mati dapat dihitung. Adapun kerugian dari metode ini yaitu kesalahan
menghitung akan didapat kalau sistem pengencerannya tidak homogen lagi.
Menghitung dengan cara kekeruhan. Cara ini menggunakan alat spektrofotometer. Dasar teknik ini adalah banyaknya cahaya yang diabsopsi sebanding dengan banyaknya sel bakteri pada batas-batas
tertentu. Jumlah mikroba dalam suspensi dapat ditentukan dengan menentukan kerapatan optik. Pengukuran kerapatan optik menggunakan
kolorimeter yang membiaskan cahaya dengan gelombang tertentu. Gelombang cahaya melewati suspensi biakan dan banyaknya cahaya yang ditransmisikan setelah melewati suspensi diukur. Jumlah cahaya yang
ditransmisikan setelah melewati suspensi biakan berbanding terbalik dengan jumlah mikroba dan jumlah cahaya yang diabsorpsi. Jumlah
cahaya yang diabsorpsi tergantung pada bentuk dan besar sel.
Spektrofometer dapat mengukur kepekatan sel dari suspensi dalam %T (transmitance) atau OD(jumlah cahaya yang diabsorpsi dan
disebarkan). Dalam mikrobiologi digunakan OD sebagai satuan hitungan, karena OD sebanding dengan kepekatan sel dalam suspensi biakan
(Lay,1994)
b. Jumlah bakteri yang hidup (viable count). Cara ini hanya menggambarkan jumlah sel yang hidup, sehingga dikatakan lebih tepat bila dibandingkan
mikroba hidup dalam suspensi akan tumbuh menjadi 1 koloni setelah diinkubasikan dalam media biakan dan lingkungan yang sesuai. Setelah
masa inkubasi, jumlah koloni yang tumbuh dihitung dan merupakan perkiraan atau dugaan dari jumlah mikroba dalam suspensi tertentu
(Hadioetomo,1985). Koloni yang tumbuh tidak selalu berasal dari 1 sel mikroba, karena beberapa mikroba tertentu cenderung untuk berkelompok atau berantai. Bila ditumbuhkan pada media dan lingkungan yang sesuai
kelompok bakteri ini hanya akan menghasilkan 1 koloni. Berdasarkan hal tersebut seringkali digunakan istilah colony forming units (CFU) untuk
menghitung jumlah mikroba hidup. Sebaiknya hanya lempeng agar yang mengandung 30-300 koloni saja yang digunakan dalam perhitungan. Lempeng agar dengan koloni >300 sulit untuk dihitung sehingga
kemungkinan kesalahan perhitungan sangat besar. Pengenceran sampel akan membantu untuk memperoleh penghitungan jumlah yang benar,
h. Landasan Teori
Penggunaan jamu gendong biasanya berdasarkan kebiasaan turun-temurun
secara umum, sudah diketahui manfaat jamu gendong, namun secara tertulis belum banyak mengidentifikasikan khasiat dan manfaatnya. Pemanfaatan jamu
gendong lebih banyak sebagai upaya promotif dan preventif kesehatan (Handayani & Suharmiati, 2001).
Dalam pembuatan jamu belum ada standarisasi, sehingga ada beberapa hal
yang perlu diperhatikan agar produk jamu gendong yang dihasilkan aman dikonsumsi oleh masyarakat adalah (Prabowo, 2001).
a. Bahan baku (simplisia) :
Bahan baku yang digunakan tidak boleh tercemar oleh cemaran fisik, mikroba dan senyawa kimia beracun (insektisida).
b. Air yang dipergunakan
Air yang sehat adalah yang tidak tercemar secara fisik, organisme
merugikan, dan tidak tercemar secara senyawa beracun tidak berbau, tidak berwarna dan tidak keruh.
c. Alat yang digunakan
Agar jamu yang dihasilkan mempunyai keamanan, maka harus dibuat menggunakan peralatan yang bersih dan tidak mencemari jamu.
d. Kebersihan dan perilaku penjual
Perilaku merupakan pangkal terjadi kondisi bersih atau kotor. Bakteri
Angka Lempeng Total, yang merupakan metode perhitungan jumlah mikroba hidup yang paling sensitif untuk menentukan mikroba karena beberapa
hal yaitu hanya sel yang masih hidup yang dapat dihitung, beberapa jenis mikroba dapat dihitung sekaligus, dapat digunakan untuk isolasi dan identifikasi mikroba,
karena koloni yang terbentuk mungkin berasal dari suatu mikroba yang mempunyai penampakan pertumbuhan spesifik.
i. Hipotesis
Pembuatan jamu gendong beras kencur yang beredar dipasaran tidak
BAB III
METODOLOGI PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini merupakan penelitian non eksperimental dengan rancangan penelitian deskriptif dan komparatif.
B. Variabel Penelitian dan Definisi Operasional 1. Variabel penelitian
a. Variabel bebas : jamu gendong beras kencur yang beredar di tiga pasar di kodya Yogyakarta.
b. Variabel tergantung : Angka Lempeng Total (ALT)
c. Variabel pengacau terkendali : sterilisasi media, sterilisai alat,
media yang digunakan, waktu inkubasi 18 – 48 jam, suhu inkubasi.
2. Definisi operasional :
a. Jamu gendong beras kencur yang digunakan adalah jamu beras
kencur dalam bentuk cairan yang diramu dan dijual dengan wadah botol plastik maupun plastik yang dijual di tiga pasar di kotamadya Yogyakarta.
c. Tiga pasar di Kotamadya Yogyakarta : Pasar Karangwaru, pasar Kranggan, pasar Pingit.
d. Angka Lempeng Total adalah jumlah bakteri aerob mesofil dalam tiap 1 ml sampel jamu gendong beras kencur.
e. Mesofil adalah kelompok mikroba yang hidup pada suhu 20°C-40°C.
C. Subyek dan Bahan Penelitian 1. Subyek Penelitian
Subyek uji yang digunakan untuk penelitian ini adalah cemaran mikroba jamu gendong. Jamu gendong ini diperoleh dari tiga pasar yang ada di Kotamadya Yogyakarta, yaitu Pasar Karangwaru, pasar Kranggan, pasar Pingit.
2. Bahan Penelitian
Ekstrak Jamu gendong , mediaPlate Count Agar(PCA) + Triphenyl Tetrazolium Chloride (TTC), pereaksi Pepton Dilution Fluid (PDF).
D. Alat Penelitian
E. Tata cara penelitian
1. Pengambilan sampel
Sampel diperoleh dari beberapa penjual jamu di pasar di kotamadya Yogyakarta yaitu pasar Karangwaru, pasar Pingit, dan pasar Kranggan.
2. Persiapan dan homogenisasi sampel Penanganan wadah/ kemasan
Wadah terbuat dari plastik bagian wadah yang akan dibuka dibersihkan dengan kapas beralkohol 70%, kemudian dibuka secara aseptik didekat
nyala api Bunsen.
Dengan cara aseptik dipipet 10 ml cuplikan, ke dalam wadah steril
yang sesuai ditambahkan 90 ml LB kemudian dihomogenkan dengan stomacher sehingga diperoleh suspensi pengenceran 1:10
3. Cara Pembuatan Media a. Plate Count Agar (PCA),
22,5 gram PCA dilarutkan dalam 2 liter air suling, dipanaskan sampai mendidih (sambil diaduk), dinginkan hingga 45-60oC. Tuangkan dalam wadah yang lebih kecil, sterilkan pada suhu 121oC selama 15
b. Pepton Dilution Fluid (PDF),
1 gram peptone dilarutkan dalam 1 liter air suling dan diukur pH 7,0 +
1. didisikan ke dalam labu dengan volume tertentu, kemudian disterilkan dengan autoklaf 121oC selama 15 menit.
c. Letheen broth (LB),
37,8 gram LB dilarutkan dalam air 1 liter air suling dan diukur pH 7,2 + 2. didisikan ke dalam labu dengan volume tertentu, kemudian
disterilkan dengan autoklaf 121oC selama 15 menit.
4. Uji Angka Lempeng Total
Disiapkan 5 buah tabung atau lebih yang masing-masing telah diisi dengan 9 ml pengencer PDF. Dari hasil homogenisasi pada penyiapan
contoh dipipet pengenceran 10-1sebanyak 1 ml ke dalam tabung yang berisi pengencer PDF pertama hingga diperoleh pengenceran 10-2dan
dikocok hingga homogen. Dibuat pengenceran selanjutnya hingga 10-6 atau sesuai dengan yang diperlukan. Dibuat pengenceran dipipet 1 ml ke dalam cawan petri dan dibuat duplo. Ke dalam tiap cawan petri
dituangkan 15-20 ml media PCA (45 + 1oC). Segera cawan petri digoyang dan diputar sedemikian rupa hingga suspensi tersebar merata.
selama 24-48 jam dengan posisi terbalik. Jumlah koloni yang tumbuh diamati dan dihitung.
5. Cara Perhitungan Koloni
1. Dipilih cawan petri dari satu pengenceran yang menunjukkan
jumlah koloni antara 30-300. Jumlah koloni rata-rata dari kedua cawan dihitung lalu dikalikan dengan faktor pengencerannya. Hasil dinyatakan sebagai Angka Lempeng Total dalam tiap gram contoh.
2. Bila salah satu dari cawan Petri menunjukkan jumlah koloni 30 atau lebih dari 300 koloni, dihitung jumlah rata-rata koloni,
kemudian dikalikan dengan faktor pengencerannya. Hasil kali dinyatakan sebagai Angka Lempeng Total dalam tiap ml /gram contoh.
3. Jika terdapat cawan-cawan dari dua tingkat pengenceran yang berurutan menunjukkan jumlah koloni antara 30-300, maka
dihitung jumlah koloni dari masing-masing tingkat pengenceran kemudian dikalikan dengan factor pengencerannya. Apabila hasil perhitungan pada tingkat yang lebih tinggi diperoleh jumlah
koloni rata-rata lebih besar dari 2 kali jumlah koloni rata-ratapada pengenceran dibawahnya, maka Angka Lempeng Total dipilih dari
Bila hasil perhitungan pada tingkat pengenceran lebih tinggi diperoleh jumlah koloni rata-rata kurang dari 2 kali jumlah koloni
rata-rata pada pengenceran dibawahnya, maka Angka Lempeng Total dihitung dari rata-rata jumlah koloni kedua tingkat
pengenceran tersebut ( Misal pada pengenceran ( 10-2 jumlah koloni rata-rata 293, pada pengenceran 10-3jumlah koloni rata-rata
41, maka Angka Lempeng Total adalah 2 2
10 x 2 , 351 10 x 2
410
293
).
4. Bila tidak satupun koloni dalam cawan maka angka lempeng total dinyatakan sebagai < dari 1 dikalikan faktor pengenceran terendah. 5. Jika seluruh cawan menunjukkan jumlah koloni lebih dari 300,
dipilih cawan dari tingkat pengenceran tetinggi kemudian dibagi menjadi beberapa sektor (2,4 atau 8) dan dihitung jumlah koloni
dari satu sektor. Angka Lempeng Total adalah jumlah koloni dikalikan dengan jumlah sektor, kemudian dihitung rata-rata dari kedua cawan dan dikalikan dengan factor pengenceran
6. Jika jumlah koloni rata-rata dari 1/8 bagian cawan lebih dari 200 maka angka lempeng total dinyatakan lebih besar dari 200 x 8
dikalikan faktor pengenceran.
7. Perhitungan dan pencatatan hasil angka lempeng total hanya ditulis dalam dua angka. Angka berikutnya dibulatkan ke bawah bila
kurang dari 5 dan dibulatkan dibulatkan ke atas bila lebih dari 5. Sebagai contoh 523 x 103dibulatkan menjadi 52 x 104untuk 83,6 x
8. Jika dijumpai koloni “spreader” meliputi seperempat sampai setengah bagian cawan, maka dihitung koloni yang tumbuh di luar
daerah “spreader”. Jika 75% dari seluruh cawan mempunyai koloni
“spreader” dengan keadaan seperti diatas maka dicatat sebagai
“Spr”. Untuk keadaan ini harus dicari penyebabnya dan diperbaiki
cara kerjanya pengujian diulang.
9. Jika dijumpai koloni spreader tipe rantai, maka tiap satu deret
koloni yang terpisah dihitung sebagai satu koloni, dan bila dalam kelompok spreader terdiri dari beberapa rantai, maka tiap rantai
dihitung sebagai 1 koloni.
F. Analisis Data
Setelah jumlah koloni dihitung dan dikalikan dengan faktor pengencerannya maka didapat angka lempeng total, kemudian dibandingkan
dengan keputusan Menteri Kesehatan Republik Indonesia Nomor : 661/Menkes/SK/VII/1994 tentang persyaratan obat tradisional mengenai batas angka lempeng total tidak boleh lebih dari 104 koloni/ml.Dari perbandingan
BAB IV
HASIL DAN PEMBAHASAN
A. Pengambilan Sampel Jamu Gendong Beras Kencur
Pengambilan sampel jamu gendong dilakukan dengan mengambil sampel 5 penjual jamu gendong dari 3 pasar di wilayah DIY. Pengambilan sampel dengan random sampling tidak mungkin dilakukan, meskipun demikian, juga karena
untuk mengidentifikasi satu persatu anggota populasi menghadapi kesulitan,maka yang paling mudah pengambilan sampel menggunakan metode convenience
sampling, yaitu mengambil anggota populasi yang mudah ditemukan saja, memang dalam sampel yang non random ketepatan untuk mencerminkan populasinya kurang akurat atau dapat menimbulkan bias, tetapi karena
populasinya tidak homogen dan sulit diidentifikasi, maka digunakan metode ini. Pengambilan sampel dilakukan pada 3 pasar yaitu pasar Kranggan, pasar Jetis,
pasar Karangwaru. Pengambilan sampel berdasarkan tipe penelitian, untuk penelitian deskriptif sampel dapat diambil 10% dari seluruh populasi. Menurut data pasar yang diperoleh dari dinas pasar di DIY, jumlah populasi pasar di DIY
adalah 30. Masing-masing pasar diambil sampel sebanyak 3 kali pada waktu yang berbeda dengan selang waktu 1 minggu, tujuannya adalah untuk mengetahui
keseragaman sediaan jamu gendong beras kencur yang diuji.
Jamu merupakan ramuan tradisional yang sangat umum ditemukan di Indonesia yang digunakan baik sebagai tambahan/ suplemen sehari-hari maupun
masyarakat menengah-bawah, jamu masih kerap menjadi pilihan pertama untuk mengatasi gangguan kesehatan sehari-hari. Tidak semua jamu-jamuan di
Indonesia masuk ke dalam daftar Badan Pengawas Obat dan Makanan (POM). Jamu gendong, yang pembuatannya dilakukan langsung oleh si penjual jamu
yang turun-temurun.
Jamu beras kencur dikatakan oleh sebagian besar penjual jamu sebagai jamu yang dapat menghilangkan pegal-pegal pada tubuh. Dengan membiasakan
minum jamu beras kencur, tubuh akan terhindar dari pegal-pegal dan linu yang biasa timbul bila bekerja terlalu payah. Selain itu, banyak pula yang berpendapat
bahwa jamu beras kencur dapat merangsang nafsu makan, sehingga selera makan meningkat dan tubuh menjadi lebih sehat. Dalam pembuatan jamu beras kencur, terdapat beberapa variasi bahan yang digunakan, namun terdapat dua bahan dasar
pokok yang selalu dipakai, yaitu beras dan kencur. Kedua bahan ini sesuai dengan nama jamu, dan jamu ini selalu ada meskipun komposisinya tidak selalu sama di
antara penjual jamu. Bahan-bahan lain yang biasa dicampurkan ke dalam racikan jamu beras kencur adalah biji kedawung, rimpang jahe, biji kapulogo, buah asam, kunci, kayu keningar, kunir, jeruk nipis, dan buah pala. Sebagai pemanis
digunakan gula merah dicampur gula putih dan seringkali mereka juga mencampurkan gula buatan. Cara pengolahan pada umumnya tidak jauh berbeda,
yaitu direbus dan dibiarkan sampai dingin, kemudian disediakan sesuai kebutuhan. Mula-mula beras disangan, selanjutnya ditumbuk sampai halus. Bahan-bahan lain sesuai dengan komposisi racikan ditumbuk menggunakan
disaring dengan saringan atau diperas melalui kain pembungkus bahan. Sari perasan bahan dicampurkan ke dalam air matang yang sudah tersedia, diaduk rata.
Selanjutnya dimasukkan ke dalam botol-botol. Dilihat dari proses pengolahan yang sederhana tersebut banyak sekali kemungkinan adanya kontaminasi bakteri.
Pengambilan sampel dengan cara aseptis sebisa mungkin dilakukan untuk menghindari kontaminasi pada saat mengambil, membawa dan memindahkannya. Sampel diambil menggunakan plastik steril untuk menghindari adanya
kontaminasi pada saat membawa, serta menggunakan es batu untuk menjaga agar suhu tetap dingin, tujuannya adalah untuk memperlambat pertumbuhan mikroba,
meskipun beberapa jenis mikroba tertentu, yaitu kelompok psikrofilik dan mesofilik dapat tumbuh pada suhu dingin. Yang termasuk ke dalam psikrofil adalah bakteri, ragi, dan jamur yang dapat tumbuh pada kisaran suhu 0oC hingga
20oC. Suhu pertumbuhan optimum organisme adalah adalah dibawah 15oC, dan dapat tumbuh meskipun lambat pada suhu 0oC. Patogen mesofilik dapat bertahan
pada kondisi pendinginan. Mesofil dapat tumbuh dengan baik pada suhu 20-45oC dengan suhu optimum untuk pertumbuhan antara 30-40oC.
B. Sterilisasi alat
Sebelum digunakan alat harus disterilisasi terlebih dahulu. Alat disterilisasi dengan panas kering, menggunakan oven karena dengan panas uap hanya efektif apabila uap berhubungan kontak dengan permukaan yang akan disterilkan, panas
sterilisasi uap, Gelas, botol, pipa, pipet yang sudah bersih tidak disterilkan di dalam autoklaf, karena barang-barang tersebut akan tetap basah sehabis sterilisasi.
Alat-alat dari gelas dimasukkan di dalam oven kering selama 2 – 3 jam pada temperatur 160o – 170o C; hal ini bergantung kepada banyak sedikitnya muatan
yang dimasukkan dalam oven. Kapas masih dapat bertahan dalam oven kering selama waktu dan pada temperatur seperti tersebut di atas. Alat-alat yang belum bersih dan belum kering tidak boleh dimasukkan dalam oven kering, karena dapat
timbul bercak-bercak bekas air yang dapat mengganggu pada saat penelitian.
C. Sterilisasi Media
Media yang akan disterilkan ditempatkan di dalam autoklaf ini selama 15 sampai 20 menit; hal ini bergantung kepada banyak sedikitnya barang yang perlu
disterilkan. Setelah pintu autoklaf ditutup rapat, barulah kran pada pipa uap dibuka, dan temperatur akan terus menerus naik sampai 121oC. Biasanya autoklaf
sudah diatur demikian rupa, sehingga pada suhu tersebut, tekanan ada sebesar 15 lbs (pounds) per inch persegi yang berarti 1 atmosfer per 1 cm2. Perhitungan waktu 15 atau 20 menit itu dimulai semenjak termometer pada autoklaf menunjuk
121oC. Setelah selesai autoklaf tidak boleh langsung dibuka, karena jika dilakukan, maka isi botol yang ada di dalam autoklaf akan meluap. Sebaiknya
ditunggu hingga manometer menunjukkan 0, barulah autoklaf kita buka. Pendinginan dilakukan sedikit demi sedikit. Jika media mengandung vitamin, gelatin atau gula, maka setelah sterilisasi dalam autoklaf, media tersebut haruslah
untuk menghindarkan terurainya zat-zat tersebut. Media yang sudah steril dapat disimpan dalam almari es.
D. Homogenisasi Sampel
Persiapan dan homogenisasi sampel meliputi cara persiapan contoh obat tradisional untuk memperoleh distribusi bakteri secara merata didalam contoh yang diuji. Media yang digunakan dalam homogenisasi sampel adalah Letheen
broth. Letheen brothmengandung Peptic digest of animal ,Beef extract, NaCl, TweenTM80,Lechitin.
Wadah terbuat dari plastik bagian wadah yang akan dibuka dibersihkan dengan kapas beralkohol 70%, fungsi alkohol adalah sebagai disinfektan, kerja germisida alkohol adalah denaturasi protein, konsentrasi alkohol yang paling
efektif bergantung pada jumlah kelembaban yang ada, dalam etil alkohol larutan 70% merupakan konsentrasi yang paling efektif. Setelah di bersihkan dengan
alkohol kemudian dibuka secara aseptik didekat nyala api Bunsen.
Dengan cara aseptik dipipet 10 ml cuplikan, ke dalam wadah steril yang sesuai ditambahkan 90 ml LB kemudian dihomogenkan dengan stomacher sehingga
E. Pengenceran
Fungsi dari pengenceran adalah untuk mempermudah penghitungan jumlah
koloni, dan untuk mendapatkan jumlah koloni antara 30-300, karena jika tidak dilakukan pengenceran, koloni bakteri sangat pekat dan tidak dapat dihitung.
Disiapkan 5 buah tabung yang masing masing telah diisi dengan 9 ml Pepton Dilution Fluid (PDF), untuk membuat seri pengenceran sekaligus sebagai nutrisi bagi bakteri karena mengandungpepton.Pepton ialah protein yang terdapat pada
daging, pada air susu, pada kedelai, dan pada putih telur. Pepton mengandung banyak N2, sedang kaldu berisi garam-garam mineral dan lain-lainnya lagi, jadi
sedikit asam atau netral, keadaan yang demikian ini sesuai bagi kebanyakan bakteri. Cara pembuatannya adalah satu gram pepton dilarutkan dalam 1 liter air suling, dan diukur pH 7,0 + 1, jika pada saat pembuatan PDF didapatkan pH yang
sedikit asam maka perlu ditambahkan beberapa tetes basa kuat KOH. PDF yang sudah disterilkan didiinginkan sampai dengan suhu kamar kemudian digunakan
sesuai kebutuhan. PDFyang sudah disterilkan, jika tidak digunakan simpan pada suhu kamar.
F. Uji Angka lempeng Total (ALT)
Uji ALT adalah penghitungan jumlah mikroba dengan caraviable countatau
disebut juga sebagai standard plate count didasarkan pada asumsi bahwa setiap sel mikroba hidup dalam suspensi akan tumbuh menjadi satu koloni setelah diinkubasikan dalam media biakan dan lingkungan yang sesuai. Setelah masa
dugaan dari jumlah mikroba dalam suspensi tersebut. Penghitungan jumlah mikroba hidup adalah jumlah minimum mikroba. Hal ini disebabkan koloni yang
tumbuh pada lempengan agar merupakan gambaran mikroba yang dapat tumbuh dan berbiak dalam media dan suhu inkubasi tertentu. Prinsip dari uji Angka
Lempeng Total (ALT) adalah pertumbuhan mikroba aerob mesofilik setelah contoh diinkubasikan dalam media agar pada suhu 35°C ± 1°C selama 24 jam 48 jam ± 1 jam mikroba ditumbuhkan pada suatu media agar, maka mikroba tersebut
akan tumbuh dan berkembang biak dengan membentuk koloni yang dapat langsung dihitung.
Uji angka lempeng total dapat digunakan dalam pemeriksaan cemaran mikroba pada bahan baku obat dengan anggapan bahwa setiap sel mikroba yang hidup pada bahan tersebut akan tumbuh menjadi 1 koloni setelah diinkubasikan
dalam media biakan dan lingkungan yang sesuai. Setelah masa inkubasi jumlah koloni yang tumbuh dihitung dan merupakan perkiraan atau dugaan dari jumlah
mikroba pada bahan tersebut. Metode ini hanya digunakan untuk perhitungan terhadap mikroba yang hidup, yang memungkinkan sel yang hidup dapat membentuk koloni pada kondisi percobaan yang sesuai, oleh karena itu metode ini
disebut viable count atau standard plate count. Karena pertumbuhan koloni dan jumlah koloni yang teramati yang dipergunakan dalam perhitungan jumlah, maka
satuan yang digunakan adalah satuan colony forming units (CFU/ml) atau koloni/ml. Untuk perhitungan jumlah mikroba hidup, sebaiknya pada metode ini hanya lempeng agar yang mengandung jumlah koloni antara 30 –300 koloni saja
lebih dari 300 koloni akan sangat sulit untuk dihitung, sehingga kemungkinan kesalahan perhitungan sangat besar yang akhirnya akan mengurangi keabsahan
penelitian. Pengenceran sampel akan akan membantu dalam memperoleh perhitungan yang benar, namun pengenceran yang terlalu tinggi akan
menghasilkan jumlah koloni yang rendah (< 30 koloni). Pada jumlah koloni yang terlalu rendah tersebut perhitungan statistik menjadi tidak sah karena terjadi perbedaan mencolok dan tidak bisa digunakan untuk perhitungan. Bila pada
seluruh seri pengenceran tidak terdapat jumlah koloni yang memenuhi persyaratan 30-300 koloni, maka tata cara perhitungannya menggunakan cara yang tertulis
pada tata cara analisis hasil.
Pada pengujian ini akan diketahui jumlah cemaran bakteri pada sediaan jamu gendong di tiga pasar di DIY. Pengujian cemaran bakteri dari sampel jamu
gendong beras kencur dengan metode uji angka lempeng total dilakukan sebanyak 3 kali pengambilan sampel, masing-masing sampel dilakukan replikasi duplo,
sebanyak 1 ml suspensi hasil pengenceran sampel dituang ke dalam cawan petri. Ke dalam setiap piring petri tersebut dituangkan media Plate Count Agar (PCA) steril yang telah dicairkan dengan temperatur media berkisar pada 40oC. Plate
Count Agar(PCA), (gambar. 1). Pembuatannya Bahan-bahan dilarutkan dalam air suling dan dipanaskan sampai mendidih (sambil diaduk) dinginkan hingga suhu
yang telah disterilkan jika tidak digunakan disimpan pada suhu 5-15oC, jika akan digunakan lagi dipanaskan lagi dengan penangas air.
Gambar. 1 MediaPlate Count Agar (PCA)
Tetrazolium chloride (TTC) ditambahkan ke dalam agar. Untuk menandai kehadiran bakteri di dalam agar dengan warna merah. Warna merah adalah hasil
dari metabolisme bakteri. TTC menerima elektron dari bakteri. Ketika dioksidasi, TTC dapat larut dan tanpa mewarnai. ketika direduksi, TTC berwarna merah dan
membentuk endapan yang tidak dapat larut( tidak menyebar di luar agar). berarti di mana terdapat warna merah maka di sana terdapat koloni. Warna yang merah bukan ciri khas bakteri tersebut. Hal itu disebabkan oleh pengurangan
Tetrazolium Klorida secara kimiawi sebagai hasil metabolisme hasil bakteri. Cawan petri selanjutnya diinkubasi pada temperatur 35-37oC selama 24-48
Metode yang digunakan adalah metode uji angka lempeng total, prosedur kerja menggunakan MA PPOMN Nomor : 95/MIK/00, metode ini digunakan
untuk menetapkan angka bakteri aerob mesofil yang terdapat dalam sediaan obat tradisional.
Dalam rangkaian pemeriksaan terhadap bahan baku obat dan dalam menjamin mutu kualitas, dan manfaat dari bahan baku obat sebelum dikatakan boleh diproses lebih lanjut, maka salah satu parameter yang harus dipenuhi adalah
pemeriksan bahan baku dari cemaran mikroba. Departemen Kesehatan menyarankan bahwa baku obat boleh positif mengandung cemaran mikroba tetapi
sampai batas tertentu, dan tidak boleh mengandung cemaran patogen
Supaya mikroba yang tumbuh pada cawan Petri adalah benar merupakan cemaran yang berasal dari suspensi serbuk bahan, maka teknik aseptis dalam
laboratorium merupakan hal yang sangat penting, ada beberapa cara yang dapat dilakukan untuk mengurangi resiko masuknya cemaran dari luar antara lain
mensterilisasikan bahan dan alat yang dipakai dalam penelitian, penggunaan laminar air flow (LAF), dan pembuatan blangko dari media dan pengencer yang dipakai dalam penelitian agar memastikan cemaran tidak berasal dari media dan
pengencer. Pada sterilisasi media, media yang tahan panas disterilkan dalam autoklaf selama 15 menit pada suhu 121oC. Pada keadaan suhu seperti ini maka
bakteri thermofil yang tahan terhadap suhu sampai 80oC sekalipun akan mati. Setelah dituang dalam cawan Petri, dibiarkan beberapa saat supaya memadat, kemudian dibalik dan diinkubasi pada suhu 35-37oC selama 24-48 jam.
tidak menetes pada media yang dapat mengacaukan perhitungan koloni, karena koloni tidak memisah. Suhu inkubasi pada 35-37oC karena sebagian besar bakteri
terutama golongan mesofil mempunyai suhu optimum pertumbuhan sekitar 20-40oC.
Setelah diinkubasi selama 24-48 jam pada suhu 35-37oC, koloni bakteri yang tumbuh dapat dihitung. Sebagai blanko digunakan media PCA, PCA+LB, PCA+PDF, dan dipakai untuk mengurangi angka lempeng total jika terdapat
kontaminasi pada media.
Gambar 3. BlankoStandard Plate Count(SPC) agar
Gambar 4. BlankoStandard Plate Count(SPC) danPepton Dilution Fluid
Dari penghitungan jumlah koloni bakteri kemudian dipilih koloni seri
pengenceran yang memiliki jumlah 30-300 koloni, dan dihitung sesuai dengan cara penghitungan ALT menurut MA PPOMN Nomor : 95/MIK/00. Dari
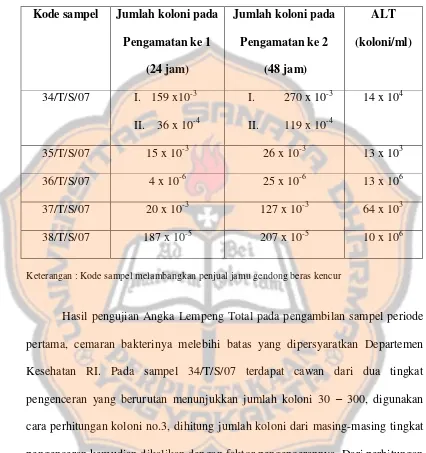
Tabel I. Hasil Perhitungan ALT pada Pengambilan Sampel Periode Pertama dari 5 Penjual setelah Pengamatan 24 jam, dan Setelah 48 jam
Kode sampel Jumlah koloni pada Pengamatan ke 1
(24 jam)
Jumlah koloni pada Pengamatan ke 2
(48 jam)
ALT (koloni/ml)
34/T/S/07 I. 159 x10-3
II. 36 x 10-4
I. 270 x 10-3
II. 119 x 10-4
14 x 104
35/T/S/07 15 x 10-3 26 x 10-3 13 x 103
36/T/S/07 4 x 10-6 25 x 10-6 13 x 106
37/T/S/07 20 x 10-3 127 x 10-3 64 x 103
38/T/S/07 187 x 10-5 207 x 10-5 10 x 106
Keterangan : Kode sampel melambangkan penjual jamu gendong beras kencur
Hasil pengujian Angka Lempeng Total pada pengambilan sampel periode pertama, cemaran bakterinya melebihi batas yang dipersyaratkan Departemen Kesehatan RI. Pada sampel 34/T/S/07 terdapat cawan dari dua tingkat
pengenceran yang berurutan menunjukkan jumlah koloni 30 – 300, digunakan cara perhitungan koloni no.3, dihitung jumlah koloni dari masing-masing tingkat pengenceran kemudian dikalikan dengan faktor pengencerannya. Dari perhitungan
yang lebih tinggi didapatkan jumlah koloni rata-rata lebih besar dari 2 kali jumlah koloni rata-rata dibawahya sehingga dipilih jumlah koloni 270 untuk menghitung
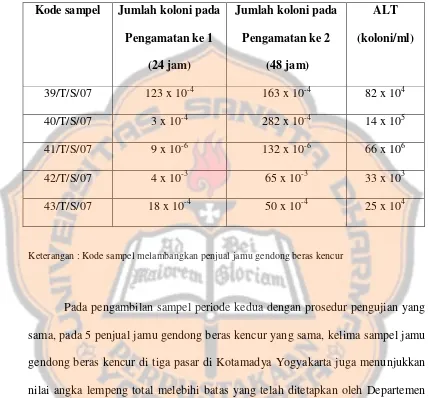
Tabel II. Hasil Perhitungan ALT pada Pengambilan Sampel Periode Kedua dari 5 Penjual setelah Pengamatan 24 jam, dan Setelah 48 jam Kode sampel Jumlah koloni pada
Pengamatan ke 1 (24 jam)
Jumlah koloni pada Pengamatan ke 2
(48 jam)
ALT (koloni/ml)
39/T/S/07 123 x 10-4 163 x 10-4 82 x 104
40/T/S/07 3 x 10-4 282 x 10-4 14 x 105
41/T/S/07 9 x 10-6 132 x 10-6 66 x 106
42/T/S/07 4 x 10-3 65 x 10-3 33 x 103
43/T/S/07 18 x 10-4 50 x 10-4 25 x 104
Keterangan : Kode sampel melambangkan penjual jamu gendong beras kencur
Pada pengambilan sampel periode kedua dengan prosedur pengujian yang
sama, pada 5 penjual jamu gendong beras kencur yang sama, kelima sampel jamu gendong beras kencur di tiga pasar di Kotamadya Yogyakarta juga menunjukkan
Tabel III. Hasil Perhitungan ALT pada Pengambilan Sampel Periode Ketiga dari 5 Penjual setelah Pengamatan 24 jam, dan Setelah 48 jam
Kode sampel Jumlah koloni pada Pengamatan ke 1
(24 jam)
Jumlah koloni pada Pengamatan ke 2
(48 jam)
ALT (koloni/ml)
44/T/S/07 128 x 10-4 148 x 10-4 74 x 104
45/T/S/07 235 x 10-2 272 x 10-2 14 x 103
46/T/S/07 35 x 10-6 177 x 10-6 89 x 106
47/T/S/07 82 x 10-3 198 x 10-3 99 x 103
48/T/S/07 29 x 10-5 83 x 10-5 42 x 105
Keterangan : Kode sampel melambangkan penjual jamu gendong beras kencur
Pada pengambilan sampel periode ketiga dengan prosedur pengujian yang sama, pada 5 penjual jamu gendong beras kencur yang sama, kelima sampel jamu
gendong beras kencur di tiga pasar di Kotamadya Yogyakarta juga menunjukkan nilai angka lempeng total melebihi batas yang telah ditetapkan oleh Departemen Kesehatan yaitu 104. ALT yang ditunjukkan berbeda bermakna dengan pada saat
pengambilan sampel pertama dan kedua, Angka Lempeng Total dalam jamu gendong beras kencur dari seorang penjual bisa berbeda untuk setiap kali
penjualan. Hal ini bisa berarti tidak adanya keseragaman dalam sediaan.
Dari ketiga data hasil uji angka lempeng total diatas yang sangat tinggi menunjukkan kurangnya kebersihan penjual. Dalam koloni yang teramati
Seri pengenceran yang digunakan untuk menghitung jumlah koloni berbeda-beda tergantung pada kepekatan cemaran mikroba dari masing-masing
sampel, dari tabel dapat dilihat bahwa sampel 45/T/S/07pengambilan sampel ketiga, pada seri pengenceran 10-2 sudah dapat dihitung koloninya, tetapi ada
beberapa sampel yang hingga seri pengenceran 10-6 baru dapat dihitung jumlah koloninya.
Gambar.5 Hasil dari pengujian angka lempeng total, dengan 9 seri pengenceran Keterangan : (1). Seri pengenceran 10-1, (2) seri pengeceran 10-2, (3) seri pengeceran 10-3, (3) seri pengeceran 10-3, (4) seri pengeceran 10-4, (5) seri pengeceran 10-5, (6) seri pengeceran 10-6, (7) seri pengeceran 10-7, (8) seri pengeceran 10-8, (9) seri pengeceran 10-9
Angka lempeng total (ALT) dari sejumlah sampel jamu yang diperiksa
melebihi batas cemaran mikroba,di mana batas cemaran yang dipersyaratkan untuk sediaan tersebut sebesar 104koloni/ml.
Tabel IV. Perhitungan Angka Lempeng Total Jamu Gendong dari 5 Produsen di Kotamadya Yogyakarta Hasil Penelitian Sylvia
Tahun 2005
Rerata Sampel (CFU) / ml Produsen
1 2 3
A 1.993.000* 220.200 1.798.000*
B 2.138.500* 1.806.000* 1.536.500*
C 1.061.500* 184.050 138.700
D 133.450 128.600 170.750
E 146.500 168.050 144.700
Keterangan * : melebihi ambang batas kontaminasi bakteri standar SNI 19-2897-1992 sebesar < 106CFU /ml
Dalam penelitian Sylvia tahun 2005 meyatakan bahwa produsen-produsen jamu gendong di DIY terkontaminasi oleh bakteri dengan jumlah kontaminan yang melebihi ambang batas konsumsi, yaitu sebesar <106CFU (Colony Forming
Unit) per ml untuk bakteri. Hasil penghitungan angka lempeng total dibandingkan dengan standar uji cemaran mikroba SNI 19-2897-1992. Penelitian yang kami
lakukan mengacu kepada Permenkes RI tentang persyaratan obat tradisional yang menyatakan bahwa angka lempeng total tidak boleh lebih dari 104koloni/ml.
Jumlah cemaran melebihi batas, hal ini terjadi kemungkinan karena
beberapa faktor, antara lain kondisi air cuci, peralatan yang digunakan, debu, wadah yang digunakan kurang bersih, faktor lingkungan pasar yang mempunyai
sanitasi buruk, kebiasaan pedagang, dan simplisia yang digunakan. Untuk mencegah hal tersebut sebaiknya pedagang menggunakan air panas untuk mencuci alat, menggantinya apabila kotor dan pedagang mencuci tangan lebih
Perhitungan cemaran bakteri dengan menghitung ALT mempunyai beberapa kelemahan :
1. Hasil perhitungan tidak menunjukan jumlah sel yang sebenarnya, karena beberapa sel yang berdekatan mungkin membentuk satu koloni.
2. Media dan kondisi inkubasi yang berbeda mungkin menghasilkan nilai yang berbeda.
3. Mikroba yang ditumbuhkan harus dapat tumbuh pada media padat dan
membentuk koloni yang kompak dan jelas dan tidak menyebar. 4. Memerlukan persiapan dan waktu yang relatif lama
Keberadaan mikroba pada makanan penting artinya karena mikroba tersebut dapat menyebabkan terjadinya kerusakan pada makanan atau dapat memproduksi toksin (racun) yang dapat menimbulkan penyakit pada manusia.
Misalnya, 10 sel bakteri Escherichia coli yang bersifat sangat membahayakan (extreme virulent) apabila termakan dapat menyebabkanhemorrhagic colitis yang
BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
1. Cemaran mikroba pada jamu gendong beras kencur yang dijual di 3 pasar di kotamadya Yogyakarta dengan pengujian ALT
Sampel 1 = 14x104koloni/mL; 82x104koloni/mL; 74x104koloni/mL,
Sampel 2 = 13x103koloni/mL; 14x105koloni/mL; 14x103koloni/mL, Sampel 3 = 13x106koloni/mL; 66x106koloni/mL; 89x106koloni/mL,
Sampel 4 = 64x103koloni/mL; 33x103koloni/mL; 99x103koloni/mL, Sampel 5 = 50x106koloni/mL; 25x104koloni/mL; 42x105koloni/mL 2. Kelima sampel tersebut mengandung cemaran bakteri melebihi 104
koloni/ml. Jamu gendong beras kencur yang beredar dipasar tercemar oleh bakteri dan melebihi batas yang telah ditentukan Departemen Kesehatan
Republik Indonesia.
B. Saran
1. Perlu adanya standarisasi dalam pembuatan sediaan obat tradisional jamu gendong, dengan cara dipublikasikan ke pihak yang berwenang yaitu
BPOM agar dapat ditindak lanjuti dengan pengawasan dan pembinaan dalam pembuatan jamu gendong.
DAFTAR PUSTAKA
Anonim, 1977, Materia Medika Indonesia, jilid I Departemen Kesehatan Republik Indonesia, Jakarta, hal 55.
Anonim, 1994a, Peraturan Perundang-undangan Obat Tradisional, jilid I, 29-46,1-5, Departemen Kesehatan Republik Indonesia, Jakarta.
Anonim, 1994b, Teknologi Pengeringan Simplisia Untuk Pedesaan, Prosiding Symposium Penelitian Bahan Obat Alami, VII, 79-78, Balai Penelitian Tanaman Rempah dan Obat, Bogor.
Anonim, 1995, Farmakope Indonesia, jilid IV, 847, Departemen Kesehatan Republik Indonesia, Jakarta.
Anonim, 2000a, Parameter Terstandar Umum Ekstrak Tumbuhan Obat, 28-30, 64-65, Departemen Kesehatan Republik Indonesia, Jakarta.
Anonim, 2000b,Pedoman Pelaksanaan Uji Klinik Obat Tradisional, 1-12, 27-37,, Departemen Kesehatan Republik Indonesia, Jakarta.
Anonim, 2007, Pemastian Mutu Obat Kompendium Pedoman dan Bahan-Bahan Terkait GMP dan Inspeksi, vol. 2, diterjemahkan oleh Fabiola C.R. Hutabarat , 93,144-148,Penerbit Buku Kedokteran,Jakarta.
Atlas, R.M., 1997, Handbook of Microbiological Media, 2nd edition, 207, 497, 506, 796, CRC Press Inc, New York.
Atlas M.R, 1997, Principles of Microbiology, 2nd Wm. C. Brown Publisher Kentucky, USA.
Bonang, G., & Koeswardono, S., 1982, Mikrobiologi Kedokteran untuk Laboratorium dan Klinik Bagian Mikrobiologi, Fakultas Kedokteran Universitas Atmajaya, Jakarta.
Dwijoseputro, D, 1978,Dasar-Dasar Mikrobiologi, Penerbit Djambatan, Jakarta. Fardiaz, S, 1992, Mikrobiologi Pangan, 118-129, Gramedia Media Utama,
Jakarta.
Hadioet