i
SINTESIS MEMBRAN ELEKTROLIT SELULOSA ASETAT DARI DAUN PANDAN LAUT (Pandanus tectorius) DENGAN PEMLASTIS DIMETIL
FTALAT UNTUK APLIKASI BATERAI ION LITIUM
SKRIPSI
Diajukan kepada Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Negeri Yogyakarta
untuk Memenuhi Sebagai Persyaratan Guna Memperoleh Gelar Sarjana Sains Kimia
Oleh:
APRILIYANI DWI IRIYANTI NIM 12307144034
PROGRAM STUDI KIMIA JURUSAN PENDIDIKAN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS NEGERI YOGYAKARTA
v MOTTO
“Bagaimana kamu ingkar kepada Allah, padahal kamu (tadinya) mati, lalu Dia menghidupkan kamu, kemudian Dia mematikan kamu lalu Dia menghidupkan
kamu kembali. Kemudian kepada-Nyalah kamu dikembalikan.”
(QS. Al-Baqarah (2): 28)
“... Cukuplah Allah (menjadi penolong) bagi kami dan Dia sebaik-baik pelindung.”
(QS. Ali „Imran (3): 173)
vi
PERSEMBAHAN
Dengan menyebut nama Allah Yang Maha Pengasih lagi Maha Penyayang
Alhamdulillah syukur kepada-Mu, akhirnya tugas akhir skripsi ini terselesaikan. Karya tulis ini saya persembahkan untuk:
1. Orangtuaku (bapak Iriyanto dan ibu Giyati), terimakasih atas dukungan, do’a, nasehat dan semua hal yang telah diberikan baik seca ra materi maupun non materi.
2. Kakakku (mbak Vera dan mas Joko) terimakasih atas do’a, dan dukungannya.
3. Sahabat-sahabatku dalam Kawanan Wanita Bahagia (Ariqah, Dhaulika, Fia, Ifa, Kara, Nado, Sita, Tika, Titik, dan Zainab) terimakasih atas motivasi dan bantuannya.
4. Teman satu perjuangan skripsi, Nur Syarifah Sukarno. Terimakasih atas bantuan, kerjasama dan kebersamaannya dalam mengerjakan skripsi. 5. Demas Aji, mbak Utha, mbak Wija, Mutia, Tiara, Ratna terimakasih atas
bantuannya.
6. Teman-teman mahasiswa Kimia swadana angkatan 2012 terimakasih telah memberikan dukungan dan motivasinya.
vii
SINTESIS MEMBRAN ELEKTROLIT SELULOSA ASETAT DARI DAUN PANDAN LAUT (Pandanus tectorius) DENGAN PEMLASTIS DIMETIL
FTALAT UNTUK APLIKASI BATERAI ION LITIUM Oleh :
Apriliyani Dwi Iriyanti NIM. 12307144034
Pembimbing: Prof. Dr. Endang Widjajanti LFX dan Marfuatun, M.Si
ABSTRAK
Penelitian ini bertujuan untuk mengetahui pengaruh DMP terhadap nilai konduktivitas serta mengetahui karakter membran elektrolit selulosa asetat.
Subjek penelitian ini adalah selulosa asetat hasil sintesis dari daun pandan laut sedangkan objeknya adalah konduktivitas, gugus fungsi, dan foto permukaan dari membran elektrolit selulosa asetat. Selulosa diisolasi dari daun pandan laut dan diasetilasi dengan asam asetat anhidrida dengan menggunakan katalis asam sulfat pekat. Pembuatan membran menggunakan metode casting larutan polimer dengan pen-doping-an garam litium 35% dan penambahan pemlastis DMP dengan komposisi 10%, 15%, 20%, 25%, dan 30%. Nilai konduktivitas membran didapatkan dari Elkahfi 100, analisis gugus fungsi menggunakan FTIR, dan analisis foto permukaan menggunakan mikroskop optik.
Semakin tinggi komposisi DMP, konduktivitas membran cenderung meningkat dan konduktivitas optimum diperoleh pada komposisi DMP 25% Sebesar 2,44x10-2 Scm-1. Berdasar analisis FTIR menunjukkan adanya gugus O-H, C=O, dan C=C aromatik. Foto permukaan menunjukkan membran yang paling homogen adalah pada komposisi DMP 25%.
viii
SYNTHESIS OF CELULOSE ACETATE ELECTROLYTE MEMBRANE FROM PANDAN LAUT (Pandanus tectorius) LEAVES WITH DIMETHIL
PHTHALATE AS PLASTICIZER FOR APPLICATION OF LITHIUM-ION BATTERY
By :
Apriliyani Dwi Iriyanti Number of Student:12307144034
Supervisor: Prof. Dr. Endang Widjajanti LFX and Marfuatun,M.Si
ABSTRACT
This research aimed to determine effect of DMP plasticizer toward conductivity cellulose acetate electrolyte membrane, and its character.
Subject of the research was cellulose acetate from pandan laut leaves and the object were conductivity, the functional group, and surface photo of cellulose acetate electrolyte membrane. Cellulose was obtained by isolation of pandan laut leaves. It was acetylized using anhydride acetate acid and concentrated sulfuric acid as a catalyst. The cellulose acetate electrolyte membrane was synthesized by polymer solution-cast method, in which was doped 35% LiCl. DMP was added which were 10%, 15%, 20%, 25%, 30%. The conductivity membrane was observed by Elkahfi 100, the functional group by FTIR, and surface photo by optic microscope.
The higher concentrate of DMP was added, the conductivity electrolyte membrane tend to increase. The highest conductivity of cellulose acetate electrolyte membrane was 2.44x10-2 Scm-1 at 25% dimethyl phthalate. Observed by FTIR analysis is obtained O-H, C=O, and C=C(aromatic) group. The surface photo shows that membrane is most homogeneous at 25% DMP
.
ix
KATA PENGANTAR Assalamu‟alaikum Warahmatullahi Wabarakatuh
Puji syukur saya panjatkan kehadirat Allah SWT atas limpahan rahmat,
karunia, dan hidayah-Nya sehingga skripsi ini mampu penulis selesaikan.
Sholawat serta salam semoga terlimpah kepada Nabi Muhammad SAW beserta
keluarga, sahabat, dan para pengikutnya sampai hari kiamat.
Skripsi berjudul “Sintesis membran elektrolit selulosa asetat dari daun pandan laut (Pandanus tectorius) dengan pemlastis Dimetil Ftalat untuk aplikasi baterai ion litium” telah dapat diselesaikan dengan baik sebagai persyaratan untuk memperoleh gelar sarjana sains yang telah ditetapkan oleh
Jurusan Pendidikan Kimia di Universitas Negeri Yogyakarta. Pada kesempatan ini
perkenankanlah penulis mengucapkan terimakasih kepada:
1. Bapak Dr. Hartono selaku Dekan FMIPA Universitas Negeri Yogyakarta yang
telah memberikan izin dalam penulisan skripsi ini.
2. Bapak Drs. Jaslin Ikhsan, M.App.Sc., Ph.D selaku Ketua dan Koordinator
Tugas Akhir Skripsi Program Studi Kimia, Jurusan Pendidikan Kimia,
Universitas Negeri Yogyakarta yang telah memberikan kelancaran pelayanan
dan urusan akademik.
3. Ibu Eddy Sulistyowati Apt, Ms selaku Dosen Penasehat Akademik yang telah
memberikan dorongan dalam penulisan skripsi ini.
4. Ibu Prof. Dr. Endang Widjajanti LFX selaku dosen pembimbing utama yang
telah memberikan waktu, bimbingan, pengarahan, saran, dan ilmu yang sangat
x
5. Ibu Marfuatun, M.Si selaku dosen pembimbing pendamping yang telah
memberikan waktu, bimbingan, pengarahan, saran, dan ilmu yang sangat
bermanfaat selama penulisan skripsi ini.
6. Bapak Heru Pratomo Al. M.Si selaku penguji utama, atas pertanyaan, kritik,
dan saran yang diberikan.
7. Ibu Dr. Isana Supiah YL. selaku penguji pendamping, atas pertanyaan, kritik,
dan saran yang diberikan.
8. Seluruh Dosen, Staf, dan Laboran Jurusan Pendidikan Kimia FMIPA UNY
yang telah banyak membatu selama perkuliahan dan penelitian.
9. Seluruh pihak yang telah membantu terselesaikannya skripsi ini yang tidak
bisa penulis sebutkan satu persatu.
Penulis menyadari bahwa skripsi ini jauh dari kesempurnaan, oleh karena itu
penulis mengharapkan kritik dan saran yang membangun dari berbagai pihak
demi kesempurnaan skripsi ini. Semoga skripsi ini dapat bermanfaat bagi kita
semua. Amin.
Wassalamu‟alaikum Warahmatullahi Wabarakatuh
Yogyakarta, Oktober 2016
xi DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN ... ii
HALAMAN PERNYATAAN ... iii
HALAMAN PENGESAHAN ... iv
HALAMAN MOTTO ... v
HALAMAN PERSEMBAHAN ... vi
ABSTRAK ……… vii
ABSTRACT ……….. viii
KATA PENGANTAR ... ix
DAFTAR ISI ... xi
DAFTAR TABEL ... xiii
DAFTAR GAMBAR ... xiv
DAFTAR LAMPIRAN ... xv
BAB I PENDAHULUAN A.Latar Belakang ... 1
B. Identifikasi Masalah ... 4
C.Batasan Masalah ... 5
D.Rumusan Masalah ... 5
E. Tujuan Penelitian ... 6
F. Manfaat Penelitian ... 6
BAB II KAJIAN TEORI A.Kerangka Teori ... 7
1. Tanaman Pandan Laut ... 7
2. Selulosa ... 8
3. Selulosa Asetat ... 9
4. Litium Klorida (LiCl) ... 12
5. Baterai Ion Litium... 12
xii
7. Karakterisasi Membran Selulosa Asetat ... 14
a. Analisis FTIR ... 14
b. Foto Permukaan dengan Mikroskop Optik... 15
c. Uji Konduktivitas ……….. 16
8. Penelitian Relevan ... 17
9. Kerangka Berpikir... 18
BAB III METODE PENELITIAN A.Subjek dan Objek Penelitian ... 20
B. Alat dan Bahan Penelitian ... 21
C.Prosedur Penelitian ... 21
D.Teknik Analisis Data ... 26
BAB IV HASIL PENELITIAN DAN PEMBAHASAN A.Hasil penelitian... 28
1. Karakter Selulosa dan Selulosa Asetat Hasil Sintesis ……….……. 28
2. Uji Konduktivitas dengan Elkahfi 100 ………. 30
3. Gugus fungsi Membran Elektrolit Selulosa Asetat ……….. 30
4. Foto Mikroskop Optik ……….. 32
B. Pembahasan ... 33
1. Isolasi Selulosa dan Sintesis Selulosa Asetat... 34
2. Pembuatan Membran Elektrolit Selulosa Asetat... 38
3. Uji konduktivitas……….. 39
4. Karakterisasi Membran Elektrolt Selulosa Aset………….………. 40
a. Gugus Fungsi Membran Selulosa Asetat………. 40
b. Analisi Foto Permukaan dengan Mikroskop Optik ……... 41
BAB V KESIMPULAN DAN SARAN A.Kesimpulan ... 43
B. Saran ... 43
DAFTAR PUSTAKA ... 45
xiii
DAFTAR TABEL
Halaman
Tabel 1. Hubungan Derajat Substitusi dan Persen Asetil Selulosa Asetat... 10
Tabel 2. Absorpsi Inframerah Beberapa Gugus Fungsi Organik... 15
Tabel 3. Puncak serapan spektrum FTIR standar... 26
Tabel 4. Sifat Fisik Selulosa dan Selulosa Asetat dari Pandan Laut …...… 28
Tabel 5. Interprestasi Gugus Fungsi Spektrum FTIR Selulosa dan Selulosa Asetat Hasil Sintesis... 29
Tabel 6. Nilai Konduktivitas Membran elektrolit selulosa asetat pada berbagai Komposisi DMP... 30
xiv
DAFTAR GAMBAR
Halaman
Gambar 1. Tanaman pandan laut (Pandanus tectorius)... 8
Gambar 2. Struktur Selulosa ... 8
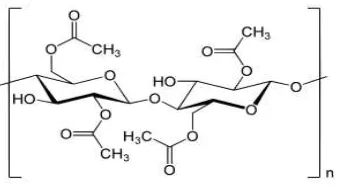
Gambar 3. Struktur Selulosa Asetat …... 9
Gambar 4. Reaksi Sintesis Selulosa Asetat ... 10
Gambar 5. Struktur Baterai Ion Litium ... 13
Gambar 6. Struktur Dimetil Ftalat…….……… 14
Gambar 7. Grafik linier data Elkahfi-100 Hubungan Kuat Arus (I) dengan Tegangan (V)………..………. 27
Gambar 8. Selulosa dan selulosa asetat ... 28
Gambar 9. Spektrum FTIR Selulosa dan Selulosa Asetat dari Daun Pandan Laut... 29
Gambar 10. Spektrum FTIR membran elektrolit selulosa asetat blangko dan penambahan DMP 25%... 31
Gambar 11. Penampang Mikroskop Optik Membran Elektrolit Selulosa Asetat dengan Variasi Konposisi DMP... 32
Gambar 12. Reaksi Bleaching Selulosa ... 34
xv
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Diagram Alir Penelitian ... 49
Lampiran 2. Penentuan Derajat Asetil… ... 53
Lampiran 3. Grafik Uji Konduktivitas ... 54
Lampiran 4. Perhitungan Konduktivitas ……….. 56
Lampiran 5. Gambar spektra FTIR ……….. 58
Lampiran 6. Gambar Foto Mikroskop Optik ………... 60
Lampiran 7. Dokumentasi ……… 61
1 BAB I PENDAHULUAN A. Latar Belakang.
Perkembangan teknologi yang semakin maju membuat meningkatnya
penggunaan perangkat elektronik. Sebuah laporan baru dari Emarketer
(id.techinasia.com) tahun 2014 menyatakan bahwa akan terdapat dua miliar
pengguna smartphone aktif di seluruh dunia pada tahun 2016 dan akan terus
meningkat hingga tahun 2018. Berdasarkan data tersebut, dengan meningkatnya
pengguna smarthphone atau handphone tentunya semakin meningkat pula
konsumsi baterai. Baterai menghasilkan sumber energi untuk peralatan tersebut.
Baterai banyak dikembangkan dalam hal efisiensi yang meliputi
pengembangan sistem penyimpanan energi, salah satunya adalah baterai ion
litium. Baterai ion litium merupakan rangkaian elektrokimia yang terdiri dari
anoda, katoda, dan elektrolit sebagai komponennya. Baterai jenis ini banyak
digunakan karena sifatnya yang dapat diisi ulang, mudah dan fleksibel dalam
penggunaanya. Namun disamping kelebihannya, baterai ion litium mempunyai
kelemahan pada elektrolitnya. Elektrolit yang digunakan pada baterai ion litium
merupakan elektrolit cair dan bersifat tidak terbiodegradasi (Dhika Yetty, 2012).
Sifat elektrolit yang tidak terbiodegradasi dan berbentuk cairan akan
mempunyai dampak pencemaran lingkungan. Selain itu cairan elektrolit akan
mudah terbakar jika baterai mengalami kebocoran (Rikukawa dan Sanui, 2000).
Oleh karena itu, diperlukan suatu elektrolit yang bersifat ramah lingkungan. Salah
2
Membran elektrolit merupakan elektrolit berupa padatan yang bersifat
ramah lingkungan dan dapat terbiodegradasi. Membran elektrolit banyak
dikembangkan karena memiliki banyak keuntungan yaitu dapat mereduksi
kebocoran cairan elektrolit dan memiliki rentang aplikasi terhadap sumber daya
baterai (Bambang R, Akhirudun, dan Ratna, 2004). Salah satu bahan polimer yang
dapat digunakan adalah selulosa asetat.
Selulosa asetat merupakan turunan dari selulosa yang dapat diperoleh dari
reaksi esterifikasi yang salah satunya menggunakan asam asetat anhidrida
(Cequeira, Filho, dan Meireles, 2007). Selulosa asetat memiliki keunggulan dalam
sifat fisik sehingga banyak digunakan sebagai serat untuk tekstil, plastik, filter
rokok, dan membran (Indra Surya, 2013). Selain itu selulosa asetat juga bersifat
dapat diuraikan, tidak mudah terbakar dan dapat diperbaharui (Mohebby, Talaii,
dan Najafi, 2007).
Selulosa asetat mudah diproduksi melalui proses esterifikasi. Selulosa
yang digunakan untuk sintesis selulosa asetat dapat diisolasi dari
tumbuhan-tumbuhan terutama pada batang maupun daun. Indonesia yang merupakan negara
dengan kekayaan keanekaragaman hayati yang melimpah, tentunya banyak
tanaman yang berpotensi tinggi mengandung selulosa, salah satunya adalah
pandan laut (Pandanus tectorius).
Pandan laut merupakan tanaman yang mudah tumbuh di kawasan pantai
Indonesia. Pemanfaatan tanaman pandan laut sebatas pada daunnya yang
3
limbah. Daun pandan laut mengandung selulosa sebesar 81,6% yang dapat
diperoleh dari pelarutan alkali dan bleaching (Sheltami, dkk, 2012).
Sebagai membran, selulosa asetat memiliki beberapa keuntungan yaitu
diantaranya mudah diproduksi dan bahan mentahnya merupakan sumber yang
dapat diperbaharui (Dwi, Tri, dan Sari, 2009). Namun tidak semua jenis polimer
dapat dikembangkan menjadi membran elektrolit. Menurut Meyer, dkk dalam
(Marfuatun, 2011), salah satu syarat dari membran elektrolit ialah mempunyai
konduktivitas ion yang tinggi yaitu lebih dari 10-5 Scm-1.
Pembuatan membran elektrolit selain dibutuhkan konduktivitas yang
tinggi juga diperlukan pula sifat mekanik yang lentur dan fleksibel. Oleh karena
itu dalam pembuatan membran elektrolit dibutuhkan bahan tambahan berupa
pemlastis. Pemlastis diharapkan dapat meningkatkan sifat fisik maupun
konduktivitas membran elektrolit. Dimetil Ftalat atau Dimethyl phthalate (DMP)
merupakan bahan pemlastis yang dapat meningkatkan kerapatan suatu membran
sehingga dapat berpengruh pada elastisitas yang dihasilkan (Ali Muhammad,
Soliha, dan Fauzia, 2006).
Pada penelitian ini, dalam pembuatan membran elektrolit selulosa asetat
dari daun pandan laut dilakukan beberapa tahapan yaitu isolasi selulosa dari daun
pandan laut, yang selanjutnya dilakukan proses asetilasi untuk memperoleh
selulosa asetat, pen-doping-an garam LiCl dan penambahan bahan pemlastis DMP
dengan metode casting larutan polimer. Metode casting larutan polimer
digunakan karena menghasilkan konduktivitas tinggi dibandingkan dengan
4
elektrolit selulosa asetat hasil sintesis dilakukan dengan menggunakan
spektrofotometer FTIR (Fourier Transform Infrared) untuk mengidentifikasi
gugus fungsi yang ada pada membran. Elkahfi 100 digunakan untuk mengetahui
nilai konduktivitas pada membran, dan analisis foto permukaan menggunakan
mikroskop optik.
B. Identifikasi Masalah
Berdasarkan latar belakang masalah yang telah diuraikan, maka dalam
penelitian ini masalah yang dapat diidentifikasi adalah:
1. Membran elektrolit yang digunakan pada baterai ion litium dalam bentuk
cairan yang tidak mudah terdegradasi sehingga perlu dikembangkan membran
elektrolit berupa padatan yang mudah terdegradasi.
2. Pemanfaatan daun pandan laut di Indonesia yang belum optimal.
C. Batasan masalah
Berdasarkan identifikasi masalah yang telah disampaikan, maka penelitian
ini memiliki batasan masalah antara lain:
1. Sintesis selulosa asetat dilakukan dengan asetilasi selulosa dari daun pandan
laut.
2. Pen-doping-an garam litium menggunakan metode casting larutan polimer dan
garam litium yang digunakan adalah LiCl.
3. Jenis pemlastis yang ditambahkan dalam pembuatan membran adalah DMP
5
4. Karakteristik menggunakan Elkahfi 100, FTIR,dan mikroskop optik.
D. Rumusan Permasalahan
Berdasarkan uraian di atas, maka rumusan masalah yang diangkat dalam
penelitian ini antara lain:
1. Bagaimana pengaruh komposisi DMP terhadap nilai konduktivitas membran
elektrolit selulosa asetat dari daun pandan laut?
2. Bagaimana karakter membran elektrolit selulosa asetat hasil pen-doping-an
berdasarkan spektra FTIR, dan foto permukaan?
E. Tujuan Penelitian
Penelitian ini memiliki tujuan sebagai berikut:
1. Mengetahui pengaruh komposisi pemlastis DMP terhadap nilai konduktivitas
membran selulosa asetat dari daun pandan laut.
2. Mengetahui karakter membran selulosa asetat berdasarkan spektrum FTIR,
dan foto permukaan.
F. Manfaat Penelitian
Manfaat yang diharapkan dari penelitian ini ialah:
1. Memberikan solusi dalam pemanfaatan selulosa dari bahan alam seperti daun
pandan laut.
2. Meningkatkan nilai ekonomi dari daun pandan laut.
6 BAB II TINJAUAN PUSTAKA A. Kerangka Teori
1. Tanaman Pandan Laut
Pandanus tectorius atau disebut juga pandan laut banyak dijumpai dan
menjadi pemandangan umum di daerah pantai. Asal mula tanaman ini dari
Australia Timur dan Kepulauan Pasifik. Berikut merupakan klasifikasi dari
pandan laut:
Kingdom : Plantae
Divisi : Magnoliophyta
Kelas : Liliopsida
Ordo : Pandanales
Family : Pandanaccae
Genus : Pandanus
Spesies : Pandanus tectorius
Jenis pandan ini merupakan salah satu sumber daya yang dipergunakan
secara luas untuk produksi tenun, makanan, dan obat-obatan. Pandan laut telah
banyak digunakan bagian daunnya untuk bahan kerajinan tangan seperti anyaman
tas, topi, meja dan kursi (Giesen, dkk, 2006).
Daun pandan laut (Pandanus tectorius) memiliki komponen kimia antara
lain selulosa 37,3±0,6%, hemiselulosa 34,4±0,2%, pentosa 15,7±0,5%, lignin dan
abu 24,3±0,8%, dan ekstraktif 2,5±0,02 (Sheltami, dkk, 2012). Adapun ciri fisik
7
Gambar 1. Tanaman pandan laut
2. Selulosa
Selulosa merupakan polisakarida yang terdiri atas satuan glukosa yang
terikat dengan ikatan β-1,4-glykosidik dengan rumus (C6H10O5)n dengan n adalah derajat polimerasinya. Struktur kimia inilah yang membuat selulosa bersifat
kristalin dan tidak mudah larut, sehingga tidak mudah didegradasi secara kimia
atau mekanis. Ketersediaan selulosa dalam jumlah besar akan membentuk serat
yang kuat, tidak larut dalam pelarut organik dan berwarna putih.
Terdapat dua sumber utama selulosa yaitu tumbuhan dan serat selulosa
yang dihasilkan oleh bakteri atau disebut bacterial cellulose (BC). Serat selulosa
dari tumbuhan memilik keunggulan yaitu jumlah bahan baku yang sangat
melimpah dan mudah didapat. Struktur selulosa ditunjukkan pada Gambar 2.
8 3. Selulosa asetat
Selulosa asetat merupakan asam sintetik ester selulosa yang berupa
padatan putih. Selulosa yang digunakan untuk pembuatan selulosa asetat harus
memiliki kemurnian yang tinggi. Hal yang perlu diperhatikan dalam pembuatan
selulosa asetat ialah pemurnian selulosanya (Khairil Anwar, 2006). Struktur
selulosa asetat dapat dilihat pada Gambar 3.
Gambar 3. Struktur Selulosa Asetat (Nurhayati dan Rinta K, 2014)
Dietrich Fengel dan Gerd Wegener (Dian Cipta S, 2012) menyatakan
bahwa kereaktifan gugus –OH pada selulosa menyebabkan masuknya gugus asetil. Jenis dan sifat selulosa asetat tergantung pada derajat substitusinya atau
derajat asetilnya. DS menyatakan banyaknya gugus –OH pada selulosa yang tergantikan oleh gugus asetil. Menurut (Indra Surya, dkk, 2013), berdasarkan
DS-nya selulosa asetat dibagi menjadi tiga yaitu:
1. Selulosa monoasetat dengan DS 0<DS<2 larut dalam aseton.
2. Selulosa diasetat dengan DS 2,0-2,8 dengan kandungan % asetilasinya 35 – 43,5%.
3. Selulosa triasetat dengan DS 2,8-3,5 mempunyai kandungan asetil
43,5-44,8%.
Derajat asetil merupakan ukuran jumlah asam asetat yang diesterifikasi
9
substitusinya. Menurut Fengel (Indra Surya, dkk, 2013), bahwa hubungan antara
derajat substitusi dengan derajat asetil dapat dilihat pada Tabel 1.
Tabel 1. Hubungan DS dan Derajat Asetil Selulosa Asetat No. Derajat
substitusi
Derajat asetil (%)
Pelarut yang lazim
Aplikasi
1 0,6-0,9 13,0-18,7 Diklorometan - 2 1,2-1,8 22,2-32,2 Metoksietanol Plastik 3 2,2-2,7 36,5-42,2 Aseton Benang, Film 4 2,8-3,0 43,0-44,8 Kloroform Kain pembungkus
Pada sintesis selulosa asetat terdiri dari tahap penggembungan (swelling)
tahap asetilasi dan tahap hidrolisis (Wafiroh, 2012). Umumnya hidrolisis
dilakukan paada suhu 40oC-50oC agar struktur selulosa tidak rusak. Waktu
hidrolisis akan berpengaruh terhadap kadar asetil yang diperoleh (Febri Rufian P.,
2006). Berdasarkan Galuh Yuliani (Muhammad Lindu, Tita, dan Ismi Erna 2010),
waktu hidrolisis optimum selulosa membutuhkan waktu esterifikasi selama 20
jam dengan suhu 40 oC.
Menurut (Nurhayati dan Rinta Kusumawati, 2014) reaksi sintesis selulosa
asetat dari selulosa dapat dilihat pada Gambar 4:
Gambar 4. Reaksi Sintesis Selulosa Asetat
Selulosa asetat banyak dimanfaatkan salah satunya sebagai membran.
10
pemisah selektif antara dua fasa karena bersifat semipermiabel. Berdasarkan
asalnya, membran dapat diklasifikasikan menjadi membran polimer, membran
anorganik, dan membran biologi (Widayanti, 2013). Membran polimer
merupakan jenis membran yang dapat diaplikasikan sebagai membran elektrolit.
Meyer, Aurora dan Zhang dalam (Marfuatun, 2011), menyatakan suatu membran
dapat diaplikasikan menjadi membran elektrolit jika memenuhi syarat antara lain
mempunyai kekuatan mekanik yang cukup tinggi untuk menahan tekanan antara
katoda dan anoda, bersifat inert dan mempunyai konduktivitas yang tinggi.
4. Litium klorida (LiCl)
Litium merupakan logam pertama dari golongan alkali. Litium tidak dapat
ditemukan di alam dalam keadaan bebas, namun dalam bentuk senyawa. Litium
yang bersenyawa hanya ditemukan 0,0007% dalam kerak bumi, biasanya
ditemukan dalam batuan api dan dalam air mineral. Sumber utama litium
diperoleh dari mineral spedumen, LiAlSi2O6. Litium terdapat dalam air laut
hingga kira-kira 0,1 ppm massa. Litium memiliki densitas setengah dari air, litium
merupakan unsur yang paling kecil rapat massanya dibandingkan dengan semua
unsur padatan pada temperatur dan tekanan kamar. (Kristian H. Sugiyarto, 2003:
86-89). Litium mempunyai standar potensial reduksi paling negatif daripada
unsur-unsur lain yaitu:
Li+ (aq)+ e Li (s) Eo = -3,05 V
Densitas muatan litium sangat besar dibandingkan logam alkali lainnya
11
bahkan LiCl banyak larut dalam pelarut dengan polaritas rendah seperti etanol dan
akuades sehingga ikatan senyawa litium mempunyai tingkat kovalensi yang cukup
tinggi. (Kristian H. Sugiyarto, 2003: 86-89).
LiCl merupakan garam kristalin yang sering digunakan sebagai bahan
elekrolit cair dalam baterai ion litium (Bambang Prihandoko, 2010). Bentuk dari
LiCl berupa kristal putih yang terdapat dalam bentuk hidrat. LiCl memiliki titik
lebur yang sangat tinggi yaitu lebih dari 600oC dan kelarutannya yang sangat baik
dalam akuades (Nourma Sari, 2012). LiCl dapat diperoleh dari reaksi litium
karbonat dengan asam klorida. Adapun reaksinya sebagai berikut:
Li2CO3(s)+ HCl(aq) 2 LiCl(s) + CO2(g) + H2O(l)
Selain itu litium dapat diperoleh dari larutan litium klorida melelui reaksi
elektrolisis. Berikut merupakan reaksi elektrolisis dari larutan LiCl:
Katoda: Li+ (aq) + 2 e- → 2Li(s) Anoda: 2Cl‾(aq) → Cl2 (g)+ 2e-
2Li+(aq) + 2Cl-(aq) →2Li(s)+ Cl2 (g)
5. Baterai ion litium
Baterai ion litium termasuk dalam kategori baterai sekunder atau
rechargeable battery. Baterai ion litium memiliki 3 lapisan yang terdiri dari
elektrode positif, elektrode negatif, dan lapisan pemisah. Baterai ion litium dibuat
menggunakan litium kobalt oksida (LiCoO2) atau litium mangan oksida
12
larutan organik yang dioptimasi untuk karbon khusus sebagai larutan elektrolit
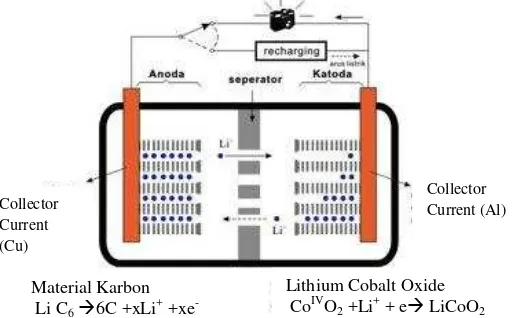
(Prayogo dan Wibowo, 2010). Adapun struktur dari baterai ion litium disajikan
pada Gambar 5.
Gambar 5. Struktur Baterai Ion Litium
Proses penghasilan listrik pada baterai ion litium sebagai berikut: Jika
anoda dan katoda dihubungkan, maka elektron mengalir dari anoda menuju
katoda, bersamaan dengan itu listrik pun mengalir. Pada bagian dalam baterai,
terjadi proses pelepasan ion litium pada anoda, kemudian ion tersebut berpindah
menuju katoda melalui elektrolit. Pada katoda bilangan oksidasi kobalt berubah
dari 4 menjadi 3 karena masuknya elektron dan ion litium dari anoda (Dyah P.
dan Hari S., 2012)
Reaksi yang terjadi pada saat penggunaan baterai (Marfuatun, 2011) ialah
sebagai berikut:
Kutub positif : Li1-xCoO2 +xLi+ + xe LiCoO2
Pemisah : Li+ Polimer
Kutub negatif : C6Lix 6C +xLi+ +xe- Lithium Cobalt Oxide CoIVO
2 +Li+ + e LiCoO2 Material Karbon
Li C6 6C +xLi+ +xe
-Collector Current (Al) Collector
13 6. Dimetil Ftalat
Dimetil Ftalat merupakan pemlastis yang bersifat dapat larut dalam
alkohol, eter, dan kloroform, tetapi tidak dapat larut dalam air. sifat fisik DMP
adalah tidak berwarna dan tidak berbau. DMP memiliki rumus molekul
C6H4(COOCH3)2 dengan bobot molekul 166,14 g/mol. DMP sering digunakan
sebagai pemlastis pada industri plastik polyvinyl chloride (PVC) untuk
menghasilkan plastik polyvinyl chloride yang lebih lentur dan fleksibel (Science
Lab.com, 2006). Struktur DMP dapat dilihat pada Gambar 6.
Gambar 6. Struktur Dimetil Ftalat
7. Karakterisasi Membran Selulosa Asetat a. Analisis gugus fungsi dengan FTIR
Spektrometri Infra merah merupakan suatu metode pengamatan interaksi
dengan radiasi elektromagnetik yang berada pada daerah panjang gelombang
tertentu. Daerah panjang gelombang yang digunakan pada alat spektrofotometer
ini adalah pada daerah infra merah pertengahan yaitu pada panjang gelombang
2,5-50 mikro meter atau pada bilangan gelombang 4000-200 cm-1 (Hardjono
Sastroamidjojo, 2007:45). Informasi adsorpsi inframerah beberapa gugus fungsi
14
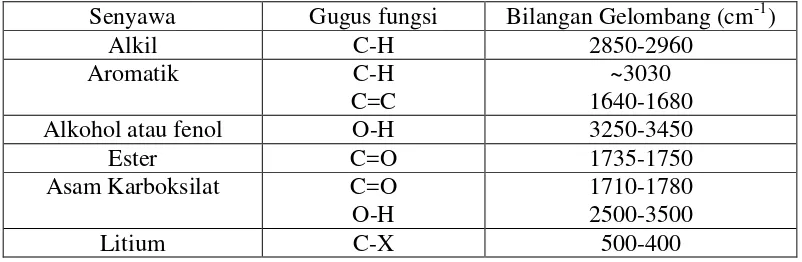
Tabel 2. Absorpsi Inframerah Beberapa Gugus Fungsi Organik
Senyawa Gugus fungsi Bilangan Gelombang (cm-1)
Alkil C-H 2850-2960
Aromatik C-H
C=C
~3030 1640-1680 Alkohol atau fenol O-H 3250-3450
Ester C=O 1735-1750
Asam Karboksilat C=O O-H
1710-1780 2500-3500
Litium C-X 500-400
Absorpsi energi pada beberapa frekuensi dapat dideteksi oleh spektrometer
infra merah dengan memplot jumlah radiasi inframerah yang diteruskan melalui
cuplikan sebagai fungsi frekuensi radiasi yang disebut spektrum inframerah.
Spektrum tersebut akan memberikan informasi gugus fungsional suatu molekul
(Sumar Hendrayana, 1994: 2).
b. Foto Permukaan dengan Mikroskop Optik
Mikroskop merupakan alat bantu yang dapat mengamati bentuk dalam
ukuran kecil (mikroskopis). Mikroskop optik merupakan mikroskop yang
menggunakan cahaya dalam sistem lensa dapat memperbesar tampilan hingga
perbesaran 1000 kali. Informasi yang dapat diperoleh dari analisa menggunakan
mikroskop optik berupa bentuk, ukuran, warna, indeks bias, sudut, dan elongasi
15 c. Uji konduktivitas
Suatu material dapat dibedakan menjadi tiga yaitu isolator,
semikonduktor, dan konduktor. Bahan organik umumnya bersifat konduktor
karena memiliki kandungan air yang sangat tinggi. Konduktivitas merupakan
suatu bahan yang dapat menghantarkan arus listrik. Konduktivitas bergantung
pada sifat material, susunan kimia, serta dimensinya. Sifat konduktivitas pada
suatu material dapat diubah-ubah dengan menambahkan material lain yang biasa
disebut dengan doping yang dapat meningkatkan pembawa mayoritas elektron
atau lubang (hole) pada suatu material (Nurlaily, 2009).
Elkahfi 100 merupakan salah satu alat yang digunakan dalam mengukur
konduktivitas membran yang dirancang untuk mengukur karakterisasi arus
tegangan (IV). Terdiri dari sebuah sumber tegangan dan pikoamperemeter IV
Meter Elkahfi 100 dapat mengukur arus mulai dari 100 pA sampai 3,5 mA. Pada
saat pengukuran, data hasil pengukuran diolah dengan menggunakan software
Elkahfi 100 yang terkoneksi dengan PC (Personal Computer). Elkahfi 100
menggunakan metode two probe (Santi Yuli Astuti, 2011). Metode two probe
merupakan teknik pengukuran untuk mengetahui resistivitas pada bahan
semikonduktor. Cara kerja dalam metode ini dengan menyentuhkan dua titik
kontak yang beraliran listrik pada sampel dengan jarak antar titik kontak yang
telah diatur, kemudian diplotkan pada grafik arus terhadap tegangan. Rumus
resistivitas dapat ditentukan dari bentuk sampel. Sampel thick sheet, merupakan
16
dibandingkan dengan jarak antar probe. Wina Indra Lavina (Nourma Sari, 2012:
16), rumus yang digunakan yaitu:
ρ= x R dan σ ...(1)
keterangan : ρ = Resistivitas bahan (Ω m) R = hambatan (Ohm)
t = ketebalan membran (m)
σ = konduktivitas bahan (S cm-1)
B. PENELITIAN YANG RELEVAN
Penelitian yang relevan mengenai aplikasi selulosa asetat untuk membran
elektrolit baterai ion litium sudah mulai dilakukan. Sheltami, dkk (2012)
mengenai “Extraction Of Cellulose Nanocrystals From Mengkuang Leaves
(Pandanus tectorius)”. Ekstraksi selulosa pandan laut menggunakan pelarut basa
(4% NaOH) dan bleaching dengan NaOCl2 pada pH 4,5 menghasilkan selulosa
sebesar 81,6%.
Arniz Hanifa (2015) mengenai “Sintesis dan Karakterisasi Membran Selulosa Asetat dari Limbah Cair Tahu untuk Aplikasi Baterai Ion Litium”. Pembuatan membran menggunakan dua metode yaitu metode coating dan casting
larutan polimer. Pada metode casting larutan polimer menghasilakan sifat
mekanik yang lebih baik dari metode coating. Pembuatan membran tersebut
didoping dengan garam LiCl dengan konsentrasi 35%. Metode casting larutan
17
Endang WL., Marfuatun, dan Demas (2016) mengenai “ Conductivity of Cellulose Acetate Membranes from Pandan Duri Leaves (Pandanus tectorius) for
Li-ion Battery”. Kondutivitas membran elktrolit selulosa asetat maksimal diperoleh pada pen-doping-an konsentrasi garam LiCl 35%.
David Mecerreyes, dkk (2004) mengenai “Porous polybenzimidazole Membranes Doped with Phosphoric Acid: Highly Proton-Conducting Solid
Electrolytes”. Perbedaan penambahan pemlastis akan meningkatkan kerapatan
pori. Pori-pori membran yang tinggi akan memberikan konduktivitas ion
sebesar 5 × 10-2 Scm-1 pada larutan asam fosfat.
C. KERANGKA BERFIKIR
Dengan meningkatnya penggunaan barang elektronik, meningkat pula
industri baterai ion litium. Baterai ion litium yang berkembang sekarang bersifat
tidak ramah lingkungan. Karena pada umumnya membran elektrolit yang
digunakan pada baterai ion litium merupakan elektrolit yang berupa cairan dan
bersifat tidak terbiodegradasi. Hal ini merupakan salah satu kelemahan dari
baterai ion litium. Sehubungan dengan ini maka diperlukan solusi untuk membuat
membran yang bersifat ramah lingkungan dan bersumber dari bahan yang ramah
lingkungan dan mudah untuk di dapatkan. Salah satunya dengan menggunakan
selulosa asetat yang merupakan turunan dari selulosa. Selulosa diperoleh dari
daun pandan laut.
Pandan laut merupakan tumbuhan yang banyak tumbuh di daerah pesisir
18
pandan laut mengandung selulosa sebesar 81,6% yang dapat diperoleh dari
pelarutan alkali dan bleaching.
Selulosa yang diperoleh dari daun pandan laut kemudian diesterifikasi
dengan menambahkan asam asetat anhidrida dengan katalis H2SO4 sehingga
diperoleh selulosa asetat. Pada tahap asetilasi menggunakan waktu swelling
selulosa 1 jam untuk mengetahui derajat asetil tertinggi. Selulosa asetat hasil
sintesis selanjutnya dikembangkan menjadi membran polimer elektrolit
menggunakan metode casting larutan polimer. Doping garam litium
menggunakan garam LiCl yang selanjutnya dilakukan penambahan pemlastis
DMP untuk meningkatkan sifat mekanik membran elektolit. Membran elektrolit
yang dihasilkan berbentuk padatan yang bersifat ramah lingkungan serta
memiliki konduktivitas yang tinggi.
Berdasarkan hat tersebut, akan dilakukan sintesis membran selulosa asetat
dari daun pandan laut (Pandanus tectorius) untuk aplikasi membran baterai ion
litium dengan penambahan pemlastis DMP. Selulosa yang diperoleh dari daun
pandan laut diasetilasi membentuk selulosa asetat yang selanjutnya ditentukan
derajat asetilnya sehingga dapat diketahui jenis selulosa asetat dan pelarut yang
tepat untuk melarutkan selulosa asetat. Selulosa asetat yang diperoleh kemudian
digunakan untuk sintesis membran dengan pen-doping-an garam LiCl konsentrasi
35% menggunakan metode casting larutan polimer dan penambahan pemlastis
DMP dengan komposisi 10%, 15%, 20%, 25%, dan 30%. Hasil isolasi, asetilasi
dan preparasi membran elektrolit dikarakterisasi menggunakan spektrofotometer
19 BAB III
METODE PENELITIAN A. Subjek dan Objek Penelitian
1. Subjek Penelitian
Subjek penelitian ini adalah membran elektrolit selulosa asetat dari daun
pandan laut.
2. Objek Penelitian
Objek penelitian ini meliputi konduktivitas, gugus fungsi, dan foto
permukaan dari membran elektrolit selulosa asetat.
B. Alat dan Bahan
1. Alat yang digunakan meliputi: a. Pipet volum
b. Hotplate stirrer
c. Neraca analitik
d. Gelas ukur
e. Termometer
f. Gelas beker
g. Erlenmeyer
h. Buret
i. Magnetic stirrer
j. pH meter
k. FTIR
l. Mikroskop optik
m. Elkahfi
n. Penyaring Buchner
o. Kertas saring
p. Pengaduk
q. Pipet tetes
r. Labu ukur
20 2. Bahan yang digunakan
a. Daun pandan laut
b. Natrium hidroksida (Merck)
c. Asam sulfat pekat (Merck)
d. Etanol 96% (Merck)
e. Asam asetat glasial (Merck)
f. Asam asetat glasial 67% (Merck)
g. Asam Asetat anhidrida (Merck)
h. Akuades
i. Asam klorida (Merck)
j. LiCl (Merck)
k. Indikator fenolftalein
l. Dimetil ftalat (Merck)
m. NaOCl
n. Kertas pH
C. Prosedur Penelitian
1. Isolasi Selulosa dari Daun Pandan Laut
Selulosa dapat diperoleh dari daun pandan laut dengan prosedur berikut:
a. Memotong daun pandan laut menjadi bagian-bagian kecil dan menghilangkan
duri dan bagian duri.
21
c. Merendam daun pandan laut di dalam air selama 3 hari dengan mengganti air
rendaman secara berkala.
d. Merebus daun pandan laut selama 20 menit dan mengeringkannya.
e. Melarutkan daun pandan laut dalam NaOH 2M selama 2 jam pada suhu
kamar dan dilanjutkan pada suhu 80 oC dan menyaringnya.
f. Melarutkan daun pandan laut dalam NaOCl 0,5% selama 24 jam pada suhu
kamar dan menyaring.
g. Mencuci dengan aquades beberapa kali hingga pH netral.
h. Mengeringkan dan menimbang serbuk selulosa.
2. Sintesis Selulosa Asetat
Asetilasi selulosa untuk memperoleh selulosa asetat dapat dilakukan
dengan prosedur sebagai berikut:
a. Memasukkan selulosa sebanyak 10 gram ke dalam Erlenmeyer kemudian
menambahkan 24 mL asam asetat glasial dan mengaduk pada suhu 40 oC
dengan waktu 1 jam.
b. Menambahkan H2SO4 pekat sebanyak 0,1 mL dan asam asetat glasial
sebanyak 60 mL kemudian mengaduk selama 45 menit pada suhu kamar.
c. Menambahkan asam asetat anhidrit sebanyak 27 mL (suhu 15oC) pada
campuran (suhu 18oC).
d. Menambahakan H2SO4 pekat 1 mL dan asam asetat glasial sebanyak 60 mL
ke dalam campuran kemudian mengaduk dengan waktu asetilasi selama 0,5
22
e. Menambahakan asam asetat 67% (v/v) sebanyak 30 mL ke dalam campuran
tetes demi tetes selama 2 jam pada suhu kamar dan melanjutkan pengadukan
selama 15 jam pada suhu kamar.
f. Menambahakan akuades tetes demi tetes dan diaduk hingga diperoleh
endapan yang berbentuk serbuk.
g. Menyaring endapan dengan penyaring Buchner. Mencuci sampai netral dan
mengeringkan selulosa yang dihasilkan.
3. Penentuan derajat asetil
Penentuan derajat asetil dapat dilakukan dengan prosedur sebagai berikut:
a. Menimbang selulosa asetat sebanyak 0,5 gram dan memasukkan ke dalam
labu erlenmeyer 250 mL.
b. Menambahkan 20 mL alkohol 75% dan mengaduk campuran pada suhu 50°C
selama 30 menit.
c. Menambahkan NaOH 0,5 M sebanyak 20 mL ke dalam campuran dan
mengaduknya selama 15 menit pada suhu 50-60 °C.
d. Mengaduk campuran selama 3 hari pada suhu ruang.
e. Menetesi campuran dengan indikator fenolftalein dan mentitrasi dengan HCl
0,5 M.
f. Menambahkan HCl 1 mL ke dalam campuran titrasi dan mengaduk terus
menerus selama 22 jam.
g. Mentitrasi kembali campuran dengan NaOH 0,1 M dengan menambahakan
23
4. Pen-doping-an selulosa asetat dengan metode casting larutan polimer a. Melarutkan selulosa asetat sebanyak 0,9 gram dengan asam asetat glasial.
b. Menambahkan DMP dengan variasi 10%, 15%, 20%, 25% dan 30% ke dalam
selulosa asetat yang telah larut.
c. Menambahkan garam LiCl 35 % kemudian mengaduk campuran selama 24
jam.
d. Mencetak campuran tersebut ke dalam cawan petri dan membiarkan pelarut
menguap hingga diperoleh membran elektrolit.
5. Tahap karakterisasi Selulosa Asetat dan Membran Selulosa Asetat a. Uji Konduktivitas Menggunakan Elkahfi 100.
Uji konduktifitas digunakan untuk mengetahui seberapa baik sampel dapat
menghantarkan arus listrik. Elkahfi 100 merupakan alat untuk menguji daya
hantar sampel. Metode yang digunakan merupakan metode two probe yaitu
metode pengukuran untuk mengetahui resistivitas pada bahan semikonduktor.
Metode ini dilakukan dengan menyentuhkan dua jarum kontak yang telah dialiri
arus. Dua jarum yang disentuhkan dan diatur jaraknya kurang lebih 0,5 cm.
Sampel dengan ukuran 1 cm x 1 cm dimasukkan ke plat kaca dan dijepit dua
kutub beraliran listrik kemudian dianalisis Metode ini akan memperoleh data
berupa arus (I) dan tegangan (V). Alat ini berada di laboratorium Elektro dan
24 b. Foto permukaan dengan mikroskop optik
Foto permukaan suatu membran dapat diamati menggunakan mikroskop
optik. Pengamatan menggunakan mikroskop optik dilakukan dengan perbesaran
100 kali dengan lensa Nikon. Mikroskop optik ini berada di laboratorium Biologi
Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Negeri Yogyakarta
(FMIPA UNY).
c. Analisa Gugus Fungsi dengan FTIR
FTIR dapat menganalisa gugus fungsi suatu sampel baik dalam bentuk
serbuk. Analisa FTIR berupa serbuk berada di laboratorium terpadu Universitas
Islam Indonesia (UII). Metode yang digunakan dalam preparasi sampel adalah
dengan menggunakan pellet KBr. Adapun tahapan preparasi sampel sebagai
berikut:
1) Sampel padat yang akan dianalisis dicampur terlebih dahulu dengan serbuk
KBr (5%-10% sampel dalam serbuk KBr), haluskan dengan mortar.
Campuran yang sudah homogen dan dibuat pellet dengan alat mini hand
press.
2) Pelet KBr ditempatkan pada tempat sampel. Sampel dianalisis dengan
menggunakan FTIR pada daerah 400-4000cm-1, sehingga diperoleh spektrum
FTIR. FTIR digunakan untuk melihat puncak serapan dari gugus fungsi yang
25 D. Teknik Analisis Data
1. Penetuan Derajat asetil.
Penentuan derajat asetil bertujuan untuk mengetahui kandungan asetil
yang terdapat dalam selulosa asetat hasil sintesis dari serat daun pandan laut
sehingga golongan selulosa asetat tersebut dapat diketahui. Derajat asetil dihitung
dengan persamaan:
Derajat Asetil (%) = (3)
Keterangan :
A = Volume NaOH yang diperlukan untuk titrasi sampel B = Volume NaOH yang diperlukan untuk titrasi blangko C = Volume HCL yang diperlukan untuk titrasi sampel D = Volume HCL yang diperlukan untuk titrasi blangko Ma = Molaritas sampel HCL
Mb = Molaritas sampel NaOH N = derajat asetil
W = Massa sampel
2. Karakterisasi Gugus Fungsi
Analisis spektrum FTIR dapat dilakukan dengan cara menginterpretasi dan
membandingkan spektrum FTIR hasil sintesis. Puncak serapan spektrum FTIR
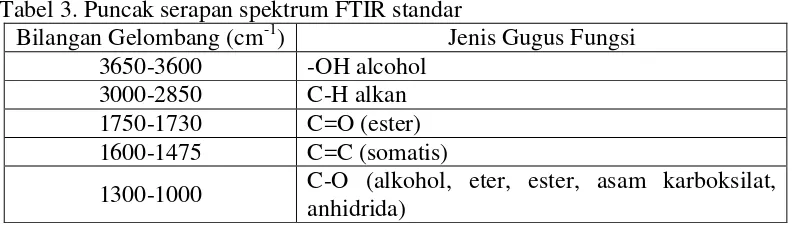
[image:40.595.114.515.532.645.2]standar ditunjukkan pada Tabel 3.
Tabel 3. Puncak serapan spektrum FTIR standar
Bilangan Gelombang (cm-1) Jenis Gugus Fungsi 3650-3600 -OH alcohol
3000-2850 C-H alkan 1750-1730 C=O (ester) 1600-1475 C=C (somatis)
26 3. Penentuan Nilai Konduktivitas
Konduktivitas listrik merupakan kemampuan suatu bahan untuk
menghantarkan arus listrik. Data elkahfi 100 diperoleh data berupa besaran arus
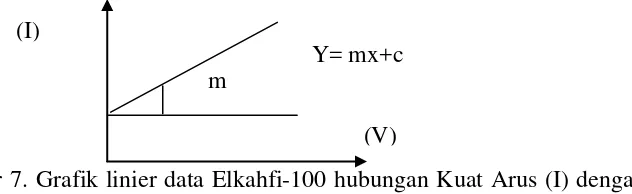
[image:41.595.187.503.216.313.2]dan tegangan kemudian dibuat grafik linier seperti pada Gambar 7.
Gambar 7. Grafik linier data Elkahfi-100 hubungan Kuat Arus (I) dengan Tegangan (V)
Berdasarkan Gambar 7 gradien garis (m) merupakan nilai konduktansi (G=1/R).
Menghitung nilai konduktivitas dari alat elkahfi 100 dapat dicari dengan
persamaan sebagai berikut:
ρ
eterangan:
ρ = resistivitas (Ω cm) t = tebal membran (cm)
R = resistensi (ohm)
m
Y= mx+c
27 BAB IV
HASIL PENELITIAN DAN PEMBAHASAN A. Hasil Penelitian
1. Karakter Selulosa dan Selulosa Asetat Hasil Sintesis
Hasil pengamatan terhadap sifat fisik selulosa dan selulosa asetat yang
[image:42.595.112.523.411.577.2]dihasilkan dari daun pandan laut secara rinci dapat dilihat pada Tabel 4.
Tabel 4. Sifat Fisik Selulosa dan Selulosa Asetat dari Pandan Laut No. Sifat yang diamati Hasil pengamatan
Selulosa Selulosa asetat 1. Bentuk Serbuk berserat Serbuk halus
2. Warna Putih kecoklatan Putih
3. Tekstur Kasar dan ringan Halus dan ringan 4. Bau Tidak berbau Tidak berbau 5. Kelarutan dalam air Tidak larut Tidak larut
Adapun gambar dari selulosa dan selulosa asetat hasil sintesis dapat dilihat pada Gambar 8.
(a) (b)
Gambar 8. (a) Selulosa, dan (b) Selulosa Asetat
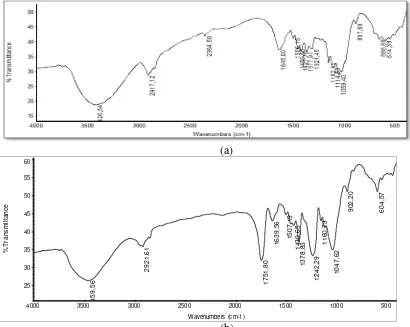
Untuk spektrum FTIR selulosa dan selulosa asetat dari daun pandan laut
[image:42.595.266.508.437.578.2]28 (a) 6 0 4 ,5 7 9 0 2 ,2 0 1 0 4 7 ,6 2 1 1 6 0 ,7 3 1 2 4 2 ,2 9 1 3 7 8 ,8 3 1 4 3 0 ,6 5 1 5 0 7 ,1 9 1 6 3 9 ,5 6 1 7 5 1 ,8 0 2 9 2 1 ,6 1 3 4 5 9 ,5 6 25 30 35 40 45 50 55 60 % T ra n sm it ta n ce 500 1000 1500 2000 2500 3000 3500 4000 Wavenumbers (cm-1) (b)
Gambar 9. Spektrum FTIR (a) Selulosa, dan (b) Selulosa Asetat dari Daun Pandan Laut
Adapun interpretasi gugus fungsi spektrum FTIR selulosa dan selulosa
asetat dapat dilihat pada Tabel 5.
Tabel 5. Interprestasi Gugus Fungsi Spektrum FTIR Selulosa dan Selulosa Asetat Hasil Sintesis
No Jenis gugus fungsi Bilangan gelombang
Selulosa (cm-1) Selulosa asetat(cm-1)
1. -OH ulur 3426,54 3459,56
2. C=O ester - 1751,80
3. C-H tekuk 1427,76 1430,65
4. C-O ulur 1059,40 1047,62
[image:43.595.113.521.558.662.2]29 2. Uji Konduktivitas dengan Elkahfi 100
Berdasarkan penelitian, harga konduktivitas membran elektrolit selulosa
asetat dengan variasi konsentrasi garam litium 35% serta penambahan DMP
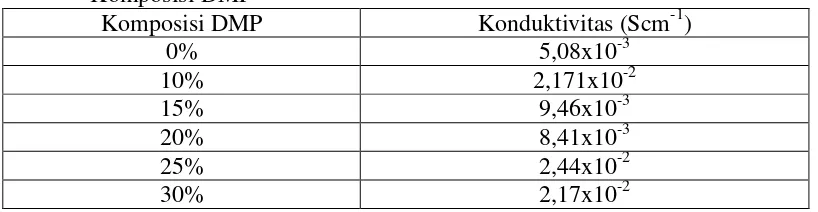
[image:44.595.111.520.219.325.2]dengan berbagai variasi komposisi dapat dilihat pada Tabel 8.
Tabel 6. Nilai Konduktivitas Membran elektrolit selulosa asetat pada berbagai Komposisi DMP
Komposisi DMP Konduktivitas (Scm-1)
0% 5,08x10-3
10% 2,171x10-2
15% 9,46x10-3
20% 8,41x10-3
25% 2,44x10-2
30% 2,17x10-2
3. Gugus Fungsi Membran Elektrolit Selulosa Asetat
Spektrum membran elektrolit selulosa asetat blangko dengan membran
elektrolit selulosa asetat DMP 25% dapat dilihat pada Gambar 10.
[image:44.595.125.501.458.625.2]30
Interpretasi gugus fungsi spektrum FTIR membran elektrolit selulosa
[image:45.595.253.501.533.671.2]asetat dengan DMP25% dan membran blangko dapat dilihat pada Tabel 7.
Tabel 7. Interprestasi Gugus Fungsi Spektrum FTIR Membran Elektrolit Selulosa Asetat dengan DMP 25% dan Membran Blangko
No Gugus Fungsi
Membran blangko Membran elektrolit selulosa asetat dengan
DMP 25% Bilangan gelombang
(cm-1)
Bilangan gelombang (cm-1)
1. -OH ulur 3439,08 3431,39
2. C=O 1638,94 1638,26
3. C=O ester - 1737,69
4. C-H Tekuk 1382,26 1380,06
5. C-O-C 1250,69 1126,78
C-O ester 1054,75 1051,88
6. Li- 620,89 604,01
7. C=C aromatik - 1436,51
4. Foto Mikroskop Optik
Foto permukaan membran elektrolit dengan pemlastis DMP dalam
berbagai variasi komposisi dapat dilihat pada Gambar 11.
31
DMP 20% DMP 25%
[image:46.595.114.504.81.415.2]DMP 30% Blangko
Gambar 11. Penampang Mikroskop Optik Membran Elektrolit Selulosa Asetat dengan Variasi Komposisi DMP
B. Pembahasan
1. Isolasi Selulosa dan Sintesis Selulosa Asetat
Selulosa yang digunakan merupakan hasil ekstraksi dari daun pandan laut.
Pandan laut yang telah dibersihkan, dihilangkan bagian tengah dan duri yang ada
kemudian dikeringkan dan digiling hingga halus. Setelah didapatkan serat yang
halus, kemudian dilakukan penghilangan kandungan gula pentosa, tanin, dan zat
pigmen dalam daun dengan perendaman air selama 3 hari dan kemudian
32
hemiselulosa dan lignin atau delignifikasi dengan cara direndam dengan NaOH
dan NaOCl.
Adanya lignin dalam senyawa tersebut ditandai dengan adanya larutan
yang berwarna hitam pekat (black liquor). Indikasi hilangnya lignin dalam sampel
dapat diidentifikasi dari sampel filtrat yang berwarna jernih dan dengan cara
ditetesi asam sulfat pekat, jika lignin sudah hilang dari sampel maka filtrat tidak
menghasilkan endapan. Karena lignin dalam asam sulfat akan membentuk
gumpalan (Dhika Yetty, 2012).
Setelah perendaman dengan NaOH, proses selanjutnya ialah pemutihan
(bleaching) dengan menggunakan larutan NaOCl dan penambahan NaOH padat.
Penambahan NaOH padat akan mempercepat jalannya proses bleaching, karena
senyawa NaOCl bekerja optimum pada pH 7 (netral). Selain itu penambahan
NaOH membantu proses pelarutan lignin yang masih tersisa. Pada proses ini
terjadi reaksi :
OCl-(aq) + H2O(aq) OH-(aq) + HOCl(aq)
HOCl merupakan senyawa yang tidak stabil sehingga akan mengoksidasi zat lain
membentuk klor bebas.
HOCl(aq) + H+(aq) + Cl-(aq) Cl2(aq) + H2O(l)
Menurut Yetty (Demas Aji, 2016), klor yang dihasilkan akan mengoksidasi
pigmen daun pandan laut sehingga mengubah warna menjadi lebih putih. Reaksi
33
Gambar 12. Reaksi Bleaching Selulosa
Selulosa yang dihasilkan berwarna putih kecoklatan dan berserat. Selulosa
yang didapat diidentifikasi gugus fungsi menggunakan spektrofotometer FTIR.
Berdasarkan Tabel 5 memperlihatkan puncak serapan pada daerah 3426,54 cm-1
menandakan adanya vibrasi regang –OH, puncak daerah 1427,76 cm-1 menandakan C-H, dan pada puncak serapan 1059,40 cm-1 menandakan C-O ulur.
Setelah dapat dipastikan sampel yang diperoleh merupakan selulosa, kemudian
selulosa disintesis menjadi selulosa asetat melalui proses asetilasi. Hasil isolasi
daun pandan laut didapatkan selulosa seperti pada Gambar 8.
Proses pembuatan selulosa asetat dilakukan melalui 3 tahap. Tahap
pertama adalah menambahkan asam asetat glasial yang bertujuan untuk menarik
air yang masih tersisa di dalam selulosa yang tidak diharapkan. Adanya air pada
selulosa akan mengganggu jalannya proses asetilasi. Selain itu, asam asetat glasial
menyebabkan terjadinya swelling (penggembungan) pada serat-serat selulosa.
Adanya penggembungan dapat memperluas permukaan selulosa yang dapat Selulosa
Selulosa
Selulosa
34
membantu peningkatan reaktivitas selulosa terhadap reaksi asetilasi (Muhammad
Lindu, Tita, dan Ismi Erna 2010).
Tahap kedua adalah asetilasi dengan penambahan anhidrida asetat dengan
katalis asam sulfat. Reaksi asetilasi berlangsung secara eksoterm, sehingga
pencampuran selulosa asetat dengan asam asetat anhidrida dikondisikan pada
suhu rendah yaitu 15oC-18oC. Pengadukan dilakukan pada suhu ruang agar tidak
terjadi depolimerasi rantai selulosa. Depolimerasi mengakibatkan selulosa
berubah menjadi senyawa yang lebih sederhana, sehingga akan mengakibatkan
produk asetilasi yang dihasilkan menurun.
Asam sulfat bereaksi dengan anhidrida asetat membentuk asetil sulfat,
yang kemudian bereaksi dengan selulosa membentuk selulosa asetat. Proses
asetilasi dapat terjadi reaksi berikut:
2H2SO4(l) + (CH3CO)2O(l) 2CH3COOSO3H(l) + H2O(l)
Asam sulfat bereaksi dengan selulosa menggantikan gugus –OH dengan gugus – OSO3H. Dalam proses ini asam sulfat tidak tersisa dalam larutan dan telah
bereaksi dengan selulosa dan menghasilkan produk sebagai berikut (Asrining P,
2010):
Rsel (OH)3(l) +H2SO4(l) +3(CH3CO)2O(l) Rsel H2SO4 + 4CH3COOH(l)
(CH3COO)2
Pada proses asetilasi ini, gugus sulfat akan lepas dan digantikan oleh gugus asetil.
Tahap ketiga adalah hidrolisis dimana larutan direaksikan dengan asam
asetat 67% (Cynthia L dan Senny, 2007). Penambahan larutan asam asetat 67%
35
anhidrida menjadi asam asetat (Wafiroh, 2012). Proses ini dilakukan selama 22
jam. Besarnya kadar asetil yang dihasilkan tergantung pada lamanya proses
hidrolisis. Semakin lama proses hidrolisis maka semakin lama terjadinya proses
deasetilasi sehingga semakin kecil kadar asetil yang dihasilkan.
Larutan hasil hidrolisis direndam pada air es sehingga akan terlihat
endapan putih. Kemudian endapan disaring menggunakan Buchner dan dicuci
dengan aquades hingga netral. Tujuan dari proses tersebut untuk menghilangakan
zat pengotor dan asam asetat yang masih tersisa. Endapan hasil penyaringan
dikeringkan pada udara terbuka hingga didapatkan serbuk putih.
Pada dasarnya reaksi dalam sintesis selulosa asetat merupakan pergantian
satu, dua, atau tiga gugus hidroksil dalam unit glukosa dengan adanya katalis
asam. Gugus-gugus hidroksil pada selulosa dapat diesterifikasi dengan asam
karboksilat menghasilkan suatu gugus ester (Tresnawati, 2006). Sampel yang
dihasilkan dianalisis menggunakan FTIR.
Berdasarkan Gambar 8 dan Tabel 4 memperlihatkan hasil analisis dengan
FTIR adanya perbedaan serapan antara selulosa dan selulosa asetat, yaitu pada
puncak serapan 1751,80 cm-1 menandakan adanya C=O ester dan 1242,29 cm-1
puncak serapan C-O-C ester. Puncak serapan tersebut manandakan gugus asetil
36
2. Pembuatan Membran Elektrolit Selulosa Asetat
Pencetakan membran elektrolit selulosa asetat menggunakan metode
casting larutan polimer, yaitu semua bahan dilarutkan hingga homogen dan
dicampur kemudian di bentuk pada suatu cetakan hingga pelarut menguap habis.
Pen-doping-an selulosa asetat dengan garam litium bertujuan untuk
mengikat ion-ion litium ke dalam matriks polimer. Pada penelitian ini
menggunakan LiCl dengan konsentrasi 35%. Penambahan pemlastis DMP
bertujuan untuk meningkatkan elastisitas membran agar tidak rapuh.
Selulosa asetat hasil sintesis yang berwarna putih dilarutkan dalam asam
asetat glasial, kemudian ditambahakan DMP, selanjutnya ditambahkan garam
litium yang telah dilarutkan dalam akuades sebelumnya. Pengadukan dilakukan
selama 24 jam untuk memperoleh larutan yang homogen. Larutan yang telah
homogen dicetak dalan cawan petri dengan metode casting larutan polimer.
Membran elektrolit selulosa asetat yang dihasilkan berwarna coklat kekuningan.
Pengadukan dilakukan selama 24 jam untuk memperoleh larutan yang
homogen. Hal ini dibuktikan dengan ketebalan membran elektrolit yang
dihasilkan. Dalam penelitian ini membran elektrolit selulosa asetat memiliki
37 3. Uji konduktivitas
Konduktivitas membran elektrolit selulosa asetat ditentukan menggunakan
alat konduktometer Elkahfi 100. Alat ini menggunakan metode two probe untuk
mengukur resistivitas membran. Hubungan antara kuat arus dan tegangan yang
dihasilkan akan diperoleh persamaan grafik, gradien garis menunjukkan nilai
konduktansi (G). Grafik hubungan konduktivitas terhadap kuat arus pada berbagai
komposisi DMP secara lengkap dapat dilihat pada lampiran 3 . Sedangkan untuk
grafik hubungan komposisi DMP terhadap konduktivitas dapat dilihat pada
Gambar 13.
Gambar 13. Grafik Hubungan Komposisi DMP terhadap Konduktivitas Membran Elektrolit Selulosa Asetat
Berdasarkan Gambar 14 terlihat bahwa dengan penambahan DMP
menaikan konduktivitas membran elektrolit selulosa asetat. Hal tersebut sesuai
dengan penelitian David Mecerreyes, dkk (2004) bahwa keberadaan DMP sebagai
parogen membuat porositas membran berukuran besar. Porositas yang besar
tersebut membuat kemampuan adsorbsi litium juga besar sehingga dapat
meningkatkan konduktivitas membran elektrolit selulosa asetat. Konduktivitas
[image:52.595.119.507.340.488.2]38
4. Karakterisasi Membran Elektrolit Selulosa Asetat a. Gugus Fungsi Membran Elektrolit Selulosa Asetat
Pada penelitian ini, untuk mengidentifikasi gugus fungsi pada membran
elektrolit selulosa asetat dapat dianalisa dengan menggunakan FTIR. Berdasarkan
spektrum FTIR, pada Gambar 10 dapat dilihat perbedaan membran elekrolit
selulosa asetat sebelum dan sesudah penambahan DMP. Perbedaan serapan
frekuensi dari kedua membran elektrolit selulosa asetat dapat dilihat pada Tabel 5.
Perbedaan terjadi pada membran blangko dan membran elektrolit pada
pergeseran bilangan gelombang serapan –OH ulur yaitu dari 3439,08 cm-1 menjadi 3431,39 cm-1. Hal ini terjadi karena adanya DMP yang mempunyai gugus
benzena tersubstitusi ortho. Adanya posisi ortho pada gugus benzena akan
mengakibatkan pergeseran bilangan gelombang yang lebih kecil pada serapan – OH ulur (Hardjono Sastrohamidjojo, 1992: 38). Adanya gugus benzena pada
DMP juga menyebabkan adanya perbedaan pergeseran bilangan gelombang pada
bilangan gelombang 1436,51 cm-1 terjadi serapan puncak C=C aromatis yang
menandakan DMP telah masuk pada sistem membran elektrolit selulosa asetat.
Perbedaan juga terjadi pada serapan gugus C=O. Membran dengan
penambahan DMP 25% menunjukkan adanya serapan gugus C=O pada bilangan
gelombang 1737,69 cm-1. Jika dihubungkan dengan konduktivitasnya membran
elektrolit dengan komposisi DMP 25% memiliki konduktivitas optimum. Hal
tersebut terjadi karena ikatan C=O mengakibatkan tingginya kepolaran membran
elektrolit sehingga konduktivitas yang dihasilkan oleh membran elektrolit juga
39
b. Analisis Foto Permukaan dengan Mikroskop Optik
Analisis foto permukaan dilakukan guna mengetahui homogenitas
membran. Seluruh membran elektrolit selulosa asetat dilakukan analisa foto
permukaan agar dapat dilihat pengaruh penambahan DMP dengan membran
elektrolit selulosa asetat tanpa DMP. Foto permukaan membran elektrolit selulosa
asetat dapat dilihat pada Gambar 11.
Berdasarkan pengamatan foto permukaan terdapat beberapa bagian yaitu
bintik putih yang menandakan selulosa asetat, lapisan putih menandakan DMP,
dan noda hitam mengidentifikasi adanya LiCl, karena LiCl apabila terkena udara
lembab dengan cepat akan tertutup oleh lapisan tebal hitam akibat reaksinya
dengan oksigen yang diikuti reaksi lanjut dengan gas karbon dioksida membentuk
litium karbonat dan dapat membentuk oksida hitam apabila terkena air (Kristian
H. Sugiyarto).
Berdasarkan Gambar 11, membran elektrolit selulosa asetat dengan
komposisi DMP 0% selulosa asetat dan DMP jarang terlihat di permukaan
membran. Sedangkan untuk LiCl tersebar mengisi bagian permukaan membran.
Membran dengan komposisi DMP 10% terlihat masih adanya selulosa asetat yang
tidak merata, pada komposisi DMP 15%, 20%, dan 30% terlihat masih adanya
bagian lapisan DMP dan LiCl yang tidak merata, sedangkan untuk DMP 25%
permukaan membran terlihat halus merata.
Komposisi DMP berpengaruh pada homogenitas membran elektrolit yang
dihasilkan. Membran elektrolit selulosa asetat dengan DMP 15%, 20%, dan 30%
40
masih ditemukan lapisan selulosa asetat, LiCl, maupun DMP. Sedangakan pada
komposisi 25% campuran terlihat homogen. Hal tersebut sesuai dengan
penelitian Ali Muhammad, Soliha, Fauzia (2006) kenaikan komposisi DMP akan
meningkatkan kerapatan atau homogenitas karena pemlastis membentuk ikatan
hidrogen antara selulosa asetat, namun dalam kondisi tertentu, ketika jumlah
selulosa asetat berkurang maka kerapatan atau homogenitas akan menurun.
Selulosa asetat berperan penting dalam terjadinya ikatan hidrogen.
Berkurangnya jumlah selulosa asetat maka jumlah atom O dalam membran juga
berkurang sehingga mengakibatkan kemungkinan adanya interaksi tarik menarik
antara atom O dengan atom hidrogen yang terikat dalam satu molekul maupun
antar molekul akan menurun, akibatnya jumlah ikatan hidrogen dalam membran
akan lemah sehingga mengakibatkan kerapatan membran menurun. Jika
dihubungkan dengan konduktivitasnya, berkurangnya atom O akan
memperlambat mobilitas Li+ sehingga konduktivitas yang dihasilkan menurun
akibat menurunnya kerapatan membran.
Membran elektrolit dengan homogenitas tinggi (DMP 25%) memiliki
konduktivitas yang tinggi pula. Hal tersebut dapat dijelaskan bahwa berdasarkan
Marfuatun (2011) konduktivitas ionik pada membran elektrolit disebabkan oleh
adanya konformasi dari rantai polimer yang membentuk suatu lapisan-lapisan
yang memungkinkan adanya mobilitas ion Li+ melalui proses loncatan.
Berdasarkan hal tersebut, homogenitas yang tinggi memungkinkan jarak antar
molekul menjadi dekat sehingga mobilitas ion Li+ untuk melakukan loncatan
41 BAB V KESIMPULAN A. Kesimpulan
Berdasarkan hasil penelitian yang telah dilakukan, dapat ditarik beberapa
kesimpulan sebagai berikut:
1. Peningkatan komposisi pemlastis DMP memberikan nilai konduktivitas
yang cenderung meningkat. Nilai konduktivitas membran selulosa asetat
optimum pada komposisi DMP 25% yaitu sebesar 2,44x10-2 Scm-1.
2. Berdasarkan hasil analisis FTIR membran elektrolit selulosa asetat dengan
penambahan DMP menunjukkan penurunan frekuensi serapan gugus –OH pada daerah 3439,08 cm-1 menjadi 3431,39 cm-1 adanya frekuensi serapan
gugus C=C aromatik pada daerah 1436,51 cm-1 dan frekuensi serapan
gugus C=O pada daerah 1737,69 cm-1. Homogenitas tertinggi membran
elektrolit selulosa asetat diperoleh pada komposisi DMP 25%.
B. Saran
Dalam memperbaiki dan meningkatkan kualitas membran elektrolit
selulosa asetat hasil sintesis, perlu dilakukan penelitian lebih lanjut antara
lain:
1. Perlu dikembangkan metode-metode lain dalam sintesis selulosa asetat
maupun pembuatan membran elektrolit selulosa asetat agar mendapatkan
42
2. Perlu dilakukan karakteristik lebih lanjut pada membran elektrolit selulosa
asetat untuk mengetahui detail karakteristik lain pada membran elektrolit
selulosa asetat.
3. Perlu optimalisasi waktu pengadukan pada proses pembuatan membran
43 Daftar Pustaka
Ahmad Arban Khori. (2007). Pengaruh Penambahan Pemlastis Polietilen Glikol 400, Dietilen Glikol, dan Dimetil Ftalat terhadap Proses Biodegradasi Bioplastik Poli-Β-Hidroksialkanoat pada Media Cair dengan Udara Terlimitasi. Skripsi: hal 20-23.
Ali Muhammad Y S., Soliha L., Fauzia R T. (2006). Modifikasi Membran Selulosa Asetat sebagai Membran Ultrafiltrasi: Studi Pengaruh Komposisi Terhadap Kinerja Membran. Laporan PKM-P. Universitas Jember.
Asrining Prahastuti. (2010). Perancangan Pabrik Selulosa Asetat dari Selulosa dan Asetat Anhidrid dengan Proses Asetilasi Kapasitas 25.500 Ton Per Tahun.
Laporan Tugas Perancangan Pabrik. Universitas Muhammadiyah
Surakarta
Arniz Hanifa. (2015). Sintesis dan Karakterisasi Membran Selulosa Asetat dari Limbah Cair Tahu untuk Aplikasi Baterai Ion Litium. Jurnal student UNY. Vol.4 (7): hal 1-8.
Bambang R., Akhiruddin M., Ratna S D. (2011). Baterai Cerdas dari Elektrolit Polimer Kitosan-PVA dengan Penambahan Amonium Nitrat. Jurnal
pengolahan hasil perikanan Indonesia. Vol. 16 (2): hal 70-77.
Cequeira, D. A., Filho, G. R., and Meireles, M. S. (2007). Otimization of Sugarcane Bagasse Cellulose Acetylation. Carbohydrate Polymers. 69: hal 578-582.
Cut Meurah Rosnelly. (2003). Pengaruh Rasio Aditif Polietilen Glikol terhadap Selulosa Asetat pada Pembuatan Membran Selulosa Asetat Secara Inversi Fasa. Jurnal rekayasa kimia dan lingkungan. Universitas Syiah kuala. 1:hal 1.
Cynthia L Radiman dan Senny Widyaningsih. (2007). Pembuatan Selulosa Asetat dari Pulp Kenaf. Jurnal molekul. Vol. 2 (1): hal 13-16.
Dhika Yetty. (2012). Sintesis Selulosa Asetat dari Kulit Jagung untuk Aplikasi Baterai Ion Litium. Jurnal Student UNY. Vol. 2(1): hal 9-16.
Dian Cipta Sari. (2012). Sintesis Selulosa Asetat dari Jerami Padi untuk Aplikasi Baterai Ion Litium. Jurnal Student UNY. 1(3) No. 3: hal 14-21.
44
Dyah Purwaningsih dan Hari Sutrisno. (2012). Pengembangan Material Lil+Xmn2-Xo4 untuk Aplikasi Elektroda Positif Baterai Litium. Prosiding
seminar nasional penelitian, pendidikan dan penerapan MIPA. FMIPA
UNY: K-3.
Eli Rohaeti. (2005). Kajian tentang poliuretan dan karakterisasinya. Prosiding seminar nasional penelitian, pendidikan dan penerapan MIPA, FMIPA UNY. Yogyakarta, K1-19.
Endang W Laksono, Marfuatun, Demas Aji. (2016). Conductivity of Cellulose Acetate Membran from Pandan Duri (Pandanus tectorius) For Li-Ion Battery. MATEC Web of Converenes Vol. 64(04001): hal 1-4.
Emerketer. (2014). Jumlah Pengguna Smartphone di Indonesia. Diakses dari https://id.techinasia.com/jumlah-pengguna-smartphone-di-indonesia-2018. Pada tanggal 22 januari 2016, Jam 11:30 WIB.
Febri R Palsa. (2006). Pencirian Membran Selulosa Asetat Berbahan Dasar Selulosa Bakteri dari Limbah Nanas. Skripsi. Institut Pertanian Bogor: FMIPA IPB.
Foster, Bob. (2007). Fisika Dasar. Jakarta: Gramedia
Giesen, W., Wulffraat, S., Zieren, M. and Scholten, L. (2006). Mangrove Guide
Book for Southe