BAB II
TINJAUAN PUSTAKA
2.1 Tauco
2.1.1Definisi Tauco
Dalam Standar Nasional Indonesia (1996) tauco adalah produk makanan hasil olahan tauco dan cabai, dengan penambahan atau tanpa penambahan bahan tambahan makanan yang diizinkan.Tauco berbentuk semi padat dan digunakan sebagai sambal penyedap makanan. Jenis tauco ada dua macam yaitu tauco kering dan tauco basah, sedangkan dari rasanya dibdakan menjadi 2 yaiu rasa asin dan manis perbedaannya terletak dari jumlah kadar air dan gula yang ditambahkan (SNI, 1996).
Pada umumnya tauco dibuat secara spontan, sehingga jenis mikroba yang tumbuh akan bermacam-macam jenis dan keadaan yang demikian ini akan berpengaruh terhadap mutu dari tauco yang dihasilkan baik dari segi rasa maupun kandungan proteinnya (Anonim, 1981).
2.1.2 Bahan-bahan dalam Pembuatan Tauco dan Fungsinya
Tujuan dari perendaman pada tahap pertama adalah untuk memudahkan pengupasan kulit kacang kedelai dan untuk membantu mempercepat pengukusan.Perendaman kacang kedelai, biasanya dilakukan selama 20-22 jam. Penambahan tepung pada pembuatan tauco bertujuan untuk merangsang pertumbuhan kapang, menambah volume produk dan mengurangi kadar air. Pada proses fermentasi kapang mikroba, yang berperan adalah kapang Aspergillus oryzae. Penambahan kapang biasanya hanya 1 gram untuk setiap Kg kacang kedelai, fermentasi kapang dilakukan selama 2-3 hari.
2.2 Syarat Mutu Tauco
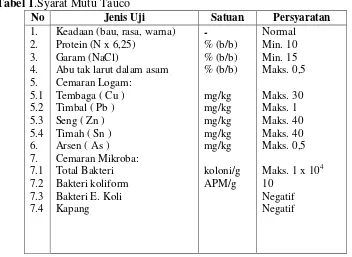
Syarat mutu untuk tauco yang ditetapkan oleh Sandar Nasional Indonesia pada tahun 1996 dapat dilihat pada Tabel 1.
Tabel 1.Syarat Mutu Tauco
No Jenis Uji Satuan Persyaratan
1.
Keadaan (bau, rasa, warna) Protein (N x 6,25)
Garam (NaCl)
Abu tak larut dalam asam Cemaran Logam:
Protein merupakan zat yang tersusun dari berbagai asam amino.Protein didalam tubuh dirubah menjadi asam amino.Dari 20 macam asam amino, tubuh kita membutuhkan 10 macam asam amino yang tidak dapat dibuat oleh tubuh kita.Dari 10 asam amino 8 diantaranya merupakan asam amino esensial (asam amino yang tidak dapat diroduksi oleh tubuh) yang diperoleh dari makanan, selebihnya merupakan asam amino non esensial (asam amino yang dapat diproduksi oleh tubuh) (Budianto, 2009).
Pada sebagian besar jaringan tubuh, protein merupakan komponen erbesar setelah air. Diperkirakan separuh atau 50% dari berat kering sel dalam jaringan sepeti misalnya hati dan daging terdiri dari protein, dan sekitar 20% dalam betuk molekul protein utuh. Dalam tubuh manusia terutama dalam sel jaringan, protein bertindak sebagai bahan membrane sel yang dapat membentuk jaringan pengikat misalnya kolagen dan elastin, serta membentuk protein yang inert seperti pada protein rambut dan kuku (Yazid dan Nursanti, 2006).
2.3.1 Ciri-ciri Molekul Protein
Menurut Ellya (2010), ciri-ciri molekul protein yaitu:
1. Berat molekulnya besar, ribuan sampai jutaan sehingga merupakan suatu makro molekul.
2. Strukturnya tidak stabil terhadap beberapa faktor seperti pH, radiasi, temperatur, medium pelarut organik dan deterjen.
3. Terdapat ikatan kimia lain yang menyebabkan terbentuknya lengkungan-lengkungan rantai polipeptida menjadi struktur tiga dimensi protein.
5. Umumnya reaktif dan sangat spesifik, disebabkan terdapatnya gugusan samping yang reaktif dan susunan khas struktur makromolekul.
2.3.2 Klasifikasi Protein
Berdasarkan keanekaragaman penyusunan struktur protein, maka protein dapat diklasifikasikan sebagai berikut:
1. Protein Fibriler (skleroprotein) adalah protein yang berbentuk serabut. Contohnya kolagen, keratin
2. Protein Globuler (steroprotein) yaitu protein yang berbentuk bola. Contohnya: albumin, globulin (Sudarmadji dan Suhardi, 1989).
2.3.3 Struktur Protein
Protein merupakan makromolekul dengan struktur yang berbeda. Adanya ikatan-ikatan kimia yang terbentuk antar gugus fungsional asam amino maka protein dapat membentuk struktur primer, sekunder, tersier dan kuartener.
− Struktur primer adalah struktur dasar dari protein. Struktur primer protein
menentukan identitas, mengatur struktur sekunder, tersier, dan kuartener. Struktur primer protein dibentuk oleh ikatan peptida yang menghubungkan asam amino penyusun protein.
− Struktur sekunder protein terbentuk oleh adanya ikatan hidrogen antar asam
− Struktur tersier. Dengan adanya ikatan antar asam amino-ikatan hidrogen,
interaksi hidrofobik, jembatan garam, interaksi elektrostatik dan jembatan sulfida pada struktur molekul protein sehingga terbentuk struktur tersier.
− Struktur kuartener terbentuk oleh adanya interaksi antar beberapa rantai
molekul protein yang berbeda melalui ikatan hidrogen, interaksi hidrofobik, interaksi elektrostatik dan jembatan sulfida. Struktur kolagen dan insulin membentuk struktur kuartener (Kusnandar, 2010).
2.3.4 Fungsi Protein
1. Sebagai Enzim
Hampir semua reaksi biologis dipercepat oleh suatu senyawa makromolekul yang disebut enzim. Protein memiliki peranan besar terhadap perubahan-perubahan kimia dalam sistem biologis yang dilakukan oleh enzim (Djaeni, 1976).
2. Pertumbuhan dan Pemeliharaan
Sebelum sel-sel dapat mensintesis protein baru, harus tersedia semua asam amino esensial yang dapat diperlukan dan cukup nitrogen atau ikatan amino (NH2) guna pembentukan asam amino non esensial yang diperlukan (Almatsier, 2004).
3. Pembentukan Ikatan-ikatan Esensial tubuh
4. Pertahanan Tubuh
Salah satu bentuk pertahanan tubuh adalah dalam bentuk antibodi, yaitu suatu protein khusus yang dapat mengenal dan menempel atau mengikat dan meghancurkan benda-benda asing yang masuk kedalam tubuh seperti virus, bakteri, dan sel-sel asing lainnya (Budianto, 2009).
5. Alat Pengangkut dan alat Penyimpan
Banyak molekul dengan berat molekul kecil serta beberapa ion dapat diangkut atau dipindahkan oleh protein-protein tertentu. Misalnya hemoglobin mengangkut oksigen dalam eritrosit, sedangkan mioglobin mengangkut oksigen dalam otot. Ion besi diangkut dalam plasma darah oleh transferin dan disimpan dalam hati sebagai kompleks dengan feritin (Budianto, 2009).
2.3.5 Sumber Protein
1. Protein hewani
Protein hewani adalah protein dalam bahan makanan yang berasal dari binatang/hewan yang memakan tumbuhan mengubah protein nabati menjadi protein hewani. Contoh protein hewani yaitu:
a. Protein daging
b. Protein susu
Protein susu sapi dapat dikelompokkan yaitu: kasein (fosfoprotein ± 78% dari bobot total), dan serum susu (± 17% dari bobot total).
c. Protein telur
Protein telur terbagi atas: protein putih telur, dan protein kuning telur. Protein putih telur mengandung sekurang-kurangnya 8 jenis protein yang berbeda.
2. Protein nabati
Protein nabati adalah protein dalam bahan makanan yang berasal dari tumbuhan, seperti dari jagung, terigu, kacang-kacangan. Kacang kedelai merupakan sumber protein nabati yang mempunyai mutu paling tertinggi, sedangkan sumber protein nabati yang bermutu lebih rendah adalah padi-padian dan hasil olahannya. Contoh protein nabati:
a. Protein kedelai
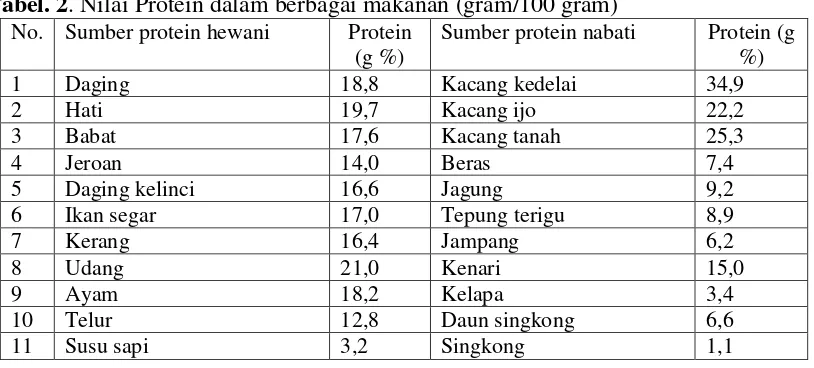
Didalam kedelai terdapat kandungan protein sebesar 34,9 gram. Kandungan protein kacang kedelai merupakan kandungan yang paling tinggi bila dibandingkan dengan jenis kacang-kacangan yang lain.
Tabel. 2. Nilai Protein dalam berbagai makanan (gram/100 gram) No. Sumber protein hewani Protein
(g %)
2.3.6 Akibat Kelebihan dan Kekurangan Protein
Mengonsumsi protein dalam jumlah yang berlebihan akan membebani kerja ginjal. Makanan yang tinggi proteinnya, biasanya juga tinggi lemaknya sehingga dapat menyebabkan obesitas. Kelebihan protein pada bayi dapat memberatkan ginjal dan hati yang harus memetabolisme dan mengeluarkan kelebihan nitrogen dan juga dapat menyebabkan asidosis, dehidrasi, diare, kenaikan amonia darah dan ureum darah, dan demam (Ellya, 2010).
Sebaliknya, jika kurang mengonsumsi protein maka dapat menyebabkan penyakit Kwashiorkor dan Marasmus. Kwashiorkor adalah istilah yang pertama kali digunakan oleh Cecily Williams bagi gejala yang sangat ekstrim yang diderita oleh bayi dan anak-anak kecil akibat kekurangan konsumsi protein yang sangat parah, meskipun gizi yang lain telah tercukupi kebutuhannya. Gejala dari Kwashiorkor yang spesifik adalah adanya oedem, ditambah dengan adanya gangguan pertumbuhan serta terjadinya perubahan-perubahan psikomotorik (Ellya, 2006).
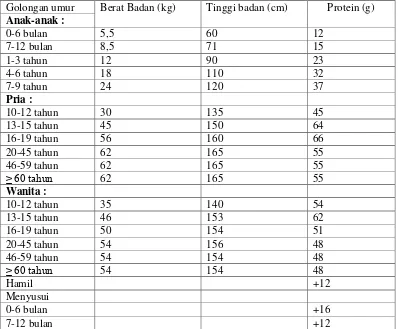
Tabel 3. Angka kecukupan protein yang dianjurkan (tiap orang per hari) Golongan umur Berat Badan (kg) Tinggi badan (cm) Protein (g)
Anak-anak :
2.4 Metode Analisa Protein
2.4.1 Analisa Kualitatif
2. Reaksi Biuret dilakukan dengan cara : larutan protein dibuat alkalis dengan NaOH kemudian ditambahkan larutan CuSO4 encer. Uji ini untuk menunjukkan adanya senyawa-senyawa yang mengandung gugus amida asam yang berada bersama gugus amida yang lain. Uji ini memberikan reaksi positif yaitu ditandai dengan timbulnya warna merah violet atau biru violet (Sudarmadji dan Suhardi, 1989).
2.4.2 Analisa Kuantitatif
1. Titrasi Formol
Larutan protein dinetralkan dengan NaOH, kemudian ditambahkan formalin dan akan membentuk dimenthiol. Dengan terbentuknya dimenthiol ini berarti gugus aminonya sudah terikat dan tidak akan mempengaruhi reaksi antara asam (gugus karboksil) dengan basa NaOH sehingga titrasi dapat diakhiri dengan tepat. Indikator yang digunakan adalah fenolftalein, akhir titrasi bila tepat terjadi perubahan warna menjadi merah mudah yang tidak hilang dalam 30 menit. Titrasi formol ini hanya tepat untuk penentuan protein (Sudarmadji dan Suhardi, 1989). 2. MetodeKjeldahl
tidak langsung karena senyawa yang dianalisisnya adalah kadar nitrogennya. Dengan mengalikan hasil analisis tersebut dengan faktor konversi 6,25 diperoleh nilai protein dalam bahan makanan tersebut (Sudarmadji dan Suhardi, 1989).
Penetapan kadar protein dengan metode ini memiliki kelemahan karena adanya senyawa lain yang bukan protein yang mengandung nitrogen akan tertentukan sehingga kadar protein yang diperoleh langsung dengan metode Kjeldahl ini disebut dengan kadar protein kasar (crude protein) (Sudarmadji dan Suhardi, 1989).
Metode kjeldahl dilakukan dengan beberapa tahapan kerja yaitu : a. Tahap Destruksi
Pada tahap ini sampel dipanaskan dengan asam sulfat pekat sehingga terjadi destruksi menjadi unsur-unsurnya, dimana seluruh N organik dirubah menjadi N anorganik yaitu elemen karbon (C) teroksidasi menjadi karbondioksida (CO2), elemen hidrogen (H) teroksidasi menjadi air (H2O), dan elemen nitrogen (N) berubah menjadi ammonium sulfat {(NH4)2SO4)}. Asam sulfat yang dipergunakan untuk destruksi harus dalam jumlah yang cukup dan diperhitungkan untuk dapat menguraikan bahan protein, lemak, karbohidrat di dalam sampel (Bintang, 2010).
destruksi berkisar antara 370oC-410oC. Proses destruksi diakhiri jika larutan telah berwarna hijau jernih (Bintang, 2010).
Reaksi yang terjadi pada proses destruksi adalah:
Protein + H2SO4(p) + katalisator (NH4)2SO4 + CO2 + SO2 + H2O b. Tahap Destilasi
Pada tahap ini ammonium sulfat {(NH4)2SO4)} yang terbentuk pada tahap destruksi dipecah menjadi amonia (NH3) dengan penambahan NaOH sampai alkalis dan dipanaskan. Amonia yang dibebaskan selanjutnya akan ditangkap oleh larutan baku asam. Larutan baku asam yang dipakai adalah H3BO3 (asam borat). Agar kontak antara asam dan amonia berjalan sempurna, maka ujung selang pengalir destilat harus tercelup kedalam larutan asam. Destilasi diakhiri apabila semua amonia terdestilasi sempurna yang ditandai dengan destilat tidak bereaksi basis (Yazid dan Nursanti, 2006).
Reaksi yang terjadi pada tahap destilasi adalah:
(NH4)2SO4) + 2 NaOH NH3 + 2 H2O + Na2SO4 c. Tahap titrasi
Penampung destilat yang digunakan adalah asam borat berlebih, maka sisa asam borat yang tidak bereaksi dengan amonia dititrasi dengan HCl 0,01 N menggunakan indikator campuran. Titik akhir titrasi dapat ditandai dengan perubahan warna dari warna ungu menjadi hijau (Sudarmadji dan Suhardi, 1989). Reaksi yang terjadi pada tahap titrasi adalah:
3NH3 + H3BO3 (NH4)3BO3
Kadar protein (% P) dapat dihitung dengan persamaan sebagai berikut: % P= 𝑚𝑚𝑚𝑚𝑚𝑚𝑚𝑚𝑚𝑚𝑚𝑚 (𝑏𝑏𝑚𝑚𝑚𝑚𝑏𝑏𝑏𝑏𝑏𝑏 −𝑠𝑠𝑚𝑚𝑚𝑚𝑠𝑠𝑠𝑠𝑚𝑚)
𝑏𝑏𝑠𝑠𝑒𝑒𝑚𝑚𝑒𝑒𝑠𝑠𝑚𝑚𝑚𝑚𝑠𝑠𝑠𝑠𝑚𝑚 (𝑔𝑔)𝑥𝑥 1000 x N NaOH x 14,007 x FK x 100% FK= faktor konversi atau perkalian = 6,25
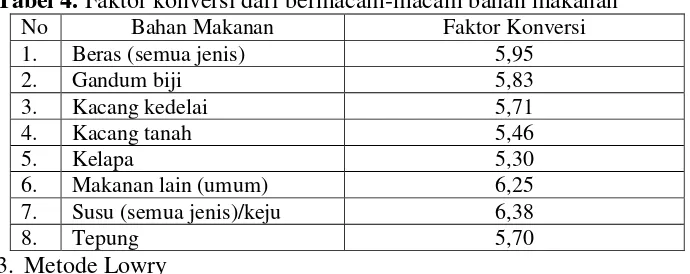
Besarnya faktor konversi nitrogen tergantung pada persentase nitrogen yang menyusun protein dalam bahan pangan yang dianalisa tersebut (Budianto, 2009). Besarnya faktor konversi dari bermacam-macam bahan makanan dapat dilihat pada Tabel berikut ini :
Tabel 4. Faktor konversi dari bermacam-macam bahan makanan
No Bahan Makanan Faktor Konversi
1. Beras (semua jenis) 5,95
2. Gandum biji 5,83
3. Kacang kedelai 5,71
4. Kacang tanah 5,46
5. Kelapa 5,30
6. Makanan lain (umum) 6,25
7. Susu (semua jenis)/keju 6,38
8. Tepung 5,70
3. Metode Lowry