1
PENETAPAN KADAR PROTEIN PADA TAHU PUTIH DAN
TAHU KUNING DENGAN METODE KJELDAHL
TUGAS AKHIR
Oleh:
ULFA RAHMAYANI LUBIS
NIM 122410018
PROGRAM STUDI DIPLOMA III
ANALIS FARMASI DAN MAKANAN
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
2
LEMBAR PENGESAHAN
PENETAPAN KADAR PROTEIN PADA TAHU PUTIH DAN
TAHU KUNING DENGAN METODE KJELDAHL
TUGAS AKHIR
Diajukan Untuk Memenuhi Salah Satu Syarat Untuk Memperoleh Gelar Ahli Madya Pada Program Studi Diploma III Analis Farmasi dan Makanan
Fakultas Farmasi Universitas Sumatera Utara
Oleh:
ULFA RAHMAYANI LUBIS NIM 122410018
Medan, Juni 2015
Disetujui Oleh: Dosen Pembimbing,
Prof. Dr. Siti Morin Sinaga, M.Sc., Apt. NIP 195008281976032002
Disahkan Oleh: a.n. Dekan, Wakil Dekan I,
3
KATA PENGANTAR
Puji dan Syukur kehadirat Allah SWT yang telah memberikan rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan tugas akhir yang berjudul “Penetapan Kadar Protein Pada Tahu Putih dan Tahu Kuning Dengan Metode Kjeldahl”. Tugas Akhir ini diajukan sebagai salah satu syarat untuk memperoleh gelar Program Studi Diploma III Analis Farmasi dan Makanan dari Fakultas Farmasi Universitas Sumatera Utara.
Selama menyusun tugas akhir ini, penulis mendapatkan dukungan baik secara moral dan materil sehingga dapat terselesaikan dan dalam kesempatan ini penulis mengucapkan terima kasih kepada:
1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi Universitas Sumatera Utara.
2. Ibu Prof. Dr. Julia Reveny, M.Si., Apt., selaku Wakil Dekan I Fakultas Farmasi Universitas Sumatera Utara.
3. Bapak Prof. Dr. Jansen Silalahi, M.App.Sc., Apt., selaku Ketua Program Studi Diploma III Analis Farmasi dan Makanan Fakultas Farmasi Universitas Sumatera Utara.
4
5. Bapak dan Ibu dosen staf pengajar Fakultas Farmasi Universitas Sumatera Utara atas semua ilmu, didikan dan bimbingan kepada penulis selama di perguruan tinggi dan Staf administrasi Fakultas Farmasi yang telah membantu kemudahan administrasi selama ini.
6. Bapak Alhamra, Kepala Laboratorium Makanan Minuman Hasil Pertanian dan Ibu Sri Chansnawati dan Bapak Handrian Syahputra Siregar selaku Pembimbing Praktek Kerja Lapangan di Laboratorium Makanan Minuman Hasil Pertanian Balai Riset dan Standarisasi (Baristand) Industri Medan.
Penulis juga mengucapkan rasa terima kasih serta penghargaan yang tulus dan tak terhingga kepada orangtua tersayang Ayahanda Fachrul Irsan Lubis, Ibunda Ida Rohayani Harahap, Abangda Achmad Sofyan Lubis, Adinda Khaira Maulida Lubis, Chairunnisa Lubis dan Fajar Prasetya Kembaren atas segala do’a dan telah memberikan dorongan baik moril maupun materil sehingga tugas akhir ini dapat diselesaikan.
Penulis menyadari bahwa tugas akhir ini jauh dari sempurna, penulis mengharapkan kritik dan saran yang bersifat mambangun. Semoga tugas akhir ini berguna bagi pembaca secara umum dan penulis secara khusus. Akhir kata penulis mengucapkan terima kasih.
Medan, Juni 2015 Penulis,
5
DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... ii
KATA PENGANTAR ... iii
DAFTAR ISI ... v
DAFTAR LAMPIRAN ... vii
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Tujuan dan Manfaat ... 2
1.2.1 Tujuan ... 2
1.2.2 Manfaat ... 2
BAB II TINJAUAN PUSTAKA ... 3
2.1 Kedelai ... 3
2.2 Tahu ... 3
2.2.1 Komposisi Gizi Tahu ... 4
2.2.2 Proses Pembuatan Tahu ... 4
2.2.3 Persyaratan Mutu Tahu ... 6
2.2.4 Manfaat Tahu ... 7
2.3 Protein ... 7
2.3.1 Sifat-sifat Karakteristik Protein ... 8
6
2.3.3 Fungsi Protein ... 9
2.4 Penetapan Kadar Protein ... 10
BAB III METODOLOGI PERCOBAAN ... 13
3.1 Tempat dan Waktu Percobaan ... 13
3.2 Alat-alat ... 13
3.3 Bahan-bahan ... 13
3.3.1 Sampel ... 13
3.3.2 Pembuatan Pereaksi ... 14
3.4 Prosedur Percobaan ... 14
BAB IV HASIL DAN PEMBAHASAN ... 16
4.1 Hasil dan Pembahasan ... 16
BAB V KESIMPULAN DAN SARAN ... 19
5.1 Kesimpulan ... 19
5.2 Saran ... 19
7
DAFTAR LAMPIRAN
8
BAB I
PENDAHULUAN
1.1 Latar Belakang
Menurut SNI 01-3142-1998 tahu adalah suatu produk makanan berupa padatan lunak yang dibuat melalui proses pengolahan kedele (Glycine species) dengan cara pengendapan proteinnya, dengan atau tanpa penambahan bahan lain yang diizinkan.
Tahu yang diperdagangkan di pasar memiliki berbagai variasi bentuk, ukuran, nama dan berciri khas, tahu memiliki berbagai jenis yaitu, tahu sumedang, tahu bandung, tahu putih, tahu kuning dan tahu sutera (Sarwono dan Pieter, 2001). Protein adalah sumber asam amino terdiri atas rantai-rantai panjang asam amino, yang terikat satu sama lain dengan ikatan peptida yang mengandung unsur-unsur C, H, O dan N. Protein merupakan suatu zat makanan yang amat penting bagi tubuh, karena zat ini disamping berfungsi sebagai bahan bakar dalam tubuh juga berfungsi sebagai zat pembangun dan pengatur dalam tubuh (Budiyanto, 2004).
9
Sesuai atau tidaknya kadar protein yang terkandung pada tahu putih dan tahu kuning yang beredar di Indonesia dilihat berdasarkan persyaratan mutu Standar Nasional Indonesia (SNI) 01-3142-1998.
Berdasarkan hal diatas, penulis tertarik untuk mengambil judul tugas akhir berjudul “Penetapan Kadar Protein Pada Tahu Putih dan Tahu Kuning Dengan Metode Kjeldahl”.
1.2 Tujuan dan Manfaat
1.2.1 Tujuan
Untuk mengetahui kadar protein pada tahu putih dan tahu kuning dengan metode Kjeldahl.
1.2.2 Manfaat
10
BAB II
TINJAUAN PUSTAKA
2.1 Kedelai
Menurut Adisarwanto (2005) kedelai merupakan tanaman asli daratan Cina dan telah dibudidayakan oleh manusia sejak 2500 SM, tanaman kedelai tersebar ke berbagai tujuan perdagangan tersebut, yaitu Jepang, Korea, Indonesia, India, Australia dan Amerika. Klasifikasi tanaman kedelai sebagai berikut:
Kingdom : Plantae
Divisi : Spermatophyta Kelas : Dicotyledoneae Famili : Leguminosae Genus : Glycine
Spesies : Glycine max (L.) Merrill
2.2 Tahu
11
Tahu putih berupa tahu cina, teksturnya lebih padat, halus, kenyal dibandingkan dengan tahu yang lain, ukurannya sekitar 12 cm x 8 cm dan ukuran bobot tahu relatif seragam karena proses pembuatannya dicetak dengan menggunakan papan kayu (Sarwono dan Pieter, 2001).
Tahu kuning berupa tahu takwa khas Kediri, Jawa Timur dan mirip dengan tahu putih, bentuknya tipis dan lebar, kalau dipijit tahunya terasa padat. Tahu ini banyak digunakan dalam masakan cina, dijual dan disimpan dalam keadaan kering tanpa perlu direndam air seperti tahu putih (Sarwono dan Pieter, 2001).
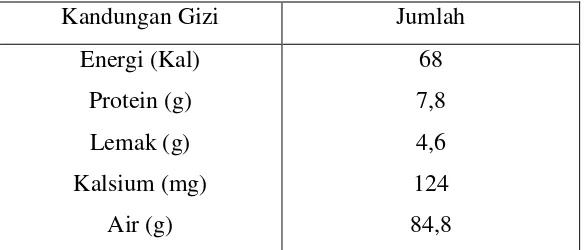
2.2.1 Komposisi Gizi Tahu
Komposisi gizi tahu per 100 g, dapat dilihat pada Tabel 2.1.
Tabel 2.1 Komposisi gizi tahu per 100 g
Kandungan Gizi Jumlah
Energi (Kal) Sumber: Khomsan dan Anwar (2008)
2.2.2 Proses Pembuatan Tahu
Menurut Adisarwanto (2005) proses pembuatan tahu yang dilakukan dengan tahapan-tahapan sebagai berikut:
a. Sortasi biji
12 b. Pencucian dan Perendaman
Biji-biji kedelai hasil sortiran dimasukkan ke dalam bak atau ember, kemudian dicuci hingga bersih, pencucian disarankan menggunakan air yang mengalir. Perendaman biji kedelai dilakukan di dalam bak semen selama 6 – 12 jam, tujuannya agar biji kedelai menjadi lunak dan kulit arinya mudah terkelupas. c. Pengupasan kulit ari biji kedelai
Proses pengupasan kulit ari dapat dilakukan secara manual menggunakan tangan dengan cara diremas-remas. Selain itu, bisa juga menggunakan alat pengupas kulit ari. Hasil pengupasan biji kedelai berupa keping-keping biji kedelai.
d. Penggilingan
Penggilingan dilakukan dengan alat penggiling yang telah ditambahkan air panas agar enzim lipoksigenase (penyebab bau langu) tidak aktif. Hasil gilingan berupa bubur putih.
e. Pendidihan
Bubur putih hasil penggilingan dimasukkan dalam wajan besar dan dipanaskan dengan api sampai mendidih, besarnya api harus tetap stabil. Adonan dalam tungku tersebut perlu diaduk-aduk agar tidak timbul busa. Lama periode pendidihan sekitar 15 – 30 menit.
f. Penyaringan dan Penggumpalan
13
keluar. Penyaringan ini dapat diulangi beberapa kali agar diperoleh sari bubur kedelai yang terbaik. Kalsium sulfat (batu tahu) atau asam cuka ditambahkan ke dalam sari bubur kedelai yang diperoleh agar terbentuk gumpalan tahu dan siap dikonsumsi atau dijual.
Proses pengolahan tahu kuning pada prinsipnya sama dengan tahu putih, warna kuning dikarenakan sepuhan atau larutan sari kunyit, sebelum dipasarkan tahu kuning dimasak atau dicelup beberapa menit dalam air kunyit mendidih sehingga warnanya menjadi kuning (Sarwono dan Pieter, 2001).
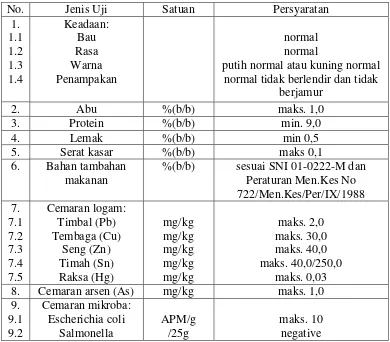
2.2.3 Persyaratan Mutu Tahu
Persyaratan mutu pada tahu, dapat dilihat pada Tabel 2.2.
Tabel 2.2 Persyaratan mutu tahu
No. Jenis Uji Satuan Persyaratan
1.
putih normal atau kuning normal normal tidak berlendir dan tidak
berjamur
14
2.2.4 Manfaat Tahu
Tahu yang kaya akan protein dan asam amino sangat baik untuk pembentukan, pemeliharaan dan perbaikan sel-sel tubuh, pembentukan antibodi dan meningkatkan kecerdasan anak, bermanfaat mencegah penyakit jantung, stroke, alzheimer (pikun) dan pembentukan sel darah merah (Anggraini dan Surbakti, 2008).
2.3 Protein
Istilah protein berasal dari kata Yunani proteos, yang berarti yang utama atau yang didahulukan. Kata ini diperkenalkan oleh seorang ahli kimia Belanda. Gerardus Mulder (1802 – 1880), karena ia berpendapat bahwa protein adalah zat yang paling penting pada setiap organisme (Almatsier, 2001).
Protein adalah makromolekul polipeptida yang tersusun dari sejumlah asam amino yang dihubungkan oleh ikatan peptida, suatu senyawa organik yang berbobot molekul tinggi berkisar antara beberapa ribu sampai jutaan dan tersusun dari atom C, H, O dan N yang membentuk unit-unit asam amino. Suatu molekul protein disusun oleh sejumlah asam amino tertentu, urutan susunan asam amino dalam protein maupun hubungan antara asam amino yang satu dan asam amino lainnya (Girindra, 1986).
15
yang terdapat pada protein mempunyai satu gugus karboksil dan satu gugus amino. Gugus amino terletak pada atom C yang berdamping dengan gugus
karboksil, karena itu disebut asam α-amino. Tiap asam amino mempunyai gugus
R yang sangat khas sifatnya (Almatsier, 2001).
Suatu peptida ialah suatu amida yang dibentuk dari dua asam amino atau
lebih. Ikatan amida antara suatu gugus α-amino dari suatu asam amino dan gugus
karboksil dari asam amino lain disebut ikatan peptida (Fessenden, 1982).
2.3.1 Sifat-sifat Karakteristik Protein
Protein kebanyakan merupakan senyawa yang amorf, tidak berwarna, tidak mempunyai titik cair atau titik didih yang tertentu dan bila dilarutkan dalam air akan memberikan larutan koloidal (Sastrohamidjojo, 2009).
Protein sangat cenderung mengalami beberapa bentuk perubahan yang dinyatakan sebagai denaturasi. Denaturasi adalah terbukanya lipatan alamiah struktur protein, proses denaturasi mengubah bentuk dan lipatan tapi tidak merusak ikatan peptida yang terdapat antara asam amino dalam struktur primer (Martoharsono, 1988).
2.3.2 Struktur Protein
Menurut Girindra (1986) para ahli biokimia membagi makro molekul protein atas empat struktur dasar sebagai berikut:
a. Struktur Primer
16 b. Struktur Sekunder
Istilah ini dipakai untuk struktur protein di mana rantai asam amino bukan hanya dihubungkan oleh ikatan peptida tetapi juga diperkuat oleh ikatan hidrogen. Struktur sekunder protein adalah struktur dua dimensi dari protein.
c. Struktur Tersier
Dalam hal ini rantai polipeptida cenderung untuk membelit atau melipat membentuk struktur yang kompleks. Kestabilan struktur ini bergantung pada gugus R pada setiap asam amino yang membentuknya dan distabilkan oleh ikatan hidrogen, ikatan disulfida, interaksi hidrofilik dan interaksi hidrofobik.
d. Struktur Kuartener
Molekul protein ini terbentuk dari beberapa tersier dan biasa terdiri dari protomer yang sama atau protomer yang berlainan. Protein yang dibentuk oleh protomer yang sama disebut homogenus, jika terdiri dari protomer berlainan disebut heterogenus.
2.3.3 Fungsi Protein
Menurut Almatsier (2001) fungsi protein sebagai berikut: a. Mengangkut Zat- zat Gizi
17 b. Pembentukan Antibodi
Kemampuan tubuh untuk memerangi infeksi bergantung pada kemampuannya untuk memproduksi antibodi terhadap organisme yang menyebabkan infeksi tertentu terhadap bahan-bahan asing yang memasuki tubuh. Tingginya tingkat kematian pada anak-anak yang menderita kurang gizi kebanyakan disebabkan oleh menurunnya daya tahan terhadap infeksi dan kemampuan untuk menghalangi pengaruh toksik berkurang karena ketidakmampuannya membentuk antibodi dalam jumlah yang cukup.
c. Mempertahankan Netralisasi Tubuh
Protein tubuh bertindak sebagai buffer (penyangga) yaitu bereaksi dengan asam dan basa untuk menjaga pH pada taraf konstan. Sebagian besar jaringan tubuh berfungsi dalam keadaan pH netral atau sedikit alkali (pH 7,35 – 7,45).
2.4 Penetapan Kadar Protein
1. Metode Kjeldahl
Menurut SNI 01-2891-1992, prinsip penetapan kadar protein adalah senyawa nitrogen diubah menjadi amonium sulfat oleh asam sulfat pekat. Amonium sulfat yang terbentuk diuraikan dengan natrium hidroksida. Ammonia yang dibebaskan diikat dengan asam borat dan kemudian dititar dengan larutan baku asam.
18
Dasar perhitungan penentuan protein menurut Kjeldahl ini umumnya protein alamiah mengandung unsur N rata-rata 16%, apabila jumlah unsur N dalam bahan telah diketahui maka jumlah protein dapat diperhitungkan dengan jumlah N x 100/16 atau jumlah N x 6,25. Untuk campuran senyawa-senyawa protein yang belum diketahui komposisi unsur-unsur penyusunnya secara pasti, maka faktor perkalian 6,25 inilah yang dipakai (Sudarmadji, 1989).
19 2. Metode Spektrofotometer UV
Kebanyakan protein mengabsorbsi sinar ultraviolet maksimum pada 280 nm. Hal ini terutama oleh adanya asam amino tirosin, triptophan dan fenilalanin yang ada pada protein tersebut. Pengukuran protein berdasarkan absorbsi sinar UV adalah cepat, mudah dan tidak merusak bahan (Sudarmadji, 1989).
3. Metode Lowry
Konsentrasi protein diukur berdasarkan optikal density pada panjang gelombang 600 nm. Untuk mengetahui banyaknya protein dalam larutan, dibuat kurva standar yang melukiskan hubungan antara konsentrasi dengan optikal density. Larutan Lowry ada dua macam yaitu larutan A yang terdiri dari dari fosfotungstat-fosfomolibdat (1:1) dan larutan B yang terdiri dari Na2CO3 2% dalam NaOH 0,1 N, CuSO4 dan Na-K-tartrat 2%. Cara penentuannya adalah: 1 ml larutan protein ditambahkan 5 ml Lowry B, dikocok dan dibiarkan selama 10 menit. Kemudian ditambah 0,5 ml Lowry A dikocok dan dibiarkan 20 menit, selanjutnya diamati optikal densitynya pada panjang gelombang 600 nm (Sudarmadji, 1989).
4. Metode Biuret
20
BAB III
METODOLOGI PERCOBAAN
3.1 Tempat dan Waktu Percobaan
Percobaan ini dilaksanakan di Laboratorium Makanan Minuman Hasil Pertanian Balai Riset dan Standarisasi (Baristand) Industri Medan yang berada di Jalan Sisingamangaraja No. 24 Medan pada tanggal 02 – 27 Februari 2015.
3.2 Alat-alat
Alat-alat yang digunakan alat penyulingan dan kelengkapannya, batang pengaduk, beaker glass, botol semprot, buret, corong, erlenmeyer, klem, labu Kjeldahl 100 ml, labu ukur 100 ml, neraca analitik, pipet tetes, pipet volum, spatula dan statif.
3.3 Bahan-bahan
Bahan-bahan yang digunakan H3BO3 4%, HCl 0,01 N, H2SO4(p), indikator campuran metil red dan bromocresol green, NaOH 30%, SeO2 dan akuades.
3.3.1 Sampel
21
tahu putih dan tahu kuning yang masing-masing diperoleh dari Jalan Bunga Cempaka Gg. Bunga Cempaka Sari dan Jalan A. R. Hakim Medan.
3.3.2 Pembuatan pereaksi
Pembuatan pereaksi asam borat (H3BO3) 4%: Dilarutkan 40 g H3BO3 dengan air suling menjadi 1000 ml dan tambahkan 3 ml larutan indikator campuran metil red dan bromocresol green, aduk (larutan akan berwarna kuning terang) dan dipindahkan ke dalam botol gelas bertutup (SNI 2973-2011).
Pembuatan pereaksi asam klorida (HCl) 0,01 N: Ditimbang 0,3647 g HCl(p), kemudian larutkan dalam 1000 ml air (Ditjen POM, 1979).
Pembuatan indikator campuran metil red dan bromocresol green: Disiapkan larutan bromocresol green 0,1% dan metil red 0,1% dalam alkohol 95% secara terpisah. Campur 10 ml bromocresol green dengan 2 ml metil red (SNI 01-2891-1992).
Pembuatan pereaksi natrium hidroksida (NaOH) 30%: Dilarutkan 150 g kristal NaOH ke dalam 350 ml air suling, simpan dalam botol bertutup karet (SNI 01-2891-1992).
Pembuatan pereaksi selen (SeO2): Dicampuran 4 g serbuk SeO2, 150 g K2SO4 atau Na2SO4 dan 30 g CuSO4. H2O (SNI 01-2891-1992).
3.4 Prosedur Percobaan
22
menjadi jernih kehijau-hijauan (sekitar 2 jam). Biarkan dingin, kemudian encerkan dan masukkan ke dalam labu ukur 100 ml, tepatkan sampai tanda garis. Pipet 25 ml larutan dan masukkan kedalam alat penyuling, tambahkan 50 ml NaOH 30%. Sulingkan selama lebih kurang 10 menit, sebagai penampung gunakan 25 ml H3BO3 4% dan 1 tetes indikator campuran metil red dan bromocresol green. Bilasi ujung pendingin dengan air suling. Titrasi dengan larutan HCl 0,01 N. Kerjakan penetapan blanko (SNI 01-2891-1992).
Perhitungan:
Kadar Protein = (V1 − V2) x N x 0,014 x FK x FP
W x 100%
Dimana :
V1 = volume HCl 0,01 N yang dipergunakan penitaran sampel V2 = volume HCl yang dipergunakan penitaran blanko
N = normalitas HCl
FK = faktor konversi untuk protein dari makanan secara umum: 6,25 FP = faktor pengenceran
23
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil dan Pembahasan
Sampel yang digunakan untuk uji organoleptis dan kadar protein yaitu tahu putih dan tahu kuning. Gambar tahu putih dan tahu kuning dapat dilihat pada Gambar 1 dan Gambar 2.
Gambar 1. Tahu putih Gambar 2. Tahu kuning
Hasil uji organoleptis pada tahu putih dan tahu kuning, dapat dilihat pada Tabel 4.1.
Tabel 4.1 Uji organoleptis pada tahu putih dan tahu kuning
No. Keadaan Tahu putih Tahu kuning
1. Bau normal Normal
2. Rasa normal Normal
3. Warna putih normal kuning normal
4. Penampakan normal dan tidak berlendir normal dan tidak berlendir
24
Tahu yang beredar di pasar tradisional saat ini mutunya masih beragam, oleh karena itu, para konsumen perlu mengetahui tahu yang berkualitas baik. Pilihlah tahu yang tidak diberi pewarna, bila menyukai tahu berwarna amatilah warnanya dengan cermat, apabila warna terlalu cerah atau mencolok sebaiknya jangan dibeli karena pewarna yang digunakan berupa pewarna sintetik, seperti bahan pewarna cat atau kain. Untuk mengetahui kesegaran, peganglah tahu, tahu yang tidak segar lagi, selain aromanya masam sampai busuk, permukaannya berlendir dan ada yang telah berjamur (Sarwono dan Pieter, 2001).
Hasil penetapan kadar protein yang dilakukan pada tahu putih dan tahu kuning, dapat dilihat pada Tabel 4.2.
Tabel 4.2 Penetapan kadar protein pada tahu putih dan tahu kuning
No. Sampel Kadar Protein (%) Persyaratan
1. Tahu putih 8,87% SNI 01-3142-1998 min. 9,00% 2. Tahu kuning 10,68% SNI 01-3142-1998 min. 9,00%
Berdasarkan Tabel 4.2 diatas, dapat dilihat kadar protein pada tahu putih dan tahu kuning masing-masing sebesar 8,87% dan 10,68%. Hal ini menunjukkan tahu putih tidak memenuhi persyaratan SNI dan tahu kuning memenuhi persyaratan SNI 01-3142-1998. Rendahnya kadar protein pada tahu putih disebabkan pada proses pembuatan tahu seperti pemilihan biji kedelai, penggilingan dengan penambahan air, penggumpalan dan pencetakannya.
25
Penggilingan biji kedelai dengan penambahan air panas untuk menghilangkan bau langu dapat mempengaruhi kadar protein yang tidak tahan panas. Kadar protein yang ada dalam suatu bahan sangat ditentukan dari proses pembuatannya, dimana salah satu sifat dari protein tidak tahan terhadap panas. Adanya panas yang tinggi menyebabkan protein akan rusak sehingga kadarnya menurun (Fessenden, 1982).
Penggumpal kalsium sulfat (batu tahu) sebagai bahan penggumpal keadaan ini menyebabkan sari biji kedelai yang dihasilkan akan semakin pekat dan banyak sehingga kadar protein semakin tinggi dibandingkan dengan penggumpal asam cuka (Sarwono dan Pieter, 2001). Protein bila dilarutkan dalam air akan memberikan larutan koloidal, protein diendapkan dari larutannya bila ditambahkan dengan garam-garam anorganik (Na2SO4, NaCl) dan juga dengan menggunakan zat-zat organik yang larut dalam air (Sastrohamidjojo, 2009).
Pencetakan tahu yang menggunakan papan kayu ditekan sekuat tenaga sehingga semua air yang berada didalam bubur kedelai terperas keluar, sebab umumnya makanan yang berkadar air tinggi mengandung protein yang agak rendah (Khomsan dan Anwar, 2008).
26
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Kadar protein pada tahu putih tidak memenuhi persyaratan sebesar 8,87%, sedangkan kadar protein pada tahu kuning memenuhi persyaratan sebesar 10,68%.
5.2 Saran
27
DAFTAR PUSTAKA
Adisarwanto, T. (2005). Kedelai. Jakarta: Penebar Swadaya. Halaman 6, 90 – 92. Almatsier, S. (2001). Prinsip Dasar Ilmu Gizi. Jakarta: PT. Gramedia Pustaka
Umum. Halaman 77 – 78, 96 – 97, 100 – 104.
Anggraini, D.R., dan Surbakti, Y. (2008). Super Komplit Menu Sehari-hari
Sepanjang Masa. Jakarta: PT. Wahyu Media. Halaman 120.
Badan Standarisasi Nasional. Cara Uji Makanan Dan Minuman. SNI 01-2891-1992. Jakarta: Dewan Standarisasi Nasional.
Badan Standarisasi Nasional. Tahu. SNI 01-3142-1998. Jakarta: Dewan Standarisasi Nasional.
Badan Standarisasi Nasional. Biskuit. SNI 2973-2011. Jakarta: Dewan Standarisasi Nasional.
Budiyanto, A.K. (2004). Dasar-dasar Ilmu Gizi. Malang: Universitas Muhammadiyah Malang. Halaman: 37, 40 – 41.
Direktorat Jenderal Pengawasan Obat dan Makanan, (1979). Farmakope
Indonesia. Edisi III. Jakarta: Departemen Kesehatan Republik Indonesia.
Halaman 744.
Fessenden, J.S., dan Fessenden, R.J. (1982). Kimia Organik. Jilid II. Jakarta: Erlangga. Halaman 375.
Girindra, A. (1986). Biokimia I. Jakarta: PT. Gramedia. Halaman 66, 80 – 82, 89. Khomsan, A dan Anwar, F. (2008). Sehat Itu Mudah, Wujudkan Hidup Sehat
dengan Makanan Tepat. Jakarta: PT Mizan Publika. Halaman 26 – 27.
Martoharsono, S. (1988). Biokimia. Jilid I. Yogyakarta: Universitas Gadjah Mada. Halaman 45.
Sarwono, B dan Pieter Y.S. (2001). Membuat Aneka Tahu. Jakarta: Penebar Swadaya. Halaman 2, 4 – 6, 15, 17.
Sastrohamidjojo, H. (2009). Kimia Organik. Yogyakarta: Universitas Gadjah Mada. Halaman 117 – 119, 120, 180.
Sudarmadji, S., Haryono, B., dan Suhardi. (1989). Analisa Bahan Makanan dan
28
LAMPIRAN
Lampiran 1. Bagan Alir Prosedur Percobaan
Ditimbang 1 g sampel (tahu putih dan tahu kuning) Dimasukkan kedalam labu Kjeldahl 100 ml
Ditambahkan 1 g SeO2 dan 25 ml H2SO4(p)
Dipanaskan diatas pemanas listrik atau api pembakaran sampai larutan jernih selama 2 jam Dibiarkan sampai dingin
Diencerkan dan dimasukkan ke dalam labu ukur 100 ml, tepatkan sampai tanda garis
Dipipet 25 ml larutan sampel dan dimasukkan ke dalam alat penyuling
Ditambahkan 50 ml NaOH 30%
Ditambahkan 25 ml H3BO3 4% dan 1 tetes
indikator campuran metil red dan bromocresol green Disuling selama kurang lebih 10 menit
Dititrasi dengan larutan HCl 0,01 N Sampel
Proses Destruksi
Proses Destilasi
Proses Titrasi
Hasil
29
Lampiran 2. Penetapan Kadar Protein
Kadar Protein = (V1 − V2) x N x 0,014 x FK x FP
W x 100%
Dimana:
V1 = volume HCl 0,01 N yang dipergunakan penitaran sampel V2 = volume HCl yang dipergunakan penitaran blanko
N = normalitas HCl
FK = faktor konversi untuk protein dari makanan secara umum: 6,25 FP = faktor pengenceran
W = bobot sampel
30
Lampiran 3. Gambar Proses Penetapan Kadar Protein
Gambar 1. Proses destruksi Gambar 2. Proses destilasi