3 BAB II
TINJAUAN PUSTAKA
2.1 Kedelai
Menurut Adisarwanto (2005) pada tahun 1948 telah disepakati bahwa nama botani yang dapat diterima dalam istilah ilmiah, yaitu Glycine max (L.) Merill. Klasifikasi tanaman kedelai sebagai berikut:
Kingdom : Plantae
Divisi : Spermatophyta Kelas : Dicotyledoneae Ordo : Rosales
Famili : Leguminosae Genus : Glycine
Spesies : Glycine max (L.) Merill
2.2 Susu Kedelai
Menurut SNI 01-3830-1995 susu kedelai adalah produk yang berasal dari ekstrak biji kacang kedelai dengan air atau larutan tepung kedelai dalam air, dengan atau tanpa penambahan bahan makanan lain yang diizinkan.
4
Sejak abad II sebelum Masehi, susu kedelai sudah dibuat di negeri Cina, kemudian teknologinya mengalir ke Jepang. Setelah perang dunia ke II, susu kedelai mulai dikenal di Asia Tenggara termasuk Indonesia, Filipina, Malaysia dan Singapura hingga saat ini susu kedelai mengalami perkembangan yang sangat pesat. Masyarakat Malaysia mengenal susu kedelai dengan nama Vitabean, pengembangannya telah dimulai sejak tahun 1952, sedangkan di Filipina susu kedelai populer dengan nama Philsoy (Hartoyo,2005).
2.2.1 Komposisi Gizi Susu Kedelai
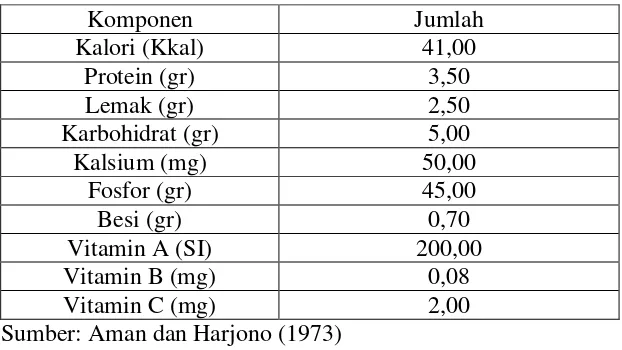
Komposisi gizi susu kedelai, dapat dilihat pada Tabel 2.1. Tabel 2.1. Komposisi Gizi Susu Kedelai (dalam 100 gr)
Komponen Jumlah
Kalori (Kkal) 41,00
Protein (gr) 3,50
Lemak (gr) 2,50
Karbohidrat (gr) 5,00
Kalsium (mg) 50,00
Sumber: Aman dan Harjono (1973) 2.2.2 Pembuatan Susu Kedelai
Menurut Hartoyo (2005) pembuatan susu kedelai sebagai berikut:
5
b. Didihkan rendaman kacang kedelai, setelah mendidih tiriskan dan bilas dengan air segar, pisahkan kulitnya untuk dibuang. Bau dan rasa langu dapat dihilangkan dengan cara mematikan enzim lipsigenase dengan suhu panas. Cara yang dapat dilakukan antara lain menggunakan air panas (suhu 80 - 100˚C) pada penggilingan kacang kedelai, atau merendam kacang kedelai dalam air panas selama 10 – 15 menit sebelum digiling.
c. Kacang kedelai digiling hingga menjadi bubur. Bubur yang diperoleh ditambah air mendidih sehingga jumlah air secara keseluruhan mencapai 10 kali lipat bobot kacang kedelai. Bubur encer disaring dengan kain kasa dan filtratnya merupakan susu kedelai mentah.
d. Untuk meningkatkan citarasa, ke dalam susu kedelai mentah ditambahkan gula pasir sebanyak 5 – 7% dan perasa seperti coklat, moka, pandan, stroberi secukupnya, kemudian dipanaskan sampai mendidih.
e. Setelah mendidih, api dikecilkan dan dibiarkan dalam api kecil selama 20 menit. Jaga jangan sampai susu pecah karena suhu kompor terlalu panas. f. Jika akan dibotolkan, seringkali susu kedelai menjadi tidak stabil. Timbul
endapan pada bagian dasar. Untuk mencegahnya bisa menambahkan tepung agar dengan jumlah 1%.
6 2.2.3 Persyaratan Mutu Susu Kedelai
Persyaratan mutu susu kedelai, dapat dilihat pada Tabel 2.2. Tabel 2.2 Persyaratan Mutu Susu Kedelai
No Kriteria uji Satuan Persyaratan
Susu (milk) Minuman (drink) 1. Keadaan:
Sesuai dengan SNI 01-0222-1987 6.1 Pemanis buatan
6.2 Pewarna 9. Cemaran mikroba:
7 2.2.4 Manfaat Susu Kedelai
Susu kedelai bermanfaat bagi penderita intoleransi laktosa, yaitu seseorang yang tidak mempunyai enzim laktase dalam tubuhnya sehingga orang tersebut tidak dapat mencerna makanan yang berlemak. Banyaknya kejadian lain berupa diare akibat minum susu hewani yang disebabkan oleh berkurangnya aktivitas enzim laktase di dalam tubuh, maka dianjurkan untuk mengkonsumsi produk susu olahan bebas laktosa seperti susu kedelai dan susu kacang hijau. Fungsi laktase adalah untuk mencerna laktosa (gula susu) dan menguraikannya menjadi glukosa dan galaktosa (Hartoyo,2005).
2.3 Protein
Istilah protein berasal dari kata Yunani proteos, yang berarti yang utama atau yang didahulukan. Kata ini diperkenalkan oleh seorang ahli kimia Belanda Gerardus Mulder (1802 – 1880), karena ia berpendapat bahwa protein adalah zat yang paling penting pada setiap organisme (Almatsier, 2001).
Protein merupakan senyawa bermolekul besar dan kompleks yang tersusun dari unsur-unsur C, H, O, N, S dan dalam keadaan kompleks ada unsur P (Sudarmadji, 1989).
8
unsur utama protein, karena terdapat di dalam semua protein akan tetapi tidak terdapat di dalam karbohidrat dan lemak (Almatsier, 2001).
Asam amino terdiri atas atom karbon yang terikat pada satu gugus karboksil (-COOH), satu gugus amino (-NH2), satu atom hidrogen (-H) dan satu
gugus alkil (-R) atau rantai cabang (Almatsier, 2001).
Suatu peptida ialah suatu amida yang dibentuk dari dua asam amino atau lebih. Ikatan amida antara suatu gugus α-amino dari suatu asam amino dan gugus karboksil dari asam amino lain disebut ikatan peptida (Fessenden, 1982).
2.3.1 Struktur Protein
Menurut Girindra (1986) para ahli biokimia membagi makro molekul protein atas empat struktur dasar sebagai berikut:
a. Struktur Primer
Pada struktur primer ini ikatan antar asam amino hanya ikatan peptida. Disini tidak terdapat ikatan atau kekuatan lain yang menghubungkan asam amino yang satu dengan lainnya.
b. Struktur Sekunder
Istilah ini dipakai untuk struktur protein di mana rantai asam amino bukan hanya dihubungkan oleh ikatan peptida tetapi juga diperkuat oleh ikatan hidrogen, struktur sekunder protein adalah struktur dua dimensi dari protein.
c. Struktur Tersier
9
gugus R pada setiap asam amino yang membentuknya, dan distabilkan oleh ikatan hidrogen serta ikatan disulfida.
d. Struktur Kuarterner
Molekul protein ini terbentuk dari beberapa tersier dan biasa terdiri dari protomer yang sama atau protomer yang berlainan. Protein yang dibentuk oleh protomer yang sama disebut homogenus, jika terdiri dari protomer berlainan disebut heterogenus.
2.3.2 Sifat Karakteristik Protein
Denaturasi meliputi perubahan-perubahan kimia dalam molekul protein, perubahan-perubahan disebabkan karena protein peka terhadap panas, tekanan yang tinggi, alkohol, alkali, urea, kalium iodida, asam dan pereaksi-pereaksi tertentu lain. Baik denaturasi maupun pengendapan efek totalnya dikenal sebagai penggumpalan atau koagulasi (Sastrohamidjojo, 2009).
Protein sangat cenderung mengalami beberapa bentuk perubahan yang dinyatakan sebagai denaturasi. Denaturasi adalah terbukanya lipatan alamiah struktur protein, proses denaturasi mengubah bentuk dan lipatan tapi tidak merusak ikatan peptida yang terdapat antara asam amino dalam struktur primer (Martoharsono, 1988).
2.3.3 Fungsi Protein
10
Menurut Budiyanto (2002) protein mempunyai berbagai macam fungsi lain bagi tubuh, yaitu:
a. Sebagai enzim
Hampir semua reaksi biologis dipercepat atau dibantu oleh suatu senyawa makro molekul spesifik, dari reaksi yang sangat sederhana seperti reaksi transportasi karbondioksida sampai yang sangat rumit seperti replikasi kromosom.
b. Alat pengangkut dan alat penyimpan
Banyak molekul dengan berat molekul kecil serta beberapa ion dapat diangkut atau dipindahkan oleh protein-protein tertentu. Hemoglobin mengangkut oksigen dalam eritrosit, sedang mioglobin mengangkut oksigen dalam otot. c. Pengatur pergerakan
Protein merupakan komponen utama daging, gerakan otot terjadi karena adanya dua molekul protein yang berperan yaitu aktin dan miosin. Pergerakan flagella sperma disebabkan oleh protein flagelin.
d. Penunjang mekanis
Kekuatan dan daya tahan robek kulit dan tulang disebabkan adanya kolagen, suatu protein berbentuk bulat panjang dan mudah membentuk serabut.
e. Pertahanan tubuh
11 f. Media perambatan implus syaraf
Protein yang mempunyai fungsi ini biasanya berbentuk reseptor misalnya rodopsin, suatu protein yang bertindak sebagai reseptor/ penerima warna atau cahaya pada sel-sel mata.
2.4 Penetapan Kadar Protein 1. Metode Kjeldahl
Menurut SNI 01-2891-1992 prinsip penetapan kadar protein adalah senyawa nitrogen diubah menjadi amonium sulfat oleh asam sulfat pekat, amonium sulfat yang terbentuk diuraikan dengan natrium hidroksida, ammonia yang di bebaskan diikat dengan asam borat dan kemudian dititar dengan larutan baku asam.
Metode Kjeldahl digunakan untuk menganalisis kadar protein kasar dalam bahan makanan secara tidak langsung, karena yang dianalisis dengan cara ini adalah kadar nitrogennya. Dengan mengalikan hasil analisis tersebut dengan angka konversi 6,25 diperoleh nilai protein dalam bahan makanan itu. Angka 6,25 berasal dari angka konversi serum albumin yang biasanya mengandung 16% nitrogen (Budiyanto, 2004).
Analisa dengan metode Kjeldahl pada dasarnya dibagi menjadi tiga tahap yaitu tahap destruksi, tahap destilasi dan tahap titrasi. Pada tahap destruksi sampel dipanaskan dalam asam sulfat pekat sehingga akan terurai. Unsur karbon, hidrogen teroksidasi menjadi CO, CO2, dan H2O. Sedangkan nitrogennya akan
12
ditambahkan katalis seperti selenium. Tahap destruksi sudah selesai apabila
larutan menjadi jernih atau tidak berwarna. Pada tahap destilasi, ammonium sulfat dipecah menjadi ammonia dengan penambahan natrium hidroksida sampai alkalis dan dipanaskan. Ammonia yang dibebaskan akan ditangkap oleh larutan asam standar, seperti asam borat 4%. Destilasi diakhiri bila semua ammonia terdestilasi sempurna dengan ditandai destilat tidak bereaksi. Pada tahap titrasi apabila penampung destilat asam borat berlebih, maka asam borat yang bereaksi dengan ammonia dapat diketahui dengan titrasi menggunakan asam klorida 0,1 N dengan indikator campuran metil red dan bromocresol green, selisih jumlah titrasi sampel dan blanko merupakan jumlah ekuivalen nitrogen (Sudarmadji, 1989). 2. Metode Spektrofotometer UV
Kebanyakan protein mengabsorbsi sinar ultraviolet maksimum pada 280 nm. Hal ini terutama oleh adanya asam amino tirosin, triptofan dan fenilalanin yang ada pada protein tersebut. Pengukuran protein berdasarkan absorbsi sinar UV adalah cepat, mudah dan tidak merusak bahan (Sudarmadji, 1989).
3. Metode Lowry
Konsentrasi protein diukur berdasarkan optikal densiti pada panjang gelombang 600 nm. Untuk mengetahui banyaknya protein dalam larutan, lebih dahulu dibuat kurva standar yang melukiskan hubungan antara konsentrasi dengan OD (absorbansi). Larutan lowry ada dua macam yaitu larutan A yang terdiri dari fosfotungstat-fosfomolibdat (1:1) dan larutan B yang terdiri dari Na2CO3 2%
dalam NaOH 0,1 N, CuSO4 dan Na-K-tartrat 2%. Cara penentuannya: 1 ml larutan
13
Kemudian ditambah 0,5 ml lowry A dikocok dan dibiarkan 20 menit, selanjutnya diamati OD-nya pada panjang gelombang 600 nm (Sudarmadji, 1989).
4. Metode Biuret
Larutan protein dibuat alkalis dengan NaOH kemudian ditambahkan larutan CuSO4 encer. Uji ini menunjukkan adanya senyawa-senyawa yang
mengandung gugus amida (-CONH2) yang berada bersama gugus amida asam