LAPORAN RESMI
PRAKTIKUM DASAR TEKNIK KIMIA I
Materi :
SPEKTROFOTOMETRI ORGANIK
Oleh :
Abdul Wasi NIM : 21030113120096
Febrina Faradhiba NIM : 21030113120190
Ridwan Risky Ardiansyah NIM : 21030113120088
PRAKTIKUM DASAR TEKNIK KIMIA I TEKNIK KIMIA FAKULTAS TEKNIK
UNIVERSITAS DIPONEGORO SEMARANG
Laboratorium Dasar Teknik Kimia 1
ii LAPORAN RESMIPRAKTIKUM DASAR TEKNIK KIMIA I
Materi :
SPEKTROFOTOMETRI ORGANIK
Oleh :
Abdul Wasi NIM : 21030113120096
Febrina Faradhiba NIM : 21030113140190 Ridwan Risky Ardiansyah NIM : 21030113120088
PRAKTIKUM DASAR TEKNIK KIMIA I TEKNIK KIMIA FAKULTAS TEKNIK
UNIVERSITAS DIPONEGORO SEMARANG
2013
Laboratorium Dasar Teknik Kimia 1
ii 1. Materi Praktikum : Spektrofotometri Organik2. Kelompok : IX/Kamis Siang
3. Anggota :
1. Nama : Febrina Faradhiba
NIM : 21030113140190
Jurusan : Teknik kimia
Universitas/Institut : Universitas Diponegoro
2. Nama : Abdul Wasi
NIM : 21030113120096
Jurusan : Teknik kimia
Universitas/Institut : Universitas Diponegoro
3. Nama : Ridwan Risky A
NIM : 21030113120088
Jurusan : Teknik kimia
Universitas/Institut : Universitas Diponegoro
Telah disahkan pada :
Hari :
Tanggal :
Semarang, Desember 2013 Disahkan oleh
Asisten Pembimbing
Bagus Muliajaya Lutfi NIM.21030112120001
Laboratorium Dasar Teknik Kimia 1
ii Puji syukur kami panjatkan kepada Allah SWT berkat rahmat dan hidayah-Nya kami dapat menyelesaikan laporan resmi Praktikum Dasar Teknik Kimia 1 materi spektrofotometri dengan lancar dan sesuai dengan harapan kami.Tujuan penyusunan laporam resmi Praktikum Dasar Teknik Kimia I ini di tujukan sebagai syarat untuk penentuan kelulusan praktikum dasar yang sedang kami lakukan pada semester ini.
Tak lupa ucapan terima kasih juga kami sampaikan kepada : Bapak Dr. Widayat ST, MT selaku dosen penanggung jawab Laboratorium Dasar Teknik Kimia I, Ibu Ir. C. Sribudiati M.T selaku dosen pembimbing, Bapak Muhammad Rustam dan Ibu Dini Iswandari selaku Laboran Laboratorium Dasar Teknik Kimia I, Puji Lestari selaku coordinator asisten Laboratorium Dasar Teknik Kimia I, Bagus Muliajaya Lutfi selaku asisten pembimbing dan semua asisten Laboratorium Dasar Teknik Kimia I, serta semua pihak yang telah membantu dalam pembuatan laporan
Laporan resmi praktikum dasar teknik kimia I ini berisi materi tentang spektrofotometri organik. Spektrofotometri organik adalah metode yang digunakan untuk menganalisa konsentrasi suatu zat dalam suatu larutan berdasarkan absorbansi terhadap warna dari larutan pada panjang gelombang tertentu. Tujuan praktikum spektrofotometri organic yaitu untuk menentukan panjang gelombang optimum antosianin, menetukan kurva hubungan konsentrasi antosianin vs absorbansi pada panjang gelombang optimum dan menentukan konsentrasi antosianin pada sampel.
Laporan resmi ini merupakan laporan resmi terbaik yang saat ini bisa kami ajukan, namun kami menyadari pasti ada kekurangan yang perlu kami perbaiki. Maka, kami memohon maaf bila dalam menyajikan makalah ini masih ada kekurangannya. Saran dan kritik, kami harapkan untuk kedepannya, Semoga makalah ini memberikan manfaat bagi orang lain.
Semarang, Desember 2013
Penyusun DAFTAR ISI
Laboratorium Dasar Teknik Kimia 1
iiHALAMAN PENGESAHAN ... ii
PRAKATA ... iii
DAFTAR ISI ... iv
DAFTAR TABEL ... vi
DAFTAR GAMBAR ... vii
INTISARI ... viii
SUMMARY ... BAB I PENDAHULUAN ... 1
I.1 LATAR BELAKANG ... 1
I.2 TUJUAN PERCOBAAN ... 1
I.3 MANFAAT PERCOBAAN ... 1
BAB II TINJAUAN PUSTAKA ... 2
BAB III METODOLOGI PERCOBAAN ... 4
III.1 BAHAN DAN ALAT YANG DIGUNAKAN ... 4
III.2 GAMBAR ALAT ... 4
III.3 KETERANGAN GAMBAR ... 4
III.4 CARA KERJA ... 5
BAB IV HASIL PERCOBAAN DAN PEMBAHASAN ... 8
IV.1 HASIL PERCOBAAN ... 8
IV.2 PEMBAHASAN ... 9 BAB V PENUTUP ... 14 V.1 KESIMPULAN ... 14 V.2 SARAN ... 14 DAFTAR PUSTAKA ... 15 LAMPIRAN
A. LEMBAR PERHITUNGAN... A-1 B. LAPORAN SEMENTARA ... B-1 C. REFERENSI ... C-1 LEMBAR ASISTENSI
Laboratorium Dasar Teknik Kimia 1
ii Tabel 2.1 Hubungan antara energi terabsorbsi dengan gerakan molekul….…...….2 Tabel 2.2 Spektrum sinar tampak dan warna komplementer ... 2 Tabel 4.1.1 Menentukan panjang gelombang optimum antosianin………….. ... Tabel 4.1.2 Menentukan absorbansi antosianin dalam beberapa konsentrasi ... 9 Tabel 4. 1.3 Menentukan nilai faktor pengenceran pada pH 1 dan pH 4,5 .…...…...10 Tabel 4.1.4 PenentuanKonsentrasi antosianin pada larutan semangka………. 10 Tabel 4.1.4 Konsentrasi antosianin ...DAFTAR GAMBAR
Laboratorium Dasar Teknik Kimia 1
iiGambar 3.2.2 . Tabung Reaksi ……… 5
Gambar 3.2.3. Kuvet……….………5
Gambar 3.2.4. Beaker Glass……….………5
Gambar 3.2.5. Pipet tetes………..………5
Gambar 3.2.6. Gelas Ukur………5
Gambar 3.2.7. Indikator Universal………...………6
Gambar4.2.1 Grafik konsentrasi panjang gelombang vs absorbansi...………...11
INTISARI
Spektrofotometri dapat digunakan untuk menganalisa konsentrasi suatu zat di dalam larutan berdasar absorbansi terhadap warna dari larutan pada panjang gelombang tertentu. Metode spektrofotometri memerlukan larutan standar yang
Laboratorium Dasar Teknik Kimia 1
ii telah diketahui konsentrasinya. Larutan standar terdiri dari beberapa tingkat rendah sampai konsentrasi tinggi. Keuntungan utama dalam pemilihan metode ini adalah metode ini merupakan metode yang sangat sederhana untuk menetapkan kunatitas yang sangat kecil.Spektrofotometri merupakan metode analisa untuk menentukan identitas suatu komponen/konsentrasi dalam larutan yang didasarkan pada pengukuran serapan sinar monokromatis di suatu larutan berwarna. Persen transmitan adalah pembanding Antara intensitas cahaya yang keluar dari sampel terhadap intensitas cahaya yang masuk : %T=I/Io . 100% sedangkan absorbansi dinyatakan sebagai A = log 1/T = -log I/Io = 2-log %T. Banyaknya cahaya/sinar yang diabsorpsi tergantung pada jenis larutannya, panjang kuvet, konsentrasi larutan. Parameter tersebut dinyatakan secara matematis, hukum Beer : A = log I/Io = a.b.c. dari hukum Beer dapat dinyatakan bahwa hubungan Antara absorbansi vs konsentrasi memberikan garis lurus.Pada percobaan ini, langkah kerja yang kami lakukan adalah kalibrasi alat, menentukan panjang gelombang optimum, membuat kurva kalibrasi antara absorbansi vs konsentrasi, dan menentukan kadar antosianin dalam larutan. Kalibrasi alat dilakukan dengan meamasukkan kuvet berisi air demin, kemudian atur T=100. Setelah itu masukkan kuvet sampel yang akan diamati. Untuk menentukan panjang gelombang optimum, lakukan kalibrasi alat kemudian ukur pada panjang gelombang yang berbeda, cari yang menghasilkan absorbansi maksimum. Kemudian mengukur transmitansi sampel pada panjang gelombang optimum dengan komposisi yang berbeda-beda. Kemudain sampel dibuat pH=1 dan pH=4.5 dan diukur pada 520nm dan 700nm guuna mengetahui kadar antosianin.
Hasil percobaan yang kami dapat dari percobaan yaitu panjang gelombang optimum yang kami temukan 560nm. pH dibuat 1 dan pH dibuat 4.5 supaya dapat menghitung antosianin yang ada, pH=1 mewakilkan antosianin dan pengotor, pH 4.5 mewakilkan pengotor.Salah satu cara mengambil ekstrak antosianin dengan menggunakan larutan HCl pada etanol. Hasil percobaan juga tidak sesuai dengan hukum Beer karena keberadaan enzim,pengaruh cahaya,dan pengaruh gula terhadap stabilitas antosianin. Konsentrasi yang didapat pada semangka 2 ml,4ml, 6ml,8ml,dan 10 ml yaitu 0.99ppm, 1.16ppm, 0.52ppm,0.42ppm,dan 5.02ppm.
Sebagai saran kami pada percobaan ini yaitu, atur pH = 1 dan pH= 4.5 dengan tepat supaya hasil konsentrasi yang didapat tepat, larutan sampel yang digunkaan harus jernih, perlu adanya variasi sampel supaya konsentrasi yang didapat akurat. Jangan lupa kalibrasi alat, tambahkan variasi panjang gelombang supaya panjang gelombang optimum dapat ditentukan dengan akurat.
SUMMARY
Spectrophotometry can be used to analyze the concentration of a substance in a solution based on the color of the solution absorbance at a particular wavelength. Spectrophotometric method requires a standard solution of known concentration.
Laboratorium Dasar Teknik Kimia 1
ii Standard solution consists of several levels of low to high concentration. The main advantage of this method is in the selection of this method is a very simple method to establish quantity very small.Spectrophotometry is an analytical method to determine the identity of a component / concentration in a solution based on the measurement of monochromatic light absorption in a colored solution. Percent transmittance is the comparison between the intensity of light emitted from the sample to the intensity of light entering : % T = I / Io . 100 % while the absorbance is expressed as A = log 1 / T = - log I / Io = 2 - log % T. The number of light / light absorbed depends on the type of the solution, the length cuvette , the concentration of the solution . These parameters expressed mathematically, Beer's law: A = log I / Io = abc from Beer's law can be stated that the relationship between the absorbance vs concentrationgave a straight line.
In this experiment , we do the work step is calibration tool , determine the optimum wavelength , making the calibration curve between absorbance vs concentration and determine the levels of anthocyanin in solution . Calibration is done with inserting cuvette containing aquadest, and set T = 100 . After that insert the sample cuvette to be observed. To determine the optimum wavelength, then calibrate the measuring instrument at different wavelengths , which results in searching the maximum absorbance . Then measure the transmittance of the sample at the optimum wavelength with different compositions. Then samples were made of pH = 1 and pH = 4.5 and measured at 520nm and 700nm for determine levels of
anthocyanin .
Our experimental results of experiments that can be the optimum wavelength 560nm we found. made pH 1 and pH 4.5 was made in order to calculate the existing anthocyanin , pH = 1 represents anthocyanin and impurities , pH 4.5 represents an impurity. One way to take the anthocyanin extracts using a solution of HCl in ethanol. The experimental results are also not in accordance with Beer's law due to enzyme,light’s influence,and glucose to stability of antosianin.Concentration obtained in watermelon 2 ml,4ml, 6ml,8ml,dan 10 ml yaitu 0.99ppm, 1.16ppm, 0.52ppm,0.42ppm,dan 5.02ppm.Our advice on this experiment , adjust pH = 1 and pH = 4.5 with the appropriate concentration results obtained so precise , sample solution should be clear , there needs to be variation concentration of the sample to obtain accurate . Do not forget the calibration tool, add the wavelength variation so that the optimum wavelength can be determined accurately .
BAB I PENDAHULUAN
Laboratorium Dasar Teknik Kimia 1
ii Spektrofotometri dapat digunakan untuk mengalisa konsetnrasi usatu zat didalam larutan berdasarkan abosrbansi terhadap warna dari larutan pada panjang gelombang tertentu. Metode spektrofotometri memerlukan larutan standar yang telah diketahui konsentrasinya. Larutan standar terdiri dari beberapa tingkat rendah sampai konsentrasi tinggi.Keuntungan utama dalam pemilihan metode ini adalah metode ini merupakan metode yang sangat sederhana untuk menetapkan kuantitas yang sangat kecil. Spektrofotometri diaplikasikan dalam menentukan beberapa parameter ekologi laut. Tingkat kesuburan suatu perairan ditunjukkan oleh besarnya produksi zat organik yang dihasilkan atau jua disebut produktivitas primer. Salah satu cara yang sudah umum dan luas dipakai adalah mengetahui banyaknya biomassa plankton di laut dengan menentukan kadar klorofil fitoplankton dengan metode spektrofotometri.
I.2. Tujuan Percobaan
a. Menentukan nilai panjang gelombang pada sampel dengan spektrofotometer metode spetrofometri.
b. Menentukan kurva hubungan konsentrasi antosianin vs absorbansi pada panjang gelombang optimumnya dengan spektrofotometer metode spetrofometri.
c. Menetukan konsentrasi antosianin pada sampel dengan spektrofotometer metode spetrofometri.
I.3. Manfaat percobaan
a. Menentukan kurva hubungan konsentrasi antosianin vs absorbansi pada panjang gelombang optimumnya dengan spektrofotometer metode spektrofotometri.
b. Menentukan konsentrasi antosianin pada sampel dengan spektrofotometer metode spektrofotometri.
BAB II
Laboratorium Dasar Teknik Kimia 1
ii Spektrofotometri adalah kata yuang digunakan untuk ilmu yang mengacu pada absorbs, emisi, scattering, dan cahaya dari molekul, ion, atom. Spektrofotometri (teknik spectroscopy) merupakan metode analisa untuk menentukan identitas suatu komponen /konsentrasi dalam larutan yang didasarkan pada pengukuran serapan sinar monokromatis di suatu larutan berwarna.Tabel 2.1 Hubungan Antara Energy Terabsorbsi Dengan Gerakan Molekul Gerakan Molekul Cahaya yang Diabsorbsi Energi
Rotasi Microwave, infrared Rendah
Vibrasi Infrared Sedang
Transit electron Tampak,Ultraviolet Tinggi
Persen transmitan adalah pembanding antara intensitas cahaya yang keluar dari sampel terhadap intensitas yang masuk : %T=I/Io x 100% sedang absorbansi dinyatakan sebagai : A=log1/T = - log (I/Io) = 2 – log (%T)
Tabel 2.2 Spektrum sinar tampak dan warna komplementer (vogel 1989) Panjang Gelombang
(nm)
Warna (terabsorbsi) Warna komplementer (terlihat) 400-435 Violet Kuning-hijau 435-480 Biru Kuning 480-490 HIjau-Biru Orange 490-500 Biru-Hijau Merah 500-560 Hijau Ungu
560-580 Kuning hijau Violet
580-595 Kuning Biru
595-610 Orange Hijau-biru
610-750 Merah Biru-hijau
Banyaknya cahaya /sinar yang diabsorbsi tergantung pada jenis larutannya, panjang sel / kuvet, konsentrasi larutan. Parameter 2 tersebut dinyatakaan secara matematis sesuai dengan hukum Beer sebagai berikut:
A= log (Io/It) = abc Dimana : Io = Intensitas sinar datang
It = Intensitas sinar yang diteruskan
Laboratorium Dasar Teknik Kimia 1
ii a = Absorbtivitasb = Panjang cuvet
c = Konsentrasi (mg/L)
Pada praktikum ini nilai a dan b tidak berubah, sehingga ab dianggap sebagai konstanta baru yaitu K sehingga persamaan A = kc atau bisa dinyatakan dengan persamaan garis lurus. Dari hukum Beer dapat dinyatakan bahwa hubungan antara absorbansi vs konsentrasi akan memberikan garis lurus.
BAB III
METODOLOGI PERCOBAAN
III.1. Alat dan Bahan III.1.1.Bahan
Laboratorium Dasar Teknik Kimia 1
ii 1. Air demin secukupnya2. KCl 20ml
3. Natrium Asetat 20ml 4. Ekstrak strawberry 100ml III.1.2.Alat
1. Spektrofotometri Optima Sp-300 2. Buah Beaker glass 250ml
3. 6 tabung reaksi beserta 1 rak tabung reaksi 4. 1 pipet ukur 10 cc
5. pH meter
6. 4 buah beaker glass 50 cc
Laboratorium Dasar Teknik Kimia 1
ii 1. Spektrofotometri Optima SP-300Gambar 3.2.1 . Spektrofotometri Optima SP-300
2. Tabung Reaksi
Gambar 3.2.2 . Tabung Reaksi
3. Beaker Glass
Gambar 3.2.3. Beaker Glass
4. Kuvet
Gambar 3.2.4. Kuvet 5. Gelas Ukur
Gambar 3.2.5. Gelas Ukur
6. Pipet tetes
Laboratorium Dasar Teknik Kimia 1
ii 7. Indikator UniversalGambar 3.2.7. Indikator Universal
III.3. Keterangan Alat:
1. Spektrofotometri Optima SP-300 : Pengukur % transmitran dengan panjang gelombang tertentu. 2. Beaker Glass : Tempat melarutkan larutan.
3. Gelas Ukur : Untuk mengukur larutan
4. Indikator Universal : Mengukur pH larutan. 5. Tabung Reaksi : Tempat mereaksikan zat
6. Kuvet : Wadah sampel yang akan dimasukkan
ke spektrofotometri optima SP-300 untuk dihitung % transimtrannya. 7. Pipet Tetes : Mengambil larutan dalam skala kecil.
III.4.Cara Kerja
III.4.1. Cara Kalibrasi Alat Spektrofotometri
1. Menghidupkan Optima SP-300 dengan memutar tombol power sampai bunyi klik dan indicator lampu menyala. Biarkan dalam kondisi ini selama 20 menit untuk pemanasan sebelum digunakan. 2. Mengatur panjang gelombang sesuai dengan percobaan yang akan
dilakukan.
3. Pilih mode pembacaan transmitan.
4. Mengosongkan tempat sampel pada spektrofotometer, kemudian tutup. Skala pembacaan transmitan diatur 0%
5. Mengambil cuvet dan membersihkan kemudian mengisi cuvet dengan air demin sampai ¾ nya. Bagian luar cuvet dibersihkan dengan hati-hati
Laboratorium Dasar Teknik Kimia 1
ii 6. Membuka tutup sampel pada spektrofotometer, masukkan cuvet dantutup kembali
7. Mengatur pembacaan transmitan 100% 8. Spektrofotometer siap digunakan
III.4.2. Menentukan Panjang Gelombang Optimum untuk Antosianin 1. Siapkan larutan sampel, masukkan dalam cuvet hingga ¾ nya. Atur
panjang gelombang (490nm), lakukan kalibrasi alat dahulu sebelum menggunakannya.
2. Bila menunjukkan T=0, larutan sampel terlalu pekat, maka harus diencerkan terlebih dahulu, hingga T tidak menunjukkan angka 0. 3. Lakukan kalibrasi alat setiap setelah menggunakan spektrofotometer. 4. Bila larutan sampel yang diuji sudah tidak menunjukkan angka 0,
catat % transmitannya, dan hitung absorbansinya. A = 2-log%T 5. Menaikkan panjang gelombang setiap 10nm, hingga panjang
gelombang 560nm. Lakukan kalibrasi alat saat akan mengganti panjang gelombang. Ulangi langkah 1.
6. Membuat kurva hubungan antara absorbansi versus panjang gelombang, kemudian tentukan nilai panjang gelombang optimum untuk jenis larutan sampel.
III.4.3. Membuat Kurva Kalibrasi Antara Absorbansi Versus Konsentrasi Antosianin
1. Membuat larutan sampel pada berbagai variasi sampel.
2. Mengatur panjang gelombang sesuai dengan panjang gelombang optimum yang ditemukan
3. Melakukan kalibrasi alat spektrofotometri
4. Mengisi cuvet lainnya dengan sampel, masukkan ke dalam tempat sampel, tutup kembali, baca skala % transmitan dan hitung
Laboratorium Dasar Teknik Kimia 1
ii III.4.4. Menentukan Kadar Antosianin Total Dalam Larutan1. Larutan sampel tadi, dibagi menjadi 2 bagian dan dimasukkan dalam beaker glass 50cc sehingga volumenya menjadi 5ml dan 5ml.
2. Ambil beaker glass, atur pH nya menjadi 1 dengan menggunakan larutan buffer KCl. Hitung berapa jumlah volume yang ditambahkan sehingga pH = 1. Lakukan hal yang sama untuk sampel lainnya 3. Mengatur panjang gelombang 520nm, lakukan kalibrasi alat. Setelah
itu masukkan sampel yang sudah diatur pH nya = 1 ke dalam cuvet hingga ¾ bagian. Catat % transmitannya dan hitung absorbansinya. Lakukan hal yang sama untuk sampel lainnya.
4. Mengatur panjang gelombang 700nm, lakukan kalibrasi alat. Setelah itu masukkan sampel yang sudah diatur pH nya = 4,5 ke dalam cuvet hingga ¾ bagian. Catat % transmitannya dan hitung absorbansinya. Lakukan hal yang sama untuk sampel lainnya.
5. Ulangi langkah 2-4 dengan beaker glass lainnya, atur pH menjadi 4,5 dengan larutan NaAsetat
6. Menghitung konsentrasi antosianin total seuai dengan rumus C =
C = Konsentrasi antosianin (mg/L) A = (A520-A700)pH1 - (A520-A700)pH 4.5 MW = Bobot molekul = 449,2 gram/mol DF = Faktor pengenceran
E = 26900 L/mol cm
1000 = Konversi dari gram ke mgr B = Panjang sel atau cuvet
7. Buatlah persamaan Beer untuk konsentrasi antosianin dengan persamaan : A=kc
BAB IV
HASIL PERCOBAAN DAN PEMBAHASAN
Laboratorium Dasar Teknik Kimia 1
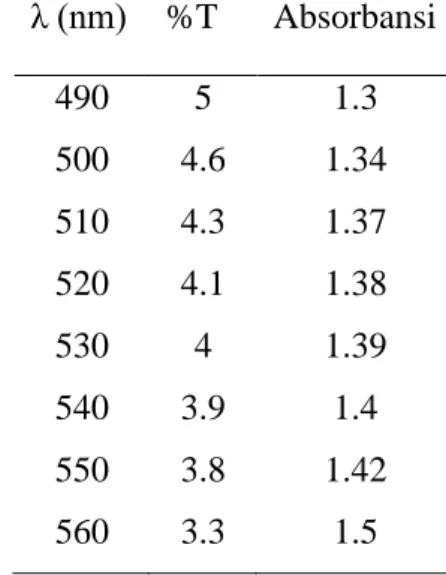
ii IV.1.1 Menentukan Panjang Gelombang Optimum AntosianinTabel 4.1.1 Panjang Gelombang optimum λ (nm) %T Absorbansi 490 5 1.3 500 4.6 1.34 510 4.3 1.37 520 4.1 1.38 530 4 1.39 540 3.9 1.4 550 3.8 1.42 560 3.3 1.5
IV.1.2 Menentukan Absorbansi Larutan
Tabel 4.1.2 Data absorbansi antosianin pada beberapa konsentrasi
Air Demin (ml)
Semangka(ml) %T Absorbansi Konsentrasi(mgr/L)
0 10 3.3 1.48 5.02 2 8 4.3 1.37 0.42 4 6 7.3 1.14 0.52 6 4 13.6 0.87 1.16 8 2 40.3 0.39 0.99 10 0 100 0 -
IV.1.3 Menentukan Nilai Faktor Pengenceran Pada Ph 1 dan Ph 4,5 Tabel 4.1.3 Data pengenceran volume sampel
Volume 1 Volume 2 pH=1 Volume 2 pH=4.5 dF pH1 dF pH 4.5 dF rata-rata
Laboratorium Dasar Teknik Kimia 1
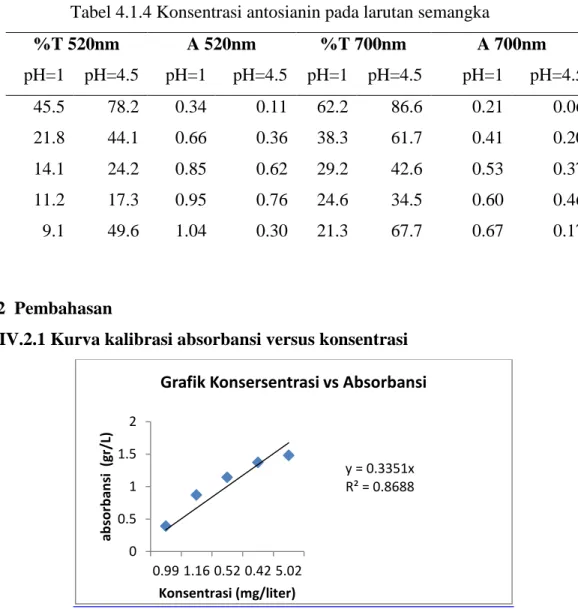
ii 5 6.1 2.4 1.22 4.8 3.01 5 6.5 14.7 1.3 2.94 2.12 5 7.7 10.3 1.54 2.06 1.8 5 8 12.4 1.6 2.48 2.04 5 8.7 42 1.74 8.4 5.07IV.1.4. Penentuan Konsentrasi Antosianin Pada Larutan Semangka Tabel 4.1.4 Konsentrasi antosianin pada larutan semangka
%T 520nm A 520nm %T 700nm A 700nm pH=1 pH=4.5 pH=1 pH=4.5 pH=1 pH=4.5 pH=1 pH=4.5 45.5 78.2 0.34 0.11 62.2 86.6 0.21 0.06 21.8 44.1 0.66 0.36 38.3 61.7 0.41 0.20 14.1 24.2 0.85 0.62 29.2 42.6 0.53 0.37 11.2 17.3 0.95 0.76 24.6 34.5 0.60 0.46 9.1 49.6 1.04 0.30 21.3 67.7 0.67 0.17 IV.2 Pembahasan
IV.2.1 Kurva kalibrasi absorbansi versus konsentrasi
Gambar 4.2.1 Hubungan konsentrasi vs absorbansi antosianin ekstrak semangka
Grafik diatas menunjukan bahwa semakin besar % sampel dalam larutan semakin besar konsentrasinya,dan hasil yang diperoleh sudah menunjukkan gejala yang benar.Hukum Lambert-Beer menyatakan bahwa apabila seberkas monokromatis dengan intensitas I0 melalui suatu material/zat maka banyak
y = 0.3351x R² = 0.8688 0 0.5 1 1.5 2 0.99 1.16 0.52 0.42 5.02 ab sor b an si (gr /L) Konsentrasi (mg/liter)
Laboratorium Dasar Teknik Kimia 1
ii sinar yang di absorbs pada suatu senyawa tergantung dari konsentrasi senyawa tersebut dan media yang dilaluinya.Hubungan antara penerapan konsentrasi (C)dan panjang media dinyatakan dengan :A = a.b.c (gr/L) atau A=ε.b.c (mol/L)
Karena menggunakan larutan dan cuvet yang sama,maka variable a dan b dapat konstan sehingga persamaan menjadi :
A= k.c ; A sumbu y,c sumbu x,maka y=k.x
Persamaan diatas merupakan persamaan linier yang seharusnya menunjukkan bahwa kian pekat sampel,kian tinggi konsentrasinya.Hal ini berlaku pada grafik kami karena molar (ε) yang didapat dari persamaan A= ε.b.c bukanlah suatu penetapan yang bergantung pada konsentrasi.Untuk system ini harus menggunakan nilai absorbantivitas molar yang tergantung pada sifat dasar,spesies pengorbansi dalam larutan dan juga pada panjang gelombang radiasi.
IV.2.2. Kadar Antosianin Praktis Lebih Kecil dari Kadar Teori
Pada Percobaan yang kami lakukan kadar antosianin yang ditemukan adalah sebesar 5.02 ppm sedangkan kadar antosianin yang kami temukan pada journal adalah 70.10 ppm.Hal ini disebabkan oleh factor-faktor sebagai berikut:
a) Keberadaan enzim
Keberadaan enzim seperti glukosidase dan polifenol oksidase (PPO) merupakan salah satu factor pendukung degradasi antosianin.Enzim glukosidase secara langsung menyerang antosianin dengan cara menghidrolisis ikatan antara gugus aglikon dengan gugus glikon.Hal ini menyebabkan cincin aromatic antosianin terbuka menjadi senyawa kalkon yang tidak berwarna.Berbeda dengan enzim glukosidase,enzim PPO tidak secra langsung menyerang antosianin.Enzim ini mengoksidasi senyawa fenolik menjadi o-benzoquinon.
Senyawa o-benzoquinon yang kemudian dapat mengalami kondensasi dengan antosianin sehingga antosianin terdegradasi menjadi senyawa tidak berwarna.
Laboratorium Dasar Teknik Kimia 1
ii b) Pengaruh CahayaKondisi Lab.Dasar Teknik Kimia ! yang memiliki banyak jendela besar membuat sampel yang kami gunakan banyak terpapar sinar matahari.Padahal cahaya berpengaruh terhadap konsentrasi antosianin,yaitu mampu mendegradasi pigmen antosianin dan membentuk kalkon yang tidak berwarna.Energi yang dikeluarkan cahaya memicu terjadinya reaksi fitokimia atau fitooksidasi yang dapat membuka cincin antosianin.Seperti reaksi berikut:
Paparan yang lebih lama menyebabkan terjadinya degradasi lanjutan dan terbentuk senyawa turunan lain seperti 2,4,6-trihidroksi benzaldehid dan asam benzoate tersubstitusi.Hal tersebut meneyebabkan kadar antosianin yang ditemukan lebih kecil dari kadar asli.
(Anonim,2013)
c) Pengaruh Gula terhadap Stabilitas Antosianin
Gula yang terdapat pada semangka dapat menginduksi peningkatan intensitas warna antosianin terutama pada kondisi sedikit asam.Namun ada beberapa pendapat bahwa keberadaan asam askorbat,glukosa,dan fruktosa secara bersama – sama dapat mempercepat degradasi
Laboratorium Dasar Teknik Kimia 1
ii dapat diketahui dapat mempercepat degradasi antosianin.Hal inimenyebabkan kadar antosianin yang ditemukan lebih kecil dari kadar asli.
(Anonim,2013) IV.2.3 Cara Ekstraki Antosianin
Ekstraksi adalah suatu cara untuk mendapatkan zat dari bahan yang diduga mengandung zat tersebut. Pada buah atau sayuran, pigmen antosianin umumnya terletak pada sel-sel dekat permukaan. Ekstraksi antosianin dari bahan nabati umumnya menggunakan larutan pengekstrak HCl dalam etanol. Hcl dalam etanol akan mendenaturasi membrane sel tanaman kemudian melarutkan pgimen antosianin keluar dari sel. Pigmen antosianin dapat larut dalam etanol karena sama-sama polar. Misalnya pada ekstraksi antosianin dari bunga pacar air, pelarut yang paling baik digunakan adalah etanol 95%. Ini disebabkan tingkat kepolaran antosianin hamper sama dengan etanol 95% sehingga dapat larut dengan baik pada 95%. Selain pelarut, factor yang mempengaruhi yaitu waktu ekstraksi, pH, dan temperatur. Asam sitrat juga digunakan pada saat ekstraksi dimana asam sitrat akan berfungsi sebagai pengontrol keasaman.
(Simon,2013)
IV.2.4 Pengaruh pH 1 dan pH 4.5 pada Antosianin
Salah satu karakteristik utama antosianin adalah perubahan warna yang merespon adanya perubahan pH lingkungan warna dan stabilitas antosianin sangat bergantung dari pH.Antosianin paling stabil pada pH rendah dan perlahan kehilangan warnanya seiring dengan peningkatan pH dan menjadi tidak berwarna pada pH 4,0 sampai 5,0.Menurut Rein (2005) antosianin lebih stabil pada larutan asam daripada larutan netral atau alkali.Gerak warn antosianin akan kembali dengan adanya peningkatan derajat keasaman.
Untuk membuat pH larutan menjadi rendah/pH = 1,digunakan larutan buffer asam berupa KCl yang diturunkan pHnya dengan HCl pekat menjadi sama dengan 1.Pada larutan sampel (semangka)tidak hanya tekandung antosianin saja,namun juga ada zat –zat lain yang dalam prakyikum ini mengganggu pengamatan (zat pengotor).Pada suasana asam,antosianin menjadi lebih stabil sehingga warna merah menjadi lebih terlihat sedangkan
Laboratorium Dasar Teknik Kimia 1
ii zat pengotor akan menjadi tidak stabil dan pudar.Lalu untuk membuat larutan pH 4.5 digunakan larutan Natrium Aseta yang telah diturunkan pHnya dengan HCl pekat menjadi sama dengan 4.5.Pada pH 4.5,antosianin menjadi tidak stabil sehingga warna merahmenjadi pudar.Dengan begitu,zat pengotor dapat transmitannya.Maka dari itu dengan menghitung selisih antara abrorbansi pada pH=1 daimana antosianin lebih stabil dengan pH=4.5 dimana zat pengotor yang terukur,dapat diketahui absorbansi dari antosianin.(Arya,2012)
IV.2.5 Penggunaan Panjang Gelombang 520 nm dan Panjang Gelombang 700 nm
Semangka mengandung antosianin yang merupakan zat warna merah.Semangka memiliki kandungan antosianin yang dominan,hal inilah yang menyebabkan semangka berwarna merah.Semangka mempunyai panjang gelombang optimum 520 nm.Pada panjang gelombang 520nm,warna yang terabsorbsi adalah hijau biru dan warna yang terlihat (komplementer) adalah merah.Maka dari itu,pada panjang gelombang 520nm semangka memiliki nilai absorbansi maksimum.
Namun pada panjang gelombang 700 nm,warna yang terabsorbsi adalah warna merah dan warna yang terlihat ( komplementernya ) adalah hijau – biru.Maka dari itu ,pada panjang gelombang 700 nm,semangka memilki nilai absorbansi minimum.Jika dihitung selisih absorbansi pada panjang gelombang 520 nm dengan panjang gelombang 700 nm,akan di dapat absorbansi untuk mengukur antosianin.
(Dykirana,2012)
BAB V PENUTUP
V.1.Kesimpulan
1. Nilai panjang gelombang optimum pada sampel dengan spektrofotometri terdapat pada panjang gelombang 560 nm.
Laboratorium Dasar Teknik Kimia 1
ii 2. Kadar semangka yang ditemukan pada journal adalah 79.10 ppm.Data yang kami temukan lebih kecil yaitu 5.02 ppm.Hal ini dikarenakan kebeeradaan enzim,pengaruh cahata,dan pengaruh gula terhadap antosianin.3. Hubungan kurva konsentrasi antosianin dan absorbansi memiliki y = 0.335x ,dimana y adalah absorbansi dan x adalah konsentrasi antosianin.
V.2.Saran
1. Atur pH=1 dan pH=4.5 dengan tepat dengan menambah buffer Kcl dan buffer NaAsetat supaya konsentrasi yang dihasilkan tepat.
2. Sebaiknya larutan yang digunakan harus jernih supaya sesuai dengan hukum Lambert-Beer
3. Perlu adanya variasi sampel supaya konsentrasi yang dihasilkan akurat.
4. Kalibrasi alat supaya hasil yang ditunjukkan tepat.
5. Tambahkan variasi panjang gelombang supaya panjang gelombang optimumnya lebih akurat.
DAFTAR PUSTAKA
Anonim.2013.Merah Ungu Antosianin. http://seafast.ipb.ac.id/tpc-project/wp-content/uploads/2013/03/06-merah-ungu-antosianin.pdf.3 November 2013
Barners,kw,dkk. 2005. Determination of otal morometric antosianin pigmen content of fruit juice, beverage, natural colorants, and louise by the ph
Laboratorium Dasar Teknik Kimia 1
ii differential Groggins, pH. 1950. “unit porses in organic synthesis”. 5 ed.PP.700-783 McGraw Hill Book Company. Inc. New York.Dwidjanarko,Simon.2013.EkstraksiAntosianin.http://simonbwidjanarko.wordpress. com/2008/06/ekstrak_antosianin_2.doc.5 November 2013
Dykirana.2012.Spektrofotometer.http://dykirana.blogspot.com/2012/08/spektrofotom eter.html.5 November 2013
J.pharm.2006. Solubilization and quantification o lycopene in aqueous media I the form of cyclodextrin Binari System. Diakses tanggal 4 Mei 2013. Keer.R.W. 1950. Chemistry and industry of starch. 2&d. PP375-403. Academic
press. Inc. New York.
Method Collaboration study. Journal of AOAC international. Vol 85.rb.5.PP 1269-1278
Penelope,perkins veanic. 2002. Composition of orange, yellow, and red fleshes watermelon.
Ulilalbab,Arya.2012.Stabilitas Antosianin.http://aryaulilalbab.webunair.ac.id.5 November 2013
Vogel.1989. Texbook of quantitative Chemical analysis.longman scientific and technical. PP 645-676 great Britain.
Woodman, A. 1941. “Food analysis”. 4 ed.PP 264-261. Mc Graw Hill Book Company Inc. New York.
LEMBAR PERHITUNGAN 1. Menentukan Absorbansi dan Konsentrasi
1. A = (A520-A700)pH1 - (A520-A700)pH 4.5
= (0,34-0,21) – (0.11-0.06)
= 0.08
Laboratorium Dasar Teknik Kimia 1
ii = = 0.99 mg/L 2. A = (A520-A700)pH1 - (A520-A700)pH 4.5 = (0.66-0.41) – (0,36-0.20) = 0.09 C = = = 1.16 mg/L 3. A = (A520-A700)pH1 - (A520-A700)pH 4.5 = (0,85-0.53) – (0,62-0,37) = 0.07 C = = = 0.52 mg/L 4. A = (A520-A700)pH1 - (A520-A700)pH 4.5 = (0,95-0.60) – (0,76-0,46) = 0.05 C = =Laboratorium Dasar Teknik Kimia 1
ii = 0.42 mg/L 5. A = (A520-A700)pH1 - (A520-A700)pH 4.5 = (1.04-0,67) – (0,30-0.17) = 0.24 C = = = 5.02 mg/L = 1,591ppmLaboratorium Dasar Teknik Kimia I
B-1
LAPORAN SEMENTARAPRAKTIKUM DASAR TEKNIK KIMIA I
Materi :
SPEKTROFOTOMETRI ORGANIK
Oleh :
Kelompok : IV / Kamis Siang
Anggota : Abdul Wasi NIM : 21030113120096 Febrina Faradhiba NIM : 21030113120190 Ridwan Risky A NIM : 21030113120088
LABORATORIUM DASAR TEKNIK KIMIA I TEKNIK KIMIA FAKULTAS TEKNIK
UNIVERSITAS DIPONEGORO SEMARANG
Laboratorium Dasar Teknik Kimia I
B-4
I.TUJUAN PERCOBAANa. Menentukan nilai panjang gelombang pada sampel dengan spektrofotometer metode spetrofometri.
b. Menentukan kurva hubungan konsentrasi antosianin vs absorbansi pada panjang gelombang optimumnya dengan spektrofotometer metode spetrofometri.
c. Menetukan konsentrasi antosianin pada sampel dengan spektrofotometer metode spetrofometri.
II. PERCOBAAN
2.1Bahan Yang Digunakan 1.Air demin secukupnya 2.KCl 20ml
3.Natrium Asetat 20ml 4.Ekstrak strawberry 100ml
2.1 Alat Yang Dipakai
8. Spektrofotometri Optima Sp-300 9. Buah Beaker glass 250ml
10.6 tabung reaksi beserta 1 rak tabung reaksi 11.1 pipet ukur 10 cc
12.pH meter
13.4 buah beaker glass 50 cc
2.3 Cara Kerja
IV.1.1.Cara kalibrasi alat spektrofotometri
1.Menghidupkan Optima SP-300 dengan memutar tombol power sampai bunyi klik dan indicator lampu menyala. Biarkan dalam kondisi ini selama 20 menit untuk pemanasan sebelum digunakan.
2.Mengatur panjang gelombang sesuai dengan percobaan yang akan dilakukan.
Laboratorium Dasar Teknik Kimia I
B-4
3.Pilih mode pembacaan transmitan.4.Mengosongkan tempat sampel pada spektrofotometer, kemudian tutup. Skala pembacaan transmitan diatur 0%
5.Mengambil cuvet dan membersihkan kemudian mengisi cuvet dengan air demin sampai ¾ nya. Bagian luar cuvet dibersihkan dengan hati-hati 6.Membuka tutup sampel pada spektrofotometer, masukkan cuvet dan tutup
kembali
7.Mengatur pembacaan transmitan 100% 8.Spektrofotometer siap digunakan
VI.4.2.Menentukan panjang gelombang optimum untuk antosianin 1.Siapkan larutan sampel, masukkan dalam cuvet hingga ¾ nya. Atur
panjang gelombang (490nm), lakukan kalibrasi alat dahulu sebelum menggunakannya.
2.Bila menunjukkan T=0, larutan sampel terlalu pekat, maka harus diencerkan terlebih dahulu, hingga T tidak menunjukkan angka 0. 3.Lakukan kalibrasi alat setiap setelah menggunakan spektrofotometer. 4.Bila larutan sampel yang diuji sudah tidak menunjukkan angka 0, catat %
transmitannya, dan hitung absorbansinya. A = 2-log%T
5.Menaikkan panjang gelombang setiap 10nm, hingga panjang gelombang 560nm. Lakukan kalibrasi alat saat akan mengganti panjang gelombang. Ulangi langkah 1.
6.Membuat kurva hubungan antara absorbansi versus panjang gelombang, kemudian tentukan nilai panjang gelombang optimum untuk jenis larutan sampel.
VI.4.3.Membuat kurva kalibrasi antara absorbansi versus konsentrasi antosianin
1.Membuat larutan sampel pada berbagai variasi sampel.
2.Mengatur panjang gelombang sesuai dengan panjang gelombang optimum yang ditemukan
Laboratorium Dasar Teknik Kimia I
B-4
4.mengisi cuvet lainnya dengan sampel, masukkan ke dalam tempat sampel,tutup kembali, baca skala % transmitan dan hitung absorbansinya. A = 2-log%T. Ulangi untuk sampel lainnya.
VI.4.4.Menentukan kadar antosianin total dalam larutan
1. Larutan sampel tadi, dibagi menjadi 2 bagian dan dimasukkan dalam beaker glass 50cc sehingga volumenya menjadi 5ml dan 5ml.
2. Ambil beaker glass, atur pH nya menjadi 1 dengan menggunakan larutan buffer KCl. Hitung berapa jumlah volume yang ditambahkan sehingga pH = 1. Lakukan hal yang sama untuk sampel lainnya
3. Mengatur panjang gelombang 520nm, lakukan kalibrasi alat. Setelah itu masukkan sampel yang sudah diatur pH nya = 1 ke dalam cuvet hingga ¾ bagian. Catat % transmitannya dan hitung absorbansinya. Lakukan hal yang sama untuk sampel lainnya.
4. Mengatur panjang gelombang 700nm, lakukan kalibrasi alat. Setelah itu masukkan sampel yang sudah diatur pH nya = 4,5 ke dalam cuvet hingga ¾ bagian. Catat % transmitannya dan hitung absorbansinya. Lakukan hal yang sama untuk sampel lainnya.
5. Ulangi langkah 2-4 dengan beaker glass lainnya, atur pH menjadi 4,5 dengan larutan NaAsetat
6. Menghitung konsentrasi antosianin total seuai dengan rumus C =
C = Konsentrasi antosianin (mg/L) A = (A520-A700)pH1 - (A520-A700)pH 4.5 MW = Bobot molekul = 449,2 gram/mol DF = Faktor pengenceran
E = 26900 L/mol cm
1000 = Konversi dari gram ke mgr B = Panjang sel atau cuvet
Laboratorium Dasar Teknik Kimia I
B-5
6. Buatlah persamaan Beer untuk konsentrasi antosianin denganpersamaan : A=kc
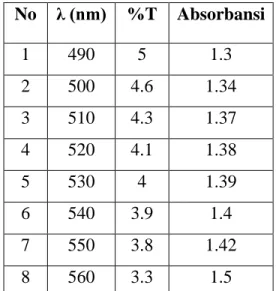
II. Hasil Percobaan
No λ (nm) %T Absorbansi 1 490 5 1.3 2 500 4.6 1.34 3 510 4.3 1.37 4 520 4.1 1.38 5 530 4 1.39 6 540 3.9 1.4 7 550 3.8 1.42 8 560 3.3 1.5
Tabel 4.1.1 Panjang Gelombang optimum
No Air Demin (ml) Antosianin (ml) %T Absorbansi Konsentrasi(mgr/L) 1 0 10 3.3 1.48 5.02 2 2 8 4.3 1.37 0.42 3 4 6 7.3 1.14 0.52 4 6 4 13.6 0.87 1.16 5 8 2 40.3 0.39 0.99 6 10 0 100 0 -
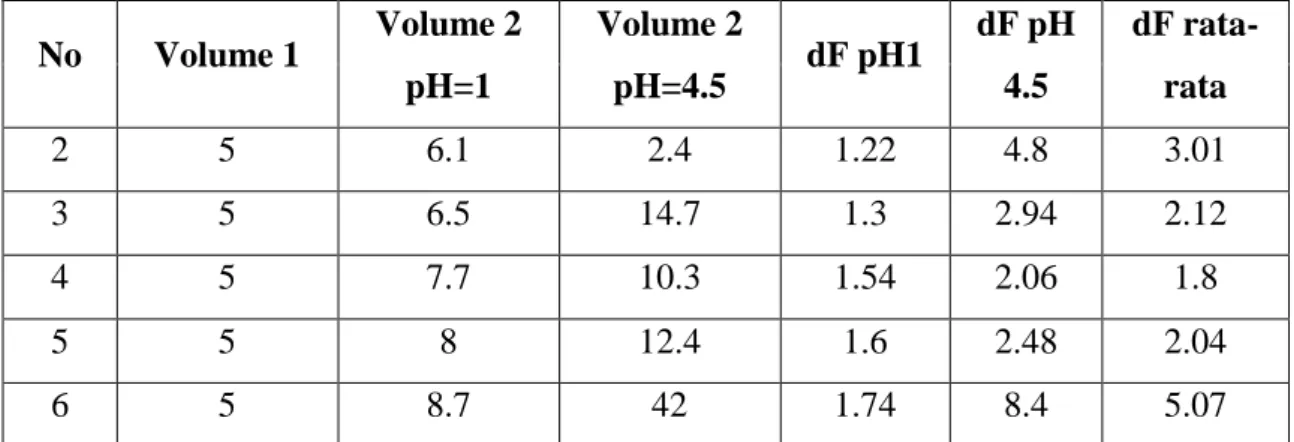
Laboratorium Dasar Teknik Kimia 1
C-2 No Volume 1 Volume 2 pH=1 Volume 2 pH=4.5 dF pH1 dF pH 4.5 dF rata-rata 2 5 6.1 2.4 1.22 4.8 3.01 3 5 6.5 14.7 1.3 2.94 2.12 4 5 7.7 10.3 1.54 2.06 1.8 5 5 8 12.4 1.6 2.48 2.04 6 5 8.7 42 1.74 8.4 5.07Tabel 4.1.3 Pengenceran volume sampel
%T 520nm A 520nm %T 700nm A 700nm pH=1 pH=4.5 pH=1 pH=4.5 pH=1 pH=4.5 pH=1 pH=4.5 45.5 78.2 0.34 0.11 62.2 86.8 0.21 0.06 21.8 44.1 0.66 0.36 38.3 61.7 0.41 0.20 14.1 24.2 0.85 0.62 29.2 42.6 0.53 0.37 11.2 17.3 0.95 0.76 24.6 34.5 0.60 0.46 9.1 49.6 1.04 0.30 21.3 67.7 0.67 0.17
Tabel 4.1.4 Konsentrasi antosianin
MENGETAHUI
PRAKTIKAN ASISTEN
Laboratorium Dasar Teknik Kimia I
C-1
REFFERENSICahaya seperti halnya panas, mampu mendegradasi pigmen antosianin dan
membentuk kalkon yang tidak berwarna. Energi yang dikeluarkan oleh cahaya mampu memicu terjadinya reaksi fitokimia atau fotooksidasi yang dapat membuka cincin antosianin. Paparan yang lebih lama menyebabkan terjadinya degradasi lanjutan dan terbentuk senyawa turunan lain seperti 2,4,6-trihidroksibenzaldehid dan asam benzoat tersubstitusi.
Jenis pelarut antosianin secara nyata mempengaruhi warna yang diekspresikannya. Sifat antosianin yang hidrofilik menyebabkannya sering diekstrak dengan menggunakan pelarut alkohol atau air. Pelarut alkohol menghasilkan warna antosianin yang lebih biru dibandingkan dengan pelarut air.
Pengaruh gula terhadap stabilitas antosianin masih menjadi perdebatan. Bebrapa sumber menyebutkan bahwa gula dapat menginduksi peningkatan intensitaswarna antosianin, terutama pada kondisi asam. Namun sumber lain menyebutkan bahwa keberadaan asam askorbat, glukosa, dan fruktosa secara bersama-sama dapat mempercepat degradasi antosianin karena keempat senyawa tersebut dapat berkondensasi dengan antosianin menghasilkan phlobafen yang berwarna coklat. Keberadaan enzim seperti glukosidase dan polifenol oksidase (PPO) diketahui merupakan salah satu faktor pendukung degradasi antosianin. Enzim glukosidase secara langsung menyerang antosianin dengan cara menghidrolisis ikatan antara gugus aglikon dengan gugus glikon. Hal ini menyebabkan cincin aromatik antosianin terbuka menjadi senyawa kalkon yang tidak berwarna. Berbeda dengan enzim glukosidase, enzim PPO tidak secara langsung menyerang antosianin. Enzim ini mengoksidasi senyawa fenolik menjadi o-benzoquinon. Senyawa o-benzoquinon yang kemudian dapat mengalami kondensasi dengan antosianin. Sehingga antosianin terdegradasi menjadi senyawa tidak berwarna (kalkon).
http://seafast.ipb.ac.id/tpc-project/wp-content/uploads/2013/03/06-merah-ungu-antosianin.pdf
Laboratorium Dasar Teknik Kimia I
C-4
Pada buah atau sayuran, pigmen antosianin umumnya terletak pada sel-sel dekatpermukaan (Markakis, 1982). Ekstraksi pigmen antosianin dari bahan nabati umumnya menggunakan larutan pengekstrak HCl dalam etanol (Gao and Mazza, 1996). HCl dalam etanol akan mendenaturasi membran sel tanaman kemudian melarutkan pigmen antosianin keluar dari sel. Pigmen antosianin dapat larut dalam etanol karena sama-sama polar (Broillard, 1982).
Pada penelitian Saati (2002) untuk ekstraksi antosianin dari bunga pacar air, pelarut yang paling baik digunakan adalah etanol 95 %. Begitu juga dengan penelitian Wijaya (2001) tentang ekstraksi pigmen dari kulit buah rambutan. Hal ini disebabkan tingkat kepolaran antosianin hampir sama dengan etanol 95 % sehingga dapat larut dengan baik pada etanol 95 %. Selain pelarut, menurut Pifferi and Vaccari (1998), faktor-faktor yang dapat mempengaruhi hasil ekstraksi antosianin adalah waktu ekstraksi, pH dan temperatur ekstraksi.
Asam Sitrat
Asam sitrat adalah asam organik yang banyak ditemukan pada buah-buahan dan
sayuran. Konsentrasi tertinggi terdapat pada buah lemon dan jeruk nipis yaitu sekitar 8
% dari berat kering buah. Keasaman asam sitrat disebabkan karena tiga gugus karboksil
COOH yang dapat melepaskan proton ke dalam larutan. Jika hal ini terjadi, ion yang
dihasilkan disebut ion sitrat (Wikipedia, 2004).
Pada suhu ruangan, asam sitrat berbentuk bubuk kristal putih. Asam sitrat bisa terdapat dalam bentuk “anhydrous” (bebas air) atau monohidrat yang mengandung satu molekul air tiap molekul asam sitrat. Asam sitrat aman digunakan dalam bahan pangan
walaupun dalam jumlah besar. Ini didasarkan pada peraturan pangan nasional dan
internasional. Asam sitrat bisa dimetabolisme dan dikeluarkan dari tubuh (Wikipedia,
2004).
Industri makanan dan minuman banyak menggunakan asam sitrat. Pemilihan jenis
Laboratorium Dasar Teknik Kimia I
C-4
diinginkan dan dipasaran tersedia dalam jumlah besar. Asam sitrat merupakan bahantambahan pangan yang mempunyai fungsi bervariasi. Industri makanan dan minuman
kebanyakan mengkonsumsinya untuk mempertegas flavor dan warna. Fungsi lainnya
adalah mengontrol keasaman. Pengontrolan pH yang tepat akan mencegah pertumbuhan
mikroorganisme dan bertindak sebagai pengawet serta membantu mencegah terjadinya
reaksi pencoklatan (Hui, 1992).
Tabel 4 Sifat-Sifat Asam Sitrat.
Karakteristik Asam sitrat
Nama lain Rumus kimia Berat molekul Densitas Pka
Asam 2-hidroksi-1,2,3-propan trikarboksilat C6H8O7 192 1,665 x 103 kg/m3 8,2 x 10-4 Sumber : Wikipedia (2004) http://simonbwidjanarko.wordpress.com/2008/06/ekstrak_antosianin_2.doc
Laboratorium Dasar Teknik Kimia I
C-4
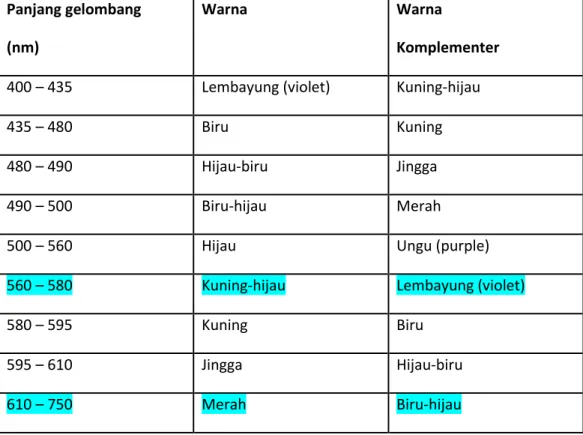
Tabel 3. Spektrum cahaya tampak
http://dykirana.blogspot.com/2012/08/spektrofotometer.html
Panjang gelombang (nm)
Warna Warna
Komplementer
400 – 435 Lembayung (violet) Kuning-hijau
435 – 480 Biru Kuning
480 – 490 Hijau-biru Jingga
490 – 500 Biru-hijau Merah
500 – 560 Hijau Ungu (purple)
560 – 580 Kuning-hijau Lembayung (violet)
580 – 595 Kuning Biru
595 – 610 Jingga Hijau-biru
610 – 750 Merah Biru-hijau
Warna Intervalλ Intervalν
Red 625 to 740 nm 480 to 405 THz Orange 590 to 625 nm 510 to 480 THz Yellow 565 to 590 nm 530 to 510 THz Green 520 to 565 nm 580 to 530 THz Cyan 500 to 520 nm 600 to 580 THz Blue 430 to 500 nm 700 to 600 THz Violet 380 to 430 nm 790 to 700 THz
Laboratorium Dasar Teknik Kimia I
C-5
LEMBAR ASISTENSIDIPERIKSA KETERANGAN
TANDA TANGAN