I. Pendahuluan
A. Latar Belakang
Senyawa organik terutama mengandung atom karbon dan atom hidrogen, ditambah nitrogen, dan oksigen. Atom-atom tersebut berikatan dan tersusun dalam susunan yang unik. Susunan unik tersebut memberikan sifat dan fungsi khusus. Sifat dari senyawa tersebut juga berhubungan erat dengan penggunaannya dalam kehidupan nyata (Williamson, 1998).
Gugus funsional sebagai ciri utama suatu senyawa organik yang pada dasarnya dapat diketahui secara jelas dengan mengelompokkan molekul-molekul tersebut saling berkaitan sehingga sulit untuk membahas suatu gugus fungsional tanpa menyinggung gugus fungsional yang lainnya. Tetapi secara sederhana dapat dikatakan bahwa gugus fungsional adalah suatu atom-atom, gugus atom dalam suatu senyawa organik yang boleh dikatakan paling menentukan sifat zat tersebut (Arsyad, 2001). Zat yang memiliki gugus fungsional yang berbeda dapat memiliki sifat yang berbeda walaupun molekul lain yang mengikat gugus fungsionalnya identik. Zat yang memiliki gugus fungsional yang sama akan mengalami reaksi kimia yang sama, apapun bentuk atau jenis kerangka karbonnya. Akan tetapi, reaktivitas relatifnya dapat dipengaruhi oleh keberadaan gugus fungsional lain di dekatnya. (Ratnawati, 2011).
Beberapa contoh gugus fungsional yang ada dan sering ditemui dalam senyawa organik adalah –OH (alkohol), O (eter), CHO (aldehid), CO (keton), –COOH (asam karboksilat), -COO- (ester) dan benzena. Beberapa diantaranya dapat menghasilkan turunan senyawa seperti fenol, amina, dan amida (Feseden, 1994). Setiap gugus yang berbeda memiliki sifat yang berbeda, hal tersebut berarti saat direaksikan akan terjadi reaksi yang berbeda terhadap suatu indikator. Oleh karena itu, zat tertentu dapat digunakan sebagai indikator untuk menunjukkan adanya suatu gugus secara kualitatif (Arsyad, 2001).
B.Tujuan
Untuk memahami konsep dasar dalam pengujian gugus fungsional tertentu dan memiliki keterampilan dalam melakukan pengujian suatu gugus fungsional.
II. Bahan dan Metode
A.Waktu dan Tempat Praktikum
Praktikum dilaksanakan pada tanggal 12 September 2012, pukul 08.00-11.00 WIB. Bertempat di Laboratorium Biokimia dan Biologi Molekuler, Fakultas Biologi, Universitas Kristen Satya Wacana, Salatiga.
B. Alat dan Bahan
Alat yang digunakan antara lain tabung reaksi, rak tabung reaksi, pipet tetes, batang pengaduk, bunsen, panci, dan sendok plastik.
Bahan uji yang digunakan antara lain K2Cr2O7, KMnO4, asam formiat, padatan asam
salisilat, fenol, akuades, metanol, formaldehid, aseton, anilin, padatan urea, dan etanol. Sedangkan bahan analisis yang digunakan adalah H2SO4 pekat, H2SO4 1 M, FeCl3, larutan Br2, reagen d.n.p.,
AgNO3 1 M, NH4OH 1 M, reagen Schiff, NaOH 5%, NaOH 4 M, larutan I2, kertas lakmus, dan gas.
C. Metode
1. Alkohol
a. Uji Oksidasi Alkohol
Disiapkan 2 tabung reaksi. Satu tabung di tetesi K2Cr2O7 sebanyak 3 tetes. Kemudian
di tetesi lagi dengan H2SO4 1 M sebanyak 2 tetes. Ditambah lagi 5 tetes etanol 96%.
Kemudian dipanaskan kurang lebih 1 menit dan diamati perubahan warnanya. Diulangi tahapan yang sama untuk kontrol (akuades) namun tidak ditambah etanol. Untuk KMnO4
dilakukan hal yang sama seperti K2Cr2O7 dan juga kontrolnya.
b. Pembentukan Ester dari Alkohol
Disiapkan dua tabung reaksi. Satu tabung reaksi di tetesi asam formiat sebanyak 10 tetes. Kemudian ditetesi etanol 5 tetes. Ditambahkan 5 tetes H2SO4 pekat. Tabung reaksi
kedua dimasukki 1 ujung asam salisilat kemudian di tetesi metanol sebanyak 5 tetes dan H2SO4 sebanyak 5 tetes. Kedua tabung tersebut kemudian di panaskan dalam air mendidih
2. Fenol
a. Uji dengan FeCl3
Disiapkan dua tabung reaksi. Satu tabung reaksi ditetesi fenol 5 tetes. Tabung kedua ditetesi akuades sebagai kontrol. Masing-masing tabung kemudian ditetesi FeCl3 sebanyak
3 tetes. Diamati perubahan warnanya.
b. Uji dengan Brom
Disiapkan 2 tabung reaksi. Satu tabung reaksi di tetesi fenol sebanyak 5 tetes. Kemudian brom diteteskan setetes demi setetes sambil diamati perubahan warnanya. Begitu juga dengan akuades dilakukan tahapan-tahapan yang sama.
3. Karbonil
a. Reaksi dengan Reagen d.n.p (2,4-dinitrofenilhidrogina)
Disiapkan 3 tabung reaksi. Ketiganya ditetesi d.n.p masing-masing sebanyak 3 tetes. Pada tabung pertama ditambah 1 tetes aseton. Pada tabung kedua ditambah 1 tetes formaldehid dan pada tabung ketiga di tambah 1 tetes akuades sebagai kontrol. Diamati perubahan warnanya.
b. Oksidasi Aldehid dengan Pengoksidasi Kuat
Disiapkan 2 tabung reaksi. Satu tabung dimasukki 3 tetes K2Cr2O7. Tabung kedua
dimasukki 3 tetes akuades sebagai kontrol. Kemudian kedua tabung ditetesi formaldehid sebanyak 3 tetes. Kemudian diamati perubahan warna yang terjadi.
c. Oksidasi Aldehid dengan Reagen Tollens
Disiapkan sebuah tabung reaksi. Tabung reaksi dimasukki 5 tetes Ag NO3.
Kemudian dimasukki 5 tetes NH4OH dan 3 tetes formaldehid. Tabung reaksi tersebut
kemudian dipanaskan dalam air mendidih. Setelah beberapa saat, tabung diangkat dan diamati terbentuknya cermin perak.
d. Oksidasi Aldehid dengan reagen Schiff
Disiapkan sebuah tabung reaksi. Sebanyak 5 tetes reagen Schiff dimasukkan kedalam tabung. Kemudian 2 tetes formaldehid dimasukkan. Diamati perubahan warna yang terjadi.
e. Uji Iodoform
Disiapkan sebuah tabung reaksi. Sebanyak 10 tetes akuades dimasukkan ke dalam tabung. Dimasukkan juga 2 tete aseton dan 10 tetes NaOH 5% ke dalam tabung Setetes demi setetes KI/I2 diteteskan sampai warna Iodium tidak hilang. Diamkan selama 2 – 3
menit. Diamati terbrntuknya Kristal Idoform atau tidak.Jika tidak terbentuk kristal, tabung di panaskan, kemudian ditetesi KI/I2 setetes demi setetes sampai warna tidak hilang.
4. Asam Karboksilat a. Keasaman
Asam karboksilat diteteskan pada lakmus merah. Diamati perubahan warna yang terjadi pada kertas lakmus.
b. Pembentukan Ester
Disiapkan satu tabung reaksi. Tabung reaksi dimasukki 1 ujung asam salisilat. Kemudian dimasukki 5 tetes etanol dan 5 tetes H2SO4. Dipanaskan dalam air mendidih
kemudian dicium aroma yang dihasilkan.
5. Amina
a. Daya Larut
Sebanyak 2-3 tetes HCl 1 M dimasukkan ke dalam tabung reaksi. Sebanyak satu tetes anilin dimasukkan kedalam tabung. Diamati yang terjadi. Ditambahkan 2 tetes NaOH 1 M ke dalam tabung dan diamati penggumpalan yang terjadi.
b. Uji dengan Brom
Sebanyak 10 tetes etanol dimasukkan ke dalam tabung reaksi. Ditambahkan 5 tetes anilin ke dalamnya. Ke dalam tabung ditetesi brom setetes demi setetes dan diamati perubahan warnanya.
6. Amida
Satu ujung sendok urea dimasukkan ke dalam tabung reaksi. Ditambahkan sebanyak 10 tetes NH4OH 4 M kemudian dipanaskan di dalam air mendidih untuk beberapa saat. Tabung
reaksi kemudian diangkat dan dimasukki kertas lakmus merah. Diamati perubahan warna yang terjadi pada lakmus.
III. Hasil dan Pembahasan
A. Hasil
1. Alkohol
a. Uji Oksidasi Alkohol
Berdasarkan hasil pengujian dan pengamatan oksidasi alcohol, diperoleh hasil pada tabel 1. berikut:
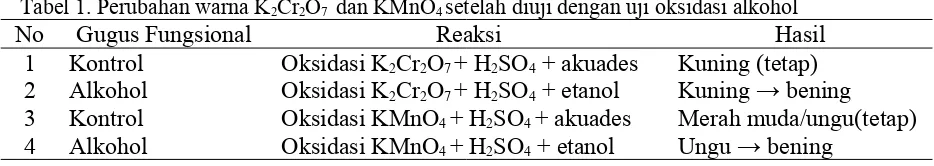
Tabel 1. Perubahan warna K2Cr2O7 dan KMnO4 setelah diuji dengan uji oksidasi alkohol
No Gugus Fungsional Reaksi Hasil
1 Kontrol Oksidasi K2Cr2O7 + H2SO4 + akuades Kuning (tetap)
2 Alkohol Oksidasi K2Cr2O7 + H2SO4 + etanol Kuning → bening
3 Kontrol Oksidasi KMnO4 + H2SO4 + akuades Merah muda/ungu(tetap)
b. Pembentukan Ester dari Alkohol
Berdasarkan hasil pengujian dan pengamatan pembentukn ester dari alkohol, ditampilkan hasil pada tabel 2. berikut:
Tabel 2. Aroma yang dihasilkan dalam pengujian pembentukan ester
No Gugus Fungsional Reaksi Hasil
1 Alkohol Esterifikasi asam formiat + etanol + H2SO4 Aroma buah
2 Alkohol Esterifikasi asam salisilat + metanol + H2SO4 Aroma balsem
2. Fenol
a. Uji dengan FeCl3
Berdasarkan hasil pengujian gugus fenol menggunakan FeCl3, diperoleh hasil pada
tabel 3. berikut:
Tabel 3. Perubahan warna yang terjadi pada pengujian menggunakan FeCl3
No Gugus Fungsional Reaksi Hasil
1 Fenol Fenol + FeCl3 Putih → ungu kehitaman
2 Kontrol Akuades + FeCl3 Putih → kuning
b. Uji dengan Brom
Berdasarkan hasil pengujian gugus fenol menggunakan brom, diperoleh hasil pada tabel 4. berikut:
Tabel 4. Perubahan warna yang terjadi setelah diuji dengan Brom
No Gugus Fungsional Reaksi Hasil
1 Fenol Fenol + FeCl3 Pada tetesan Br2 ke-3 berubah jadi
kuning+
2 Kontrol Akuades + FeCl3 Pada tetesan Br2 ke-1 berubah jadi kuning
3. Karbonil
a. Reaksi dengan Reagen d.n.p (2,4-dinitrofenilhidrogina)
Berdasarkan hasil pengujian gugus karbonil menggunakan reagen d.n.p, diperoleh hasil pada tabel 5. berikut:
Tabel 5. Perubahan warna yang terjadi setelah ditetesi reagen d.n.p
No Gugus Fungsional Reaksi Hasil
1 Karbonil Reagen d.n.p + aseton Kuning → kuning ++
dengan endapan
2 Karbonil Reagen d.n.p + formaldehid Kuning → kuning + dengan endapan
3 Kontrol Reagen d.n.p + akuades Kuning (tetap)
b. Oksidasi Aldehid dengan Pngoksidasi Kuat
Berdasarkan hasil pengujian gugus karbonil menggunakan pengoksidasi kuat, diperoleh hasil pada tabel 6. berikut:
Tabel 6. Perubahan warna yang terjadi setelah di uji dengan pengoksidasi kuat
No Gugus Fungsional Reaksi Hasil
2 Kontrol akuades + formaldehid Bening (tetap)
c. Oksidasi Aldehid dengan Reagen Tollens
Berdasarkan hasil pengujian gugus karbonil menggunakan reagen Tollens, diperoleh hasil pada tabel 7. berikut:
Tabel 7. Pembentukan cermin perak setelah diuji dengan reagen Tollens
No Gugus Fungsional Reaksi Hasil
1 Karbonil AgNO3 + NH4OH + formaldehid Terbentuk cermin perak
d. Oksidasi Aldehid dengan Reagen Schiff
Berdasarkan hasil pengujian gugus karbonil menggunakan reagen Schiff, diperoleh hasil pada tabel 8. berikut:
Tabel 8. Pembentukan cermin perak setelah diuji dengan reagen Tollens
No Gugus Fungsional Reaksi Hasil
1 Karbonil Reagen Schiff + formaldehid Tidak berwarna → ungu
e. Uji Iodoform
Berdasarkan hasil pengujian gugus karbonil menggunakan Iodoform, diperoleh hasil pada tabel 9. berikut:
Tabel 9. Pembentukan kristal setelah diuji menggunakan Iodoform
No Gugus Fungsional Reaksi Hasil
1 Karbonil Akuades + aseton + NaOH 5% + I2 Tidak terbentuk kristal
4. Asam Karboksilat a. Keasaman
Berdasarkan hasil pengujian gugus asam karboksilat menggunakan keasaman, diperoleh hasil pada tabel 10. berikut:
Tabel 10. Perubahan warna setelah diuji keasaman
No Gugus Fungsional Reaksi Hasil
1 Asam karboksilat Asam format + kertas lakmus merah Merah (tetap)
b. Pembentukan Ester
Berdasarkan hasil pengujian gugus asam karboksilat menggunakan pembentukan ester, diperoleh hasil pada tabel 11. berikut:
Tabel 11. Aroma yang dihasilkan dalam pembentukan ester
No Gugus Fungsional Reaksi Hasil
1 Asam karboksilat Asam salisilat + etanol + H2SO4 Aroma buah
5. Amina
a. Daya Larut
Berdasarkan hasil pengujian gugus amina menggunakan uji daya larut, diperoleh hasil pada tabel 12. berikut:
Tabel 12. Penggumpalan yang terjadi setelah diuji daya larut
No Gugus Fungsional Reaksi Hasil
1 Amina HCl + Anilin + NaOH 1 M Penggumpalan anilin
Berdasarkan hasil pengujian gugus amina menggunakan brom, diperoleh hasil pada tabel 13. berikut:
Tabel 13. Perubahan warna setelah diuji dengan brom
No Gugus Fungsional Reaksi Hasil
1 Amina Etanol + aniline + Br2 Merah kehitaman
6. Amida
Berdasarkan hasil pengujian gugus amida, diperoleh hasil pada tabel 14. berikut:
Tabel 14. Perubahan warna lakmus merah pada zat amida yang diuji
No Gugus Fungsional Reaksi Hasil
1 Amida Urea + NH4OH 4M + lakmus merah Lakmus merah → biru
B. Pembahasan
1. Alkohol
a. Uji Oksidasi Alkohol
Alkohol digolongkan menjadi 3 golongan. Penggolongan tersebut didasarkan terhadap banyaknya ikatan atom karbon dengan karbon yang lain dan mengandung gugus −OH. Ketiga golonga tersebut adalah alkohol primer, alkohol sekunder, dan alkohol tersier. Alcohol primer adalah alcohol yang gugus - OH nya terikat pada atom C primer (atom C yang mengikat 1 atom C yang lain). Alcohol sekunder adalah alcohol yang gugus - OH nya terikat pada atom C sekunder (atom C yang mengikat 2 atom C yang lain). Alcohol tersier adalah alcohol yang gugus - OH nya terikat pada atom C tersier (atom C yang mengikat 3 atom C yang lain) (Anonim, 2011).
Tampak pada tabel 1. bahwa gugus fungsi alkohol setelah bereaksi berubah warna menjadi bening, baik dengan oksidator K2Cr2O7 maupun KMnO4. Setelah direaksikan dan
dipanaskan bahan berubah warna menjadi bening karena –OH bereaksi dengan pereaksi atau oksidator sehingga membentuk etanal dan H2O. Karena rantai –OH berpisah dan
berikatan dengan pereaksi/oksidator, maka membuat warna awal pun berubah menjadi bening (Williamson, 1989).
b. Pembentukan Ester dari Alkohol
Ester dapat dihasilkan dari reaksi antara alkohol dengan asam karboksilat. Ester memiliki ciri-ciri yang khas. Ciri khas tersebut terdapat pada aroma yang dimiliki ester. Pada pengujian ini digunakan katalisator H2SO4 pekat unutuk asam formiat dan etanol serta
salisilat yang memiliki aroma mint atau seperti balsam karena ikatan atom C-nya pendek (Feseden, 1994).
2. Fenol
a. Uji dengan FeCl3
Fenol memiliki cincin benzene dan gugus fungsional alkohol. Dalam pengujian fenol ini warna putih berubah menjadi ungu kehitaman setelah fenol di tetesi FeCl3. Warna putih
memudar terjadi karena FeCl3 bereaksi dengan fenol membentuk kompleks fenol dengan
Cl sehingga ion Fe3+ tereduksi dan kehilangan warnanya (Chang, 2005).
b. Uji dengan Brom
Kejadian yang terjadi pada uji dengan brom juga hampir sama dengan uji menggunakan FeCl3. Warna putih berubah warna pada tetesan ke 3 menjadi kuning lebih
tua dari kuning kontrol. Hal ini terjadi karena selama 2 tetes Br2 bereaksi sehinga warnanya
tetap putih. Namun saat tetesan ke-3 warnanya berubah. Hal tersebut menunjukkan bahwa jumlah Br2 yang direaksikan terlalu banyak dan membuatnya tidak dapat bereaksi lagi
dengan fenol. Akibatnya terjadi perubahan warna menjadi kuning (Chang, 2005).
3. Karbonil
a. Reaksi dengan reagen d.n.p (2,4-dinitrofenilihidrogina)
Jika gugus karbonil direaksikan dengan reagen d.n.p akan menghasilkan endapan berwarna kuning hingga kemerahan. Pada pengujian menggunakan d.n.p digunakan aseton dan formaldehid. Aseton menghasilkan endapan dengan cairan berubah warna menjadi kuning tua. Sedangkan pada formaldehid ditemukan endapan dan cairan berubah menjadi warna kuning yang lebih muda dari aseton. Warna kuning aseton lebih tua dibanding formaldehid bisa jadi dikarenakan ikatan rangkap yang dimiliki aseton sedangkan aldehid tidak memiliki (Depdikbud, 1981).
b. Oksidasi Aldehid dengan Pengoksidasi Kuat
Senyawa karbonil yang dengan mudah dioksidasi adalah aldehid. Aldehid jika dioksidasi akan tetap atau tidak berubah warnanya. Dan dalam pengujian ini terbukti benar bahwa zat tersebut bergugus karbonil (Depdikbud, 1981).
c. Oksidasi Aldehid dengan Reagen Tollens
Dengan reagen Tollens dihasilkan cermin perak sebagai hasil dari reaksi. Dalam pengujian ini digunakan formaldehid, AgNO3 dengan NH4OH atau reagen Tollens. Saat
pemanasan terjadi reaksi antara AgNO3 dan reagen Tollens. Reaksi terebut memicu
terbentuknya cermin perak (Arsyad, 2001).
Reagen Schiff saat bereaksi dengan formaldehid akan mebuat perubahan warna. Semula tidak berwarna kemudian saat bereaksi berubah menjadi ungu. Hal ini membuktikan memang benar bahwa yang diuji memilki gugus karbonil (Feseden, 1994).
e. Uji Iodoform
Seharusnya terbentuk kristal berwarna kuning dalam pengujian iodofom ini. Kristal tersebut seharunya menjadi hasil reaksi bertahap aseton dengan iodoform. Dalam hasil pengujian tidak dapat ditemukan kristal. Kemungkinan terjadi kesalahan teknis dalam pengujian. Saat memasukkan NaOH 5% seharusnya dilakukan secara perlahan sambil dikocok sedikit tabung reaksinya. Karena tergesa-gesa dalam menambahkan NaOH dan mendiamkannya yang hanya sebentar dapat mengakibatkan kristal tidak terbentuk (Williamson, 1989).
4. Asam Karboksilat
Untuk pengujian keasaman yang menggunakan lakmus merah. Lakmus merah tetap merah atau tidak berubah warna sehingga menunjukkan bahwa bersifat asam. Untuk pembentukan ester, berdasarkan hasil aroma yang dihasilkan adalah aroma buah. Senyawa ester akan terbentuk jika gugus karboksil bereaksi dengan gugus alkohol. Dan dikarenakan rantai atom C kurang dari 10 maka aromanya adalah aroma buah (Williamson, 1989).
5. Amina
a. Daya Larut
Amina adalah senyawa turunan amonia yang satu atau beberapa atom H-nya digantikan oleh alkil atau gugus aromatik. Anilin merupakan salah satu contoh amina primer. Aniline bersifat basa lemah sehingga larut dalam larutan asam. HCl bersifat asam sedangkan aniline bersifat basa lemah, berarti aniline larut dalam HCl. Pada percobaan ini terjadi pemisahan saat anilin diteteskan ke HCl. Setelah ditetesi NaOH terjadi penggumpalan. Hal ini menunjukkan penggumpalan terjadi saat basa lemah dimasukkan pada larutan asam kuat dan kemudian diberi basa kuat (Depdikbud, 1981).
b. Uji dengan Brom
Saat diuji dengan brom, anilin bereaksi dengan FeCl3 sehingga dapat membentuk
kompleks Fe dengan anilin. Seiring dengan kompleks reaksi yang terjadi perubahan warna menjadi kecoklatan. Hasil percobaan menunjukkan terjadinya perubahan warna menjadi merah kehitaman atau mendekati warna coklat. Terbukti zat tersebut benar-benar memiliki gugus amina (Williamson, 1989).
6. Amida
dipanasi akan mengalami proses hidrolisis yang menghasilkan garam dari asam karboksilat dan ammonium hidroksida. Dalam pengujian ini, didaptkan bahwa kerta lakmus merah berubah nejadi biru. Menunjukkan bahwa larutan tersebut bersifat basa sesuai dengan teori (Feseden, 1994).
IV. Kesimpulan
Gugus fungsional merupakan gugusan atau susunan kelompok atom dalam suatu senyawa organik yang paling menentukan ciri khas dari senyawa tersebut. Terdapat banyak jenis gugus fungsional diantaranya alkohol, fenol, karbonil, asam karboksilat, amina, dan amida. Identifikasi gugus alkohol dapat diketahui dari perubahan warna dan aroma. Identifikasi Fenol dapat diketahui dari perubahan warna. Identifikasi gugus karbonil dapat diketahui dengan perubahan warna, terbentuknya cermin perak, dan endapan kristal Iodoform. Gugus asam karboksilat dapat diketahui dengan perubahan warna kertas lakmus dan aroma. Identifikasi gugus amina dapat diketahui dengan ada tidaknya penggumpalan anilin dan perubahan warna. Serta untuk identifikasi gugus amida dapat diketahui dengan perubahan warna kertas lakmus. Setiap gugus fungsional memiliki susunan atom yang berbeda, dengan susunan berbeda berarti sifat dan fungsi, dan reaksi terhadap indikator/pereaksi berbeda pula. Zat tertentu dapat digunakan sebagai indikator/pereaksi untuk menunjukkan adanya suatu gugus fungsi secara kualitatif.
Daftar Pustaka
Anonim. 2011. Reaksi Identifikasi Alkohol Primer, Sekunder, dan Tersier.
(http://www.jejaringkimia.web.id/2011/01/reaksi-identifikasi-alkohol-primer.html). Diakses tanggal 19 Oktober 2012.
Arsyad, 2001. Kamus Kimia. Jakarta: Gramedia.
Chang, R. 2005. Kimia Dasar Konsep-Konsep Inti Edisi Ketiga Jilid I. Jakarta: Erlangga. Depdikbud. 1981. Petunjuk Praktikum Ilmu Kimia. Jakarta: Depdikbud.
Feseden, Ralph J. 1994. Kimia Organik Terjemahan A.H. Pudjaatmaka. Jakarta:Erlangga.
Ratnawati,2011. Gugus Fungsional. (
http://tekim.undip.ac.id/staf/ratnawati/files/2011/09/BAB-3-GUGUS-FUNGSIONAL.pdf). Diunduh tanggal 19 Oktober 2012.