Dasar Teori Perhitungan Jumlah TAHAP:
ABSORBER BERTALAM -JAMAK YANG BEROPERASI SECARA “Counter-Current”
Counter-current Multi-stage Absorption (
Tray absorber
)
Di dalam
Menara Abrober Bertalam
(
tray absorber
), berlangsung operasi perpindahan massa
secara kontak multi-tahap (bertahap-jamak) antara gas dan cairan. Dalam setiap
tray
(talam)
tersebut, cairan (yang berperan sebagai
absorben
) dikondisikan ke dalam suatu sistem kontak
intensif dengan gas (yang mengandung
absorbat
atau
absorptif
) sehingga tercapai keadaan
keseimbangan, yang berarti terjadi sau tahap yang ideal pada talam tersebut. Pada tahap yang ideal
tersebut,
komposisi
rata-rata cairan yang meninggalkan talam berada dalam kesetimbangan dengan
jumlah
cairan yang meninggalkan talam tersebut. Langkah yang terutama dan terpenting dalam
perancangan Menara Abrober Bertalam adalah penentuan atau perhitungan jumlah talam (
number
of trays
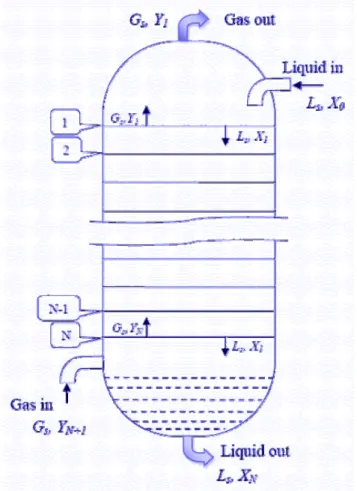
). Skematis menara talam dimaksud disajikan pada
Gambar 1
di bawah ini. Cairan masuk
dari atas kolom (
Liquid in
) sedangkan gas diumpankan dari bawah (
Gas in
). Efisiensi dari tahap
dapat dihitung sebagai:
Jumlah dari TAHAP
Efisiensi Tahap
Jumlah dari TAHAP Sesungguhnya (
)
=
Ideal
Nyata
Parameter-parameter di bawah ini harus diketahui dalam penentuan (perhitungan)
jumlah
tahap
, yaitu:
1.
Laju Gas Umpan
(simbol:
G
s)
2.
Konsentrasi gas
pada masukan (
inlet
,
Y
N+1) dan keluaran (
outlet
,
Y
1) dari menara absorpsi
3.
Laju Cairan Minimum
(simbol:
L
min); sedangkan
Laju Cairan Aktual
(simbol:
L
s)
dapat ditentukan antara 1,2 – 2 kali dari
L
min.
4.
Data Kesetimbangan
yang diperlukan untuk konstruksi
Kurva Kesetimbangan
.
Setelah semua data atau parameter di atas diketahui, maka
Jumlah Tahap Teoretis
dapat
diperoleh, baik secara
grafis
ataupun melalui
persamaan aljabar
.
A. Penentuan Jumlah Tahap Ideal secara Grafis
Neraca massa
secara menyeluruh (dalam keadaan kesetimbangan) dari sistem operasi
Absorpsi
di
dalam Menara Talam dimaksud dapat dinyatakan sebagai:
(
1 1)
(
0)
s N s N
G Y
+−
Y
=
L X
−
X
(1)
Persamaan di atas disebut sebagai
Garis Operasi
(
Operating Line
) dari Menara Talam.
Jika
tahap
operasinya (absorpsi) adalah
ideal
dan identik dengan
talam
nya, maka titik
(
X Y
n,
n)
harus terletak pada garis kesetimbangan,
Y
*=
f X
( )
.
Tahap (talam) teratas terletak di
P X Y
(
0,
1)
dan pelat di bagian dasar berada pada titik
(
N,
N 1)
Q X
Y
+di bidang
X Y
−
. Dari garis operasi tersebut, dibuat suatu garis tegak (vertikal) dari
titik
Q
ke titik
D
dalam Garis Kesetimbangan pada
(
X
N,
Y
N)
. Dari titik
D X
(
N,
Y
N)
dalam
Garis Kesetimbangan tersebut, dibuat garis horizontal sebagai perpanjangannya hingga memotong
Garis Operasi kembali di titik
E X
(
N−1,
Y
N)
. Dalam hal ini, daerah segitiga
QDE
merupakan
representasi dari talam yang ke-
N
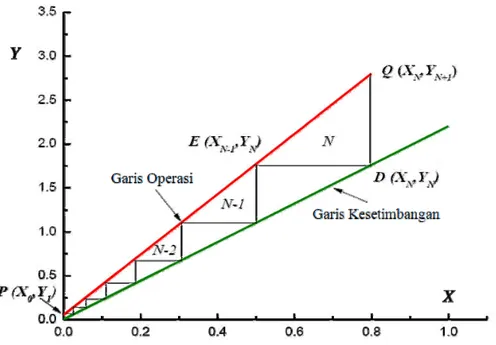
(lihat
Gambar 2
di bawah ini).
Dari daerah segitiga
QDE
seperti di atas, sesungguhnya telah kita dapatkan fraksi atau bagian
(kecil) dari talam dalam posisi tertentu. Diambil dari posisi tersebut, maka jumlah talam secara
menyeluruh adalah merupakan penjumlahan dari talam-talam ideal yang dihasilkan. Selanjutnya,
jika efisiensi tahap secara menyeluruh diketahui, maka jumlah talam nyatanya (sesungguhnya)
dapat diperoleh dari
Persamaan (1)
seperti di atas.
B. Penentuan Jumlah Tahap Ideal menggunakan Persamaan Aljabar
Jika keduanya, Garis Operasi dan Garis Kesetimbangan membentuk garis-garis lurus, maka jumlah
tahap ideal dapat ditentukan (dihitung) menggunakan persamaan aljabar.
Dalam
kasus Absorpsi
, yaitu jika terjadi peristiwa perpindahan
solute
(
absorbat
atau
absorptif
)
dari fasa gas ke fasa cairan, maka akan berlaku persamaan
Garis Kesetimbangan
seperti di bawah ini:
Y
=
m X
⋅
(2)
Dalam hal ini, kelandaian
m
adalah sebagai
konstanta Henry
(seringkali dinyatakan dalam
H
). Oleh
karenanya, titik
(
X
N,
Y
N)
haruslah berada pada Garis Kesetimbangan seperti di atas, atau dapat
juga dinyatakan sebagai:
N N
Y
=
m X
⋅
(3)
Di sisi lain, Garis Operasinya dapat dinyatakan sebagai berikut:
(
)
(
)
(
)
(
)
(
)
1 1 0 1 1 0 1 1 0 s N N s s N N s s N N sL
Y
Y
X
X
G
L
Y
Y
Y
X
G
m
L
Y
Y
Y
m X
G m
+ + +⎫
−
=
⋅
−
⎪
⎪
⎪
⎛
⎞
⎪
−
=
⋅
⎜
−
⎟
⎬
⎝
⎠
⎪
⎪
−
=
⋅
−
⋅
⎪
⋅
⎪⎭
(4)
sehingga diperoleh,
(
Y
N+1−
Y
1)
=
A Y
⋅
(
N−
m X
⋅
0)
(5)
dengan
Garis Operasi
Garis Kesetimbangan
s sL
Kelandaian
A
G m
Kelandaian
=
=
=
⋅
Faktor Absorpsi
Sekarang, Persamaan (5) di atas dapat dimodifikasi menjadi suatu “
Persamaan Linier
order-1”
dalam bentuk “
Persamaan Beda
” (
Difference Equation
) non-homogen berikut ini:
(
)
(
)
(
) (
)
1 1 0 1 1 0 N N N NY
Y
A Y
A m X
Y
A Y
Y
A m X
+ +⎫
−
=
⋅
−
⋅ ⋅
⎪
⎬
−
⋅
=
−
⋅ ⋅
⎪⎭
(6)
Langkah-langkah penyelesaian dengan menggunakan
Metode
Finite Difference
, dapat diberikan
secara ringkas sebagai berikut:
Berhubungan dengan Persamaan Homogen:
(
Y
N+1−
A Y
⋅
N)
=
0
(7)
Solusi dari Persamaan Homogen seperti di atas adalah:
Y
N=
c Z
1 n(8)
Maka, persamaan asalnya menjadi:
c Z
1 n+1−
A c Z
⋅ ⋅
1 n=
0
(9)
Sehingga, diperoleh:
Z
=
A
(10)
Yang berarti, bahwa Persamaan Non-homogen yang dimaksud ternyata memliki “Solusi Partikular”
(khusus) berupa suatu konstanta (tetapan).
Selanjutnya, dengan asumsi
Y
N=
Y
N+1, didapatkan
Y
=
c
2dan kemudian akan diperoleh
relasi berikut:
2 2 1 0 1 0 21
c
A c
Y
m A X
Y
m A X
c
A
⎫
−
⋅
=
−
⋅ ⋅
⎪
⎬
−
⋅ ⋅
=
⎪
−
⎭
(11)
Sehingga, solusi lengkapnya adalah sebagai berikut:
1 0 1 2 1
1
N N NY
m A X
Y
c A
c
c A
A
−
⋅ ⋅
=
⋅
+
=
⋅
+
−
(12)
Selanjutnya, dengan harga-harga pada kondisi awal:
0 0
0
N
Y
m X
=
⎫
⎬
=
⋅
⎭
akan diperoleh:
0 1 0 0 11
Y
m A X
m X
c A
A
−
⋅ ⋅
⋅
=
⋅
+
−
selanjutnya:
0 0 1 0 1 0 1 11
1
m X
m A X
Y
m A X
c
A
m X
Y
c
A
⎫
⋅
−
⋅ ⋅
−
+
⋅ ⋅
=
⎪
−
⎪
⎬
⋅
−
⎪
=
⎪
−
⎭
(13)
dan kemudian:
0 1 1 01
1
N Nm X
Y
Y
m A X
Y
A
A
A
⋅
−
−
⋅ ⋅
=
⋅
+
−
−
(14)
Pada saat
N
=
N
+
1
, persamaan (14) di atas menjadi:
1 0 1 1 0 1
1
1
N Nm X
Y
Y
m A X
Y
A
A
A
+ +=
⋅
−
−
⋅
+
−
−
⋅ ⋅
Jika di ruas kanan dari persamaan di atas, kedua faktor yang ada dikalikan dengan
1 1 A A, maka akan
diperoleh
1 0 0 1 11
1
1
1
N NY
m X
m X
Y
A
Y
A
A
A
+−
⋅
⋅
−
=
⋅
+
⎛
−
⎞
⎛
−
⎞
⎜
⎟
⎜
⎟
⎝
⎠
⎝
⎠
(
)
1 1 0 1 01
1
Y
Nm X
Y
A
NY
m X
A
+A
⎛
⎞
⎛
−
⎞
⋅
=
⋅
−
⋅
+
−
⋅
⎜
⎟
⎜
⎟
⎝
⎠
⎝
⎠
(
)
1 0 1 1 01
1
N NY
m X
Y
A
Y
m X
A
+A
⎛
⎞
⎛
⎞
⋅
−
⋅
=
⎜
−
⎟
⋅
−
⎜
−
⋅
⎟
⎝
⎠
⎝
⎠
kemudian
(
)
1 1 0 0 11
1
N NY
Y
m X
A
A
A
m X
Y
+⎛
⎞
⎛
−
⎞
⋅
−
−
⋅
⎜
⎟
⎜
⎟
⎝
⎠
⎝
⎠
=
⋅
−
atau
1 0 1 01
1
1
NY
Nm X
A
Y
m X
A
A
+⎛
−
⋅
⎞
⎛
⎞
=
⎜
⎟ ⎜
⋅
−
⎟
+
−
⋅
⎝
⎠
⎝
⎠
(15)
Dari persamaan (15) terakhir di atas, jika kedua sisinya dilogaritmakan dan dengan syarat
A
≥
1
, maka
( )
1 0 1 01
1
1
ln
ln
Y
Nm X
N
A
Y
m X
A
A
+⎡
⎛
−
⋅
⎞
⎛
⎞
⎤
⋅
=
⎢
⎜
⎟ ⎜
⋅
−
⎟
+
⎥
−
⋅
⎝
⎠
⎢
⎝
⎠
⎥
⎣
⎦
atau
( )
1 0 1 01
1
1
ln
ln
NY
m X
Y
m X
A
A
N
A
+⎡
⎛
−
⋅
⎞
⋅
⎛
−
⎞
+
⎤
⎢
⎜
−
⋅
⎟ ⎜
⎝
⎟
⎠
⎥
⎢
⎝
⎠
⎥
⎣
⎦
=
bila
A
>
1
(16)
Namun, bila harga
A
=
1
, maka persamaan (6) menjadi
Persamaan Garis Operasi
, yaitu dalam
bentuk sebagai berikut:
(
Y
N+1−
Y
N) (
=
Y
1−
m X
⋅
0)
Dan, jika kita jumlahkan semua suku-suku deret yang terbentuk dari persamaan di atas, yaitu
penjumlahan suku dengan harga
N
mulai dari
N
=
N N
,
−
1
,
N
−
2
, , ,
… …
sampai dengan
2 1
, ,
N
=
…
, maka akan didapatkan:
atau, jika disusun ulang menjadi
(
)
(
1 1 10)
NY
Y
N
Y
m X
+−
=
−
⋅
bila
A
=
1
(17)
Dalam
kasus Desorpsi
(
Stripping
atau
Regernerasi
), yaitu jika terjadi peristiwa perpindahan
solute
(
absorbat
atau
absorptif
) dari fasa cairan ke fasa gas, maka akan berlaku:
(
)
1 0 11
1
ln
ln
N N NY
X
m
A
A
Y
X
m
N
A
+ +⎡
⎛
−
⎞
⎤
⎢
⎜
⎟ ⋅ −
+
⎥
⎢
⎜
⎜
⎟
⎟
⎥
−
⎢
⎝
⎠
⎥
⎣
⎦
=
⎛ ⎞
⎜ ⎟
⎝ ⎠
bila
A
>
1
(18)
Bila harga
A
=
1
, maka penurunan persamaan (6) seperti di atas menjadi sebagai berikut:
(
0)
1 N N NX
X
N
Y
X
+m
−
=
⎛
−
⎞
⎜
⎟
⎝
⎠
bila
A
=
1
(19)
Keempat persamaan di atas, yaitu persamaan-persamaan (16), (17), (18), dan (19) disebut juga sebagai
Contoh Soal #1
It
is
desired
to
absorb
95%
of
Acetone
(CH
3COCH
3)
by
Water
(H
2O)
from
a
Gas
mixture
of
Acetone
and
Air
containing
1.5%
of
the
component
in
a
counter
‐
current
tray
tower.
Total
Gas
mixture
input
is
30
kmol/hr
and
Water
enters
the
tower
at
a
rate
of
90
kmol/hr.
The
tower
operates
at
27ºC
and
1
atm.
The
equilibrium
relation
is
Y
=
m
·X;
where
m
is
Henry
constant
equal
to
2.53
.
Determine
the
number
of
ideal
stages
necessary
for
the
separation
using
(a)
graphical
method
as
well
as
(b)
Kremser
analysis
method.
Penyelesaian Soal #1
Basis
: 1 jam
sG
=
30 kmol
1 Ny
+=
0,015
0L
=
90 kmol
Jumlah mole
Acetone
(absorbat) masuk ke Absorber = 30 kmol ×
1001 5,= 0.45 kmol
Jumlah mole
udara
(bersih) yang masuk ke Absorber = (30 – 0.45) kmol = 29.55 kmol
Jumlah mole
Acetone
terikut
udara
(95% terabsorpsi) = 0.45 × (1 - 0.95) moles = 0.0225 kmol
s
G
=
29.55 kmol
s
L
=
90 kmol
m
=
H
=
konstanta
Henry
=
2.53
; [
¨
Persamaan Kesetimbangan:
y
=
2 53
.
x
]
Hitung:
10 0225
29 55
0 0225
.
.
.
y
=
=
+
7,6084 x 10
-4Hitung:
10 0225
29 55
.
.
Y
=
=
7,6142 x 10
-4(solute-free basis)
Diketahui:
11 5
0 015
100
kmol Aceton di Gas Masuk
.
.
kmol Udara Masuk
N
y
+=
=
=
Hitung:
11 5
100
1 5
.
0,0152
.
NY
+=
=
−
(solute-free basis)
Gunakan: Persamaan (1) untuk menghitung
x
N,
G Y
s(
N+1−
Y
1)
=
L X
s(
N−
X
0)
29.55
x
(0.015 – 7,6142 x 10
-4) = 90
x
(
X
N- 0)
X
N=
0,0047 = 4,700
x
10
-3Maka, setelah ini kita SIAP untuk penyelesaian dengan Metode Grafis ataupun Persamaan Aljabar
(
Persamaan Kremser
).
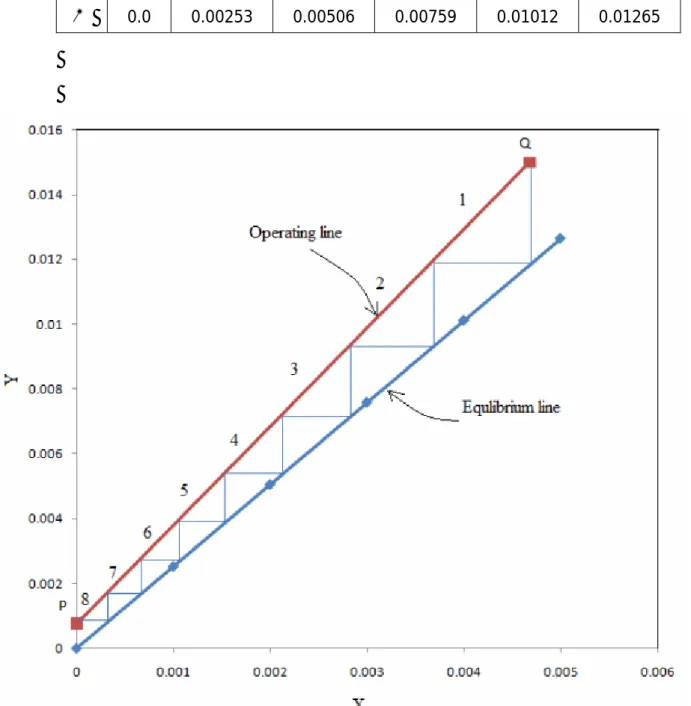
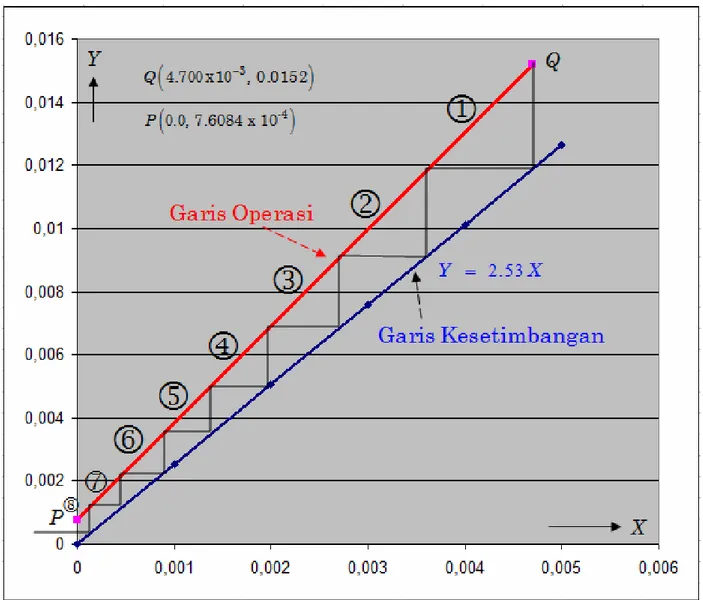
A. Penyelesaian dengan Metode GRAFIK
¨
Buat Kurva Garis Operasi: mulai dari titik
P X Y
(
0,
1)
=
P
(
0 0
. , 7.6084 x 10
-4)
sampai ke titik
Q X
(
N,
Y
N+1)
=
Q
(
4.7 x1
00
0
−3, 0.0152
)
.
¨
Buat Kurva Garis Kesetimbangan:
Y
=
2 53
.
X
X
0.0 0.001 0.002 0.003 0.004 0.005
Y
0.0 0.00253 0.00506 0.00759 0.01012 0.01265
B. Penyelesaian dengan Metode Kremser
¨
Periksa dahulu: harga
90
30 2 53
,
1,1858
s sL
A
G m
=
=
=
⋅
⋅
¨
Karena harga
A
>
1
, maka menurut
Metode (Analisis Kremser)
, dapat digunakan
persamaan untuk Kolom Absorpsi berikut:
( )
(
)
(
) (
)
(
)
1 0 1 01
1
1
2 53
0 0
1
1
1
2 53
0 0
0
ln
ln
0,0152
,
,
ln
1,1858
1,1858
,
,
,
ln 1,1858
ln 19,9627
0,1567
0,8433
ln 1,1858
8, 927
9
NY
m X
Y
m X
A
A
N
A
+ −⎡
⎛
−
⋅
⎞
⋅
⎛
−
⎞
+
⎤
⎢
⎜
−
⋅
⎟ ⎜
⎝
⎟
⎠
⎥
⎢
⎝
⎠
⎥
⎣
⎦
=
⎡
⎛
−
×
⎞
⋅
⎛
−
⎞
+
⎤
⎢
⎜
−
×
⎟ ⎜
⎝
⎟
⎠
⎥
⎢
⎝
⎠
⎥
⎣
⎦
=
⎡
⋅
+
⎤
⎣
⎦
=
=
≈
47 6142 x 10
¨
Maka, tahp ideal yang diperoleh adalah 9.
Catatan
: coba dianalisis, mengapa ada perbedaan hasil penyelesaian antara Metode Grafis dan
Metode Kremser?
Contoh Soal #2
Di bawah ini diberikan tabel data kelarutan gas P (Mr 29) dalam air murni (sebagai
solvent
)
pada suhu 28 ºC dan tekanan udara sebesar 101,3 kPa (1 atm).
P
C
(g P per 100 g H2O)
P
p
(tekanan parsial, kPa)
x
(fraksi mol
P
, cairan)y
(fraksi mol
P
, gas)0,50 0,4650 0,74 0,6850 0,99 0,9150 1,49 1,3750 1,77 1,6280 1,98 1,8210 2,55 2,3410
Dari sistem larutan
P
−
H O
2seperti di atas, maka:
(a).
Hitunglah
x
dan
y
!
(b).
Lakukan plot dari kurva atau diagram kesetimbangan yang terbentuk!
(c).