PENGARUH KONSENTRASI HPMC (Hydroxypropyl Methylcellulose) SEBAGAI GELLING AGENT TERHADAP SIFAT FISIK DAN STABILITAS GEL HAND SANITIZER MINYAK ATSIRI DAUN MINT
(Oleum Mentha piperita L.)
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh:
Albertus Agung Argiyanditya Putra NIM : 108114041
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
PENGARUH KONSENTRASI HPMC (Hydroxypropyl Methylcellulose) SEBAGAI GELLING AGENT TERHADAP SIFAT FISIK DAN STABILITAS GEL HAND SANITIZER MINYAK ATSIRI DAUN MINT
(Oleum Mentha piperita L.)
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh:
Albertus Agung Argiyanditya Putra NIM : 108114041
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
ii
Persetujuan Pembimbing
PENGARUH KONSENTRASI HPMC (Hydroxypropyl Methylcellulose) SEBAGAI GELLING AGENT TERHADAP SIFAT FISIK DAN STABILITAS
GEL HAND SANITIZER MINYAK ATSIRI DAUN MINT (Oleum Mentha piperita L.)
Skripsi yang diajukan oleh: Albertus Agung Argiyanditya Putra
NIM : 108114041
Telah disetujui oleh:
Pembimbing
iii
Pengesahan Skripsi Berjudul
PENGARUH KONSENTRASI HPMC (Hydroxypropyl Methylcellulose) SEBAGAI GELLING AGENT TERHADAP SIFAT FISIK DAN STABILITAS GEL HAND SANITIZER MINYAK ATSIRI DAUN MINT
(Oleum Mentha piperita L.)
Oleh :
Albertus Agung Argiyanditya Putra NIM : 108114041
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi
Universitas Sanata Dharma pada tanggal : 24 Juli 2014
Mengetahui Fakultas Farmasi Universitas Sanata Dharma
Dekan
(………)
Panitia Penguji : Tanda Tangan
iv
HALAMAN PERSEMBAHAN
KARYA INI KU PERSEMBAHKAN UNTUK :
TUHAN YESUS KRISTUS,
BAPAK, IBU, WIWIT DAN KELUARGA,
ODILIA, SAHABAT DAN TEMAN-TEMAN SEPERJUANGAN,
v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan di bawah ini, saya mahasiswa Universitas Sanata Dharma : Nama : Albertus Agung Argiyanditya Putra
NIM : 108114041
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul :
PENGARUH KONSENTRASI HPMC (Hydroxypropyl Methylcellulose)
SEBAGAI GELLING AGENT TERHADAP SIFAT FISIK DAN
STABILITAS SEDIAAN GEL HAND SANITAIZER MINYAK ATSIRI DAUN MINT (Oleum Mentha piperita L.)
beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan kepada Perpustakaan Universitas Sanata Dharma hak untuk menyimpan, mengalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas dan mempublikasikannya di internet atau media lain untuk kepentingan akademis tanpa perlu meminta izin dari saya maupun memberikan royalti kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini saya buat dengan sebenarnya.
Dibuat di Yogyakarta Pada tanggal : 05 Juni 2014
Yang menyatakan
vi
PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang saya tulis ini tidak memuat karya atau bagian karya orang lain, kecuali yang telah disebutkan dalam kutipan dan daftar pustaka, sebagaimana layaknya karya tulis ilmiah.
Apabila di kemudian hari ditemukan indikasi plagiarism dalam naskah ini, maka saya bersedia menanggung segala sanksi sesuai peraturan perundang- undangan yang berlaku.
Yogyakarta, 05 Juni 2014
Penulis,
vii PRAKATA
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Esa atas semua berkat dan penyertaan-Nya sehingga penulis dapat menyelesaikan skripsi yang berjudul “PENGARUH KONSENTRASI HPMC (Hydroxypropyl
Methylcellulose) SEBAGAI GELLING AGENT TERHADAP SIFAT FISIK DAN STABILITAS GEL HAND SANITIZER MINYAK ATSIRI DAUN MINT (Oleum Mentha piperita L.)” sebagai salah satu syarat memperoleh gelar Sarjana Farmasi (S. Farm.) di Fakultas Farmasi, Universitas Sanata Dharma, Yogyakarta.
Penulis menyadari bahwa dalam penyusunan naskah ini, penulis mendapatkan bimbingan dan bantuan dari berbagai pihak. Oleh karena itu, dengan tulus penulis hendak menyampaikan ungkapan terimakasih kepada :
1. Bapak Ipang Djunarko, M.Sc.,Apt. selaku Dekan Fakultas Farmasi Universitas Sanata Dharma.
2. Bapak Septimawanto Dwi P, S.Farm., M.Si., Apt. selaku dosen pembimbing skripsi yang telah memberikan waktu, pengarahan, bimbingan, dukungan serta semangat dan motivasi selama penelitian sampai penyusunan proposal skripsi. 3. Bapak Enade Perdana Istyastono, Ph.D., Apt. dan Ibu Erna Tri Wulandari,
M.Si., Apt. selaku dosen penguji yang telah berkenan memberikan masukan dan pengarahan demi perbaikan skripsi ini.
viii
5. Segenap laboran dan karyawan terutama Mas Agung, Bapak Musrifin, Bapak Mukminin, dan Mas Darto yang telah membantu selama penelitian berlangsung.
6. Bapak dan ibu atas segala doa dan dukungannya selama penulis menyusun skripsi.
7. Teman-teman skripsi senasib dan sepenanggungan Verica Septi Permata Sari dan Stephani Alvia Septiana Putri.
8. Odilia Arum Narwastu yang selalu membantu dan memberikan dukungan selama ini.
9. Teman-teman angkatan 2010 Fakultas Farmasi Universitas Sanata Dharma yang juga memberikan warna selama masa perkuliahan penulis.
10.Semua pihak yang tidak dapat penulis sebutkan satu persatu yang telah memberikan doa, bantuan, dan dukungan selama penelitian skripsi.
Penulis menyadari bahwa penyusunan skripsi ini masih banyak kekurangan mengingat keterbatasan kemampuan serta pengalaman yang dimiliki. Oleh sebab itu, kritik dan saran yang membangun sangat diperlukan oleh penulis untuk menyempurnakan skripsi ini. Semoga skripsi ini dapat bermanfaat bagi perkembangan ilmu pengetahuan.
Yogyakarta, 05 Juni 2014
ix DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
PERNYATAAN PERSETUJUAN PUBLIKASI ... v
PERNYATAAN KEASLIAN KARYA ... vi
x
A. Jenis dan Rancangan Penelitian ... 20
B. Variabel Penelitian dan Definisi Operasional ... 20
1. Variabel Penelitian ... 20
2. Definisi Operasional ... 21
C. Alat Penelitian ... 23
xi
E. Tata Cara Penelitian ... 23
1. Verifikasi minyak atsiri daun mint ... 23
a. Identifikasi bahan ... 24
b. Verifikasi indeks bias minyak atsiri daun mint ... 24
c. Verifikasi bobot jenis minyak atsiri daun mint ... 24
2. Formula ... 25
3. Proses sterilisasi ... 26
4. Pembuatan gel hand sanitizer minyak atsiri daun mint ... 26
5. Uji organoleptis dan pH gel hand sanitizer minyak atsiri daun mint ... 26
6. Uji sifat fisik dan stabilitas gel hand sanitizer minyak atsiri daun mint ... 27
a. Uji viskositas dan pergeseran viskositas ... 27
b. Uji daya sebar ... 27
7. Uji daya antibakteri gel hand sanitizer minyak atsiri daun mint secara difusi sumuran ... 27
a. Pembuatan suspensi bakteri uji Escherichia coli ... 27
b. Pengujian aktivitas antibakteri bakteri Escherichia coli dengan metode difusi sumuran ... 28
F. Analisis Hasil ... 28
BAB IV. HASIL DAN PEMBAHASAN ... 30
A. Verifikasi minyak atsiri daun mint ... 30
B. Formulasi sediaan gel hand sanitizer ... 31
C. Uji organoleptis dan pH ... 35
xii
1. Uji viskositas ... 36
2. Uji daya sebar ... 39
3. Uji pergeseran viskositas ... 40
E. Data Statistik ... 41
1.Uji normaitas data ... 41
2. Uji kesamaan varians ... 42
3. Uji TukeyHSD ... 43
F. Uji potensi antimikroba ... 45
BAB V. KESIMPULAN DAN SARAN ... 49
A. Kesimpulan... 49
B. Saran ... 49
DAFTAR PUSTAKA ... 50
LAMPIRAN ... 53
xiii
DAFTAR TABEL
Halaman
Tabel I. Klasifikasi gel ... 15
Tabel II. Formula gel hand sanitizer ekstrak daun sirih acuan ... 25
Tabel III. Formula gel hand sanitizer minyak atsiri daun mint yang telah dimodifikasi (200 g) ... 25
Tabel IV. Verifikasi minyak atsiri daun mint ... 30
Tabel V. Hasil uji organoleptis dan pH 48 jam ... 35
Tabel VI. Hasil uji organoleptis 1 bulan... 35
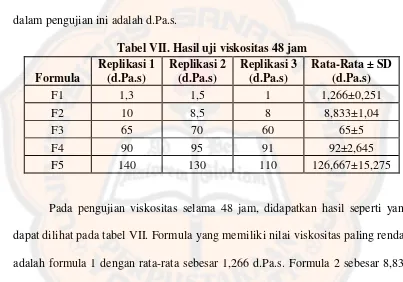
Tabel VII. Hasil uji viskositas 48 jam ... 37
Tabel VIII. Hasil uji daya sebar 48 jam ... 39
Tabel IX. Hasil perhitungan pergeseran viskositas ... 40
Tabel X. Hasil uji normalitas Shapiro-Wilk ... 42
Tabel XI. Hasil uji kesamaan varians ... 42
Tabel XII. Hasil uji TukeyHSD viskositas 48 jam ... 43
Tabel XII. Hasil uji TukeyHSD daya sebar 48 jam ... 44
xiv
DAFTAR GAMBAR
Halaman
Gambar 1. Struktur kandungan minyak atsiri daun mint ... 8
Gambar 2. Struktur Kulit ... 9
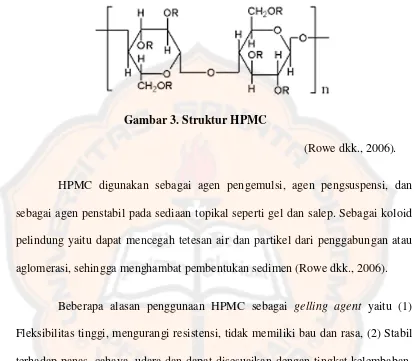
Gambar 3. Struktur HPMC ... 17
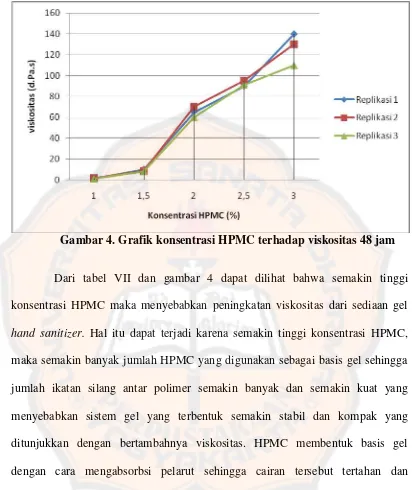
Gambar 4. Grafik konsentrasi HPMC terhadap viskositas 48 jam ... 38
Gambar 5. Grafik konsentrasi HPMC terhadap daya sebar 48 jam ... 39
xv
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Certificate of Analysis (CoA) minyak atsiri daun mint ... 53
Lampiran 2. Certificate of Analysis (CoA) HPMC ... 54
Lampiran 3. Verifikasi minyak atsiri daun mint ... 55
Lampiran 4. Hasil uji sifat fisik dan stabilitas gel ... 57
Lampiran 5. Hasil pengolahan data dengan Software R 3.1.0 ... 58
Lampiran 6. Dokumentasi sediaan gel minyak atsiri daun mint ... 63
xvi INTISARI
Minyak atsiri daun mint (Oleum Mentha piperita L.) diyakini memiliki khasiat sebagai antimikroba. Senyawa minyak atsiri daun mint yang dipercaya memiliki aktivitas tersebut adalah menthol. Minyak atsiri daun mint diyakini dapat diformulasikan ke dalam bentuk sediaan topikal yaitu gel. Sifat fisik dan stabilitas sediaan gel dapat dipengaruhi oleh konsentrasi gelling agent. Penelitian ini bertujuan untuk mengetahui pengaruh konsentrasi gelling agent dalam gel minyak atsiri daun mint terhadap sifat fisik dan stabilitasnya.
Penelitian ini merupakan eksperimental murni dengan menentukan 5 konsentrasi HPMC (Hydroxypropyl Methylcellulose) yaitu formula 1 (1%), formula 2 (1,5%), formula 3 (2%), formula 4 (2,5%), formula 5 (3%). Uji yang dilakukan untuk tiap formula adalah uji sifat fisik yang meliputi uji viskositas dan daya sebar, serta uji stabilitas yang meliputi uji pergeseran viskositas. Analisis data menggunakan R 3.1.0.
Hasil dari penelitian menunjukkan bahwa HPMC berpengaruh terhadap sifat fisik dan stabilitas gel hand sanitizer minyak atsiri daun mint. Formula 4 dan 5 memenuhi kriteria sifat fisik sediaan gel hand sanitizer yang ditentukan dengan nilai viskositas dan daya sebar masing-masing sebesar 92 ± 2,645 d.Pa.s dan 6,208 ± 0,08 (formula 4) dan 126,667 ± 15,275 d.Pa.s dan 5,881 ± 0,112 cm (formula 5). Sedangkan yang memenuhi kriteria stabilitas sediaan gel hand sanitizer hanya formula 5 dengan nilai pergeseran viskositas 8,4%.
xvii ABSTRACT
Peppermint oil (Oleum Mentha piperita L.) is known to have an antimicrobial effect. The substance from peppermint oil that responsible for that effect is menthol. Peppermint oil can be made available in a topical solution such as gel. Physical properties and stability of gel can be affected by it’s gelling agents. This research aimed to know the effect of gelling agent’s concentration in the peppermint oil gel by physical properties and stability.
The research is categorized as purely experimental by using 5 concetrations of HPMC (Hydroxypropyl Methylcellulose). The consentrations are HPMC 1%(formula 1), HPMC 1,5%(formula 2), HPMC 2%(formula 3), HPMC 2,5%(formula 4), HPMC 3%(formula 5). Observed physical properties were focused on viscosity, spreadability and stability of gel, which was viscosity shift between the viscosity of 48 hours and after 1 month of storage. The data were analyzed by using R 3.1.0.
The result showed that HPMC can be affected in physical properties and stability gel hand sanitizer. Formula 4 and 5 had good physical properties of gel hand sanitizer. The viscosity and spreadability values of each formula were 92 ± 2,645 d.Pa.s and 6,208 ± 0,08 cm (formula 4) and 126,667 ± 15,275 d.Pa.s and 5,881 ± 0,112 cm (formula 5). Only formula 5 had a good stability showed by viscosity shift value 8,4%.
1
BAB I PENGANTAR
A. Latar Belakang
Diare adalah suatu penyakit dimana tinja atau feses berubah menjadi cair atau lembek yang terjadi lebih dari 3 kali sehari. Menurut data yang dirilis UNICEF pada bulan September 2012, angka kematian pada anak balita di bawah usia 5 tahun di dunia mencapai 2.000 anak setiap hari karena diare (UNICEF, 2012). Dari jumlah tersebut, sekitar 1.800 anak yang meninggal karena diare disebabkan karena kurangnya air bersih, sanitasi dan kebersihan dasar. Di Indonesia sendiri, kematian pada anak balita mencapai angka 130.000 setiap tahunnya dan seperempatnya disebabkan oleh diare. Penyebab munculnya penyakit diare adalah kurangnya kesadaran masyarakat dalam menjaga kebersihan salah satunya adalah kebiasaan mencuci tangan (UNICEF, 2012).
Dewasa ini masyarakat cenderung menyukai produk-produk yang serba praktis dan instan. Begitu pula dalam dunia kesehatan yang juga mulai memberikan produk-produk yang praktis dan instan bagi penggunanya, salah satunya adalah gel pembersih tangan (hand sanitizer). Gel pembersih tangan jauh lebih praktis dan baik daripada mencuci tangan menggunakan sabun. Hal tersebut dikarenakan sabun sangat tidak aman apabila digunakan secara bersama-sama dan bergantian. Sebab ada kemungkinan bahwa pengguna sebelumnya membawa mikroorganisme yang berbahaya dan menempel pada sabun. Selain itu, air yang biasanya digunakan untuk membilas juga kadang susah dan tidak bisa dipastikan bahwa air tersebut bersih dan sesuai keinginan.
Sediaan hand sanitizer merupakan sediaan gel yang mempunyai kemampuan antibakteri dalam menghambat hingga membunuh bakteri (Retnosari dan Isadiartuti, 2006). Sediaan hand sanitizer yang dijual di pasaran banyak yang menggunakan alkohol sebagai antiseptik untuk membunuh kuman. Akan tetapi penggunaan alkohol pada kulit dirasa kurang aman karena alkohol adalah pelarut organik yang dapat melarutkan sebum pada kulit, dimana sebum tersebut bertugas melindungi kulit dari mikroorganisme (Retnosari dan Isadiartuti, 2006). Selain itu alkohol memiliki sifat mudah terbakar dan dapat menyebabkan iritasi dan kekeringan pada kulit (Block, 2001).
aktivitas sebagai antimikroba terhadap Staphylococcus aureus, Staphylococcus epidermidis, Bacillus subtilis, Bacillus cereus, Bacillus sp., Listeria monocytogenes, Micrococcus luteus, Escherichia coli, Klebsiella sp. dan Pseudomonas aeruginosa (Gupta dkk., 2008). Minyak atsiri daun mint memiliki aktivitas sebagai antimikroba dengan nilai KHM dan KBM sebesar 0,12 % v/v terhadap bakteri Escherichia coli (Hammer dkk., 1999).
Permasalahan formulasi yang muncul dari sediaan yang menggunakan bahan aktif berbasis minyak atau tidak larut air adalah akan muncul rasa lengket dan tidak nyaman pada tangan ketika diaplikasikan. Oleh karena itu formulasi hand sanitizer menggunakan minyak atsiri daun mint (Oleum Mentha piperita L.) dibuat menjadi sediaan gel yang berbasis air. Sediaan gel adalah sediaan semisolid yang terdispersi dari molekul kecil atau besar dalam suatu cairan yang terdapat gelling agent (Allen, 2005). Gelling agent merupakan bahan yang bertanggung jawab membentuk basis gel dan menjaga stabilitas gel dengan mempengaruhi kekentalan gel. Salah satu gelling agent yang digunakan dalam formulasi sediaan topikal adalah HPMC (Hydroxypropyl Methylcellulose). Keuntungan dari penggunaan HPMC sebagai gelling agent adalah dapat membentuk basis gel yang jernih dan netral serta stabil dalam penyimpanan jangka panjang (Rowe dkk., 2009). HPMC juga mengembang terbatas dalam air sehingga cocok dalam membentuk basis hidrogel yang baik (Arikumalasari dkk., 2013).
menjadi alternatif pemakaian hand sanitizer yang lebih aman. Selain itu penggunaan HPMC sebagai gelling agent juga menarik untuk diteliti pengaruhnya terhadap sifat fisik dan stabilitas sediaan gel hand sanitizer serta perlu dilakukan uji potensi antimikroba untuk melihat seberapa besar aktivitas sediaan gel hand sanitizer tersebut membunuh atau menghambat mikroba.
1. Perumusan Masalah
Berdasarkan latar belakang yang telah dipaparkan di atas, maka dimunculkan masalah sebagai berikut :
a. Apakah ada pengaruh konsentrasi HPMC pada rentang konsentrasi yang ditentukan sebagai gelling agent terhadap sifat fisik (viskositas dan daya sebar) dan stabilitas (pergeseran viskositas) sediaan gel hand sanitizer minyak atsiri daun mint ?
b. Formula manakah yang memenuhi syarat kriteria sifat fisik (viskositas sebesar 80-150 d.Pa.s. dan daya sebar sebesar 5-7 cm) dan stabilitas (nilai pergeseran viskositas ≤ 10%) ?
2. Keaslian Penelitian
Nadhiksor dkk. (2013) melakukan penelitian tentang “Formulation
and Evaluation of Herbal Sanitizer”. Dalam penelitian tersebut menggunakan
ekstrak daun kemangi dan eucalyptus sebagai senyawa yang diharapkan memiliki aktivitas antimikroba. Hasil dalam penelitian tersebut adalah formula herbal sanitizer yang dibuat dapat memberikan efek antimikroba terhadap berbagai macam mikroorganisme yaitu E. coli, Ps. aeruginosa, B. subtilis, S. aureus, C. albicans, S. cerevisiae.
Menurut Hammer dkk. (1999) yang melakukan penelitian tentang aktivitas antimikroba dari minyak atsiri dan berbagai ekstrak tanaman menyatakan bahwa nilai KHM dan KBM dari tanaman mint adalah sebesar 0,12 % v/v terhadap bakteri Escherichia coli.
Sejauh pengetahuan dan penelusuran beberapa pustaka yang telah dilakukan oleh penulis, penelitian tentang pengaruh konsentrasi HPMC (Hydroxypropyl Methylcellulose) sebagai gelling agent terhadap sifat fisis dan stabilitas gel hand sanitizer minyak atsiri daun mint (Oleum Mentha piperita L.) belum pernah dilakukan.
3. Manfaat Penelitian a. Manfaat Teoretis
b. Manfaat Praktis
Menghasilkan formulasi sediaan gel hand sanitizer minyak atsiri daun mint dengan sifat fisik dan stabilitas yang baik sehingga bermanfaat bagi masyarakat.
B. Tujuan Penelitian 1. Tujuan Umum
Menghasilkan gel hand sanitizer minyak atsiri daun mint dengan sifat fisik (viskositas dan daya sebar) dan stabilitas (pergeseran viskositas) yang memenuhi kriteria.
2. Tujuan Khusus
a. Mengetahui pengaruh konsentrasi HPMC sebagai gelling agent terhadap sifat fisik (viskositas dan daya sebar) dan stabilitas (pergeseran viskositas) sediaan gel hand sanitizer minyak atsiri daun mint.
7
BAB II
PENELAAHAN PUSTAKA
A. Tanaman Mint 1. Sistematika
Sistematika tanaman Mentha piperita L. adalah sebagai berikut: Kingdom : Plantae
Divisi : Spermatophyta Subdivisi : Angiospermae Kelas : Dicotyledonae Ordo : Lamiaceae Famili : Lamiales Genus : Mentha
Jenis : Mentha piperita L.
(Corteau dkk., 2005) 2. Uraian tanaman
majemuk semu. Karangan bunga ini tumbuh pada ujung batang atau cabang (bunga terminal).
3. Kandungan kimia
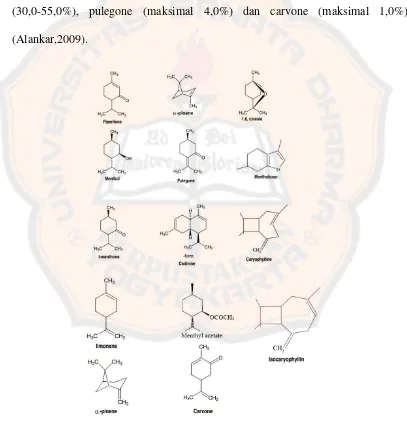
Kandungan kimia dalam tanaman mint adalah limonene (1,0-5,0%), cineole (3,4-14,0%), menthone (14-32%), menthofuran (1,0-9,0%), isomenthone (1,5-10,0%), menthyl acetate (2,8-10%), isopulegol (maksimal 0,2%), menthol (30,0-55,0%), pulegone (maksimal 4,0%) dan carvone (maksimal 1,0%) (Alankar,2009).
Gambar 1. Struktur kandungan minyak atsiri daun mint
4. Manfaat
Minyak atsiri daun mint memiliki efek terapi seperti stimulant diffusible kuat, antisplasmodik dan antimuntah. Oleh karena itu, minyak atsiri daun mint biasa digunakan untuk meredakan perut kembung, gastrodynia, mual, kejang perut, dan untuk menutupi rasa obat lain. Selain itu, pada tanaman mint mengandung golongan senyawa monoterpen dan telah diteliti dan diketahui memiliki aktivitas antibakteri dan insektisida (Oyedeji dan Afolayan, 2006; Pavela, 2005).
B. Kulit
Kulit merupakan suatu organ besar yang berlapis-lapis, menutupi
permukaan lebih dari 20.000 cm2 yang mempunyai bermacam-macam fungsi dan kegunaan. Merupakan jaringan pelindung yang lentur dan elastis, melindungi seluruh permukaan tubuh dan mempunyai berat 5% dari total berat badan. Secara anatomi, kulit terdiri dari banyak lapisan jaringan, tetapi pada umumnya kulit dibagi dalam tiga lapisan jaringan yaitu: epidermis, dermis dan hipodermis (Lachman dkk., 1994).
Gambar 2. Struktur kulit
Epidermis merupakan bagian terluar yang dibentuk oleh epitelium dan terdiri dari sejumlah lapisan sel yang disusun atas dua lapisan yang jelas tampak, yaitu selapis lapisan tanduk dan selapis zona germinalis. Pada epidermis tidak ditemukan pembuluh darah, sehingga nutrisi diperoleh dari transudasi cairan pada dermis karena banyaknya jaringan kapiler pada papila (Lachman dkk., 1994; Junqueira dan Kelley, 1997).
Dermis atau korium tersusun atas jaringan fibrus dan jaringan ikat yang elastik.Pada permukaan dermis tersusun papila-papila kecil yang berisi pembuluh darah kapiler. Tebal lapisan dermis kira-kira 0,3-1,0 mm. Dermis merupakan jaringan penyangga berserat yang berperan sebagai pemberi nutrisi pada epidermis (Lachman dkk., 1994; Junqueira dan Kelley, 1997).
Hipodermis bukan merupakan bagian dari kulit, tetapi batasnya tidak jelas. Kedalaman dari hipodermis akan mengatur kerutan-kerutan dari kulit (Lachman dkk., 1994; Junqueira dan Kelley, 1997).
Bakteri yang banyak ditemukan disekitar manusia, misal tangan manusia karena banyak berinteraksi dengan dunia luar. Terdapat berbagai jenis bakteri yang ada ditangan manusia. Adapun bakteri yang umum ditemukan pada tangan diantaranya adalah Staphylococcus aureus, E. coli, Salmonella, Vibrio cholerae, dan Shigella (BSN Medical, 2009). Beberapa jenis mikroorganisme yang dapat menyebabkan diare adalah Escherichia coli, Clostridium difficile, Campylobacter, Salmonella dan Shigella.
C. Minyak Atsiri
Minyak atsiri adalah salah satu jenis minyak nabati yang multi manfaat. Bahan baku minyak atsiri diperoleh dari berbagai bagian tanaman seperti daun, bunga, buah, biji, kulit biji, batang, akar atau rimpang. Salah satu ciri utama minyak atsiri yaitu mudah menguap dan beraroma khas. Pada umumnya minyak atsiri larut dalam etanol dan pelarut organik polar lain dan kelarutannya akan menurun jika kadar etanol kurang dari 70 %. Bila minyak atsiri mengandung fraksi terpen (senyawa non polar) dalam jumlah besar maka kelarutannya dalam etanol relatif kecil.
D. Bakteri Escherichia coli
Escherichia coli termasuk dalam famili Enterobaktericeae, yaitu kelompok batang gram negatif yang besar dan heterogen. Ciri-ciri dari E.coli adalah mempunyai flagel, berukuran 0,4-0,7 µm x 1,4 µm, dan mempunyai simpai (Radji dan Biomed, 2009). E. coli merupakan flora normal dengan habitat alami di saluran cerna manusia (Brooks, Butel, Morse, 2004).
Bakteri ini merupakan penyebab infeksi saluran kemih dan penyakit diare, terutama pada anak-anak (Gupte, 2006). Virulensi E. coli disebabkan karena E. coli memiliki 2 jenis fimbria, yaitu pili dan manosa resisten yang berfungsi sebagai faktor kolonisasi yang melekatkan sel bakteri ke sel hospes. Selain itu, E. coli menghasilkan enterotoksin yang akan meningkatkan permeabilitas sel epitel usus dengan merangsang enzim adenilat siklase, sehingga cairan di dalam usus terakumulasi dan terjadi diare (Radji dan Biomed, 2009).
Klasifikasi E. Coli berdasarkan ciri khas virulensinya menyebabkan diare, yaitu:
2. Enterotoxigenic E. coli (ETEC), yaitu penyebab “traveler’s diarrhea”. Kolonisasi ETEC yang spesifik untuk manusia menimbulkan pelekatan ETEC pada sel epitel usus kecil. Beberapa strain ETEC menghasilkan eksotoksin yang labil terhadap panas yang secara genetik dikontrol oleh plasmid. Subunit B melekat pada ganglioside GM1 pada bagian brush border di sel epitel usus kecil yang menyebabkan masuknya subunit A ke dalam sel dan mengaktivasi adenilin siklase sehingga meningkatkan konsentrasi adenosine monofosfat (cAMP) dan menimbulkan hipersekresi air dan klorida yang terus menerus dan lama. Hal tersebutlah yang kemudian menyebabkan diare.
3. Enterohemorrhagic E. coli (EHEC), memproduksi verotoksin yang memberikan efek sititoksik pada sel Vero. Verotoksin mempunyai kesamaan dengan Shiga toksin yang diproduksi oleh Shigella dysenteriae tipe 1. EHEC berhubungan dengan hemorrhagic colitis, diare, penyakit yang mengakibatkan penyakit ginjal, microangiopathic, hemolitik anemia, dan trombositopenia.
4. Enteroinvasive E. coli (EIEC), yaitu penyebab penyakit yang sangat mirip dengan shigellosis yang menyerang anak-anak di negara berkembang dan wisatawan yang mengunjungi negara tersebut. EIEC menimbulkan penyakit dengan menginvasi sel epitel mukosa usus (Brooks dkk., 2004).
E. Hand Sanitizer
Gel pembersih tangan merupakan gel yang memiliki kemampuan sebagai antibakteri dalam menghambat hingga membunuh bakteri (Retnosari dan Isadiartuti, 2006). Banyak dari gel ini berasal dari bahan beralkohol atau etanol yang dicampurkan bersama dengan bahan pengental, misal karbomer, gliserin, dan menjadikannya serupa jelly, gel, atau busa untuk memudahkan penggunaan dan menghindari perasaan kering karena penggunaan alkohol.
Sanitizer adalah suatu bahan yang dapat mengurangi mikroba kontaminan sampai 99,9% yang sedang tumbuh. Efektivitas sanitizer terutama sanitizer kimia dipengaruhi oleh faktor fisik kimia seperti waktu kontak, suhu, konsentrasi, pH, kebersihan peralatan, kesadahan air, dan serangan bakteri (Marriot, 1999).
F. Gel 1. Definisi dan klasifikasi gel
Tabel I. Klasifikasi gel
Klasifikasi Contoh
Organogel
1. Tipe hidrokarbon Petrolatum, gel minyak mineral-polietilen
2. Lemak hewani dan nabati
Lard, minyak nabati
terhidrogenasi, minyak teobroma 3. Lemak basis sabun Alumunium stearat, gel minyak
mineral
4. Organogel hidrofolik Basis carbowax, salep polietilen glikol
Hidrogel
1. Hidrogel organik Pasta pectin, jelly tragakan
2. Hidrogel anorganik Gel bentonit, gel koloid magnesium
(Martin, 1993) 2. Sifat fisik dan stabilitas gel
Sifat fisik suatu sediaan gel dapat dilihat dari besarnya viskositas dan daya sebarnya. Viskositas merupakan suatu tahanan dari suatu sediaan untuk mengalir. Semakin kental atau semakin besar nilai viskositasnya, maka semakin besar tahanannya (Sinko, 2006). Pengujian viskositas dapat dilakukan dengan menggunakan berbagai jenis viskometer sesuai kebutuhan (Garg dkk., 2002). Sedangkan daya sebar merupakan karakteristik penting dalam formulasi yang menjamin kemudahan saat sediaan diaplikasikan di kulit. Besarnya nilai daya sebar suatu sediaan dipengaruhi oleh karakteristik sediaan, lama tekanan dan kekuatan yang menghasilkan kelengketan. Daya sebar suatu sediaan biasanya berbanding terbalik dengan nilai viskositas. Semakin tinggi nilai viskositasnya, maka nilai daya sebar akan semakin rendah (Garg dkk., 2002).
sederhana, dan tidak memerlukan banyak biaya. Tetapi, metode ini kurang sensitif karena data yang didapat harus dihitung secara manual. Nilai daya sebar yang baik untuk sediaan gel adala sebesar 5-7 cm (Garg dkk., 2002).
Tujuan pemeriksaan stabilitas sediaan adalah untuk menjamin bahwa sediaan yang dihasilkan memenuhi persyaratan yang telah ditentuan walaupun sudah cukup lama dalam penyimpanan. Pemeriksaan stabilitas dapat digunakan sebagai dasar penentuan batas kadaluarsa (Lachman, 1994). Pengukuran stabilitas yang dilakukan salah satunya adalah dengan menghitung nilai pergeseran viskositas. Nilai pergeseran viskositas dihitung dari selisih nilai viskositas 48 jam dan 1 bulan, dibagi viskositas 48 jam dikalikan 100%. Sediaan dianggap memiliki stabilitas yang baik jika memiliki persentase pergeseran viskositas ≤ 10%.
G. HPMC
Bahan pembentuk gel (gelling agent) adalah bahan tambahan yang digunakan untuk mengentalkan dan menstabilkan sediaan. Beberapa bahan penstabil dan juga bahan pengental yang termasuk dalam gelling agent antara lain xanthan gum, carbopol, HPMC dan berbagai material lain turunan sellulosa (Tambunan, 2008).
secara luas banyak digunakan dalam aplikasi produk kosmetik dan aplikasi lainnya.
Gambar 3. Struktur HPMC
(Rowe dkk., 2006).
HPMC digunakan sebagai agen pengemulsi, agen pengsuspensi, dan sebagai agen penstabil pada sediaan topikal seperti gel dan salep. Sebagai koloid pelindung yaitu dapat mencegah tetesan air dan partikel dari penggabungan atau aglomerasi, sehingga menghambat pembentukan sedimen (Rowe dkk., 2006).
H. Landasan Teori
Kandungan kimia utama pada tanaman mint adalah minyak atsiri yang mudah menguap dimana kandungannya adalah limonene (1,0-5,0%), cineole (3,4-14,0%), menthone (14-32%), menthofuran (1,0-9,0%), isomenthone (1,5-10,0%), menthyl acetate (2,8-10%), isopulegol (maksimal 0,2%), menthol (30,0-55,0%), pulegone (maksimal 4,0%) dan carvone (maksimal 1,0%) (Alankar, 2009). Tanaman mint mengandung golongan senyawa monoterpen yang telah diteliti dan diketahui memiliki aktivitas antibakteri dan insektisida (Oyedeji dan Afolayan, 2006; Pavela, 2005).
Gel pembersih tangan merupakan gel yang memiliki kemampuan sebagai antibakteri dalam menghambat hingga membunuh bakteri (Retnosari dan Isadiartuti, 2006). Gel merupakan sistem semisolid yang terdiri dari dispersi molekul-molekul kecil atau besar di dalam pembawa cairan berair yang membentuk seperti jeli penambahan gelling agent. Di antara gelling agent yang digunakan berupa makromolekul sintetik, seperti carbomer 934, derivat selulosa (karboksimetilselulosa atau hidroksipropil metilselulosa), dan natural gum (tragacanth) (Allen, 2005).
Beberapa alasan penggunaan HPMC sebagai gelling agent yaitu (1) Fleksibilitas tinggi, mengurangi resistensi, tidak memiliki bau dan rasa, (2) Stabil terhadap panas, cahaya, udara dan dapat disesuaikan dengan tingkat kelembaban, (3) Mempunyai kemampuan untuk mencampurkan zat warna atau zat aditif lainnya ke dalam lapisan tipis tanpa kesukaran (Lachman dkk., 1994). Dibanding dengan turunan metilselulosa lainnya, HPMC meghasilkan cairan gel yang lebih jernih dan lebih stabil terhadap pH.
I. Hipotesis
1. Konsentrasi HPMC sebagai gelling agent memiliki pengaruh terhadap sifat fisik (viskositas dan daya sebar) dan stabilitas (pergeseran viskositas) sediaan gel hand sanitizer minyak atsiri daun mint.
20 BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini termasuk jenis penelitian eksperimental murni rancangan acak lengkap pola searah.
B. Variabel Penelitian dan Definisi Operasional 1. Variabel Penelitian
a. Variabel bebas
Variabel bebas dalam penelitian ini adalah konsetrasi HPMC sebagai gelling agent dalam basis sediaan gel hand sanitizer
b. Variabel tergantung
Variabel tergantung dalam penelitian ini adalah sifat fisik (daya sebar dan viskositas) dan stabilitas (pergeseran viskositas) gel hand sanitizer, zona hambat.
c. Variabel pengacau terkendali
d. Variabel pengacau tak terkendali
Variabel pengacau tak terkendali dalam penelitian ini adalah kondisi penyimpanan (suhu dan kelembaban ruangan) dan laju penguapan minyak atsiri daun mint.
2. Definisi Operasional
a. Gel hand sanitizer ekstrak minyak atsiri daun mint merupakan sediaan semisolid yang memiliki efek antimikroba yang bertujuan untuk melindungi dari infeksi bakteri yang dibuat dari ekstrak minyak atsiri daun mint dengan HPMC sebagai gelling agent yang dibuat sesuai dengan formula dan prosedur yang telah ditentukan pada pembuatan gel dalam penelitian ini.
b. Gelling agent adalah bahan yang digunakan untuk membentuk kekentalan atau pembentuk sifat alir sediaan gel hand sanitizer. Gelling agent yang digunakan dalam penelitian ini adalah HPMC.
c. Formula 1 adalah formula sediaan gel hand sanitizer minyak daun mint dengan konsentrasi HPMC sebesar 1 %.
d. Formula 2 adalah formula sediaan gel hand sanitizer minyak daun mint dengan konsentrasi HPMC sebesar 1,5 %.
e. Formula 3 adalah formula sediaan gel hand sanitizer minyak daun mint dengan konsentrasi HPMC sebesar 2 %.
g. Formula 5 adalah formula sediaan gel hand sanitizer minyak daun mint dengan konsentrasi HPMC sebesar 3 %.
h. Sifat fisik gel hand sanitizer minyak atsiri daun mint merupakan parameter yang digunakan untuk mengetahui kualitas fisik dari sediaan gel hand sanitizer minyak atsiri daun mint. Dalam penelitian ini adalah organoleptis, viskositas, dan daya sebar.
i. Viskositas adalah suatu ketahanan gel hand sanitizer minyak atsiri daun mint untuk mengalir setelah di berikan gaya. Semakin kecil viskositas, maka gel hand sanitizer minyak atsiri daun mint akan semakin mudah untuk mengalir.
j. Daya sebar adalah diameter penyebaran tiap 1 gram gel hand sanitizer minyak atsiri daun mint pada alat uji daya sebar yang di beri beban 125 gram dan didiamkan selama 1 menit.
k. Stabilitas gel adalah besarnya nilai pergeseran viskositas sebelum dan sesudah penyimpanan selama 1 bulan.
l. Pergeseran viskositas merupakan presentase selisih dari viskositas gel hand sanitizer minyak atsiri daun mint setelah 1 bulan penyimpanan dengan viskositas gel hand sanitizer minyak atsiri daun mint setelah 48 jam pembuatan.
n. Zona hambat merupakan zona jernih yang dihasilkan dimana tidak ada pertumbuhan bakteri Escherichia coli atau terdapat pertumbuhan sedikit sekali dibandingkan dengan kontrol pertumbuhan.
C. Alat Penelitian
Alat-alat yang digunakan dalam penelitian ini adalah Glassware (Pyrex- Japan), neraca analitik (Mettler Toledo GB 3002), Mixer (Philips Type HR 1170 120V-130W Made In Holland), Viscotester seri VT 04 (Rion-Japan), Stopwatch, alat pengukur daya sebar, piknometer, vortex, refractometer, pipet mikro 5-100 µL, autoklaf, jarum ose, cawan petri, dan inkubator, dan alat-alat gelas lainnya.
D. Bahan Penelitian
Bahan-bahan yang digunakan dalam penelitian ini adalah Minyak atsiri daun mint (PT. Brataco), HPMC (Honest), Gliserin (PT. Bartaco), Natrium Metabisulfit (Merck), Muller Hinton Agar (MHA) (Merck), Muller Hinton Broth (MHB) (Merck), bakteri uji Escherichia coli, etanol 70%, gel hand sanitizer merek Nuvo, dan aquadest.
E. Tata Cara Penelitian
1. Verifikasi minyak atsiri daun mint
a. Identifikasi bahan
Minyak atsiri daun mint yang telah diuji identitasnya, dibuktikan dengan Certificate of Analysis.
b. Verifikasi indeks bias minyak atsiri daun mint
Indeks bias dari minyak atsiri daun mint diukur dengan menggunakan refraktometer. Minyak atsiri daun mint diteteskan pada prisma utama, kemudian prisma ditutup dan ujung refraktometer diarahkan ke cahaya terang, sehingga cahaya terang akan melalui lensa skala sehingga dapat dilihat dengan jelas dan ditentukan nilai indeks biasnya. Refraktometer dialiri air mengalir dan diatur suhunya menjadi 20ºC. Nilai indeks bias minyak atsiri daun mint ditunjukkan oleh garis batas yang memisahkan sisi terang dan sisi gelap pada bagian atas dan bagian bawah. Dilakukan replikasi sebanyak 3 kali (Depkes RI, 1995).
c. Verifikasi bobot jenis minyak atsiri daun mint
2. Formula
Formula gel hand sanitizer yang digunakan dalam penelitian ini adalah formula modifikasi dari penelitian Retnosari dan Isadiartuti (2006).
Tabel II. Formula gel hand sanitizer ekstrak daun sirih acuan (200 g)
Bahan Formula
Ekstrak daun sirih 15%
Carbopol 940 0,5%
TEA 0,5%
Gliserin 1%
Koringen Odoris (melon) 8 gtt Natrium Metabisulfit 0,02 %
Aquadest ad 200 g
(Retnosari dan Isadiartuti, 2006)
Tabel III. Formula gel hand sanitizer minyak atsiri daun mint yang telah dimodifikasi (200 g)
Bahan F1 F2 F3 F4 F5
Minyak atsiri daun mint 0,5 % 0,5 % 0,5 % 0,5 % 0,5 %
HPMC 1% 1,5% 2% 2,5% 3%
Gliserin 1% 1% 1% 1% 1%
Natrium Metabisulfit 0,02 % 0,02 % 0,02 % 0,02 % 0,02 %
3. Proses sterilisasi
Pengembangan HPMC dan proses pencampuran dilakukan di laboratorium steril dalam MSC (Microbiologycal Safety Cabinet) yang telah disterilisasi dengan sinar UV selama 3 jam dan dilakukan secara aseptis. Seluruh alat gelas dan logam di sterilisasi menggunakan autoklaf selama 20 menit dengan suhu 121oC. Alat-alat lain yang tidak tahan panas, disterilisasi dengan sinar UV selama 3 jam dan etanol 70% sebelum digunakan.
4. Pembuatan gel hand sanitizer minyak atsiri daun mint
Aquadest sebanyak 20 kali jumlah HPMC dipanaskan sampai suhu 80o C-90oC, kemudian HPMC ditaburkan sampai terbasahi dan terdispersi ke dalamnya. Kemudian setelah terjadi pengembangan (kurang lebih satu hari), aquadest sisa dicampur bahan-bahan lain yang larut air. Setelah itu, gel HPMC dicampur dengan minyak atsiri daun mint kemudian dicampur dengan bahan yang larut air tadi, kemudian dicampur menggunakan mixer dengan kecepatan putar tingkat 1 selama 10 menit pada suhu ruangan (Arikumalasari dkk., 2013).
5. Uji organoleptis dan pH gel hand sanitizer minyak atsiri daun mint
6. Uji sifat fisik dan stabilitas gel hand sanitizer minyak atsiri daun mint a. Uji viskositas dan pergeseran viskositas
Pengukuran viskositas menggunakan alat Viscometer Rion seri VT 04. Gel dimasukkan ke dalam wadah hingga penuh dan dipasang pada portable viskotester. Viskositas gel diketahui dengan mengamati jarum penunjuk viskositas (Instruction Manual Viscotester VT-04E). Untuk mengetahui persentase pergeseran viskositasnya dilakukan pengukuran pada 48 jam dan 1 bulan selama penyimpanan. Besarnya pergeseran viskositas merupakan selisih antara viskositas awal dan viskositas setelah penyimpanan dibagi viskositas awal dikalikan 100%. Sediaan dianggap memiliki stabilitas yang baik jika memiliki persentase pergeseran viskositas kurang dari 10%. Dilakukan replikasi sebanyak 3 kali
b. Uji daya sebar
Sediaan gel ditimbang seberat 1 gram dan diletakkan di tengah kaca bulat berskala. Di atas gel diletakkan kaca bulat lain dengan berat 125 gram sebagai pemberat, didiamkan selama 1 menit, kemudian dicatat penyebarannya. Dilakukan replikasi sebanyak 3 kali (Garg dkk., 2002).
7. Uji daya antibakteri gel hand sanitizer minyak atsiri daun mint secara difusi sumuran
a. Pembuatan Suspensi Bakteri uji Escherichia coli
b. Pengujian aktivitas antibakteri bakteri Escherichia coli dengan metode difusi sumuran
Metode yang digunakan adalah metode double layer dengan membuat 2 lapisan pada media yaitu base dan seed layer. Dituang media MHA sebagai base layer sebanyak 10 ml, lalu setelah memadat dituang media MHA sebanyak 15 ml ditambah 1 ml suspensi bakteri sebagai seed layer. Setelah memadat, dibuat 3 lubang sumuran. Kemudian dimasukkan sampel berupa formula yang memenuhi kriteria sifat fisik dan stabilitas, kontrol positif (gel hand sanitizer merek NUVO®) dan kontrol negatif (basis) pada tiap lubang sebanyak 1 ml. Setelah itu, diinkubasi selama 24 jam pada suhu 37oC kemudian diamati zona hambat yang terbentuk. Dilakukan replikasi sebanyak 3 kali (Brooks dkk., 2004 ; Pratiwi, 2008).
F. ANALISIS HASIL
tidak. Selanjutnya data akan dianalisis untuk mengetahui signifikasi HPMC terhadap respon yaitu daya sebar, viskositas. Taraf kepercayaan yang digunakan dalam anilisis ini adalah 95%. Setelah itu, dilakukan uji TukeyHSD untuk melihat kebermaknaan masing-masing data yang didapat.
Data pergeseran viskositas didapat dari menghitung selisih antara viskositas awal dan viskositas setelah penyimpanan dibagi viskositas awal dikalikan 100%. Dari hasil penghitungan tersebut kemudian dapat dilihat data yang masuk kriteria pergeseran viskositas yang diinginkan yaitu kurang dari 10%.
30 BAB IV
HASIL DAN PEMBAHASAN
A. Verifikasi minyak atsiri daun mint
Pada penelitian ini, minyak atsiri daun mint yang digunakan berasal dari PT. Brataco Yogyakarta. Keaslian minyak atsiri daun mint ini dibuktikan dengan adanya Certificate of Analysis (CoA) pada lampiran 1. Berdasarkan pengujian organoleptis (bau, warna dan bentuk) diketahui bahwa minyak atsiri daun mint berbau khas, berwarna kuning jerami dan berbentuk cair.
Tahap awal penelitian ini adalah melakukan uji verifikasi dari minyak atsiri daun mint yang akan digunakan. Tujuannya adalah untuk mengetahui kualitas dan keaslian minyak atsiri daun mint yang digunakan dalam penelitian. Uji verifikasi meliputi uji indeks bias dan bobot jenis. Hasil yang didapat dari proses pengujian dapat dilihat pada tabel IV.
Tabel IV. Verifikasi minyak atsiri daun mint
Sifat Fisik Teoritis (BP) Spesifikasi CoA Hasil uji
Indeks bias π 1,457-1,467 1,4560-1,4660 1,4587 ± 0,0006
Bobot jenis d 0,900 - 0,916 0,888-0,908 0,8901 ± 0,0009
Hasil penelitian yang diperoleh menunjukkan bahwa nilai bobot jenis
minyak atsiri daun mint yang diuji tidak masuk range nilai bobot jenis dari
yang diuji masuk ke dalam range nilai indeks bias literatur. Menurut spesifikasi CoA (Certificate of Analysis), nilai indeks bias dan bobot jenis dari minyak atsiri daun mint sudah sesuai dengan nilai indeks bias yang terdapat dalam spesifikasi yang menjadi parameter PT. Brataco Yogyakarta. Jadi minyak atsiri yang diuji adalah benar minyak atsiri daun mint menurut spesifikasi dari PT. Brataco Yogyakarta yang memiliki kualitas kemurnian yang berbeda dengan literatur. Perbedaan ini diduga karena adanya perbedaan kandungan dari menthol yang terdapat dalam minyak atsiri. Kandungan menthol dalam penelitian sebesar 50,20 % (lampiran 1) sedangkan kandungan menthol dalam literatur sebesar 30-55 %. Perbedaan ini juga bisa disebabkan karena perbedaan asal tanaman mint yang digunakan, sebab setiap tanaman memiliki perbedaan jumlah senyawa yang dikandung berdasarkan tempat asalnya.
B. Formulasi sediaan gel hand sanitizer
gel pembersih tangan. Formula gel hand sanitizer yang digunakan berdasarkan hasil penelitian yang dilakukan oleh Retnosari dan Isadiartuti (2006). Formula tersebut kemudian dimodifikasi karena menggunakan zat aktif dan gelling agent yang berbeda dalam penelitian ini.
Bahan yang digunakan dalam pembuatan gel hand sanitizer meliputi zat aktif, gelling agent, humektan, pengawet, dan pelarut. Gelling agent merupakan bahan yang bertanggung jawab membentuk kekentalan atau pembentuk sifat alir sediaan gel hand sanitizer. Sedangkan humektan merupakan bahan yang digunakan untuk mencegah lepasnya air dari sediaan serta mengabsorsi lembab dari lingkungan saat di aplikasikan. Bahan lain yang digunakan dalam formulasi adalah pengawet yang berguna untuk mengawetkan sediaan agar tahan lama dan tidak ditumbuhi jamur atau bakteri. Pelarut yang digunakan dalam formulasi sediaan gel hand sanitizer adalah aquadest.
Gelling agent yang dipilih dalam penelitian ini adalah HPMC. Pemilihan HPMC sebagai gelling agent adalah karena HPMC memiliki sifat dapat membentuk gel yang jernih dan bersifat netral serta memiliki viskositas yang stabil dalam penyimpanan jangka panjang (Rowe dkk., 2009). Selain itu HPMC mengembang terbatas dalam air sehingga cocok digunakan dalam sediaan gel hand sanitizer. Dalam penelitian ini akan diteliti bagaimana pengaruh penambahan HPMC terhadap sifat fisik dan stabilitas sediaan gel hand sanitizer. Oleh karena itu dilakukan dahulu orientasi untuk menentukan variasi konsentrasi dari gel HPMC. Hasil dari orientasi adalah didapatkan variasi konsentrasi HPMC sebesar 1%, 2%, 3%, 4%, 5%.
Keunggulan dari HPMC sebagai gelling agent dibanding gelling agent lain adalah HPMC dapat membentuk basis gel yang lebih jernih dan stabil terhadap pH dibandingkan CMC-Na. Selain itu, HPMC tidak memerlukan basa untuk menetralkan keasaman seperti Carbomer yang memerlukan basa untuk menetralkan keasaman agar bisa membentuk basis gel.
Suatu sediaan memerlukan bahan pengawet agar tidak mudah ditumbuhi bakteri dan jamur. Hal itu disebabkan sediaan yang dibuat mempunyai komposisi sebagian besar berupa air yang sangat mudah ditumbuhi bakteri dan jamur. Na-metabisulfit digunakan sebagai bahan pengawet dalam formula karena aman untuk makanan menurut FDA (Food and Drug Administration) pada batas maksimum konsentrasi 2000-3000 ppm. Konsentrasi Na-metabisulfit yang dipakai adalah sebesar 0,02%. Menurut Rowe dkk. (2009) konsentrasi Na-metabisulfit yang diperkenankan untuk sediaan oral, parenteral dan topikal adalah sebesar 0,01%-1% w/v.
C. Uji organoleptis dan pH
Pengujian organoleptis bertujuan untuk mengetahui secara visual kualitas dan stabilitas gel selama masa penyimpanan. Parameter yang diamati adalah bau, bentuk, dan warna sediaan. Pengamatan dilakukan pada 48 jam setelah pembuatan dan 1 bulan setelah pembuatan.
Tabel V. Hasil uji organoleptis dan pH 48 jam
Kriteria F1 F2 F3 F4 F5
Bentuk Semisolid Semisolid Semisolid Semisolid Semisolid
Bau Khas Khas Khas Khas Khas
Warna Putih keruh Putih keruh Putih keruh Putih keruh Putih keruh
pH 6 6 6 6 6
Tabel VI. Hasil uji organoleptis 1 bulan
Kriteria F1 F2 F3 F4 F5
Bentuk Semisolid Semisolid Semisolid Semisolid Semisolid
Bau Khas Khas Khas Khas Khas
Warna Putih keruh Putih keruh Putih keruh Putih keruh Putih keruh
Pada tabel V dan VI dapat dilihat bahwa hasil uji organoleptis sediaan gel selama 48 jam dan 1 bulan setelah pembuatan sama. Oleh karena itu dapat disimpulkan bahwa tiap formula sediaan gel hand sanitizer stabil.
Dari tabel V, didapat besarnya pH formula 1 sampai 5 adalah sebesar 6. Hal itu menyatakan bahwa sediaan aman dan sesuai dengan pH kulit sehingga sediaan gel tidak akan mengiritasi kulit apabila diaplikasikan ke tangan.
D. Sifat fisik dan stabillitas gel hand sanitizer
Parameter sifat fisik sediaan yang baik antara lain adalah viskositas dan daya sebar. Parameter lain yang dapat digunakan untuk melihat bahwa suatu sediaan baik selain sifat fisik adalah stabilitas sediaan tersebut. Stabilitas sediaan dapat dilihat dari nilai pergeseran viskositanya. Pengujian sifat fisik bertujuan untuk melihat bahwa sediaan yang dibuat memenuhi syarat yang ditentukan untuk membentuk sediaan gel yang baik. Sedangkan pengujian stabilitas bertujuan untuk menjamin bahwa sediaan yang dihasilkan memenuhi persyaratan yang telah ditentuan walaupun sudah cukup lama dalam penyimpanan. Pemeriksaan stabilitas dapat digunakan sebagai dasar penentuan batas kadaluarsa (Lachman, 1994). Pada penelitian ini akan dilihat pengaruh penambahan HPMC sebagai gelling agent terhadap sifat fisik dan stabilitas sediaan gel hand sanitizer.
1. Uji Viskositas
Sehingga pengujian dilakukan 48 jam setelah pembuatan dengan harapan sistem gel yang dihasilkan sudah stabil. Pengujian 1 bulan setelah penyimpanan dilakukan untuk mengetahui stabilitas sediaan dengan mengukur pergeseran viskositas gel. Pengujian viskositas dilakukan dengan menggunakan viscotester. Sediaan diambil dan dimasukkan ke dalam wadah dan dihitung viskositasnya dengan melihat angka yang ditunjukkan dalam viscotester. Satuan yang digunakan dalam pengujian ini adalah d.Pa.s.
Tabel VII. Hasil uji viskositas 48 jam Formula
Gambar 4. Grafik konsentrasi HPMC terhadap viskositas 48 jam
0
Uji daya sebar bertujuan untuk menjamin kemudahan saat sediaan diaplikasikan di kulit. Besarnya nilai daya sebar suatu sediaan dipengaruhi oleh karakteristik sediaan, lama tekanan dan kekuatan yang menghasilkan kelengketan. Daya sebar suatu sediaan biasanya berbanding terbalik dengan nilai viskositas. Semakin tinggi nilai viskositasnya, maka nilai daya sebar akan semakin rendah (Garg dkk., 2002). Metode pengujian daya sebar adalah dengan menimbang gel seberat 1,0 gram, diletakkan ditengah kaca bulat berskala. Diatas gel diletakkan kaca bulat lain dan pemberat dengan berat total 125 gram, didiamkan selama 1 menit, kemudian dicatat diameter penyebarannya (Grag dkk., 2002).
Tabel VIII . Hasil uji daya sebar 48 jam Formula
Dari tabel VIII dan gambar 5 dapat dilihat bahwa semakin tinggi konsentrasi HPMC menyebabkan daya sebar sediaan semakin kecil dan viskositas semakin besar. Hal ini sesuai dengan teori yang menyatakan bahwa viskositas mempengaruhi daya sebar. Dimana semakin tinggi viskositas, maka daya sebarnya semakin kecil (Garg dkk., 2002). Dari ke-5 formula, yang memenuhi kriteria daya sebar yang diinginkan adalah formula 3, 4, dan 5. Dimana daya sebar yang baik untuk sediaan gel adalah sebesar 5 cm-7cm (Garg dkk., 2002).
3. Uji pergeseran viskositas
Uji pergeseran viskositas dilakukan untuk mengetahui stabilitas sediaan gel selama masa penyimpanan. Uji ini dihitung dengan mengetahui viskositas sediaan gel selama 2 hari dan 1 bulan selama masa penyimpanan. Besarnya pergeseran viskositas merupakan selisih antara viskositas awal dan viskositas setelah penyimpanan dibagi viskositas awal dikalikan 100%. Suatu sediaan memiliki stabilitas yang baik jika nilai pergeseran viskositasnya ≤ 10%. Rumus penghitungan pergeseran viskositas:
Pergeseran viskositas= x 100%
Tabel IX. Hasil perhitungan pergeseran viskositas
Formula F1 F2 F3 F4 F5
Pergeseran viskositas(%)
68,4 16,9 67,6 32,6 8,4
viskositas ≤ 10%. Sehingga formula 5 merupakan formula yang stabil selama
penyimpanan 1 bulan dibandingkan formula yang lainnya.
E. Data statistik
Data yang didapat yaitu daya sebar dan viskositas, kemudian dianalsis menggunakan program R 3.1.0, dengan uji ANOVA satu arah pada taraf kepercayaan 95%.
Tahap pertama dalam uji ANOVA adalah uji normalitas dengan uji Shapiro-Wilk, karena jumlah sampel kurang dari 50. Tujuannya adalah untuk mengetahui distribusi dari data tersebut normal atau tidak.
Setelah diketahui data terdistribusi normal, dilanjutkan dengan uji kesamaan varians. Uji ini bertujuan untuk mengetahui kesamaan varians dari suatu populasi. Uji kesamaan varians dilakukan dengan mengunakan Levene’s Test.
Apabila data menunjukkan kesamaan varians, maka dapat dilanjutkan dengan melihat nilai efek faktor terhadap respon dengan melakukan uji one way ANOVA. Untuk mengetahui kebermaknaan masing-masing formula secara statistik, dapat dilakukan uji TukeyHSD.
1. Uji normalitas data
Tabel X. Hasil uji normalitas Shapiro-Wilk Jenis Data Formula p-value
Viskositas disimpulkan bahwa data yang didapat terdistribusi normal. Oleh karena itu, uji statistik dapat dilanjutkan dengan uji kesamaan varians.
2. Uji kesamaan varians
Setelah data terdistribusi normal, maka dilanjutkan dengan melakukan uji kesamaan varians. Uji kesamaan varians menggunakan Levene’s Test. Hasil uji kesamaan varians untuk viskositas dan daya sebar selama 48 jam dapat dilihat pada tabel XI.
Tabel XI. Hasil Uji Kesamaan Varians Jenis Data p-value
Viskositas 0,152
Pada tabel XI menyatakan bahwa nilai p-value dari ke-2 jenis data (viskositas dan daya sebar) memiliki nilai p-value >0,05. Hal itu memnunjukkan bahwa ke-2 jenis data bervariansi sehingga bisa dilanjutkan dengan ANOVA. 3. Uji TukeyHSD
Uji selanjutnya yang dilakukan adalah ANOVA untuk melihat efek faktor terhadap respon. Hasil dari ANOVA adalah nilai p viskositas sebesar 4,72x10-9 dan nilai p daya sebar sebesar 4,03x10-14. Hasil tersebut dibawah nilai p <0,05 sehingga dapat disimpulkan bahwa ada efek faktor terhadap respon sehingga perlu dilanjutkan dengan uji TukeyHSD untuk melihat kebermaknaan masing-masing formula secara statistik. Hasil dari uji TukeyHSD viskositas dan daya sebar selama 48 jam dapat dilihat pada tabel XII dan XIII.
Tabel XII. Hasil uji TukeyHSD viskositas 48 jam Perbandingan
Formula p-adj Keterangan*
F2:F1 0,7141952 Tidak berbeda
F3:F1 0,0000067 Berbeda
Tabel XIII. Hasil uji TukeyHSD daya sebar 48 jam Perbandingan
Formula p-adj Keterangan*
F2:F1 0,0000000 Berbeda
F3:F1 0,0000000 Berbeda
F4:F1 0,0000000 Berbeda
F5:F1 0,0000000 Berbeda
F3:F2 0,0000001 Berbeda
F4:F2 0,0000000 Berbeda
F5:F2 0,0000000 Berbeda
F4:F3 0,065153 Tidak berbeda
F5:F3 0,0000335 Berbeda
F4:F5 0,0012187 Berbeda
Keterangan : *= secara statistik dengan taraf kepercayaan 95%
F. Uji potensi antimikroba
Minyak atsiri daun mint memiliki aktivitas potensi antimikroba dan dapat menghambat pertumbuhan mikroba baik gram negatif maupun positif. Zona hambat yang dihasilkan dari minyak atsiri daun mint menurut penelitian adalah sebesar 13mm terhadap bakteri Escherichia coli (Saeed dkk., 2006). Penelitian lainnya tentang minyak atsiri daun mint yang menyatakan bahwa nilai KHM minyak atsiri daun mint terhadap bakteri Escherichia coli sebesar 0,5% v/v (Hammer dkk., 1999). Berdasarkan penelitian tersebut maka dilakukan pengujian untuk mengetahui seberapa besar potensi antimikroba gel hand sanitizer minyak atsiri daun mint terhadap bakteri Escherichia coli. Digunakan bakteri Escherichia coli karena bakteri ini merupakan salah satu penyebab penyakit diare.
Pengujian potensi antimikroba menggunakan metode difusi sumuran karena sampel yang digunakan adala sediaan semisolid. Prinsip kerja difusi sumuran adalah senyawa uji ditempatkan ke dalam media padat yang telah diinokulasikan bakteri. Senyawa uji berdifusi ke dalam media dan menghambat pertumbuhan bakteri uji.
Kontrol positif bertujuan untuk melihat seberapa besar potensi antimikroba dari produk di pasaran dibandingkan dengan sampel gel hand sanitizer minyak atsiri daun mint. Produk gel hand sanitizer yang digunakan sebagai kontrol positif adalah gel hand sanitizer merek NUVO®. Digunakan gel hand sanitizer merek NUVO® karena produk ini merupakan salah satu produk gel hand sanitizer yang digemari masyarakat dan sering digunakan oleh masyarakat. Kontrol positif yang digunakan bukan dari antibiotik yang sudah teruji aktivitas antimikrobanya sebab dalam penelitian ini ingin melihat seberapa besar aktivitas antimikroba sediaan gel hand sanitizer minyak atsiri daun mint dibanding dengan sediaan gel hand sanitizer yang beredar di pasaran.
Sampel yang digunakan dalam uji potensi antibakteri adalah sediaan gel hand sanitizer minyak atsiri daun mint formula 5. Pemilihan sampel berupa gel hand sanitizer minyak atsiri daun mint formula 5 karena berdasarkan uji sifat fisik dan stabilitasnya, hanya formula 5 yang memenuhi kriteria sehingga sampel yang dipilih adalah sediaan gel hand sanitizer minyak atsiri daun mint formula 5.
Tabel XIV. Hasil zona hambat uji potensi antibakteri terhadap
Gambar 6. Hasil uji potensi antimikroba
Berdasarkan gambar 6 dan tabel XIV, maka dapat diketahui bahwa basis sebagai kontrol negatif tidak memberikan zona hambat. Hal itu membuktikan bahwa dalam formula, yang memberikan efek potensi antimikroba hanya minyak atsiri daun mint. Pada sampel dan gel hand sanitizer merek NUVO® sebagai kontrol positif didapatkan zona jernih yang merupakan zona hambat dari sediaan. Zona hambat ini memberikan bukti bahwa sampel dan kontrol positif memiliki potensi sebagai antimikroba terhadal bakteri Escherichia coli . Besarnya rata-rata zona hambat pada sampel adalah sebesar 10,00 mm sedangkan pada kontrol
kontrol (+) sampel
49 BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
1. HPMC memberikan pengaruh pada kelima formula. Semakin meningkat konsentrasi HPMC, maka akan menaikkan respon viskositas, dan menurunkan respon daya sebar.
2. Formula gel minyak daun mint yang memenuhi kriteria sifat fisik dan memenuhi kriteria stabilitas adalah formula 5.
B. Saran
1. Perlu dilakukan optimasi formula yang digunakan agar mendapatkan sediaan yang memenuhi kriteria sifat fisik, stabilitas, dan daya antimikroba yang baik. 2. Perlu dilakukan uji terhadap berbagai jenis bakteri terutama bakteri yang ada di tangan atau kulit seperti Staphylococcus aureus, E. coli, Salmonella, Vibrio cholerae, dan Shigella.
DAFTAR PUSTAKA
Achmad, S. A., 1986, Kimia Organik Bahan Alam, Modul 1-6, Karunika, Jakarta. Alankar, S., 2009, A Review on Peppermint Oil, Asian Journal of Pharmaceutical
and Clinical Research, Vol.2, pp. 27-32.
Allen Jr., L. V., 2005, The Art, Science, and Technology of Pharmaceutical Compounding, 2th ed., American Pharmaceutical Association, USA, p. 301.
Arikumalasari, J., Dewantara, IG.N.A., Wijayanti, N.P.A.D., 2013, Optimasi HPMC Sebagai Gelling Agent Dalam Formula Gel Ekstrak Kulit Buah Manggis (Garcinia mangostana L.), Jurnal Farmasi Udayana, Vol.2, pp. 145-152.
Balai Penelitian Tanaman Obat dan Aromatik, 1986, Kemungkinan Pembudidayaan Tanaman Penghasil Minyak Atsiri Potensial, Panili, dan Lidah Buaya, Departemen Pertanian, Bogor.
Benson, H.A.E dan Watkinson, A.C., 2012, Transdermal and Topical Drug Delivery Principels and Practice, Jhon Wiley and Son, inc. Publication, New Jersey, pp. 3-281.
Block, S., 2001, Disinfection, Sterilization and Preservation, 4th Edition, Williams and Wilkins. P, p. 38.
Brooks, GF., Butel SJ., Morse AS., 2004, Medical Microbiology, Edisi ke 23, diterjemahkan oleh Hartanto, H., Chaerunnisa R., Alifa D., Aryana D., Penerbit Buku Kedokteran, Jakarta, pp. 57, 170, 176-178, 181, 225,229, 254-257.
BSN Medical, 2009, Bakteri luka yang umum di temukan dalam luka terinfeksi, http://www.cutimed-sorbact.com/Indonesia/start.html, diakses tanggal 16
September 2013.
Charu Gupta, Amar P. Garg, Ramesh C. Uniya dan Archana Kumari, 2008, Antimicrobial activity of some herbal oils against common food-borne pathogens, African Journal of Microbiology Research, Vol.(2), pp. 258-261.
Depkes RI, 1995, Farmakope Indonesia, Edisi IV, Departemen Republik Indonesia, Jakarta, pp. 1030-1031.
Garg, A., Aggarwal, D., Garg, S., dan Singla, A.K., 2002, Spreading of Semisolid Formulation, Pharmaceutical Technology, USA, pp. 84-104.
Guenther, E., 1947, Essential Oils, diterjemahkan oleh Ketaren, 1987, pp. 21-25, 90, 132-134, 244-245, UI Press, Jakarta.
Gupte, J., 2006, The Short Textbook of Medicinal Microbiology, 9th ed., Jaypee Brother Medical Publisher Ltd., New Delhi, pp. 161, 223.
Hammer, K. A., Carson, C. F., dan Riley, T. V., 1999, Antimicrobial activity of essential oils and other plant extracts, Journal of Applied Microbiology, Vol.86, pp. 985-990.
Harborne, J. B., 1973, Phytochemical Methods, diterjemahkan oleh Padmawinata, K., dan Sudiro, I., 1987, ITB Press, Bandung.
Junqueira, C., dan Kelley, R., 1997, Histologi Dasar, Edisi Kedelapan, Kedokteran ECG, Jakarta, pp. 357-360.
Lachman, L., Liebermann, H.A., dan Kanig, J.I., 1994, Teori and Praktek Farmasi Industri II, Edisi III, UI Press, Jakarta, pp. 652-653, 657-660. Marriott, N.G., 1999, Principle of Food Sanitation, 4th edition, Aspen Publisher
Inc., Gaithtersbug, Maryland.
Martin, A., 1993, Physical Pharmacy, Lea & Febiger, Philladephia, pp. 566-572.
Nandkhisor, S.W., Bhalerao, K. A., Ranaware, P.V., dan Zanje, R., 2013, Formulation and Evaluation of Herbal Sanitizer, International Journal of PharmTech Research, Vol.5, No.1, pp. 40-43.
Okhuysen, P.C. dan DuPont, H.L., 2010, Enteroaggregative Escherichia coli (EAEC): A Cause of Acute and Persistent Diarrhea of Worldwide Importance, Editorial Commentary, JID 2010:202, pp. 503-505.
Oyedeji, O.A., dan Afolayan, A.J., 2006, Chemichal Composition and Antibacterial Activity Of The Essential Oil Isolated from South Africa Mentha longifolia (L.) subsp. Capensis (Thunb.) Briq, Journal of Essential Oil Research, Vol. 18, pp. 57-59.
Pratiwi, S.T., 2008, Mikrobiologi Farmasi, Erlangga, Jakarta, pp.165-168, 188-191.
Radji, M. dan Biomed, M., 2009, Buku Ajar Mikrobiologi: Panduan Mahasiswa Farmasi dan Kedokteran, Penerbit Buku Kedokteran EGC, Jakarta, pp. 129-130, 178-180.
Retnosari dan Isadiartuti, D., 2006, Studi efektivitas sediaan gel antiseptik tangan ekstrak daun sirih (Piper betle Linn.), Majalah Farmasi Indonesia, pp. 163-169.
Rowe, R.C., Paul J., Sheskey, Owen, S.C., 2006, Handbook of Pharmaceutical Excipients, 5th ed, Pharmaceutical Press, London, pp. 346 – 348.
Rowe, R.C., Sheskey, P.J., and Quinn, M.E., 2009, Handbook of Pharmaceutical Exipients, 6th ed, Pharmaceutical Press, London, pp. 283-286, 326-329, 654-656.
Saeed, S., Asa, N., dan Tariq, P., 2006, In Vitro Antibacterial Activity of Peppermint, Park, J. Bot., Vol.38(3), pp. 869-872.
Sinko, P.J., 2006, Physical Chemical and Biopharmaceutical Principles in the Pharmaceutical Sciences, 5th ed, Lippincott Williams & Wilkins Philadelphia, pp. 481-483, 512.
Tambunan, L. A., 2008, Bioetanol Antitumpah,Trubus, Vol XXXIX, pp. 24-25. The Departement of Health, 2009, British Pharmacopeia, Vol. IV, The Stationery
Office, London, pp. 7233-7237.
UNICEF, 2012, Pada Hari Cuci Tangan Sedunia, UNICEF mengatakan: Ini tidak rumit, tapi penting, http://www.unicef.org/indonesia/id/media 19772.html, diakses tanggal 16 September 2013.
LAMPIRAN
Lampiran 3. Verifikasi minyak daun mint
1. Indeks bias minyak daun mint
2. Bobot jenis minyak daun mint
Rumus untuk menghitung kerapatan minyak daun mint (25oC) :
ρ minyak daun mint =
Replikasi 1 2 3
Bobot piknometer (g) 24,0050 24,0010 24,0120
Bobot piknometer + air (g) 34,0160 34,0130 34,0180
Bobot air (g) 10,0110 10,0120 10,0060
Kerapatan air (250C)
(g/mL) 0,99707 0,99707 0,99707
Volume air (mL) 10,0404 10,0414 10,0354
Replikasi 1 2 3
Bobot piknometer (g) 24,0010 24,0560 24,0220
Bobot piknometer + minyak mint (g) 32,9010 32,9730 32,9340
Bobot minyak mint (g) 8,9000 8,9170 8,9120
Volume minyak mint (mL) 10,0400 10,0410 10,0350
ρ minyak mint (g/mL) 0,8865 0,8881 0,8881
Bobot jenis minyak mint 0,8891 0,8907 0,8907
Rumus untuk menghitung bobot jenis minyak daun mint (25oC) :
BJ =
Replikasi Bobot jenis
I 0,8891
II 0,8907
III 0,8907
Lampiran 4. Hasil uji sifat fisik dan stabilitas gel
Rumus menghitung pergeseran viskositas gel minyak daun mint :
Pergeseran viskositas =
x
100%Formula F1 F2 F3 F4 F5
Pergeseran viskositas(%)
Lampiran 5. Hasil pengolahan data dengan Sofware R3.1.0 1. Viskositas
a. Uji normalitas dengan Shapiro-Wilk Formula 1
p-value > 0.05 data terdistribusi normal Formula 2
p-value > 0.05 data terdistribusi normal Formula 3
p-value > 0.05 data terdistribusi normal >shapiro.test(vis48$f1)
Shapiro-Wilk normality test
data: vis48$f1
W = 0.9868, p-value = 0.7804
>shapiro.test(vis48$f2)
Shapiro-Wilk normality test
data: vis48$f2
W = 0.9231, p-value = 0.4633
>shapiro.test(vis48$f3)
Shapiro-Wilk normality test